Escolar Documentos
Profissional Documentos
Cultura Documentos
Introdução à Química Experimental
Enviado por
mamaemtolokoDescrição original:
Título original
Direitos autorais
Formatos disponíveis
Compartilhar este documento
Compartilhar ou incorporar documento
Você considera este documento útil?
Este conteúdo é inapropriado?
Denunciar este documentoDireitos autorais:
Formatos disponíveis
Introdução à Química Experimental
Enviado por
mamaemtolokoDireitos autorais:
Formatos disponíveis
CQ092 - Introduo Qumica Experimental Curso: Engenharia Qumica - CQ092 Profa Giovana Gioppo Nunes 2 Semestre de 2009
1 lista de exerccios - Cintica
1. Para a reao S2O82-(aq) + 2 I-(aq) 2 SO42-(aq) + I2(aq) a velocidade de formao do I2(aq) foi determinada como 2,5 x 10-3 mol dm-3 s-1. Determine: (a) a velocidade de formao do SO42- (aq) e (b) a velocidade de consumo do S2O82-. 2. Mostrar, para cada reao em fase gasosa seguinte, como a velocidade de desaparecimento de cada reagente est relacionada com a velocidade de aparecimento do produto: (a) CH4(g) + 2 H2O(g) CO2(g) + 4 H2(g) (b) 3 C2H2(g) C6H6(g) (c) 2 NO(g) + Br2(g) 2 NOBr(g) 3. A velocidade mdia da reao N2(g) + 3 H2(g) 2 NH3(g), durante um certo tempo, registrada como sendo 1,15 (mmol NH3)L-1h-1. (a) Qual a velocidade mdia, no mesmo perodo de tempo, em termos do desaparecimento de H 2 (g)? (b) Qual a velocidade mdia nica? 4. A velocidade de decrscimo de [A] numa reao foi medida como segue: Tempo, minuto 0,0 20,0 40,0 60,0 80,0 [A], mol/L 1,00 0,819 0,670 0,549 0,449 Calcule a velocidade mdia da reao -[A]/t entre: (a) 40,0 e 60,0 min; (b) 20 e 80 min; (c) 0,0 e 100,0 min 100,0 0,368
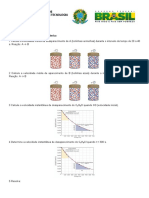
5. Esboce um grfico mostrando como pode diminuir a concentrao de um reagente com o tempo. Recorrendo ao seu grfico, explique a diferena entre as velocidades mdia e instantnea de uma reao. 6. Ao dobrarmos a concentrao de NO, a velocidade da reao 2 NO(g) + O2(g) 2 NO2(g) aumenta 4 vezes. Ao dobrarmos as concentraes de NO e de O2, a velocidade aumenta 8 vezes. Quais so (a) a ordem de reao dos reagentes; (b) a ordem total da reao; (c) as unidades de k, se as unidades forem expressas em mols por litro por segundo? 7. Em quais condies as velocidades mdias e as velocidades instantneas so essencialmente iguais? 8. Uma certa reao de primeira ordem em relao a A, segunda ordem em relao a B e terceira ordem em relao a C. Qual a influencia sobre a velocidade da reao se duplicarmos a concentrao de (a) A; (b) B; (c) C. 9. Uma reao segue a seguinte lei de velocidade: velocidade = k[A][B]2. (a) Se houver alterao de [A] haver alterao da velocidade? Haver alterao da constante de velocidade? Explique. (b) Qual a ordem da reao em relao a A? (c) Qual a ordem global da reao? 10. Quatro experimentos foram realizados para descobrir como a velocidade inicial de consumo de ons BrO3- na reao BrO3- (aq) + 5 Br-(aq) + 6 H3O+(aq) 3 Br2(aq) + 9 H2O(l) varia quando as concentraes dos reagentes variam. (a) Use os dados
experimentais da tabela a seguir para determinar a ordem da reao para cada reagente e a ordem total. (b) Escreva a lei da velocidade da reao e (c) determine o valor de k. Concentrao inicial (mol L-1) Velocidade inicial Experimento BrO3BrH3O+ (mol BrO3-)L-1s-1 1 0,10 0,10 0,10 1,2 x 10-3 2 0,20 0,10 0,10 2,4 x 10-3 3 0,10 0,30 0,10 3,5 x 10-3 4 0,20 0,10 0,15 5,5 x 10-3 11. Se as concentraes fossem medidas em mol L-1 e o tempo em segundos, quais seriam as unidades das constantes de velocidade para os seguintes casos: (a) uma reao de primeira ordem; (b) uma reao de segunda ordem; (c) uma reao de terceira ordem. 12. A velocidade inicial da reao hipottica A + B C foi medida com diferentes concentraes iniciais de A e de B; Os resultados foram os seguintes: Experiment [A] (mol L-1) [B] (mol L-1) Velocidade inicial (mol L-1s-1) o 1 0,100 0,100 4,0 x 10-5 2 0,100 0,200 4,0 x 10-5 3 0,200 0,100 16,0 x 10-5 Com estes dados, determine: (a) a lei da velocidade da rao; (b) a constante de velocidade; (c) a velocidade da reao quando as concentrao de A 0,050 mol L-1 e B 0,100 mol L-1.
Você também pode gostar
- Helen Palmer O Eneagrama Compreendendo-Se A Si Mesmo e Aos Outros em Sua VidaDocumento267 páginasHelen Palmer O Eneagrama Compreendendo-Se A Si Mesmo e Aos Outros em Sua Vidaalmircorrea100% (18)
- Quím CinéticaDocumento8 páginasQuím CinéticaJoão Ribeiro Franco NetoAinda não há avaliações
- Embalagens vidro alimentosDocumento34 páginasEmbalagens vidro alimentosPedro CampeloAinda não há avaliações
- Exercícios de Cinética Química Com GabaritoDocumento10 páginasExercícios de Cinética Química Com Gabaritoguilhermegb100% (5)
- Cinética QuímicaDocumento6 páginasCinética QuímicaSirlei Gonçalves PoffoAinda não há avaliações
- Lista de Exercicios Cinetica Quimica EQM061Documento13 páginasLista de Exercicios Cinetica Quimica EQM061Mariana DomicianoAinda não há avaliações
- Nas Fronteiras Da Loucura2Documento524 páginasNas Fronteiras Da Loucura2csilvin100% (2)
- Processos de Preparacao de MassaDocumento137 páginasProcessos de Preparacao de MassaRafael VieiraAinda não há avaliações
- Lista de Exercícios de Cinética QuímicaDocumento5 páginasLista de Exercícios de Cinética QuímicaCamila Geovana Gonçalves FerreiraAinda não há avaliações
- Lista de exercícios de cinética e equilíbrio químicoDocumento7 páginasLista de exercícios de cinética e equilíbrio químicoLeonardo Alves de OliveiraAinda não há avaliações
- Conservação e Restauro de Arte Sacra em MadeiraDocumento326 páginasConservação e Restauro de Arte Sacra em MadeiraFabio Zarattini100% (1)
- Alfa - Módulo 40Documento28 páginasAlfa - Módulo 40Luiza FreitasAinda não há avaliações
- MECÂNICA QUÍMICA E CINÉTICA REACIONALDocumento4 páginasMECÂNICA QUÍMICA E CINÉTICA REACIONALguilhermegbAinda não há avaliações
- 7 Lista QGE2001 CineticaDocumento5 páginas7 Lista QGE2001 CineticaWashington RamosAinda não há avaliações
- Cinetica Quimica If ExercDocumento5 páginasCinetica Quimica If ExercRaquel Andreola ValenteAinda não há avaliações
- Lista de Exercícios de Cinética QuímicaDocumento2 páginasLista de Exercícios de Cinética QuímicasheldonsingAinda não há avaliações
- Cinética Química - Lista de ExercíciosDocumento4 páginasCinética Química - Lista de ExercíciosLael EduardoAinda não há avaliações
- Lista Cinética PDFDocumento9 páginasLista Cinética PDFLeydiane Araujo BrandaoAinda não há avaliações
- Cinetica CompletaDocumento5 páginasCinetica CompletaConta ReservaAinda não há avaliações
- Lista de Exercicios 1Documento4 páginasLista de Exercicios 1Mariana MartinsAinda não há avaliações
- Lista de Exercícios Cinética QuímicaDocumento6 páginasLista de Exercícios Cinética QuímicagabezmirandaAinda não há avaliações
- Físico-Química II - Lista de Exercícios Cinética QuímicaDocumento3 páginasFísico-Química II - Lista de Exercícios Cinética QuímicaLucas CamargoAinda não há avaliações
- Cinética Química: Ordem, Constante e Lei de VelocidadeDocumento2 páginasCinética Química: Ordem, Constante e Lei de VelocidadeJoão Valdir Miranda100% (2)
- 7 Lista de Exercicios de Quimica Geral Cinetica Quimica Com Respostas 19.05.2011 1Documento5 páginas7 Lista de Exercicios de Quimica Geral Cinetica Quimica Com Respostas 19.05.2011 1Suzany ToledoAinda não há avaliações
- Cinética químicaDocumento6 páginasCinética químicaRanked PlayerAinda não há avaliações
- 1Documento4 páginas1Larissalola50% (2)
- 3 Lista de Exercicios - Cinética Química e Equilíbrio Químico (Gabarito)Documento3 páginas3 Lista de Exercicios - Cinética Química e Equilíbrio Químico (Gabarito)Dvmr AnapAinda não há avaliações
- Determinação da ordem e constante de velocidade de reações químicasDocumento7 páginasDeterminação da ordem e constante de velocidade de reações químicasRodrigo BertaciniAinda não há avaliações
- Cinética Química - Exercicios 08-10-2022Documento8 páginasCinética Química - Exercicios 08-10-2022FELIPE SILVAAinda não há avaliações
- CNPJDocumento5 páginasCNPJDavi AraújoAinda não há avaliações
- Lista Exercícios CinéticaB - 23Documento8 páginasLista Exercícios CinéticaB - 23isamatias01Ainda não há avaliações
- LISTA_DE_EXERCCIOS_Tpico_7_e_8Documento4 páginasLISTA_DE_EXERCCIOS_Tpico_7_e_8a.mendesAinda não há avaliações
- UFCE - Lista 3 de exercícios de QuímicaDocumento2 páginasUFCE - Lista 3 de exercícios de Químicapedro alcantara100% (1)
- Reações Químicas: Velocidade e FatoresDocumento30 páginasReações Químicas: Velocidade e FatoresromezioAinda não há avaliações
- Aula 14 - Revisão e Lista de ExercíciosDocumento4 páginasAula 14 - Revisão e Lista de ExercíciosLílian Barreto GonçalvesAinda não há avaliações
- Lista de Exercícios de Química Geral com Reações de VelocidadeDocumento2 páginasLista de Exercícios de Química Geral com Reações de VelocidadePedro MarizAinda não há avaliações
- Cinética química - Lista de exercíciosDocumento4 páginasCinética química - Lista de exercíciosKelly FigueiraAinda não há avaliações
- Lista Área II Química FundamentalDocumento20 páginasLista Área II Química FundamentalGuillaume HaddadAinda não há avaliações
- q3 - Aula 21 A 22 - Cinét Ica Quimica I AulaDocumento2 páginasq3 - Aula 21 A 22 - Cinét Ica Quimica I AulaAnanda MuxAinda não há avaliações
- Questionário sobre Química geral experimental (2021/1Documento5 páginasQuestionário sobre Química geral experimental (2021/1Abraao SantanaAinda não há avaliações
- Exercícios de Físico-químicaDocumento5 páginasExercícios de Físico-químicaLisiane AliesAinda não há avaliações
- Reações Químicas e EletroquímicaDocumento3 páginasReações Químicas e EletroquímicaLeo CrozAinda não há avaliações
- Cinética Química: Fatores e ExpressõesDocumento4 páginasCinética Química: Fatores e ExpressõesLourdilene BritoAinda não há avaliações
- Lista de exercícios de termodinâmica e cinética químicaDocumento5 páginasLista de exercícios de termodinâmica e cinética químicaJoice SchuhAinda não há avaliações
- Química Cinética Reações Ordens VelocidadesDocumento51 páginasQuímica Cinética Reações Ordens VelocidadesCarlos Henrique0% (1)
- Lista Cinética QuímicaDocumento2 páginasLista Cinética QuímicaMatheusFigueiredodeSouzaAinda não há avaliações
- Folha 2 de Cinética Química-IME-ITADocumento3 páginasFolha 2 de Cinética Química-IME-ITAHelton MoreiraAinda não há avaliações
- ListacineticaDocumento2 páginasListacineticaSARAHAinda não há avaliações
- Lista Da Aula 3 - Cinética QuímicaDocumento5 páginasLista Da Aula 3 - Cinética QuímicaE P Som RJAinda não há avaliações
- Alfa - Módulo 37Documento23 páginasAlfa - Módulo 37Jackson Rodrigo Sousa PintoAinda não há avaliações
- Cálculos de velocidade de reação químicaDocumento6 páginasCálculos de velocidade de reação químicaIara Da CostaAinda não há avaliações
- Exercícios Revisão CinéticaDocumento20 páginasExercícios Revisão CinéticaIara DaherAinda não há avaliações
- I Lista de ExerciciosDocumento2 páginasI Lista de ExerciciosVitor Hugo MelloAinda não há avaliações
- Lista Cinética 2023 - 2TDocumento2 páginasLista Cinética 2023 - 2TRafael playeraleAinda não há avaliações
- Matéria e Suas PropriedadesDocumento28 páginasMatéria e Suas PropriedadesGleisonAinda não há avaliações
- Cinética QuímicaDocumento3 páginasCinética QuímicaParth PrinceAinda não há avaliações
- Lista de Exercícios - CinéticaDocumento5 páginasLista de Exercícios - CinéticaGleison MendesAinda não há avaliações
- Química Fundamental: Cinética e Equilíbrio QuímicoDocumento5 páginasQuímica Fundamental: Cinética e Equilíbrio QuímicoHugo ChavesAinda não há avaliações
- Lista de exercícios de química com reações químicasDocumento2 páginasLista de exercícios de química com reações químicasAna Maria DinizAinda não há avaliações
- Lista I - Reatores IDocumento13 páginasLista I - Reatores IVilmar Bertotti JuniorAinda não há avaliações
- 1 Lista de Exercicios de Cinetica QuimicaDocumento5 páginas1 Lista de Exercicios de Cinetica QuimicaTyler KörnAinda não há avaliações
- Exercícios Cinética Com RespostaDocumento29 páginasExercícios Cinética Com Respostagreicifrauches57% (7)
- Apostila Química Orgânica: Carbono, Dienos E AromáticosNo EverandApostila Química Orgânica: Carbono, Dienos E AromáticosAinda não há avaliações
- Casas Tradicionais Nyaneka-nkhumbiDocumento19 páginasCasas Tradicionais Nyaneka-nkhumbimamaemtolokoAinda não há avaliações
- Manual Instrução Elsys 2.0 e 2.5Documento2 páginasManual Instrução Elsys 2.0 e 2.5Guilher Campagnaro Carrareto40% (15)
- Benefícios da Caminhada na Qualidade de Vida dos AdultosDocumento72 páginasBenefícios da Caminhada na Qualidade de Vida dos AdultosmamaemtolokoAinda não há avaliações
- Cores Do Cérebro (Interpretação)Documento7 páginasCores Do Cérebro (Interpretação)mamaemtolokoAinda não há avaliações
- Procedimento de Entrega Chave AcessoDocumento2 páginasProcedimento de Entrega Chave AcessomamaemtolokoAinda não há avaliações
- Denomina Logradouros PúblicosDocumento1 páginaDenomina Logradouros PúblicosmamaemtolokoAinda não há avaliações
- Ulfba - A Baba Mortífera Dos Dragões de KomodoDocumento4 páginasUlfba - A Baba Mortífera Dos Dragões de KomodomamaemtolokoAinda não há avaliações
- Sobre As Afinidades Entre A Filosofia de Francis Bacon E O CeticismoDocumento25 páginasSobre As Afinidades Entre A Filosofia de Francis Bacon E O CeticismomamaemtolokoAinda não há avaliações
- Casa Na PraiaDocumento21 páginasCasa Na PraiamamaemtolokoAinda não há avaliações
- 3 Es 391Documento16 páginas3 Es 391mamaemtolokoAinda não há avaliações
- Case Canecas EpejDocumento4 páginasCase Canecas EpejmamaemtolokoAinda não há avaliações
- Identidade Capixaba 1Documento9 páginasIdentidade Capixaba 1tuttysfAinda não há avaliações
- Gliconeogenese GlicogenoliseDocumento1 páginaGliconeogenese GlicogenolisemamaemtolokoAinda não há avaliações
- FotofosforilacaoDocumento1 páginaFotofosforilacaomamaemtolokoAinda não há avaliações
- Anatel12 001 01Documento16 páginasAnatel12 001 01mamaemtolokoAinda não há avaliações
- Matriz Curricular Completa Do CursoDocumento1 páginaMatriz Curricular Completa Do CursomamaemtolokoAinda não há avaliações
- Lista de ExercíciosDocumento1 páginaLista de Exercíciosmamaemtoloko0% (2)
- Acoplador ArtigoDocumento6 páginasAcoplador Artigoasd34Ainda não há avaliações
- Ginkgo Biloba L. e Memória1Documento3 páginasGinkgo Biloba L. e Memória1HelimarcosNunesAinda não há avaliações
- Tabela CNVW - 20140314 - InternetDocumento2 páginasTabela CNVW - 20140314 - InternetmamaemtolokoAinda não há avaliações
- ProgramaDocumento2 páginasProgramamamaemtolokoAinda não há avaliações
- Pratica2 VandergraaffDocumento4 páginasPratica2 VandergraaffmamaemtolokoAinda não há avaliações
- O Que É Modulação - Telecomhall BRDocumento11 páginasO Que É Modulação - Telecomhall BRmamaemtolokoAinda não há avaliações
- Volume CPDocumento3 páginasVolume CPjackAinda não há avaliações
- A História Da Televisão IDocumento97 páginasA História Da Televisão IValéria CristinaAinda não há avaliações
- Volume CPDocumento3 páginasVolume CPjackAinda não há avaliações
- Eletromagnetismo UFMGDocumento38 páginasEletromagnetismo UFMGCamila VieiraAinda não há avaliações
- Exercícios ResolvidosDocumento27 páginasExercícios ResolvidosWadson Barcellos RibeiroAinda não há avaliações
- Substantivos HomônimosDocumento2 páginasSubstantivos HomônimosLenine ReinaldoAinda não há avaliações
- Entrevista PsiquiatricaDocumento38 páginasEntrevista Psiquiatricakbianca26Ainda não há avaliações
- República Federativa Do Brasil Ministério Da Saúde Agência Nacional de Vigilância SanitáriaDocumento1 páginaRepública Federativa Do Brasil Ministério Da Saúde Agência Nacional de Vigilância Sanitáriahqwy6kjdkqAinda não há avaliações
- Hipotálamo e Hipófise 1Documento24 páginasHipotálamo e Hipófise 1Aluana Santana CarlosAinda não há avaliações
- Destilação Por Arraste A VaporDocumento5 páginasDestilação Por Arraste A VaporFellipe ChenAinda não há avaliações
- Principais processos e índices de reciclagem no Brasil e no mundoDocumento10 páginasPrincipais processos e índices de reciclagem no Brasil e no mundoLuciana NoronhaAinda não há avaliações
- Orcamento..Pontetijela - ModeloDocumento4 páginasOrcamento..Pontetijela - ModeloSamaPromoções SamaAinda não há avaliações
- 5º Ano Sistema RespiratórioDocumento2 páginas5º Ano Sistema RespiratóriorafaeltramonteAinda não há avaliações
- 1 Budesonida e Beclometasona CE e CEI ApresntaçaoDocumento12 páginas1 Budesonida e Beclometasona CE e CEI ApresntaçaoKelielson CruzAinda não há avaliações
- 28.04.2020 Decreto 64953 Estende Prazo Quarentena - 10 de MaioDocumento1 página28.04.2020 Decreto 64953 Estende Prazo Quarentena - 10 de MaioApeoespjauAinda não há avaliações
- Ficha Técnica GolDocumento1 páginaFicha Técnica GolRanieri Meireles OliveiraAinda não há avaliações
- Manual de Operação Bp2000 - Hdr20 PorDocumento212 páginasManual de Operação Bp2000 - Hdr20 PorAugusto OliveiraAinda não há avaliações
- A Neuropsicologia e A Arteterapia Como Reabilitação Nos Transtornos de Ansidedade PDFDocumento16 páginasA Neuropsicologia e A Arteterapia Como Reabilitação Nos Transtornos de Ansidedade PDFPatrícia PatyAinda não há avaliações
- Projeto Campo e MesaDocumento33 páginasProjeto Campo e MesaCida MacaúbasAinda não há avaliações
- Piovan Sseries PTDocumento2 páginasPiovan Sseries PTcaf1024Ainda não há avaliações
- Imunologia Atividade 2Documento7 páginasImunologia Atividade 2jessicaAinda não há avaliações
- Catálogo Técnico Polia de Ferro Canal V - MADEMILDocumento3 páginasCatálogo Técnico Polia de Ferro Canal V - MADEMILRobson PereiraAinda não há avaliações
- Teste 3ADocumento7 páginasTeste 3ALiliana GuimarãesAinda não há avaliações
- Catálises SayerlackDocumento2 páginasCatálises SayerlackRodrigo TeodoroAinda não há avaliações
- Slides Aula 1 - Intervenção PsicossocialDocumento22 páginasSlides Aula 1 - Intervenção PsicossocialAdriana SilvaAinda não há avaliações
- Engenharia e Meio AmbienteDocumento15 páginasEngenharia e Meio AmbientevascoinovasaoAinda não há avaliações
- Instrucao Apresentacao Projeto Transposicao Volume IIIDocumento114 páginasInstrucao Apresentacao Projeto Transposicao Volume IIIlucaslp17Ainda não há avaliações
- Argamassa Especial Superflex Ficha de SegurançaDocumento2 páginasArgamassa Especial Superflex Ficha de Segurançaabdenego velosoAinda não há avaliações
- Catalogoritz2023 PDFDocumento302 páginasCatalogoritz2023 PDFAlcides NetoAinda não há avaliações
- Pop Tuberculose 2023Documento13 páginasPop Tuberculose 2023Raquele MathiasAinda não há avaliações
- Revestimento de pisos: etapas e materiaisDocumento20 páginasRevestimento de pisos: etapas e materiaisRafael BadaueAinda não há avaliações