Escolar Documentos
Profissional Documentos
Cultura Documentos
O Processo de Haber Bosch
Enviado por
Karla RomãoDireitos autorais
Formatos disponíveis
Compartilhar este documento
Compartilhar ou incorporar documento
Você considera este documento útil?
Este conteúdo é inapropriado?
Denunciar este documentoDireitos autorais:
Formatos disponíveis
O Processo de Haber Bosch
Enviado por
Karla RomãoDireitos autorais:
Formatos disponíveis
Processo de Haber Bosch Produo Industrial da Amnia
O processo de Haber (tambm conhecido como Processo Haber-Bosch) uma reao entre nitrognio e hidrognio para produzir amonaco. Esta reao catalisada com o ferro, sob as condies de 200 atmosferas de presso e uma temperatura de 450 C.: N2(g) + 3H2(g) 2NH3(g) + energia H = -92,22 Kj
O processo foi desenvolvido por Fritz Haber e Carl Bosch em 1909 e patenteado em 1910. Foi usado pela primeira vez, escala industrial, na Alemanha durante a Primeira Guerra Mundial. Para a produo de munio os alemes dependiam do nitrato de sdio importado do Chile, que era insuficiente e incerto. Por isso passaram a utilizar prontamente o processo de Haber para a produo de amonaco. Atualmente, a amnia muito utilizada na indstria. Ela serve como material de partida de compostos importantes, tais como pesticidas e fertilizantes, tambm est presente nas formulaes de tintas de cabelo que so muito vendidas atualmente. Se fssemos simplesmente sintetizar amnia a partir do nitrognio e do oxignio obteramos muito pouco produto, pois esta reao tem um rendimento muito baixo. Alm disso, esta reao muito lenta e como as indstrias querem produtividade, no se pode esperar muito tempo para a reao se processar.Para sintetizar a amnia industrialmente, a partir do nitrognio e do hidrognio, uma maneira conveniente aumentar a velocidade da reao, utilizando um catalisador, por exemplo. Para a produo da amnia, o nitrognio obtido do ar atmosfrico, e o hidrognio como resultado da reao entre a gua e o gs natural: Fritz Haber ganhou o prmio CH4(g) + H2O(g) CO(g) + 3H2(g) Nobel por viabilizar a sntese da amnia. Condies de equilbrio do processo A reao entre nitrognio e hidrognio reversvel, portanto, o rendimento na produo do amonaco depende de algumas condies: Temperatura A formao da amnia, apesar de muito lenta, exotrmica. Assim, poderamos imaginar que se aumentarmos a temperatura do sistema, a reao se deslocaria na formao de nitrognio e hidrognio. Assim como, se diminuirmos a temperatura, a reao se deslocaria na formao de mais amnia. No entanto, quando aquecemos o sistema reacional, podemos aumentar a velocidade da reao, pois a baixas temperaturas a reao to lenta que perderamos muito tempo com esta reao. Sendo assim, baixas temperaturas favorecem a produo do NH3 e o incremento da temperatura tende a deslocar o equilbrio da reao no sentido inverso, de acordo com o Princpio de Le Chatelier. Por outro lado, a reduo da temperatura diminui a velocidade da reao, portanto, uma temperatura intermdia a ideal para favorecer o processo. Experincias demonstraram que a temperatura ideal de 450 C. Presso Se aumentarmos a temperatura, o equilbrio se deslocar na formao de nitrognio e oxignio, o que desfavorvel, assim podemos aumentar a presso, o que faz com que a produo de amnia tambm aumente, pois a alta presso faz com que o equilbrio se desloque no sentido de menor volume de gs. Uma forma de aumentar o rendimento remover a amnia e isto feito em muitas indstrias do mundo. Logo, o incremento da presso aumenta o rendimento de formao do produto, mas por outro lado este incremento deve ser economicamente vivel, ou seja, no deve tornar os custos de produo demasiado elevados. A presso considerada tecnicamente e economicamente vivel de 200 atmosferas.
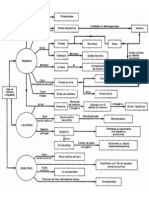
Catalisador: O catalisador no afeta o equilbrio, porm, acelera a velocidade da reao para atingir o equilbrio. A adio de um catalisador permite que o processo se desenvolva favoravelmente em temperaturas mais baixas. No incio, para a reao Haber-Bosch, usava-se o smio e urnio como catalisadores. Atualmente, utiliza-se de maneira extensiva o ferro. Na indstria, o ferro cataltico preparado pela exposio da magnetita, um xido de ferro, ao hidrognio aquecido. A magnetita reduzida a ferro metlico com a eliminao do oxignio no processo. A amnia formada um gs, porm, refrigerando e sob alta presso obtm-se num estado liquefeito. Nestas condies, sob a forma lquida, no ocorre reversibilidade, ou seja, a reao de decomposio em nitrognio e hidrognio no acontece. Repare que esta equao de formao da amnia no estado gasoso, veja agora alguns procedimentos da produo artificial de amnia lquida: 1. Uma mistura gasosa de N2 e H2 colocada em um reator; 2. Ao reagir e atingir o equilbrio, a mistura de N2 e H2 transferida para um condensador; 3. Nesta etapa a amnia formada se encontra no estado gasoso: NH3(g), mas quando passa pelo condensador se converte em lquida; 4. Estando a amnia liquefeita ento retirada e pode ser usada.
Você também pode gostar
- Processo de Ostwald Na Indústria QuímicaDocumento13 páginasProcesso de Ostwald Na Indústria QuímicaVOLDI MANUEL VM100% (2)
- Indústria Amônia e Ácido NítricoDocumento22 páginasIndústria Amônia e Ácido NítricoNan CiprianoAinda não há avaliações
- Produção de amônia e ácido nítrico por métodos clássicos e modernosDocumento26 páginasProdução de amônia e ácido nítrico por métodos clássicos e modernosJéssica Hamada50% (2)
- Proposta de Planta de Amônia no ESDocumento22 páginasProposta de Planta de Amônia no ESalexnoticias100% (1)
- AmôniaDocumento18 páginasAmôniaJoao MarcosAinda não há avaliações
- Obtenção e caracterização da amôniaDocumento17 páginasObtenção e caracterização da amôniaNayara SaldanAinda não há avaliações
- Indústrias do nitrogênio: amônia, cianamida, uréia e fertilizantesDocumento26 páginasIndústrias do nitrogênio: amônia, cianamida, uréia e fertilizantesMichel H RAinda não há avaliações
- Produção e Aplicações do Ácido FosfóricoDocumento23 páginasProdução e Aplicações do Ácido FosfóricoJoao Marcos100% (2)
- Processos químicos da indústria carboquímicaDocumento23 páginasProcessos químicos da indústria carboquímicaIoanna DutraAinda não há avaliações
- Produção do álcool industrialDocumento10 páginasProdução do álcool industrialFábioRibeiroPinheiroAinda não há avaliações
- Introdução aos Processos Químicos - 5a Lista de ExercíciosDocumento3 páginasIntrodução aos Processos Químicos - 5a Lista de ExercíciosNáthaly CoelhoAinda não há avaliações
- Aula1 de PROCESSOS INDUSTRIAIS ORGÂNICOSDocumento24 páginasAula1 de PROCESSOS INDUSTRIAIS ORGÂNICOSPaulo Victor SouzaAinda não há avaliações
- Apresentacao Biotecnologia - BiolixiviaçãoDocumento37 páginasApresentacao Biotecnologia - BiolixiviaçãoGuilherme Rodrigues100% (1)
- Aula Produção de Etanol - Materia PrimaDocumento26 páginasAula Produção de Etanol - Materia PrimaRosana Galev OliveiraAinda não há avaliações
- Derivados Petroquímicos do PropenoDocumento6 páginasDerivados Petroquímicos do PropenoAlexandre WakanoAinda não há avaliações
- O que é óleo fúsel: composição, origem e aplicaçõesDocumento8 páginasO que é óleo fúsel: composição, origem e aplicaçõesluizugaAinda não há avaliações
- Processo de Fabricação de Materiais Poliméricos na FATEC-BADocumento3 páginasProcesso de Fabricação de Materiais Poliméricos na FATEC-BARodrigo FerreiraAinda não há avaliações
- Síntese de Ésteres de FrutasDocumento16 páginasSíntese de Ésteres de FrutasGlaucio TestaAinda não há avaliações
- Aula Obtenção Do Enxofre e Ácido SulfúricoDocumento31 páginasAula Obtenção Do Enxofre e Ácido SulfúricoGriff DGriffAinda não há avaliações
- Apresentação N2 ProfDocumento22 páginasApresentação N2 ProfIsaac AngeloAinda não há avaliações
- Síntese do Salicilato de MetilaDocumento7 páginasSíntese do Salicilato de MetilaJenniferCarvalhoAinda não há avaliações
- Destilação: separação por diferença de ponto de ebuliçãoDocumento78 páginasDestilação: separação por diferença de ponto de ebuliçãoEduardo CastroAinda não há avaliações
- Preparação do corante laranja de metilaDocumento5 páginasPreparação do corante laranja de metilaEziquielMartinsAinda não há avaliações
- Relatório BoroDocumento5 páginasRelatório Borosuelen pinheiroAinda não há avaliações
- Volumetria de Oxi - Redução Grupo 8Documento14 páginasVolumetria de Oxi - Redução Grupo 8carlosmauriciopereiraAinda não há avaliações
- Produção de óxido de etilenoDocumento52 páginasProdução de óxido de etilenofernandoibalves100% (1)
- Prática Destilação - UFVDocumento8 páginasPrática Destilação - UFVMateus TomazAinda não há avaliações
- Processos de Saponificação e DetergênciaDocumento7 páginasProcessos de Saponificação e DetergênciaJosiel Dimas FroehlichAinda não há avaliações
- Processos de carvão mineral e suas aplicaçõesDocumento10 páginasProcessos de carvão mineral e suas aplicaçõesunholy_confessionsAinda não há avaliações
- Relatório AdsorçãoDocumento7 páginasRelatório Adsorçãogabianunes3Ainda não há avaliações
- Relatório - Obtenção de BiodieselDocumento10 páginasRelatório - Obtenção de BiodieselAmanda AlmerindoAinda não há avaliações
- Oxidação Lipídica E Antioxidantes Extraídos De Fontes NaturaisNo EverandOxidação Lipídica E Antioxidantes Extraídos De Fontes NaturaisAinda não há avaliações
- Relatório - Álcool em GelDocumento15 páginasRelatório - Álcool em GelJeff SilvaAinda não há avaliações
- A Utilização De Material Lignocelulósico Na Produção De BioetanolNo EverandA Utilização De Material Lignocelulósico Na Produção De BioetanolAinda não há avaliações
- Slide 02 - (Indústria Química)Documento40 páginasSlide 02 - (Indústria Química)Rodrigo dos Santos BritoAinda não há avaliações
- Síntese da ftalimidaDocumento10 páginasSíntese da ftalimidaPaulo Roberto Vieira de CastroAinda não há avaliações
- Relatório - NITROGÊNIO AMONIACALDocumento10 páginasRelatório - NITROGÊNIO AMONIACALPedro Henrique AlmeidaAinda não há avaliações
- Processos Químicos Industriais Ácido Sulfúrico e FosfóricoDocumento38 páginasProcessos Químicos Industriais Ácido Sulfúrico e FosfóricoKaio Ferreira100% (1)
- 12 - UstulaçãoDocumento37 páginas12 - UstulaçãoNicolas Mamede0% (1)
- Técnicas EDTA PDFDocumento9 páginasTécnicas EDTA PDFAlessandrafsaAinda não há avaliações
- Pratica 1 - Destilacao SimplesDocumento3 páginasPratica 1 - Destilacao SimplesLuisAinda não há avaliações
- Umidificação e DesumidificaçãoDocumento31 páginasUmidificação e DesumidificaçãoWall LimaAinda não há avaliações
- Processo de Obtenção - Ácido SulfricoDocumento24 páginasProcesso de Obtenção - Ácido Sulfricoquimicaufu100% (2)
- Curva destilação gasolinaDocumento5 páginasCurva destilação gasolinaAndré Luís Della VolpeAinda não há avaliações
- Determinação de sulfato por gravimetria e espectrofotometriaDocumento21 páginasDeterminação de sulfato por gravimetria e espectrofotometriaIngrid Vasconcelos0% (1)
- Obtenção da anilina por hidrogenação do nitrobenzenoDocumento29 páginasObtenção da anilina por hidrogenação do nitrobenzenoThaynara MotaAinda não há avaliações
- APOSTILA QUI INORGÂNICA Parte2 1Documento33 páginasAPOSTILA QUI INORGÂNICA Parte2 1Danilo CoelhoAinda não há avaliações
- Principais conversões químicasDocumento16 páginasPrincipais conversões químicasNiltonBragaAinda não há avaliações
- Síntese AASDocumento3 páginasSíntese AASthiagomaddAinda não há avaliações
- Lei de Lambert-Beer confirmada por espectrofotometriaDocumento6 páginasLei de Lambert-Beer confirmada por espectrofotometriaisabellaAinda não há avaliações
- ALARANJADODocumento10 páginasALARANJADOEdna AzevedoAinda não há avaliações
- Fluxograma - Processo de Produção de Fertilizante Nitrato de AmonioDocumento1 páginaFluxograma - Processo de Produção de Fertilizante Nitrato de AmonioAmanda OliveiraAinda não há avaliações
- Gravimetria por precipitação - Exercícios de Química Analítica 2Documento4 páginasGravimetria por precipitação - Exercícios de Química Analítica 2Laisa SilvaAinda não há avaliações
- Capitulo 1 Processos Unitários Orgânicos IntroduçãoDocumento52 páginasCapitulo 1 Processos Unitários Orgânicos IntroduçãoEveline BuenoAinda não há avaliações
- Projeto de Controle de Poluentes AtmosféricosDocumento11 páginasProjeto de Controle de Poluentes AtmosféricosRafael Antonio PazzaAinda não há avaliações
- Preparo e Padronização de NaOHDocumento3 páginasPreparo e Padronização de NaOHÉrika FernandesAinda não há avaliações
- Síntese de partículas esféricas de catalisadores Ziegler-Natta contendo argilaDocumento6 páginasSíntese de partículas esféricas de catalisadores Ziegler-Natta contendo argilaGenilson E Neliane Silva100% (1)
- Reatores Químicos em Leito Fluidizado: modelagem e simulaçãoNo EverandReatores Químicos em Leito Fluidizado: modelagem e simulaçãoAinda não há avaliações
- Avaliação da erva-mate como biossorventeNo EverandAvaliação da erva-mate como biossorventeAinda não há avaliações
- QAI, COV, Poluição e Nano TiO2: estudo de fotodegradação de benzeno por nano TiO2 em revestimento cerâmico comercial e assistida por radiação ultravioletaNo EverandQAI, COV, Poluição e Nano TiO2: estudo de fotodegradação de benzeno por nano TiO2 em revestimento cerâmico comercial e assistida por radiação ultravioletaAinda não há avaliações
- Exercício para Fixação Do VocabulárioDocumento1 páginaExercício para Fixação Do VocabulárioKarla RomãoAinda não há avaliações
- O Refrigerador DomésticoDocumento1 páginaO Refrigerador DomésticoKarla RomãoAinda não há avaliações
- A Matriz BCGDocumento2 páginasA Matriz BCGKarla RomãoAinda não há avaliações
- Sensação térmica após mergulho em água quente e friaDocumento1 páginaSensação térmica após mergulho em água quente e friaKarla RomãoAinda não há avaliações
- A vida celular emDocumento2 páginasA vida celular emKarla RomãoAinda não há avaliações
- Indices de Prazos MediosDocumento3 páginasIndices de Prazos MediosKarla RomãoAinda não há avaliações
- Processo Haber-Bosch produz amôniaDocumento2 páginasProcesso Haber-Bosch produz amôniaKarla RomãoAinda não há avaliações
- Inscrição Nome Cargo ResultadoDocumento34 páginasInscrição Nome Cargo ResultadoIvo JoseAinda não há avaliações
- Cálculo do Nível de Ruído EquivalenteDocumento6 páginasCálculo do Nível de Ruído Equivalentehallyson123Ainda não há avaliações
- Farmacêutico clínico: atribuições e especializaçõesDocumento2 páginasFarmacêutico clínico: atribuições e especializaçõesJacson JúniorAinda não há avaliações
- AVA 2 - Processos DecisóriosDocumento2 páginasAVA 2 - Processos DecisóriosJessicaAinda não há avaliações
- Sistemas de Esgoto Faculdades DoctumDocumento18 páginasSistemas de Esgoto Faculdades DoctumKILDER CRISTIANO SILVEIRAAinda não há avaliações
- C 2 LTD WXH ZG8 T Mi 0 y MDIz LW1 HD GVT YXRp Y2 Ex NDA3 MJ Ay M1 QX MJ U5Documento22 páginasC 2 LTD WXH ZG8 T Mi 0 y MDIz LW1 HD GVT YXRp Y2 Ex NDA3 MJ Ay M1 QX MJ U5Jhean MonteiroAinda não há avaliações
- O acordar do cortiçoDocumento2 páginasO acordar do cortiçoLucas Veiga ChiesorinAinda não há avaliações
- Direito de Urbanismo e de AmbienteDocumento4 páginasDireito de Urbanismo e de Ambientejoana silvaAinda não há avaliações
- Campinas, SP: Editora Da UNICAMP, 2005.: Linsu KimDocumento2 páginasCampinas, SP: Editora Da UNICAMP, 2005.: Linsu KimMARCOS VINICIUS SOARES LOPESAinda não há avaliações
- Caderno Técnico FAG - 2006 Sintomas, Causas, Soluções Oficina de RolamentosDocumento24 páginasCaderno Técnico FAG - 2006 Sintomas, Causas, Soluções Oficina de RolamentosBrunoMoreiraAinda não há avaliações
- Projeto ...Documento12 páginasProjeto ...Barbara GuimarãesAinda não há avaliações
- Questões Semana 4Documento5 páginasQuestões Semana 4Eduardo MullerAinda não há avaliações
- Principais DoencasDocumento34 páginasPrincipais DoencasNádia Cristina de OliveiraAinda não há avaliações
- (Versão Extendida) Ata Da Assembleia Geral Dos Estudantes Da Uefs 06.10.2023Documento7 páginas(Versão Extendida) Ata Da Assembleia Geral Dos Estudantes Da Uefs 06.10.2023Avila CruzAinda não há avaliações
- Aristoteles Metafisica Trad-Vallandro Livros-01-02 No-Intro 2pp TuiDocumento18 páginasAristoteles Metafisica Trad-Vallandro Livros-01-02 No-Intro 2pp TuiClara CruzAinda não há avaliações
- Eletros PotenciaDocumento4 páginasEletros Potenciaericofelipe81Ainda não há avaliações
- Avaliação Geografia - Ii BimestreDocumento4 páginasAvaliação Geografia - Ii BimestreVerônica de Fátima Gonçalves AlvesAinda não há avaliações
- Plano de Aula 01Documento2 páginasPlano de Aula 01Emeb Armindo De Arruda CamposAinda não há avaliações
- Apostila RESUMO RANGÉ E KNAPP TCCDocumento31 páginasApostila RESUMO RANGÉ E KNAPP TCCRebecca DornelesAinda não há avaliações
- Avaliação de MarcosDocumento19 páginasAvaliação de MarcosGabrielly GoncalvesAinda não há avaliações
- Informacoes MBA em Ciencias de Dados Turma 2022Documento24 páginasInformacoes MBA em Ciencias de Dados Turma 2022Nícolas LaraAinda não há avaliações
- Unidade 2Documento26 páginasUnidade 2LucivanioJatobaAinda não há avaliações
- Lista de Exercícios 1 - Propriedades Dos Fluidos e Estática Dos FluidosDocumento6 páginasLista de Exercícios 1 - Propriedades Dos Fluidos e Estática Dos FluidosMárcio Ferreira do NascimentoAinda não há avaliações
- ABNT NBR 5419-1: Princípios gerais de proteção contra descargas atmosféricasDocumento78 páginasABNT NBR 5419-1: Princípios gerais de proteção contra descargas atmosféricasCleber Souza de OliveiraAinda não há avaliações
- Now Youre Mine - Morgan Bridges 1710985082991-PortuguêsDocumento102 páginasNow Youre Mine - Morgan Bridges 1710985082991-PortuguêsmeduardabragAinda não há avaliações
- Poder de Convencimento - Parte III: LiderançaDocumento17 páginasPoder de Convencimento - Parte III: LiderançaVitoria Camargo da SilvaAinda não há avaliações
- Ensaios de Agregados e AglomerantesDocumento9 páginasEnsaios de Agregados e AglomerantesNatoRenatoAinda não há avaliações
- Planejamento Do Maternal I - A (Férias)Documento10 páginasPlanejamento Do Maternal I - A (Férias)Luana Daniel da SilvaAinda não há avaliações
- O Anus Solar - Georges Bataille-Páginas-12-16Documento5 páginasO Anus Solar - Georges Bataille-Páginas-12-16Andriolli CostaAinda não há avaliações
- Horários das aulas presenciais do curso de ensino em inglêsDocumento4 páginasHorários das aulas presenciais do curso de ensino em inglêsWilliamAinda não há avaliações