Escolar Documentos
Profissional Documentos
Cultura Documentos
Previo Prop Coligativas
Enviado por
Enzo YaelDireitos autorais
Formatos disponíveis
Compartilhar este documento
Compartilhar ou incorporar documento
Você considera este documento útil?
Este conteúdo é inapropriado?
Denunciar este documentoDireitos autorais:
Formatos disponíveis
Previo Prop Coligativas
Enviado por
Enzo YaelDireitos autorais:
Formatos disponíveis
Previo Prop.
Coligativas Ortiz Ortuo Yael
1. Investigar los conceptos de soluto, disolvente y disolucin. Soluto: se llama soluto a la sustancia minoritaria en una disolucin, esta sustancia se encuentra disuelta en un determinado disolvente. Tambin se le conoce como la sustancia que se disuelve, por lo que se puede encontrar en un estado de agregacin diferente al comienzo del proceso de disolucin. Disolvente: es una sustancia liquida que disuelve o disocia a otra sustancia en una forma ms elemental, y que normalmente est presente en mayor cantidad que esa otra sustancia. Disolucin: es la mezcla homognea resultante tras disolver cualquier sustancia en un lquido.
2. Explicar que es una disolucin ideal de no electrolito. Una disolucin ideal es aquella que obedece a la Ley de Raoult, la cual establece que la presin de vapor del disolvente en la disolucin es igual a la presin de vapor del disolvente puro multiplicada por la fraccin mol del disolvente. La presin parcial de un disolvente sobre una disolucin P1 est dada por la presin de vapor del disolvente puro Po1, multiplicada por la fraccin molar del disolvente en la disolucin X1. P_1 = X_1 P^o_1 Es decir que la presin de vapor del soluto crece linealmente con su fraccin molar. En una solucin que slo contenga un soluto, se tiene que X1=1-X2, donde X2 es la fraccin molar del soluto, pudiendo escribir la formulacin de la ley como: P_1 = \left( 1- X_2\right) P^o_1 P^o_1 - P_1 = \Delta P = X_2 P^o_1
Se puede ver de esta forma que una disminucin en la presin de vapor, P es directamente proporcional a la concentracin del soluto presente Una disolucin de no electrlitos es aquella que no conduce la electricidad, ya que no genera iones. Conduce altamente la electricidad, ya que contiene iones completamente disociados.
Previo Prop. Coligativas Ortiz Ortuo Yael
3. Definir el trmino molalidad e indicar qu unidades tiene. La molalidad (m) es el numero de moles de soluto disueltos en 1 kg (1000 g) de un disolvente.
Por lo tanto las unidades de la molalidad es: mol/kg
4. De qu factores dependen las propiedades coligativas de disoluciones de no electrolitos? Las propiedades coligativas de las soluciones dependen de la concentracin total de partculas de soluto, sin importar si las partculas son iones o molculas.
5. Explicar que es una curva de enfriamiento y cul es su utilidad. Las curvas de enfriamiento son una representacin grfica de la temperatura de un material frente al tiempo conforme este se enfra. Ej.: cuando se elimina calor de una masa de agua pura a velocidad constante, su temperatura desciende hasta alcanzar los 0 grados C, momento eque empieza a separarse el hielo. La temperatura permanece constante hasta que toda el agua es transformada en hielo porque el calor se elimina de la masa del agua en forma de calor latente de cambio de estado. Despus de la formacin total de hielo, la temperatura desciende de nuevo. La presencia de solutos disueltos cambia la curva de enfriamiento del agua como consecuencia del descenso crioscpico 6. Calcular la cantidad de soluto- (a) urea, (b) dextrosa que se requiere para preparar 25 ml de una disolucin 1.0 m.
Você também pode gostar
- Termodinámica de Soluciones PoliméricasDocumento10 páginasTermodinámica de Soluciones PoliméricasEnzo YaelAinda não há avaliações
- Conclusion Propia KNO3Documento1 páginaConclusion Propia KNO3Enzo YaelAinda não há avaliações
- Ejercicios Genetica MendelDocumento2 páginasEjercicios Genetica MendelEnzo YaelAinda não há avaliações
- Genética de gatos: alelos dominantes para orejas rizadas y color negroDocumento1 páginaGenética de gatos: alelos dominantes para orejas rizadas y color negroEnzo YaelAinda não há avaliações
- Compuestos Volátiles de La Rancidez Oxidativa ResumenDocumento1 páginaCompuestos Volátiles de La Rancidez Oxidativa ResumenEnzo YaelAinda não há avaliações
- Celdas Galvánicas o Celdas VoltaicasDocumento9 páginasCeldas Galvánicas o Celdas VoltaicasEnzo YaelAinda não há avaliações
- Betas y PKD S-CorrDocumento7 páginasBetas y PKD S-CorrEnzo YaelAinda não há avaliações
- Nutricion IDR y ToxicidadDocumento2 páginasNutricion IDR y ToxicidadEnzo YaelAinda não há avaliações
- Práctica 03Documento5 páginasPráctica 03Enzo YaelAinda não há avaliações
- Conclusión Prac 8Documento1 páginaConclusión Prac 8Enzo YaelAinda não há avaliações
- Cuestionario 2-Productos Cárnicos FermentadosDocumento1 páginaCuestionario 2-Productos Cárnicos FermentadosEnzo YaelAinda não há avaliações
- Cuestionario Análisis y Discusión de ResultadosDocumento4 páginasCuestionario Análisis y Discusión de ResultadosEnzo YaelAinda não há avaliações
- Matriz de Planificacion Del Nectar de MangoDocumento2 páginasMatriz de Planificacion Del Nectar de MangoEnzo YaelAinda não há avaliações
- Geometría 1Documento10 páginasGeometría 1Enzo YaelAinda não há avaliações
- PRevio 8Documento4 páginasPRevio 8Enzo YaelAinda não há avaliações
- Pract Prop Coligativas ElectrolitosDocumento15 páginasPract Prop Coligativas ElectrolitosEnzo YaelAinda não há avaliações
- Practica Casi CompletaDocumento10 páginasPractica Casi CompletaEnzo YaelAinda não há avaliações
- Compuestos Volátiles de La Rancidez Oxidativa ResumenDocumento1 páginaCompuestos Volátiles de La Rancidez Oxidativa ResumenEnzo YaelAinda não há avaliações
- Re Acci OnesDocumento2 páginasRe Acci OnesEnzo YaelAinda não há avaliações
- Serie 05 (3 Hojas)Documento3 páginasSerie 05 (3 Hojas)Adam VangAinda não há avaliações
- Presión de vapor y equilibrio de fasesDocumento3 páginasPresión de vapor y equilibrio de fasesEnzo YaelAinda não há avaliações
- Cuestionario Análisis y Discusión de ResultadosDocumento4 páginasCuestionario Análisis y Discusión de ResultadosEnzo YaelAinda não há avaliações
- Plantilla para Ensayos de Divulgacion CientificaDocumento3 páginasPlantilla para Ensayos de Divulgacion CientificaAldrick HbAinda não há avaliações
- Resultados, Tablas, Graficas, Analisis.Documento3 páginasResultados, Tablas, Graficas, Analisis.Enzo YaelAinda não há avaliações
- Aldo LesDocumento5 páginasAldo LesEnzo YaelAinda não há avaliações
- Las Bandas Del Grupo Nitro Practica 7Documento1 páginaLas Bandas Del Grupo Nitro Practica 7Enzo YaelAinda não há avaliações
- Tipos de CancerDocumento1 páginaTipos de CancerEnzo YaelAinda não há avaliações
- Dioses LatinDocumento2 páginasDioses LatinEnzo YaelAinda não há avaliações
- IntroDocumento1 páginaIntroEnzo YaelAinda não há avaliações
- CORRECCIÓN - Orimet - Ameno Ameno - Latire - Latiremo - OrimetDocumento4 páginasCORRECCIÓN - Orimet - Ameno Ameno - Latire - Latiremo - OrimetCarlos Abelardo Becerra BermúdezAinda não há avaliações
- Muestreo Discrecional o Por JuicioDocumento3 páginasMuestreo Discrecional o Por JuicioJorge Javier Granda Granadino100% (1)
- Laboratorio 03 - Cisco Packet Tracer 5.3.2, Instalación y Unos EjerciciosDocumento22 páginasLaboratorio 03 - Cisco Packet Tracer 5.3.2, Instalación y Unos EjerciciosJhon Huaringa0% (1)
- Reparar TV Que No Enciende PDFDocumento7 páginasReparar TV Que No Enciende PDFluisAinda não há avaliações
- Ast T-Set 017 Instalacion de Interruptor de Potencia Con Camión GrúaDocumento3 páginasAst T-Set 017 Instalacion de Interruptor de Potencia Con Camión GrúaCarlos RodasAinda não há avaliações
- Catalogo Productos ImexoilDocumento6 páginasCatalogo Productos ImexoilEdwin KaNaAinda não há avaliações
- PRACTICA N°10 YilmerDocumento20 páginasPRACTICA N°10 YilmerCARLOS ENRIQUE DOMINGUEZ PALACIOSAinda não há avaliações
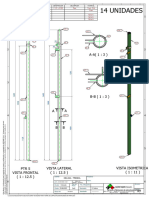
- Planos de Parantes de Dos y MediaDocumento5 páginasPlanos de Parantes de Dos y Mediassoma serfabriAinda não há avaliações
- Diagrama de Análisis Del Proceso Actual OkDocumento2 páginasDiagrama de Análisis Del Proceso Actual OkJose TapiaAinda não há avaliações
- Sistema Job Shop-Flow ShopDocumento2 páginasSistema Job Shop-Flow ShopGisela GonzalezAinda não há avaliações
- Ahd1 Ra2 PRG PRCS ContinuosDocumento3 páginasAhd1 Ra2 PRG PRCS ContinuosJosue AguilarAinda não há avaliações
- IACC Investigacion de Operacionestarea Semana4Documento6 páginasIACC Investigacion de Operacionestarea Semana4Toledo Miguel50% (2)
- Aluviales Expo 3 ParcialDocumento15 páginasAluviales Expo 3 ParcialJULIA HUAMANI HUARACAAinda não há avaliações
- Transistor de Unión BipolarDocumento30 páginasTransistor de Unión BipolarGerwin AlcalaAinda não há avaliações
- Nte Inen 2956 PDFDocumento13 páginasNte Inen 2956 PDFDaniel MaGaAinda não há avaliações
- Requerimientos Instalacion ElectricaDocumento14 páginasRequerimientos Instalacion ElectricasalgoraAinda não há avaliações
- Practica 2 El Perfil Del SueloDocumento3 páginasPractica 2 El Perfil Del SueloPablo Muñoz CastellanosAinda não há avaliações
- Manual operación y mantenimiento malacate planetarioDocumento16 páginasManual operación y mantenimiento malacate planetarioEliodoro SardinhaAinda não há avaliações
- GIMPDocumento8 páginasGIMPraul francisco avila medinaAinda não há avaliações
- Invent A RiosDocumento9 páginasInvent A RiosYss NarváezAinda não há avaliações
- Informe de Nivelacion CerradaDocumento25 páginasInforme de Nivelacion CerradaMaikol Medrano50% (2)
- Estructura Filtro LentoDocumento3 páginasEstructura Filtro LentoLouis AlbertAinda não há avaliações
- PA3 Geometria TerminadoDocumento26 páginasPA3 Geometria TerminadoRobertoespinozaq100% (1)
- Catalogo Herramientas Bosch PDFDocumento50 páginasCatalogo Herramientas Bosch PDFRebeca AlvarezAinda não há avaliações
- MEDICION de Sensibilidad12 DB 2Documento3 páginasMEDICION de Sensibilidad12 DB 2David Israel Escorza UribeAinda não há avaliações
- Concentrado estimado de obra de introducción de red de drenaje sanitarioDocumento1 páginaConcentrado estimado de obra de introducción de red de drenaje sanitarioRuben CM100% (1)
- McCormack 4.2Documento3 páginasMcCormack 4.2SVGC870Ainda não há avaliações
- Administración de niveles de servicio TIDocumento2 páginasAdministración de niveles de servicio TIAhmed Yamil Chadid EstradaAinda não há avaliações
- Centro de Formación Tumbaco ServDocumento13 páginasCentro de Formación Tumbaco ServGianFranco De La Cruz LamaAinda não há avaliações
- Ensayo de Propiedades de Cimentacion de Diferentes Tipos de Suelo y RocasDocumento10 páginasEnsayo de Propiedades de Cimentacion de Diferentes Tipos de Suelo y RocasFernandaTuzAinda não há avaliações