Escolar Documentos
Profissional Documentos
Cultura Documentos
Neurobiología de La Adicción PDF
Enviado por
myfreudDescrição original:
Título original
Direitos autorais
Formatos disponíveis
Compartilhar este documento
Compartilhar ou incorporar documento
Você considera este documento útil?
Este conteúdo é inapropriado?
Denunciar este documentoDireitos autorais:
Formatos disponíveis
Neurobiología de La Adicción PDF
Enviado por
myfreudDireitos autorais:
Formatos disponíveis
MAQUETA RET 18 21/12/1999 17:16 Pgina 15
Neurobiologa de la adiccin
Roy A. Wise
Las drogas adictivas tienen unos mecanismos de creacin de hbito que se pueden localizar en diferentes
regiones del cerebro. Avances recientes en el mayor conocimiento de las "zonas de estallido" qumicas, en las que
drogas individuales de abuso inician su actividad de formacin de hbito, han revelado que drogas tan dispares
como la herona, la cocana, la nicotina, el alcohol, la fenciclidina y el canabis activan un mismo sistema de circuitos de recompensa en el cerebro. Aunque estas drogas
tengan unos mecanismos muy distintos, sus mecanismos
de formacin de hbito (y quizs los elementos relevantes
de sus dispares sntomas de abstinencia) se presentan con
un denominador comn, a saber, unos efectos similares en
los mecanismos de recompensa del cerebro.
Introduccin
La adiccin ofrece un modelo interesante de conducta motivada. En realidad, ofrece un modelo interesante del
papel de la motivacin en la conducta de adaptacin, pese
al hecho de que tal adiccin se cree generalmente que
refleja un comportamiento de mala adaptacin. Como las
propiedades de creacin de hbito de las drogas de abuso
se han ido vinculando cada vez ms a los mecanismos del
sistema de circuitos cerebral, que se producen en servicio
de gratificaciones ms naturales como son la comida o la
relacin sexual(1), la adiccin est siendo objeto de inters
creciente entre los neurocientficos. Incluso las teoras de
"dependencia" de la droga, dominadas durante mucho
tiempo por el estudio de tejidos perifricos y por adaptaciones drogo-inducidas del sistema nervioso autnomo,
han comenzado recientemente a enfocar unos fenmenos
de abandono ms sutiles, que producen adaptaciones dentro del propio sistema de circuitos central de recompensa.
Al igual que las vas endgenas de control del dolor conforman el marco de referencia dentro del que comprendeRET, Revista de Toxicomanas. N. 18 1999
mos los efectos analgsicos de los opiceos, as tambin
los circuitos endgenos de recompensa son el marco de
referencia dentro del cual podemos comprender mejor los
efectos de formacin de hbito de las distintas drogas de
abuso.
En este estudio examinar los puntos del cerebro en
donde distintas drogas adictivas desencadenan sus mecanismos de formacin de hbito y los circuitos anatmicos
que conectan tales puntos. Estudiar as mismo los sndromes de abstinencia que estn patentes en ese sistema de
circuitos, y mencionar tambin una serie de cuestiones
emergentes en el campo de la neurobiologa de la adiccin.
Marco de referencia
La historia de la primera poca de la investigacin
sobre la adiccin estaba dominada por los intentos de comprender el fundamento celular de los fenmenos de drogodependencia(2), fenmenos que aparecen reflejados a
menudo en los tejidos del intestino o del sistema nervioso
autnomo. Lo que crea la mayora era que la autoadministracin compulsiva de droga llegaba a dominar el comportamiento de los animales fisiolgicamente dependientes,
por la capacidad de la droga para aliviar los sndromes de
abstinencia aversivos. Esto constituye un modelo de adiccin de "refuerzo negativo"(2), en el que se resalta el papel
de la droga para aliviar los estados de aversin asociados
con la disforia, ms que el papel de la droga para producir
estados positivos asociados, al menos en ocasiones, con la
euforia. Los avances ms recientes en la teora de la adiccin han subrayado el papel del sistema nervioso central en
mediar el refuerzo positivo y la euforia(3-7).
Bastantes factores han contribuido a la percepcin
actual de que los secretos de la adiccin deben de conocerse a partir del estudio de los mecanismos de recompensa del cerebro, que identificaron por primera vez Olds
15
MAQUETA RET 18 21/12/1999 17:16 Pgina 16
y Milner(8), utilizando la estimulacin elctrica del cerebro,
y que heursticamente, o por simplicidad, denominaron
"centros de placer en el cerebro"(9). Olds lleg pronto a la
conclusin de que haba descubierto unos mecanismos
cerebrales implicados en el refuerzo positivo, y tal conclusin se sigue manteniendo todava ampliamente. Tena
varias razones originales: la estimulacin daba recompensa en animales felices y sanos, y no satisfaca ningn estado de necesidad fisiolgica evidente (en efecto, si cabe,
ms que satisfacer induca los impulsos generalmente asociados a las necesidades fisiolgicas); el efecto de recompensa de la estimulacin no disminua con la saciedad, ni
se intensificaba con la privacin; y los animales preferan
ignorar las recompensas habituales de comida, y en lugar
de eso trabajar hasta la muerte por privacin de alimentos autoinflingida- por la estimulacin recompensante del
hipotlamo.
Mientras Olds y los otros delineaban los mecanismos
cerebrales, que presuponan que servan de base al refuerzo positivo, se estaban desarrollando unos mtodos que
permitan a unos animales libres de movimientos llegar a
unas inyecciones intravenosas de drogas. Con el desarrollo de esta tecnologa, los farmaclogos del comportamiento empezaron a caracterizar unas drogas, en trminos
del concepto de Skinner del refuerzo operativo que se fundamentaba en la fenomenologa de los hbitos que creaban. La farmacologa del comportamiento de la autoadministracin de drogas por va intravenosa se estudi
ampliamente en animales que tenan un acceso intermitente a substancias adictivas; esto se hizo en parte por la conveniencia de los experimentadores, y en parte porque los
animales que tenan un acceso directo las 24 horas a estimulantes intravenosos como consecuencia enseguida
moran. De tales estudios, rpidamente se lleg a la conclusin de que la dependencia fsica no era una condicin
necesaria para crear o mantener hbitos de autoadministracin de estimulantes u opiceos. Pickens y Harris(10)
compararon el comportamiento de los animales que se afanaban por la anfetamina intravenosa, con los animales que
se esforzaban por la estimulacin elctrica lateral del hipotlamo. Este descubrimiento favoreci la teora, considerablemente sostenida por la escasez de seales de
16
abandono despus de una anfetamina crnica, de que las
drogas estimulantes, como la estimulacin cerebral del
hipotlamo, eran refuerzos positivos.
Al igual que el criterio de que las drogas adictivas
servan de refuerzo positivo iba acaparando la atencin,
los testimonios en contra de la teora de la dependencia
iban en aumento. La bsqueda de un modelo de alcoholismo animal condujo a la inesperada conclusin de que el
simple hecho de crear una dependencia alcohlica no era
suficiente para crear una autoadministracin voluntaria en
los roedores. Adems, a los alcohlicos humanos se les
enseaba a abstenerse de alcohol voluntariamente, durante periodos de angustia grave por abandono (para volver a
beber nicamente cuando tal angustia era ya mnima). Es
ms, aunque las inyecciones directas de morfina en ciertas
regiones cerebrales bastaban para crear los clsicos signos
de dependencia fsica, las ratas no aprendan a autoadministrarse tales inyecciones; y por otra parte, las ratas
aprendieron a autoadministrarse las inyecciones de morfina en otra regin del cerebro, regin sta en la que las
inyecciones no causaban signos de dependencia fsica(11).
Tales descubrimientos favorecen la teora de que la razn
principal por la que los adictos buscan la droga es el
refuerzo positivo habitualmente asociado con el placer o la
euforia, y los mismos descubrimientos contribuyeron a la
disminucin temporal del inters por los fenmenos de
drogodependencia y de la angustia por la abstinencia(2).
Los estudios ms recientes en la neurobiologa de la
adiccin surgen de los esfuerzos para comprender la organizacin anatmica de los sistemas de recompensa por
droga en el cerebro. El sistema de dopamina mesolmpico
est fuertemente conectado con las propiedades de formacin de hbitos de distintos tipos de drogas de abuso(1), que
sugieren un comn denominador en adicciones que, hace
un par de dcadas, pareca que no tenan nada que ver unas
con otras(2-4). Actualmente, se estn consiguiendo una gran
cantidad de progresos para identificar los aferentes y los
eferentes del sistema de dopamina mesolmpico, y para
localizar las zonas de desencadenamiento de recompensa de
diferentes drogas asociadas a estos aferentes y eferentes.
Las investigaciones ms recientes en la teora de la adiccin
sugieren que una adaptacin desapercibida anteriormente
RET, Revista de Toxicomanas. N. 18 1999
MAQUETA RET 18 21/12/1999 17:16 Pgina 17
del sistema nervioso, una insensibilizacin drogo-inducida
del mecanismo de refuerzo positivo, ofrece una posible
explicacin del componente ms potente del ansia de droga
continuo y creciente del comportamiento de los adictos(12,13).
CIRCUITOS NEURONALES DE RECOMPENSA
POR DROGA
Las drogas de abuso copian o potencian el funcionamiento de los mensajeros qumicos endgenos
en el cerebro.
Las drogas de abuso afectan, en su mayor parte, a los
receptores de los mensajeros qumicos endgenos del sistema nervioso. Por ejemplo, se cree que los opiceos crean
hbito por causa de sus intervenciones en los receptores
opiceos, y se cree que la nicotina crea hbito por su intervencin en los receptores acerilclnicos de nicotina. Otra
substancia adictiva, la fenciclidina, interviene en el
NMDA y en los receptores sigma, y bloquea tambin la
readmisin de dopamina; la droga demuestra ser creadora
de hbito principalmente por su actuacin en los receptores del NMDA(14). Un emocionante descubrimiento reciente ha sido el encontrar un nexo endgeno del receptor de
canabinoides(15*, 16-18). Aunque la anfetamina y la cocana no
afectan directamente a los receptores de dopamina, crean
hbito porque incrementan la concentracin de dopamina
en los receptores de dopamina situados en el ncleo acumen y en el crtex frontal(1).
Proceso de creacin de hbito de la droga localizada en el rea ventral tegmentada
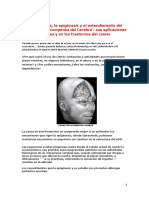
La morfina tiene su funcionamiento de recompensa
ms estudiado en el rea ventral tegmentada(19, 20) (figura 1).
Los dos agonistas opiceos mu y delta recompensan en
esta regin(21*,22). Los opiceos mu son conocidos por
desinhibir el encendido de las neuronas dopaminrgicas
en esta regin, mediante la inhibicin de las neuronas
GABArgicas que normalmente suprimen a sus vecinas
dopaminrgicas(23); el resultado de esta desinhibicin es el
aumento de emisin de dopamina en el ncleo acumen(24,25). Aunque todava no se conoce el fundamento
celular de la intervencin de los agonistas delta en esta
regin(26), la eficacia relativa del agonista mu DAMGO y la
RET, Revista de Toxicomanas. N. 18 1999
del agonista delta DPDPE, actuando como recompensas(21*), se pronostica por su eficacia relativa en aumentar
los niveles de dopamina del ncleo acumen(25): el agonista
mu es aproximadamente 100 veces ms efectivo en los
dos casos. Los opiceos Kappa no presentan recompensa
cuando se inyectan en esta regin(22), y estas inyecciones
no modulan los niveles de dopamina en el ncleo acumen(25); las inyecciones sistmicas de opiceos Kappa son
aversivas(27) e inhiben la emisin de dopamina del ncleo
acumen(25).
Est claro que el circuito ventral tegmentado activado por la recompensa intracraneal de morfina se activa
tambin por la recompensa intravenosa de herona; las
dosis autoadministradas de herona intravenosa causan
una emisin de dopamina desde la proyeccin mesolmbica hasta el ncleo acumen, como puede comprobarse con
las muestras de microdilisis, o por los registros de voltaje de los comportamientos de los animales(28,29,30*). Los
niveles de dopamina fluctan por encima de una lnea de
base elevada durante las sesiones de autoadministracin
de herona, sin embargo, no se llega a un acuerdo entre la
evidencia voltamtrica y de microdilisis en cuanto a si
los niveles de dopamina aumentan como anticipacin, o
como respuesta a cada inyeccin de herona conseguida.
Estos descubrimientos implican tanto a las clulas dopaminrgicas ventrales tegmentadas como a sus aferentes
GABArgicos en la recompensa de los opiceos.
Tambin se observa que la creacin de adiccin de la
nicotina se desencadena en los receptores del rea ventral
tegmentada (figura 1). En este caso, los receptores de
nicotina de una importancia hipottica se localizan en las
propias neuronas dopaminrgicas(31): la nicotina sistmica
eleva los niveles de dopamina del ncleo acumen(32), por
estimulacin directa de la clula de encendido dopaminrgico(33). Adems, tambin las inyecciones ventral tegmentadas del agonista de la nicotina o cistina son
recompensantes(3), y las inyecciones ventral tegmentada
sistmicas de los antagonistas de la dopamina trastornan
la autoadministracin intravenosa de nicotina, como tambin lo hacen las lesiones del sistema mesolmbico de
dopamina(35-37). Aunque las infusiones de nicotina en el
ncleo acumen pueden causar una emisin de dopamina,
17
MAQUETA RET 18 21/12/1999 17:16 Pgina 18
las inyecciones de los antagonistas de la dopamina en el
ncleo acumen no trastornan la autoadministracin intravenosa de nicotina(37); as pues, se cree que el rea ventral
tegmentada, y no el ncleo acumen, es la zona de encendido habitual de los hbitos de autoadministracin de
nicotina. Adems, se piensa que las clulas colinrgicas
del ncleo tegmentado laterodorsal o del ncleo pednculopontino proporcionan la innervacin colinrgica normal
de las neuronas de dopamina ventral tegmentada, que
expresan los receptores de nicotina.
Proceso de creacin de hbito de la droga localizada en el ncleo acumen
Las neuronas de dopamina ventral tegmentadas se
proyectan con mayor fuerza hacia el ncleo acumen (figura 1); las proyecciones se dirigen tambin hacia el crtex
frontal y hacia una serie de objetivos lmbicos distintos.
Bastantes de las drogas de abuso tienen unas funciones de
creacin de hbito en el ncleo acumen, y constituyen
(respectivamente) una o dos sinapsis eferentes para las ya
mencionadas funciones de la nicotina y la morfina. La ms
conocida de estas funciones de los ncleos acumens incluye a los estimulantes psicomotores anfetamina y cocana.
Cada una eleva las concentraciones extracelulares de
dopamina en el ncleo acumen(5), y los efectos de creacin
de hbito de ambas se atenan con los antagonistas de
dopamina o las reducciones de dopamina en el ncleo acumen(1).Los niveles extracelulares de dopamina aumentan
con la autoadministracin de dosis de cocana(38,39) y de
anfetamina (K.Leeb, RA Wise, Soc Neurosci Abstr 1994,
20:1622); en cada caso, los niveles de dopamina fluctan
por encima de un nivel de meseta elevada, que a lo largo
de la sesin de auto-adminstracin se mantiene en fase con
el ciclo de autoadministracin(40*,41,42,43*). De nuevo, los
datos de los estudios recientes de microdilisis y voltamtricos no coinciden en cuanto a si, una vez el nivel tnico
de dopamina se eleva con las primeras inyecciones, la fase
subsiguiente de aumento ocurre como respuesta a(43*), o
como anticipacin de(40*,41,42) cada una de las inyecciones
estimulantes. Algunas estructuras de encendido de las neuronas ventral tegmentadas y del ncleo acumen sugieren
que algunos elementos de este sistema participan en la
18
deteccin, mientras que otros participan en la anticipacin
de la recompensa de cocana, y de herona, y la de comida
y agua(44*,45-57). La anfetamina y la nomifensina(50*) (que
comparten la capacidad de la cocana para bloquear la
recepcin de dopamina, pero que no comparten la accin
anestsica local de la cocana) se autoadministran ambas
en el ncleo acumen. El sistema de circuitos abarca las
sinapsis dopaminrgicas en las neuronas medio espinales
GABArgicas(51).
Mientras que se considera que la cocana tiene su
accin de refuerzo ms importante en el ncleo acumen
(las administraciones del ncleo acumen de neurotoxinas
selectivas de dopamina o de antagonistas bloquean o reducen agudamente los efectos de recompensa de las dosis de
cocana autoadministradas), la cocana no se puede administrar fcilmente de forma directa en el ncleo acumen(50*,52). Esto parece una paradoja, por cuanto que las
infusiones de cocana en el ncleo acumen elevan los niveles de dopamina locales extracelulares(53), y las inyecciones
en el ncleo acumen de dopamina exgena(54) o de anfetamina (que aumenta la emisin local de dopamina)(48,49*) son
recompensantes por derecho propio. Adems, el inhibidor
de recepcin de dopamina nomifensino se autoadministra
en el ncleo acumen, como pueden hacerlo unas dosis
altas de cocana despus de pruebas prolongadas(50*). El
hecho de que la cocana ya no sea fcilmente autoadministrada en el ncleo acumen es de lo ms sorprendente,
porque la cocana (aunque no la nomifensina) se autoadministra fcilmente en el crtex frontal (ver a continuacin).
La morfina(55) y la metionina enceflica(56) tambin se
autoadministran en el ncleo acumen. Se cree que sus funciones de creacin de hbito en esa zona son muy independientes del sistema mesolmpico de dopamina; en su
lugar, sus funciones abarcan las neuronas medio espinales
GABArgicas, que tienden a proyectarse hacia atrs,
directa o trans-sinpticamente, hacia la substancia nigra y
el rea ventral tegmentada. Aunque no se sabe qu subpoblacin de neuronas ncleo acumens est implicada, hay
unas neuronas mensajeras intracelulares de ncleo acumen que s que intervienen en los efectos recompensantes
tanto de la cocana como de la herona. Los efectos recomRET, Revista de Toxicomanas. N. 18 1999
MAQUETA RET 18 21/12/1999 17:16 Pgina 19
pensantes de las inyecciones de cocana y de herona intravenosas se reducen en ambos casos mediante infusiones
intra-acumen de toxina pertussis, que desactiva las protenas G1 y G0 que intervienen en la conduccin de seales en
los receptores de dopamina tipo D2 y en los receptores
opiceos delta y mu(57). Es posible que distintas subpoblaciones de neuronas ncleo acumens medien los efectos de
la toxina pertussi en la autoadministracin de opiceos y
estimulantes, pero existe una posibilidad an mayor de
que estos comportamientos de las toxinas marquen una va
comn definitiva para los efectos de creacin de hbito de
estas dos clases de drogas adictivas(58).
La fenciclidina y otros antagonistas de NMDA presentan tambin mecanismos de recompensa en el ncleo
acumen(14). Igual que en el caso de las fibras dopaminrgicas del rea ventral tegmentada, las fibras glutamatrgicas
que van desde el crtex central al ncleo acumen terminan
principalmente en las neuronas GABArgicas medio espinales(59). Mientras que las fibras dopaminrgicas forman
contactos simtrico sinpticos (de tipo inhibidor) con las
neuronas medio espinales, las neuronas glutamatrgicas
forman sinapsis asimtricas (de tipo excitante) en tales
clulas(59). Por tanto, la produccin GABArgica del
ncleo acumen estara influenciada igualmente por las
inyecciones locales de antagonistas de NMDA, por las
inyecciones locales de agonistas indirectos de dopamina
(como la anfetamina y la cocana), y por las inyecciones
distales de substancias que activan la entrada dopaminrgica en el ncleo acumen (como la nicotina y la morfina);
en todos los casos las clulas de salida del ncleo acumen
aparecen inhibidas como consecuencia de la autoadministracin de droga(14).
Aunque la nicotina puede causar una emisin de
dopamina mediante una intervencin pre-sinptica en el
ncleo acumen, y tambin por intervenciones en el rea
ventral tegmentada, las comprobaciones ms recientes
sugieren que nicamente la intervencin en el rea ventral
tegmentada contribuye a la creacin de hbito de la nicotina en dosis autoadministradas(37).
En el caso de los antagonistas del NMDA fenciclidina, MK-801, y CPP(58), as como en el caso del inhibidor de
recepcin de dopamina la nomifensina(50*), los puntos de
RET, Revista de Toxicomanas. N. 18 1999
recompensa efectiva se encuentran en la regin ventromedial del ncleo acumen, llamada regin "perifrica", y no
en la regin ms dorsal y lateral, llamada regin "nuclear".
Tal descubrimiento puede resultar importante, ya que las
regiones nuclear y perifrica del ncleo acumen tienen
distintas proyecciones eferentes y subtipos de receptores
de dopamina D2 y D3 que se expresan diferencialmente.
Las clulas de la periferia del ncleo acumen se proyectan
con ms fuerza hacia el rea ventral tegmentada, mientras
que las clulas del ncleo se proyectan con ms fuerza
hacia la zona compacta de la substancia nigra(60). Los
receptores D2 aparecen en la periferia(61) y juegan un papel
en la estimulacin del comportamiento(62), mientras que los
receptores D3 aparecen patentes en el ncleo(61) y juegan un
papel de inhibicin del comportamiento.
Proceso de creacin de hbito de las drogas en
el crtex medio frontal
Aunque las ratas no se autoadministran fcilmente la
cocana en el ncleo acumen, s que se autoadministran con
mucha ms facilidad esta droga directamente en el crtex
medio frontal(63,64). El crtex medio frontal recibe los aferentes dopaminrgicos del rea ventral tegmentada (figura
1), y las inyecciones locales de los antagonistas de dopamina(64) o las neurotoxinas de dopamina(63) bloquean los
efectos de recompensa de la cocana del crtex frontal; por
tanto la cocana tiene la capacidad de elevar los niveles de
dopamina extracelulares mediante el bloqueo de la recepcin de dopamina, que se supone que responde a su funcin
de recompensa aqu, igual que en el ncleo acumen.
Lo que no est claro es la intervencin del crtex frontal en el refuerzo intravenoso de la cocana. Las lesiones en
el crtex no trastornan la autoadministracin intravenosa de
cocana(65,66); por el contrario se ha comprobado que causan
una supersensibilidad en los efectos recompensantes de la
cocana intravenosa(66). La interpretacin de esta supersensibilidad es problemtica, porque la supersensibilidad de la
dopamina local debera de ser recompensada por la prdida
de las terminales de dopamina lesionadas, que proporcionan
el sustrato para la accin inmediata de la cocana en el crtex central. Una posibilidad es que las inyecciones de cocana en el crtex frontal sean recompensantes porque eleven
19
MAQUETA RET 18 21/12/1999 17:16 Pgina 20
indirectamente los niveles de dopamina en el ncleo acumen(67); los efectos indirectos de las lesiones del crtex frontal en los niveles de dopamina del ncleo acumen podran
tambin responder a los efectos paradjicos de las lesiones.
Sin embargo, otro problema de esta hiptesis es el descubrimiento de que las inyecciones en el crtex frontal de la
anfetamina emisora de dopamina no son recompensantes
por s mismas(64).
Sea cual sea la explicacin definitiva de los efectos
recompensantes de la cocana en el crtex frontal, esta
estructura desempea algn papel en el sistema de circuitos
de recompensa del cerebro. La fenciclidina, el MK-801, y el
CPP no slo son recompensantes cuando se inyectan en el
ncleo acumen, tambin son recompensantes en las dosis
del mismo nivel cuando se inyectan en el crtex medio frontal(14). Al igual que el MK-801 y el CPP comparten ambos la
capacidad de la fenciclidina para bloquear los receptores de
NMDA, y no comparten la capacidad de la fenciclidina o de
la cocana para bloquear la readmisin de dopamina, el aminocido de excitacin as como los circuitos de dopamina en
el crtex frontal muestran su capacidad para desempear un
papel en la funcin de recompensa de la droga.
Proceso de creacin de hbito de la droga en el
hipocampo
Tambin se les ense a las ratas a presionar una
palanca para las inyecciones de morfina(68) o para el opiceo endgeno dinorfina A(69), en la regin CA3 del hipocampo. El efecto queda bloqueado por un antagonista
opiceo mu(69), y por la toxina pertussis desactivadora de la
protena G(68). El hipocampo enva una proyeccin de glutamato al ncleo acumen, y una proyeccin del hipocampo a las sinapsis del ncleo acumen en las neuronas
acumenes que reciben tambin entradas de catecolamina
desde el rea ventral tegmentada(70). La estimulacin elctrica de la proyeccin que contiene dinorfina, desde los
giros dentados hasta el CA3 es recompensante; sus efectos
se bloquean con naloxona(71).
Papel del ncleo tegmentado pedunculopontino
Un enlace ms aferente en el sistema de circuitos de
recompensa del cerebro puede producirse en el dorsal.
20
Yeomans y sus colegas(72) sostuvieron que al recompensar
el haz del cerebro anterior medial, la estimulacin elctrica activa el sistema de dopamina mesolmbico de modo
transinptico, mediante una proyeccin colinrgica del
ncleo pednculopontino (figura 1). El ncleo pednculopontino est tambien implicado en la recompensa de la
droga; las lesiones de este ncleo atenan las preferencias
de lugar acondicionado de morfina -y de anfetamina-(73).
Son estas clulas y las clulas del ncleo adyacente laterodorsal tegmentado las que emiten acetilclolina en los
receptores de nicotina en las neuronas que contienen
dopamina del tegumento ventral.
NEUROBIOLOGA DE LA DROGODEPENDENCIA
La teora clsica de la dependencia se ha concentrado
en una serie de sndromes de abstinencia que son el resultado de la accin de las drogas en distintos puntos que van
desde los intestinos y el sistema nervioso autnomo, hasta
los mecanismos centrales de las convulsiones. Las diferentes drogas pueden tener efectos contrapuestos en varios
de estos mecanismos. Sin depender de estas seales de
dependencia, esta abstinencia de las distintas drogas, que
activan el sistema de dopamina mesolmbico(5) y potencian
los efectos de recompensa de la estimulacin elctrica del
hipotlamo lateral(74*), causa una depresin de rechazo del
mecanismo de refuerzo positivo. Este sndrome de abstinencia es un denominador comn de distintos tipos de drogas adictivas, y algunos consideran que es el origen o el
que modula la motivacin del comportamiento de bsqueda de droga.
El comprender que la depresin del propio sistema de
recompensa poda ser una consecuencia del abandono de
la droga comenz con la observacin de Leith y Barret(75)
de que la recompensa de la estimulacin cerebral se vuelve menos efectiva durante el abandono desde un tratamiento crnico con anfetamina(75,76). Desde entonces, se
han ido encontrando depresiones similares del mecanismo
de recompensa, asociados al abandono de cocana(13,77,78), y
de etanol(79). Que la reduccin drogo-inducida de dopamina poda ser la razn de tales efectos lo sugirieron en primer lugar Dackis y Gold(12), que sostenan que la
intoxicacin crnica de cocana reduca la dopamina del
RET, Revista de Toxicomanas. N. 18 1999
MAQUETA RET 18 21/12/1999 17:16 Pgina 21
cerebro, causaba sentimientos de depresin, e impulsaba a
la bsqueda y a la autoadministracin de cocana. Aunque
Dackis y Gold no podan disponer de comprobaciones
directas, y aunque la hiptesis que presentaban se aplicaba nicamente a la cocana, los estudios de microdilisis
han confirmado que la reduccin de dopamina puede
acompaar al abandono de una intoxicacin crnica de
cocana(80-83), de anfetamina(82,84), de opiceos(82,85), y de etanol(82). En relacin a los efectos opuestos de la intoxicacin
por droga y del abandono de la droga en niveles de dopamina extracelulares, existen los efectos contrarios de
drogo-intoxicacin y abandono en los segundos mensajeros del sistema de recompensa; de nuevo, los opiceos
tienen unos efectos similares a los estimulantes psicomotores, dentro de las clulas del sistema de recompensa(86**).
El significado de estas variantes nuevas de la teora de
la dependencia es que, a diferencia de la teora clsica de
la adiccin, identifican como consecuencia fundamental
del hbito de drogas un nico efecto de abandono, en lugar
de todo un caudal de incidentes aparentemente aversivos.
El sndrome de abstinencia significativo se da como hecho
comn en una amplia gama de tipos de drogas, que comprende los estimulantes psicomotores, los opiceos narctico/analgsicos, el etanol sedativo hipntico, y la difcil
de clasificar (por sus funciones autonmico bifsicas y
centrales) nicotina. Por tanto, la variante nueva de la teora de la dependencia, al igual que la teora anterior del
estimulante psicomotor, sugiere una base comn para el
abuso de los estimulantes y los opiceos, y posiblemente
para otros casos distintos de adiccin. No obstante, est
an por ver si este sndrome de abstinencia nuevo es una
causa necesaria o suficiente para la conducta de bsqueda
de droga(87,88*).
CUESTIONES DESTACADAS
Existen varias cuestiones crticas que son actualmente objeto de intensa investigacin. Uno de los principales
interrogantes sobre la adiccin, que ha sido largamente
cuestionado, y que contina sindolo, es si los estados
similares a la droga o en contra de la droga son la fuente
de motivacin principal del comportamiento compulsivo
de bsqueda de drogas. Parece que est claro que las adapRET, Revista de Toxicomanas. N. 18 1999
taciones contrarias a la droga desarrollan un sistema de
circuitos durante la intoxicacin crnica por drogas adictivas. Tambin queda manifiesto que las primeras inyecciones de la propia droga estimulan el comportamiento de
bsqueda de drogas(89); todava no se ha determinado si los
estados cerebrales contrarios a la droga junto a la abstencin de droga son fuente de ansiedad y de bsqueda de
droga, o son ms bien fuente de depresin y de apata que
se asocian a la disminucin de probabilidades de realizar
esfuerzos (ver los ej. 87).
Un segundo tema de gran inters es la existencia de
diferencias individuales significativas en cuanto a la susceptibilidad ante la adiccin. Unas diferencias tensas en el
consentimiento para beber soluciones alcohlicas, opiceos,
o estimulantes psicomotores sugieren esa posibilidad, y
tales diferencias, que podran explicar las diferencias en
las tomas, resultan evidentes en las caractersticas intracelulares del circuito de recompensa (ver ej. 86). An as, las
diferencias en el consentimiento para probar las disoluciones de droga oral no son necesariamente el reflejo de las
diferencias de vulnerabilidad ante la adiccin. Muy raramente, si es que ocurre, los animales de laboratorio desarrollan unos hbitos de autoadministracin oral de droga,
lo suficientemente fuertes para poderlos considerar como
verdadera adiccin. Los intentos de demostrar unas diferencias marcadas en la autoadministracin intravenosa de
drogas no han obtenido todava resultados positivos.
Tambin con relacin a un asunto de inters actual
es la posibilidad de que puedan establecerse las diferencias individuales formales en la susceptibilidad ante la
adiccin segn ciertas clases de historiales de drogas o
de estrs. De hecho, los animales que tienen un historial
de experiencia con drogas alcanzan la autoadministracin de drogas ms rpidamente que los animales que
experimentan la droga por primera vez (90,91). No obstante,
todava no est claro que esos animales presenten realmente una mayor respuesta al impacto de recompensa de
la droga; pueden tener un riesgo ms acusado de caer en
la adiccin simplemente porque estn ms inclinados a
explorar y manipular lo que les rodea, hasta el punto de
que aprendan que existe a su disposicin una recompensa por droga. Por otra parte, es posible que esos animales
21
MAQUETA RET 18 21/12/1999 17:16 Pgina 22
Figura 1
mFCx
SC
mThal
NAcc(shell)
SNC/VTA
PPTg
LDTg
SNr/VTA
Dopamina
Glutamate
Acetylcholine
sean ms susceptibles habitualmente a cualquier tipo de
aprendizaje(92*). Adems, las diferencias en la adquisicin
de hbitos de autoadministracin de drogas, as como las
demostraciones de la capacidad de los refuerzos alternativos de reducir la autoadministracin de drogas, se
observan slo cuando se experimenta con animales con
dosis de drogas reducidas. Por definicin, la variabilidad
en la respuesta a un ED50 (la dosis justa adecuada para
producir un efecto dado en el 50% de los animales seleccionados) es mayor que la variabilidad de respuesta a un
ED85. Por lo general, las diferencias predecibles en la
autoadministracin de droga se han demostrado con
dosis marginales de refuerzo (ED50) de la droga(90,91). En
nuestro caso, aproximadamente el 85% de nuestras ratas
Long-Evans y Sprague-Dawley (unas 200 de cada lado)
aprenden a auto-administrarse cocana o herona intravenosas, sin ningn tipo de respuesta especial, durante
cinco das con droga a su disposicin. As pues, queda
an por establecer que cualquier mamfero est realmente a salvo de la adiccin a dosis fuertes de herona o
cocana intravenosas.
22
GABA
El tema de la relevancia del estrs en acelerar el consumo de droga, o en contribuir a la susceptibilidad ante la
droga est siendo progresivamente sometido a un mayor
examen(ver ej. 88**,93**). Parece evidente que el estrs puede
desempear un papel primordial y complejo en la autoadministracin de droga, en la reincidencia en la autoadministracin de droga, y que se espera una labor de
interaccin entre el estrs y el consumo de droga mucho
ms acusada durante los prximos aos.
La utilizacin de tcnicas de biologa celular en el
estudio de la funcin recompensante de la droga y en la
adiccin est despertando un inters creciente(86**,94). Cada
vez con ms frecuencia, estn apareciendo estudios sobre
las respuestas de los segundos mensajeros dentro de las
neuronas relacionadas con la recompensa(86**), as como
estudios sobre los efectos del consumo de drogas en la
fisonoma de los genes neurotransmisores inmediatos(95), y
tambin comienzan a mostrarse estudios de los efectos de
los oligonucletoides antisensoriales en el consumo de
droga. Por tanto, se puede esperar un desarrollo rpido en
la neurobiologa celular de la adiccin(86**,94).
RET, Revista de Toxicomanas. N. 18 1999
MAQUETA RET 18 21/12/1999 17:16 Pgina 23
CONCLUSIONES
BIBLIOGRAFIA Y RECOMENDACIONES PARA SU LECTURA
Las investigaciones en la neurobiologa de la adiccin
nos recuerdan que los mecanismos cerebrales por los que
las drogas pueden llegar a controlar el comportamiento ya
estaban establecidos mucho antes del primer atisbo de
adiccin en nuestro historial evolutivo. La funcin de
recompensa de la droga controla la conducta mediante
intervenciones en los mismos mecanismos biolgicos que
se supone que explican el control de las conductas en el
caso de la recompensa alimentaria o de la satisfaccin
sexual, cuya funcin se centra en los circuitos de recompensa, que se activan mediante los sentidos en el caso de
la comida y del sexo. Aunque se haya caracterizado slo
una fraccin del sistema de circuitos principal del cerebro
(figura 1), el sistema de dopamina mesocorticolmbico y
algunos de sus aferentes y eferentes aparecen implicados
en los efectos recompensantes de los opiceos, la nicotina,
la anfetamina, la cocana, y la fenciclidina. Exactamente
igual que los opiceos delta y mu, la anfetamina, la cocana, la nicotina, el alcohol, el canabis y la fenciclidina activan un mecanismo de recompensa comn, as tambin, el
abandono de un tratamiento crnico con opiceos, anfetamina, cocana y etanol causa un efecto rebote de depresin
en ese sistema. De este modo, el estudio de los mecanismos de recompensa del cerebro sugieren un denominador
comn para la capacidad de abuso de distintas substancias
adictivas.
Los artculos de especial inters, publicados sin la revisin anual, estn
resaltados como sigue: ** de especial inters
RECONOCIMIENTOS
17- Evans DM, Lake JT, Johnson MR, Howlett AC: Endogenous cannabinoid receptor binding activity released from rat brain silices by depolarization, J Pharmacol Exp Ther 1994, 268:1271-1277
Esta revisin se ha realizado con el apoyo de la infraestructura de Fonds pour la formation de Chercheurs et
lAide la Recherche (Qubec).
Este artculo se ha publicado en la revista Current Opinion in Neurobiology en 1996.
1- Wise RA, Rompr P-P: Brain dopamine and reward, Annu Rev Psychol
1989,40:191-225
2- Wise RA: The role of reward pathways in the development of drug dependence, Pharmacol Ther 1987,35:227-263
3- Wise RA, Bozarth MA: A psychomotor stimulant theory of addiction,
Psychol Rev 1987,94:469-492
4- Wise RA: The neuorobiology of craving: Implications for understanding
and treatment of addiction, J Abnorm Psychol 1988,97:118-132
5- Di Chiara G, Imperato A: Drugs of abuse preferentially stimulate dopamine release in the mesolimbic system of freely moving rats, Proc Natl Acad
Sci USA 1988:5274-5278
6- Koob GF, Bloom FE: Cellular and molecular mechanism of drug dependence, Science 1988,242:715-723
7- Robinson TE, Berridge KC: The neural basis of drug craving: an incentive-sensitization theory of addiction, Brain Res Rev 1993,18:247-292
8- Olds J, Milner PM: Positive reinforcement produced by electrical stimulation of septal area and other regions of rat brain, J Comp Physiol Psychol
1954,47:419-427
9- Olds J: Pleasure centers in the brain, Sci Am 1956,195:105-116
10- Pickens R, Harris WC, Self-administration of D-amphetamine by rats,
Psychopharmacologia 1968,12:158-163
11- Bozarth MA, Wise RA: Anatomically distinct opiate receptor fields
mediate reward and physical dependence, Science 1984,224:516-518
12-Dackis CA, Gold MS: New concepts in cocaine addiction: the dopamine
depletion hypothesis, Neurosci Biobehav Rev 1985,9:469-477
13- Markou A, Koob GF, Postcocaine anhedonia: an animal model of cocaine withdrawal, Neuropsychopharmacology 1991,4:17-26
14- Carlezon WA Jr, Wise RA: Rewarding actions of phencyclidine and related drugs in nucleus accumbens shell and frontal cortex, J Neurosci 1996, in
press
15- * Devane WA, Axeirod J: Enzymatic synthesis of anandamine, an endogenus ligand for the cannabinoid receptor, by brain membranes, Proc Natl
Acad Sci USA 1994,91:6698-6701
16- Di Marzo V, Fontana A, Cadas H, Schinell S, Cimino G, Schwartz JC,
Piomelli D: Formation and inactivation of endogenus cannabinoid anandamine in central neurons, Nature 1994,372:686-691
18 Vogel A, Barg J, Levy R, Saya D, Heldman E, Mechoulan R:
Anandamine, a brain endogenous compound, interacts specifically with cannabinoid receptors and inhibits adenylate cyclase, J Neurochem
1993,61:352-355
19 Bozarth MA, Wise RA: Intracranial self-administration of morphine into
the ventral area in rats, Life Sci 1981,28:551-555
20- Phillips AG, LePiane FG: Reinforcing effects of morphine microinjection into the ventral tegmental area, Pharmacol Biochem Behav
1980,12:965-968
21- * Devine DP, Wise RA: Self-administration of morphine, DAMGO, and
DPDPE into the ventral tegmental area of rats, J Neurosci 1994,14:19781984
22- Bals-Kubik R, Ableinter A, Hertz A, Shippenberg TS: Neuroanatomical
sites mediating the motivational effects of opioids as mapped by the condicioned place preference paradigm in rats, JPharmacol Exp Ther
1993,264:489-495
23- Johnson SW, North RA:Opioids excite dopamine nuerons by hyperpolarization of local interneurons, J Neurosci 1992,12:483-488
RET, Revista de Toxicomanas. N. 18 1999
23
MAQUETA RET 18 21/12/1999 17:16 Pgina 24
24- Leone P, Pocock D, Wise RA: Morphine-dopamine interaction: ventral
tegmental morphine increases nucleus accumbens dopamine release,
Pharmacol Biochem Behav 1991,39:469-472
45- Carelli RM, King VC, Hampson RE, Deadwyler SA: Firing patterns of
nucleus accumbens neurons during cacaine self-administration in rats, Brain
Res 1993,626:14-22
25- Devine DP, Leone P, Pocock D, Wise RA: Differential involvement of
ventral tegmental mu, delta, and kappa opioid receptors in modulation of
basal mesolimbic dopamine release: in vivo microdialysis studies, J
Pharmacol Exp Ther 1993,266:1236-1246
46- Chang JY, Sawyer SF, Lee RS, Woodward DJ: Electrophysiological and
pharmacological evidence for the role of the nucleus accumbens in cocaine
self-administration in freely moving rats, J Neurosci 1994,14:1224-1244
26- Devine DP, Leone P, Carlezon WA Jr, Wise RA: Ventral mesencephalic
& opioid receptors are involved in modulation of basal mesolimbic dopamine neurotransmission, Brain Res 1993,622:348-352
27- Mucha RF, Hertz A: Motivational properties of k and m opioid receptor
agonists studied with place and taste preference conditioning,
Psychopharmacology 1985,86:274-280
28- Wise RA, Leone P, Rivest R, Leeb K: Elevations of nucleus accumbens
dopamine and DOPAC levels during intravenous heroin self-administration,
Synapse 1995, 21:140-148
29- Kiyatkin EA, Wise RA, Gratton A: Drug - and behavior- associated
changes in dopamine-related electrochemical signals during intravenous
heroin self-administration in rats, Synapse 1993,14:60-72
30- * Hemby SE, Martin TJ, Co C, Dworkin SI, Smith JE: The effects of
intravenous heroin administration on extracellular nucleus accumbens dopamine concentrations as determined by in vivo microdialysis, J Pharmacol
Exper Ther 1995,273:591-598
47- Schults W, Apicella P, Ljungberg T: Responses of monkey dopamine
neurons to reward and conditioned stimull during successive steps of learning a delayed response task, J Neurosci 1993,13:900-913
48- Hoebel BG, Monaco AP, Hernandez L, Aulisi EF, Stanley BG, Lenard
L:Self- injection of amphetamine directly into the brain,
Psychopharmacology 1983,81:158-163
49- * Philips GD, Robbins TW, Everitt BJ: Bilateral intra-accumbens selfadministration of D-amphetamine: antagonism with intraaccumbens SCH23390 and sulpride, Psychopharmacology 1994,114:477-485
50- * Carlezon WA Jr, Devine DP, Wise RA: Habit-forming actions of nomifesine in nucleus accumbens, Psychopharmacology 1995,122:194-197
51- Pickel VM, Chan J: Spiny neurons lacking choline acetylcholine transferase inmunoreactivity are major targets of cholinergic and catecholaminergic terminals in rat striatum, J Neurosci Res 1990,25:263-280
52- Goeders NE, Smith JE: Cortical dopaminergic involvement in cocaine
reinforcement, Science 1983,221:773-775
31- Clarke PBS, Pert A: Autoradiographic evidence for nicotine receptors on
nigrostrial and mesolimbic dopaminergic neurons, Brain Res 1985,348:355358
53- Hurd YL, Ungerstedt U: Cocaine: an in vivo microdialysis evaluation of
its acute action dopamine transmission in rat striatum, Synapse 1989,3:4854
32- Imperato A, Mulas A, Di Chiara G: Nicotine preferentially stimulates
dopamine release in the limbic system of freely moving rats, Eur J
Pharmacol 1986,132:337-338
54- Deworkin SI, Goeders NE, Smith JE: The reinforcinig and rate effects
of intracranial dopamine administration, NIDA Res Monogr 1986,67:242248
33- Mereu G, Yoon K-WP, Boi V, Gessa GL, Naes L, Westfall TC:
Preferential stimulation of ventral tegmental area dopaminergic neurons by
nicotine, Eur J Pharmacol 1987,141:395-400
55- Olds ME: Reinforcing effects of morphine in the nucleus accumbens,
Brain Res 1982,237:429-440
34- Museo E, Wise RA: Place preference conditioning with ventral tegmental injections of cytisne, Life Sci 1994,55:1179-1186
35- Corrigall WA, Coen KM: Selective dopamine antagonists reduce nicotine self-administration, Psychopharmacology 1991,104:171-176
36- Corrigall WA, Franklin KBJ, Coen KM, Clarke P: The mesokimbic
dopaminergic system is implicated in the reinforcing effects of nicotine,
Psychopharmacology 1992,107:285-289
37- Corrigall WA, Coen KM, Adamson KL: Self-administered nicotine activates the mesolimbic dopamine system through the ventral tegmental area,
Brain Res 1994,653:278-284
38- Pettit HO, Justice JB: Dopamine in the nucleus accumbens during cocaine self-administration as studied by in vivo microdialysis, Pharmacol
Biochem Behav 1989,34:899-904
39- Hurd JL, Weiss F, J Koob GF, Anden N-E Ungerstedt U: Cocaine reinforcement and extracellular dopamine overflow in rat nucleus accumbens:
an in vivo microdialysis study, Brain Res 1989,498:199-203
40-* Kiyatkin EA, Stein EA: Fluctuations in nucleus accumbens dopamine
during cocaine self-administration behavior: an in vivo electrochemical
study, Neuroscience 1995,64:599-617
56- Goeders NE, Lane JD, Smith JE: Self-administration of methionine
enkephalin into the nucleus accumbens, Pharmacol Biochem Behav
1984,20:451-455
57- Self DW, Terwilliger RZ, Nestler EJ, Stein L: Inactivation of Gi and Go
proteins in nucleous accumbens reduces both cocaine and heroin reinforcement, J Neurosci 1994,14:6239-6247
58- Terwilliger RZ, Beitner-Johnson D, Sevarino KA, Crain SM, Nestler EJ:
A general role for adaptations in G-proteins and the cyclic AMP system in
mediating the chronic actions of morphine and cocaine on neuronal function, Brain Res 1991,548:100-110
59- Sesack SR, Pickel VM: Prefrontal cortical efferents in the rat synapse on
unlabeles neuronal targets of catecholamine terminals in the nucleus accumbens septi and on dopamine neurons in the ventral tegmental area, J Comp
Neurol 1992,320:145-160
60 Zahm DS, Brog JS: On the significance of subterritories in the `accumbenspart of the rat ventral striatum, Neuroscience 1992,50:751-767
61- Larson ER, Ariano MA: D3 and D4 dopamine receptors: visualization
of cellular expression patterns in motor and limbic structures, Synapse
1995,20:325-337
41- Kiyatkin EA, Stein EA: Biophasic changes in mesolimbic dopamine signal during caocaine self-administration 1994,5:1005-1008
62- Waters N, Svensson K, Haadsma-Svensson SR, Smith MW, Carisson A:
The dopamine D3-receptor: a postsynaptic receptor inhibitory on rat locomotor activity, J Neural Transm 1993,94:11-19
42- Gratton A, Wise RA: Drug-and behavior- associated changes in dopamine -related electrochemical signals during intravenous caocaine selfadministration in rats, J Neurosci 1994
63- Goeders NE, Smith JE: Reinforcining properties of cocaine in the
medial prefrontal cortex: primary action on presynaptic dopaminergic terminals, Pharmacol Biochem Behav 1986,25:191-199
43- * Wise RA, Newton P, Leeb K, Burnette B, Pocock D, Justice JB Jr:
Fluctuations in nucleus accumbens dopamine concentration during intravenous
cocaine self-administration in rats, Psychopharmacology 1995,120:10-20
64- Goeders NE, Dworkin SI, Smith JE: Neuropharmacological assessment
of cocaine self-adminitration into the medial prefrontal cortex, Pharmacol
Biochem Behav 1986,24:1429-1440
44- Carelli RM, Deadwyler SA: A comparison of nucleus accumbens neuronal firing patterns during cocaine self-administration and water reinforcement in rats, J Neurosci 1994, 14:7735-7746
65- Martin-Iverson MT, Szostak C, Fibiger HC: 6-Hydroxdopamine lesions
of the medial prefrontal cortex fail to influence intravenous self-administration of cocaine, Psicopharmacology 1986,88:310-314
24
RET, Revista de Toxicomanas. N. 18 1999
MAQUETA RET 18 21/12/1999 17:16 Pgina 25
66- Schenk S, Horger BA, Peltier R, Shelton K: Supersensitiivity to the reinforcing effects of cocaine following 6-hydroxdopamine lesions to the medical prefrontal cortex in rats, Brain Res 1991,543:227-235
88- ** Shaham Y, Stewart J: Stress reinstates heroin-seeking in drug-free
animals: an effect mimicking heroin, not withdrawal, Psychopharamcology
1995, 119:334-341
67- Goeders NE, Smith JE: Intracranial cocaine self-administration into the
medial prefrontal cortex increases dopamine turnover in the nucleus accumbens, J Pharmacol Exp Ther 1993,265:592-600
89- Stewart J, De Wit H, Eikelboom R: Role of unconditioned and conditioned drug effects in the self-administration of opiates and stimulates, Psychol
Rev 1984,91:251-268
68- Self DW, Stein L: Pertussis toxin attenuates intracranial morphine selfadministration Pharmacol Biochem Behav 1993,46:689-695
90- Piazza PV, Deminiere JM, Le Moal M, Simon H: Factors that predict
individual vulnerability to amphetamine self-administration, Science
1989,245:1511-1513
69- Stevens KE, Shiotsu G, Stein L: Hippocampal u-receptors mediate
opioid reinforcement in the CA3 region, Brain Res 1991,545:8-16
70- Sesack SR, Pickel VM: In the rat medial nucleus accumbens hippoampal and catecholaminergic terminals converge on spiny neurons and are in
opposition to each other, Brain Res 1990, 527:266-279
71- Collier TJ, Routtenberg A: Electrical self-stimulation of dentate gyrus
granule cells, Behav Neural Biol 1984,42:85-90
91- Horger BA, Shelton K, Schenk S: Preexposure sensitizes rats to the
rewarding effects of cocaine, Pharmacol Biochem Behav 1990,37:707-711
92- * Jodogne C, Marinelli, Le Moal M, Piazza PV: Animals predisposed to
develop maphetamine self-administration show higher susceptibility to
develop contextual conditioning of both aphetamine-induced hyperlocomotion and sensitization, Brain Res 1994,657:236-224
72- Yeomans JS, Mathur A, Tampakeras M: Rewarding brain stimulation:
role of tegmental cholinergic neurons that activate dopamine neurons, Behav
Neurosci 1993,107:1077-1087
93- ** Piazza PV, Marinelli M, Jodogne C, Deroche V, Rouge-Pont F,
Maccari S, Le Moal M, Simon H: Inhibition of corticosterone synthesis by
Metrypone decreases cocaine-induced locomotion and relapse of cocaine
self-administration, Brain Res 1994,658:259-264
73- Bechara A, Van der Kooy D: The tegmental peducnculopontine nucleus:
a brain-stem output of the limbic system critical for the conditioned place
preferences produced by morphine and amphetamine, J Neurosci 1989,
9:3400-3409
94- Daunais JB, Roberts DCS, McGinty JF: Short-term cocaine self-administrtion alters strial gene expression, Brain Res Bull 1995,37:523-527
74- * Wise RA: Addictive drugs and brain stimulation reward, Annu Rev
Neurosci 1996,19:319-340
75-Leith NJ, Barret RJ: Amphetamine and the reward system: evidence for
tolerance and post-drug depression, Psychopharmacology 1976,46:19-25
95- Nestler EJ, Hope BT, Widnell KL: Drug addiction: a model for the molecular basis of neutral plasticity, Neuron 1993,11:995:1006
96- Van Bockstaele EJ, Pickel VM: GABA-containing neurons in the ventral
tegmental area project to the nucleus accumbens in rat brain, Brain Res
1995,682:215-221
76- Wise RA, Munn E: Withdrawal from chronic amphetamine elevates
baseline intracranial self-stimulation thresholds, Psychopharmacology 1994,
117:130-136
77- Frank RA, Martz S, Pommering T: The effect of chronic cocaine on selfstimulation train-duration thresholds, Pharmacol Biochem Behav
1988,29:755-758
78- Kokkinidis L, McCarter BD: Postcocaine depression and sensitization of
brain-stimulation reward: analysis of reinforcement and performance
effects, Physiol Behav 1990,36:463-471
79- Schulteis G, Markou A, Cole M, Koob GF:Decreased brain reward produced by ethanol withdrawal, Proc Natl Acad Sci USA 1995,92:5880-5884
80- Parsons LH, Smith AD, Justice JB: Basal extracellular dopamine is
decreased in the rat nucleus accumbens during abstinence from honic cocaine, Synapse 1991,9:60-65
81- Imperato A, Mele A, Scrocco MG, Puglisi-Allegra S: Chronic cocaine
alters limbic extracellular dopamine Neurochemical basis for addiction, Eur
J Pharmacol 1992,212:299-300
82- Rosetti ZL, Hmaidan Y, Gessa GL: Market inhibition of mesolimbic
dopamine release: a common feature of ethanol, morphine, cocaine, and
amphetamine abstinence in rats, Eur J Pharmacol 1992,221:227-234
83- Robertson MW, Leslie CA, Bennett JP: Apparent sunaptic dopamine
deficiency induced by withdrawal from chronic cacaine treatment, Brain Res
1991,538:337-339
84- Paulson PE, Camp DM, Rubinson TE: Time course of transient behavioral depression and persistent behaioral sensitization in relation to regional brain monoamine concentrations during aphetamine withdrawal in rats,
Psychopharamcology 1991,103:480-492
85- Pothos E, Rada P, Mark GP, Hoebel BG: Chronic morphine increases
synaptic dopamine in the nucleus accumbens and naloxone decreases it
inless withdrawal is blocked with clonidine, Brain Res 1991,566:348-350
86- ** Self DW, Nestler EJ: Molecular mechanisms of drug reinforcement
and addiction, Annu Rev Neurosci 1995,18:463-495
87- Stewart J, Wise RA: Reinstatement of heroin self-administration habits:
morphine prompts and naltrexone discourages renewed responding after
extinction, Psychopharamcology 1992,108:779-784
RET, Revista de Toxicomanas. N. 18 1999
25
Você também pode gostar
- Apuntes dietéticos y nutricionales durante la lactanciaNo EverandApuntes dietéticos y nutricionales durante la lactanciaAinda não há avaliações
- Tres Puntos de Vista Sobre La AdicciónDocumento12 páginasTres Puntos de Vista Sobre La AdicciónMaitte Carrión UribeAinda não há avaliações
- Factor THIQ PDFDocumento3 páginasFactor THIQ PDFRene LopezAinda não há avaliações
- Psicopatología-Clínica-Basada en DSM5-Margarita-Ortiz-TalloDocumento8 páginasPsicopatología-Clínica-Basada en DSM5-Margarita-Ortiz-TalloPamVarAinda não há avaliações
- Tres Puntos de Vista Sobre La AdicciónDocumento21 páginasTres Puntos de Vista Sobre La AdicciónGerson de la Fuente OlaveAinda não há avaliações
- Drogas FinishDocumento10 páginasDrogas FinishAlvaro Andres Sanchez HurtadoAinda não há avaliações
- Wolf, C.C. (2013) : Sistema de RecompensaDocumento6 páginasWolf, C.C. (2013) : Sistema de Recompensaakme73Ainda não há avaliações
- BasesneurobiologicasDocumento6 páginasBasesneurobiologicasErendira BarrientosAinda não há avaliações
- Articulo Adicciones y Psicoanalisis Revista CientificaDocumento21 páginasArticulo Adicciones y Psicoanalisis Revista Cientificaayaibex montasAinda não há avaliações
- Tema 4 - Teorías, Proceso Adictivo y VulnerabilidadDocumento8 páginasTema 4 - Teorías, Proceso Adictivo y VulnerabilidadAna Rodríguez MartínAinda não há avaliações
- 4ºmotivación y DrogasDocumento44 páginas4ºmotivación y DrogasmarcoAinda não há avaliações
- Presentación de Proyecto Bases LLDocumento15 páginasPresentación de Proyecto Bases LLYovana MezaAinda não há avaliações
- Mecanismos de Recompensa CerebralDocumento12 páginasMecanismos de Recompensa CerebralEunice PluaAinda não há avaliações
- Contreras (2008) Emocion AdiccionDocumento6 páginasContreras (2008) Emocion AdiccionDaniel GalindoAinda não há avaliações
- Neuro Adiccion Neurofisiologia CerebroDocumento15 páginasNeuro Adiccion Neurofisiologia CerebroBeba AragónAinda não há avaliações
- Manual-Adicciones Cap 2 Neurobiología de Las AdiccionesDocumento9 páginasManual-Adicciones Cap 2 Neurobiología de Las AdiccionesVianey Gómez GuzmánAinda não há avaliações
- Bases Biológicas de Las AdiccionesDocumento11 páginasBases Biológicas de Las AdiccionesFrancisco Pardo100% (2)
- Tema 2 - Psicobiología Del Refuerzo-2Documento10 páginasTema 2 - Psicobiología Del Refuerzo-2lara martinezAinda não há avaliações
- Helen Kaplan. ModeloDocumento1 páginaHelen Kaplan. ModeloDaiana Piacenza0% (1)
- PSICOFARMACOLOGIA HerlynDocumento253 páginasPSICOFARMACOLOGIA HerlynDani ReartesAinda não há avaliações
- La Epigenesis y El Sistema de La Recompensa en El Cerebro en Las AdiccionesDocumento14 páginasLa Epigenesis y El Sistema de La Recompensa en El Cerebro en Las AdiccionesDeisy Mirian Acuña LaymeAinda não há avaliações
- Amor y Adicción - Revista Chilena de NeuropsicologíaDocumento7 páginasAmor y Adicción - Revista Chilena de NeuropsicologíaAnonymous x82e9Nb0Ainda não há avaliações
- Adicción A Las Drogas - Una Enfermedad CerebralDocumento15 páginasAdicción A Las Drogas - Una Enfermedad CerebralfaniaintensaAinda não há avaliações
- Psicofarmacos Primer Parcial Semanas 1 A 6Documento251 páginasPsicofarmacos Primer Parcial Semanas 1 A 6Facundo LopezAinda não há avaliações
- Sistema NerviosoDocumento7 páginasSistema NerviosoAnnel LopezAinda não há avaliações
- Antidepresivos Cap3Documento19 páginasAntidepresivos Cap3SofiaSolDupinAinda não há avaliações
- El Cerebro y Sus AdiccionesDocumento11 páginasEl Cerebro y Sus AdiccionesRakel CastroAinda não há avaliações
- Primer Control de Lectura-AdiccionesDocumento12 páginasPrimer Control de Lectura-AdiccionesLETICIA ISIS ESPINOZA VARGASAinda não há avaliações
- Porque El Alcohol Es AdictivoDocumento9 páginasPorque El Alcohol Es AdictivoCandi Kamira BalladaresAinda não há avaliações
- PsicofarmacologíaDocumento47 páginasPsicofarmacologíaRosa Balmaseda CasabóAinda não há avaliações
- Circuitos de RecompensaaDocumento12 páginasCircuitos de RecompensaamajotojoAinda não há avaliações
- Psicofisiología de Las AdiccionesDocumento5 páginasPsicofisiología de Las Adiccionesyorleny PerezAinda não há avaliações
- A DicciónDocumento8 páginasA Dicciónsebas0716Ainda não há avaliações
- Bases Biológicas de La AdicciónDocumento29 páginasBases Biológicas de La AdicciónLiam CasanovaAinda não há avaliações
- Sustrato Neuroanatómico de La Adicción A Drogas PDFDocumento7 páginasSustrato Neuroanatómico de La Adicción A Drogas PDFmyfreudAinda não há avaliações
- Los Efectos Que Tiene La Pornografía en El CerebroDocumento10 páginasLos Efectos Que Tiene La Pornografía en El CerebroAntonioGutirresPrado100% (1)
- Guia Sistema Nervioso PDFDocumento8 páginasGuia Sistema Nervioso PDFBRAYAN DAVID CALDERÓN TOSCANOAinda não há avaliações
- Lüscher, Christian (2015) : La Trampa de La AdicciónDocumento8 páginasLüscher, Christian (2015) : La Trampa de La Adicciónakme73Ainda não há avaliações
- Neurociencia de Las Adicciones PDFDocumento6 páginasNeurociencia de Las Adicciones PDFcarlos perez leonAinda não há avaliações
- Psi Co Farm Acolo GiaDocumento4 páginasPsi Co Farm Acolo GiaxnanuxAinda não há avaliações
- Monogvii 4. Dependencia Por El TabacoDocumento17 páginasMonogvii 4. Dependencia Por El Tabacodianab1983Ainda não há avaliações
- Act - 3.1 - Control Aversivox3Documento4 páginasAct - 3.1 - Control Aversivox3Karen BarreraAinda não há avaliações
- Adicción A Las Drogas y Circuitos de Recompensa Del CerebroDocumento7 páginasAdicción A Las Drogas y Circuitos de Recompensa Del CerebroUssiel RamírezAinda não há avaliações
- Sistema Del Are Com Pens ADocumento20 páginasSistema Del Are Com Pens AKaren Andrea MESA BARRERAAinda não há avaliações
- Sistemas Dopaminergicos, Opioides, Cananaboideos en AdiccionesDocumento4 páginasSistemas Dopaminergicos, Opioides, Cananaboideos en AdiccionesDanny LopezAinda não há avaliações
- Introducción A La Farmacología Del SNCDocumento2 páginasIntroducción A La Farmacología Del SNCLeonardo GiraldoAinda não há avaliações
- Razones Evolutivas Que Son Inconsistentes Con El Consumo de Sustancias PsicoactivasDocumento21 páginasRazones Evolutivas Que Son Inconsistentes Con El Consumo de Sustancias PsicoactivasAlvaro CastroAinda não há avaliações
- Koob, G.F. Volkow, Nora D. (2016) : Neurobiología de La Adicción: Un Análisis de NeurocircuitoDocumento31 páginasKoob, G.F. Volkow, Nora D. (2016) : Neurobiología de La Adicción: Un Análisis de Neurocircuitoakme730% (1)
- Cerebro AdictoDocumento11 páginasCerebro AdictoveronicaAinda não há avaliações
- Corominas, M. (Et Al.) (2009) : El Sistema Dopaminérgico en Las AdiccionesDocumento11 páginasCorominas, M. (Et Al.) (2009) : El Sistema Dopaminérgico en Las Adiccionesakme73Ainda não há avaliações
- Entrega 1 Escenario 4 N NeurofisiologiaDocumento5 páginasEntrega 1 Escenario 4 N NeurofisiologiaDuranyAinda não há avaliações
- Resumen para El 1º Parcial - Psicofarmacología (Herly - 2013) - Psicología - UBADocumento20 páginasResumen para El 1º Parcial - Psicofarmacología (Herly - 2013) - Psicología - UBANico NicoAinda não há avaliações
- Ensayo de NeurofarmacologiaDocumento13 páginasEnsayo de NeurofarmacologiaMartín Campos IslasAinda não há avaliações
- El Cerebro Adicto Eric NestlerDocumento4 páginasEl Cerebro Adicto Eric NestlerGera NauthizAinda não há avaliações
- Biologia D e La DepresiónDocumento10 páginasBiologia D e La DepresiónTirso VazquezAinda não há avaliações
- Fisiopatología de La AdicciónDocumento6 páginasFisiopatología de La AdicciónALISON YESSENIA LARIOS MENDEZAinda não há avaliações
- Neuropsicología: Los fundamentos de la materiaNo EverandNeuropsicología: Los fundamentos de la materiaNota: 5 de 5 estrelas5/5 (1)
- Las sustancias de los sueños: NeuropsicofarmacologíaNo EverandLas sustancias de los sueños: NeuropsicofarmacologíaNota: 5 de 5 estrelas5/5 (1)
- Teoría polivagal: Descubrir el poder curativo del nervio vago para superar la ansiedad, el trauma, la depresión y el estrés emocionalNo EverandTeoría polivagal: Descubrir el poder curativo del nervio vago para superar la ansiedad, el trauma, la depresión y el estrés emocionalNota: 4 de 5 estrelas4/5 (6)
- Braunstein - Por El Camino de FreudDocumento204 páginasBraunstein - Por El Camino de FreudDaysilirion100% (2)
- Adler - El Caracter NeuroticoDocumento186 páginasAdler - El Caracter NeuroticoUsua1100% (2)
- Dibujo Infantil y Comprensión Escénica Análisis Crítico Hermenéutico Desde Enfoque Psicoanalítico PDFDocumento28 páginasDibujo Infantil y Comprensión Escénica Análisis Crítico Hermenéutico Desde Enfoque Psicoanalítico PDFmyfreudAinda não há avaliações
- Arancel Clinico ReferencialDocumento1 páginaArancel Clinico ReferencialMíchel ÁngeloAinda não há avaliações
- Cooper, David (Editor) - La Dialéctica de La Liberación. 228p PDFDocumento228 páginasCooper, David (Editor) - La Dialéctica de La Liberación. 228p PDFmyfreudAinda não há avaliações
- Abordaje Psicoanalítico Grupal de Niños PDFDocumento18 páginasAbordaje Psicoanalítico Grupal de Niños PDFmyfreudAinda não há avaliações
- Cooper, David. La Muerte de La Familia. 308p PDFDocumento308 páginasCooper, David. La Muerte de La Familia. 308p PDFmyfreudAinda não há avaliações
- Familias Fuertes - Manual de Recursos para El FacilitadorDocumento113 páginasFamilias Fuertes - Manual de Recursos para El FacilitadormyfreudAinda não há avaliações
- Dibs, en Busca Del YoDocumento56 páginasDibs, en Busca Del YoAddrianna Allvarez D Tello100% (6)
- Revista Sopnia 2012-2Documento69 páginasRevista Sopnia 2012-2myfreudAinda não há avaliações
- Pautas Terapia Familiar Breve DeShazerDocumento103 páginasPautas Terapia Familiar Breve DeShazermyfreud100% (18)
- Clase 24 - Toxicologia de Aditivos AlimentariosDocumento17 páginasClase 24 - Toxicologia de Aditivos AlimentariosAnapaula Peña FloresAinda não há avaliações
- Trastorno Paranoide de La PersonalidadDocumento20 páginasTrastorno Paranoide de La Personalidadsilvana8989Ainda não há avaliações
- Dermatofitosis GatosDocumento10 páginasDermatofitosis Gatosvetspain5448100% (1)
- 1 Normas de Bioseguridad y Buenas Prc3a1cticas de LaboratorioDocumento5 páginas1 Normas de Bioseguridad y Buenas Prc3a1cticas de LaboratorioMarco Sebastián BenavidesAinda não há avaliações
- Prueba Primero Medio, Texto Expositivo, Argumentativo - Docx Versión 1Documento6 páginasPrueba Primero Medio, Texto Expositivo, Argumentativo - Docx Versión 1Volatile SlothAinda não há avaliações
- NP31 G192 TDocumento2 páginasNP31 G192 Treyesman100% (2)
- EpidemiologíaDocumento65 páginasEpidemiologíaGary Rios Dionicio50% (2)
- Simulacro Ciencias 03 PDFDocumento17 páginasSimulacro Ciencias 03 PDFGloria Luciana Muñoz VillalobosAinda não há avaliações
- TEB - IAAS, Precauciones Estandar y AdicionalesDocumento30 páginasTEB - IAAS, Precauciones Estandar y AdicionalesFabiola Andrea Munoz Salinas100% (1)
- Taller NE FormulasDocumento11 páginasTaller NE FormulasFLOR LILIANA HUANANBAL GUEVARAAinda não há avaliações
- Peret - El Gran JuegoDocumento170 páginasPeret - El Gran JuegoSiyosequesoy DiegoAinda não há avaliações
- Act Morfofisiologia Corregidos UnadDocumento36 páginasAct Morfofisiologia Corregidos UnadEdgar Garcia Enriquez100% (4)
- V 22 N 2 A 08Documento8 páginasV 22 N 2 A 08Milagros VargasAinda não há avaliações
- La Rendija para Enviar EditorialDocumento740 páginasLa Rendija para Enviar EditorialursulaAinda não há avaliações
- Higiene Fisica y MentalDocumento12 páginasHigiene Fisica y MentalgardexxAinda não há avaliações
- Campo - Año 16 - Numero 185 - Noviembre 2016 - Paraguay - PortalguaraniDocumento142 páginasCampo - Año 16 - Numero 185 - Noviembre 2016 - Paraguay - PortalguaraniPortalGuarani3Ainda não há avaliações
- Cardiopatiìas Congeìnitas CianoìticasDocumento32 páginasCardiopatiìas Congeìnitas CianoìticaspolineAinda não há avaliações
- Carta de Pau DonésDocumento3 páginasCarta de Pau DonésZar FiorentiniAinda não há avaliações
- Departamento de Pediatria Facultad de Medicina Universidad Salvadoreña "Alberto MasferrerDocumento15 páginasDepartamento de Pediatria Facultad de Medicina Universidad Salvadoreña "Alberto MasferrerTeresita GuzmánAinda não há avaliações
- Clorfenamina y ResfrioDocumento2 páginasClorfenamina y ResfrioEstefanía PérezAinda não há avaliações
- 2parte Grupo 5 y 6Documento23 páginas2parte Grupo 5 y 6CharmolypiAinda não há avaliações
- Listado de Medicamentos VirtualDocumento42 páginasListado de Medicamentos VirtualCatherinaAndreaAinda não há avaliações
- BANFEDocumento11 páginasBANFEAnDrés BenavIdesAinda não há avaliações
- Los Fructanos y Su Papel en La Promocion de La SaludDocumento6 páginasLos Fructanos y Su Papel en La Promocion de La SaludFelipe NatarenAinda não há avaliações
- Esquema DepresiónDocumento1 páginaEsquema DepresiónMarco Salazar NúñezAinda não há avaliações
- Enfermedades de Transmisión SexualDocumento11 páginasEnfermedades de Transmisión SexualProfe JeremiasAinda não há avaliações
- Seminario de CancerDocumento28 páginasSeminario de CancerKevin García Murga100% (1)
- Actividad 4Documento8 páginasActividad 4Yadir Andres PinzonAinda não há avaliações
- Medicina Del Viajero Alejandra Macchi Coordinadora Medica CTHDocumento36 páginasMedicina Del Viajero Alejandra Macchi Coordinadora Medica CTHGABRIELA DELAinda não há avaliações