Escolar Documentos
Profissional Documentos
Cultura Documentos
Fisiología Renal Guyton Cap. 25-26-27
Enviado por
vxnheDescrição original:
Título original
Direitos autorais
Formatos disponíveis
Compartilhar este documento
Compartilhar ou incorporar documento
Você considera este documento útil?
Este conteúdo é inapropriado?
Denunciar este documentoDireitos autorais:
Formatos disponíveis
Fisiología Renal Guyton Cap. 25-26-27
Enviado por
vxnheDireitos autorais:
Formatos disponíveis
FACULTAD DE CIENCIAS MDICAS-ULEAM
POR MIGUEL BARZALLO
FISIOLOGA HUMANA GUYTON CAPTULO 25
LOS COMPARTIMIENTOS LIQUIDOS DEL CUERPO LIQUIDOS
EXTRACELULARE E INTRACELULAR; LQUIDO INTERSTICIAL Y EDEMA
Los ingresos y las perdidas de liquidos deben estar equilibrados en
condiciones de estabilidad; Existe un intercambio continuo de lquidos y de
solutos con el medio externo, y tambin entre los distintos compartimientos del
cuerpo.
El agua que ingresa en el organismo procede:
-La que se ingiere como lquidos, o formando parte de los alimentos slidos,
unos 2100 ml/da.
-La que se sintetiza en el organismo como resultado de la oxidacin de los
hidratos de carbono unos 200ml/da.
Ingreso total de agua de unos 230ml/da
PERDIDAS DIARIAS DE AGUA
Perdidas insensibles de agua.
Por evaporacin en el aparato respiratorio y por difusin a travs de la piel, que en conjunto representan unos 700ml/da de
agua en condiciones normales.
-Como perdida insensible de agua porque ocurre sin que el individuo la perciba o sea consciente de ella, es independiente
al sudor y existe incluso en las personas que han nacido sin glndulas sudorparas; perdida difusin, la piel representa
alrededor de 300 a 400 ml/da, minimizada por la capa cornea de la piel, cargada de colesterol, una barrera contra la
excesiva perdida de agua por difusin.
-La prdida insensible a travs del aparato respiratorio es de 300 a 400 ml/da, el aire que entra en las vas respiratorias, se
satura de humedad alcanzando una presin del vapor de unos 74 mm Hg. En el tiempo de frio la presin del vapor
atmosfrica se reduce casi hasta 0. Esto explica la sensacin de sequedad que se percibe en las vas respiratorias cuando
hace frio.
Perdidas de lquido por el sudor
Depende del ejercicio fsico y de la temperatura ambiente. El volumen de sudor es normalmente de 100 ml/da, pero en un
clima muy clido o con ejercicio fsico intenso, la prdida de agua por el sudor se eleva en ocasiones hasta 1 a 2 litros/hora.
Perdida de agua por los riones
Las restantes perdidas se producen con la orina excretada por los riones los cuales se enfrentan a la tarea de ajustar la
excrecin de agua y electrolitos para equipararlas exactamente a las cantidades de las sustancias que ingresan en el
organismo y, asimismo, de compensar las prdidas excesivas de lquidos y electrolitos que ocurren el algunos procesos
patolgicos. El volumen de la orina puede ser tan escaso como 0.5 l/da o 20 l/da en las personas deshidratada o las que
beben enormes cantidades de agua.
Perdida de agua por las heces
Normalmente se pierden unos 100ml/da pero esto puede aumentar en personas con diarreas intensas.
COMPARTIMIENTOS DE LOS LIQUIDOS CORPORALES
Lquidos corporales estn distribuido en dos grandes compartimientos; el lquido extracelular y el lquido intracelular lo que
a su vez el lquido extracelular se divide a su vez en lquido intersticial y plasma sanguneo.
Los
lquidos de los espacios sinovial, peritoneal, pericardico e intraocular, liquido cefalorraqudeo; su composicin puede ser
bastante distinta a la del plasma o a la del liquido intersticial por ello se le denomina Liquido transcelular. Todos los lquidos
transcelulares suman en conjunto de 1 a 2 litros aproximadamente.
COMPARTIMIENTO DEL LQUIDO INTRACELULAR
Unos 28 o 42 litros de lquido del cuerpo estan dentro de los 75 billones de clulas del cuerpo y que se denominan en
conjunto lquido intracelular. El lquido intracelular constituye el 40% aproximadamente del peso corporal en una persona, es
decir de unos 70 kg que es un 60%. Se considera que el lquido intracelular de todas las clulas juntas est formandado por
un solo compartimiento lquido.
COMPARTIMIENTO DEL LQUIDO EXTRACELULAR
Todos los lquidos situados fuera de las clulas se conocen en conjunto como liquido extracelular. Estos 20%
aproximadamente del peso corporal, es decir, unos 14 litros para un adulto normal de 70 kg de peso. Los dos mayores
compartimiento del liquido extracelular, el plasma representa 1/4 de las cuatro partes que se divide el liquido extracelular, o
sean unos 3 litros. El plasma es la porcin de la sangre acelular que intercambian sustancias con el lquido intersticial a
travs de los poros de la membrana capilar, lo cuales son muy permeables a casi todo los solutos del liquido extracelular
excepto las protenas, que estn ms concentradas en el plasma.
VOLUIMEN SANGUINEO
La sangre contiene lquido extracelular (del plasma) y liquido intracelular (de los eritrocitos) se considera como un
compartimiento liquido separado porque se encuentra alojada en su propia cmara el aparato circulatorio.
FACULTAD DE CIENCIAS MDICAS-ULEAM
POR MIGUEL BARZALLO
FISIOLOGA HUMANA GUYTON CAPTULO 25
El volumen sanguneo en los adultos normales es en promedio de un 7% del peso corporal, unos 5 litros. El 60%
aproximadamente de sangre es plasma y el 40 % son eritrocitos, pueden variar por edad, sexo.
HEMATOCRITO (VOLUMEN DE LOS HEMATIES EMPAQUETADOS O CONCENTRADOS)
El hematocrito es la parte de la sangre que est formada por los hemates. En los varones normales, se obtiene un
hematocrito de 0.40, aproximadamente, y en las mujeres normales, es de alrededor de 0.36. En la anemia intensa, el
hematocrito puede descender incluso al 0.10, una cifra que apenas es suficiente para mantener la vida. Proceso en una
produccin excesiva de hemates y que dan lugar a una policitemia. El hematocrito puede elevarse hasta 0.65.
Las composiciones ionicas del plasma y el lquido intersticial son similares
El plasma y los lquidos intersticiales estn separados nicamente por membranas
capilares que son muy permeables, la diferencia entre estos dos compartimientos
es la mayor concentracin de protenas que tiene el plasma; los capilares son
pocos permeables a las protenas del plasma y, por tanto, solo se escapan
pequeas cantidades de protenas hacia los espacios intersticiales en la mayora de
los tejidos, el efecto Donnan consiste en que los iones con cargadas positivas,
tienden a unirse a los cationes, como son los iones de sodio o potasio, que los liga
a las portenas plasmticas que tienen cargas negativas. A la inversa, los iones con
cargas negativas (aniones) tienden a estar algo ms concentrados en el lquido
intersticial que en el plasma, porque las cargas negativas de las protenas
plasmticas repelen a los aniones con carga negativa. Se considera que la
concentracin de los iones existentes en el plasma y el lquido intersticial es
aproximadamente la misma. El plasma y el lquido intersticial, contiene grandes
cantidades de iones sodio y cloruro, cantidades bastante elevadas de iones
bicarbonato, pequeas cantidades de iones potasio, calcio, magnesio, fosfato y de
cidos orgnicos.
Constituyentes importantes del liquido intracelular
El lquido intracelular est separado del lquido extracelular por una membrana
celular selectiva que es muy permeable al agua, pero no a la mayora de los electrolitos del cuerpo. A diferencia del lquido
extracelular, el lquido intracelular solo contiene pequeas
cantidades de iones sodio y cloruro y casi nada de iones calcio.
En cambio, contiene grandes cantidades de iones potasio y
fosfato, adems de cantidades moderadas de iones magnesio y
sulfato, todos los cuales se encuentran a bajas concentraciones
en el lquido extracelular. Las clulas contienen gran cantidad de
protenas, casi cuatro veces ms que en el plasma.
1)
2)
3)
DETERMINACION DEL VOLUMEN DE LOS LIQUIDOS
EL PRINCIPIO DE LA DILUCION DEL INDICADOR.
La masa total de una sustancia tras la dispersin en un
comportamiento lquido ser la misma que la masa total que se
ha inyectado en el compartimiento. No ha salido nada de esa
sustancia la masa total de esa sustancia en el compartimiento
(Volumen B x Concentracin de B) ser igual a la masa total de la
sustancia que inyecto (Volumen A x Concentracin A
Este metodo se puede utilizar prcticamente para medir el
volumen de cualquier compartimiento del cuerpo mientras:
El indicador se distribuya homogneamente por todo el
compartimiento.
El indicador se disperse solo en el compartimiento que se va a medir.
El indicador no se metabolice ni se elimine.
DETERMINACION DEL AGUA TOTAL.
Se puede usar agua reactiva, agua pesada, para medir el agua total del cuerpo. otra sustancia es la antipirina, muy
liposoluble y puede atravesar rpidamente las membranas celulares y distribuirse homogneamente por la totalidad de los
compartimientos intracelulares y extracelulares
DETERMINACION DEL VOLUMEN LQUIDO EXTRACELULAR.
El volumen de lquido extracelular se puede calcular usando cualquiera de las sustancias que se distribuyen en el plasma y
el lquido intersticial, pero no atraviesan fcilmente las membranas celulares. Tales son el sodio reactivo, el cloruro
radiactivo, el yotalamato radiactivo, el ion tiosulfato y la inulina suele dispersarse casi completamente por todos los lquidos
extracelulares en 30 a 60 minutos.
CALCULO DEL VOLUMEN DEL LQUIDO INTRACELULAR
El volumen del lquido intracelular no puede medirse directamente, pero puede calcular as:
Volumen intracelular = Agua corporal total Volumen extracelular. (Vo Int.= 60% - 20%= 40%)
FACULTAD DE CIENCIAS MDICAS-ULEAM
POR MIGUEL BARZALLO
FISIOLOGA HUMANA GUYTON CAPTULO 25
CALCULO DEL VOLUMEN DEL LQUIDO INTERSTICIAL
El volumen del lquido intersticial no puede medirse directamente, pero puede calcular as:
Volumen de Lq. intersticial = V. de lquido extracelular Volumen plasmtico (Vo Liq. Int= 20% - 0.5% =15%)
REGULACION DE LOS INTERCAMBIOS DE LIQUIDOS Y DE LOS EQUILIBRIOS OSMOTICOS ENTRE LOS LIQUIDOS
INTRACELULAR Y EXTRACELULAR.
La distribucin de los lquidos entre los comportamientos intracelular y extracelular est determinada principalmente por la
accin osmtica de los solutos ms pequeos como el sodio, el cloruro y otros electrolitos, actan a travs de la membrana
celular. Las membranas celulares son muy permeables al agua, pero es relativamente impermeable incluso a los iones
pequeos, como el sodio y el cloruro. El agua se desplaza rpidamente a travs de la membrana celular, de modo que el
lquido intracelular se mantiene isotnico con el lquido extracelular.
Principios basicos de la osmosis y la presion osmotica
La osmosis es la difusin neta de agua a travs de una membrana con permeabilidad selectiva desde una zona de gran
concentracin de agua a otra con menor concentracin de agua. Cuanto mayor es la concentracin de solutos en una
solucin menor en la concentracin de agua. El agua difunde desde una zona con baja concentracin de solutos
(concentracin elevada de agua) a otra que tiene una concentracin elevada de solutos (concentracin baja de agua). La
membrana celular es bastante impermeable a la mayora de los solutos, pero es muy permeable al agua (permeabilidad es
selectiva), siempre que haya una concentracin se solutos ms alta a un
lado de la membrana pasando hacia la zona con mayor concentracin de
solutos. Que si se aade un soluto, como el cloruro sdico, al lquido
extracelular, el agua difunde rpidamente desde las clulas atravesando
las membranas celulares hasta que se iguala la concentracin de agua a
ambos lados de la membrana. A la inversa, si se extrae un soluto, como el
cloruro sdico, del liquido extracelular atravesando las membranas
celulares para pasar al interior de las clulas. La velocidad de difusin del
agua se denomina velocidad de la osmosis.
Relacion entre miles y osmoles.
Trmino que define la concentracin total de las partculas de soluto
disueltas, independientemente de la cual sea su composicin exacta. El
nmero total de partculas en una solucin se mide en trminos de
osmoles. Un osmol (osm) es igual a 1 mol de partculas del soluto. Una
solucin que contiene un mol de glucosa por litro tiene una concentracin
de 1 osmol/L. Si una molcula se disocia en dos iones como ocurre
cuando el cloruro sdico se ioniza y da iones de cloruro e iones sodio, una
solucin que contiene 1 mol/L. tendr una concentracin osmtica de 2 osm/L, por tanto el trmino osmol seala el nmero
de partculas osmticamente activas que existen en una solucin, y no a la concentracin molar. Habitualmente el trmino
miliosmol (mOsm), que equivale a 1/1000 osmoles.
Osmolalidad y osmolaridad
La concentracin osmolal de una solucin se llama osmolalidad cuando la concentracin se expresa en osmoles por
kilogramo de agua; y se llama osmoralidad cuando se expresa en osmoles por litro de solucin.
Presion osmotica
La magnitud exacta de presin que se necesita para impedir la osmosis se llama
presin osmtica. La presin osmtica es una med ida indirecta de la
concentracin de agua y solutos de una solucin. Cuando mayor es la presin
osmtica de una solucin, menor es la concentracin de agua, pero mayor es la
concentracin de solutos de la solucin.
Relacion entre la presion osmotica y la osmoralidad
La presin osmtica de una solucin es directamente proporcional a la
concentracin de las partculas osmticamente activas de la presin osmtica de
esa solucin, esta presin es proporcional a su osmolaridad, una medida de la
concentracin de partculas de solutos.
Calculo de la osmolaridad y de la presion osmotica de una solucion
Los iones sodio y cloruro no se comportan como partculas completamente
independientes en la solucin debido a la atraccin que existe entre esos dos iones. Se puede corregir estas
desviaciones, factor de correccin llamado coeficiente osmtico. El coeficiente osmtico del cloruro sdico es
de 0.93 aproximadamente. La osmolaridad real de una solucin de cloruro sdico al 0.9% es de 308 x 0.93, es
decir unos 286 mOsm/L.
FACULTAD DE CIENCIAS MDICAS-ULEAM
POR MIGUEL BARZALLO
FISIOLOGA HUMANA GUYTON CAPTULO 25
Osmolaridad de los liquidos corporales
Alrededor de 80% de la osmolaridad total del lquido intersticial y del plasma se debe a los iones sodio y
cloruro, mientras que en el lquido intracelular, casi la mitad de la osmolalidad se debe a los iones potasio y el
resto se distribuye entre otras muchas sustancias intracelulares.
LIQUIDOS ISOTONICOS, HIPOTONICOS E HIPERTONICOS
Si se coloca a una clula en la solucin que contengan solutos no difusibles y cuya osmolaridad sea de 282 mOsm/L, la
clula no se encoger no se hinchara porque las concentraciones del agua en los lquidos intracelular y extracelular son
iguales y los solutos no pueden entrar y salir de la clula. Esa solucin es isotnica porque no produce retraccin no
hinchazn de las clulas. Ejemplos de la solucin isotnicas la solucin de cloruro sdico al 0.9% o la solucin glucosa al
5%. Pueden administrarse en la sangre sin peligro de que se altere el
equilibrio osmtico, si se coloca una clula en la solucin hipotnica
que contenga menores concentraciones de solutos no difusibles
(menos de 282 mOsm/L), el agua penetrara en la clula haciendo que
esta se hinche; el agua seguir pasando y diluyendo el liquido
extracelular se ir concentrando hasta que ambas soluciones tengan
aproximadamente la misma osmolaridad, de cloruro sdico con inferior
a 0.9% hipotnicas y producen hinchazn de las clulas. Una clula en
una solucin hipertnica que tenga una concentracin ms alta de
solutos no difusibles, el agua saldr de las clulas hacia el espacio
extracelular, con lo que se concentrara el lquido intracelular y se diluir
el lquido extracelular. La clula se encoger hasta que se igualen
ambas concentraciones. Cloruro sdico es mayor del 0.9% son
hipertnicas.
LIQUIDOS ISOSMOTICOS, HIPEROSMOTICOS
E HIPOSMOTICOS.
Los trminos isotnicos, hipotnico e hipertnico se refiere al hecho de
que las soluciones produzcan o no cambios en el volumen d las clulas.
La cantidad de las soluciones depende de las concentraciones de los
solutos no difusibles. Las soluciones que tienen la misma osmolalidad
que las clulas se llaman isosmoticas, independientemente de que los solutos sean capaces o no de atravesar la
membrana celular.
Los trminos hiperosmotico e hipsomotico se refieren a las soluciones que tienen de mayor o menor
osmolaridad, respectivamente, que el lquido extracelular normal, sin tener en cuenta si los solutos atraviesan o no la
membrana celular.
El equilibrio osmotico entre los liquidos intracelular y extracelular se alcanza rapidamente
El paso de lquido a travs de la membrana celular se produce tan rpidamente que cualquier diferencia de osmolaridad
entre estos dos compartimientos se corrige habitualmente en cuestin de segundos o, como mucho, en unos minutos, la
razn de esto es que los lquidos suelen llegar al cuerpo a travs del intestino y deben transportarse por la sangre a todos
los tejidos antes de que pueda producirse el equilibrio osmtico completo. Suelen transcurrir unos 30 minutos antes de que
obtenga el equilibrio osmtico en todo el cuerpo despus de beber agua.
Volumenes y osmolalidades de los liquidos extracelular e intracelular en condiciones anormales
Factores que pueden hacer que los volmenes de los lquidos extracelular e intracelular cambien intensamente son: la
ingestin de agua, la deshidratacin, la administracin intravenosa de los distintos tipos de soluciones existentes, la perdida
de grandes cantidades de liquido por el tracto gastrointestinal, y la prdida de cantidades anormales de liquido en el sudor
o a travs de los riones. Principios bsicos:
1.
2.
El agua se desplaza rpidamente a travs de las membranas celulares; por tanto, la osmolaridades de los
lquidos intracelular y extracelular se mantienen casi exactamente iguales entre s, salvo durante escasos minutos
despus de un cambio en cualquiera de esos comportamientos.
Las membranas celulares son casi totalmente impermeables a muchos solutos, por tanto, el nmero de osmoles
del lquido extracelular o intracelular se mantiene constante salvo que se aadan o se pierdan solutos del
comportamiento extracelular.
Consecuencias de la adiccion de solucion salina al lquido
Se aade una solucin salina isotnica al compartimiento del lquido
extracelular, la osmolaridad del liquido extracelular no se modifica; por
tanto, no se produce osmosis a travs de las membranas celulares.
Si se aade
una solucin hipertnica extracelular, aumenta la
osmolaridad extracelular y se produce osmosis con salida del agua de
las clulas hacia el compartimiento celular, y el lquido difunde desde las
clulas hacia el espacio extracelular para que se produzca el equilibrio
osmtico. El resultado final es un aumento de volumen celular, si se
aade una solucin hipotnica al lquido extracelular, y parte del agua
extracelular difunde al interior de las clulas hasta que los
comportamientos intracelular y extracelular tienen la misma
osmoralidad.
FACULTAD DE CIENCIAS MDICAS-ULEAM
POR MIGUEL BARZALLO
FISIOLOGA HUMANA GUYTON CAPTULO 25
ALTERACIONES CLINICAS DE LA REGULACION DEL VOLUMEN DE LOS LIQUIDOS:
HIPONATREMIA E HIPERNATREMIA
La concentracin de sodio en plasma es un indicador bastante fiel de la osmoralidad del plasma en muchas situaciones.
Cuando la concentracin de sodio en plasma desciende por debajo de lo normal (unos 142 mEq/L), tiene hiponatremia.
Cuando se eleva por encima de lo normal tiene hipernatremia.
Causas de hiponatremia: exceso de agua o prdidas de sodio
La disminucin de la concentracin de sodio en el plasma puede deberse a la perdida de cloruro sdico del liquido
extracelular o a la adiccin de un exceso de agua al liquido extracelular. La prdida primaria de cloruro sdico produce una
deshidratacin hiposmotica y se asocia a una reduccin de volumen del lquido extracelular. Los procesos que pueden
producir hiponatremia por perdida de cloruro sdico comprenden la diarrea y los vmitos. El consumo excesivo de diurticos
que inhiben la capacidad de los riones para retener el sodio y algunas formas de nefropatas con prdida de sodio tambin
puede producir una hiponatremia de intensidad moderada la enfermedad de Addison, con menor secrecin de la hormona
aldosterona, deteriora la capacidad de los riones para reabsorber el sodio y puede producir un grado moderado de
hiponatremia. Tambin puede asociarse hiponatremia a un exceso de retencin de agua, la cual diluye el sodio del lquido
extracelular, un proceso que se denomina sobrehidratacion hiposmotica. La secrecin excesiva de hormonas antidiuretica,
que hace que los tbulos renales reabsorban ms agua, puede dar lugar a hiponatremia y sobrehidratacion.
Causas de hipernatremia: perdida de agua o exceso de sodio
El aumento de la concentracin de sodio en el plasma, que produce tambin un aumento de la osmolaridad, puede deberse
bien a una prdida de agua del liquido extracelular, con la consiguiente concentracin de los iones sodio, o bien a un
exceso de sodio en el liquido extracelular. Cuando la alteracin primaria es la perdida de agua del espacio extracelular se
produce una deshidratacin hiperosmotica (hipertnica). Cuando hay una incapacidad para la secrecin de la hormona
antidiuretica, sustancias necesarias para que los riones conserven el agua. Cuando la falta de la hormona antidiuretica, los
riones secretan grandes cantidades de orina diluida (un proceso llamado diabetes inspida), que produce deshidratacin y
aumento de la concentracin de cloruro de sdico en el liquido extracelular. Una causa ms frecuente de hipernatremia
asociada a una disminucin del volumen del lquido extracelular es la deshidratacin producida por una ingestin de agua
inferior al agua que pierde el cuerpo, como ocurre con la sudoracin que se produce en el ejercicio fsico intenso.
Tambin puede aparecer hipernatremia como consecuencia de un exceso de cloruro sdico aadido al lquido extracelular.
Esto se produce con frecuencia por una sobrehidratacion hiperosmotica, por el exceso de cloruro sdico extracelular suele
asociarse tambin a cierto grado de retencin de agua por los riones. La secrecin excesiva de la hormona que retiene
sodio, la aldosterona, puede producir una ligera hipernatremia y sobrehidratacion. La razn de que la hipernatremia no sea
ms intensa es que la secrecin elevada de aldosterona hace que los riones reabsorban mayores cantidades de agua y
sodio.
EDEMA: EXCESO DE LQUIDO EN LOS TEJIDOS
El edema es la presencia de un exceso de lquido en los tejidos corporales, se produce principalmente en el compartimiento
del lquido extracelular, pero puede afectar tambin a los lquidos intracelulares.
Edema intracelular
Hay dos procesos que predisponen especialmente a la hinchazn intracelular:
1) la depresin de los sistemas metablicos de los tejidos, 2) la falta de nutricin suficiente de las clulas. Por ejemplo,
cuando el riego sanguneo de un tejido disminuye, el aporte de oxigeno y de nutrientes desciende; si el riego sanguneo se
vuelve demasiado lento para mantener el metabolismo normal, la bomba de iones de la membrana celular reduce su
funcionamiento. Los iones sodio que incluso normalmente penetran en las clulas ya no pueden bombearse hacia el
exterior y el exceso de sodio intracelular produce, por osmosis el paso de agua al interior de las clulas. Esto puede
producir el aumento del volumen intracelular en alguna zona de tejido hasta dos o tres veces lo normal. Cuando ocurre esto,
suele ser el anuncio de la muerte del tejido.
Edema extracelular
Se produce cuando hay retencin excesiva de lquido en los espacios extracelulares. En general, hay dos causas de
edema extracelular:
1) La salida anormal de liquido desde el plasma a los espacios intersticiales a travs de los capilares y,
2) El fracaso de los linfticos para retornar el lquido desde el intersticio de la vuelta hacia la sangre.
FACTORES QUE PUEDEN AUMENTAR LA FILTRACION CAPILAR
Filtracin = Kf x (Pc- Pli c + li)
En esta ecuacin puede verse que la filtracin capilar puede aumentar con cualquiera de los cambios siguientes:
Aumento del coeficiente de filtracin capilar.
Aumento de la presin hidrosttica capilar.
Disminucin o reduccin de la presin coloidosmtica del plasma.
La obstruccion linfatica produce edema
Cuando se produce un bloqueo de los linfticos, el edema puede ser especialmente intenso, porque las protenas
plasmticas que se escapan al intersticio no tienen posibilidad de eliminarse. Al elevarse la concentracin de las protenas,
aumenta la presin coloidosmotica del lquido intersticial, la cual retira aun ms lquidos de los capilares.
Puede haber bloqueo de los vasos linfticos en algunas formas de cncer o despus de una intervencin quirrgica en la
que se elimina los vasos linfticos o quedan obstruidos, o por infecciones producidas por nemtodos como las filarias.
FACULTAD DE CIENCIAS MDICAS-ULEAM
POR MIGUEL BARZALLO
FISIOLOGA HUMANA GUYTON CAPTULO 25
RESUMEN DE LAS CAUSAS DE EDEMA EXTRACELULAR
Hay muchos procesos que pueden causar retencin de lquidos en los espacios intersticiales, bien sea por escapes anormales de
lquido de los capilares. O bien porque impiden que los vasos linfticos devuelvan los lquidos desde el intersticio a la circulacin.
I.
Aumento de la presin capilar
III.
Aumento de la permeabilidad capilar
A. Retencin excesiva de agua y sal por el rin
A.
Reacciones inmunitarias que producen
1. Insuficiencia renal aguda o crnica
liberacin de histamina y otras sustancias
2. Exceso de mineral o corticoides
inmunitarias
B. Elevacin de presin venosa
B. Toxinas
1. Insuficiencia cardiaca
C. Infecciones bacterianas
2. Obstruccin venosa
D. Carencia vitamnicas, especialmente de
3. Impulsin insuficiente de la sangre venosa
vitamina C
a) Parlisis de los msculos
E. Isquemia prolongada
b) Inmovilizacin de partes del cuerpo
F. Quemaduras
c) Insuficiencia de las vlvulas venosas
IV.
Obstruccin al drenaje linftico
C. Disminucin de la resistencia arteriolar
A. Cncer
1. Excesivo calor corporal
B. Infecciones (p.ej., por nematodos filarias)
2. Insuficiencia
del
sistema
nervioso
C. Intervenciones quirrgicas
simptico
D. Ausencia o anomalas congnitas de los
3. Frmacos vasodilatores
vasos linfticos.
II.
Disminucin de las protenas plasmticas
A. Perdidas de protenas por la orina
B. Perdida de protenas por zonas cutneas
denudadas
1. Quemaduras
2. Heridas
C.
Sntesis insuficiente de protenas
1. Hepatopatas
2. Malnutricin grave de protenas o caloras
En resumen hay tres factores importantes:
1)
2)
3)
El aumento de la presin hidrosttica capilar.
La disminucin de la presin coloidosmotica del plasta, y
El aumento de la permeabilidad capilar, que produce escape de las protenas y de liquido a travs de los poros de los capilares
Edema producido por la insuficiencia cardiaca
En la insuficiencia cardiaca, el corazn no es capaz de impulsar normalmente la sangre procedente de las venas hacia las
arterias; esto produce elevacin de la presin venosa y de la presin capilar, que va seguida de aumento de la filtracin
capilar. La presin arterial tiene a descender, dando lugar a menor excrecin de agua y sal por los riones, lo cual aumenta
el volumen sanguneo y eleva mas la presin hidrosttica capilar, lo que causa todava ms edema, el menor riego
sanguneo a los riones estimula la secrecin de renina que da lugar a mayor formacin de angiotensina II y un aumento
de la secrecin de aldosterona, cosas ambas que dan lugar a mayor retencin de agua y sal por los riones.
En los pacientes con insuficiencia cardiaca izquierda, pero sin insuficiencia significativa del lado derecho del corazn, la
sangre es bombeada a los pulmones normalmente por el lado derecho del corazn, pero no puede salir fcilmente de las
venas pulmonares hacia el lado izquierdo del corazn porque esa parte del corazn est muy debilitada. Todas las
presiones vasculares pulmonares, incluida la presin capilar pulmonar, se elevan muy por encima de la normal,
produciendo un edema pulmonar grave que pone la vida en peligro. No se trata, la acumulacin de lquido en los pulmones
puede empeorar rpidamente y causar la muerte en pocas horas.
Edema debido a un excrecion disminuida de agua y sal por los riones
En las enfermedades renales que comprometen la excrecin urinaria de sal y agua. Hay grandes cantidades de agua y
sodio acumuladas en el espacio extracelular. La mayora de esta sal y agua excesiva se escapa de la sangre y penetra en
los espacios intersticiales, aunque en parte permanece en la sangre. Las consecuencias principales de estos son:
1. Aumento generalizado del volumen del liquido intersticial (edema extracelular) y
2. Hipertensin debida a aumento generalizado del volumen de sangre.
Edema debido a la disminucion de las proteinas plasmaticas.
Si disminuye la concentracin de las protenas del plasma, sea por dficit de formacin de las mismas en cantidades
normales, sea por escape de protenas del plasma, se produce un descenso de la presin coloidosmotica del plasma. Da
lugar a un aumento de la filtracin capilar en todo el cuerpo, seguido de edema extracelular. Perdida de protenas por la
orina, como ocurre en ciertas enfermedades renales, un proceso denominado sndrome nefrotico.
Haciendo que esas membranas se vuelvan permeables a las protenas del plasma y, a menudo, permitiendo que grandes
cantidades de estas protenas pasen a la orina. Cuando estas prdidas exceden a la capacidad del organismo para
FACULTAD DE CIENCIAS MDICAS-ULEAM
POR MIGUEL BARZALLO
FISIOLOGA HUMANA GUYTON CAPTULO 25
sintetizar protenas se produce un descenso de la concentracin de las protenas plasmticas. Cuando esa concentracin
desciende por debajo de 2.5 g/100mL, aparece un intenso edema generalizado.
La cirrosis heptica es otro proceso que produce la disminucin de la concentracin de protenas plasmticas. Cirrosis
significa la forma de gran cantidad de tejido fibroso entre las clulas parenquimatosas del hgado. Es que la fibrosis heptica
comprime los vasos que drenan la sangre de las vena porta a su paso por el hgado, antes de vaciarse en la circulacin
general. La dificultad para la salida de esta sangre por tal produce una elevacin de la presin hidrosttica capilar en todo el
territorio gastrointestinal y el consiguiente aumento de la filtracin de lquido que abandona el plasma para pasar a los
espacios intrabdominales. Las consecuencias combinadas de una menor concentracin de protenas plasmticas y una
elevacin de la presin capilar portal dan lugar a la trasudacin de grandes cantidades de lquido y protenas al interior de
la cavidad abdominal, un proceso que se conoce como ascitis.
FACTORES DE SEGURIDAD QUE NORMALMENTE IMPIDEN LOS EDEMAS
Existen tres factores de seguridad importantes que se oponen a la retencin de lquido en los espacios intersticiales:
1) La escasa distensibilidad del intersticio cuando la presin del lquido intersticial es negativa.
2) La capacidad del drenaje linftico para aumentar de 10 a 50 veces por encima de lo normal, y
3) La dilucin que experimenta las protenas del lquido intersticial, y que reduce la presin coloidosmotica del
lquido intersticial conforme aumenta la filtracin capilar.
Factores de seguridad debido a la escasa distensibilidad del intersticio mientras existe presion negativa.
La presin hidrosttica del lquido intersticial en la mayora de los tejidos subcutneos laxos del cuerpo es ligeramente
inferior a la presin atmosfrica, siendo su valor de 3-mm Hg por trmino medio. Este ligero efecto de succin que existe en
los tejidos ayuda a que estos se mantengan unidos. A una presin del lquido intersticial de -3mm Hg, el volumen de lquido
intersticial es de unos 12 litros. Mientras la presin del liquido intersticial esta en los limites negativos, todo pequeo cambio
del volumen del liquido intersticial se acompaa de cambios relativamente grandes en la presin hidrosttica del liquido
intersticial. Mientras se mantiene una presin negativa, la distensibilidad de los tejidos, que se define como el cambio de la
presin es escasa.
Cuando aumenta la presin hidrosttica del lquido intersticial, este aumento de presin tiende a oponerse a que prosiga la
filtracin capilar, mientras la presin hidrosttica del lquido intersticial siga siendo negativa, bastaran pequeos aumentos
del volumen del lquido intersticial, y estos actuaran oponindose a la filtracin y al paso de ms liquido al interior de los
tejidos. El factor de seguridad que acta contra el edema por este efecto consiste en un cambio de presin en el lquido
intersticial de alrededor de 3 mm Hg. En cuanto la presin del liquido intersticial aumenta por encima de 0 mm Hg, la
distensibilidad de los tejidos aumenta considerablemente, pudindose acumular grandes cantidades de liquido en los tejidos
en cuanto se producen aumentos adicionales relativamente pequeos de presin hidrosttica del liquido intersticial.
Importancia del gel intersticial para evitar la acumulacion de lquido en el intersticio.
En los tejidos normales que tienen una presin del liquido intersticial negativa, prcticamente todo el liquido del intersticio
est formando un gel. Que el lquido queda retenido o fijado a una red de proteoglucanos, de tal modo que prcticamente
no existen espacios con lquido libre mayores de unos centenares de micras de dimetro.
La importancia de este gel es que impide que el lquido se desplace o circule fcilmente por los tejidos debidos al
impedimento creado por las superficie en cepillo que forman los billones de filamentos de los proteoglucanos. Adems,
cuando la presin de los lquidos intersticiales desciende a valor muy negativo, el gel no se retrae mucho porque la red de
los filamentos de proteoglucanos ofrece resistencia elstica a la comprensin. La distensibilidad de los tejidos es muy baja
cuando las presiones son negativas, cuando la presin del lquido intersticial alcanza valores positivos, se produce una
enorme retencin de lquido libre en los tejidos. La mayor parte de ese lquido suplementario que se acumula es lquido libre
porque empuja y separa los filamentos que, en forma de cepillo, forman los proteoglucanos. De este modo. El edema se
denomina edema con fvea, y edema sin fvea
Importancia de los filamentos de proteoglucanos como espaciadores de las celulas y en la prevencion de la
circulacion rapida de lquido en los tejidos
Los filamentos de proteoglucanos junto con las fibrillas de colgeno mucho mayores que existen en los espacios
intersticiales, actan como espaciadores entre las clulas. Los nutrientes y los iones no difunden fcilmente a travs de las
membranas celulares; por tantos sin espacios adecuados entre las clulas, estos nutrientes, los electrolitos y los productos
de desecho de las clulas no podran intercambiarse rpidamente entre los capilares sanguneos y las clulas situadas a
cierta distancia unas de otras.
Los filamentos de proteoglucanos tambin impiden un flujo de lquidos demasiados fcil a travs de los espacios tisulares.
Si no hubiera filamentos de de proteoglucanos, la simple permanencia de una persona en pie, producir el desplazamiento
de gran cantidad de liquido en el intersticio, como ocurre en el edema, este liquido suplementario da lugar a que aparezcan
grandes conductos que permiten al liquido circular fcilmente a travs del intersticio. Por tanto cuando aparecen edemas
intensos en las piernas, es frecuente que parte del lquido del edema pueda disminuir simplemente elevando las piernas.
Aumento del flujo linfatico como factor de seguridad contra el edema
Una funcin importante del sistema linftico es devolver a la circulacin los lquidos y protenas que se filtran de los
capilares y al intersticio. Sin esta circulacin continua de retorno de las protenas filtradas y el lquido hacia la sangre, el
volumen plasmtico se agotara rpidamente y simultneamente se producir un edema intersticial. El factor de seguridad
representado por la circulacin linftica se ha calculado que es de unos 7 mm Hg.
Lavado de las proteinas del lquido intersticial como factor de seguridad
Se filtran al intersticio mayores cantidades de lquidos, la presin del lquido intersticial se eleva, aumentando la circulacin
de la linfa. En la mayora de los tejidos, la concentracin de protenas en el intersticio disminuye conforme la circulacin
linftica aumenta, porque la cantidad de protenas que se transportan hacia el exterior es mayor que las que pueden filtrarse
FACULTAD DE CIENCIAS MDICAS-ULEAM
POR MIGUEL BARZALLO
FISIOLOGA HUMANA GUYTON CAPTULO 25
en los capilares y pasar al intersticio; la razn de esto es que los capilares son bastantes impermeables a las protenas en
comparacin a los vasos linfticos. Por tanto, las protenas se lavan del lquido intersticial conforme aumenta el flujo
linftico. El factor de seguridad de este efecto frente al edema se ha calculado que es de unos 7 mm Hg.
Resumen de los factores de seguridad que evitan el edema
Los factores de seguridad que se oponen al edema:
1. El factor de seguridad que presenta la baja distensibilidad tisular cuando la presin del lquido intersticial es
negativa, es de unos 3 mm Hg.
2. El factor de seguridad que constituye el aumento de la circulacin linftica es de unos 7 mm Hg.
3. El factor de seguridad producido por el lavado de las protenas de los espacios intersticiales es de 7 mm Hg
El factor defensivo contra la formacin de edemas est constituido por unos 17 mm Hg. Esto significa que la presin de los
capilares en un tejido perifrico podra elevarse tericamente en 17 mm Hg, o duplicar aproximadamente su valor normal,
antes de que apareciera edema significativo.
LIQUIDOS DE LOS ESPACIOS POTENCIALES DEL CUERPO
Quiz la mejor manera de describir un espacio potencial es poner algunos ejemplos como son: la cavidad pleural, la
cavidad pericardica, la cavidad peritoneal, y la cavidades sinoviales que incluyen las cavidades articulares y las bolsas
serosas. Presentan superficies que casi estn en contacto unas con otras, pues solo existe una fina capa de lquido entre
ellas, y as esas superficies se deslizan fcilmente una sobre otra. Para favorecer ese deslizamiento, existe un lquido
proteinceo que acta como lubricante de esas superficies.
Los liquidos se intercambian entre los capilares y los espacios potenciales.
La membrana superficial de un espacio potencial no suele ofrecer una resistencia significativa al paso de los lquidos, los
electrolitos, ni las protenas siquiera pudiendo todos ellos entrar y salir entre el espacio y el lquido intersticial del tejido
circundante con relativa facilidad. Por tanto, cada espacio potencial es, en realidad, un gran espacio tisular.
Los vasos linfaticos drenan las proteinas d los espacios potenciales
Las protenas se acumulan en los espacios potenciales despus de escaparse de los capilares, lo mismo que sucede con
las protenas que se acumulan en los espacios intersticiales de todo el cuerpo, esas protenas deben eliminarse atraves de
los linfticos u otros conductos para devolverse a la circulacin. Cada espacio potencial esta unido directa o indirectamente
a los vasos linfticos.
El lquido de edema en los espacios potenciales se llama derrame
Cuando aparece edema en los tejidos subcutneos adyacentes a un espacio potencial, suele acumularse tambin lquido
del edema en dicha cavidad, y ese lquido se denomina derrame. De ah que la obstruccin de los linfticos o cualquier
otro trastorno capaz de producir derrames de la misma manera que causa edema intersticial. La cavidad abdominal esta
especialmente predispuesta a recoger liquido de derrame y, en este caso, el derrame se llama ascitis. En caso intenso,
puede acumularse 20 litros de lquido asctico o ms.
Los otros espacios potenciales, como la cavidad pleural, la cavidad pericardica y los espacios articulares, pueden hincharse
intensamente cuando hay edema generalizado. Adems, una lesin o una infeccin local de cualquier cavidad son
frecuentes que obstruya el drenaje linftico y que produzca una hinchazn aislada en cualquiera de las cavidades.
Tienen inters resaltar que la presin del liquido en la mayora en todos los espacios potenciales, sin que existe un estado
adematoso, es negativa, de la misma manera que esa presin es negativa (inferior a la atmosfrica) en los tejidos
subcutneos laxos. La presin hidrosttica del liquido intersticial es de unos -3 a -5 mm Hg en los espacios articulares, de -5
a -6 mm Hg en la cavidad pericardica y de unos -7 a -8 mm Hg en la cavidad pleural.
FACULTAD DE CIENCIAS MDICAS-ULEAM
POR MIGUEL BARZALLO
FISIOLOGA HUMANA GUYTON CAPTULO 26
FORMACION DE LA ORINA POR LOS RIONES;
GLOMERULAR, FLUJO SANGUINEO RENAL Y SU CONTROL.
FILTRACION
FUNCIONES MULTIPLES DE LOS RIONES EN LA HOMEOSTASIS.
Eliminar del cuerpo las sustancias de desecho que se han ingerido o se han
producido en el metabolismo. La regulacin del volumen y la composicin de los
lquidos corporales. Los riones realizan sus funciones ms importantes filtrando
el plasma y eliminando sustancias del filtrado en cuanta variable, segn las
necesidades del organismo, los riones depuran o aclaran las sustancias de
desecho del filtrado glomerular, los riones realizan numerosas funciones:
Excrecin de los productos metablicos de desecho y de las sustancias
qumicas extraas.
Regulacin del equilibrio hdrico y electroltico.
Regulacin de la osmolalidad de los lquidos corporales y de las
concentraciones de electrolitos.
Regulacin del equilibrio acidobsico.
Regulacin de la presin arterial.
Secrecin, metabolismo y excrecin de hormonas.
Gluconeogenesis.
Excrecin de los productos metablicos de desecho, sustancias qumicas extraas, frmacos
y metablicos de hormonas.
Eliminar los productos de desechos del metabolismo que ya no son necesarios. La urea (del metabolismo de los
aminocidos), la creatinina (de la creatina muscular), el acido rico (de los cidos nucledos) los productos finales de la
degradacin de la hemoglobina (como la bilirrubina) y los metabolitos de algunas hormonas. Eliminan tambin la mayora de
las toxinas y otras sustancias extraas que han producido por el cuerpo o han sido ingeridas, como los plaguicidas, los
frmacos y aditivos de los alimentos.
Regulacin del equilibrio hdrico y electroltico.
Los riones restablece el equilibrio entre los ingresos y las prdidas. Sin
embargo, durante los 2 a 3 das de adaptacin del rin a los ingresos elevados
de sodio, se produce una moderada retencin de sodio que aumenta ligeramente
el volumen del lquido extracelular y desencadena cambios hormonales.
Los riones tienen una capacidad enorme para modificar la excrecin de sodio en
respuesta a las variaciones en el ingreso de este catin. El ingreso de sodio
puede aumentar hasta 1500 mEq/da (menos la decima parte de lo normal), esto
tambin es cierto para el agua y la mayora de otros electrolitos, como los iones
de cloruro, potasio, calcio, hidrogeno, magnesio y fosfato.
Regulacin de la presin arterial.
Papel dominante en la regulacin a largo plazo de la presin arterial mediante la
excrecin de cantidades variables de sodio y agua. Contribuyen a la regulacin de
la presin arterial a corto plazo mediante la secrecin de factores o sustancias
vasoactivas, como la renina, que da lugar a la formacin de productos vasoactivos
(por ejemplo, la angiotensina II)
Regulacin del equilibrio acido bsico.
Los riones participan en la regulacin del equilibrio acido bsico, junto con los pulmones y los amortiguadores de los
lquidos corporales, mediante la excrecin de cidos y regulando las reservas de las sustancias amortiguadores en los
lquidos corporales.
Regulacin de la produccin de eritrocitos.
Los riones secreta eritropoyetina, una sustancia que estimula la produccin de
hemates. La hipoxia es un estimulo importante para la secrecin de eritropoyetina por
los riones. En las personas normales, los riones elaboran casi todas la eritropoyetina
secretada a la circulacin.
Regulacin de la formacin de 1,25-dihidroxivitamina d3
Los riones producen la forman activa de la vitamina D, la 1.25-dihidroxivitamina D3
(calcitriol). El calcitriol es esencial para el depsito normal de calcio en el hueso y la
absorcin de calcio en el tubo digestivo.
Sntesis de glucosa
Los riones sintetizan glucosa a partir de aminocidos y de otros percusores en
situaciones de ayuno prolongado, un proceso que se conoce como Gluconeogenesis.
Cuando la insuficiencia renal llega a su trmino, se produce una retencin en el
organismo de potasio, cidos, lquidos y otras sustancias que, en pocos das, es
suficiente producir la muerte.
FACULTAD DE CIENCIAS MDICAS-ULEAM
POR MIGUEL BARZALLO
FISIOLOGA HUMANA GUYTON CAPTULO 26
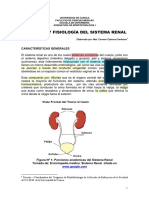
ANATOMIA FISIOLOGICA DE LOS RIONES
Organizacin general de los riones y de las vias urinarias
Los riones estn situados en la pared posterior del abdomen, por fura de la cavidad peritoneal, pesa unos 150 g y tiene el
tamao aproximado de un puo cerrado. La cara interna de cada rin tiene una regin en forma de muesca, llamada hilio,
atraves de la cual pasan la arteria y la vena renal, los linfticos, los nervios y el urter, que lleva la orina final desde el rin
a la vejiga, las dos regiones principales que pueden verse son la corteza externa y la regin interna llamada medula. La
medula est dividida en numerosas masas de tejido de forma cnica llamada
pirmides renales. La base de cada pirmide nace en el lmite entre la corteza y la
medula y termina en la papila que penetra en el espacio de la pelvis renal. El borde
externo de la pelvis se divide en pequeas bolsitas de extremos abiertos llamadas
clices mayores, los cuales se extienden por abajo y se dividen en los clices
menores, que recogen la orina de los tbulos de cada papila.
Aporte sanguneo renal.
El flujo sanguneo a los dos riones constituyen en condiciones normales, 22% del
gasto cardiaco, es decir, unos 1100 mL/-min. La arteria renal entra en el rin
atraves del hilio y, luego, se ramifica sucesivamente para formar las arterias
interlobulares, las arterias arciformes, las arterias interlobilillares (llamadas tambin
arterias radiales) y las arteriolas aferentes, que dan lugar a los capilares
glomerulares, donde se filtra gran cantidad de liquido y de solutos (excepto las
protenas del plasma) para empezar a formar la orina. Los extremos distales de los
capilares de cada glomrulo confluyen y forman la arteriola eferente, que da lugar
a una segunda red capilar formada por los capilares peritubulares que rodean a los
tbulos renales.
La circulacin renal es peculiar por tener dos lechos capilares estn dispuestos en
series y separados por las arteriolas eferente, las cuales ayudan a regular la
presin hidrosttica en los dos grupos de capilares. Una presin hidrosttica
elevada en los capilares glomerular (alrededor de 60 mm Hg) produce una
filtracin de lquido rpida, mientras que una presin hidrosttica mucho ms baja
en los capilares peritubulares permite la rpida reabsorcin de lquidos. Los
capilares peritubulares vacan en los vasos del sistema venoso, que discurren
paralelamente a los vasos arteriolares y forman sucesivamente la vena
interlobulillar, la vena arciforme, la vena interlobular y la vena renal.
La nefrona es la unidad funcional del rin
Cada rin est formado por 1 milln de nefronas, todas ellas son capaces de formar orina. El rin no puede regenerar
nefronas nuevas; por tanto, las lesione o las enfermedades renales, o el envejecimiento normal, producen una prdida
progresiva del numero de nefronas. Pasado los 40 aos de edad, el nmero de nefronas funcionantes suelen descender un
10 % cada ao; as que a los 80 aos muchas personas tienen
un 40 % menos de nefronas funcionantes que a los 40 aos.
Cada nefrona contiene:
Un penacho de capilares glomerulares, denominado
glomrulo, a travs del cual se filtran grandes cantidades de
liquido de sangre y
Un largo tbulo en el que el liquido filtrado se convierte
en orina en su recorrido hacia la pelvis renal.
El glomrulo est formado por una red de capilares glomerulares
que se ramifican y anastomosan entre si y que, comparados con
otros capilares, tienen unas presiones hidrostticas elevadas
(unos 60 mm Hg). Los capilares glomerulares estn recubiertos
por clulas epiteliales, y la totalidad del glomrulo est revestido
por la capsula de Bowman. El liquido que se filtra en los capilares
glomerulares discurre por el interior de la capsula de Bowman y,
luego por el tbulo proximal, que se encuentra en la corteza del
rin, desde el tbulo proximal, el liquido fluye al interior del asa
de Henle que se hunde en la medula renal. Cada asa est
formada por una rama descendente y una rama ascendente. Las
paredes de la rama descendente son muy delgadas y, por eso se
les llama segmento delgado del asa de Henle. Despus sus paredes se vuelven tan gruesas como las del resto del sistema
tubular y por eso se llama segmento grueso de la rama ascendente.
Al final de la rama ascendente gruesa hay un segmento corto que, en realidad, es una placa situada en la pared, que se
conoce como macula densa. Desempea un papel importante regulando la funcin de las nefronas. Pasando la macula
densa, el liquido atraviesa el tbulo distal se encuentra en la corteza renal. El tbulo distal va seguido del tbulo de
conexin y del tbulo colector cortical, que termina en el conducto colecto cortical. 8 o 10 conductos colectores corticales
se juntan para formar un solo conducto colector ms grande que discurre hacia abajo, penetra en la medula y se convierte
en el conducto colector medular confluyen para formar conductos cada vez mayores que finalmente vacan su contenido en
la pelvis renal en la que apunta de las papilas renales. En cada rin hay unos 250 conductos colectores muy grandes cada
uno de los cuales recoge la orina de unas 4000 nefronas.
FACULTAD DE CIENCIAS MDICAS-ULEAM
POR MIGUEL BARZALLO
FISIOLOGA HUMANA GUYTON CAPTULO 26
Diferencias regionales en la estructura de la nefrona: Nefronas Corticales
y Nefronas Yuxtamedulares.
Diferencias entre las nefronas dependiendo de la profundidad a que se
encuentran dentro de la masa renal. Las nefronas cuyos glomrulos estn
situados en la parte externa de la corteza se llaman nefronas corticales, y se
distinguen por tener asas de Henle cortas que tienen solo un breve recorrido
dentro de la medula, las nefronas tienen sus glomrulos situados
profundamente en la corteza renal, cerca de la medula, y se llama nefronas
yuxtamedulares. Estas nefronas tienen largas asas de Henle que penetran
profundamente en la medula y, a veces, todo su recorrido es intramedular
hasta alcanzar la punta de las papilas renales.
Las nefronas corticales, en estas ltimas, todo el sistema tubular est rodeado
de una extensa red de capilares peritubulares. Las nefronas yuxtamedulares,
las largas arteriolas aferentes se extienden desde los glomrulos hacia abajo
penetrando en la parte externa de la medula y entonces se dividen en
capilares peritubulares especializados llamados vasos rectos, los cuales se
extienden hacia abajo y dentro de la medula, adosados al asa de Henle. Los
vasos rectos vuelven a la corteza para terminar desembocando en las venas
corticales, esta red especializada de capilares de la medula desempea un
papel esencial en la formacin de una orina concentrada.
LA FORMACION DE LA ORINA ES EL RESULTADO DE LA FILTRACION
GLOMERULAR, LA REABSORCION TUBULAR Y LA SECRECION TUBULAR.
Tres procesos renales:
1) La filtracin glomerular
2) La reabsorcin de sustancias desde los tbulos renales a la sangre
3) La secrecin de sustancias desde la sangre al interior de los tbulos renales.
Velocidad de excrecin urinaria = velocidad de Filtracin velocidad de Reabsorcin + velocidad de Secrecin
La formacin de la orina comienza con la filtracin de una gran cantidad de liquido que prcticamente carece de protenas,
desde los capilares glomerulares a la capsula de Bowman. La mayora de las sustancias del plasma, excepto las protenas
se filtran libremente, de tal modo que sus concentraciones en el filtrado glomerular de la capsula de Bowman son casi las
mismas que en el plasma. Cuando el liquido filtrado sale de la capsula de Bowman y pasa por los tbulos, su composicin
se va modificando debido a la reabsorcin de agua y de determinados solutos, que son devueltos a la sangre, debidos a la
secrecin de otras sustancias que pasan desde los capilares peritubulares al interior de los tbulos.
La sustancia se filtra libremente por los
capilares glomerulares, pero no reabsorbe
ni se secreta. Por tanto, su tasa de
excrecin es igual a la tasa con que fue
filtrada
Determinados productos de desecho como la
creatinina, la sustancia se filtra libremente pero
tambin se reabsorbe parcialmente en los
tbulos y vuelve a la sangre. Por tanto la tasa
de excrecin urinaria es inferior a la tasa de
filtracin en los capilares glomerulares
La sustancia se filtra tambin libremente en
los capilares glomerulares, pero no se
excreta a la orina, porque toda la sustancia
filtrada se reabsorbe en los tbulos y vuelve
a la sangre. Este modelo lo constituyen los
aminocidos y la glucosa, permitiendo que
estas sustancias se conserven en los
lquidos corporales.
La sustancia se filtra libremente en los
capilares glomerulares y no se absorbe,
pero nuevas cantidades de estas
sustancias que circulan con la sangre por
los capilares peritubulares son secretadas
y pasan a los tbulos. Esto permite que las
sustancias sea depurada rpidamente de
la sangre y excretada por la orina.
Filtracin, Reabsorcin y Secrecin de las distintas sustancias
La reabsorcin tubular es cuantitativamente ms importante que la secrecin tubular dentro del proceso de formacin de la
orina, pero la secrecin desempea un papel importante en determinar las cantidades de iones de potasio e hidrgeno y de
algunas otras sustancias que se excretan por la orina, las sustancias de la sangre los productos finales del metabolismo
como la urea, la creatinina, el acido rico y los uratos, se reabsorben poco y, por tanto, se excreta en grandes cantidades
por la orina. Algunas sustancias extraas y los frmacos tambin se reabsorben poco pero, adems se secretan desde la
sangre a los tbulos, de modo que sus tasas de excrecin son elevadas, los electrolitos como los iones sodio, cloruro y
bicarbonato se reabsorben intensamente, por lo que solo aparecen en la orina en pequeas cantidades.
Los aminocidos y la glucosa, se reabsorben completamente en los tbulos y no aparecen en la orina aunque hayan filtrado
en grandes cantidades por los capilares glomerulares.
Para la mayora de las sustancias, las tasas de filtracin y de reabsorcin son extraordinariamente grandes en comparacin
con las tasas de excrecin. Los cambios en la filtracin glomerular y en la reabsorcin tubular suelen actuar de una manera
coordinada para que se produzcan los cambios necesarios por la excrecin renal.
FACULTAD DE CIENCIAS MDICAS-ULEAM
POR MIGUEL BARZALLO
FISIOLOGA HUMANA GUYTON CAPTULO 26
Por que se filtran en el rin grandes cantidades de solutos y se reabsorben despus?
Una ventaja de una TFG voluminosa es que permite a los riones eliminar rpidamente del cuerpo los productos del
desecho cuya excrecin depende principalmente de la filtracin glomerular. La mayora de las sustancias de desecho se
reabsorben mal en los tbulos y, por tanto, su eliminacin efectiva del cuerpo depende de una TFG elevada.
El volumen total del plasma es solo de unos 3 L, mientras que el TFG es de unos 180 L/da, esto significa que el plasma
puede ser filtrado y procesado unas 60 veces cada da. Esta TFG elevada permite a los riones controlar con presin y
rapidez el volumen y las composiciones de los lquidos corporales.
Composicin del filtrado glomerular
La formacin de la orina comienza con la filtracin de grandes cantidades de liquido a travs de los capilares glomerulares a
la capsula de Bowman. Los capilar glomerulares son relativamente impermeables a las protenas, por lo que el lquido
filtrado carece prcticamente de protenas y de elementos celulares, incluidos los hemates.
Casi la mitad del calcio del plasma y la mayora de los cidos grasos del plasma estn unidas a protenas, y esas fracciones
unidas no se filtran por los capilares glomerulares.
La TFG aproximadamente el 20% del flujo plasmtico renal
La TFG est determinada por:
1. El equilibrio de las fuerzas hidrostticas y coloidosmotica que actan a travs de la membrana capilar.
2. El coeficiente de filtracin capilar (Kf) que es el producto de la permeabilidad por el rea superficial de filtro de los
capilares.
Los capilares glomerulares tienen una tasa de filtracin mucho mayor que otros capilares debido a su elevada presin
hidrosttica glomerular y a su mayor Kf. En el adulto normal, la TFG es, en promedio, de 125 Ml/min, o sea, unos 180
L/da. Alrededor de unos 20 % del plasma que pasa por el rin se filtra en los capilares glomerulares se calcula
Fraccin de filtracin = TFG/Flujo plasmtico renal.
LA MEMBRANA DE LOS CAPILARES GLOMERULARES
Tres capas principales:
El endotelio capilar;
Una membrana basal, y
Una capa de clulas epiteliales (los podositos) que rodean la superficie
externa de la membrana basal capilar.
Estas capas, forman la barrera filtrante que a pesar de sus tres capas, es capaz de
filtrar varios cientos de veces las cantidades de agua y solutos que suelen atravesar la
membrana de los capilares habituales, impiden normalmente la filtracin de las
protenas del plasma. El endotelio capilar esta perforando por miles de pequeos
agujeros llamados fenestraciones (ventanas), que se parecen a los capilares
fenestrados que se encuentran en el hgado, son bastantes grandes, poseen una gran
cantidad de cargas negativas fijas que impiden el paso de las protenas del
plasmticas. Rodeando al endotelio esta la membrana basal que consta de una red de
colgeno y de fibrillas de proteoglucano con grandes espacios a travs de los cuales
se pueden filtrar grandes cantidades de agua y de solutos pequeos. La membrana
basal impide eficazmente la filtracin de las protenas plasmticas. La ltima parte es
una capa de clulas epiteliales que reviste la superficie externa del glomrulo. Estas
clulas no forman una capa continua, sino que tienen largas expansiones parecidas a
un pie (podocitos) que rodean la superficie externa de los capilares. Las expansiones
de los podocitos estn separadas por huecos llamados poros de rendija, (en
hendidura) a travs de los cuales se desplaza el filtrado glomerular. Las clulas
epiteliales, que tambin tienen carga negativa, proporcionan una restriccin adicional a la filtracin de las protenas
plasmticas.
Las grandes moleculas con carga negativa se filtran con menos facilidad que las moleculas de igual tamao
molecular cargadas positivamente
El dimetro molecular de la albmina plasmtica es solo de 6 nanmetros, mientras que los poros de la membrana
glomerular se cree que tienen 8 nanmetros (80 angstroms). Sin embargo, la filtracin de la albumina est restringida,
debido a su carga negativa y a la repulsin electrosttica que ejercen sobre ellas las cargas negativas de los
proteoglucanos de la pared capilar glomerular. La razn de estas diferencias de filtracin est en que las cargas negativas
de la membrana basal constituyen un medio importante para restringir la filtracin de grandes molculas cargadas
negativamente, como las protenas plasmticas. En un proceso que se conoce como nefropata de cambios mnimos;
debido a esa prdida de las cargas negativas sobre la membrana basal, algunas de las protenas de peso molecular ms
bajo, especialmente la albumina, se filtran y aparecen en la orina, dando como resultado lo que se llama proteinuria o
albuminuria.
Determinacin de la tasa del filtrado glomerular
La TFG est determinada por:
La suma de las fuerzas hidrostticas y coloidosmoticas a travs de la membrana glomerular, que nos da la
presin de filtracin neta, por
El coeficiente de filtracin capilar glomerular.
FACULTAD DE CIENCIAS MDICAS-ULEAM
POR MIGUEL BARZALLO
FISIOLOGA HUMANA GUYTON CAPTULO 26
TFG = Kf x presin de filtracin neta.
La presin de filtracin neta es la suma de las fuerzas hidrostticas y coloidosmoticas que favorecen o se oponen a la
filtracin a travs de los capilares glomerulares. Estas fuerzas son:
1)
2)
3)
4)
La presin hidrosttica en el interior de los capilares glomerulares que favorecen la filtracin
La presin hidrosttica en la capsula de Bowman fuera de los capilares que se oponen a la filtracin
La presin coloidosmotica de las protenas plasmticas de los capilares glomerulares que se oponen a
la filtracin, y
La presin coloidosmotica de las protenas en la capsula de Bowman que favorece la filtracin
Tiene fuerzas para favorecer la filtracin (mm Hg)
Presin hidrosttica glomerular
Presin coloidosmotica en la capsula de Bowman
Fuerzas que se oponen a la filtracin (mm Hg)
Presin hidrosttica de la capsula de Bowman
60
0
18
32
Presin coloidosmotica en los capilares glomerulares
Presin de filtracin = 60 18 32 = +10 mm Hg
Tericamente, el aumento del Kf aumenta la TFG, mientras que un Kf disminuido reduce la TFG. Sin embargo, los cambios
del Kf probablemente no representan un mecanismo importante para la regulacin da a da de la TFG. Pero algunas
enfermedades disminuyen el Kf reduciendo el nmero de capilares glomerulares funcionales (disminuyendo el rea o
superficie de filtracin), o aumentando el grosor de la membrana capilar glomerular y disminuyendo su conductividad
hidrulica. Por ejemplo, la hipertensin crnica no controlada y la diabetes mellitus reducen gradualmente el K f
aumentando el grosor de la membrana basal de los capilares glomerulares y, finalmente, lesionando los capilares tan
intensamente que se produce una prdida de la funcin capilar.
El aumento de la presion hidrostatica en la capsula de bowman disminuye la TFG.
La presin hidrosttica en la capsula de Bowman y en distintos puntos del tbulo proximal, segn clculos aproximados, de
unos 18 mm Hg en condiciones normales. El aumento de la presin hidrosttica en la capsula de Bowman disminuye la
TFG, mientras que la disminucin de esa presin aumenta la TFG. La precipitacin de calcio o de cido rico puede dar
lugar a la formacin de clculos que se alojan en las vas urinarias, con frecuencia en el urter, obstruyendo la salida de las
vas urinarias y aumentando la presin en la capsula de Bowman. Esto disminuye la TFG, y finalmente, puede daar o
incluso destruir al rin, a menos que se alivie la obstruccin.
El aumento de la presion coloidosmotica capilar glomerular disminuye la TFG
Cuando la sangre pasa desde la arteriola aferente atraves de los capilares glomerulares a las arteriolas eferentes, la
concentracin de las protenas plasmticas aumenta entorno al 20 %. La razn de esto es que una quinta parte
aproximadamente del lquido que atraviesa los capilares se filtra a la capsula de Bowman, concentrndose as las protenas
plasmticas glomerulares que no se filtran. Por tanto, la presin coloidosmotica promedio de las protenas plasmticas de
los capilares glomerulares est a mitad de camino entre los 28mm Hg lo habitual y aumenta unos 36 mm Hg, cuando la
sangre alcanza el extremo eferente de los capilares y exclusivamente en el capilar glomerular es, alrededor de 32 mm Hg.
Hay dos factores que influyen en la presin coloidosmotica capilar glomerular:
La presin coloidosmotica del plasma arterial.
La fraccin del plasma que se filtra en los capilares glomerulares (fraccin de filtracin)
Si aumenta la presin coloidosmotica del plasma arterial, se eleva la presin coloidosmotica glomerular, la cual a su vez,
disminuye la TFG. Si aumenta la fraccin de filtracin tambin se concentran las protenas plasmticas y se eleva la presin
coloidosmotica glomerular, la fraccin de filtracin puede elevarse aumentando la TFG o reduciendo el flujo plasmtico
renal, es decir una disminucin del flujo plasmtico renal sin ningn cambio inicial de la TFG tendera a aumentar la fraccin
de filtracin, lo cual elevara la presin coloidosmotica capilar glomerular y tendera a disminuir la TFG. Por esta razn, los
cambios del flujo sanguneo renal pueden influir en la TFG independientemente de los cambios que sufra la presin
hidrosttica glomerular. Aunque se mantenga una presin hidrosttica glomerular constante, el aumento del flujo sanguneo
que pasa por el glomrulo tiende a elevar la TFG, y el descenso del flujo sanguneo que atraviesa el glomrulo tiende a
disminuir la TFG.
El aumento de la presion hidrostatica capilar glomerular aumenta la TFG
Se calcula que la presin hidrosttica capilar glomerular es de unos 60 mm Hg en circunstancias normales. Los cambios de
la presin hidrosttica glomerular constituyen el principal medio que permite la regulacin fisiolgica de la TFG. Al aumentar
la presin hidrosttica glomerular, aumenta la TFG, mientras que al disminuir la presin hidrosttica glomerular desciende la
FACULTAD DE CIENCIAS MDICAS-ULEAM
POR MIGUEL BARZALLO
FISIOLOGA HUMANA GUYTON CAPTULO 26
TFG. La presin hidrosttica glomerular se determina mediante tres variables, cada una de las cuales est sometida a
control fisiolgico.
1.
2.
3.
La presin arterial
La resistencia de la arteriola aferente, y
La resistencia de la arteriola eferente.
El aumento de la presin arterial tiende a elevar la presin hidrosttica glomerular y, por tanto a aumentar la TFG. La
constriccin de las arteriolas eferentes aumenta la resistencia al paso de la sangre procedente de los capilares
glomerulares. Esto eleva la presin hidrosttica glomerular, y mientras el aumento de las resistencias en el lado eferente no
reduzca demasiado el flujo sanguneo renal, la TFG aumentara ligeramente, por tanto, si la constriccion de las arteriolas
eferentes es intensa (elevando ms del triple la resistencia), la elevacin de la presin coloidosmotica superara el aumento
de la presin hidrosttica capilar glomerular causada por la constriccion de las arteriolas eferentes. Cuando ocurre esto, la
fuerza neta de filtracin desciende de hecho, produciendo una disminucin de la TFG. As pues, la concentracin de las
arteriolas eferentes tiene un efecto bifsico sobre la TFG. La causa principal del descenso final de la TFG es la siguiente:
conforme a la constriccin de las arterias eferentes se vuelve ms intensa y a medida que aumenta la concentracin con las
protenas plasmticas, hay un aumento rpido, no lineal, de la presin coloidosmotica causado por el efecto Donnan; a
mayor concentracin de protena, ms rpidas es la elevacin de la presin coloidosmotica debido a la interaccin de los
iones unidos a las protenas plasmtica, que tambin ejercen un efecto osmtico, la concentracin de las arteriolas
aferentes disminuye la TFG. Sin embargo, el efecto de la constriccin de la arteria eferente depende de la intensidad de la
misma; si la constriccin eferente es moderada, la TFG aumenta, pero la constriccion eferente intensa tiende a descender
la TFG.
FLUJO SANGUINEO RENAL
En un varn normal de 70 kg de peso, la suma del flujo sanguneo de los dos riones es de uno 1100 mL/min o alrededor
del 22 % del gasto cardiaco. El flujo sanguneo del rin es tan abundante que excede esas necesidades. La finalidad de
ese flujo suplementario es el aporte de plasma suficiente para que se produzcan las grandes tasas de filtracin glomerular
que se necesitan para regular adecuadamente los volmenes de los lquidos y las concentraciones de soluto corporales.
Determinantes del flujo sanguineo renal
El flujo renal est determinado por el gradiente de presin a travs de la vascularizacin renal (la diferencia entre las
presiones hidrostticas de la arteria renal y la vena renal) dividido por la resistencia vascular total renal. La presin en la
arteria renal es igual aproximadamente a la presin arterial sistmica, y la presin en la vena renal es, es promedio, de unos
3 a 4 mm Hg en la mayora de los casos. La mayora de las resistencias vasculares renales residen en tres segmentos
principales:
Las arterias interlobulillares
Las arteriolas aferentes
Las arteriolas eferentes.
La resistencia de estos vasos est controlada por el sistema nervioso simptico, varias hormonas y los mecanismos locales
renales internos de control. El aumento de la resistencia en cualquier segmento vascular de los riones tiende a disminuir el
flujo sanguneo renal, mientras que la disminucin de las resistencias vasculares aumenta el flujo sanguneo renal si las
presiones de la arteria y la vena renal permanecen constantes. Los riones poseen mecanismos eficaces para mantener el
flujo sanguneo renal y la TFG relativamente constantes, en un margen de presin arterial entre 80 y 170 mm Hg, proceso
que se conoce autorregulacin que procede de unos mecanismos intrnsecos.
El FS en los vasos rectos de la medula renal es muy baja comparado con el FS de la corteza renal.
La porcin externa o corteza del rin, recibe la mayor cantidad del flujo sanguneo renal porque el flujo sanguneo de la
medula renal es tan solo de 1 a 2 % de la totalidad del flujo sanguneo renal. El flujo a la medula renal lo suministra una
parte especializada del sistema de los capilares peritubulares llamada vasos rectos. Estos vasos descienden penetrando en
la medula paralelamente a las asas de Henle, y despus de formar un asa o curva, retroceden conjuntamente con las asas
de Henle volviendo a la corteza antes de desembocar en el sistema venoso.
CONTROL FISIOLOGICO DE LA FILTRACION GLOMERULAR Y DEL FLUJO SANGUINEO RENAL
La presin hidrosttica glomerular y la presin coloidosmotica capilar glomerular. Estas variables, a su vez, influidas por el
sistema nervioso simptico, las hormonas y autacoides y otros sistemas de control por retroaccin intrnsecos de los
riones.
La activacion del sistema nervioso simpatico disminuye la TFG
La fuerte activacin de los nervios simpticos renales puede producir constriccion de las arteriolas renales y disminuir el
flujo sanguino renal y la TFG. Los impulsos simpticos moderados o ligeros tienen poca influencia sobre el flujo sanguneo
renal y la TFG. Los nervios simpticos renales parece que son ms importantes para disminuir la TFG cuando existen
trastornos intensos agudos, que actan durante minutos u horas, ante una reaccin de defensa, una isquemia cerebral o
una hemorragia intensa. En personas sanas en reposo tiene poca influencia sobre el flujo sanguneo renal.
CONTROL DE LA CIRCULACION RENAL POR LAS HORMONAS Y LOS AUTACOIDES
Noradrenalina, Adrenalina y Endotelina producen constriccion de los vasos sanguineos renales y disminuye la TFG
Las hormonas que producen constriccion de las arteriolas aferentes y eferentes, produciendo descensos en la TFG y el flujo
sanguneo renal son la noradrenalina y la adrenalina liberadas por la medula suprarrenal. Estas hormonas son paralelas a la
FACULTAD DE CIENCIAS MDICAS-ULEAM
POR MIGUEL BARZALLO
FISIOLOGA HUMANA GUYTON CAPTULO 26
actividad del sistema nervioso simptico; por eso tienen poca influencia sobre la hemodinmica renal salvo en
circunstancias extremas, como ante una intensa hemorragia. Otra sustancia vasoconstrictora, la endotelina, es un pptido
que puede liberarse por las clulas del endotelio vascular lesionado, de los riones o de otros tejidos. La endotelina, puede
favorecer la hemostasia (reduciendo al mnimo la perdida de la sangre). Cuando un vaso sanguneo es seccionado, lo cual
comporta un dao al endotelio y este libera entonces a ese potente vasoconstrictor.
La Angiotensina II constrie las arteriolas eferentes.
La angiotensina II, que es una sustancia dotada de un potente efecto vasoconstrictor, puede considerarse como una
hormona circulante y tambin como un autacoide producido localmente, puesto que se forma en los riones y tambin en la
circulacin general. Como la angiotensina II produce perfectamente la constriccion de las arteriolas eferentes, al elevarse
los niveles de angiotensina II, aumenta la presin hidrosttica glomerular al tiempo que disminuye el flujo sanguneo renal.
En estos casos, los mayores niveles de angiotensina II, al producir constriccion de las arteriolas eferentes, ayudan a evitar
que descienda la presin hidrosttica glomerular y la TFG; aunque, al mismo tiempo, la disminucin del flujo sanguneo
renal producido por la constriccion de las arteriolas eferentes favorece la disminucin del riego sanguneo a travs de los
capilares peritubulares, lo que a su vez aumenta la reabsorcin de sodio y de agua, la constriccion de las arteriolas
eferentes inducida por la angiotensina II produce un aumento de la reabsorcin de sodio y agua, lo que ayudan a
restablecer el volumen sanguneo y la presin arterial. Este efecto de la angiotensina II de ayuda a la autorregulacin de la
TFG.
El Oxido ntrico de origen endotelial disminuye las resistencias vasculares reanales y aumenta la TFG
El oxido ntrico de origen endotelial que es liberado por el endotelio vascular en todo el cuerpo es un autacoide que
disminuye la resistencia vascular renal. La produccin basal de oxido ntrico parece ser importante para evitar una
vasoconstriccin renal excesiva y para favorecer la excrecin de cantidades normales de sodio y agua. En algunos
pacientes hipertensos, el deterioro de la produccin de oxido ntrico puede contribuir a la vasoconstriccin renal y al
incremento de la presin sangunea.
Las prostaglandinas y la bradicinina tienden a aumentar la TFG
Las hormonas autacoides que producen vasodilatacin y aumento del flujo sanguneo renal y de la TFG, comprenden las
prostaglandinas, y la bracinina. Pueden amortiguar los efectos vasoconstrictores renales de los nervios simpticos o de la
angiotensina II especialmente sus efectos de constriccion de las arteriolas eferentes. Al contrarrestar la vasoconstriccin de
las arteriolas eferentes, las prostaglandinas pueden ayudar a vitar la disminucin excesiva de la TFG y del flujo sanguneo
renal.
Autorregulacion de la TFG y del FSR.
Los mecanismos de retroalimentaccin intrnsecos de los riones mantienen normalmente un flujo sanguneo renal y una
TFG relativamente constantes, a pesar de producirse cambios intensos de la presin arterial. Estas constancia de la TFG y
del flujo sanguneo renal se conoce como autorregulacin, es mantener el aporte de oxigeno y otros nutrientes a los tejidos
en cantidades normales y eliminar productos de desecho del metabolismo, a pesar de los cambios que puedan
experimentar la presin arterial. En los riones, flujo sanguneo normal es mucho ms elevado que el se precisa para
cumplir estas funciones. El principio objetivo de la autorregulacin en los riones es mantener una TFG relativamente
constante y permitir un control exacto de la excrecin de agua y de solutos por el rin. El flujo sanguneo renal se
autorregula paralelamente a la TFG, si bien la TFG se autorregula todava con ms eficacia en algunas circunstancias.
Importancia de la utorregulacion de la TFG para evitar cambios extremos de la excrecion renal
Se puede comprender la importancia cuantitativa de la autorregulacin considerando las magnitudes relativas de la filtracin
glomerular, la reabsorcin tubular y la excrecin renal y los cambios en la excrecin renal que se producirn si no existieran
esos mecanismos de autorregulacin. Normalmente, la TFG es de unos 180 litros/da y la reabsorcin tubular es de 178.5
litros/da, quedando 1.5 litros/da del liquido para que se excrete en la orina. Si la reabsorcin tubular permaneciera
constante en 178.5 litros/da la cantidad diaria de orina a eliminar seria de 46.5 litros/da, haciendo que la orina aumentara
ms de 30 veces! Como el volumen plasmtico total es solo de unos 3 litros, el
cambio citado producir rpidamente el agotamiento del volumen sanguneo. Ese
cambio de presin arterial ejerce efectos muchos menores sobre el volumen de la
orina por dos razones:
La autorregulacin renal impide que haya cambios importantes de la TFG
que, de otro modo, se producirn, y
Hay otros mecanismos de adaptacin en los tbulos renales que les
permiten aumentar la tasa de reabsorcin cuando se incrementa la TFG,
un fenmeno que se conoce como equilibrio glomerulotubular.
Los cambios de la presin arterial siguen teniendo efectos significativos sobre la
excrecin renal de agua y sodio; esto se conoce como diuresis por presin o
natriuresis por presin, y es algo esencial para la regulacin de los volmenes de los
lquidos corporales y de la presin arterial.
Papel de la retroaccion tubuloglomerular en la autorregulacion de la TFG
Para llevar a cabo la funcin de autorregulacin, los riones tienen mecanismos de
retroaccin que ponen en relacin los cambios de la concentracin de cloruro sdico
en la mcula densa con el control de las resistencias de las arteriolas renales. Este
mecanismo de retroaccin ayuda a que se mantenga un aporte relativamente
constante de cloruro sdico al tbulo distal y sirve para evitar fluctuaciones espurias
FACULTAD DE CIENCIAS MDICAS-ULEAM
POR MIGUEL BARZALLO
FISIOLOGA HUMANA GUYTON CAPTULO 26
de la excrecin renal que, de otro modo se producirn. Como este mecanismo se dirige especficamente a estabilizar la
TFG, hay casos en que la TFG se autorregula a expensas de que se produzcan cambios del flujo sanguneo renal, como se
ver seguidamente. El mecanismo de retroaccin tubuloglomerular consta de dos elementos que actan conjuntamente
para regular la TFG:
Un mecanismo de retroaccin de la arteriola aferente, y
Un mecanismo de retroaccin de la arteriola eferente.
Ambos dependen de la especial disposicin anatmica del complejo yuxtaglomerular. Est formado por las clulas de la
mcula densa en la porcin inicial del tbulo distal y las clulas yuxtaglomerulares en las paredes de las arteriolas aferente
y eferente. La mcula densa es un grupo especializado de clulas epiteliales en los tbulos distales que guardan estrecho
contacto con las arteriolas aferente y eferente.
Contienen aparatos de Golgi, que son unos orgnulos intracelulares secretores, dirigidos hacia las arteriolas, lo que sugiere
que estas clulas pueden secretar unas sustancias hacia las arteriolas.
La disminucion de cloruro sodico en la mcula densa produce dilatacin de las arteriolas aferentes y aumento de la
liberacion de renina
Las clulas de la macula densa detectan cambios del aporte de volumen al tbulo distal. El descenso de la concentracin
de cloruro sdico pone en marcha, a su vez, una seal desde la mcula densa que produce dos efectos:
Disminuye la resistencia de las arteriolas aferentes, lo cual eleva la presin hidrosttica glomerular y favorece la
vuelta a la normalidad de la TFG, y
Aumenta la liberacin de renina liberada por las clulas yuxtaglomerulares de las arteriolas aferente y eferente,
las cuales son los principales lugares de almacenamiento de la renina.
La renina liberada por estas clulas funciona seguidamente como una enzima que aumenta la formacin de angiotensina I,
que se convierte en angiotensina II. Por ltimo, la angiotensina II produce la constriccion de las arteriolas eferentes, lo que
eleva la presin hidrosttica glomerular y restablece una TFG normal.
Los dos mecanismos de retroalimentacin tubuloglomerular, actuando conjuntamente con el aparato yuxtaglomerular
manda seales para que la autorregulacin de la TFG funcione eficazmente cuando se produce cambios de la presin
arterial. Dentro de los lmites de presin arterial son 75 a 160 mm Hg.
El bloqueo de la formacin de angiotensina II reduce aun ms la TFG durante la hipoperfusion renal.
Accin vasoconstrictora preferente de al angiotensina II sobre las arteriolas eferentes ayuda a prevenir las reducciones
intensas de la presin hidrosttica glomerular y de la TFG cuando las presiones de perfusin renal descienden por debajo
de lo normal. La administracin de frmacos que bloquean la formacin de angiotensina II (inhibidores de la enzima
convertidora de la angiotensina) o que bloquean la accin de la angiotensina II (antagonistas de la angiotensina II) produce
mayores descensos de la TFG de lo habitual cuando la presin arterial renal desciende por debajo de lo normal.
Autorregulacin miogena del flujo sanguineo renal y de la TFG
Un segundo mecanismo que contribuye al mantenimiento de un flujo sanguneo renal y una TFG relativamente constante es
la capacidad de cada uno de los vasos sanguneos para resistir el estiramiento, producido por el aumento de la presin
arterial, fenmeno que se conoce como mecanismo miogeno. El estiramiento de las paredes vasculares permite que
aumente el desplazamiento de los iones calcio desde el lquido extracelular al interior de las clulas, dando lugar a que
estas se contraigan. Esta contraccin impide la distensin excesiva del vaso y, al mismo tiempo, al elevar la resistencia
vascular, ayuda a prevenir los aumentos excesivos del flujo sanguneo renal y de la TFG cuando se eleva la presin arterial.
Aunque el mecanismo miogeno acta probablemente en la mayora de las arteriolas de todo el cuerpo, su importancia en la
autorregulacin del flujo sanguneo renal y de la TFG ha sido puesta en duda por algunos fisilogos, porque este
mecanismo sensible a la presin carece de medios propios para detectar directamente los cambios del flujo sanguneo renal
o de la TFG.
Otros factores que aumentan el FSR y la TFG: Ingreso elevado de proteinas y aumento de la glucosa sanguinea
Se sabe que un elevado ingreso de protenas aumenta el flujo sanguneo renal y la TFG. Siguiendo prolongadamente una
dieta con abundantes protenas, como ocurre con las dietas que contienen gran cantidad de carne, el aumento de la TFG y
del flujo sanguneo renal se debe en parte al crecimiento de los riones. La TFG y el flujo sanguneo renal aumentan de un
20 a 30 % en 1 a 2 horas despus de que una persona tome una comida con carne, con abundante protenas. Una comida
rica en protenas aumenta la liberacin de aminocidos a la sangre, reabsorbindose estos en el tbulo proximal. Como los
aminocidos y el sodio se reabsorben juntos en el tbulo proximal, la mayor reabsorcin de aminocidos estimulara
tambin la reabsorcin de sodio en los tbulos proximales. Al llegar menos sodio a la macula densa, se producira un
descenso de las resistencias de las arteriolas aferentes, mediado por el mecanismo de retroaccin tubuloglomerular. La
menor resistencia de las arteriolas aferentes eleva seguidamente el flujo sanguneo renal y la TFG. Esta mayor TFG permite
que las excreciones de sodio se mantengan a un nivel casi normal, al tiempo que aumenta la excrecin de los productos de
desecho del metabolismo de las protenas, como la urea. Un mecanismo parecido puede explicar tambin el fuerte aumento
del flujo sanguneo renal y de la TFG que se produce con las elevaciones intensas de las concentraciones de glucosa
sangunea en la diabetes mellitus descompensada. Como el objetivo primordial de este mecanismo de retroaccin es
asegurar un aporte constante de cloruro sdico al tbulo distal, donde se producen las ltimas modificaciones en el proceso
de elaboracin de la orina. Por lo tanto, los trastornos que tienden aumentar la reabsorcin de cloruro sdico en los lugares
del tbulo situados por delante de la macula densa tendra tendencia a producir un aumento del flujo sanguneo renal y de
la TFG, lo cual a continuacin, ayudara a que normalizara el aporte de cloruro sdica al tbulo distal, de modo que
pudieran mantenerse unas tasas normales de excrecin de sodio y agua. Una secuencia opuesta de hechos se produce
FACULTAD DE CIENCIAS MDICAS-ULEAM
POR MIGUEL BARZALLO
FISIOLOGA HUMANA GUYTON CAPTULO 26
cuando disminuye la reabsorcin en el tbulo proximal. Por ejemplo, cuando los tbulos proximales estn lesionados, como
sucede como consecuencia de la intoxicacin por metales pesados, como el mercurio, o con dosis elevadas de ciertos
frmacos como las tetraciclinas disminuye la capacidad de los tbulos para reabsorber el cloruro sdico. Llegan al tbulo
distal grandes cantidades de cloruro sdico, las cuales, si no se producen las compensaciones apropiadas, provocaran
una rpida disminucin de volumen de los lquidos corporales. Una de las respuestas compensadoras importantes parece
ser una vasoconstriccin renal mediada por el mecanismo de retroaccin tubuloglomerular que se desencadena en
respuesta a la llegada de mayor cantidad de cloruro sdico a la molcula densa en estas circunstancias. Estos mecanismos
de rotacin para garantizar que el tbulo distal reciba la tasa adecuada de cloruro de sdico, otros solutos del liquido tubular
y un volumen de liquido tubular en proporciones suficientes para que puedan excretarse a la orina unas cantidades
adecuadas de estas sustancias.
FACULTAD DE CIENCIAS MDICAS-ULEAM
POR MIGUEL BARZALLO
FISIOLOGA HUMANA GUYTON CAPTULO 27
FORMACION DE LA ORINA POR LOS RIONES:
PROCESAMIENTO TUBULAR DEL FILTRADO GLOMERULAR
REABSORCION Y SECRECION POR LOS TUBULOS RENALES
Cuando el filtrado glomerular pasa por los tbulos renales, atraviesa
sucesivamente las distintas partes del mismo: el tbulo proximal, el
asa de Henle, el tbulo distal, el tbulo colector y finalmente el
conducto colector, este recorrido, algunas sustancias se reabsorben
selectivamente en los tbulos volviendo a la sangre, mientras que
otras son secretadas desde la sangre a la luz tubular. La orina ya
formada y todas las sustancias que contienen, la suma de los tres
procesos bsicos que se producen en el rin: la filtracin
glomerular, la reabsorcin tubular y la secrecin tubular.
Excrecin urinaria= Filtracin glomerular Reabsorcin tubular + secrecin tubular
La secrecin da cuenta de una cantidad significativa de los iones potasio, los iones hidrogeno y algunas otras sustancias
que aparecen en la orina.
La reabsorcion tubular es selectiva y cuantitativamente importante
Filtracin = Filtracin glomerular x Concentracin en el plasma
Si la concentracin de glucosa en el plasma es de 1 g/litro, la cantidad de glucosa que se filtra cada da es de unos 180
litros/da x 1 G/litro, es decir, 180 g/da. Los procesos de la filtracin glomerular y de la reabsorcin tubular son
cuantitativamente muy grandes en comparacin con la excrecin urinaria de muchas sustancias, esto significa que un
pequeo cambio de filtracin glomerular o de la reabsorcin tubular puede producir, posiblemente, un cambio bastante
importante de la excrecin urinaria. Pero la reabsorcin tubular y la filtracin glomerular estn inmediatamente coordinados,
de modo que no se produce fluctuaciones importantes de la excrecin urinaria. A diferencia de la filtracin glomerular, que
es relativamente no selectiva (todos los solutos del plasma se filtran excepto las protenas o sustancias ligadas a estas), la
reabsorcin tubular es muy selectiva. Algunas sustancias, como la glucosa y los aminocidos, se reabsorben casi
completamente en los tbulos, por lo que su excrecin urinaria es prcticamente nula. Mucho de los iones del plasma, como
el sodio, el cloruro y el bicarbonato, tambin se reabsorben en abundancia, pero su tasa de reabsorcin y de excrecin
urinaria vara mucho dependiendo de las necesidades del organismo, urea y la creatinina se reabsorben mal en los tbulos
y se excretan en cantidades relativamente grandes. Gracias a que los riones controlan la tasa de reabsorcin de diversas
sustancias, estos rganos regulan la excrecin de solutos independientemente unos de otros.
La reabsorcin tubular comprende mecanismo pasivos y activos
Una sustancia se reabsorba, primero debe ser transportada:
A travs de las membranas del epitelio tubular hasta el liquido intersticial renal, y luego
A travs de las membranas de los capilares peritubulares hasta la sangre.
La reabsorcin de agua y de solutos se efecta mediante un transporte que comprende una serie de pasos. La reabsorcin
a travs del epitelio tubular para pasar al lquido intersticial se lleva a cabo mediante un transporte activo o pasivo, el agua y
los solutos pueden transportarse, bien a travs de las propias membranas celulares (va transcelular), bien a travs de los
espacios intermedios que existen entre las clulas contiguas (va paracelular). Luego una vez producida la reabsorcin a
travs de las clulas epiteliales tubulares hasta el lquido intersticial, el agua y los solutos recorren el resto del camino
atravesando las paredes de los capitales peritubulares para pasar a la sangre por ultrafiltracin (paso principal), proceso
que esta mediado por fuerzas hidrostticas y coloidosmoticas. Los capilares peritubulares se comportan de forma muy
parecida a los extremos venosos de la mayora de los dems capilares del organismo porque existe una fuerza de
reabsorcin neta que moviliza al lquido y a los solutos desde el intersticio a la sangre.
Transporte activo
Un soluto puede desplazarse en contra de un gradiente electroqumico,
necesitando la energa que proporciona el metabolismo. El transporte acoplado
directamente a una fuente de energa, como la hidrlisis del trifosfato de
adenosina (ATP) y se llama transporte activo primario. Un buen ejemplo de esto
es la bomba ATPasa de sodio-potasio, que funcionan en la mayora de los
tramos del tbulo renal. El transporte que esta acoplado indirectamente a una
fuente de energa, como el debido a un gradiente inico, se conoce como
transporte activo secundario. La reabsorcin de la glucosa por el tbulo renal es
un ejemplo de transporte activo secundario. El agua siempre se reabsorbe por
un mecanismo fsico pasivo (no activo) que es la osmosis, que significa que la
difusin de agua efecta desde una zona de baja concentracin de solutos
(alta concentracin de agua) a otra de alta concentracin de solutos (baja
concentracin de agua).
FACULTAD DE CIENCIAS MDICAS-ULEAM
POR MIGUEL BARZALLO
FISIOLOGA HUMANA GUYTON CAPTULO 27
Los solutos pueden transportarse a traves de las celulas epiteliales o entre ellas.
Las clulas del tbulo renal, al igual que otras clulas epiteliales, se mantienen juntas, por medio de uniones hermticas
(uniones estrechas). Los espacios intercelulares laterales estn situados por detrs de esas uniones hermticas y separan
las clulas epiteliales del tbulo. Los solutos pueden reabsorberse o secretarse a travs de las clulas por va transcelular
o atravesando las uniones hermticas y los espacios intercelulares, siguiendo la va paracelular. El sodio es una sustancia
que se desplaza por ambas vas, aunque la mayora lo hace a travs de la va transcelular. En algunos segmentos de la
nefrona, especialmente en el tbulo proximal, el agua se reabsorbe tambin a travs de la va paracelular y las sustancias
disueltas en el agua, sobre todo los iones potasio, magnesio y cloruro son transportados junto con el lquido que se
reabsorbe entre las clulas.
El transporte activo primario a travs de la membrana tubular esta ligado a la hidrlisis de ATP.
La importancia especial del transporte activo primario es que puede mover solutos en contra de un gradiente
electroqumico. La energa para este transporte activo procede de la hidrlisis del ATP realizada por la ATPasa unida a la
membrana. Los transportadores activos primarios que conocemos son la ATPasa de sodio-potasio, la ATPasa de
hidrogeno, la ATPasa de hidrogeno-potasio y la ATPasa de calcio. Un buen ejemplo es la reabsorcin de sodio a travs de
la membrana del tbulo proximal. Gracias al funcionamiento de esta bomba de iones, se mantiene una concentracin
intracelular de sodio baja y una concentracin intracelular de potasio alta y
se genera una carga negativa final de unos -70 milivoltios dentro de la
clula. El bombeo de sodio de la clula a travs de la membrana basolateral
de la misma favorece la difusin pasiva de sodio a travs de la membrana
luminal de la clula, desde la luz tubular al interior de la clula por dos
razones:
1.
2.
Existe un gradiente de concentracin que favorece la difusin de
sodio hacia el interior de la clula porque la concentracin
intracelular de sodio es baja y la concentracin de sodio del
lquido tubular es alta.
El potencial negativo intracelular de -70 milivoltios atrae a los
iones sodio positivo desde la luz tubular hacia el interior de la
clula.
La reabsorcin activa de sodio mediante la bomba de sodio-potasio tiene
lugar en la mayor parte de los tbulos. En el tbulo proximal, hay extenso
borde en cepillo en el lado luminal de la membrana. Tambin existen
protenas transportadoras de sodio, que unen los iones sodio en la superficie luminal de la membrana y los liberan dentro de
la clula, proporcionando as una difusin facilitada de sodio a travs de la membrana, al interior de la clula. Estas
protenas transportadoras de sodio son tambin importantes para el transporte activo secundario de otras sustancias, como
la glucosa y los aminocidos, la reabsorcin neta de los iones sodio desde la luz tubular hacia la sangre supone al menos
tres pasos.
El sodio difunde a travs de la membrana luminal (llamada tambin membrana apical) al interior de la clula a
favor de un gradiente electroqumico creado por la ATPasa de sodio-potasio en el lado basolateral de la
membrana.
El sodio atraviesa la membrana basolateral tubular en contra de un gradiente electroqumico gracias a la bomba
ATPasa de sodio-potasio.
El sodio, el agua y otras sustancias se reabsorben del lquido intersticial y pasan a los capilares peritubulares por
ultrafiltracin, un proceso pasivo gobernado por gradientes de presin hidrosttica y coloidosmotica.
Reabsorcion activa secundaria a traves de la membrana tubular.
Hay dos o ms sustancias que se ponen en contacto con una determinada protena de la membrana (una molcula
trasportadora) y ambas atraviesan juntas la membrana. Cuando una sustancia (el sodio, por ejemplo) difunde a favor de su
gradiente electroqumico, la energa liberada se utiliza para que la otra sustancia (la glucosa, por ejemplo) pase en contra
de su gradiente electroqumico (un co-transporte). Por eso, el
transporte activo secundario no precisa energa directamente del ATP
o de otras fuentes do fosfato de alta energa. La fuente directa de
energa es la que se libera por la simultnea difusin facilitada de la
otra sustancia transportada a favor de su propio gradiente
electroqumico. Una vez dentro de la clula, la glucosa y los
aminocidos salen atravesando las membranas basolaterales por
difusin facilitada, impulsada por las elevadas concentraciones de
glucosa y aminocidos que existen en la clula. La reabsorcin de la
glucosa depende de la energa gastada por la bomba activa ATPasa
primaria de sodio-potasio de la membrana basolateral. Gracias a la
actividad de esta bomba, se mantiene un gradiente electroqumico
para la difusin facilitada de sodio, a favor de la corriente hacia el
interior para el transporte simultneo contra gradiente de la glucosa
travs de la membrana luminal. Esta reabsorcin de la glucosa se llama transporte activo secundario por que la glucosa se
reabsorbe con muchas dificultades contra un gradiente qumico, por eso es secundario al transporte primario activo de
sodio. En la reabsorcin de la glucosa, el transporte activo secundario se produce en la membrana luminal, mientras que la
FACULTAD DE CIENCIAS MDICAS-ULEAM
POR MIGUEL BARZALLO
FISIOLOGA HUMANA GUYTON CAPTULO 27
difusin facilitada tiene lugar en la membrana basolateral, y la captacin pasiva debida al paso masivo o principal se
produce en los capilares peritubulares.
Secrecin activa secundaria en los tubulos
Hay algunas sustancias que son secretadas por los tbulos mediante un
transporte activo secundario, esto supone un contratransporte, la energa liberada
por el desplazamiento facilitado de una de las sustancia permite el paso contra
gradiente de una segunda sustancia en direccin opuesta. La entrada de sodio en
la clula esta acoplada con la expulsin de hidrogeno por la clula mediante el
contratransporte de sodio-hidrogeno. Este transporte esta mediado por una
protena especifica que se encuentra en el borde en cepillo de la membrana
luminal.
Pinocitos, un mecanismo de trasporte activo para
reabsorcion de proteinas
Las del tbulo proximal, reabsorben molculas
grandes, como las protenas, mediante pinocitosis, la
protena se une al borde en cepillo de la membrana
luminal. Una vez dentro de la clula, la protena es
digerida a sus aminocidos integrantes, los cuales se
reabsorben a travs de la membrana basolateral y
pasan al lquido intersticial. Como la pinocitosis requiere energa, se considera una forma de
transporte activo.
TRANSPORTE MAXIMO DE LAS SUSTANCIAS QUE SE REABSORBEN ACTIVAMENTE.
Las sustancias que se reabsorben o se secretan activamente hay un lmite de la tasa de soluto
que puede transportarse y que se denomina el transporte mximo. Este lmite se debe a la
saturacin del sistema de transporte especfico cuando la cantidad de soluto suministrada al tbulo (conocida como carga
tubular) supera la capacidad de las protenas transportadoras y de las enzimas especificas que intervienen en el proceso de
transporte. Normalmente, no hay glucosa detectable en la orina, porque prcticamente toda la glucosa filtrada se reabsorbe
en el tbulo proximal. Pero cuando la carga filtrada supera a la capacidad de los tbulos para reabsorber la glucosa, hay
excrecin urinaria de glucosa. En los adultos, el transporte mximo de la glucosa es, en promedio, de unos 320 mg/min,
mientras que la carga filtrada de glucosa es solo de 125 mg/min que cuando la carga tubular esta en sus lmites normales
de 125 mg/min, ni hay perdida de glucosa por la orina. Sin embrago, cuando la carga tubular asciende por encima de 220
mg/min, empieza aparecer una pequea cantidad de glucosa en la orina, un punto que ha sido denominado como umbral de
la glucosa. Obsrvese que esta aparicin de glucosa en la orina (al nivel del umbral) se produce antes de llegar al
transporte mximo. Una razn de la diferencia entre el umbral y el transporte mximo es que no todas las nefronas tienen el
mismo transporte mximo para la glucosa, y algunas nefronas excretan glucosa antes de que otras hayan alcanzado su
transporte mximo, el transporte mximo en los riones se alcanza cuando todas las nefronas han llegado a su mxima
capacidad de reabsorcin de la glucosa. En la diabetes mellitus descompensada (incontrolada), la glucosa plasmtica
puede elevarse a concentraciones altas que producen una carga de glucosa filtrada que sobre pasa el transporte mximo y
da lugar a la excrecin de glucosa en la orina.
Sustancias que se transportan pero que no muestran un transporte mximo
Las sustancias que reabsorben pasivamente no muestran transporte mximo porque su tasa de transporte est
determinada por otros factores, como son:
El gradiente electroqumico para la difusin de las sustancias a travs de la membrana
La permeabilidad de la membrana para la sustancia, y
El tiempo que el lquido que contienen esa sustancia permanece dentro del tbulo.
El transporte de este tipo se conoce como transporte por gradiente en funcin del tiempo porque su velocidad depende del
gradiente electroqumico y del tiempo de permanencia de la sustancia en el tbulo, que a su vez, depende de la tasa del
flujo tubular. Algunas sustancias transportadas activamente tambin tienen las caractersticas de un transporte de
gradiente-tiempo. Por ejemplo de ello es la absorcin de sodio en el tbulo proximal. La principal razn de que el transporte
de sodio en el tbulo proximal no muestre un trasporte mximo es que hay otros factores que limitan la tasa de reabsorcin
aparte de la tasa mxima de transporte activo. Una cantidad significativa de sodio que se transporta fuera de las clulas se
escapa retrgradamente y entra en la luz tubular a travs de las uniones hermticas epiteliales. La tasa de esta difusin
retrograda depende de varios factores como:
a) La permeabilidad de las uniones hermticas, y
b) Las fuerzas fsicas intersticiales, que determinan la parte ms voluminosa del flujo que se reabsorbe desde el
lquido intersticial al interior de los capilares peritubulares.
El transporte del sodio en los tbulos proximales responde principalmente a los principios del transporte por gradientes en
funcin del tiempo, ms que a las caractersticas del transporte tubular mximo. Esto significa que cuanto mayor es la
concentracin de sodio en los tbulos proximales, mayor es su tasa de reabsorcin, cuanto mas lenta es la tasa del lquido
tubular, mayor es el porcentaje de sodio que depende reabsorberse de los tbulos proximales. En las partes ms distales
de la nefrona, las clulas epiteliales, estos segmentos, la reabsorcin de sodio muestra un transporte mximo, este
transporte mximo puede aumentar en respuesta a determinadas hormonas, como la aldosterona.
FACULTAD DE CIENCIAS MDICAS-ULEAM
POR MIGUEL BARZALLO
FISIOLOGA HUMANA GUYTON CAPTULO 27
La reabsorcin pasiva de agua por smosis esta acoplada principalmente a la reabsorcion de sodio
Cuando los solutos se transportan fuera del tbulo sea por mecanismos de transporte activo primarios o secundarios, sus
concentraciones tienen tendencias a descender dentro del liquido y aumentar en el intersticio renal. Esto da lugar a una
diferencia de concentraciones que producen smosis del agua en la misma direccin en que se transportan los solutos, a
saber la luz tubular al intersticio renal. Una gran parte del flujo osmtico de agua se produce a travs de las llamadas
uniones hermticas entre las clulas epiteliales, as como a travs de las propias clulas, las uniones hermticas no son tan
hermticas como da a entender su nombre, y permiten una difusin significativa de agua y de pequeos iones. Esto es
especialmente as en los tbulos proximales, cuya permeabilidad al agua es elevada, y algo menor, aunque significativa, a
la mayora de los iones, como el sodio, el cloruro, el potasio, calcio y magnesio. Conforme el agua se desplaza y atraves de
las uniones hermticas por osmosis, tambin puede haber desplazamiento de algunos solutos, proceso que se conoce
como arrastre del disolvente. Y como la reabsorcin de agua, los solutos orgnicos y los iones esta acoplada a la
reabsorcin de sodio, los cambios de la reabsorcin de sodio influyen significativamente en la reabsorcin de agua y de
otros muchos solutos. En las partes ms distales de la nefrona, que comienzan en el asa de Henle y se extienden hasta el
tbulo colector, las uniones hermticas se vuelven mucho menos permeables al agua y los solutos, y las clulas epiteliales
tienen tambin un rea superficial de la membrana muy disminuida. Debido a ello, el agua no puede desplazarse fcilmente
por smosis a travs de la membrana tubular. Sin embargo, la hormona antidiuretetica (ADH) aumenta mucho la
permeabilidad al agua en el tbulo distal y el tbulo colector, el desplazamiento del agua a travs del epitelio tubular solo
puede producirse si la membrana es permeable al agua, independientemente de la amplitud del gradiente osmtico. En el
tbulo proximal, la permeabilidad al agua es siempre alta y el agua se reabsorbe con la misma rapidez que los solutos. En
la porcin ascendente del asa de Henle, la permeabilidad al agua es siempre baja, de modo que no se reabsorbe casi nada
de agua, a pesar del elevado gradiente osmtico que existe. La permeabilidad al agua en las ltimas porciones de los
tbulos (tbulos distal, tbulos colector y conductos colectores) puede ser alta o baja, dependiendo de la presencia o
ausencia de ADH.
Reabsorcion de cloruro, urea y otros solutos por difusion pasiva
Cuando el sodio se reabsorbe a travs de las clulas epiteliales tubular, los iones
negativas como el cloruro son transportados junto con el sodio debido a los
potenciales elctricos. El transporte de los iones sodio cargados positivamente
fuera de la luz, deja al interior de la luz cargada negativamente con respecto al
lquido intersticial. Esto hace que los iones de cloruro difundan pasivamente a
travs de la va paracelular. Tambin se produce reabsorcin de los iones cloruro
debido a un gradiente de concentracin de cloruro que se produce cuando el agua
se reabsorbe en el tbulo por smosis, con lo cual se concentran los iones cloruro
en la luz tubular la reabsorcin activa de sodio est ntimamente acoplada a la
reabsorcin pasiva del cloruro por medio de un potencial elctrico y aun gradiente
de concentracin de cloruro. Los iones de cloruro tambin pueden reabsorberse por
transporte activo secundario. El ms importante de los proceso de transporte activo
secundario que intervienen en la reabsorcin de cloruro es el co-transporte del
cloruro con el sodio a travs de la membrana luminal. La rea tambin se
reabsorbe pasivamente del tbulo, pero en una cuanta mucho menor que los iones
cloruro. Conforme el agua de los tbulos se reabsorbe, aumenta la concentracin
de la rea en la luz tubular. Pero la rea no difunde con la facilidad como lo que lo hace el agua, la mitad aproximadamente
de la rea que se filtra en los capilares glomerulares se reabsorbe pasivamente en los tbulos especialmente en el conducto
colector de la mdula interna, por unos trasportadores especficos de la rea y el resto de la urea se elimina con la orina,
dejando que los riones excreten grandes cantidades de este producto de desecho del metabolismo, creatinina no atraviesa
la membrana tubular. Por lo tanto, la reabsorcin de la creatinina que filtra es casi nula, as que prcticamente toda la
creatinina filtrada en los glomrulos se excreta por la orina.
REABSORCION TUBULAR PROXIMAL
Los tbulos proximales tienen gran capacidad para la reabsorcin
activa y pasiva
Un 65 % de la carga de sodio y de agua filtrada y un porcentaje algo
menor del cloruro filtrado se reabsorben en el tbulo proximal antes de
que el filtrado llegue al asa de Henle. La gran capacidad del tbulo
proximal para la reabsorcin se debe a sus caractersticas especiales,
las clulas epiteliales del tbulo proximal gozan de intensa actividad
metablica y tienen gran nmero de mitocondrias que sostienen sus
potentes procesos de transporte activo. Las clulas tubulares
proximales tienen un extenso borde en cepillo en el lado de la luz de la
membrana, as como un amplio laberinto de conductos intracelulares y
basales, elementos todos que proporcionan una extensa rea
superficial a la membrana de los lados luminal y basolateral del epitelio
que permite el transporte rpido de los iones sodio y de otras
sustancias. La amplia superficie del borde en cepillo de la membrana
de la clula epitelial esta tambin dotada de molcula proteicas
transportadoras, que transportan gran parte de los iones sodio a travs de la membrana luminal, ligado por el mecanismo
de co-transporte al paso de numerosos nutrientes orgnicos, como los aminocidos y glucosa. El resto de sodio se
transporta desde la luz tubular al interior de la clula mediante mecanismos de contratransporte, que reabsorben el sodio al
tiempo que secretan otras sustancias al interior de la luz tubular, especialmente iones hidrogeno.
FACULTAD DE CIENCIAS MDICAS-ULEAM
POR MIGUEL BARZALLO
FISIOLOGA HUMANA GUYTON CAPTULO 27
En la primera mitad del tbulo proximal, el sodio se reabsorbe por co-transporte junto con la glucosa, los aminocidos y
otros solutos. Pero en la segunda mitad del tbulo proximal queda poca glucosa y aminocidos para reabsorberse, y por
eso aqu el sodio se reabsorbe sobre todo junto a los iones cloruro. La segunda mitad del tbulo proximal tiene una
concentracin relativamente alta de cloruro (alrededor de 140 mEq/L) en comparacin con la primera parte del tbulo
proximal (uno 105 mEq/L) porque cuando se reabsorbe el sodio, lo hace perfectamente con la glucosa, el bicarbonato y los
iones orgnicos en el tbulo proximal, dejando tras de s una solucin que contiene una concentracin mayor de cloruro. En
la segunda mitad del tbulo proximal, la mayor concentracin de cloruro favorece la difusin de este ion desde la luz del
tbulo a travs las uniones intercelulares, y al lquido intersticial renal.
Concentraciones de los solutos a lo largo del tbulo proximal
Aunque la cantidad de sodio que se encuentra en el lquido tubular disminuye mucho a lo largo del tbulo proximal, la
concentracin del sodio (y la osmoralidad total), sigue siendo bastante constante porque la permeabilidad al agua de los
tbulos proximales es tan grande que la reabsorcin de sodio. Algunos solutos orgnicos, como la glucosa, los aminocidos
y el bicarbonato se reabsorben con mucha mayor avidez que el agua, as que sus concentraciones disminuyen
considerablemente a lo largo del tbulo proximal. La creatinina, aumenta su concentracin a lo largo del tbulo proximal. La
concentracin total de solutos reflejada por la osmoralidad, sigue siendo prcticamente la misma a todo lo largo del tbulo
proximal debido a la permeabilidad extraordinariamente alta de esa parte de la nefrona al agua.
Secrecin de cidos y bases orgnicas por el tbulo proximal
Es un sitio importante para la secrecin de cidos y bases orgnicas, tales como las sales biliares, oxalato, urato y
catecolaminas. La secrecin de estas sustancias en el tbulo proximal mas la filtracin al tbulo proximal por los capilares
glomerulares y la ausencia casi total de reabsorcin por los tbulos, contribuyen, todos ellos conjuntamente, a su rpida
excrecin por la orina. En el caso de algunos frmacos, como la penicilina y los salicilatos, el aclara miento rpido por los
riones crea un problema en lo que se refiere al mantenimiento de una
concentracin teraputica eficaz del frmaco, el cido para-aminohiprico
(PAH) y eliminarlo por la orina. Por esta razn, la tasa de aclaramiento del
PAH se puede utilizar para estimar el flujo plasmtico renal.
TRANSPORTE DE AGUA Y SOLUTOS EN EL ASA DE HENLE
Est formada por tres porciones la porcin descendente delgada, la porcin
ascendente delgada y la porcin ascendente gruesa. La porcin
descendente delgada y la porcin ascendente delgada, tiene membranas
epiteliales finas sin bordes en cepillo, con pocas mitocondrias y grados
mnimos de actividad metablica. La parte descendente de la porcin
delgada es muy permeable al agua y moderadamente permeable a la
mayora de los solutos, incluidos la urea y el sodio, permite la difusin
simple de sustancias a travs de sus paredes, alrededor del 20 % del agua
filtrada se reabsorbe en el asa Henle, y casi toda esa reabsorcin tiene
lugar en la rama descendente delgada, porque la rama ascendente, en sus
dos porciones: la delgada y la gruesa, es prcticamente impermeable al
agua, una caracterstica que es importante para la concentracin de la
orina. La porcin gruesa del asa de Henle que comienza hacia la mitad de
la rama ascendente, tienen gruesas clulas epiteliales dotadas de gran
actividad metablica y capaces de reabsorber activamente sodio, cloruro y
potasio, alrededor del 25 % de las cargas filtradas de sodio, cloruro y
potasio se reabsorben en el asa de Henle, su mayor parte en la porcin
ascendente gruesa del asa. Tambin se reabsorben en la porcin
ascendente del asa de Henle cantidades considerables de otros iones,
como calcio, bicarbonato y magnesio. La rama descendente delgada no
reabsorbe cantidades significativas de ninguno de estos solutos. Un elemento importante de la reabsorcin de solutos en la
rama ascendente gruesa es la bomba ATPasa de sodio-potasio que funciona
en las membranas basolaterales de las clulas epiteliales. Al igual que en el
tbulo proximal, la reabsorcin de otros solutos en la porcin gruesa del asa
de Henle ascendente est ntimamente relacionada con la capacidad
reabsorbida de la bomba ATPasa de sodio-potasio, la cual mantiene una baja
concentracin intracelular de sodio. Proporciona una gradiente favorable para
que el sodio se desplace desde el lquido tubular hasta el interior de la clula.
En la porcin ascendente gruesa del asas de Henle, el desplazamiento del
sodio a travs de la membrana luminal esta mediado principalmente por un
cotransportador de 1 sodio, 2 cloruro y 1 potasio. Tambin existe una
importante reabsorcin paracelular de cationes, como el Mg++, Ca++, Na+, y
K+, en la porcin gruesa de la rama ascendente, debida a ligera positividad de
carga de la luz tubular respecto al lquido intersticial. Aunque el co-transporte
de 1-sodio, 2-cloruro, 1-potasio mueve una cantidad igual de cationes y
aniones al interior de la clula, existe una ligera retrodifusion de iones, potasio
hacia la luz generando una carga positiva de unos +8 milivoltios en la luz
tubular.
La rama ascendente gruesa del asa de Henle es el lugar de accin de los
poderosos diurticos de <<asa>> furosemida, cido etacrnico y bumetanida,
los cuales inhiben la accin del co-transportador 2 cloro-potasio.
FACULTAD DE CIENCIAS MDICAS-ULEAM
POR MIGUEL BARZALLO
FISIOLOGA HUMANA GUYTON CAPTULO 27
Esta carga positiva fuerza la difusin de cationes como Mg++ y Ca++ desde la luz tubular hacia el liquido intersticial, a travs
del espacio paracelular. La rama ascendente gruesa tambin tienen un mecanismo de contra-transporte de sodio-hidrogeno
en la membrana del lado luminal de la clula, el cual hace mediador en la reabsorcin de sodio y en la secrecin de
hidrogeno por esta porcin del tbulo. Como la parte gruesa de la porcin ascendente del asa de Henle es prcticamente
impermeable al agua, la mayor parte del agua que queda libre en esta parte permanece en el tbulo, el liquido tubular de la
rama ascendente se vuelve muy diluido conforme avanza hacia el tbulo distal, un hecho que es muy importante, pues
permite que los riones diluyan o concentren la orina en diferentes
condiciones.
TUBULO DISTAL
La porcin gruesa de la rama ascendente del asa de Henle desemboca
en el tbulo distal. El extremo inicial del tbulo distal forma parte del
complejo yuxtaglomerular que proporciona una regulacin por
retroaccin de la TFG y del flujo sanguneo a esa misma nefrona, y el
ultimo extremo del tbulo distal es muy contorneada que comparte
caracterstica con el segmento grueso de la rama ascendente del asa
de henle que reabsorbe con avidez la mayora de los iones, como el
sodio, potasio y cloruro, pero es prcticamente impermeable al agua y
la urea. Se denomina porcin diluyente porque tambin diluye el lquido
tubular. Alrededor del 5% de la carga filtrada de cloruro de sodio se
reabsorbe en la primera parte del tbulo distal. El co-transportador
sodio-cloro mueve el cloruro de sodio desde la luz tubular hasta el
interior de la clula y la bomba ATPasa sodio-potasio transporta el
sodio fuera de la clula a travs de la membrana basolateral. Los
diurticos tiacdicos, para los trastornos como la hipertensin y la
insuficiencia cardaca, inhiben el co-transportador sodio-cloro.
Ultima porcion del tubulo distal y TUBULO COLECTOR CORTICAL
La segunda mitad del tbulo distal y el tubo colector cortical que le
siguen poseen caractersticas funcionales parecidas, estn formados
por dos clases distintas de clulas, las clulas principales y las clulas
intercaladas. Las clulas principales reabsorben sodio y agua de la luz
y secretan iones potasio al interior de la luz. Las clulas intercaladas
reabsorben iones potasio y
secretan iones hidrogeno al
interior de la luz tubular.
Las clulas principales reabsorben sodio y secretan potasio
La reabsorcin de sodio y la secrecin de potasio por las clulas principales
dependen de la actividad de una bomba ATPasa de sodio-potasio que se
encuentra en la membrana basolateral de cada clula. Esta bomba mantiene una
concentracin baja de sodio dentro de la clula y, por tanto, favorece la difusin de
sodio al interior de la clula por medio de conductos especiales. La secrecin de
potasio por estas clulas, desde la sangre a la luz tubular comprende dos pasos:
El potasio penetra en las clulas gracias a la bomba ATPasa de sodiopotasio, que mantiene una elevada concentracin intracelular de potasio
y luego
Una vez all, el potasio de la clula difunde a favor de su gradiente de
concentracin a travs de la membrana luminal y pasa al lquido tubular.
Las clulas principales son los primeros lugares de accin de los diurticos
ahorradores de potasio, como espironolactona, eplerenona, amilorida y triamtereno.
Los antagonistas de la aldosterona compiten con sus receptores por tanto inhiben los efectos estimulantes de esta
hormona. Los bloqueantes de los canales del sodio inhiben la entrada de sodio en sus respectivos canales en la clula.
Estos mecanismos reducen a su vez el transporte de potasio al
interior de las clulas y disminuye finalmente la secrecin de potasio
al lquido tubular.
La clulas intercaladas secretan intensamente iones hidrgeno
y reabsorben iones bicarbonato y potacio
La secrecin de iones hidrogeno por las clulas intercaladas esta
medida por el mecanismo de transporte de la ATPasa de hidrogeno.
El hidrogeno se produce en estas clulas por la accin de la
anhidrasa carbnica sobre el dixido de carbono y el agua, que
forma acido carbnico y este se diciosa seguidamente en iones
hidrogeno y bicarbonato. Los iones hidrgenos son secretados
posteriormente al interior de la luz tubular y por cada ion hidrogeno
secretado queda disponible y un ion bicarbonato para reabsorcin a
travs de la membrana basolateral. Las clulas intercaladas pueden
reabsorber tambin iones potasio.
FACULTAD DE CIENCIAS MDICAS-ULEAM
POR MIGUEL BARZALLO
FISIOLOGA HUMANA GUYTON CAPTULO 27
Las caractersticas funcionales de la ltima porcin del tbulo, colector cortical.
1)
2)
3)
4)
Las membranas tubulares de ambas porciones son impermeables casi por completo a la rea, al igual que la
porcin diluyente de la primera porcin del tbulo distal; de ah que casi toda la urea que entra en estas porciones
pase a lo largo del conducto colector para excretarse por la orina aunque alguna parte de la rea se reabsorbe en
los conductos colectores medulares.
Tanto en la ltima porcin del tbulo distal como las porciones corticales de lis tbulos colectores reabsorben
iones sodio y la tasa de reabsorcin est controlada por hormonas especialmente por la aldosterona. Al mismo
tiempo estas porciones secretan iones potasio procedente de la sangre de los capilares peritubulares y los vierten
a la luz tubular, proceso que tambin est controlado por la aldosterona y por otros factores, como la
concentracin de iones potasio en los lquidos corporales.
Las clulas intercaladas de estas porciones de la nefrona secretan intensamente iones hidrogeno gracias al
mecanismo activo de la ATPasa de hidrogeno. Este proceso es distinto a la de la secrecin activa secundaria de
los iones hidrogeno realizada por el tbulo proximal, pues es capaz de secretar iones hidrogeno contra un
elevado gradiente de concentracin, nada menos que de 1000 a 1. Las clulas intercaladas juegan un papel
esencial en la regulacin acidobasica de los lquidos corporales.
La permeabilidad al agua de la ltima porcin del tbulo distal y del conducto colector cortical est controlada por
la concentracin de la ADH, llamada tambin vasopresina. Cuando existen niveles elevados de ADH, estas
porciones del tbulo son permeables al gua, pero si no hay ADH son prcticamente impermeables al agua.
Importante para el control del grado de dilucin o concentracin de la orina.
CONDUCTO COLECTOR MEDULAR
Aunque los conductos colectores medulares absorben menos de 10 % del
agua y del sodio filtrados constituyen el ltimo sitio para la elaboracin de la
orina y por tanto, este punto desempea un papel sumamente importante
para determinar la excrecin urinaria final de agua y solutos. Las clulas
epiteliales de los conductos colectores son de formas casi cubicas con
superficies lisas y pocas mitocondrias.
La permeabilidad del conducto colector medular para el agua est
controlada por la concentracin de la ADH. Cuando la ADH es alta, el agua
se reabsorbe vidamente al intersticio medular con lo que se reduce el
volumen de la orina y se concentran en la mayora de los solutos de la
orina.
A diferencia del tbulo colector cortical, el conducto colector
medular es permeable a la urea. Por tanto, parte de la urea tubular se
reabsorbe y pasa al intersticio medular, contribuyendo la capacidad global
de los riones para formar una orina concentrada.
El conducto colector medular es capaz de secretar iones hidrogeno contra un elevado gradiente de concentracin,
como ocurre tambin en el tbulo colector cortical. El conducto colector medular tiene tambin un papel esencial
en la regulacin del equilibrio acidobsico.
Resumen de las concentraciones de los distintos solutos en las diferentes porciones tubulares.
El hecho de que un soluto llegue o no a concentrarse en el liquido tubular depende del grado relativo de reabsorcin de ese
soluto con respecto a la reabsorcin del agua. Si se reabsorbe un porcentaje de agua mayor, la sustancia queda ms
concentrada. Si se reabsorbe un porcentaje mayor de soluto, esa sustancia queda ms diluida. Cuando el filtrado se
desplaza a lo largo del sistema tubular, la concentracin se eleva progresivamente a ms de 1, si se reabsorbe mas solutos
que agua. Adems si una sustancia es secretada por el epitelio tubular al interior del tbulo, esto har que aumente tambin
su concentracin en el lquido tubular. La creatinina y la rea, se concentran mucho en la orina. En general, estas
sustancias no son necesarias para el cuerpo, y los riones se han acomodado a reabsorberlas solo ligeramente o nada en
absoluto, o inclusivo, la secretan al interior de los tbulos, las sustancias como la glucosa y los aminocidos, se reabsorben
intensamente; todas ellas son sustancias que el cuerpo debe conservar y casi nada de ellas se pierden por la orina.
REGULACION DE LA REABSORCION TUBULAR.
Equilibrio glomerulotubular: capacidad de los tbulos para aumentar la tasa de reabsorcion en respuesta del
aumento de la carga tubular.
Mecanismo ms elemental de control de la reabsorcin tubular es la capacidad intrnseca de los tbulos de aumentar la
reabsorcin en respuesta a una carga tubular excesiva. Este fenmeno se conoce como equilibrio glomerulotubular. El
equilibrio glomerulotubular indica que la tasa total de la reabsorcin aumenta conforme lo hace la carga del filtrado, aunque
permanezca relativamente constante en el porcentaje de la TFG reabsorbida en el tbulo proximal en el 65 %
aproximadamente. Es evidente que los mecanismos del equilibrio glomerulotubular pueden actuar independientemente de
las hormonas y demostrarse en riones completamente aislados e incluso en segmentos del tbulo proximal
completamente aislados. La importancia del equilibrio glomerulotubular ayuda a impedir que porciones de los segmentos
tubulares distales sufran un sobre carga cuando aumenta la TFG. El equilibrio glomerulotubular acta como una segunda
lnea de defensa amortiguando los efectos de los cambios espontneos de la TFG de la eliminacin urinaria. Actuando
conjuntamente los mecanismos de autorregulacin y el equilibro glomerulotubular impiden que se produzcan grandes
cambios de la cantidad de liquido que llega a los tbulos distales cuando la presin arterial experimenta variaciones, o
cuando hay otros trastornos que, de otro modo, produciran estragos en el mantenimiento de los homeostasis del sodio y
del volumen.
FACULTAD DE CIENCIAS MDICAS-ULEAM
POR MIGUEL BARZALLO
FISIOLOGA HUMANA GUYTON CAPTULO 27
Capilares peritubulares y fuerzas fsicas del lquido intersticial renal
Las fuerzas hidrostticas y coloidosmoticas son las que gobiernan la tasa de reabsorcin que se produce atraves de los
capilares peritubulares. Los cambios de la reabsorcin capilar peritubular pueden, a su vez, influir en la presin hidrosttica
y coloidosmotica del intersticio renal, y en el ltimo trmino, en reabsorcin de agua y solutos desde los tbulos renales.
Valores normales de las fuerzas fsicas y tasa de reabsorcin.
Cuando el filtrado glomerular pasa a travs de los tbulos renales, normalmente se reabsorbe ms de 99 % de agua y la
mayora de los solutos. Los lquidos y los electrolitos se reabsorben desde los tbulos a los intersticios renal y de aqu, a los
capilares peritubulares. La tasa normal de reabsorcin capilar peritubular es de unos 124 mL/min. La reabsorcin a travs
de los capilares peritubulares se calcula asi:
Reabsorcin = Kf x Fuerza de reabsorcin neta.
La fuerza de reabsorcin neta es la suma de las fuerzas hidrostticas y coloidosmotica que favorecen o se oponen a la
reabsorcin a travs de los capilares peritubulares. Estas fuerzas son:
1) La presin hidrosttica que existe en los capilares peritubulares que se oponen a la reabsorcin;
2) La presin hidrosttica que existe en el intersticio renal que favorece la reabsorcin
3) La presin coloidosmtica de las protenas plasmticas de los capilares peritubulares que favorecen la
reabsorcin.
4) La presin coloidosmotica de las protenas del intersticio renal que se oponen a la reabsorcin.
Como la presin capilar peritubular es normalmente de unos 13 mm Hg y la presin hidrosttica del liquido intersticial renal
es por trmino medio, de 6 mm Hg, hay un gradiente positivo de presin hidrosttica entre los capilares peritubulares y el
liquido intersticial de unos 7 mm Hg que se oponen a la reabsorcin del liquido. La presin coloidosmotica del plasma que
favorece la reabsorcin es de unos 32 mm Hg y la presin coloidosmotica del intersticio, que se opone a la reabsorcin es
de 15 mm Hg dando lugar a una fuerza coloidosmotica final de 17 mm
Hg que favorece a la reabsorcin. Por tanto, restando la fuerzas
hidrostticas netas que se oponen a la reabsorcin (7mm Hg) con las
fuerzas coloidosmoticas netas que favorecen la reabsorcin (17 mm Hg)
se obtiene una fuerza de reabsorcin de unos 10 mm Hg. El otro factor
que contribuye aumentar la reabsorcin del liquido en los capilares
peritubulares es un coeficiente de filtracin (kf) grande debido a la alta
conductividad hidrulica y la gran rea superficial de los capilares que
normalmente es de 12,4ml/min/mm Hg.
Regulacin de las fuerzas fsicas que actan en los capilares
peritubulares
Los dos factores determinantes de la reabsorcin de los capilares
peritubulares que estn directamente influidos por los cambios
hemodinmicas renales son la presin hidrosttica y la presin
coloidosmtica de los capilares peritubulares. La presin hidrosttica de
los capilares peritubulares est influida por la presin arterial y la resistencia de las arteriolas aferente y eferente.
Los aumentos en la presin arterial tienden a elevar la presin hidrosttica de los capilares peritubulares y a
disminuir la tasa de reabsorcin.
El aumento de la resistencia de las arteriolas aferentes o de las eferentes disminuye la presin hidrosttica de los
capilares peritubulares y tienden a incrementar la tasa de reabsorcin.
Aunque la constriccion de las arteriolas aferentes aumenta la presin hidrosttica de los capilares glomerulares. La
reabsorcin de los capilares peritubulares es la presin coloidosmtica del plasma que circula por esos capilares; al
aumentar la presin coloidosmtica, se incrementa la reabsorcin capilar peritubular. La presin coloidosmtica de los
capilares peritubulares est determinada por:
La presin coloidosmtica del plasma en la circulacin general (sistmica); al aumentar la concentracin de la
protena plasmticas de la sangre de todo el organismo, hay tendencia a la elevacin de la presin coloidosmotica
en los capilares peritubulares, lo que aumenta la reabsorcin.
La fraccin de filtracin; a mayor fraccin de filtracin, es la cantidad de plasma que se filtra a travs del
glomrulo y, por consiguiente mas se concentran las protenas plasmticas que quedan por detrs.
Como la fraccin de la filtracin se define como el cociente TFG/flujo plasmtico renal, la fraccin de filtracin puede
elevarse como consecuencia de aumento de la TFG o una disminucin del flujo plasmtico renal, algunos agentes
vasoconstrictores renales, como la angiotensina II, reduce el flujo plasmtico renal y aumenta la fraccin de filtracin, y al
aumentar el kf aumenta la reabsorcin, mientras que los descensos de k f disminuyen la reabsorcin en los capilares
peritubulares.
Presiones hidrostticas y coloidosmtica del intersticio renal
Las variaciones de las fuerzas fsicas que actan sobre los capilares peritubulares influyen en la reabsorcin tubular
modificando la fuerza fsica que actan en el intersticio renal que rodea a los tbulos. Un descenso de la fuerza de
reabsorcin a travs de la membrana de los capilares peritubulares debido, bien a un aumento de la presin hidrosttica
capilar peritubular, bien a una disminucin de la presin coloidosmotica capilar peritubular, disminuye la captacin de
lquidos y solutos desde el intersticio a los capilares peritubulares. Esto, a su vez, eleva la presin hidrosttica del lquido
intersticial y disminuye la presin coloidosmotica del lquido intersticial debido a la dilucin de las protenas en el intersticio
renal. Estos cambios disminuyen seguidamente la reabsorcin neta de lquidos desde los tbulos renales al intersticio,
especialmente los tbulos proximal. Una vez que los solutos han entrado en los conductos intracelulares o en el intersticio
renal, por trasporte activo o por difusin pasiva, el agua es extrada de la luz tubular y pasa al intersticio por osmosis. Una
FACULTAD DE CIENCIAS MDICAS-ULEAM
POR MIGUEL BARZALLO
FISIOLOGA HUMANA GUYTON CAPTULO 27
vez que el agua y los solutos se encuentran en los espacios intersticiales, pueden pasar a los capilares peritubulares, o
pueden difundir retrgradamente, atravesando las uniones epiteliales, hacia la luz
tubular. Las llamadas uniones hermticas que existen entre las clulas epiteliales
del tbulo proximal son en realidad, bastante permeable, por lo que hay
cantidades considerables de sodio que pueden difundir en ambas direcciones a
travs de esas uniones.
Cuando disminuye la reabsorcin en los capilares peritubulares, aparecen en un
momento de la presin hidrosttica de lquido intersticial y una tendencia a que
una mayor cantidad de solutos y de agua difundan retrgradamente hacia la luz
tubular, lo que reduce la tasa de reabsorcin neta. Lo contrario ocurre cuando hay
un aumento de la reabsorcin en los capilares peritubulares, por encima del nivel
normal. Un aumento inicial de la reabsorcin por los capilares peritubulares hace
que baje la presin hidrosttica del lquido intersticial y que aumente la presin
coloidosmotica del mismo. Esto dos factores favorecen el desplazamiento del
liquido y de solutos hasta el exterior de la luz tubular para entrar en el intersticio;
por tanto, disminuye la difusin retrograda de agua y solutos hacia la luz tubular y
aumenta la reabsorcin tubular neta. En general la fuerzas que aumentan la
reabsorcin en los capilares peritubulares aumenta tambin la reabsorcin de los
tbulos renales, al inversa, los cambios hemodinmicas que inhiben la reabsorcin
en los capilares peritubulares inhiben tambin la reabsorcin tubular de agua y
solutos.
Efecto de la presin arterial sobre la eliminacin de orina; mecanismo de la
presin-natriuresis y presin-diuresis.
Los aumentos, aunque sean pequeos, de la presin arterial es frecuente que
produzca elevaciones considerables de la excrecin urinaria de sodio y agua,
fenmenos que se conocen como natriuresis por presin y diuresis por presin. La elevacin de la presin arterial dentro de
los lmites de 75 a 160 mm Hg suelen tener solo un efecto sobre el flujo sanguneo renal y la TFG. El ligero aumento de la
TFG que se producen contribuye, en parte, al efecto que produce el aumento de la presin arterial sobre la eliminacin de
orina.
Cuando se altera la autorregulacin de la TFG, como ocurre con frecuencia de las enfermedades renales
(nefropatas), las elevaciones de la presin arterial produce aumentos muchos mayores que la TFG
Un segundo efecto que eleva la eliminacin de la orina este disminuye el porcentaje de la carga de sodio y agua
filtrada que reabsorbe los tbulos. Los mecanismos responsables de este efecto se debe en parte al ligero
ascenso de la presin hidrosttica de los capilares peritubulares, especialmente en los vasos rectos de la medula
renal, seguido de la elevacin de la presin hidrosttica del lquido intersticial renal.
Un tercer factor que contribuye a los mecanismos de la natriuresis por presin y diuresis por presin es la menor
formacin de angiotensina II. La angiotensina II eleva directamente la reabsorcin de sodio en los tbulos;
adems, estimula la secrecin de aldosterona y eso acenta ms la reabsorcin de sodio. La disminucin de la
formacin de angiotensina II contribuye al descenso de la reabsorcin tubular de sodio que se produce cuando se
eleva la presin arterial.
Control hormonal de la reabsorcin tubular
Cuando aumenta el ingreso de potasio, los riones deben excretar ms potasio al tiempo que mantiene una excrecin
normal del sodio y otros electrolitos. De igual modo, cuando al aporte de sodio varia los riones deben ajustar
adecuadamente la excrecin urinaria de sodio sin que cambie de forma importante la excrecin de los otros electrolitos.
Algunas hormonas del organismo acta favoreciendo esta especificidad de la reabsorcin tubular de los distintos electrolitos
y del agua.
Aldosterona aumenta la reabsorcin de sodio y la secrecin de potasio.
La aldosterona, secretada por las clulas de la glomerulosa (zona glomerular) de la corteza suprarrenal, es un importante
factor regulador de la reabsorcin de sodio y la secrecin de potasio por los tbulos renales. El lugar fundamental de accin
de la aldosterona son las clulas principales de los tbulos colectores corticales. El mecanismo por el cual la aldosterona
aumenta la reabsorcin de sodio y, simultneamente, la secrecin de potasio es mediante la estimulacin de la bomba
ATPasa de sodio-potasio situada en el lado basolateral de la membrana de las clulas del tbulo colector cortical. La
aldosterona aumenta tambin la permeabilidad al sodio de la cara luminal de la membrana. Si falta la aldosterona, como
ocurre en la destruccin o de una insuficiencia de las gldulas suprarrenales (enfermedad de addison), se produce una
intensa prdida de sodio y una retencin de potasio en el organismo. El exceso de secrecin de aldosterona, como ocurre
en los pacientes con tumores suprarrenales (sndrome Conn), se acompaa de retencin de sodio y de agotamiento de
potasio. La aldosterona es todava ms importante como regulador de la concentracin de potasio que de la concentracin
del sodio.
La angiotensina II aumenta la reabsorcin de sodio y agua.
La angiotensina II es quizs la hormona ms potente del cuerpo que retiene sodio. La formacin de angiotensina II aumenta
en los casos que se acompaan de descenso de la presin arterial, o de disminucin del volumen de lquido extracelular,
como despus de una hemorragia o de unas prdidas de agua y sal de los lquidos corporales. La mayor formacin de
angiotensina II ayuda entonces a la normalizacin de la presin arterial y del volumen de los lquidos extracelulares a travs
de un aumento de la reabsorcin de sodio.
1.
La angiotensina II estimula la secrecin de aldosterona, que a su vez, aumenta la reabsorcin de sodio
FACULTAD DE CIENCIAS MDICAS-ULEAM
POR MIGUEL BARZALLO
FISIOLOGA HUMANA GUYTON CAPTULO 27
2.
3.
La angiotensina II produce constriccion de las arteriolas eferentes, lo cual tiene dos efectos sobre la dinmica de
los capilares peritubulares para aumentar la reabsorcin de sodio y agua. Primero la constriccion de la arteriola
eferente disminuye la presin hidrosttica de los capilares peritubulares, y con ello aumenta la reabsorcin tubular
final, especialmente en los tbulos proximales. Segundo, la constriccion de la arteriola eferente, al reducir el flujo
sanguneo renal, aumenta la fraccin de filtracin en los glomrulos y eleva la concentracin de las protenas y la
presin coloidosmotica en los capilares peritubulares y aumenta la reabsorcin tubular de sodio y agua.
La angiotensina II estimula directamente la reabsorcin de sodio de los tbulos proximales, las asas de Henle y
los tbulos distales y los tbulos colectores. Estimula la bomba ATPasa de sodio-potasio en la membrana
basolateral en la clula epitelial tubular. Un segundo efecto es estimular el intercambio de sodio por hidrogeno de
la membrana luminal especialmente en el tbulo proximal.
La ADH aumenta la reabsorcin de agua
Aumenta la permeabilidad de agua de los tbulo distal, el tbulo colector, y los epitelios del conducto colector, este efecto
ayuda al cuerpo a conservar agua en circunstancias como la deshidratacin. Cuando falta la ADH, desempea un papel
esencial en la regulacin de la orina
El pptido auricular natriurtico disminuye la reabsorcin de sodio y agua
Existen ciertas clulas en las aurculas del corazn, que cuando se distienden debido a un aumento del volumen
plasmtico, secretan una sustancia llamada pptido auricular natriurtico. Las concentraciones elevadas de este pptido
inhiben a su vez la reabsorcin de agua y sodio por los tbulos renales, sobre todo en los conductos colectores. Esta menor
reabsorcin de sodio y de agua aumenta la excrecin de orina y eso ayuda que se normalice el volumen sanguneo
La hormona paratiroidea aumenta la reabsorcion de calcio.
Es una de las hormonas reguladoras del calcio ms importante del organismo. En los riones es aumentar la reabsorcin
tubular de calcio, sobre todo en los tubulos distales y quizs tambin en el asa Henle y otras acciones como inhibir la
reabsorcin de fosfato por el tbulo proximal y del magnesio por el asa de Henle.
La activacin del sitema nervioso simptico aumenta la reabsorcionde sodio
La activacin del sistema nervioso simpatico pueden disminuir la excrecin de sodio y agua producir constricciones de la
arteriola renal lo que disminuye la TFG. Impulso simpaticos aumentan tambin la reabsorcin de sodio en el tubulo proximal
y en porcion gruesa de la rama ascendente del asa de Henle. Aumenta la liberacin de renina y la formacin angiotensina II,
lo que se sobreaade al efecto general del aumento de la reabsorcin tubular y de disminucin de la excrecion de sodio por
el rion
EMPLEO DE LAS TECNICAS DE ACLARAMIENTO PARA CUANTIFICAR LA FUNCION RENAL
El aclaramiento renal de una sustancia es el volumen del plasma que es completamente depurado de esas sustancias por
los riones en la unidad del tiempo. El concepto de aclaramiento lo proporciona un metodo til para cuantificar la funcin
excretora de los riones, se puede usar para calcular la velocidad con la que la sangre fluye atraves de los riones y
tambin para medir las funciones bsicas del rin: filtracin glomerular, la reabsorcin
tubular, y la secrecin tubular. El aclaramiento se refiere al volumen del plasma que se
necesitara para proporcionar la cantidad de sustancias que excreta la orina en la unidad
del tiempo.
Se puede usar el aclaramiento de la inulina para carcular la TFG
Si una sustancia se filtra libremente (tan libremente como el agua) y no se reabsorbe ni
se secreta por los tbulos renales, entonces la tasa a la que se excreta esa sustancia es
la orina es igual a la tasa a la que esa sustancia se filtra por los riones. Una sustancia
que cumple estos criterios es la inulina. La inulina no la elabora el organismo, si no que
se obtiene de las races de ciertas plantas y hay que administrarla al paciente por va
intravenosa para medir la TFG. La inulina no es la nica sustancia que puede utilizarse
para medir la TFG, clnicamente, y con esta misma finalidad se han utilizado al creatinina
el yodotamalato radiactivo.
Comparaciones del aclaramiento de la inulina con los aclaramientos de distintos
solutos
Comparando el aclaramiento de una sustancia con el aclaramiento de una inulina que es, como sabemos, una medida de la
TFG, se pueden hacer algunas generalizaciones.
1.
2.
3.
Si el aclaramiento de una sustancia es igual al de la inulina, esa sustancia se filtra solamente y no se reabsorbe ni
se secreta
Si el aclaramiento de esa sustancia es menor que el de la inulina la sustancia han tenido que ser reabsorbida por
los tubulos de las nefronas,
Si el aclaramiento de dicha sustancia es mayor que de la inulina, entonces las sustancias ha sido secretada por la
porcion tubular de la nefrona.
Você também pode gostar
- Resumen Capitulo 25 Los Compartimientos Del Liquido Corporal Liquidos Extracelular e Intracelular Edema PDFDocumento9 páginasResumen Capitulo 25 Los Compartimientos Del Liquido Corporal Liquidos Extracelular e Intracelular Edema PDFAndy BrunnerAinda não há avaliações
- Capitulo 25 - Liquidos CorporeosDocumento2 páginasCapitulo 25 - Liquidos CorporeosStefano Lessa0% (1)
- Capitulo 25 FisiologiaDocumento5 páginasCapitulo 25 FisiologiaVICTORIAAinda não há avaliações
- CAPITULO 28 de GUYTONDocumento10 páginasCAPITULO 28 de GUYTONJhonier MaldonadoAinda não há avaliações
- Función Glomerular: Universidad Privada San Juan Bautista Facultad de Ciencias de La SaludDocumento5 páginasFunción Glomerular: Universidad Privada San Juan Bautista Facultad de Ciencias de La SaludAnabel ValerAinda não há avaliações
- Absorción y Secreción de Electrolitos y AguaDocumento1 páginaAbsorción y Secreción de Electrolitos y Aguaapi-370007567% (6)
- Resumen Cap 27 GuytonDocumento18 páginasResumen Cap 27 GuytonJosé F. Martínez Pérez25% (4)
- Aparato Urinario InterrogatorioDocumento58 páginasAparato Urinario InterrogatorioSolange naomi Parra avilaAinda não há avaliações
- Agua y ElectrolitosDocumento50 páginasAgua y ElectrolitosLuis Carlos Valdez LopezAinda não há avaliações
- La Nefrona, Tubulos Proximales y DistalesDocumento2 páginasLa Nefrona, Tubulos Proximales y DistalesHeidi Esther BaezAinda não há avaliações
- Cap 64 FisioDocumento24 páginasCap 64 FisioSteven SeguraAinda não há avaliações
- Hormona AntidiuréticaDocumento20 páginasHormona AntidiuréticaYeisson Ayrton Olivera PlasenciaAinda não há avaliações
- Anatomia y Fisiologia Del Sistema ExcretorDocumento19 páginasAnatomia y Fisiologia Del Sistema ExcretorHernan MezaAinda não há avaliações
- Tema 15. Función Tubular. Mecanismos de Concentración y Dilución de Orina.Documento36 páginasTema 15. Función Tubular. Mecanismos de Concentración y Dilución de Orina.Pilar del Pino67% (3)
- Electrolitos en Orina Investigación ExposiciónDocumento15 páginasElectrolitos en Orina Investigación ExposiciónKely NúñezAinda não há avaliações
- Ensayo Capitulo 33 y 34 GuytonDocumento6 páginasEnsayo Capitulo 33 y 34 Guytonfatima75% (4)
- Depuracion RenalDocumento46 páginasDepuracion RenalNath Carrasco100% (1)
- Los Aminoácidos y Las Proteinas Como ElectrolitosDocumento21 páginasLos Aminoácidos y Las Proteinas Como ElectrolitosAnonymous TTQWLEvLr67% (3)
- Circulaciones EspecialesDocumento4 páginasCirculaciones EspecialesAna Karely RamíresAinda não há avaliações
- Capítulo 28 Fisiologia de GuytonDocumento5 páginasCapítulo 28 Fisiologia de GuytonKanadeTachibana25% (4)
- Resumen Guyton Fisiologiía RenalDocumento6 páginasResumen Guyton Fisiologiía Renalnoxjosue100% (3)
- Trastornos Del Equilibrio de Líquidos y ElectrolitosDocumento78 páginasTrastornos Del Equilibrio de Líquidos y ElectrolitosluisperaAinda não há avaliações
- Alteraciones ElectrolíticasDocumento42 páginasAlteraciones ElectrolíticasVanessa Infante Liranzo100% (1)
- Filtracion GlomerularDocumento40 páginasFiltracion GlomerularElenita O-ValenciaAinda não há avaliações
- Vias BiliaresDocumento3 páginasVias BiliaresRomina VillaseñorAinda não há avaliações
- Clase 1 Gastr - Introduccion Al Musculo LisoDocumento17 páginasClase 1 Gastr - Introduccion Al Musculo LisoFelipe Ignacio Gutierrez BarriosAinda não há avaliações
- Clase 12.1 - Segmentacion HepaticaDocumento68 páginasClase 12.1 - Segmentacion HepaticaC Martin TraumatoAinda não há avaliações
- Reabsorción y Secreción TubularDocumento19 páginasReabsorción y Secreción TubularMARJHORY DEL PILAR CARRION AYALAAinda não há avaliações
- Capitulo 19 GuytonDocumento18 páginasCapitulo 19 Guytonwiliamsanchezt100% (2)
- Practica 10-Masa ProteicaDocumento5 páginasPractica 10-Masa ProteicaVictor J. OreAinda não há avaliações
- Disturbios HidroelectroliticosDocumento81 páginasDisturbios HidroelectroliticosSociedad Científica de Estudiantes de Medicina de Ica100% (2)
- Equilibrio Acido Base en El OrganismoDocumento20 páginasEquilibrio Acido Base en El OrganismoROSA ISELA LEYVA CONTRERASAinda não há avaliações
- Balance HidrosalinoDocumento6 páginasBalance Hidrosalinocalam75Ainda não há avaliações
- Electrolitos SericosDocumento35 páginasElectrolitos SericosMiguel HernandezAinda não há avaliações
- Alcalosis Metabólica y Alcalosis Respiratoria FINALDocumento26 páginasAlcalosis Metabólica y Alcalosis Respiratoria FINALGreziaTatianaAinda não há avaliações
- Capitulo 30 Resumen Guyton y Hall Compendio de Fisiologia Medica PDFDocumento6 páginasCapitulo 30 Resumen Guyton y Hall Compendio de Fisiologia Medica PDFMiguel AlejandroAinda não há avaliações
- Equilibrio Acido BaseDocumento59 páginasEquilibrio Acido BaseSoraya CardozoAinda não há avaliações
- Bioquímica Del RiñónDocumento30 páginasBioquímica Del RiñónDaniel Pinillos71% (7)
- R1 2do Cuatrimestre PDFDocumento248 páginasR1 2do Cuatrimestre PDFMicaela AleAinda não há avaliações
- Semiologia Del EdemaDocumento16 páginasSemiologia Del EdemaBeijula33% (3)
- Hormonas CorticosuprarrenalesDocumento9 páginasHormonas CorticosuprarrenalesElda Araceli Hernández DíazAinda não há avaliações
- Perfil HepaticoDocumento4 páginasPerfil HepaticoLidia CarvalhoAinda não há avaliações
- Guyton Resumen LibroDocumento6 páginasGuyton Resumen LibroDaniel VillalobosAinda não há avaliações
- Capitulo 62Documento7 páginasCapitulo 62Fernanda Maza100% (2)
- Fisiopatologia Trastorno Acido BaseDocumento59 páginasFisiopatologia Trastorno Acido BaseEnedina Sanchez Campos0% (1)
- Sesión 4 Liquidos CorporalesDocumento16 páginasSesión 4 Liquidos CorporalesAnibal Alberto Sosa EscobarAinda não há avaliações
- Arteria HepáticaDocumento15 páginasArteria HepáticaPablo GarciaAinda não há avaliações
- 04 Regulacion de La Osmolaridad Del Liquido Extracelular y de La Concentracion de SodioDocumento43 páginas04 Regulacion de La Osmolaridad Del Liquido Extracelular y de La Concentracion de SodioThulio MoutinhoAinda não há avaliações
- Analisisdel Capitulo 15 Fisiologia GuytonDocumento8 páginasAnalisisdel Capitulo 15 Fisiologia GuytonBryan LópezAinda não há avaliações
- Capitulo 7 Excitación Del Musculo EsqueleticoDocumento24 páginasCapitulo 7 Excitación Del Musculo EsqueleticoMichelle DelgadoAinda não há avaliações
- Cap 30 Guyton and Hall - Regulacion Del K, CA, Fosfato y MGDocumento6 páginasCap 30 Guyton and Hall - Regulacion Del K, CA, Fosfato y MGGabriel HernandezAinda não há avaliações
- Clase Semiología de Signos Vitales o Constantes VitalesDocumento7 páginasClase Semiología de Signos Vitales o Constantes VitalesMARLY YINETH MENDEZ ROSEROAinda não há avaliações
- Glomérulo Renal - Wikipedia, La Enciclopedi A LibreDocumento85 páginasGlomérulo Renal - Wikipedia, La Enciclopedi A LibreAngelica SuarezAinda não há avaliações
- Sindrome de Mala AbsorcionDocumento3 páginasSindrome de Mala AbsorcionEbbi DvAinda não há avaliações
- Capítulo 29 Concentración y Dilución de Orina Regulación de La OsmDocumento10 páginasCapítulo 29 Concentración y Dilución de Orina Regulación de La OsmJocelyne SgoAinda não há avaliações
- Fisio OidoDocumento40 páginasFisio OidoAriel GonzalezAinda não há avaliações
- Repaso FisiologíaDocumento8 páginasRepaso FisiologíaBrisseida Fonseca SánchezAinda não há avaliações
- Compartimientos Del Liquido CorporalDocumento16 páginasCompartimientos Del Liquido CorporalLuis CruzAinda não há avaliações
- Fisiologia Renal Guyton Cap 25 26 27 1 PDFDocumento27 páginasFisiologia Renal Guyton Cap 25 26 27 1 PDFKaren Andrea St100% (1)
- Fisiologia RenalDocumento5 páginasFisiologia RenalAndrik HernandezAinda não há avaliações
- EXAMEN FISICO DEL ANCIANO ClaseDocumento15 páginasEXAMEN FISICO DEL ANCIANO ClasevxnheAinda não há avaliações
- Anatomía Del MediastinoDocumento8 páginasAnatomía Del MediastinovxnheAinda não há avaliações
- Clase 6 - Historia Clinica NeumologicaDocumento15 páginasClase 6 - Historia Clinica NeumologicavxnheAinda não há avaliações
- Laboratorio de Enfermades RenalesDocumento26 páginasLaboratorio de Enfermades RenalesvxnheAinda não há avaliações
- Semiologia PANCREATITIS Y UN POCO DE MEDICINA INTERNADocumento24 páginasSemiologia PANCREATITIS Y UN POCO DE MEDICINA INTERNAvxnheAinda não há avaliações
- Reanimacion Avanzada: CardiopulmonarDocumento38 páginasReanimacion Avanzada: CardiopulmonarvxnheAinda não há avaliações
- Semiologia GASTROINTESTINALDocumento14 páginasSemiologia GASTROINTESTINALvxnheAinda não há avaliações
- Captura de Abimael GuzmanDocumento6 páginasCaptura de Abimael GuzmanvxnheAinda não há avaliações
- Terminologia MedicaDocumento43 páginasTerminologia MedicavxnheAinda não há avaliações
- Terminologia MedicaDocumento43 páginasTerminologia MedicavxnheAinda não há avaliações
- Sistema CardiovascularDocumento22 páginasSistema CardiovascularvxnheAinda não há avaliações
- Desnutricion SemiologiaDocumento15 páginasDesnutricion SemiologiavxnheAinda não há avaliações
- Asma BronquialDocumento29 páginasAsma Bronquialvxnhe100% (1)
- Asma BronquialDocumento29 páginasAsma Bronquialvxnhe100% (1)
- Fisiologia Renal PDFDocumento24 páginasFisiologia Renal PDFVi Ro ZeAinda não há avaliações
- Sistema UrinarioDocumento16 páginasSistema Urinarioalfredo molinaAinda não há avaliações
- Exposicion Sistema RenalDocumento39 páginasExposicion Sistema Renalruth0% (2)
- Fisio I 2doparcialDocumento143 páginasFisio I 2doparcialJoselin GalvezAinda não há avaliações
- Actividad de ExcreciónDocumento5 páginasActividad de ExcreciónLinda Patricia DCAinda não há avaliações
- Histología Aparato UrinarioDocumento12 páginasHistología Aparato UrinarioRenata AlassiaAinda não há avaliações
- Anatomía y Fisiología Del RiñónDocumento29 páginasAnatomía y Fisiología Del RiñónEmilia NarvaezAinda não há avaliações
- Farmacología EspecialDocumento156 páginasFarmacología EspecialAndrea Roman SolanoAinda não há avaliações
- 6° ExcrecionDocumento46 páginas6° ExcrecionyuniorAinda não há avaliações
- Sistema RenalDocumento33 páginasSistema RenalFrancisca Martinez100% (3)
- Preguntas de NefrologiaDocumento7 páginasPreguntas de NefrologiaSaraOconnorAinda não há avaliações
- Farmacologia Del Medio InternoDocumento21 páginasFarmacologia Del Medio InternoInes MelladoAinda não há avaliações
- Trastornos Del FosfatoDocumento29 páginasTrastornos Del FosfatoKevin Lopez MartinezAinda não há avaliações
- Sistema Renal 1Documento15 páginasSistema Renal 1Marily CabadaAinda não há avaliações
- 10 Sistema ExcretorDocumento5 páginas10 Sistema ExcretorEligio Cordobes PadillaAinda não há avaliações
- Enfermedades Del Metabolismo Del Calcio y El FósforoDocumento23 páginasEnfermedades Del Metabolismo Del Calcio y El FósforoDavid GuevaraAinda não há avaliações
- Fisiología Renal - 2022Documento5 páginasFisiología Renal - 2022Oscar Camones HuertaAinda não há avaliações
- Exposición IvDocumento35 páginasExposición IvSilvia Eche echeAinda não há avaliações
- PremedicinaDocumento95 páginasPremedicinalojaf91069Ainda não há avaliações
- Cuestionario de HistologíaDocumento36 páginasCuestionario de HistologíaHenry Perugachi MendezAinda não há avaliações
- Trabajo Monográfico de Uroanalisis.Documento18 páginasTrabajo Monográfico de Uroanalisis.Harry Ramirez Hernandez100% (1)
- AP - URINARIO Y CORRELACIONES CLINICAS (22) DR MaldonadoDocumento50 páginasAP - URINARIO Y CORRELACIONES CLINICAS (22) DR MaldonadoERIKA MARIBEL AVILE LARUTAAinda não há avaliações
- Notas Nefrología, 2020Documento50 páginasNotas Nefrología, 2020PauFlorastAinda não há avaliações
- ExcretorDocumento6 páginasExcretorCarmen Santamaría FernandezAinda não há avaliações
- Resumen de La Segunda Fase Embriologia VeterinariaDocumento41 páginasResumen de La Segunda Fase Embriologia Veterinariajheyson mendoza chumbesAinda não há avaliações
- Excrecion Grado SeptimoDocumento30 páginasExcrecion Grado SeptimoClara CerqueraAinda não há avaliações
- Anatomia y Fisiologia Renal Del Riñon - ResumenDocumento8 páginasAnatomia y Fisiologia Renal Del Riñon - ResumenEstephany MolinaAinda não há avaliações
- Anatomia Y Fisiología Del Sistema Renal: Características GeneralesDocumento15 páginasAnatomia Y Fisiología Del Sistema Renal: Características GeneralesgomezAinda não há avaliações
- Sistema UrinarioDocumento2 páginasSistema UrinarioTatiana RamírezAinda não há avaliações