Escolar Documentos
Profissional Documentos
Cultura Documentos
Equil Vol Oxido Reducao Final
Enviado por
paullinhhaDireitos autorais
Formatos disponíveis
Compartilhar este documento
Compartilhar ou incorporar documento
Você considera este documento útil?
Este conteúdo é inapropriado?
Denunciar este documentoDireitos autorais:
Formatos disponíveis
Equil Vol Oxido Reducao Final
Enviado por
paullinhhaDireitos autorais:
Formatos disponíveis
4/2/2014
EQUILBRIO E TITULOMETRIA DE XIDOXIDO- REDUO
Oxidao e reduo 2Fe3+ + Sn2+ 2Fe2+ + Sn4+ Fe3+: reduzido; Sn2+: oxidado Oxidao: perda de eltrons; Reduo: ganho de eltrons. Agente oxidante: aceita eltrons; Agente redutor: doa eltrons. Sistemas redox Fe + Cu2+ Fe2+ + Cu Cu2+ + 2eCu SEMI-REAES 2+ Fe Fe + 2e2MnO4- + 5H2O2 + 6H+ 2Mn2+ + 5O2 + 8H2O 2MnO4- + 16H+ + 10e2Mn2+ + 8H2O SEMI-REAES + 5H2O2 5O2 + 10H + 10e-
-- Sistemas redox simples Ox + neZn2+ + 2eRed Zn
-- Sistemas combinados redox e cido-base Cr2O72- + 14H+ + 6eC6H6O6 + 2H+ + 2e2Cr3+ + 7H2O C6H8O6
CLULA GALVNICA (VOLTAICA) CLULAS GALVNICAS X CLULAS ELETROLTICAS
NaNO3
Aplicao do processo de xido-reduo.
Representao de clulas eletroqumicas
2Ag+(aq, 1,0 mol L-1) + Cu(s) 2Ag(s) + Cu2+(aq, 1,0 mol L-1) Cu(s)|Cu2+(aq, 1,0 mol L-1)||Ag+(aq, 1,0 mol L-1)|Ag(s) Informaes anodo Informaes catodo
Ponte salina 2 Fe3+(aq) + H2(g) 2Fe2+(aq) + 2H+(aq) Pt |H2 (P = 1 atm)|H+(aq, 1,0 mol L-1)||Fe3+(aq, 1,0 mol L-1), Fe2+(aq, 1,0 mol L-1)
Terminologia usada em clulas eletroqumicas.
4/2/2014
Fora eletromotriz
f.e.m. = Ecel = Potencial da clula
Potenciais padro de eletrodos a 25 oC
Reao espontnea
Potencial positivo
Potencial-padro de reduo Eocel = Eored(catodo) Eored(anodo) Eo: Condies-padro
Clula eletroqumica usando um eletrodo-padro de hidrognio.
Capacidade de oxidao e reduo de Substncias em relao ao hidrognio.
Efeito da concentrao na fem de clulas eletroqumicas
Potencial de xido-reduo para diferentes sistemas
Eletrodos metlicos Me Men+ + ne-
G = G + RT ln Q
Para a reao: xA(aq) + yB(aq) zC(aq) + wD(aq)
nFE = nFE + RT ln Q
Q=
[C ] [ D ] [ A] x [ B ] y
E = E0 +
RT ln aMen+ nF
Red
E = E0 +
RT ln[Men+ ] nF
E = E
RT ln Q nF
Equao de Nernst
Sistemas redox simples Ox + ne0
Temperatura= 298 K , R = 8,315 J K-1 mol-1, F = 96.485 C mol-1 NO EQUILBRIO: G = 0 e E = 0
0 , 0592 E = E log Q n
RT aRed E=E ln nF aOx
Sn4+ + 2eSn2+
E = E0
RT [Red ] ln nF [Ox]
RT 0 , 0592 E = ln K ou E = log K nF n
nE
0
E = E0
RT aSn2+ ln nF aSn4+
E = E0
RT [Sn2+ ] ln nF [Sn4+ ]
K = 10 0 , 0592
4/2/2014
Sistemas combinados redox e cido-base Ox + mH+ + neRed + m/2H2O
Fatores que afetam os potenciais eletrdicos
Temperatura; Concentrao dos ons ativos; Fora inica; Formao de complexos;
E = E0
RT aRed ln m nF aOxaH +
E = E0
RT [Red ] ln nF [Ox][H + ]m
Cr2O72- + 14H+ + 6eE = E0 aCr3+ RT ln nF aCr O2 a14 H+
2 7
2Cr3+ + 7H2O
E = E0
RT [Cr ] ln 2 nF [Cr2O7 ][H + ]14
3+
pH; Tipo de solvente.
Para a reao: xA(aq) + yB(aq) zC(aq) + wD(aq)
Eletrodos de gs 2H+ + 2eH2
E = E
E = E0 RT [H2 ] ln nF [H + ]2
ou
E = E0
RT aH2 ln 2 nF aH +
E = E0
RT PH2 ln nF [H + ]2
RT ln Q nF
Q=
[C ] z [ D ]w [ A] x [ B ] y
Aplicaes dos potenciais eletrdicos padres
f.e.m. de uma clula eletroqumica; Ecel = Ecatodo Eanodo Constante de equilbrio das reaes de xido-reduo.
aOx1 + bRed2
c
No equilbrio E1 = E2
E10
0,0592 [Re d1 ]b 0,0592 [Re d 2 ]d 0 log log = E2 a n1 [Ox1 ] n2 [Ox2 ]c 0,0592 [Ox1 ]a [Re d 2 ]d log n1n2 [Ox2 ]c [Re d1 ]b
cOx2 + dRed1
0 E2 E10 =
K=
[Ox2 ] [Re d1 ]d ... [Ox1 ]a [Re d 2 ]b ...
bRed1
b
log
0 [Ox2 ]c [Re d1 ]d n1n2 ( E2 E10 ) = d b [Ox1 ] [Re d 2 ] 0,0592
Semi-reao: aOx1 + ne0 1
Semi-reao: cRed2 + ne0 2
dOx2
0,0592 [Re d1 ] E=E log n1 [Ox1 ]a
0,0592 [Re d 2 ]d E=E log n2 [Ox2 ]c
log K =
0 n1n2 ( E2 E10 ) 0,0592
4/2/2014
Potencial formal
Reao parcial
Ce4+ + eCe3+
Potencial formal, V
1,70, HClO4 1 mol L-1 1,61, HNO3 1 mol L-1 1,44, H2SO4 1 mol L-1 1,28, HCl 1 mol L-1
Titulometria de xidoxido-reduo
Alguns agentes oxidantes e redutores usados na preparao de solues padro
Reagente Sistema de xido-reduo OXIDANTES MnO4- + 8H+ + 5eKMnO4 I2 K2Cr2O7 KIO3 Ce(IV) Ti(III) SnCl2 Cr(III) Fe(II) H3AsO3 Na2S2O3 MnO4- + 4H+ + 3eMnO4- + eI3- + eCr2O72- + 14H+ + 6eIO3- + 2Cl- + 6H+ + 4eCe4+ + eTiO2+ + 2H+ + eSn4+ + 2eCr3+ + eFe3+ + eH3AsO4 + 2H+ + 2eS4O62- + 2eREDUTORES Ti3+ + H2O Sn2+ Cr2+ Fe2+ H3AsO3 + H2O 2S2O32+0,10 +0,15 -0,41 +0,77 +0,56 +0,08 Mn2+ + 4H2O MnO2 + 2H2O MnO423I2Cr3+ + 7H2O ICl2- + 3H2O Ce3+ +1,51 +1,69 +0,56 +0,54 +1,33 +1,23 +1,44 E0 (V)
Mn3+ + e-
Mn2+ Mn2+ + 2H2O VO2+ + 3H2O HNO2 + H2O
1,51 H2SO4 aq. 1,24, HClO4 1 mol L-1 1,02, HCl, HClO4 1 mol L-1 0,92, HNO3 1 mol L-1 0,907, HClO4 1 mol L-1 0,792, HClO4 1 mol L-1 0,77, H2SO4 1 mol L-1 0,776, HClO4 1 mol L-1 0,674, H2SO4 1 mol L-1 0,700, HCl 1 mol L-1 0,732, HClO4 1 mol L-1 0,68, H2SO4 1 mol L-1 0,577, HCl, HClO4 1 mol L-1 0,71, HCl 1 mol L-1 0,72, HClO4, H2SO4 1 mol L-1 0,14, HCl 1 mol L-1 Ti3+ + H2O 0,04, H2SO4 1 mol L-1 -0,005, HCl, HClO4 1 mol -0,14, HClO4 1 mol L-1 -0,29, H2SO4 1 mol L-1 L-1
MnO2 + 4H+ + 2eV(OH)4+ + 2H+ + eNO3- + 3H+ + 2 e2Hg2+ + 2 eAg+ + eHg22+ + 2eFe3+ + eAg Hg Fe2+ Hg2+
H3AsO4 + 2H+ + 2eH3AsO3 + H2O Fe(CN)63- + eFe(CN)64Sn4+ + 2e2H+ + 2eSn2+ H2 Pb
TiO2+ + 2H+ + ePb2+ + 2e-
Curva de titulao
Variao do potencial durante a titulao de 25,00 mL de uma soluo de FeSO4 0,1000 mol L-1 com soluo de Ce4+ 0,1000 mol L-1 em meio sulfrico
Volume soluo Ce4+ 0,1000 mol L-1 (mL) 0,00 5,00 12,50 20,00 24,90 25,00 25,10 30,00 42,50 50,00 E (volts) --0,73 0,77 0,81 0,91 1,11 (PE) 1,30 1,40 1,43 1,44
E0Fe3+/Fe2+ = + 0,771 V E0Ce4+/Ce3+ = + 1,44 V Ponto final satisfatrio se diferena nos potenciais formais 0,4 V.
Curva de titulao de 100,00 mL de soluo de Tl+ 0,01000 mol L-1 com soluo de IO3- 0,01000 mol L-1 em HCl 1,00 mol L-1. P.E. em 0,842 V. IO3- + 2Cl- + 6H+ + 4eCurva de titulao de 25,00 mL de uma sol. Fe2+ 0,1000 mol L-1 com sol. Ce4+ 0,1000 mol L-1. Tl3+ + 2eTl+ ICl2- + 3H2O E0 = +1,24 V E0 = +0,77 V
Eequivalncia =
0 n1 E10 + n2 E2 (n1 + n2 )
4/2/2014
DETECO DO PONTO FINAL
Exemplos de indicadores de xido-reduo
Indicador Safranina T Cor Oxidada Vermelho Vermelho Azul Azul Azul Violeta Violeta Azul plido Vermelho Azul plido Vermelho plido Vermelho Azul plido Azul violeta Azul plido Reduzida Incolor Incolor Incolor Incolor Incolor Incolor Incolor Vermelho Amarelo esverdeado Vermelho Amarelo esverdeado Incolor Vermelho Incolor Vermelho E0 (V) +0,24 +0,28 +0,36 +0,53 +0,67 +0,76 +0,76 +0,88 +1,00 +1,02 +1,06 +1,08 +1,15 +1,12 +1,25
Indicadores de xido-reduo (mudam de colorao quando passa do estado oxidado para o reduzido); Indicadores especficos; Reagentes auto-indicadores (KMnO4, I2, Ce(SO4)2); Mtodos potenciomtricos.
Fenossafranina Indigotetrassulfonato Azul de metileno 2,6-Dibromofenolindofenol Difenilamina Difenilbenzidina 4,7-dimetilferrona Erioglaucina A Metilferrona Setoglaucina O Ac. N-fenilantranlico Ferrona Ac. 2,3-difenilamino-dicarboxlico Nitroferrona
Indicadores especficos
Amido (titulaes I2/I3-); Complexo amilose-iodo: azul (perceptvel com conc. iodo 2,0 x 10-5 mol L-1 (necessrio I-); Complexo amilopectina-iodo: vermelho; Complexo eritroamilose-iodo e eritrogranulose-iodo: marrom avermelhado; Complexo dextrina-iodo: amarelo a marrom.
Viragem da ferrona.
Complexo amido-I6
Viragem da difenilamina.
Amilose
FAIXA DE VIRAGEM DO INDICADOR:
0,0592 E = E0 volts n
Mudana de cor na
Indicado: amidos de batata, araruta e arroz; Contra-indicado: amido de milho.
KSCN (titulao de Fe3+ com Ti3+). Para a ferrona, E0 = +1,147 V e n = 1 faixa de +1,088 V a +1,206 V.
4/2/2014
Alguns mtodos de titulao de oxi-reduo
Permanganimetria - Meio fortemente cido; - Soluo alcalina ou neutra; - Soluo fortemente alcalina. Iodometria Dicromatometria Solues de Fe(II) Tiossulfato de sdio
Permanganimetria
Permanganato de potssio (oxidante forte): Reagente auto-indicador (0,01 mL sol. 0,02 mol L-1 em 100 mL soluo).
- Meio fortemente cido (H2SO4 ou H3PO4 0,1 mol L-1) (reduo a Mn2+)
MnO4- + 8H+ + 5eMn2+ + 4H2O E0 = +1,51 V
-Soluo levemente cida, alcalina ou neutra (MnO2)
MnO4- + 4H+ + 3eMnO2(s) + 2H2O E0 = +1,69 V
- Soluo fortemente alcalina (MnO42-)
MnO4- + eMnO42E0 = +0,56 V
Caractersticas do MnO4Solues de permanganato padronizao peridica); Moderadamente estveis (requer
Aplicaes analticas das titulaes com permanganato
4MnO4- + 2H2O 4MnO2 + 3O2 + 4OH- (Reao catalisada por luz,
calor, cidos, bases, mangans(II) e dixido de mangans)
Padronizao com oxalato de sdio, trixido de arsnio ou fio de ferro eletroliticamente puro; filtrao do Para aumentar estabilidade da soluo de MnO4MnO2 antes da padronizao; No pode ser utilizada para titular solues que contenham HCl; Baixo custo.
4/2/2014
Dicromatometria
Cr2O7
2-
Consideraes sobre a dicromatometria
E0 = +1,33 V
14H+
6e-
2Cr3+
+ 7H2O
Vantagens: Pode ser obtido puro; estvel at seu ponto de fuso e, portanto, um excelente padro primrio; Solues aquosas so estveis indefinidamente se forem protegidas contra a evaporao; Utilizado somente em meio cido (HCl ou H2SO4 1 mol L-1), rapidamente reduzido a um sal de cromo(III) verde; No reagem com cido clordrico frio, desde que a concentrao do cido no exceda 1 ou 2 mol L-1; Solues menos reduzidas por matria orgnica do que as de permanganato, e so estveis sob a ao de luz e calor. Desvantagens: No um oxidante to poderoso quanto o permanganato de potssio (E0KMnO4 = + 1,69 V; E0K2Cr2O7 = + 1,33 V); Lentido de sua reao com alguns agentes redutores.
Indicador: cido difenilaminossulfnico difenilbenzidinossulfnico;
ou
cido
Aplicaes: Fe(II) (direto) e Cu(I), Cr(III), U(VI), SO32-, ClO3-, NO3-, MnO4- e perxidos orgnicos (indireto).
Iodometria e Iodimetria
I2 + 2e2IE0 = +0,5355 V
Consideraes sobre a iodimetria e a iodometria
Agente oxidante fraco (seletividade em alguns casos); Solues de iodo Relativamente instvel, especialmente solues cidas (ar, matria orgnica, luz, volatilidade do iodo) requer padronizao peridica; Padronizao com tiossulfato de sdio anidro ou tiossulfato de brio mono-hidratado ou xido de arsenioso; Disponibilidade de um indicador sensvel e reversvel (amido ou uso de clorofrmio ou tetracloreto de carbono (iodometria)); Titulaes no devem ser realizadas sob luz solar direta.
CAUSAS DE ERRO NAS TITULAES QUE ENVOLVEM IODO Volatilidade do iodo; Oxidao do on iodeto pelo ar; Hidrlise do iodo.
I 2 + I I 3
K eq =
[ I 3 ] = 710 [ I 2 ]I ]
I 3 + 2e 3I
E Io / I = +0,536 V
3
Iodimetria: uso de sol. padro de iodo diretamente como titulante em meios levemente cidos ou levemente bsicos.
X
Iodometria: iodeto (excesso) utilizado como redutor, e o iodo liberado na reao titulado em meio neutro ou levemente cido com um redutor (Ex: sol. padro de tiossulfato de sdio ou arsenito de sdio). 2S2O32- + I2 S4O62- + 2I(sol. neutra ou levemente cida)
Titulaes iodomtricas ou iodimtricas: indicador
amido
4/2/2014
Aplicaes analticas da iodimetria
Aplicaes analticas da iodometria
Você também pode gostar
- Minicurso Excel Avançado AnaDocumento8 páginasMinicurso Excel Avançado AnapaullinhhaAinda não há avaliações
- Funcionários tabela salários tempo serviçoDocumento4 páginasFuncionários tabela salários tempo serviçopaullinhhaAinda não há avaliações
- 27 Requisitos Dos FluidosDocumento16 páginas27 Requisitos Dos FluidospaullinhhaAinda não há avaliações
- Apostila Sobre TRIACDocumento9 páginasApostila Sobre TRIACpaullinhhaAinda não há avaliações
- Sumário de EletrõnicaDocumento1 páginaSumário de EletrõnicapaullinhhaAinda não há avaliações
- VBADocumento2 páginasVBAAna Paula Silva ArturAinda não há avaliações
- Curso Excel DicasDocumento2 páginasCurso Excel DicaspaullinhhaAinda não há avaliações
- Check list de inspeção em correias transportadorasDocumento2 páginasCheck list de inspeção em correias transportadoraspaullinhha80% (5)
- C8-6 - PV Antoine PDFDocumento6 páginasC8-6 - PV Antoine PDFLucasMelloAinda não há avaliações
- Checklist filtro manga operaçãoDocumento2 páginasChecklist filtro manga operaçãopaullinhha33% (3)
- Propriedades Residuais Peng RobinsonDocumento16 páginasPropriedades Residuais Peng RobinsonpaullinhhaAinda não há avaliações
- Eletrônica Industrial1Documento33 páginasEletrônica Industrial1pososvikiAinda não há avaliações
- Bibliografia de PeríodicosDocumento1 páginaBibliografia de PeríodicospaullinhhaAinda não há avaliações
- Comandos Que Foram UsadosDocumento1 páginaComandos Que Foram UsadospaullinhhaAinda não há avaliações
- Trabalho de Eletronia 2ºDocumento13 páginasTrabalho de Eletronia 2ºpaullinhhaAinda não há avaliações
- Instalação de Bombeamento 1Documento7 páginasInstalação de Bombeamento 1paullinhhaAinda não há avaliações
- ArtigoDocumento15 páginasArtigopaullinhhaAinda não há avaliações
- Como montar uma confecção de uniformes profissionaisDocumento37 páginasComo montar uma confecção de uniformes profissionaispaullinhhaAinda não há avaliações
- Como montar uma confecção de uniformes profissionaisDocumento37 páginasComo montar uma confecção de uniformes profissionaispaullinhhaAinda não há avaliações
- Coordenadas Cilindricas e EsfericasDocumento14 páginasCoordenadas Cilindricas e Esfericasdiegorossetto100% (1)
- Respostas de QuímicaDocumento2 páginasRespostas de QuímicapaullinhhaAinda não há avaliações
- Bibliografia de PeríodicosDocumento1 páginaBibliografia de PeríodicospaullinhhaAinda não há avaliações
- Comoe Labor A Rum Rela TrioDocumento6 páginasComoe Labor A Rum Rela TriopaullinhhaAinda não há avaliações
- 8 - Marcas, Conceitos e Decisões - Un.IDocumento8 páginas8 - Marcas, Conceitos e Decisões - Un.IpaullinhhaAinda não há avaliações
- Grafico 1Documento1 páginaGrafico 1paullinhhaAinda não há avaliações
- 27 Requisitos Dos FluidosDocumento16 páginas27 Requisitos Dos FluidospaullinhhaAinda não há avaliações
- Calculo VPL e TIR com ExcelDocumento2 páginasCalculo VPL e TIR com ExcelpaullinhhaAinda não há avaliações
- Apresentação Ciclos Rev.00Documento45 páginasApresentação Ciclos Rev.00paullinhhaAinda não há avaliações
- Eletrônica Industrial1Documento33 páginasEletrônica Industrial1pososvikiAinda não há avaliações
- SLIDE Individuos e GruposDocumento15 páginasSLIDE Individuos e GrupospaullinhhaAinda não há avaliações
- Farmacognosia Pura AOL3Documento5 páginasFarmacognosia Pura AOL3Patrícia OliveiraAinda não há avaliações
- Regulamento Técnico Mercosul de Identidade e Qualidade DoDocumento9 páginasRegulamento Técnico Mercosul de Identidade e Qualidade DoAnonymous OTY0ZwmAinda não há avaliações
- Produção Organica de AlfaceDocumento52 páginasProdução Organica de AlfaceandsonevaristoAinda não há avaliações
- Princípios e Aplicações de Cromatografia Por BioafinidadeDocumento36 páginasPrincípios e Aplicações de Cromatografia Por BioafinidadeAmanda DiasAinda não há avaliações
- Acetileno: Propriedades e AplicaçõesDocumento7 páginasAcetileno: Propriedades e AplicaçõescandysuhAinda não há avaliações
- Hinode VSGrifeDocumento52 páginasHinode VSGrifeGili SantanaAinda não há avaliações
- Planejamento e Projeto EPSDocumento42 páginasPlanejamento e Projeto EPSGabriela CristinaAinda não há avaliações
- História Do Plástico, Brasil, Uso História Do PlásticoDocumento14 páginasHistória Do Plástico, Brasil, Uso História Do PlásticoLuiz Antonio MottaAinda não há avaliações
- Estudo Dirigido BromatologiaDocumento3 páginasEstudo Dirigido BromatologiaMaiana TeixeiraAinda não há avaliações
- Poli MerosDocumento9 páginasPoli MerosAna Cristina GarcezAinda não há avaliações
- Guia completo para produzir húmus orgânico com minhocasDocumento13 páginasGuia completo para produzir húmus orgânico com minhocasMauroDavidRodriguesAinda não há avaliações
- Identificação Grupos FuncionaisDocumento4 páginasIdentificação Grupos FuncionaisEverton Luis de Araujo LimaAinda não há avaliações
- UNICAMP - Resolvida - 1 FaseDocumento2 páginasUNICAMP - Resolvida - 1 Fasejacob213Ainda não há avaliações
- Slide de Organica I Oleos e GordurasDocumento31 páginasSlide de Organica I Oleos e Gorduraselvis roberAinda não há avaliações
- ASBC V GowinDocumento1 páginaASBC V GowinAna Soraia100% (1)
- Número de Oxidação (Nota de Aula e Exercícios)Documento3 páginasNúmero de Oxidação (Nota de Aula e Exercícios)Sidney ChristAinda não há avaliações
- Endutex TPU RefDocumento9 páginasEndutex TPU RefStéfany Vier SteffenAinda não há avaliações
- Biologia Compostos Organicos Exercícios PDFDocumento18 páginasBiologia Compostos Organicos Exercícios PDFSimone Diehl MacielAinda não há avaliações
- Válvula de retençãoDocumento1 páginaVálvula de retençãoangelmec23Ainda não há avaliações
- Feridas TabelaDocumento6 páginasFeridas TabelaRita MachadoAinda não há avaliações
- Exercícios IsomeriaDocumento13 páginasExercícios IsomeriavieirasalesAinda não há avaliações
- Funções Bioquímicas Dos Aminoácidos Essenciais e Dos Aminoácidos Não-EssenciaisDocumento23 páginasFunções Bioquímicas Dos Aminoácidos Essenciais e Dos Aminoácidos Não-Essenciaisclailton.nascimentoAinda não há avaliações
- 08 BarreiraGasesDocumento25 páginas08 BarreiraGasesDavrison BorgesAinda não há avaliações
- Apresentação BisfenolDocumento21 páginasApresentação BisfenolCedaspy São MiguelAinda não há avaliações
- Inimigos naturais de Helicoverpa armigera em sojaDocumento12 páginasInimigos naturais de Helicoverpa armigera em sojaYago GiacomelliAinda não há avaliações
- Ação de Enzimas na Gelatina e AmidoDocumento5 páginasAção de Enzimas na Gelatina e AmidoLeonan AlvesAinda não há avaliações
- CodigosepreçosDocumento1.474 páginasCodigosepreçosmarcosAinda não há avaliações
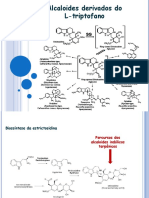
- Alcalóides Do TriptofanoDocumento26 páginasAlcalóides Do TriptofanoDiégina FernandesAinda não há avaliações
- AromaticidadeDocumento65 páginasAromaticidadeJaciara NascimentoAinda não há avaliações
- Pré-Vestibular Aula 05Documento2 páginasPré-Vestibular Aula 05Gisele RolimAinda não há avaliações