Escolar Documentos
Profissional Documentos
Cultura Documentos
Actividades de Refuerzo - Prueba de Diagnostico - Ciencias - Naturales 1° Bach
Enviado por
Roberto MartínezTítulo original
Direitos autorais
Formatos disponíveis
Compartilhar este documento
Compartilhar ou incorporar documento
Você considera este documento útil?
Este conteúdo é inapropriado?
Denunciar este documentoDireitos autorais:
Formatos disponíveis
Actividades de Refuerzo - Prueba de Diagnostico - Ciencias - Naturales 1° Bach
Enviado por
Roberto MartínezDireitos autorais:
Formatos disponíveis
MINISTERIO DE EDUCACIN DIRECCIN NACIONAL DE EDUCACIN
PROYECTO DE REFUERZO ACADMICO PARA ESTUDIANTES DE EDUCACIN MEDIA
DOCUMENTO PARA EL DOCENTE DE CIENCIAS NATURALES
Ministerio de Educacin Direccin Nacional de Educacin
PROYECTO DE REFUERZO ACADMICO PARA ESTUDIANTES DE EDUCACIN MEDIA
Presentacin El proyecto de refuerzo acadmico como accin estratgica del Programa Social Educativo 2009-2014 Vamos a la Escuela, se prev como una de las estrategias para evitar la repeticin y la desercin. En ese marco, este proyecto cobra importancia ya que a partir de ste se promover el apoyo a los estudiantes de segundo ao de bachillerato que presenten dificultades para desarrollar las competencias, conocimientos y habilidades, que se espera tengan los jvenes y seoritas que egresan de bachillerato. Para poder hacer efectivo el refuerzo acadmico se hace necesario contar con informacin que permita tener un diagnstico de las fortalezas y las limitaciones de los estudiantes que integran cada seccin de segundo ao de bachillerato; por ello, el proyecto inicia con una evaluacin diagnstica, cuyo fin no es asignar una nota a los estudiantes, tal como se describe a continuacin.
1. Finalidad de la evaluacin diagnstica La administracin de las pruebas de diagnstico tiene como finalidad poner a disposicin de los docentes de educacin media un instrumento de evaluacin, que les permita identificar en los resultados los puntos fuertes y /o dbiles de los estudiantes, con el propsito de realizar acciones pedaggicas que respondan a las necesidades individuales y de grupo, las cuales debern estar encaminadas a la mejora y aprovechamiento de los aprendizajes. sta es una evaluacin analtica y orientadora que pretende apoyar a los estudiantes que presentan ms dificultades en el aprendizaje; por lo tanto, no se debe tomar como una evaluacin para asignar calificaciones o calcular promedios en la asignatura.
Actividades de Refuerzo para Ciencias Naturales
Pgina 2
Ministerio de Educacin Direccin Nacional de Educacin
2. Documentos que se proporcionan a los docentes Pruebas por asignatura Se han elaborado pruebas de diagnstico de las 4 asignaturas bsicas: Matemtica, Lenguaje y Literatura, Estudios Sociales y Ciencias Naturales. Cada una de ellas se presenta en cuadernillo separado; los tems son de opcin mltiple con 4 opciones de respuesta de las cuales slo una es la correcta. Los insumos considerados para definir qu evaluar en cada asignatura fueron: los indicadores de logro que resultaron ms difciles para los estudiantes evaluados en la PAES 2008 y 2009; as como los indicadores de logro de los programas de estudio de primer ao de bachillerato que son prerrequisito para el dominio de otros indicadores de segundo ao, y que a la vez se consideran difciles para los estudiantes o difciles de impartir por el docente.
Actividades de Refuerzo Acadmico Es un documento por asignatura dirigido a los docentes, en el que se sugieren actividades de refuerzo orientadas a reducir las dificultades mostradas por los estudiantes en el desarrollo de las tareas propuestas en los tems. En cada asignatura se identifica el contenido que se explora en cada tem de la prueba, as como el indicador de logro del programa de estudio. Para cada tem se dan a conocer las causas posibles por las que los estudiantes lo respondieron incorrectamente. Se presenta la actividad sugerida, los recursos con los que se puede desarrollar, la descripcin de la misma y en algunos casos se brinda informacin para enriquecer el desarrollo del contenido. Las actividades de refuerzo por asignatura debern trabajarse, prioritariamente, con el grupo de estudiantes que obtuvieron menos aciertos en la prueba; aun cuando las actividades propuestas pueden ser aplicadas a todo el grupo.
Actividades de Refuerzo para Ciencias Naturales
Pgina 3
Ministerio de Educacin Direccin Nacional de Educacin
Plantilla para registrar las respuestas correctas Despus de aplicada cada prueba, el docente responsable de la asignatura y de la seccin, deber revisar las respuestas dadas por los estudiantes a cada tem; para el registro de las respuestas correctas se propone una plantilla por asignatura, en la que se identifica el nmero del tem y el literal que contiene la respuesta correcta; registrar slo las respuestas correctas; de esta manera tendr un diagnstico del desempeo de cada estudiante y del grupo. En la seccin podr identificar cules tems fueron respondidos correctamente en mayor o menor cantidad por los estudiantes.
3. Desarrollo de la Evaluacin Para que los resultados de las pruebas reflejen las dificultades o las fortalezas de los estudiantes, se sugiere desarrollar una asignatura cada da, y que sta se realice simultneamente en todas las secciones de segundo ao de bachillerato de la institucin; el tiempo mximo estimado para cada prueba es de 90 minutos. La evaluacin deber realizarse en la segunda semana del mes de febrero. Se deben administrar las pruebas dando indicaciones claras y de forma imparcial en un ambiente que genere confianza; es decir, evitar acciones que causen tensin en los estudiantes, ya que ello podra influenciar negativamente sobre el trabajo de stos en la prueba. Los estudiantes debern marcar sus respuestas en cada cuadernillo; para lo cual se debe encerrar en un crculo la letra de la opcin que contiene la respuesta correcta. El docente debe explicar a los estudiantes que la prueba no es para asignarles una nota y debern motivarlos para que realicen su mayor esfuerzo al responder todos los tems. Las indicaciones para la aplicacin de la prueba deben ser respetadas, Si un estudiante pide informacin adicional, no se le deben dar elementos de respuesta, ni informacin susceptible de orientar su respuesta. Si la indicacin no es comprendida, ser suficiente solicitar que relea la indicacin o la pregunta. La prueba debe ser realizada individualmente, para que el propsito de diagnstico de sta, realmente sea alcanzado.
Actividades de Refuerzo para Ciencias Naturales
Pgina 4
Ministerio de Educacin Direccin Nacional de Educacin
4. Proceso de registro de las respuestas dadas por los estudiantes en cada prueba Despus de la aplicacin de las pruebas, los docentes proceden al registro de las respuestas correctas de los estudiantes. Esta fase es parte integral de la evaluacin porque permite el anlisis de las respuestas y conduce a la reflexin y valoracin de decisiones pedaggicas que respondan a cada contexto. El docente responsable de la asignatura deber realizar el registro de las respuestas correctas, para ello utilizar la plantilla propuesta en la que se indica el nmero del tem y el literal que contiene la respuesta correcta de cada tem de la asignatura. Cuando existan errores o ausencias de respuesta muy frecuentes en una misma seccin, es importante verificar si los elementos referidos fueron estudiados y como se procedi. El docente podr as establecer un diagnstico y juzgar si es necesario o no desarrollar procedimientos de ayuda para algunos estudiantes. Revisar en los resultados de cada estudiante, cules tems no respondi correctamente para determinar cules contenidos son los que requieren de refuerzo acadmico, de esta manera se pueden formar grupos con dificultades en comn para poder atenderlos con las actividades sugeridas. Asimismo, es importante identificar los puntos fuertes de cada uno con el propsito de poder tomarlos como apoyo en procesos de tutora con otros estudiantes que tengan dificultades. Los resultados globales no tienen un significado importante, puesto que lo que se debe destacar no es cuntos respondi, si no cules no fueron respondidos correctamente, para planificar y orientar las actividades de refuerzo acadmico. Estos resultados conciernen a grupos de alumnos y pueden constituir referencias, pero la dimensin diagnstica de las evaluaciones toma toda su pertinencia cuando el docente se interesa en el alumno en toda su singularidad. Revisar las propuestas de actividades de refuerzo acadmico que se sugieren para los tems, si estn de acuerdo con stas, desarrollarlas con los estudiantes que lo requieran; si usted tiene experiencia con otro tipo de actividades que le han resultado exitosas para el dominio de ciertos contenidos, puede aplicarla en su clase y compartirla con otros docentes en crculos de estudio.
Actividades de Refuerzo para Ciencias Naturales
Pgina 5
Ministerio de Educacin Direccin Nacional de Educacin
Actividades de refuerzo acadmico sugeridas para que los estudiantes superen las deficiencias mostradas en el desarrollo de los tems de la prueba
ACTIVIDAD SUGERIDA PARA EL TEM NMERO 1 y 2 Bloque de contenidos: Fsica. Contenidos: Magnitudes Fsicas. Indicador de logro: 1.4 Indaga, identifica y describe con inters las magnitudes fsicas fundamentales y derivadas.
Causas posibles por las que los estudiantes no contestaron bien el tem 1. Confusin entre las magnitudes fsicas fundamentales con las magnitudes derivadas. 2. Falta claridad en la interpretacin de las unidades correspondientes a las diferentes magnitudes fsicas. 3. Confusin en la aplicacin de la frmula correspondiente para el problema planteado.
Actividad 1: Identifiquemos y diferenciemos magnitudes fsicas fundamentales y derivadas
Recursos para el desarrollo de la actividad Tablas con magnitudes
Descripcin de los pasos para el desarrollo de la actividad 1. Realizar exploracin de presaberes por medio de lluvia de ideas. 2. Organizar a los estudiantes en equipos de trabajo. 3. Proporcionar a los estudiantes informacin escrita y tablas con las magnitudes fundamentales y derivadas. 4. Pedir a los estudiantes que con la informacin proporcionada, magnitudes fundamentales y derivadas. identifiquen las
Actividades de Refuerzo para Ciencias Naturales
Pgina 6
Ministerio de Educacin Direccin Nacional de Educacin
5. En equipos de trabajo, asignarles tareas de medicin de algunos objetos en el aula (puertas, ventanas, libreras, cuadernos, libros, escritorios, pupitres, entre otros) y algunas situaciones cotidianas (velocidad de un mvil, el desplazamiento de un atleta, entre otros) pedirle a cada equipo que utilice los dos tipos de magnitudes para realizar la medicin. 6. Permitir que los estudiantes presenten sus resultados y los socialicen con el pleno. Referencias tericas Magnitudes fundamentales
Algunas magnitudes derivadas
Fuente de informacin http://raulcaroy.iespana.es/FISICA/03%20magnitudes%20fisicas%20i.pdf http://www.molwick.com/es/experimentos/108-magnitudes-fisicas.html
Actividades de Refuerzo para Ciencias Naturales
Pgina 7
Ministerio de Educacin Direccin Nacional de Educacin
ACTIVIDAD SUGERIDA PARA EL TEM NMERO 3 y 4 Bloque de contenidos: Fsica. Contenidos: Sistema Internacional de Unidades. Indicador de logro: 1.10 Identifica y describe con seguridad las unidades bsicas y derivadas del SI.
Causas posibles por las que los estudiantes no contestaron bien el tem: 1. Desconocimiento de las unidades de medicin del sistema internacional. 2. Confusin en diferenciar las unidades fundamentales de la masa en el SI y el sistema ingls. 3. Desconocimiento de las unidades del sistema CGS. 4. Poca claridad con el valor equivalente entre los diferentes sistemas de medicin.
Actividad 1: Realicemos conversiones
Recursos para el desarrollo de la actividad Tablas referidas a las equivalencias y conversiones de los sistemas: internacional, ingls y CGS Descripcin de los pasos para el desarrollo de la actividad 1. Organizar a los estudiantes en equipos de trabajo. 2. Proporcionar a los estudiantes informacin escrita y tablas de equivalencias y conversiones. 3. Pedir a los estudiantes que con la informacin proporcionada, realicen algunos ejercicios propuestos, puede realizar otros que considere necesarios. 4. Permitir que los estudiantes presenten sus resultados y los socialicen con el pleno.
Actividades de Refuerzo para Ciencias Naturales
Pgina 8
Ministerio de Educacin Direccin Nacional de Educacin
Referencias tericas a) Equivalencias entre diferentes unidades de longitud
b) Equivalencias entre diferentes unidades de masa
Actividades de Refuerzo para Ciencias Naturales
Pgina 9
Ministerio de Educacin Direccin Nacional de Educacin
/907
Actividades de Refuerzo para Ciencias Naturales
Pgina 10
Ministerio de Educacin Direccin Nacional de Educacin
Actividad 2: Reconozcamos nuestras unidades de medicin
Recursos para el desarrollo de la actividad Textos referidos a las equivalencias y conversiones de los sistemas: internacional, ingls y CGS Tarjetas con unidades y equivalencias
Descripcin de los pasos para el desarrollo de la actividad 1. Organizar a los estudiantes en equipos de trabajo. 2. Entregar a los estudiantes informacin escrita acerca de los sistemas de medicin: internacional, ingls y CGS. 3. Disear tarjetas con los nombres de las unidades de medicin de los diferentes sistemas. 4. Definir a cada equipo un sistema para identificar las unidades respectivas. 5. Dar a los estudiantes tarjetas con las diferentes unidades de cada sistema, con los nombres al azar para que ellos busquen entre los equipos hasta identificar las que corresponden al sistema de medidas que se les ha asignado. 6. Permitir que los estudiantes describan las caractersticas de sus unidades de medicin, frecuencia de uso en la vida cotidiana, contextos en los que se utilizan, entre otros. 7. Realizar una presentacin con cada equipo acerca de las unidades de medicin y sus caractersticas. 8. Esta actividad puede adecuarla o hacer variantes como un domin en el que se reconozca la abreviatura de cada unidad de medicin, la equivalencia o el nombre.
Actividades de Refuerzo para Ciencias Naturales
Pgina 11
Ministerio de Educacin Direccin Nacional de Educacin
Referencias tericas
metro cbico
m3
kilogramo
kilmetro
Newton
libra
Pie
metro metro cbico m3
kg
lb
Fuente de informacin http://raulcaroy.iespana.es/FISICA/03%20magnitudes%20fisicas%20i.pdf http://www.molwick.com/es/experimentos/108-magnitudes-fisicas.html Mdulo de Ciencias Naturales, EDUCAME, Ministerio de Educacin, Pg. 135-138, 2005
Actividades de Refuerzo para Ciencias Naturales
Pgina 12
Ministerio de Educacin Direccin Nacional de Educacin
ACTIVIDAD SUGERIDA PARA EL TEM NMERO 5 y 6 Bloque de contenidos: Fsica. Contenidos: Equivalencias y conversiones. Indicador de logro: 1.11 Resuelve con persistencia problemas de equivalencias y conversiones de unidades fsicas aplicando correctamente el anlisis dimensional.
Causas posibles por las que los estudiantes no contestaron bien el tem 1. Desconocimiento del proceso correcto de conversin de unidades, al realizar las operaciones. 2. Confusin al utilizar diferentes magnitudes y hacer conversiones a otras unidades.
Actividad 1: Juego de memoria con las equivalencias
Recursos para el desarrollo de la actividad Tablas de equivalencias y conversiones de los sistemas: internacional, ingls y CGS. Cartoncillo, cartn, tijeras.
Descripcin de los pasos para el desarrollo de la actividad 1. Organizar a los estudiantes en equipos de trabajo. 2. Dar a los estudiantes copias de las tablas de conversin con las unidades fundamentales y derivadas. 3. Disear tarjetas sobre cartoncillo, que servirn para identificar las unidades y equivalencias. (Ver modelo). 4. Pedir a los estudiantes que en equipo coloquen sobre la mesa las tarjetas al reverso permitir turnos para que se formen las parejas correspondientes de las equivalencias en los diferentes sistemas; ste puede tener variantes de acuerdo con la creatividad del estudiante y del docente. Al final del juego, el ganador ser el estudiante que haya logrado obtener mayor nmero de tarjetas.
Actividades de Refuerzo para Ciencias Naturales
Pgina 13
Ministerio de Educacin Direccin Nacional de Educacin
Referencias tericas
1 metro
1 000 mm
1 kilmetro
1 000 m
1 litro
1 000 ml
1 pie
0.3048 m
1 kilogramo
1 000 g
Actividades de Refuerzo para Ciencias Naturales
Pgina 14
Ministerio de Educacin Direccin Nacional de Educacin
Actividad 2: Realicemos conversiones
Recursos para el desarrollo de la actividad Listado de frmulas a utilizar en los ejercicios de conversin Guas de trabajo con ejercicios de conversin Descripcin de los pasos para el desarrollo de la actividad 1. Organizar a los estudiantes en equipos de trabajo. 2. Entregar a los estudiantes guas de trabajo con ejercicios de conversin. 3. Orientar a los estudiantes para que obtengan la respuesta al problema que se les plantea, permitirles que utilicen diferentes caminos para resolver el ejercicio. 4. Dar la oportunidad a los estudiantes que se equivoquen o que consulten como equipo. 5. Pedir a los estudiantes que presenten las diferentes formas en las que han resuelto los ejercicios. Referencias tericas
Actividades de Refuerzo para Ciencias Naturales
Pgina 15
Ministerio de Educacin Direccin Nacional de Educacin
El dimetro de un tubo es de 5 pulgadas, a cuntos centmetros equivale esa medida?
12.7 cm
3 lb,
3 lb
Fuente de informacin Mdulo 2 de Ciencias Naturales. MINED Edcame, El Salvador, 2005.Pgs. 131-132 http://raulcaroy.iespana.es/FISICA/03%20magnitudes%20fisicas%20i.pdf
Actividades de Refuerzo para Ciencias Naturales
Pgina 16
Ministerio de Educacin Direccin Nacional de Educacin
ACTIVIDAD SUGERIDA PARA EL TEM NMERO 7 y 8 Bloque de contenidos: Fsica. Contenidos: Errores e incertezas en las mediciones. Indicador de logro: 1.12 Explica con claridad y esmero los tipos de errores instrumentales y personales que se pueden cometer al realizar mediciones directas.
Causas posibles por las que los estudiantes no contestaron bien el tem 1. 2. No logran diferenciar entre un error personal y uno instrumental. Confunde las causas del error instrumental con el personal.
Actividad 1: Conozcamos y diferenciemos los errores instrumentales de los personales
Recursos para el desarrollo de la actividad Texto cientfico que aborde los errores personales e instrumentales Fotografas o imgenes con los diferentes tipos de error personales e instrumentales Descripcin de los pasos para el desarrollo de la actividad 1. Realizar exploracin de presaberes por medio de lluvia de ideas: Qu tipo de errores podemos cometer al hacer mediciones? Cules son los errores ms frecuentes que se cometen al medir? Cul es la diferencia entre un error instrumental y un error personal? Organizar a los estudiantes en equipos de trabajo. Presentar imgenes o fotografas que muestren los diferentes tipos de error en las mediciones. Proporcionar a los estudiantes informacin escrita referida a los tipos de error al medir. Pedir a los estudiantes que con la informacin proporcionada, construyan un cuadro donde se establezcan las caractersticas de los dos tipos de errores mencionados (Ver modelo).
2. 3.
4.
5.
Actividades de Refuerzo para Ciencias Naturales
Pgina 17
Ministerio de Educacin Direccin Nacional de Educacin
Errores instrumentales y personales
Tipos de error Caractersticas Error Instrumental Error Personal
6. Organizar a los estudiantes para que en plenaria discutan sus resultados.
Actividad 2: Errores personales e instrumentales
Recursos para el desarrollo de la actividad Texto cientfico que aborde los errores personales e instrumentales Descripcin de los pasos para el desarrollo de la actividad 1. Pedir a los estudiantes que lean el texto y que comenten las causas posibles de los errores en el proceso de la medicin. 2. Organizar a los estudiantes en equipos de trabajo, asignarles tareas de medicin de diferentes superficies, (puertas, ventanas, escritorios, cancha de basket, u otros) darle a cada equipo un instrumento diferente y que midan con cada instrumento los mismos objetos o superficies (cinta mtrica de albailera, cinta mtrica de sastrera, metro de madera, u otros). 3. Pedir que los estudiantes comparen sus resultados y que expresen sus opiniones respecto a los resultados de acuerdo a los instrumentos utilizados. 4. Pedir que respondan en plenaria A qu se deben los distintos resultados para una misma superficie?
Actividades de Refuerzo para Ciencias Naturales
Pgina 18
Ministerio de Educacin Direccin Nacional de Educacin
Referencias tericas
Actividades de Refuerzo para Ciencias Naturales
Pgina 19
Ministerio de Educacin Direccin Nacional de Educacin
Fuente de informacin http://raulcaroy.iespana.es/FISICA/03%20magnitudes%20fisicas%20i.pdf http://www.molwick.com/es/experimentos/108-magnitudes-fisicas.html
Actividades de Refuerzo para Ciencias Naturales
Pgina 20
Ministerio de Educacin Direccin Nacional de Educacin
ACTIVIDAD SUGERIDA PARA EL TEM NMERO 9 y 10
Bloque de contenidos: Fsica.
Contenidos: Error e incerteza en las medidas.
Indicador de logro: 1.14 Realiza con exactitud clculos de incertezas absolutas y relativas en medidas directas e indirectas.
Causas posibles por las que los estudiantes no contestaron bien el tem 1. No saben interpretar los datos de un problema y cmo estos deben ser trasladados a una expresin matemtica. 2. Al momento de aplicar la frmula a un ejercicio se confunden y colocan los datos del ejercicio en variables de la frmula que no les corresponde. 3. Se confunden al querer interpretar la incerteza que acompaa a una medida, en algunos casos por no tener claro el concepto.
Actividad 1: Cmo debe ser expresada la incerteza en una medida?
Recursos para el desarrollo de la actividad Textos que expliquen la teora y el desarrollo de ejercicios sobre incertezas. Descripcin de los pasos para el desarrollo de la actividad 1. Pedir a los estudiantes que lean el texto. 2. Organizar equipos de trabajo para que discutan el contenido textual. 3. Realizar una serie de preguntas orientadas a explorar el grado de compresin que los estudiantes han hecho del texto. 4. Completar el cuadro con los datos requeridos. 5. Responder las preguntas que aparecen al final y elaborar una plenaria con el objetivo de discutir y analizar las respuestas de cada uno de los grupos de trabajo.
Actividades de Refuerzo para Ciencias Naturales
Pgina 21
Ministerio de Educacin Direccin Nacional de Educacin
Referencias tericas La incerteza absoluta ( ), no nos da suficiente informacin en cuanto a la calidad de
una medida, pues la medida de 2 cantidades una grande y otra pequea, que tengan la misma incerteza absoluta, tienen diferente calidad; es mejor la calidad de la cantidad grande.
Cuando la incerteza se expresa relacionada con el tamao de la cantidad medida recibe el nombre de incerteza relativa, que s indica en forma completa la calidad de la medida. Esta incerteza relativa puede ser unitaria o porcentual.
El cociente Y la expresin Ejemplo N0 1
representa la incerteza relativa unitaria. nos da la incerteza relativa porcentual.
Se ha medido la masa de un cuerpo y el resultado se escribe m= (24.7 En esta expresin: El valor encontrado es 24.7 kg La cifra dudosa es 7 La incerteza absoluta es 0.3 kg La incerteza relativa unitaria es 0.012146 La incerteza relativa porcentual es 1.21 %
0.3) kg
Ejemplo N0 2 5 comerciantes pesan con el mismo instrumento una libra de azcar. Obtienen los siguientes resultados: Medida 1 2 441.3 3 439.9 4 440.2 5 438.9
Peso (g) 440.2
Con los resultados anteriores se calcula la media aritmtica, la cual representar el mejor valor. 440.2 g + 441.3 g+ 439.9 g +440.2 g +438.9 g= 440.1 g
Actividades de Refuerzo para Ciencias Naturales
Pgina 22
Ministerio de Educacin Direccin Nacional de Educacin
Para determinar la incerteza a cualquiera de estas medidas, se aplicara la siguiente expresin matemtica: i=XXI. Donde: X=mejor valor; Xi=valor de cada medida Ejemplo: determine la incerteza (i) para la medida 440.2g X=440.1 g Xi=440.2g Sustituyendo: i=440.1440.2=0.1g El clculo anterior permite expresar la primera medida de una forma mas refinada 440.20.1g. La incerteza 0.1 nos indica el nivel de confianza o de duda de la medida. Es sumamente probable que la medida exacta este comprendida en el intervalo 440 .0440.2g. Tomando como base el ejemplo anterior, determine la incerteza a las dems medidas y establezca el intervalo en los que pueden estar comprendidos. Medida 440.2 g 441.3 g 439.9 g 440.2 g 438.9 g Incerteza 0.1 Expresin 440.20.1 Intervalo 440440.2
En el caso de la incerteza absoluta es indispensable que el nmero de decimales significativos en la misma coincidan con los de la medida. Responder las siguientes preguntas: 1. Cul es la diferencia entre un error y una incerteza? Explique. 2. Cmo se explica el hecho de que el resultado de varias mediciones de la misma magnitud no proporcione siempre los mismos valores? 3. Si se indica que el error probable en la medida de Y es diferencia? Qu puede concluirse? Fuente de informacin Texto propio complementado con informacin de otros textos. 0.001, es significativa la
Actividades de Refuerzo para Ciencias Naturales
Pgina 23
Ministerio de Educacin Direccin Nacional de Educacin
ACTIVIDAD SUGERIDA PARA EL TEM NMERO 11 Bloque de contenidos: Fsica. Contenidos: Cada libre y tiro vertical, un caso especial del MRUV (movimiento rectilneo uniforme acelerado/ variado). Indicador de logro: 2.1 Investiga, experimenta, analiza, explica y resuelve problemas del movimiento de cada libre y tiro vertical.
Causas posibles por las que los estudiantes no contestaron bien el tem 1. 2. Falta de claridad con el concepto de aceleracin constante. No se consideraron los valores crecientes de la gravedad a la izquierda del esquema y cmo stos afectan la velocidad del objeto. 3. No se consider que el cuerpo, justo al tocar tierra, tiene una velocidad final superior a la inicial, puesto que el movimiento de cada libre es uniformemente acelerado y la velocidad aumenta cada segundo.
Actividad 1: El tiro vertical y sus componentes
Recursos para el desarrollo de la actividad 3 Pelotas de baloncesto 1 Silbato Pizarra y yeso Descripcin de los pasos para el desarrollo de la actividad 1. Pedir a los estudiantes que lean el siguiente prrafo antes de realizar el ejercicio prctico. Al igual que la cada libre, el tiro vertical es un movimiento sujeto a la aceleracin de la gravedad, slo que en este caso la aceleracin se opone al movimiento inicial del objeto. El tiro vertical comprende subida, bajada de los cuerpos u objetos considerando lo siguiente: a) Nunca la velocidad inicial es igual a 0. b) Cuando el objeto alcanza su altura mxima, su velocidad en este punto es 0. Mientras que el objeto se encuentra de subida el signo de la V es positivo; la V es 0 a su altura mxima cuando comienza a descender su velocidad ser negativa.
Actividades de Refuerzo para Ciencias Naturales
Pgina 24
Ministerio de Educacin Direccin Nacional de Educacin
c) Si por ejemplo el objeto tarda 2s en alcanzar su altura mxima, tardar 2s en regresar a la posicin original, por lo tanto el tiempo que permaneci en el aire el objeto es de 4s. d) Para la misma posicin del lanzamiento, la velocidad de subida es igual a la velocidad de bajada. 2. Realizar el siguiente ejercicio prctico. a) El grupo se desplazar a un espacio libre, de preferencia una cancha de baloncesto. Luego pasarn al frente tres voluntarios, los que se colocarn con al menos dos metros de distancia entre s. A cada uno se le proporcionar una de las pelotas. b) El resto del grupo se colocar frente a los tres jugadores. Estos, sostendrn las bolas con las dos manos a la altura del rostro. Al toque del silbato, lanzarn las bolas hacia arriba y las dejarn caer al suelo. c) Los espectadores tendrn por objetivo observar el comportamiento de las bolas: cmo alcanzan una altura mxima y luego caen. d) El ejercicio se puede repetir varias veces insistiendo en tres hechos importantes mediante preguntas: a) al subir, las pelotas tienen una velocidad inicial. Quin proporciona dicha velocidad? (en cada caso sta ser diferente debido a la complexin fsica de los tres jugadores, lo largo de sus brazos, si saltaron o no al propulsar la bola, etc.); b) al alcanzar la mxima altura, justo antes de comenzar a descender, la velocidad final de los balones es cero, por qu?; c)quin propulsa las pelotas hacia el suelo? (Evidentemente la accin de la gravedad que invariablemente ser de 9.8 m/s2). En qu momento comienza a actuar sobre los balones? e) El ejercicio puede proseguir alternando los papeles de jugadores y observadores. Lo importante es que todos y todas adviertan el impulso inicial dado a las bolas y la accin de la gravedad que les impele caer. f) Para terminar de comprender lo sucedido a cada bola se acostar hipotticamente la situacin de tiro vertical modelando lo que ocurre con los balones sobre el piso de la cancha. As: V0 (+) a = (-) 9.8 m/s2
V0 (+)
g) Lo importante es que se comprenda que la pelota se eleva con una determinada velocidad inicial y se va frenando debido a una aceleracin negativa, de manera semejante a como ocurre con el movimiento rectilneo uniformemente variado.
Actividades de Refuerzo para Ciencias Naturales
Pgina 25
Ministerio de Educacin Direccin Nacional de Educacin
3. Analizar la siguiente explicacin y el esquema. El estudiante iniciar estableciendo un marco de referencia que permita descomponer lo sucedido a cada baln. Esto implica tomar un eje vertical Y, que podr trazarse apuntando para arriba o para abajo segn ms convenga. Y
Y0
V0 (+) g (-)
a) Sobre dicho esquema debern marcarse los sentidos de la velocidad inicial (V0) y de la gravedad (g). Si V0 y g apuntan en el mismo sentido del eje, Y ser positiva (+). Si alguna va al revs del eje Y ser negativa (-). b) Luego se introducir el anlisis algebraico de la situacin introduciendo las ecuaciones horarias y la ecuacin complementaria. c) Se realizarn ejemplos de aplicacin de dichas ecuaciones, otorgndole valores a la velocidad inicial, altura desde la que descendi el baln, etc.
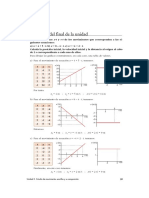
Ejemplo: Un estudiante tira una piedra hacia arriba con una velocidad inicial de 40 m/s. Calcular: a) Qu tiempo tarda en llegar a la altura mxima b) Cul es la altura mxima c) Trazar los grficos de posicin, velocidad y aceleracin en funcin del tiempo.
Actividades de Refuerzo para Ciencias Naturales
Pgina 26
Ministerio de Educacin Direccin Nacional de Educacin
Lo primero ser trazar un esquema de lo que plantea el problema. Elijo mi sistema de referencia. En este caso lo considerar positivo para arriba, por lo tanto la gravedad tendr un valor negativo hacia abajo.
Reemplazar los datos en las ecuaciones horarias, tomando el sistema de referencia para arriba (con el valor de g negativo). Aproximar el valor de la gravedad a 10 m/s2. Poner el sistema de referencia exactamente en la mano del estudiante al momento de lanzar la piedra. Y = y0 + Voy t + g t2 Vfy = Voy + g t Luego: Y = 0 + 40 m/s t + (-10m/s2) t2 Vf = 40 m/s + (-10 m/s2) t Cuando el cuerpo llega a la altura mxima su velocidad es cero. Por lo tanto, al reemplazar Vf por cero en la ecuacin de la velocidad, me queda: 0 = 40 m/s + (-10 m/s2) t max Al despejar t max: t max = -40 m/s / -10 m/s2 t max = 4 seg Reemplazando t mxima:
max
= 4 segundos en la ecuacin de la posicin, calculo la altura Y max = (40 m/s) (4s) + (-10 m/s2) (4s)2 Y max = 80 m
Para construir los grficos puedo dar valores o puedo hacerlos en forma cualitativa. Un grfico cualitativo quiere decir que indica la forma en la que ocurre el evento sin dar todos los valores exactos. En este caso quedan as:
Actividades de Refuerzo para Ciencias Naturales
Pgina 27
Ministerio de Educacin Direccin Nacional de Educacin
Fuente de informacin Texto propio complementado con informacin de otros textos. Wilson, J.D. (2003) Fsica, Editorial PEARSON Educacin, Mxico, P. 84-85 ACTIVIDAD SUGERIDA PARA LOS ITEMS 12 Y 13 Bloque Fsica de contenido: Contenidos: Cada libre y tiro vertical, un caso especial del MRUV (movimiento rectilneo uniforme acelerado/ variado). Indicador de logro: 2.1 Investiga, experimenta, analiza, explica y resuelve problemas del movimiento de cada libre y tiro vertical.
Causas posibles por las que los estudiantes no contestaron bien el tem 1. No se consider el exponente de t, por lo tanto no se sac la raz cuadrada de 25. 2. Error al despejar la ecuacin y en lugar de dividir 125 entre 4.9, los sum. 3. Error al despejar 4.9, pues si bien pas a dividir 125, a la vez, le cambi de signo positivo a negativo; es decir, no pudo sacarle raz cuadrada a un cociente negativo. 4. Confundi la altura mxima alcanzada por la piedra, con la velocidad de la piedra a los 4 segundos. 5. No interpret correctamente el grfico y pens que el eje X representaba la velocidad de la piedra en lugar del tiempo transcurrido. 6. No comprendi el esquema, escogiendo el tiempo que la piedra tard en caer (8 segundos), como si se tratara de la velocidad cuando alcanz su mxima altura.
Actividades de Refuerzo para Ciencias Naturales
Pgina 28
Ministerio de Educacin Direccin Nacional de Educacin
Actividad 1: Experimentando con cada libre
Recursos para el desarrollo de la actividad 2 Pelotas de tenis, un clavo pequeo, una tijera Un conjunto de canicas (chibolas) Pizarra y yeso
Descripcin de los pasos para el desarrollo de la actividad 1. Con mucho cuidado y con la ayuda de un clavo y unas tijeras, se har un agujero en una de las pelotas de tenis (ver figura A).
Figura A 2. Luego se introducir un buen nmero de canicas dentro de la pelota, de tal forma que su peso aumente en relacin con la otra pelota. De esta manera se tendrn dos pelotas del mismo tamao pero de diferente peso (ver figura B).
Figura B
Actividades de Refuerzo para Ciencias Naturales
Pgina 29
Ministerio de Educacin Direccin Nacional de Educacin
3. Un voluntario pasar al frente y tomar una pelota en cada mano, extendiendo hacia arriba sus brazos. Luego, las dejar caer simultneamente sobre una mesa de madera o de metal. El ruido que stas producen cuando golpeen la mesa servir para identificar si caen al mismo tiempo o si una cae primero que la otra (ver figura C).
Figura C 4. 5. El grupo advertir que ambas pelotas con diferente peso caen al mismo tiempo. La experiencia podr relacionarse con el experimento de Galileo Galilei que consisti en dejar caer varias esferas de distinto peso desde lo alto de la torre de Pisa para demostrar que estas llegaban al suelo simultneamente, hecho con el cual desafi el pensamiento aristotlico imperante en su poca. 6. Deber enfatizarse el papel de la aceleracin de la gravedad en la cada simultnea de las pelotas y qu significa que sea constante. 7. Luego se proceder a elaborar grficos en el pizarrn para esquematizar lo que ocurri a las pelotas de tenis y a partir de dichos esquemas, se relacionar la cada libre con el Movimiento Rectilneo Uniformemente Variado (MRUV). 8. Finalmente se introducir el tratamiento algebraico del tema, estableciendo las ecuaciones a utilizar en los problemas numricos de cada libre y se desarrollarn ejercicios de aplicacin.
Actividades de Refuerzo para Ciencias Naturales
Pgina 30
Ministerio de Educacin Direccin Nacional de Educacin
Hacer un listado de situaciones cotidianas en las cuales se pueda identificar cualquiera de estos dos tipos de movimiento (cada libre o tiro vertical). Luego identificar las diferencias existentes entre ellos, si es que las hay, respecto al eje de desplazamiento o la aceleracin que acta sobre los cuerpos. Por ejemplo, un fruto que al madurar se desprende del rbol donde ha crecido, qu tipo de movimiento experimenta? cul es el tipo de movimiento que experimenta una piedra lanzada hacia arriba?
Ejercicio numrico de cada libre Una persona est parada a 20 m de altura. Calcular qu tiempo tarda y con qu velocidad toca el suelo una piedra si la persona: a) La deja caer b) La tira para abajo con V0 = 10 m/s Inicialmente se hace un esquema de la situacin descrita en el problema: el tipo de la terraza que gusta de tirar piedras.
Para la situacin a) donde la persona deja caer la piedra. Se elige el sistema de referencia y se marca V0 y g con su signo. En este caso V0 vale cero porque la piedra se deja caer.
Actividades de Refuerzo para Ciencias Naturales
Pgina 31
Ministerio de Educacin Direccin Nacional de Educacin
Se reemplazan por los valores. Se calcula todo con un valor aproximado de la gravedad = 10 m/s2 Las ecuaciones del movimiento quedan as:
El tiempo que la piedra tarda en caer se despeja de la primera ecuacin. Cuando la piedra toca el suelo su posicin es y = 0. Entonces en la primera ecuacin se reemplaza y por cero. As:
2 Seg.
Reemplazando este tiempo en la segunda ecuacin se obtiene la velocidad con que toca el piso:
Actividades de Refuerzo para Ciencias Naturales
Pgina 32
Ministerio de Educacin Direccin Nacional de Educacin
El signo negativo de Vf indica que la velocidad va en sentido contrario al eje Y. Para la situacin b) cuando el individuo tira la piedra para abajo con V 0 = 10 m/s Se toma el mismo sistema de referencia que antes: eje y positivo vertical hacia arriba. Ahora la velocidad inicial es negativa, porque va en sentido contrario del eje Y.
De forma similar a la anterior, cuando la piedra toca el suelo, y = 0. Entonces:
Resulta una ecuacin cuadrtica. A continuacin se reemplazan los valores de a, b y c en la frmula de la ecuacin cuadrtica.
Actividades de Refuerzo para Ciencias Naturales
Pgina 33
Ministerio de Educacin Direccin Nacional de Educacin
La primera solucin se tacha porque un valor negativo del tiempo no tiene sentido en Fsica. As que se trabajar con la segunda solucin, 1,236 segundos, que se reemplaza en la otra ecuacin: Vf = V0 + g t Se calcula la velocidad final, que equivaldr al momento en el que la piedra toca el piso. Vf = -10 m/s 10 m/s2. 1,236 seg Vf = -22,36 m/s Velocidad final
Fuente de informacin Experimento adaptado de: http://www.correodelmaestro.com/anteriores/2008/marzo/nosotros142.htm Alvarenga lvares, B. (1983) Fsica General con Experimentos Sencillos, Editorial HARLA, Mxico, 3 Edicin, P. 69-74.
Actividades de Refuerzo para Ciencias Naturales
Pgina 34
Ministerio de Educacin Direccin Nacional de Educacin
ACTIVIDAD SUGERIDA PARA LOS ITEMS 14 y 15 Bloque de contenido: Fsica Contenidos: Movimiento parablico Indicador de logro: 2.2 Investiga, experimenta, analiza y describe correctamente el movimiento parablico.
Causas posibles por las que los estudiantes no contestaron bien el tem 1. No se consider que la rotacin de la pelota se origina en torno a un punto central y que por lo tanto sigue la trayectoria de una circunferencia y no de una parbola. 2. No se observ que la pelota al girar describe una circunferencia, hecho caracterstico del movimiento circular uniforme. 3. Se omitieron dos hechos importantes: en primer lugar el clavadista cae slo bajo accin del campo gravitatorio sin verse afectado en direccin horizontal; en segundo lugar, la pelota al girar lo hace describiendo una circunferencia, no una parbola. 4. No se consider que en P1 interviene la velocidad constante, dada por Vx y la aceleracin de la gravedad, determinada por Vy. 5. Se desconoce que en el movimiento parablico intervienen dos componentes: la velocidad constante dada por Vx y la aceleracin de la gravedad, dada por Vy. 6. Se err al considerar que cuando el paquete toca el suelo lo hace nicamente por accin de la velocidad constante y despreci la aceleracin dada por la gravedad.
Actividad 1: Analicemos el movimiento de los proyectiles
Recursos para el desarrollo de la actividad 1 catapulta con resorte cuya inclinacin pueda regularse Balines o canicas, papel carbn Descripcin de los pasos para el desarrollo de la actividad 1. Solicitar a los estudiantes que visiten el siguiente sitio web: http://www.educaplus.org/movi/4_3tparabolico.html
Actividades de Refuerzo para Ciencias Naturales
Pgina 35
Ministerio de Educacin Direccin Nacional de Educacin
All debern: a) Leer la definicin de tiro parablico b) Practicar con la simulacin computarizada cambiando la velocidad y los valores del ngulo de lanzamiento. c) Tomar nota de las ecuaciones de aceleracin, velocidad y posicin, tanto para la componente X, como para la componente Y. 2. Pedir a los estudiantes que trabajen en equipo para realizar las experiencias. NOTA: la catapulta puede elaborarse utilizando un par de clips y una banda de hule, como se muestra en la siguiente figura:
Dicha catapulta se compone de dos partes. Por un lado el soporte y por el otro el contrapeso, que ser activado por una goma elstica.
Procedimiento A:
1. Montar el sistema mostrado tal como aparece en la siguiente figura, introduciendo la
canica en el tubo.
Catapulta con resorte
2. Soltar el mvil desde una altura h y medir el desplazamiento x obtenido. Para ello,
colocar una hoja de papel y sobre sta un papel carbn en el rea donde se espera que se produzca el impacto.
Actividades de Refuerzo para Ciencias Naturales
Pgina 36
Ministerio de Educacin Direccin Nacional de Educacin
Procedimiento B
3. Cambiar el ngulo de lanzamiento y observar cmo vara el alcance de la canica
para diferentes ngulos de disparo.
Anlisis de datos
4. De acuerdo al procedimiento A, llenar la siguiente tabla indicando la posicin en cm.
5. Encontrar la velocidad de lanzamiento del proyectil, fundamentando la respuesta. 6. Comprobar experimentalmente el mayor alcance de un proyectil, llenando la siguiente tabla a partir del procedimiento B. Indicar el alcance en cm.
7. Graficar el ngulo de tiro versus el alcance promedio. Discutir la grfica y comparar con lo esperado tericamente (considerar los errores de medida). 8. Encontrar la relacin entre el ngulo de lanzamiento y el alcance.
Actividades de Refuerzo para Ciencias Naturales
Pgina 37
Ministerio de Educacin Direccin Nacional de Educacin
9. Obtener la altura mxima del proyectil. Utilizar las siguientes ecuaciones: Movimiento horizontal Debido a que ax (la aceleracin en X) = 0 se tiene: Vx0 = constante X = Xo + Vxot
Movimiento vertical Debido a que el eje Y positivo tiene direccin vertical hacia arriba y el valor de la gravedad (ay = -g) es negativo, se tiene: Vy = Vy0 gt y = y0 + vy0t gt2 Vy2 = vy02 2g(y-y0) NOTA IMPORTANTE El experimento podr realizarse de forma virtual, utilizando el simulador de la pgina web indicada en las primeras lneas. Fuente de informacin Adaptado de http://fc.uni.edu.pe/lfgeneral/pdf/fi-02-cinematica-mov-parabolico.pdf
Actividades de Refuerzo para Ciencias Naturales
Pgina 38
Ministerio de Educacin Direccin Nacional de Educacin
ACTIVIDAD SUGERIDA PARA LOS ITEMS 16, 17 y 18 Bloque de contenido: Fsica Contenidos: Leyes del movimiento de Newton Indicador de logro: 3.1 Investiga, experimenta, analiza y explica con seguridad cada una de las leyes del movimiento de Newton.
Causas posibles por las que los estudiantes no contestaron bien el tem 1. Se confunde que el resultado de la accin de unos cuerpos sobre otros, es para determinar la relatividad del movimiento, cuando lo que provoca esta variable es alterar el movimiento. 2. Falta de comprensin en cuanto a la interpretacin de una ecuacin con relacin al enunciado de una ley. 3. Confusin al relacionar la masa de los cuerpos con la causa de la relatividad del movimiento. 4. Falta de anlisis del planteamiento y aplicacin de las leyes de Newton
Actividad 1: Las Leyes de Newton
Recursos para el desarrollo de la actividad Gua de trabajo Texto con el contenido de las leyes de Newton y ejemplos de la vida cotidiana. Anexo 1 Descripcin de los pasos para el desarrollo de la actividad 1. 2. 3. Organizar a los estudiantes en parejas. Entregar la gua de trabajo a cada estudiante. Dar lectura al texto sobre las leyes de Newton, interpretarlo y comentarlo en parejas. 4. Identificar en el texto los elementos claves que conforman cada una de las leyes de Newton. 5. Observar en los esquemas del anexo 1 ejemplos de las leyes de Newton y relacionarlos con ellas a partir de los elementos claves que identifican a cada ley.
Actividades de Refuerzo para Ciencias Naturales
Pgina 39
Ministerio de Educacin Direccin Nacional de Educacin
6. 7. 8.
Utilizar los esquemas y responder en el cuadro N 1 la informacin solicitada. Solicitar a 5 parejas que comenten lo analizado en los esquemas A, B, C, D, E y F. Hacer conclusiones sobre el trabajo realizado, en plenaria.
Referencias tericas PRIMERA LEY DE NEWTON O LEY DE LA INERCIA Todo cuerpo en reposo permanecer fuerza recta acte sobre l. Todo cuerpo continuar en su estado de reposo o de movimiento rectilneo uniforme, mientras no exista una fuerza externa capaz de cambiar dicho estado. Un cuerpo permanece en estado de reposo o de movimiento rectilneo uniforme a menos que una fuerza externa no equilibrada acte sobre l. En ausencia de la accin de fuerzas, un cuerpo en reposo continuar en reposo y uno en movimiento se mover en lnea recta y con velocidad constante. El movimiento es relativo, depende de quin sea el observador que describa el movimiento, as por ejemplo, para un pasajero de un tren, el interventor viene caminando lentamente por el pasillo del tren, mientras que para alguien que ve pasar el tren desde una estacin, el interventor se est moviendo a una gran velocidad. Se necesita, un sistema de referencia al cual referir el movimiento. SEGUNDA LEY DE NEWTON Establece que si una fuerza acta sobre un cuerpo de masa (m) ese cuerpo sufrir una aceleracin (a) en la fuerza aplicada (F) cuya magnitud es proporcional a la magnitud de la fuerza e inversamente proporcional a la masa. Esta Ley se refiere a los cambios en la velocidad que sufre un cuerpo cuando recibe una fuerza. Un cambio en la velocidad de un cuerpo efectuado en la unidad de tiempo, recibe el nombre de aceleracin. As, el efecto de una fuerza desequilibrada sobre un cuerpo produce una aceleracin. Cuanto mayor sea la magnitud de la fuerza aplicada, mayor ser la aceleracin. en reposo y un cuerpo en movimiento
continuar movindose en lnea recta a velocidad constante a menos que una
Actividades de Refuerzo para Ciencias Naturales
Pgina 40
Ministerio de Educacin Direccin Nacional de Educacin
Debemos recordar que aceleracin tambin significa cambios en la direccin del objeto en movimiento, independientemente que la magnitud de la velocidad cambie o permanezca constante; tal es el caso cuando se hace girar un cuerpo atado al extremo de una cuerda, pues sta aplica una fuerza al objeto y evita que salga disparado en lnea recta acelerndolo hacia el centro de la circunferencia.
TERCERA LEY DE NEWTON La tercera Ley del Movimiento de Newton es el principio de accin y reaccin. Este postula que a cada accin corresponde una reaccin igual y contraria. Es decir, si un cuerpo A ejerce una accin sobre un cuerpo B, el cuerpo B reacciona y ejerce una fuerza igual y contraria sobre el cuerpo A. Es importante insistir que las fuerzas de accin y reaccin actan sobre diferentes cuerpos. Nunca actan sobre el mismo cuerpo. Las fuerzas de accin y reaccin constituyen un par de fuerzas. Las fuerzas siempre ocurren en pares. Nunca existe una fuerza nica en ninguna situacin. Por todas partes se observa el cumplimiento de la tercera ley de Newton. Un pez empuja el agua hacia atrs con sus aletas y el agua a su vez empuja al pez hacia delante. El viento empuja contra las ramas de un rbol con lo que generan silbidos. Las fuerzas son interacciones entre cosas diferentes. Cada contacto requiere de por lo menos un do; no hay forma de que un cuerpo pueda ejercer una fuerza sobre nada. Las fuerzas, siempre ocurren en pares, y cada miembro del par es opuesto al otro. As, no se puede tocar sin ser tocado. ANEXO 1: Observe las figuras y responda en el cuadro N 1
1- Observar en los esquemas del anexo 1, ejemplos de las leyes de Newton y
relacionarlos con ellas a partir de los elementos claves que identifican a cada ley.
2- Trabajar con los esquemas respondiendo en el cuadro N 1 la informacin solicitada. 3- Pedir a 5 parejas que comenten lo analizado en los esquemas A, B, C, D, E y F.
Actividades de Refuerzo para Ciencias Naturales
Pgina 41
Ministerio de Educacin Direccin Nacional de Educacin
FIGURA A
FIGURA B
FIGURA C
Actividades de Refuerzo para Ciencias Naturales
Pgina 42
Ministerio de Educacin Direccin Nacional de Educacin
FIGURA D
FIGURA E
FIGURA E
FIGURA F
Cuadro N 1 Figura A B C D E F
Ley identificada
Caractersticas de la ley
Actividades de Refuerzo para Ciencias Naturales
Pgina 43
Ministerio de Educacin Direccin Nacional de Educacin
Actividad 2: Aplicacin de las Leyes de Newton
Recursos para el desarrollo de la actividad Gua de trabajo Texto con el contenido de las leyes de Newton y ejemplos de la vida cotidiana. Anexo 1 Descripcin de los pasos par el desarrollo de la actividad 1. Responder y discutir en pareja: a) Describir lo que observa en la figura A. b) c) d) Cmo se aplica la ley identificada en este ejemplo? .Explique. Qu significa la m1, m2 y la flecha en la figura D? Cmo se relaciona el significado de m1, m2 y la flecha de la figura D con la ley a la que corresponde esta? e) Cul es la condicin para que se aplique la ley identificada en las figuras B y E? f) Cul de las 3 leyes de Newton se hizo ms fcil identificar en las figuras y porqu? g) Describir 3 ejemplos de la vida diaria asociado a cada una de las tres leyes de Newton. 2. Presentar conclusiones en plenaria sobre el trabajo realizado. Fuente de informacin Resnick.Fsica.4 Edicin. CECSA, Mxico, Pgs. 157-163 WWW.itescam.edu.mx/principal/sylabus/fpdb/recursos/82647/.pp.
Actividades de Refuerzo para Ciencias Naturales
Pgina 44
Ministerio de Educacin Direccin Nacional de Educacin
ACTIVIDAD SUGERIDA PARA LOS ITEMS 19, 20, 21, 22, 23 y 24 Bloque de Contenidos: Indicadores de logros: contenido: Leyes de la 4.2 Experimenta con orden y cuidado la Ley Cero de la Fsica termodinmica. Termodinmica. 4.4 Investiga, representa y describe con cuidado y esmero los efectos del calor en la dilatacin de slidos, lquidos y gases. 4.8 Investiga, experimenta, explica y resuelve problemas con seguridad de la primera Ley de la Termodinmica. 4.16 Formula, analiza y resuelve con seguridad los problemas de aplicacin de la segunda Ley de la Termodinmica. Causas posibles por las que los estudiantes no contestaron bien los tems
1. Confundir los conceptos de calor y temperatura. 2. No manejar los trminos en que se fundamentan las leyes de la termodinmica y su aplicacin. 3. Reconocer los efectos del calor en la dilatacin de los slidos, lquidos y gases.
Actividad 1: Aplicacin de las leyes de la termodinmica
Recursos para el desarrollo de la actividad Textos que se refieren a las leyes de la termodinmica, un calormetro
Descripcin de los pasos para el desarrollo de la actividad
1. 2.
Pedir a los estudiantes que lean el texto. Analizar el planteamiento de cada una de las leyes de la termodinmica haciendo nfasis en los principios en los que se basan cada una de estas leyes.
3. 4.
Hacer algunas preguntas que exploren los presaberes de los estudiantes. Pedir que en equipo hagan un cuadro comparativo entre las distintas leyes de la termodinmica.
Actividades de Refuerzo para Ciencias Naturales
Pgina 45
Ministerio de Educacin Direccin Nacional de Educacin
5. 6.
Pedir que desarrollen ejercicios de aplicacin. Orientar el uso del calormetro para determinar el calor especfico de alguna sustancia.
7.
Realizar una investigacin documental sobre la utilidad de las mquinas trmicas y anlisis del esquema general de las mquinas trmicas para explicar sus fundamentos tericos.
Referencias tericas
La termodinmica es un rea de la fsica que estudia las relaciones entre las diferentes propiedades de equilibrio de un sistema y los cambios que ellos producen en los estados de los sistemas. A las magnitudes macroscpicas que se relacionan con el estado interno de un sistema se les llama coordenadas termodinmicas; estas nos van a ayudar a determinar la energa interna de un sistema. Un sistema es una parte especfica del universo, de inters para nosotros. El resto del universo externo al sistema se denomina entorno por ejemplo, cuando realizamos una reaccin qumica en el laboratorio, las sustancias qumicas generalmente constituyen el sistema. Hay tres tipos de sistemas. Los sistemas abiertos pueden intercambiar masa y energa con su entorno. Los sistemas cerrados permiten la transferencia de energa en forma de calor, pero no de masa. Por ejemplo el agua contenida en un recipiente cerrado. Los sistemas aislados no permiten la transferencia ni de masa ni de energa. Por ejemplo, agua contenida en un recipiente totalmente aislado.
PRIMERA LEY DE LA TERMODINMICA La ley de la conservacin de la energa o primera ley de la termodinmica establece que todas las formas de energa pueden intercambiarse, pero no se pueden destruir ni crear, por lo cual la energa total del universo permanece constante. La energa total de un sistema o energa interna es una funcin de estado que se define como la suma de todas las energas cinticas y potenciales de sus partes.
Actividades de Refuerzo para Ciencias Naturales
Pgina 46
Ministerio de Educacin Direccin Nacional de Educacin
PROCESOS TERMODINMICOS 1. Proceso adiabtico Cuando no hay transferencia de calor al sistema, se dice que ocurre un proceso adiabtico. En este proceso, la variacin de la energa interna del sistema se debe, nicamente, al trabajo realizado por el sistema o al trabajo realizado sobre el sistema. 2. Proceso isotrmico Ocurre cuando a un sistema se le suministra calor y se producen cambios en la presin y el volumen, con la condicin de que la temperatura permanezca constante. Es decir, que en un proceso isotrmico, el calor suministrado al sistema se transforma en trabajo realizado por el sistema. 3. Proceso isomtrico Un proceso isomtrico ocurre a volumen constante, es decir, que se suministra calor al sistema; sin embargo, no se espera que haya variacin en el volumen. Es decir, que en un proceso isomtrico todo el calor se convierte en energa interna. SEGUNDA LEY DE LA TERMODINMICA La energa calorfica fluye de manera espontnea de una sustancia a alta temperatura, a una sustancia a baja temperatura y no fluye de manera espontnea en direccin contraria. En la forma planteada antes, la segunda ley de la termodinmica se refiere a la tendencia natural del calor a fluir de lo caliente a lo fro. Sin embargo, se debe observar que el calor puede forzarse a fluir en la direccin opuesta, en caso que se efecte trabajo para lograr lo anterior. Hay varios ejemplos conocidos de este flujo inverso forzado. Un acondicionador de aire permite un flujo de calor desde el interior fro de una casa, hacia el exterior caliente, por medio del trabajo efectuado por la energa elctrica.
ENTROPA Y SEGUNDA LEY DE LA TERMODINMICA De acuerdo con la segunda ley de la termodinmica, la entropa del universo aumenta de manera continua. En trminos de orden y desorden, lo anterior indica que el universo se convierte cada vez ms en un sitio desordenado y catico.
Actividades de Refuerzo para Ciencias Naturales
Pgina 47
Ministerio de Educacin Direccin Nacional de Educacin
La entropa, al igual que el calor, es una funcin del estado de un sistema y puede definirse como una medida del desorden del sistema. As por ejemplo los procesos naturales tienden a moverse hacia un estado de mayor desorden, por lo que su entropa aumenta.
Ejemplo: Cuando un objeto caliente se pone en contacto con un fro, el calor fluye de la temperatura alta a la baja hasta que los dos objetos alcanzan la misma temperatura intermedia. Al principio del proceso se pueden distinguir dos clases de molculas: aquellas que tienen una energa cintica alta (el objeto caliente) y las que tienen una energa cintica baja (el objeto ms fro). Despus del proceso en el que fluye calor, todas las molculas estn en una clase con la misma energa cintica promedio; ya no se tiene el arreglo ms ordenado de molculas en dos clases. El orden ha cedido el paso al desorden. Ejemplos de aplicacin: Cuntas caloras se requieren para que 500g de mercurio pasen de 10oC a 400oC? Sabiendo que el calor especifico del mercurio es 0,33 cal/g oC Desarrollo: Frmula: Q=m Ce t Q= 500g x 0,33 cal/g oC x 410oC Q=67650cal Se utilizan 2kcal para calentar 600 gr de una sustancia de 15 oC a 40oC. Cul es el calor especfico de la sustancia? Frmula: Q=mCet Ce= Ce= t= tfti=410oC
Q mt
1kcal=1000cal
2000cal 600 gr 25
Ce= 0,13cal/g oC Se comprime un gas a presin constante de 0.8 atm de un volumen de 9 lt a un volumen de 2lt. En el proceso se escapan del gas 400J de energa calorfica. a) Cul es el trabajo realizado por el gas? Formula: W=p (Vfvi)
Actividades de Refuerzo para Ciencias Naturales
Pgina 48
Ministerio de Educacin Direccin Nacional de Educacin
W=0,8 atm (2 lt9 lt) Frmula: U=QW U=400+567,5J U=167,5 J
W=567,5 J
b) Cul es el cambio de energa interna del gas?
Una pieza de plata de 50g est a 20oC. Si se agregan 400 cal al cadmio, cul ser su temperatura final? Frmula =mCet Ce de la plata=0,056cal/g oC T=
Q de donde: T=TfTi; sustituyendo: mCe Q Q ; despejando: Tf= +Ti mCe mCe
TfTi= Tf =
400cal +20OC 50 g 0,056cal / g C
Tf =142,85oC
Actividad 2: Resolucin de gua
Recursos para el desarrollo de la actividad Gua de trabajo
Descripcin de los pasos para el desarrollo de la actividad
1. 2.
Pedir a los estudiantes que en equipo respondan la siguiente gua. Determinar cules de las siguientes expresiones son verdaderas. Justificar la respuesta. a) El calor es energa trmica en trnsito. b) Para aumentar la energa trmica, es necesario realizar trabajo sobre el objeto. c) En un proceso adiabtico no hay transferencia de calor. d) La nica manera de aumentar la temperatura de un gas es suministrndole calor.
Actividades de Refuerzo para Ciencias Naturales
Pgina 49
Ministerio de Educacin Direccin Nacional de Educacin
3.
Analizar y responder. a) Qu tipo de proceso trmico ocurre cuando se calienta el agua contenida en una cpsula demasiado rgida? b) Cunto trabajo se realiza cuando ocurre un proceso isomtrico en un sistema? c) Vara la energa interna de un gas cuando se somete a un proceso isotrmico en un sistema? Por qu? d) Qu proceso tiene lugar en un gas cuando todo el calor suministrado se transforma en trabajo? e) Imagina determinada cantidad de agua en estado slido y la misma cantidad en estado lquido. Cul de las dos tiene mayor entropa? Por qu?
4. Definir los siguientes trminos: a) Energa interna b) Segunda ley de la termodinmica c) Energa qumica d) Calor e) Temperatura
5. Analizar y responder a) Cul es el fundamento de la segunda ley de la termodinmica? b) Un sistema absorbe 1 500 J de energa calorfica de sus alrededores. Determinar el cambio de energa interna del sistema cuando el sistema efecta 2 200 J de trabajo sobre sus alrededores. Esto es de acuerdo a la primera ley de la termodinmica. c) Se mezclan 100 g de hierro a 80 C con 53,5 g de agua a 20 C. Cul es la temperatura final de la mezcla? El calor especfico del hierro es 0,107 cal/g C, y el calor especfico del agua es 1 cal/g C Referencias bibliogrficas Fsica, John D. Cutnell y Kenneth W. Johnson, Editorial Limusa, 1995, #395-400
Actividades de Refuerzo para Ciencias Naturales
Pgina 50
Ministerio de Educacin Direccin Nacional de Educacin
ACTIVIDAD SUGERIDA PARA EL TEM NMERO 25 Y 26 Bloque de contenido: Qumica Contenidos: Tabla peridica moderna Indicadores de logro: 5.7 Indaga, representa, describe y explica el criterio para la organizacin y distribucin de los elementos qumicos en la tabla peridica moderna con base en el orden creciente de sus nmeros atmicos. 5.8 Identifica y ubica correctamente los elementos qumicos de la tabla peridica por sus propiedades generales.
Causas posibles por las que los estudiantes no contestaron bien el tem 1. Confunden terminologa de los conceptos bsicos de qumica como: peso atmico, masa atmica, nmero atmico y su relacin como tal en la tabla peridica. 2. Desconocen las caractersticas peridicas de los elementos qumicos en la tabla peridica. 3. Falta de Interpretacin de tablas peridicas hipotticas en las que a partir de lo aprendido en clase con una tabla peridica completa se pueden ubicar los elementos que la conforman, caractersticas peridicas de los elementos, etc. 4. Falta de habilidades para interpretar indicaciones con smbolos, o lo indicado en los textos.
Actividad 1: Comprendiendo el ordenamiento de los elementos de la tabla peridica
Recursos para el desarrollo de la actividad Texto con el contenido sobre tabla peridica Copias de tabla peridica Gua de trabajo Descripcin de los pasos para el desarrollo de la actividad 1. Organizar a los estudiantes en equipos segn la cantidad a atender. 2. Entregar la gua de trabajo a cada estudiante. 3. Dar lectura al texto sobre la tabla peridica, interpretarlo y comentarlo en el equipo.
Actividades de Refuerzo para Ciencias Naturales
Pgina 51
Ministerio de Educacin Direccin Nacional de Educacin
4. Ubicar en el esquema de la tabla hipottica contenida en la gua lo solicitado en las preguntas 1, 2, 3 y 4, que aparecen el la gua de trabajo, para la actividad 1. 5. Consultar la tabla peridica. 6. Realizar una plenaria sobre las preguntas de la gua asignando una a cada equipo. 7. Emitir conclusiones sobre el trabajo realizado. Referencias tericas
LA TABLA PERIDICA: NMERO ATMICO Y NMERO MSICO Qu es la tabla peridica? Es un sistema de organizacin de los elementos qumicos. Cmo se organizan los elementos qumicos en la tabla peridica? Se ordenan en orden creciente de sus nmeros atmicos. El nmero atmico de un elemento qumico es un nmero entero que indica la cantidad de protones (p +) que tiene en el ncleo un tomo de ese elemento, este se representa con la letra Z. Todos los elementos tienen diferente nmero atmico?
S, cada elemento tiene un valor de Z que lo caracteriza, por decirlo de otra manera, todos los tomos de Calcio tienen 20 protones y todos los de carbono tienen 6 protones. Y qu ms hay en el ncleo? El ncleo del tomo est constituido por protones (partculas con carga positiva) y neutrones (partculas neutras). A la suma de las cantidades de protones y neutrones que tiene un tomo se le llama Nmero msico y se le representa con la letra A.
Actividades de Refuerzo para Ciencias Naturales
Pgina 52
Ministerio de Educacin Direccin Nacional de Educacin
Tabla peridica
Descripcin de los pasos para el desarrollo de la actividad 1. Ubicar en la tabla hipottica todos los elementos del perodo 4 con sus respectivos nmeros atmicos. 2. Ubicar en la tabla hipottica todos los elementos del grupo 0. 3. Responder: a) Qu dudas se presentaron en el momento de la asignacin de los elementos en su respectivo perodo con su nmero atmico? b) Mencionar las caractersticas ms importantes del grupo 0. c) Por qu es importante ordenar los elementos en la tabla peridica? d) En los elementos del GRUPO VII A, uno de ellos es importante para funciones vitales del ser humano, comentar con los compaeros cul consideran que es y por qu es importante para la vida.
Actividades de Refuerzo para Ciencias Naturales
Pgina 53
Ministerio de Educacin Direccin Nacional de Educacin
Actividad 2: Identifiquemos el nmero atmico y el nmero msico
Recursos para el desarrollo de la actividad Texto con el contenido sobre tabla peridica Copias de tabla peridica Gua de trabajo Descripcin de los pasos para el desarrollo de la actividad 1. Leer de nuevo el texto contenido en la gua acerca el nmero atmico y el nmero msico. 2. Analizar el esquema que se presenta y relacionarlo con lo ledo acerca del nmero atmico y el nmero msico. 3. Trabajar con el esquema de la actividad 2 y responder las preguntas 1, 2, 3, 4 y 5. 4. Consultar la tabla peridica para la actividad 2. 5. Realizar una plenaria sobre las preguntas de la gua asignando una a cada equipo. 6. A partir del siguiente esquema y de la lectura de la gua responder:
a) El nombre del elemento descrito en el esquema y en qu grupo de la tabla peridica se encuentra. b) Explicar qu significan el smbolo A y Z y cul es la diferencia entre ambos. c) Asignar el dato correspondiente a A y Z, al elemento H, que se muestra en el esquema.
Actividades de Refuerzo para Ciencias Naturales
Pgina 54
Ministerio de Educacin Direccin Nacional de Educacin
d) Cul es la importancia de asignar un nmero atmico a cada elemento de la tabla peridica? e) Si en el esquema estuviese el elemento K, qu datos le asignara para A y Z (consultar la copia de su tabla peridica).
Fuente de informacin Qumica 1, Morales Violeta, Merino Fabio, Susaeta Ediciones Dominicanas, C. por A, 1999, primera edicin, Pgs.12-26. Brown Theodore L. y HE. Le May.Quimica, la Ciencia Central.Prentice- Hall Hispanoamericana, S.A., Mxico, 3.ed.1997.
Actividades de Refuerzo para Ciencias Naturales
Pgina 55
Ministerio de Educacin Direccin Nacional de Educacin
ACTIVIDAD SUGERIDA PARA EL TEM NMERO 27 Y 28 Bloque contenido: Qumica de Contenidos: Tabla peridica moderna; Organizacin de la tabla peridica moderna; Propiedades peridicas de los elementos qumicos Indicadores de logro: 5.7 Indaga, representa, describe y explica el criterio para la organizacin y distribucin de los elementos qumicos en la tabla peridica moderna con base en el orden creciente de sus pesos atmicos. 5.8 Identifica y ubica correctamente los elementos qumicos de la tabla peridica por sus propiedades generales.
Causas posibles por las que los estudiantes no contestaron bien el tem 1. No se tom en cuenta que un catin con un electrn que ceder, es un in con carga elctrica positiva, hecho caracterstico de los metales alcalinos del grupo IA. 2. No consider que un elemento que tiene tendencia a perder dos electrones es un agente reductor, no un oxidante y que dicha propiedad es caracterstica de los elementos del grupo II A (alcalinotrreos). 3. No ha comprendido que si las capas electrnicas de los halgenos fueran estables, estos seran inertes, como ocurre con los elementos del grupo 0, o gases nobles. 4. Desconoce que el carcter metlico aumenta de arriba hacia abajo en la tabla peridica.
Actividad 1: Criterios de ordenamiento de los elementos en la tabla peridica
Recursos para el desarrollo de la actividad Cuestionario Fuentes bibliogrficas de consulta Tabla peridica ampliada Tablas peridicas individuales Descripcin de los pasos para el desarrollo de la actividad 1. Presentar una breve introduccin terica sobre la estructura de la tabla peridica de los elementos qumicos.
Actividades de Refuerzo para Ciencias Naturales
Pgina 56
Ministerio de Educacin Direccin Nacional de Educacin
2. Asignar una investigacin bibliogrfica sobre la tabla peridica a partir del siguiente cuestionario:
a) Qu es un grupo? b) Cuntos grupos hay? c) Qu es un perodo? d) Cuntos periodos hay? e) Qu tienen en comn los elementos de la tabla peridica que estn colocados en la misma columna? Y los que estn colocados en la misma fila? f) Qu criterio es el utilizado para ordenar los elementos en la tabla peridica? Siempre ha sido as?
g) Observa la estructura electrnica de algunos elementos y su posicin en la tabla peridica, hay alguna relacin? h) La ordenacin que hicieron Mendeleiev y Meyer se bas en la masa atmica (de izquierda a derecha y de arriba abajo iba aumentando la masa atmica); la actual debida a Moseley, se basa en el nmero atmico. Esta ordenacin casi coincide con la de la masa; qu elementos no siguen la ordenacin creciente de masas atmicas? Por qu? i) En la tabla existen elementos metlicos, no metlicos, slidos, lquidos, gases, etc. Observa detalladamente la tabla peridica y entre los primeros 103 elementos escribe el nombre de aquellos que son: slidos, lquidos y gases. Menciona cuales son metales; no metales; semimetales; gases nobles; alcalinos; halgenos y lantnidos. Identifica en la tabla que se te propone los puntos de fusin y ebullicin de los veinte primeros elementos.
j)
3. Organizar una puesta en comn de las respuestas al cuestionario, procurando la participacin de todos, mediante rondas sucesivas de preguntas y respuestas. 4. Aprovechar la puesta en comn para ampliar aspectos de los contenidos investigados, aclarar dudas y proponer ejemplos. Fuente de informacin Adaptado de: http://www.iesaguilarycano.com/dpto/fyq/tabla_periodica/tabla_periodica.html Informacin complementaria: OConnor, R. (1976) La Qumica, Mxico, D.F. Editorial HARLA, S.A. de C.V.
Actividades de Refuerzo para Ciencias Naturales
Pgina 57
Ministerio de Educacin Direccin Nacional de Educacin
ACTIVIDAD SUGERIDA PARA EL TEM NMERO 29,30 Y 31 Bloque de Contenidos: Compuestos contenido: Qumica qumicos; Electrones de valencia y enlace qumico; Tipos de enlace qumico: inico, covalente y metlico. Indicador de logro: 7.2 Indaga, experimenta y explica las propiedades y tipos de enlace qumico: inico, covalente y metlico de los compuestos.
Causas posibles por las que los estudiantes no contestaron bien el tem 1. Pas por alto que en el enunciado se dice que e l carbono comparte sus electrones con el oxgeno, no que los haya cedido, como es caracterstico del enlace inico. 2. No advirti que tanto el carbono, como el oxgeno, no son metales y que no pueden establecer este tipo de enlace entre s. 3. Olvid que compartir un par electrones es la caracterstica fundamental del enlace covalente. 4. Desconoce que las Fuerzas de van der Waals son fuerzas atractivas o repulsivas entre molculas, distintas a aquellas debidas al enlace covalente o a la interaccin electrosttica de iones (como en este caso). 5. No consider que la formacin de una nube de electrones mviles sin asociacin estrecha con ninguno de los tomos de la molcula es exclusivo del enlace
metlico. Adems, ignora que el Cl es un no metal y por lo tanto incapaz de formar ese tipo de enlaces. 6. Desconoce que la presencia de iones con carga positiva y negativa es caracterstica del enlace inico, que se da entre un metal y un no metal, no entre tomos de dos metales. 7. Olvid que los metales son agentes reductores y que por lo tanto liberan cationes (iones positivos), no aniones (iones negativos) 8. Desconoce que en el enlace covalente los electrones de enlace son compartidos por ambos tomos.
Actividades de Refuerzo para Ciencias Naturales
Pgina 58
Ministerio de Educacin Direccin Nacional de Educacin
Actividad 1: Elaboracin de un glosario
Recursos para el desarrollo de la actividad Diccionarios Libros de qumica Descripcin de los pasos para el desarrollo de la actividad 1. Organizar a los estudiantes en pareja para que busquen informacin y elaboren un glosario. 2. Pedir a los estudiantes que investiguen la definicin de los siguientes trminos: tomo, electrones, neutrones, in, metales, no metales, enlace inico, enlace covalente, enlace metlico, fuerzas de van der Waals, agente reductor, agente oxidante.
Actividad 2: Elaboracin de mapa de conceptos
Descripcin de los pasos para el desarrollo de la actividad 1. A partir de las definiciones anteriores, elaborar un mapa conceptual mediante el cual establezca relaciones entre los diferentes trminos. Ejemplo:
2. Pedir a los estudiantes que socialicen sus glosarios, aclaren dudas y obtengan conclusiones en la clase.
Actividades de Refuerzo para Ciencias Naturales
Pgina 59
Ministerio de Educacin Direccin Nacional de Educacin
Actividad 3: Comprobando la conductividad elctrica de dos sustancias
Recursos para el desarrollo de la actividad Sal de mesa (NaCl) Agua para batera de auto Azcar (sacarosa: C12H22O11) Dos botes de vidrio medianos (como en los que se envasan la mostaza o la mayonesa) Una pila de 9 voltios Un foco pequeo, un pedazo de cable elctrico, barritas de metal de cobre y un interruptor Descripcin de los pasos para el desarrollo de la actividad 1. Pedir a los estudiantes que se organicen en equipo para realizar las experiencias. 2. Puede hacer algunas preguntas previas para conocer los presaberes de sus estudiantes. 3. Con la pila, el cable elctrico, las barritas de metal de cobre y el interruptor fabricar un circuito sencillo. 4. En uno de los botes de vidrio colocar agua destilada hasta la mitad y luego disolver en ella 3 4 cucharadas de sal comn. 5. Enseguida sumergir las barritas del circuito en el NaCl disuelto en agua y a continuacin abrir el interruptor de manera que deje pasar la corriente. El foco se prender, lo que significa que se tienen iones en solucin y que el NaCl se constituye de enlaces inicos (ver figura adjunta).
NaCl en solucin
Actividades de Refuerzo para Ciencias Naturales
Pgina 60
Ministerio de Educacin Direccin Nacional de Educacin
6. A continuacin se repite el experimento en el otro bote donde se colocar azcar disuelta en agua. El foco desde luego no se prender, esto quiere decir que en el azcar no hay enlaces inicos sino covalentes. 7. En la pizarra escribir las frmulas de la sal y del azcar. Ubicar los elementos que constituyen dichos compuestos en la tabla peridica. Relacionarlos con las definiciones de los enlaces inico, covalente y metlico. 8. Es importante destacar tambin el papel que las barritas de metal de cobre desempean en la experiencia, como conductores de la electricidad. Aprovechar la experiencia para destacar que los metales presentan ciertas propiedades caractersticas como alta conductividad elctrica y trmica, brillo metlico y maleabilidad; estas propiedades son el resultado de su estructura interna, de la red metlica que constituyen sus tomos y de la nube electrnica que se mueven libremente por toda la red. 9. Preguntar: Qu ocurrira si las barritas de cobre se sustituyeran por barritas de plstico o de madera? por qu?
Fuente de informacin Informacin complementaria de: Zarraga Sarmiento, J. C. et al (2003) Qumica, Mxico, D.F. Editorial McGraw-Hill Interamericana, P. 200-203 Mapa conceptual tomado de http://mchcd2.googlepages.com/EnlacesQuimicos.jpg
Actividades de Refuerzo para Ciencias Naturales
Pgina 61
Ministerio de Educacin Direccin Nacional de Educacin
ACTIVIDAD SUGERIDA PARA EL TEM NMERO 32 Y 33 Bloque de Contenidos: Indicadores de logro: contenidos: Qumica Nomenclatura de 7.6 Aplica las reglas de la compuestos inorgnicos nomenclatura IUPAC a compuestos inorgnicos. Causas posibles por las que los estudiantes no contestaron bien el tem 1. No tienen claridad que tipos de elementos estn presentes en la frmula de un compuesto. Es decir, si se trata de un metal o un no metal o se trata de un elemento electronegativo o un electropositivo. 2. No saben aplicar correctamente las reglas o normas de nomenclatura. 3. Desconocer y/o no se identifica al elemento representativo de una determinada familia de compuestos. Por ejemplo el hidrgeno en cidos hidrcidos y el oxgeno que esta presente cidos oxcidos.
Actividad 1: Aplicacin correcta de las normas de nomenclatura de compuestos inorgnicos
Recursos para el desarrollo de la actividad Textos que expliquen claramente los diferentes sistemas de nomenclatura que se conocen: stock, estequiomtrico y tradicional. Descripcin de los pasos para el desarrollo de la actividad 1. Pedir a los estudiantes que lean las normas y reglas que utiliza cada sistema de nomenclatura, as como tambin, los ejemplos de compuestos qumicos utilizados. 2. Pedir que realicen una lectura comprensiva del texto haciendo nfasis en que el estudiante sepa distinguir entre un metal y un no metal, entre un elemento electropositivo y uno electronegativo. 3. Comprender e interpretar las distintas reglas de nomenclatura que aplica cada sistema de nomenclatura.
Actividades de Refuerzo para Ciencias Naturales
Pgina 62
Ministerio de Educacin Direccin Nacional de Educacin
4. Pedir a los estudiantes que analicen, nombren, escriban y comparen compuestos inorgnicos de acuerdo con los tres sistemas de nomenclatura establecidos: el comn, el stock y el sistemtico. 5. Determinar que es una funcin qumica y un grupo funcional Referencias tericas Funcin Qumica: Grupo Funcional: Conjunto de compuestos que presentan propiedades fsicas y qumicas semejantes. Un tomo o grupo de tomos que define las propiedades fsicas y qumicas de una funcin qumica.
Ejemplos: Funcin qumica ............................................................... Grupo funcional cidos ............................................................................... Protn de Hidrgeno (H+) Bases ............................................................................... Oxidrilo (OH-) xido ................................................................................ Oxgeno (O)
Oxisal
OXCIDO
Actividades de Refuerzo para Ciencias Naturales
Pgina 63
Ministerio de Educacin Direccin Nacional de Educacin
Sistema Stock: Utiliza nmeros romanos para indicar el grado de oxidacin del elemento. Nomenclatura Sistemtica: Utiliza prefijos tales como: mono, di, tri, tetra, penta, etc. Que indican el nmero de tomos presentes en la molcula. Nomenclatura Comn o Tradicional: Utiliza sufijos tales como oso e ico para elementos que trabajan con dos valencias; oso para la valencia menor e ico para la mayor valencia.
6. Pedir a los estudiantes que en equipo completen los cuadros siguientes.
Compuesto
Nomenclatura Stock
Nomenclatura Sistemtica
Nomenclatura Comn xido de sodio xido ferroso xido frrico
Na2O FeO Fe2O3 CoO Co2O3 SO SO2 SO3
xido de sodio xido de hierro I xido de hierro II
xido de sodio Monxido de hierro Trixido de hierro
Compuesto
Nomenclatura Stock
Nomenclatura Sistemtica
Nomenclatura Comn
NaOH Mg(OH)2 Fe(OH)2 Fe(OH)3 Co(OH)2 Co(OH)3
Actividades de Refuerzo para Ciencias Naturales
Pgina 64
Ministerio de Educacin Direccin Nacional de Educacin
Nombre xido de calcio xido niqulico Anhdrido cloroso Anhdrido ciorico Anhdrido plumboso Anhdrido plmbico Hidrxido mercurioso Hidrxido estannoso
Frmula
Nombre cido telurhdrico xido de cromo IV xido de mercurio I
Frmula
cido cloroso
cido clrico
Cloruro de potasio
Sulfato de calcio Sulfato cido de potasio
Fuente de informacin Qumica 10, Educar editores, Julio Cesar Poveda, ao de edicin 2003, Pgs. 153-175
Actividades de Refuerzo para Ciencias Naturales
Pgina 65
Ministerio de Educacin Direccin Nacional de Educacin
ACTIVIDAD SUGERIDA PARA EL TEM NMERO 34 Y 37
Bloque de contenido: Qumica
Contenido: Compuestos inorgnicos
Indicador de logro: 7.6 Indaga y explica con seguridad la nomenclatura de compuestos inorgnicos y describe las propiedades de los xidos bsicos, anhdridos u xidos cidos, hidruros no metlicos, sales haloideas e hidruros metlicos.
Causas posibles por las que los estudiantes no contestaron bien el tem
1. Dificultad para identificar las caractersticas de las molculas inorgnicas. 2. Desconocimiento de las propiedades fsicas y qumicas que presentan los compuestos inorgnicos. 3. Confusin al identificar los diferentes tipos de compuestos inorgnicos: xidos bsicos, anhdridos u xidos cidos, hidruros no metlicos, sales haloideas e hidruros metlicos. 4. Falta de habilidades para buscar alternativas de solucin a problemas cotidianos asociados con la qumica.
Actividad 1: Identifiquemos sustancias inorgnicas
Recursos para el desarrollo de la actividad Textos con las caractersticas de los diferentes compuestos inorgnicos.
Descripcin de los pasos para el desarrollo de la actividad
1. Organizar a los estudiantes en equipos de trabajo y proporcionarles a cada equipo un texto y ejemplos sobre tipos de compuestos inorgnicos. 2. Permitir que investiguen la importancia de dichos compuestos en la vida cotidiana.
Actividades de Refuerzo para Ciencias Naturales
Pgina 66
Ministerio de Educacin Direccin Nacional de Educacin
3. Pedir a los estudiantes que identifiquen algunos compuestos que ellos conocen y se utilizan en diferentes actividades cotidianas o conocidas. 4. Presentar una serie de preguntas que pueden utilizar para clasificar la informacin, por ejemplo: Dnde se encuentran? Para qu se usan? Hay compuestos de uso domstico? Cules son? u otras preguntas que se consideren pertinentes. 5. Orientarles para que definan los roles en los equipos. 6. Dar un tiempo prudente para que los estudiantes realicen esta primera actividad. 7. Elaborar carteles con las conclusiones acerca de los compuestos y sus caractersticas. 8. Realizar una mesa redonda para exponerlas. 9. Generar un debate con una ronda de preguntas y respuestas. 10. Hacer sntesis de las ventajas y desventajas del uso de los compuestos. investigados.
Referencias tericas
Se denomina compuesto inorgnico a todos aquellos compuestos que estn formados por distintos elementos, pero en los que su componente principal no siempre es el carbono, siendo el agua el ms abundante. En los compuestos inorgnicos se podra decir que participan casi la totalidad de elementos conocidos. Un compuesto orgnico se forma de manera natural tanto en animales como en vegetales, uno inorgnico se forma de manera ordinaria por la accin de varios fenmenos fsicos y qumicos: electrlisis, fusin, etc. Tambin podran considerarse agentes de la creacin de estas sustancias la energa solar, el agua, el oxgeno. Los enlaces que forman los compuestos inorgnicos suelen ser inicos o covalentes. Ejemplos de compuestos inorgnicos: Cada molcula de cloruro de sodio (NaCl) est compuesta por un tomo de sodio y otro de cloro. Cada molcula de agua (H2O) est compuesta por dos tomos de hidrgeno y uno de oxgeno.
Actividades de Refuerzo para Ciencias Naturales
Pgina 67
Ministerio de Educacin Direccin Nacional de Educacin
Cada molcula de amonaco (NH3) est compuesta por un tomo de nitrgeno y tres de hidrgeno. El anhdrido carbnico se encuentra en la atmsfera en estado gaseoso y los seres vivos aerobios lo liberan hacia ella al realizar la respiracin. Su frmula qumica, CO2, indica que cada molcula de este compuesto est formada por un tomo de carbono y dos de oxgeno. El CO2 es utilizado por algunos seres vivos auttrofos como las plantas en el proceso de fotosntesis para fabricar glucosa. Aunque el CO2 contiene carbono, no se considera como un compuesto orgnico porque no contiene hidrgeno. Puntos de fusin y ebullicin En general y considerando molculas de igual masa atmica, los compuestos inorgnicos inicos tienen puntos de fusin y de ebullicin que los compuestos covalentes, debido a que el enlace inico es ms fuerte y estructurado que el enlace covalente, que es ms fcil de debilitar por calentamiento. Elementos qumicos Aunque los compuestos inorgnicos existen en menor medida que los orgnicos, en su composicin intervienen los 93 elementos naturales de la tabla peridica. Los compuestos orgnicos, formados mayoritariamente por C, H, O, N, S, por este orden y con mucha menor presencia de otros elementos en su composicin, se cuentan entre los ms numerosos. Esto se debe a la asombrosa capacidad del carbono de formar cadenas largusimas y ramificadas.
NOMENCLATURA QUMICA DE LOS COMPUESTOS INORGNICOS
Los compuestos inorgnicos presentan gran variedad de estructuras. Segn el nmero de tomos que componen las molculas, estas se clasifican en: Monoatmicas: constan de un slo tomo, como las molculas de gases nobles (He, Ne, Ar, Xe y Kr). Diatmicas: constan de dos tomos. Son diatmicas las molculas gaseosas de la mayora de elementos qumicos que no forman parte de los gases nobles, como el dihidrgeno (H2) o el dioxgeno (O2); as como algunas molculas binarias (xido de calcio).
Actividades de Refuerzo para Ciencias Naturales
Pgina 68
Ministerio de Educacin Direccin Nacional de Educacin
Triatmicas: constan de tres tomos, como las molculas de ozono (O3), agua (H2O) o bixido de carbono (CO2). Poliatmicas: contienen cuatro o ms tomos, como las molculas de fsforo (P4) o de xido frrico (Fe2O3).
COMPUESTOS BINARIOS
xidos
Los xidos son compuestos que resultan de la unin de oxgeno (O 2-) con cualquier elemento de la tabla peridica sea metal (xidos bsicos) o no metal (xidos cidos). Las nomenclaturas son las comunes, la Stock y la IUPAC. Ejemplos de xidos: xido de cloro (VII): Cl2O7 ; xido de boro: B2O3; Bixido de carbono: CO2; Bixido de silicio: SiO2 Perxidos Los perxidos son compuestos que resultan de la unin del grupo perxido (-O-O- u O2-2) con un metal. En los perxidos, el oxgeno tiene un nmero de oxidacin o valencia -1. Se nombran utilizando el trmino perxido seguido del nombre del metal. Ejemplos de perxidos: Perxido de oro (III): Au2(O2)3; Perxido de estao (IV) = Sn(O2)2; Perxido de plomo (IV) =Pb(O2)2; Perxido de litio = Li2O2 Hidruros Los hidruros son compuestos que resultan de la unin del anin hidruro (H-) con un catin metlico. Se nombran con la palabra hidruro seguida del nombre del metal. Ejemplos de hidruros: Hidruro de litio: LiH; Hidruro de berilio: BeH2 Sales binarias Los iones son tomos o conjuntos de tomos cuya carga elctrica no es neutra. Pueden ser cationes, si tienen carga positiva; o aniones, si su carga es negativa. Ejemplos de sales binarias Cloruro de calcio: CaCl2; Bromuro de hierro (III): FeBr3
Actividades de Refuerzo para Ciencias Naturales
Pgina 69
Ministerio de Educacin Direccin Nacional de Educacin
COMPUESTOS TERNARIOS Hidrxidos
Los hidrxidos son los resultantes de la unin de un grupo hidrxido o hidroxilo con un metal. Se nombran usando el trmino hidrxido (OH-) seguido del nombre del metal mediante la nomenclatura Stock o la IUPAC. Ejemplos de hidrxidos: Hidrxido de plomo (IV): Pb(OH)4; Hidrxido de sodio: NaOH; Hidrxido de cobalto (III): Co(OH)3 ; Hidrxido de germanio (IV): Ge(OH)4 Oxcidos Los oxcidos son compuestos ternarios que se forman al combinarse un anhdrido (xido cido) con el agua. La mayora de ellos responden a la frmula general HaXbOc, donde X es ordinariamente un no-metal, aunque tambin puede ser un metal de transicin con nmero de oxidacin superior a 4.
Fuente de informacin http://es.wikipedia.org/wiki/Compuesto_inorg%C3%A1nico
Actividades de Refuerzo para Ciencias Naturales
Pgina 70
Ministerio de Educacin Direccin Nacional de Educacin
ACTIVIDAD SUGERIDA PARA EL TEM NMERO 35 Y 36
Bloque de contenido: Qumica
Contenidos: Tipos de enlaces qumicos
Indicadores de logro: 7.2 Indaga, experimenta y explica las propiedades y tipos de enlace qumico: inico, covalente y metlico de los compuestos.
Causas posibles por las que los estudiantes no contestaron bien el tem
1.
No logran determinar que los enlaces covalentes son molculas elctricamente neutras con propiedades totalmente diferentes a las de los compuestos inicos.
2.
Desconocimiento de las propiedades fsicas y qumicas que presentan los compuestos con enlaces covalentes.
3.
Hay confusin al identificar los diferentes tipos de enlaces qumicos: inico, covalente, metlico y otros.
Actividad 1: Identifiquemos enlaces qumicos
Recursos para el desarrollo de la actividad Texto con el contenido de los diferentes tipos de enlaces qumicos y ejemplos de la vida cotidiana.
Descripcin de los pasos para el desarrollo de la actividad
1. Facilitar a los estudiantes un texto referido a los tipos de enlace qumico. 2. Desarrollar la comprensin de las caractersticas que presentan los diferentes tipos de enlace qumico: Inico, Covalente y Metlico. 3. Organizar a los estudiantes en equipos de trabajo y proporcionarles a cada equipo un texto y ejemplos sobre cada tipo de enlace qumico: Inico, Covalente y
Metlico, y completar el cuadro comparativo.
Actividades de Refuerzo para Ciencias Naturales
Pgina 71
Ministerio de Educacin Direccin Nacional de Educacin
4. Interpretar los ejemplos los cuales no deben estar identificados a cual enlace pertenecen. 5. Realizar una plenaria para exponer las conclusiones y proceder a una ronda de preguntas y respuestas. Cuadro comparativo Tipo de enlace Caractersticas Ejemplo Esquema
Inico
Covalente
Metlico
Referencias tericas ENLACES QUMICOS Sabemos que hay dos principales tipos de enlaces qumicos, inicos y - enlaces covalentes, adems de los enlaces metlicos. a) Enlaces Inicos En los enlaces inicos, los electrones se transfieren completamente de un tomo a otro. Durante este proceso de perder o ganar electrones cargados
Actividades de Refuerzo para Ciencias Naturales
Pgina 72
Ministerio de Educacin Direccin Nacional de Educacin
negativamente, los tomos que reaccionan forman iones. Lo iones cargados de manera opuesta se atraen entre ellos a travs de fuerzas electroestticas que son la base del enlace inico. Esta ltima caracterstica es un resultado de las fuerzas intermoleculares (fuerzas entre las molculas) en los slidos inicos. Si consideramos un cristal slido de cloruro de sodio, el slido est hecho de muchos iones de sodio cargados positivamente y un nmero igual de iones de cloro cargados negativamente. Debido a la interaccin de los iones cargados, los iones de sodio y de cloro estn organizados alternadamente como demuestra el esquema a la derecha. Cada in de sodio es atrado igualmente por todos sus iones de cloro vecinos, y de la misma manera por la atraccin del cloruro de sodio. El concepto de una molcula sola se vuelve borroso en cristales inicos ya que el slido existe como un sistema continuo. Las fuerzas entre las molculas son comparables a las fuerzas dentro de la molcula, y los compuestos inicos tienden a formar como resultado cristales slidos con altos puntos de fusin. b) Enlaces Covalentes El segundo mayor tipo de enlace atmico ocurre cuando los tomos comparten electrones. Al contrario de los enlaces inicos en los cuales ocurre una transferencia completa de electrones, el enlace covalente ocurre cuando dos (o ms) elementos comparten electrones. El enlace covalente ocurre porque los tomos en el compuesto tienen una tendencia similar hacia los electrones (generalmente para ganar electrones). Esto ocurre comnmente cuando dos no metales se enlazan. Ya que ninguno de los no elementos que participan en el enlace querr ganar electrones, estos elementos compartirn electrones para poder llenar sus envolturas de valencia. Un buen ejemplo de un enlace covalente es ese que ocurre entre dos tomos de hidrgeno. Los tomos de hidrgeno (H) tienen un electrn de valencia en su primera envoltura. Puesto que la capacidad de esta envoltura es de dos electrones, cada tomo hidrgeno 'querr' recoger un segundo electrn. En un esfuerzo por recoger un segundo electrn, el tomo de hidrgeno reaccionar con tomos H vecinos para formar el compuesto H 2. Ya que el compuesto de hidrgeno es una combinacin de tomos igualados, los
Actividades de Refuerzo para Ciencias Naturales
Pgina 73
Ministerio de Educacin Direccin Nacional de Educacin
tomos compartirn cada uno de sus electrones individuales, formando as un enlace covalente. De esta manera, ambos tomos comparten la estabilidad de una envoltura de valencia. Ya que los electrones estn compartidos en molcula covalentes, no se forman cargas inicas. Por consiguiente, no hay fuerzas intermoleculares fuertes en los compuestos covalentes tal como las hay en las molculas inicas. Como resultado, muchos compuestos inicos son gases o lquidos a temperatura ambiente en vez de slidos como los compuestos inicos en las molculas covalentes que tienden a tener una atraccin intermolecular ms dbil. Igualmente, al contrario de los compuestos inicos, los compuestos covalentes existen como verdaderas molculas. c) Enlaces Polares y No-Polares En realidad, hay dos sub tipos de enlaces covalente. La molcula H2 es un buen ejemplo del primer tipo de enlace covalente el enlace no polar. Ya que ambos tomos en la molcula H2 tienen una igual atraccin (o afinidad) hacia los electrones, los electrones que se enlazan son igualmente compartidos por los dos tomos, y se forma un enlace covalente no polar. Siempre que dos tomos del mismo elemento se enlazan, se forma un enlace no polar. Un enlace polar se forma cuando los electrones son desigualmente compartidos entre dos tomos. Los enlaces polares covalentes ocurren porque un tomo tiene una mayor afinidad hacia los electrones que el otro (sin embargo, no tanta como para empujar completamente los electrones y formar un in). En un enlace polar covalente, los electrones que se enlazan pasarn un mayor tiempo alrededor del tomo que tiene la mayor afinidad hacia los electrones. Un buen ejemplo del enlace polar covalente es el enlace hidrgeno - oxgeno en la molcula de agua. Fuente de informacin Anthony Carpi, Ph.D. "Enlaces Qumicos," Visionlearning Vol. CHE-1 (7s), 2003. http://www.visionlearning.com/library/module_viewer.php?mid=55&l=s
Actividades de Refuerzo para Ciencias Naturales
Pgina 74
Ministerio de Educacin Direccin Nacional de Educacin
ACTIVIDAD SUGERIDA PARA EL TEM NMERO 38, 39 Y 40 Bloque contenido: Biologa. de Contenidos: Anomalas cromosmicas, sndrome de Down, Turner y Klinefelter, Mutaciones. Indicador de logro: 10.11 Investiga y describe con responsabilidad algunas anomalas genticas ms frecuentes en humanos: sndromes de Down, Turner y Klinefelter.
Causas posibles por las que los estudiantes no contestaron bien el tem 1. Desconocimiento de las caractersticas de algunas mutaciones genticas. 2. Desconocimiento de los sndromes genticos comunes y sus caractersticas. 3. Confusin en las caractersticas de los sndromes referidos. 4. Dificultad para identificar las frmulas genticas de los sndromes. 5. Confusin para diferenciar las mutaciones de las no disyunciones genticas.
Actividad 1: Diferenciacin de frmulas genticas
Recursos para el desarrollo de la actividad Textos referidos a las caractersticas de los sndromes genticos Copias de los pares de cromosomas Descripcin de los pasos para el desarrollo de la actividad 1. Organizar a los estudiantes en equipos de trabajo. 2. Entregar a los estudiantes informacin escrita acerca de los sndromes de Down, Turner y Klinefelter, los cuales incluyan las frmulas genticas. 3. Dar a los estudiantes 2 copias extra de los cromosomas somticos y sexuales de una persona normal. 4. Asignar o permitir a cada equipo que escoja la construccin de un cdigo gentico: Down, Turner, Klinefelter. Los estudiantes harn nfasis en los cromosomas del par 21 y 23. 5. Recortar los pares de cromosomas para armar un cdigo gentico de cada uno de los sndromes. 6. Generar espacios para analizar las diferencias de los cdigos genticos. 7. Presentar carteles con los diferentes cdigos genticos.
Actividades de Refuerzo para Ciencias Naturales
Pgina 75
Ministerio de Educacin Direccin Nacional de Educacin
Referencias tericas Patrones genticos
Sndrome de Down. Trisoma 21
Sndrome de Turner. Monosoma 23. 45 X-0 Sndrome de Turner. Monosoma. 45 X-
Actividades de Refuerzo para Ciencias Naturales
Pgina 76
Ministerio de Educacin Direccin Nacional de Educacin
Sndrome de Klinefelter. Trisoma 23. 47 XXY
Par 23
Actividad 2: Comparemos las caractersticas de los sndromes genticos
Recursos para el desarrollo de la actividad Textos cientficos referidos a los sndromes de Down, Turner y Klinefelter. Copias de cuadros para diferenciar los sndromes. Descripcin de los pasos para el desarrollo de la actividad 1. 2. Organizar a los estudiantes en equipos de trabajo Realizar la actividad de la papa caliente para explorar presaberes , algunas sugerencias pueden ser: a) Qu son los genes? b) Cuntos cromosomas poseemos los seres humanos? c) Menciona 2 caractersticas del sndrome de Down, entre otras. 3. Presentar informacin escrita sobre las caractersticas de algunos desrdenes genticos (Down, Turner y Klinefelter). 4. Pedir a los estudiantes que con la informacin proporcionada, elaboren un cuadro comparativo diferenciando las caractersticas de cada sndrome.
Actividades de Refuerzo para Ciencias Naturales
Pgina 77
Ministerio de Educacin Direccin Nacional de Educacin
Sndrome Down
Caractersticas
Turner
Klinefelter
Diferencias entre los sndromes Sndrome Turner Diferencias Klinefelter
Sndrome Diferencias
Down
Turner
Sndrome Down Diferencias
Klinefelter
5. Organizar una mesa redonda para que en plenaria los estudiantes socialicen los resultados.
Actividades de Refuerzo para Ciencias Naturales
Pgina 78
Ministerio de Educacin Direccin Nacional de Educacin
Actividad 3: Identificacin de diferentes anomalas cromosmicas y sus caractersticas
Recursos para el desarrollo de la actividad Textos cientficos, esquemas Descripcin de los pasos para el desarrollo de la actividad 1. Por medio de preguntas, explorar conocimientos previos sobre mitosis, meiosis y gentica bsica. 2. Organizar equipos de trabajo, otorgndole a cada grupo un texto cientfico que aborde las diferentes anomalas cromosmicas. 3. Entregar cartulina, plumones y tirro para que elaboren carteles, que pueden
contener, esquemas, mapas conceptuales, cuadros u otros, dependiendo de la creatividad de cada equipo de trabajo. 4. Organizar una plenaria para que cada grupo presente sus resultados y se realice una ronda de preguntas y respuestas. 5. Aclarar los conceptos que puedan resultar confusos o errneos por parte de los y las estudiantes. Referencias tericas LAS ANOMALAS NUMRICAS: DESCRIPCIN GENERAL DE LAS TRISOMAS Y LAS MONOSOMAS a) Qu son las anomalas cromosmicas numricas? Las anomalas numricas conforman uno de los tipos de anomalas cromosmicas. Estos tipos de defectos congnitos ocurren cuando hay un nmero de cromosomas diferente en las clulas del cuerpo que el nmero normal. De modo que, en lugar de los 46 cromosomas habituales en cada clula del cuerpo, hay 45 47 cromosomas. El tener demasiados cromosomas o una cantidad insuficiente de cromosomas constituye una causa para el desarrollo de algn defecto congnito.
Actividades de Refuerzo para Ciencias Naturales
Pgina 79
Ministerio de Educacin Direccin Nacional de Educacin
b) Qu son las trisomas? El trmino "trisoma" se utiliza para describir la presencia de tres cromosomas en lugar del par habitual de cromosomas. Por ejemplo, si un nio nace con tres cromosomas 21 en lugar del par usual, se dira que posee "trisoma 21". La trisoma 21 tambin se conoce como sndrome de Down. Otros ejemplos de trisoma incluyen la trisoma 18 y la trisoma 13. Nuevamente, trisoma 18 o trisoma 13 significa simplemente que existen tres copias y no el par usual del cromosoma 18 (o del cromosoma 13) en cada clula del cuerpo. c) Qu son las monosomas? El trmino "monosoma" se utiliza para describir la ausencia de un miembro de un par de cromosomas. Por lo tanto, habr un total de 45 cromosomas en cada clula del cuerpo, en lugar de 46. Por ejemplo, si un beb nace con un solo cromosoma sexual X, en lugar del par habitual (ya sea, dos cromosomas sexuales X o un cromosoma sexual X y un cromosoma sexual Y, se dir que tiene "monosoma X." La monosoma X tambin se conoce con el nombre de sndrome de Turner.
Actividades de Refuerzo para Ciencias Naturales
Pgina 80
Ministerio de Educacin Direccin Nacional de Educacin
Fuente de informacin Biologa Peter Alexander y otros, Editorial Prentice Hall, 1992, Pg. 116-119 Biologa Thomas Overmire, 2001, Editorial Limusa, 2001, 6 reimpresin, Pg. 319-321 http://es.wikipedia.org/wiki/Aberraci%C3%B3n_cromos%C3%B3mica.
Actividades de Refuerzo para Ciencias Naturales
Pgina 81
Você também pode gostar
- Guiones 7 B 4 Unidad Tema 1Documento12 páginasGuiones 7 B 4 Unidad Tema 1Roberto MartínezAinda não há avaliações
- Guiones 7 B 4 Unidad Tema 2 IPARTEDocumento9 páginasGuiones 7 B 4 Unidad Tema 2 IPARTERoberto MartínezAinda não há avaliações
- Guiones 6 B 4° Unidad Tema 2Documento7 páginasGuiones 6 B 4° Unidad Tema 2Roberto MartínezAinda não há avaliações
- Electrostatica TodoDocumento21 páginasElectrostatica Todoanon_945473842Ainda não há avaliações
- Guiones 7 B 4 Unidad Tema 1 III PARTEDocumento4 páginasGuiones 7 B 4 Unidad Tema 1 III PARTERoberto MartínezAinda não há avaliações
- 3 +oración+de+intercesiónDocumento6 páginas3 +oración+de+intercesiónAlfonso OlayaAinda não há avaliações
- Guiones 1BACH 5 Unidad TEMA 4 IparteDocumento5 páginasGuiones 1BACH 5 Unidad TEMA 4 IparteRoberto MartínezAinda não há avaliações
- Guiones 7 B 4 Unidad Tema 3 IPARTEDocumento3 páginasGuiones 7 B 4 Unidad Tema 3 IPARTERoberto MartínezAinda não há avaliações
- Guiones 7 B 4 Unidad Tema 1 IIPARTEDocumento3 páginasGuiones 7 B 4 Unidad Tema 1 IIPARTERoberto MartínezAinda não há avaliações
- Guiones 2° BACH Unidad 6 SEGUNDO CONTENIDO III PARTEDocumento5 páginasGuiones 2° BACH Unidad 6 SEGUNDO CONTENIDO III PARTERoberto MartínezAinda não há avaliações
- Guiones 7 B 4 Unidad Tema 1 IIPARTEDocumento3 páginasGuiones 7 B 4 Unidad Tema 1 IIPARTERoberto MartínezAinda não há avaliações
- Guiones 6 B 4° Unidad Tema 1Documento7 páginasGuiones 6 B 4° Unidad Tema 1Roberto MartínezAinda não há avaliações
- Motricidad FinaDocumento4 páginasMotricidad FinaRoberto MartínezAinda não há avaliações
- Encuesta de Evaluación DocenteDocumento1 páginaEncuesta de Evaluación DocenteRoberto MartínezAinda não há avaliações
- 1900 Seguimiento Bajo RendimientoDocumento3 páginas1900 Seguimiento Bajo RendimientoRoberto MartínezAinda não há avaliações
- Plan de Emergencia y Evacuacion ModeloDocumento12 páginasPlan de Emergencia y Evacuacion ModeloRoberto MartínezAinda não há avaliações
- Guías de Estudio de CC 7º 2° Trimestre 2013Documento6 páginasGuías de Estudio de CC 7º 2° Trimestre 2013Roberto MartínezAinda não há avaliações
- Sistema muscular y sus funciones enDocumento43 páginasSistema muscular y sus funciones enRoberto MartínezAinda não há avaliações
- Los Problemas Básicos en El HogarDocumento4 páginasLos Problemas Básicos en El HogarRoberto MartínezAinda não há avaliações
- Remedios Preciosos Contra Las Artimañas Del DiabloDocumento37 páginasRemedios Preciosos Contra Las Artimañas Del Diabloapi-383598894% (16)
- Plani Ciencias 9°Documento47 páginasPlani Ciencias 9°Roberto MartínezAinda não há avaliações
- AtaquescontrahogarDocumento12 páginasAtaquescontrahogarMar HerreraAinda não há avaliações
- Manual Admin CompartirDocumento261 páginasManual Admin CompartirAlessandro RamirezAinda não há avaliações
- Desconocido - Curso de Matrimonios PDFDocumento52 páginasDesconocido - Curso de Matrimonios PDFhpaton100% (1)
- Ley de Prevencion de Riesgos en Los Lugares Trabajo de El SalvadorDocumento21 páginasLey de Prevencion de Riesgos en Los Lugares Trabajo de El SalvadorRafael GuineaAinda não há avaliações
- Notas de Estudio Sobre Hermeneutica BiblicaDocumento35 páginasNotas de Estudio Sobre Hermeneutica BiblicaKatarine Fiorela ÐßAinda não há avaliações
- Jornalización 7°Documento1 páginaJornalización 7°Roberto MartínezAinda não há avaliações
- Escueladominical 090515115028 Phpapp02Documento11 páginasEscueladominical 090515115028 Phpapp02hectormeraz673058Ainda não há avaliações
- Guías de Estudio de CC 7º 2012Documento3 páginasGuías de Estudio de CC 7º 2012Roberto MartínezAinda não há avaliações
- Guías de Estudio de CC 6º 2012Documento3 páginasGuías de Estudio de CC 6º 2012Roberto Martínez0% (2)
- Cinematica VectorialDocumento5 páginasCinematica VectorialLovera Lucas LeonelAinda não há avaliações
- Modelo de Trabajo Academico Física IDocumento6 páginasModelo de Trabajo Academico Física INavarro FelixAinda não há avaliações
- Módulo - Saber Parte 1Documento12 páginasMódulo - Saber Parte 1Tatiana Baños roblesAinda não há avaliações
- Trabajo - Energia y Potencia Fic 2010Documento97 páginasTrabajo - Energia y Potencia Fic 2010Crystal RiveraAinda não há avaliações
- Diseño y Análisis CinemáticoDocumento10 páginasDiseño y Análisis CinemáticoLeonardo MisaelAinda não há avaliações
- 4 Editor de CurvasDocumento15 páginas4 Editor de CurvasLollaAinda não há avaliações
- Algebra y Principios de Fisica Actividad 1 Unidad 4. ProblemasDocumento4 páginasAlgebra y Principios de Fisica Actividad 1 Unidad 4. Problemaskara7vel100% (2)
- EQUIPO1 E4 Evidencia4 LMEDocumento20 páginasEQUIPO1 E4 Evidencia4 LMEErick GuardiolaAinda não há avaliações
- Capítulo 4Documento68 páginasCapítulo 4ZabAinda não há avaliações
- Rata calcula tiempo para alcanzar comida y huir de depredadorDocumento18 páginasRata calcula tiempo para alcanzar comida y huir de depredadormercedeschapela50% (16)
- 26 Fisica IDocumento16 páginas26 Fisica IDavid Efraín Jovel FloresAinda não há avaliações
- Guia Fisica I T.M.Documento35 páginasGuia Fisica I T.M.Marco Cabrera QuijanoAinda não há avaliações
- Fisica Pre U Inv21 01 Analisis Dimensional y VectorialDocumento4 páginasFisica Pre U Inv21 01 Analisis Dimensional y VectorialBelenAinda não há avaliações
- Obtener Archivo RecursoDocumento122 páginasObtener Archivo RecursoAlex QuilicheAinda não há avaliações
- Estatica Cuerpo RigidoDocumento34 páginasEstatica Cuerpo RigidoMaximiliano BoschiAinda não há avaliações
- Actividades de Repaso U.D 7Documento2 páginasActividades de Repaso U.D 7mirpreciadosAinda não há avaliações
- Grado Sexto GuiasDocumento4 páginasGrado Sexto GuiasMarcela VargasAinda não há avaliações
- MVASDocumento17 páginasMVASbxkv9f2yrqAinda não há avaliações
- Cinemtica 3 ESODocumento13 páginasCinemtica 3 ESOMiller Edisson Hernández PeñaAinda não há avaliações
- Conservación de Momentum y Energía ExperimentoDocumento6 páginasConservación de Momentum y Energía ExperimentoJesus David Avellaneda MartinezAinda não há avaliações
- Ejemplo Trabajo MecanismosDocumento22 páginasEjemplo Trabajo MecanismosManuel CAinda não há avaliações
- Determinación de la aceleración de la gravedad mediante el análisis del movimiento en caída libreDocumento3 páginasDeterminación de la aceleración de la gravedad mediante el análisis del movimiento en caída libreJessi Astrid Jumbo JaramilloAinda não há avaliações
- 00042570462IE03S21068883TALLER2Documento5 páginas00042570462IE03S21068883TALLER2EduardoAinda não há avaliações
- Capitulo 4 - Estatica - Equilibrio - 1ra y 3ra Ley de NewtonDocumento18 páginasCapitulo 4 - Estatica - Equilibrio - 1ra y 3ra Ley de NewtonCesar CoaquiraAinda não há avaliações
- PC5 FUND. FÍSICA ListoDocumento30 páginasPC5 FUND. FÍSICA ListoLeonardo CastilloAinda não há avaliações
- PDF Movimiento Parabolico Mcu y Mcuv 02 Dinamicadocx DDDocumento30 páginasPDF Movimiento Parabolico Mcu y Mcuv 02 Dinamicadocx DDJuega EduardoAinda não há avaliações
- Física MecánicaDocumento18 páginasFísica Mecánicajuana valentina montealegre mosqueraAinda não há avaliações
- FÍSICADocumento6 páginasFÍSICAUnPocoDeTodo PeruAinda não há avaliações
- Movimiento Rectilíneo Uniformemente VariadoDocumento2 páginasMovimiento Rectilíneo Uniformemente VariadoPequeña DementeAinda não há avaliações
- Trabajo y EnergiaDocumento105 páginasTrabajo y EnergiaAlexis Espinoza0% (2)