Escolar Documentos
Profissional Documentos
Cultura Documentos
02 - ( - !) Clases de Neuronas PDF
Enviado por
jovi0Título original
Direitos autorais
Formatos disponíveis
Compartilhar este documento
Compartilhar ou incorporar documento
Você considera este documento útil?
Este conteúdo é inapropriado?
Denunciar este documentoDireitos autorais:
Formatos disponíveis
02 - ( - !) Clases de Neuronas PDF
Enviado por
jovi0Direitos autorais:
Formatos disponíveis
3.1.1. Clases de neuronas.
Cada parte del sistema nervioso se caracteriza microscpicamente por su tamao, su forma y arreglo de las neuronas que lo componen. Aunque algunas neuronas tienen muchas caractersticas internas en comn, sus formas varan considerablemente y esto permite que sean clasificadas de acuerdo a su estructura, funcin y tipo de neurotransmisor.
3.1.1.1. Clasificacin estructural
Las neuronas se clasifican estructuralmente de acuerdo a su nmero de procesos, entendiendo por este, terminacin o elongacin del cuerpo celular. En el sistema nervioso del embrin se observan algunas neuronas sin procesos o con un solo proceso; a estas neuronas se les llama apolares o neuropolares (Darnell, 1993). Algunas neuronas solo tienen dos procesos fundidos que en ocasiones parecen uno, se les llama seudounipolares, las cuales estn restringidas a grupos de cuerpos celulares neuronales localizados en los ganglios, en este tipo de neuronas los procesos cortos se ramifican del soma y se dividen en un proceso central que conducen impulsos hacia el cuerpo (Barr, 1994). Las neuronas que solo tienen dos procesos se les llaman bipolares, los procesos son generalmente una dendrita y un axn, y ocasionalmente dos dendritas. Este tipo de neuronas se ubica en reas especficas como los ganglios del octavo nervio craneal, la retina y el epitelio olfatorio (Travis, 1994). Las neuronas multipolares se caracterizan por poseer un axn y dos o ms dendritas. Son comunes en el sistema nervioso central. Las neuronas denominadas Golgi son clulas multipolares cuyos axones se extienden hacia distancias considerables hasta llegar a la clula Diana. Algunos ejemplos son las clulas piramidales de la corteza cerebral, las clulas de Purkinje del cerebelo y las clulas del asta anterior de la mdula espinal. Las neuronas multipolares que tienen axn corto que termina cerca del cuerpo celular de donde se origina se llaman neuronas de Golgi II; existen como clulas estrelladas o granulares de la corteza cerebral (Cooper, 1994).
3.1.1.2. Clasificacin funcional.
En el mbito funcional las neuronas se clasifican en sensoriales, motoras o interneuronas. Las neuronas sensoriales conducen impulsos desde los receptores hasta el cerebro y la mdula espinal; estos impulsos son informativos (visin, sonido, tacto, dolor, etc.). Estas neuronas son los componentes sensoriales aferentes de los nervios espinales y craneales; sus cuerpos celulares forman en gran parte la mdula espinal (raz posterior) y los ganglios craneales. Generalmente este tipo de neuronas posee una estructura de tipo seudounipolar o bipolar (Meyer, 1985). Las motoneuronas conducen el impulso desde el cerebro y la mdula espinal hasta los efectores (msculos y glndulas) lo que origina la contraccin de las fibras musculares o la secrecin glandular. Estas neuronas son el componente motor eferente de los nervios espinales y craneales. Por lo general su estructura es de tipo multipolar (Roselli, 1997). Existe otro tipo de neuronas cuyos somas y procesos permanecen en el SNC y se les conoce como interneuronas las cuales no tienen contacto directo con estructuras perifricas (receptores y efectores). Existe un grupo importante de interneuronas cuyos axones descienden y terminan en motoneuronas en el tronco del encfalo y en la mdula espinal; a estas clulas se les denomina motoneuronas altas. Las interneuronas son responsables de la modificacin, coordinacin, integracin, facilitacin e inhibicin que debe ocurrir entre la entrada sensorial y la salida motora. Por lo general su estructura es de tipo multipolar (Meyer, 1985).3.1.1.3.
Clasificacin por tipo de
neurotransmisor.
Neuronas colinrgicas Estas neuronas utilizan la acetilcolina (Ach) como neurotransmisor qumico, la cual se encuentra en los terminales de las placas motoras, que son las uniones entre el nervio y el msculo estriado, haciendo posible la contraccin de diferentes msculos y la estimulacin de las glndulas exocrinas. Para ejercer su accin posee dos tipos de receptores especficos: muscarnicos, localizados en el msculo liso y cardaco, son bloqueados por la atropina y nicotnicos, localizados en ganglios autnomos y en la unin neuromuscular, son bloqueados por el hexametonio y el curare (Rosselli, 1997). Neuronas catecolaminrgicas Dentro de este tipo de neuronas se identifican principalmente dos, de acuerdo al neurotransmisor que posean: noradrenalina (NA) o dopamina (DA). Las neuronas que utilizan como mensajero qumico la noradrenalina, actan bajo la excitacin generalizada del sistema simptico por la emocin y el ejercicio, produciendo efectos cardiovasculares: vasoconstriccin y estimulacin cardaca. La transmisin noradrenrgica tiene lugar en las sinapsis posganglionares simpticas en el msculo liso, msculo cardaco y glndulas exocrinas. La noradrenalina acta sobre dos tipos de receptores adrenrgicos: alfa y beta (Meyer, 1985). Las neuronas que utilizan dopamina como neurotransmisor provocan reacciones cardiovasculares similares a la de la adrenalina, estas acciones tienen lugar por la activacin de los receptores beta (vasodilatacin y estimulacin cardaca) y alfa (vasoconstriccin), adems, presentan propiedades especficas como el incremento del dbito renal, el flujo mesentrico y el coronario, acciones que se deben a la activacin de receptores dopaminrgicos denominados D, que estn asociados a la adenilciclasa (Bradford, 1988). Neuronas indolaminrgicas Este tipo de neuronas utiliza la serotonina como agente qumico que acta en la sinapsis neuronal. Este neurotransmisor se encuentra ubicado especialmente en las neuronas del tronco cerebral en la regin del raf medio del puente y del mesencfalo. Interviene en varios tipos de regulacin: mantenimiento del estado anmico, regulacin de la temperatura, analgesia, conducta sexual, agresividad,
control de los reflejos monosinpticos y del tono muscular e inhibicin del tono simptico. Los receptores especficos de la serotonina son bloqueados por la dietilamina del cido lisrgico y la metisergida (Meyer, 1985). Neuronas adrenrgicas Utilizan como neurotransmisor la adrenalina, se encuentran en la porcin rostral del bulbo raqudeo, sus axones ascienden gasta el hipotlamo o descienden a la mdula espinal; al igual que las neuronas noradrenrgicas actan sobre receptores adrenrgicos alfa y beta (Bradford, 1988). Neuronas GABArgicas Dichas neuronas transmiten el impulso nervioso mediante el GABA, el cual es una aminocido inhibitorio. Estn ubicadas en el cerebelo, cuernos dorsales de la mdula, retina, hipocampo y el hipotlamo, funcionan como transmisor inhibidor en el sistema nervioso de vertebrados e invertebrados (Barr, 1994). Otras Existen diversos neurotransmisores utilizados por las neuronas para conducir el impulso nervioso, dando diferentes nombres a las mismas. Dentro de estos encontramos: el glutamate (Glu) y el aspartato (Asp) considerados excitadores del sistema nervioso, la glicina (Gly) y la taurina considerados como inhibidores. El Grupo de Neuronas Recientemente existe un gran inters en enfocar el estudio de la mente intentando construir una teora global que partiendo desde la biologa conecta procesos cerebrales con procesos mentales. Uno de los autores que ha afrontado esta tarea es G. M. Edelman, premio Nobel de medicina en 1972. Edelman considera que la unidad bsica de procesamiento del cerebro es el grupo de neuronas, y presenta una teora que nos permite, al menos, iniciarnos en como surgen los pensamientos desde el cerebro. Vemosla brevemente. Edelman concibe el cerebro como un sistema selectivo, en el que la seleccin opera durante el tiempo de vida del sistema. Para sobrevivir, un organismo debe o heredar o crear criterios que le permitan clasificar el mundo en categoras perceptuales de acuerdo con sus necesidades adaptativas. Adems el mundo, incluso para el tiempo de vida de un organismo, est lleno de novedad, lo que exige que estos procesos de categorizacin puedan reestructurarse, renovarse y reiniciarse continuamente. El mundo, para el organismo, no se da por completo de una vez, sino que se construye en un proceso constante y continuo. Por tanto, los rganos que se encargan de estas tareas, es decir, el cerebro en ltimo trmino, debe ser flexible, pero tambin, como consecuencia, nico. Esto est de acuerdo con la enorme variacin funcional y estructural en muchos niveles: molecular, celular, anatmico, fisiolgico y conductual, que muestran los sistemas nerviosos por lo que, a pesar de las semejanzas en los individuos de una especie, el grado de variacin individual de cerebro en cerebro excede lo que poda tolerarse en un proceso de fabricacin de ingeniera. Visto as, cualquier teora interesante sobre la mente tendr que tener en cuenta estas observaciones y no podr generalizar, a menos que contemple en la descripcin estructural, orgnica, las fuertes diferencias y la exigencia de flexibilidad y variacin que impone la novedad del mundo. Por eso Edelman rechaza las teoras que contemplan el cerebro como un sistema que procesa informacin. A partir de aqu Edelman enuncia su tesis fundamental, a saber, que el cerebro es un sistema selectivo, en el que la seleccin opera durante el tiempo de vida del individuo. Para el desarrollo de esta tesis fundamental elabora lo que l denomina la teora de la seleccin del grupo de neuronas (TNGS). La TNGS es una teora de poblaciones que postula precisamente que la habilidad de los organismos para categorizar un mundo no etiquetado y para comportarse en l de una manera adaptativa surge no de la transferencia de instrucciones o
de informacin sino de procesos de seleccin bajo variacin. La TNGS considera que hay una generacin continua de diversidad en el cerebro. En el cerebro embrionario, hay variacin y seleccin en la migracin de poblaciones celulares y durante la muerte de clulas. Tambin en la formacin de las sinapsis. Y en el cerebro maduro, en la amplificacin diferencial de la eficacia de las sinapsis. Esto tiene como consecuencia la formacin de grupos neuronales y que el proceso es modificado continuamente por reentradas de seales. Veamos esto ms despacio. Postulados Bsicos de la TNGS La TNGS propone tres mecanismos para responder de la produccin de conductas adaptativas por parte de los organismos con sistemas nerviosos complejos: seleccin en el desarrollo, seleccin en la experiencia y reentradas de seales. Cada uno de estos mecanismos acta dentro y entre colectivos que consisten en cientos de miles de neuronas fuertemente interconectadas denominadas grupos de neuronas. Adems la teora propone que la seleccin a travs de la amplificacin sinptica diferencial est restringida por la accin de sistemas de valor derivados evolutivamente: sistemas neuromodulatorios dotados con proyecciones difusas que sealan el posible valor adaptativo para el organismo en su totalidad de la ocurrencia de ciertos eventos. 1. Variacin y Seleccin en el desarrollo. La diversidad estructural del sistema nervioso y los detalles de la neuroanatoma no estn estrictamente programados por el cdigo gentico. Esta diversidad surge durante el desarrollo en la regulacin epigentica dinmica de la divisin, adhesin, migracin y muerte de la clula, as como de la actividad neural misma. Durante la produccin del sistema nervioso se van creando neuronas y agrupaciones de clulas que permanecern o no dependiendo del refuerzo que otorgue la experiencia. La adhesin y migracin son gobernadas por unas series de molculas morforeguladoras llamadas CAMs (molculas de adhesin clular) y SAMs (molculas de adhesin de sustratos). Esto lleva a la formacin de repertorios primarios dentro de regiones anatmicas dadas que contienen un gran nmero de grupos de neuronas o circuitos locales.
2. Seleccin en la experiencia. Despus de que la mayora de las conexiones anatmicas de los repertorios primarios se han establecido, las actividades de los grupos de neuronas que funcionan particularmente continan siendo dinmicamente seleccionadas por mecanismos de cambios sinpticos subsiguientes dirigidos por la conducta y la experiencia. Ser la experiencia del organismo la que tender a reforzar algunos de los circuitos que se han establecido en la fase anterior dentro del grupo y entre grupos, otros tendern a desaparecer si el organismo no los requiere con la frecuencia que indicar su utilidad. De esta manera la maraa de conexiones que encontramos en un individuo de dos aos se ir simplificando para consolidar las
conexiones tiles dependiendo del tipo de experiencia que realice el organismo. La seleccin en la experiencia lleva finalmente a la formacin de repertorios secundarios de grupos neurales como respuesta a patrones particulares de seales.
3. Reentradas de seales. La seleccin en la experiencia conlleva correlaciones de seales estadsticas entre grupos de neuronas pre y postsinpticas, mejor que la transmisin de mensajes codificados de una neurona a otra. Si estas seales han de ser adaptativas tendrn que reflejar las seales que surjan en el mundo real. Esto se realiza sealando reentradas en y entre mapas neuronales. Estos recorridos neurales que relacionan hojas de receptores sensoriales con registros particulares del sistema nervioso central proveen un medio de reforzar regularidades espacio-temporales. Una reentrada puede definirse como una sealizacin paralela continua entre grupos de neuronas separadas que ocurre a lo largo de conexiones anatmicas ordenadas de manera bidireccional y recursiva. Es, pues, un proceso dinmico que es inherentemente paralelo y distribuido y que debe diferenciarse de la retroalimentacin. Las reentradas no tienen una direccin preferida y no tiene una funcin de input o output predefinido.
Una de las premisas fundamentales de la TNGS es, entonces, que la coordinacin selectiva de patrones complejos de interconexiones entre grupos de neuronas por medio de reentradas es la base de la conducta. Para la teora de Edelman, la reentrada es la base principal para poder trazar el puente entre la fisiologa y la psicologa. Este puente comienza a realizarse cuando mltiples mapas que estn conectados entre s por doble entrada a la conducta sensomotor del organismo comienzan a emparejar sus outputs creando un mapa global que da lugar a respuestas categoriales perceptivas. 4. Categorizacin Perceptiva: La discriminacin selectiva de un objeto o evento de otros objetos o eventos con propsitos adaptativos se produce con lo que Edelman denomina Pareja de Clasificacin. Pareja de Clasificacin: Es una unidad mnima que consiste en dos mapas funcionales diferentes conectados por doble entrada. Si, durante cierto periodo de tiempo, reentradas especficas conectan ciertas combinaciones de grupos de neuronas de un mapa con otras combinaciones en el otro, las funciones y
actividades en un mapa se conectan y correlacionan con las del otro mapa.
Si los mapas en cuestin estn conectados topogrficamente, entonces correlacionan acontecimientos en una localizacin espacial en el mundo. Este mapa global asegura la creacin de un bucle dinmico que continuamente coteja los gestos y posturas del organismo con el muestreo independiente obtenido de varias clases de seales sensoriales. El mapa global permite interaccionar con partes no concatenadas del cerebro (hipocampo, el ganglio basal y el cerebelo) en la medida en que estas estructuras estn conectadas con mapas locales mediante mltiples reentradas. Por supuesto, para la categorizacin perceptiva, que iniciar los procesos superiores y de conciencia, hay que suponer como condicin algn sistema de valor que se ha ido produciendo a lo largo de la evolucin de la especie. Edelman denomina valor a las estructuras fenotpicas que reflejan la seleccin evolutiva principal y que contribuyen a la conducta adaptativa y a la construccin del fenotipo. Estos sistemas de valor podran percibir la ocurrencia de conductas adaptativas y seleccionaran los eventos neuronales que las producen en funcin de los valores simples que contengan. Estos valores pueden expresarse en proposiciones tales como: Comer es mejor que no comer o ver es mejor que no ver. Los procesos que producen estos mapas globales (con sus patrones asociados de seleccin del grupo de neuronas y de cambio sinptico) crean una representacin espaciotemporal continua de objetos o de eventos. Dentro de estos procesos globales, los cambios de gran alcance en la fuerza sinptica tienden a favorecer la actividad mutua de reentradas de aquellos grupos cuya actividad ha sido correlacionada a travs de diferentes mapas durante la conducta pasada. Tales cambios sinpticos proveen la base para la memoria. De esta manera los recuerdos en los mapas globales no son almacenados, fijados o codificados de tal manera que puedan invocarse y recuperarse siempre de la misma manera como haramos con los registros de un disco duro de nuestros ordenadores. En lugar de ello, la memoria resulta de un proceso de recategorizacin continua, que, por su naturaleza, debe ser procedural y que debe conllevar una actividad motora continua y una repeticin frecuente. Con esto, categorizacin y memoria, obtenemos la condicin necesaria para el aprendizaje. Edelman consigue un paso ms en su teora cuando incluye, adems de los procesos de categorizacin y memoria, enlaces sinpticos entre los procesos que producen los mapas globales y la actividad de los centros hedonistas y el sistema lmbico de manera que satisfacen nuestras necesidades homeostticas, apetitivas y consumatorias. El aprendizaje se entiende entonces como la satisfaccin de necesidades del
organismo, necesidades que han creado expectativas al asociar estas necesidades con nuestras categorizaciones. Hasta aqu una explicacin estrictamente neurocientfica de los procesos iniciales por los cuales iniciamos nuestra representacin del mundo. Quiz resulte un poco complejo, pero en la continuacin del tema tendremos tiempo para ir integrando toda la explicacin.
3.2.1. Clasificacin de la neurogla
El sistema nervioso central de los mamferos contiene dos clases principales de neurogla, que se han clasificado teniendo en cuenta su tamao y morfologa celular: As se distinguen las clulas macroglales, es decir los astrocitos y los oligodendrocitos, y las clulas microglales. Estas clulas se originan en el ectodermo, a excepcin de las clulas microglales que tienen origen mesodermal. Se han descrito, asimismo, otros tipos de neurogla tales como las clulas glales radiales y las glas del sistema perifrico, es decir, las clulas de Schawnn (Bunde, 1968; Varon, 1979), las clulas telioglales (Bradford, 1988), las clulas glales satlites, las clulas ependimarias y la gla entrica. Mientras que los oligodendrocitos son un grupo de clulas muy homogneo, los astrocitos parecen ser una poblacin celular mucho ms heterognea. Los estudios clsicos distingen dos tipos de astrocitos, los fibrosos y los citoplsmicos (Cajal, 1909). Los astrocitos fibrosos se localizan preferencialmente en la sustancia blanca del SNC, su cuerpo celular es pequeo y presenta prolongaciones cilndricas que albergaran en su interior una alta densidad de filamentos intermediarios. Los astrocitos protoplsmicos, se encuentran fundamentalmente en la sustancia gris y sus prolongaciones son anchas, con un contenido menor en filamentos intermediarios. Estos filamentos intermediarios estan compuestos en su gran mayora por una protena denominada protena fibrilar cida de la gla (GFAP) (Bigmani y Dalh, 1974a). Sin embargo, existen otros tipos de clulas GFAP-inmunoreactivas dificilmente clasificables como astrocitos. Por ejemplo, las clulas radiales de la gla, presentes en el crtex cerebral durante el desarrollo (Levitt, 1980), las clulas de Bergmann del cerebelo (Bigmani y Dal h, 197 4b.) o las clulas de Mller de la retina (Newman, 1986). En cualquier caso, la caracterstica comn a todos los astrocitos, en todo momento de su desarrollo, es la presencia y expresin de la GFAP (Fedoroff, 1990), por ello, puede utilizarse para caracterizar indistintamente cualquier tipo de astrocito. La clasificacin de astrocitos fibrosos o protoplsmicos por su localizacin en el SNC no puede ser utilizada como un reflejo exacto de la realidad, dado el grado de diversidad existente dentro de esta familia de clulas. De hecho, en
cultivos de nervio ptico de rata, una regin del sistema nervioso ampliamente
empleada para el estudio de la gla ya que carece de cuerpos neuronales, se han caracterizado dos tipos de astrocitos GFAP-inmunoreactivos, denominados astrocitos tipo 1 y astrocitos tipo 2 (Raff, 1989a). Estos dos tipos difieren en cuanto a su morfologa, fenotipo antignico, linaje y capacidad proliferativa (Miller y col., 1989; Raff, 1989a). La mayor parte de los astrocitos tipo 1 son clulas planas con forma poligonal semejantes a un fibroblasto. Los astrocitos tipo 2, tienen un cuerpo celular ms pequeo y estn profusamente ramificados. Estos dos tipos de astrocitos difieren, adems, en cuanto a su respuesta a factores de crecimiento. La administracin de factor de crecimiento epidrmico (EGF) o de factor de crecimiento glal (GGF) slo induce la proliferacin de los astrocitos tipo 1 (Miller y col., 1989). En otras regiones del SNC se ha puesto de manifiesto la existencia de estos dos tipos de astrocitos empleando cultivos primarios de cerebro (Abney, 1981) y de cerebelo (Levi, 1986). La existencia de los astrocitos tipo 2 se ha puesto de manifiesto in vivo por la presencia de clulas positivas al GFAP y al antgeno A2B5 en suspensiones celulares preparadas a partir de nervio ptico y cerebro de ratas de una semana de vida postnatal (Miller, 1985; Williams, 1985). La proporcin de este tipo de astrocitos es muy baja en cerebro adulto, por lo que se discute su funcin, e incluso, su existencia (Noble, 1991a).
3.2.2. Macrogla
Los orgenes de las clulas gliales en la literatura de neuroanatoma se extiende desde el ao de 1846, en el que aparecieron los trabajos de Rudolph Virchow. Este hecho histrico ha sido documentado ampliamente por Glees, Kuffler y Nicholls. La definicin de clulas gliales se deriva esencialmente de un proceso de exclusin. Pueden definirse como clulas del tejido nervioso que no son
neuronas. Sin embargo, las clulas gliales poseen tambin uno o dos componentes bioqumicos por los que pueden distinguirse de otras clulas (Bradford, 1988). Los matices funcionales atribuidos en la actualidad a las clulas neurogliales son: * Soporte mecnico de las neuronas (astrocitos y oligodendrocitos). * Produccin de la vaina de mielina (oligodendrocitos). * Captacin rpida y, por tanto, inactivacin de neurotransmisores qumicos liberados por las neuronas (astrocitos). * Formacin del tejido cicatricial despus de lesiones cerebrales (astrocitos). * Eliminacin de residuos de tejido local despus de la muerte celular (astrocitos) (Gorovits et al., 1997; Newcomb et al., 1997). * Constitucin de un sistema de fibras entre la sangre y las neuronas (astrocitos). * Control de la composicin del lquido extracelular. Niveles de los iones de potasio y calcio (astrocitos) (Bradford, 1988).
Tipos de clulas gliales Teniendo en cuenta el tamao, forma y situacin se distinguen varios subgrupos de clulas, gliales. La gran familia de clulas gliales puede dividirse en macroglas, que son las clulas de mayor tamao, y microglas las menores. Entre la macrogla est la gla radial, astrogla, oligodendrogla y gla perifrica (Bradford, 1988). Las clulas gliales de mayor tamao son los astrocitos. Su pericarin, de 18 a 20 m de dimetro, posee un ncleo plido de gran tamao, grnulos de glucgeno y en algunos casos abundantes filamentos gliales
(gliofilamentos). Sus prolongaciones membranosas, que son largas y estrechas, proporcionan la forma caracterstica de estrella sealada en su nombre. Estas estructuras delgadas y las dilataciones que se aprecian en sus extremidades (pies terminales) rodean la superficie de los capilares sanguneos, dejando solamente unos huecos pequeos para la difusin de las sustancias desde los endotelios capilares a travs de la lmina basal y los espacios extracelulares restringidos del encfalo. Los pies terminales, que son una caracterstica especial de los astrocitos se hallan tambin
superpuestos a las membranas neuronales y a las membranas piales que cubren la superficie enceflica externa. La oligodendrogla constituye otro subgrupo glial importante. Estas clulas se distinguen claramente de los astrocitos por sus pequeos cuerpos celulares (3 a 5 m de dimetro) con pocas prolongaciones celulares. La oligodendrogla se halla en la sustancia blanca y en la sustancia gris. La de la sustancia blanca conocida como oligodendrogla interfascicular, es responsable de la formacin de la vaina de mielina aislante alrededor de los axones; en la sustancia blanca del cerebro en desarrollo, sus prolongaciones celulares se distinguen continuas con las vainas de mielina que estn produciendo ininterrumpidamente. En la sustancia gris la oligodendrogla satlite se halla frecuentemente en ntima relacin con los cuerpos celulares. La microgla es la neurogla ms pequea, con dimetro de 2 a 3 m, por lo que pueden distinguirse fcilmente de la macrogla. Su variable morfologa hace que sea difcil de definir y estudiar, sin embargo, estas son las clulas encargadas del sistema inmune del SNC (Bradford, 1988). Estas clulas se distinguen por la facilidad con que son teidas con las sales de plata, por sus ncleos pequeos y alargados, por su escaso citoplasma y por su multitud de prolongaciones celulares pequeas (Bradford, 1988). Cuando estas clulas se exponen a estmulos que provocan inflamacin u otro tipo de insulto al tejido nervioso, la microgla se transforma rpidamente desde un estado de reposo pasivo a una fagocitosis activa acompaada de proliferacin y migracin por el tejido. Es en esta fase cuyo su similitud con los macrfagos es evidente (Bradford, 1988). Las clulas gliales radiales, descritas por primera vez a finales del siglo pasado, han sido consideradas en la actualidad como un grupo especial de neurogla que tiene una importancia considerable. Estas clulas aparecen durante el desarrollo enceflico para transformarse despus en otros tipos gliales (por ejemplo, astrocitos) a medida que madura el cerebro. Muchas de estas clulas poseen una forma alargada, frecuentemente bipolar, con dos o ms prolongaciones celulares importantes que se extienden a distancias relativamente largas a travs de tejido nervioso y que terminan frecuentemente en las membranas superficiales o en las paredes de los vasos sanguneos. Al menos hay dos tipos de gla radial que sobreviven en el cerebro adulto humano: las clulas de Mller y la gla de Bergman. Las clulas de Mller se hallan en la retina y muestran una morfologa y disposicin caractersticas; son muy alargadas y se extienden entre las membranas limitantes interna y externa de la retina. La gla de Bergman conformada por clulas gliales peculiares, situadas en la capa molecular en la corteza cerebelosa de los mamferos proyecta varias prolongaciones celulares alargadas a travs de la capa molecular hasta la superficie interna de la membrana pial, donde forman pies terminales cnicos. Los cuerpos celulares de la gla de Bergman estn localizados en la capa de clulas de Purkinje (voluminosas neuronas ramificadas de la capa media de la corteza cerebelar) (Bradford, 1988). Los astrocitos como su nombre lo sugiere, son clulas en forma de estrella, con numerosas prolongaciones citoplsmicas ramificadas. Sus ncleos son grandes,
ovoides o esfricos y tienen color plido, con pocos grnulos finos de cromatina distribuidos principalmente en la periferia en unin ntima con la membrana nuclear. Los nuclolos no son patentes. El citoplasma incluye los organelos corrientes y puede observarse claramente un centrosoma. Puede haber pigmento lipocrmico (Lesson, 1976). Sus prolongaciones celulares fibrosas caractersticas, as como su pericarin, estn rellenas de gliofilamentos cuyo componente proteico ms importante, llamado protena cida fibrilar de la gla (PAFG), ha sido posible aislarlo recientemente. Los anticuerpos frente a esta protena, marcados con sustancias fluorescentes, posibilitan visualizar claramente los astrocitos (Bradford, 1988; Lesson, 1976). En ambos tipos las clulas tienen aproximadamente 8 micras; el citoplasma perinuclear se tie plidamente, por la pobreza en retculo granuloso y en ribosomas libres, y contiene algunas mitocondrias, complejos de Golgi, microfilamentos y, de ordinario, gran nmero de lisosomas y muchas partculas de glucgeno. El ncleo es ovoide y de forma irregular. Los astrocitos tienen gran nmero de prolongaciones citoplsmicas, que se tien poco y contienen algunos microfilamentos. Estas prolongaciones rodean y separan las neuronas; algunas tienen expansiones terminales que establecen contacto con los vasos sanguneos (pies perivasculares o pies terminales astrocticos) epndimo y piamadre en la superficie del SNC. Donde los astrocitos, o sus prolongaciones, establecen contacto con los astrocitos vecinos o con neuronas vecinas, puede haber desmosomas y uniones de espacio vaco. Las prolongaciones de los astrocitos y otros elementos gliales se encuentran entre los cuerpos neuronales, y sus axones y dendritas constituyen el neurpilo (Lesson, 1976). Los astrocitos pueden ser protoplasmticos (astrocitos tipo-1) que son los que tienen prolongaciones ramificadas y se encuentran principalmente en la sustancia gris dispersa entre los cuerpos neuronales; constituyen una gran proporcin del volumen citoplsmico de la sustancia gris (Bradford, 1988; Lesson, 1976). No contienen abundantes estructuras filamentosas y sus prolongaciones tienden a ser laminares o membranosas (Lesson, 1976). Tambin pueden ser fibrosos (astrocitos tipo-2), o clulas en forma de araa, que tienen prolongaciones ms largas y ms delgadas, contienen numerosas fibrillas citoplsmicas y estn situadas principalmente en la sustancia blanca, situados entre los haces de axones mielinizados (Lesson, 1976). Desarrollo de las clulas macrogliales Las primeras clulas gliales que aparecen en el perodo embrionario son las clulas gliales radiales (Cameron, 1991). De hecho, las neuronas emplean estas clulas como orientacin para encontrar su lugar definitivo en el sistema nervioso. Al final de la gestacin, las clulas gliales radiales se transforman en astrocitos fibrosos. La mayora de los astrocitos aparecen ms tardamente en el desarrollo, aproximadamente en el nacimiento ; su nmero se va incrementando hasta despus de algunas semanas de vida postnatal. Los astrocitos que se originan durante el perodo embrionario se desarrollan a partir de la zona ventricular de la placa neural, y los que se
originan postnatalm ente provienen de la zona subventric ular (SnchezAbarca, 1998). Los oligodendr ocitos surgen en perodo postnatal, aunque su diferenciac in o, lo que es lo mismo, la mielinizacin, comienza en la rata una semana despus de su nacimiento y alcanza su mximo el da 21 de vida postnatal. En el hombre, la sntesis de mielina se efecta, aproximadamente, desde la semana 25 de gestacin hasta los 20 aos de vida adulta (Gould, 1985; Martnez, 1989). Aunque esta pueda ser una consideracin general, la realidad es que el tiempo y el origen de los astrocitos y oligodendrocitos cambia dependiendo del rea del SNC analizada. As, una de las cuestiones ms importantes relacionadas con el linaje glial es si comparten sus precursores con las neuronas, es decir: derivan de una clula progenitor multipotencial (Noble, 1991). La respuesta a esta cuestin parece depender del rea del cerebro analizada. A continuacin se resume el linaje glial en cuatro regiones diferentes del SNC: * Desarrollo de las clulas macrogliales en la corteza cerebral: en este nivel del SNC hay un alto nivel de complejidad. La primera controversia del linaje glial de la corteza cerebral es si las clulas derivan de un precursor celular multipotencial o no (Davis y Temple, 1994; Wolswijk y Noble, 1989). As, algunos experimentos sugieren que la zona ventricular de la corteza est compuesta por una mezcla de diferentes precursores celulares. La mayora de ellos genera un slo tipo de clulas (neuronas, astrocitos u oligodendrocitos) y el resto genera neuronas y un slo tipo de clulas de la gla. Sin embargo, cuyo se cultivan clulas progenitoras de la zona ventricular, un pequeo porcentaje de estas clulas son pluripotenciales, es decir, son capaces de generar neuronas, astrocitos y oligodendrocitos (Davis y Temple, 1994). Estudios realizados tanto in vivo como in vitro sugieren que en el proceso de gliognesis las clulas van reduciendo su multipotencialidad a medida que avanza el desarrollo. As, una vez que los precursores gliales y neuronales estn diversificados, el linaje glial puede ser seguido por el origen de tres diferentes precursores celulares (ver figura 1). Uno de estos precursores dar lugar a las clulas gliales radiales, que son las primeras en aparecer en el SNC. Despus estas clulas gliales radiales se transformarn en clulas Bergman, clulas de Mller, clulas ependimales. Por otro lado, los astrocitos tipo-1 se generarn a partir de un precursor propio. Los oligodendrocitos se originarn a partir de las clulas de un precursor propio(Barres et al., 1992). Los oligodendrocitos se originarn a partir de las clulas progenitoras O-2A (precursores de oligodendrocitos y astrocitos tipo-2). Estas clulas progenitoras O-2A, son bipotenciales in vitro y pueden originar, tambin, una segunda poblacin de astrocitos, que son los astrocitos tipo-2 (Wolswijk y Noble, 1989). * Desarrollo de las clulas macrogliales en el nervio ptico: el nervio ptico contiene los axones de las clulas ganglionares de la retina, las dos clases de clulas macrogliales (astrocitos y oligodendrocitos) y las clulas microgliales
(Small et al., 1987). Los astrocitos se desarrolla a partir de clulas neuroepiteliales que forman el primitivo nervio ptico, mientras que los oligodendrocitos se desarrollan a partir de clulas precursoras que migran al nervio ptico en tempranos estadios del desarrollo (Small et al., 1987). Los oligodendrocitos derivan de precursores celulares bipotenciales O-2A, ya que en cultivo son capaces de originar tanto oligodendrocitos como astrocitos tipo2, dependiendo de las condiciones de cultivo (FfrenchConstant, 1986a; Ffrench-Constant, 1986b; FfrenchConstant, 1986c; Raff, 1989). Los astrocitos aparecen en el nervio ptico de rata en el da 16 del perodo embrionario y van aumentando su nmero hasta la sexta semana postnatal (Burne y Raff, 1997). Curiosamente, los axones de las clulas ganglionares de la retina dirigen la proliferacin de los astrocitos (Raff, 1989). Dado que la muerte celular normal no parece jugar un papel importante en el ajuste del nmero de astrocitos en el nervio ptico de rata, los axones son los responsables del nmero final de astrocitos, debido al control que ejercen sobre su proliferacin (Burne y Raff, 1997). Los oligodendrocitos aparecen por primera vez despus del nacimiento, su nmero alcanza el mximo en el da 21 postnatal y disminuye ligeramente en el nervio ptico adulto (Raff, 1989). Los astrocitos tipo-2 se detectan en el nervio ptico de rata a partir de la primera semana de vida postnatal, aunque en un nmero muy pequeo. * Desarrollo de las clulas macrogliales en la retina: en la retina existe una gran variedad de clulas diferentes que derivan de las clulas precursoras multipotenciales . Estas clulas precursoras retendrn su multipotencialidad mientras continen dividindose (Turner y Cepko, 1987). Estos precursores estn capacitados para generar tanto neuronas como fotorreceptores o clulas gliales Mller (Germer et al., 1997). La nica excepcin son los astrocitos; este tipo celular glial es el nico no encontrado en los clones formados a partir de los precursores multipotenciales de la retina (Watanabe y Raff, 1988). * Desarrollo de las clulas macrogliales en la mdula espinal: las clulas neurales de la mdula espinal se desarrollan a partir de clulas progenitoras pluripotenciales. De hecho, las clulas neuroepiteliales procedentes del tubo neural caudal en cultivo pueden dar origen a neuronas, astrocitos y oligodendrocitos. Por tanto, estas clulas neuroepiteliales se comportan como precursores celulares multipotenciales, capaces de generar mltiples derivados neurales.
Microglia: Son las clulas ms pequeas y se hallan dispersas en todo el SNC. En sus pequeos cuerpos celulares se originan prolongaciones ondulantes ramificadas que tienen numerosas proyecciones como espinas. Son inactivas en el SNC normal, proliferan en la enfermedad y son activamente fagocticas (su citoplasma se llena con lpidos y restos celulares). Son acompaados por los monocitos de los vasos sanguneos vecinos. Epndimo: Las clulas ependimales revisten las cavidades del encfalo y el conducto central de la mdula espinal. Forman una capa nica de clulas cbicas o cilndricas que poseen microvellosidades y cilias. Las cilias son mviles y contribuyen al flujo de lquido cefaloraqudeo.
3.2.2.1. Funciones de los astrocitos
Los astrocitos diferenciados tienen distintas funciones entre las que se destacan: regulacin de la composicin inica del lquido extracelular del sistema nervioso central, induccin de la formacin de la barrera hematoenceflica (BHE), actuar de soporte y gua de las neuronas durante la migracin y ayudar a mantener los niveles de los intermediarios del ciclo de los cidos tricarboxlicos en las neuronas (Kimelberg y Norenberg, 1989; Miller y col., 1989).
Durante el desarrollo embrionario una de las funciones principales de los astrocitos es la de servir de soporte y gua en la migracin de las neuronas postmitticas, as como, conducir la emisin de prolongaciones axnicas. En el cerebro adulto, los astrocitos realizan esta misma funcin durante la regeneracin axonal y la formacin de nuevas sinapsis. Parece ser que entre las sustancias implicadas en este mecanismo estn las molculas de adhesin celular nerviosa (NCAM) y las N-caderinas (Edelman, 1983; Takeichi, 1988). En cocultivos de neuronas con astrocitos tipo 1 astrocitos tipo 2 se ha demostrado que el crecimiento axonal se favorece cuando se emplean cultivos de clulas neonatales en vez de clulas adultas. De estas observaciones se concluye que las diferencias en la composicin molecular de las membran as astroctic as, son las responsables del crecimiento de las neuritas (Geisert, 1991; Smith, 1993). Los capilares cerebrales estn rodeados, casi en su integridad, por los pies terminales de las fibras astrocticas. A diferencia de los que ocurre en otros tejidos, las clulas endoteliales de los capilares cerebrales estn fuertemente conectadas por uniones estrechas (tight junctions). Este hecho impide el transporte paracelular de muchas sustancias. En este sentido, los astrocitos inducen a las clulas endoteliales de los capilares cerebrales a formar las uniones estrechas y a sintetizar las enzimas carcteristicas de la barrera hematoenceflica (Janzer y Raff, 1987). Las neuronas debido a la transmisin sinaptica liberan una serie de neurotransmisores al medio (glutamato, aspartato, GABA, etc.). Este hecho trae consigo una disminucin de la concentracin de intermediarios del ciclo de los cidos tricarboxlicos, principalmente oxalacetato y ! -cetoglutarato, que son fundamentalmente, los precursores de estos neurotransmisores. En este sentido, estudios recientes han puesto de manifiesto que los astrocitos podran estar implicados en el mantenimiento de los niveles de los intermediarios del ciclo de los cidos tricarboxlicos en las
neuronas (Kaufman y Driscoll, 1992). Los niveles de sodio y potasio deben estar regulados muy estrictamente en el espacio que rodea las neuronas, de manera que pueda llevarse a cabo los potenciales de accin. En otros tejidos, los iones externos residen en el espacio intersticial, que en el cerebro, est ocupado por las finas prolongaciones astrocticas. Este hecho di lugar a la hiptesis llamada amortiguacin espacial de potasio (Orkand y col., 1966). Esta hiptesis propone que los astrocitos retiran el potasio sobrante del espacio extracelular procedente de la actividad neuronal y los transfieren a zonas con baja concentracin de potasio. La fuerza determinante de este proceso sera el aumento local de potasio extracelular puesto que, los astrocitos captaran el potasio debido a la alta permeabilidad que presentan a este in (Erecinska, 1993; Kuffler, 1966a). Ms tarde lo transmitirian de unos astrocitos a otros a travs de las llamadas uniones comunicantes (gap junctions) (Gardner-Medwin, 1986; Sez y col., 1993). En efecto, el acoplamiento entre astrocitos a travs de las uniones comunicantes aumenta su capacidad de amortiguar espacialmente el potasio (Mobbs y col., 1988). Recientemente se ha comenzado a conjeturar sobre la posibilidad de que los astrocitos tengan una funcin mucho ms activa en el SNC y no un papel meramente protector de las neuronas. Se ha propuesto que los astrocitos presentan un tipo de excitabilidad basada directamente en la dinmica del in calcio intracelular y que es esencialmente independiente del potencial de membrana (Cornell-Bell y Finkbeiner, 1991; Cornell-Bell y col., 1990). As, en los astrocitos se expresan una amplia variedad de receptores funcionales para agentes neuroactivos (Dermietzel, 1991a; Cornell-Bell y col., 1990; Jensen, 1990; Salm y McCarthy, 1990). En estos estudios se ha establecido que el glutamato y otros neurotransmisores pueden provocar oscilaciones en los niveles del in calcio intracelular y la propagacin de estas ondas de calcio, creando en definitiva una forma de exitabilidad, basada en las corrientes de Ca+2 (Cornell-Bell y col., 1990; Jensen y Chiu, 1991b; Jensen y col., 1991a). Esta forma de excitabilidad comienza con la liberacin de iones calcio de los depositos intracelulares (Cornell-Bell y Finkbeiner, 1991) y continua con la oscilacin en los niveles de calcio, que se propaga dentro del astrocito exitado a los astrocitos adyacentes, a travs de las uniones comunicantes. Recientemente, se ha demostrado que las inervaciones aferentes de las neuronas glutaminrgicas provocan la formacin de las ondas de calcio en los astrocitos (Dani y col., 1992;
Nedergaard, 1994).
3.2.2.2. Oligodendrocitos y clulas de Swhann. Organizacin de las membranas de mielina.
Los axones de las neuronas estan rodeados de una capa lipdica, la mielina, que favorece la propagacin de los potenciales de accin. Dentro del SNC, los oligodendrocitos son las clulas encargadas de formar la mielina. Esta capa lipdica deriva de la membrana plasmtica de los oligodendrocitos, aunque su composicin difiere de la que presenta la membrana progenitora. En peso seco, la mielina esta compuesta por un 7075% de lpidos y un 25-30% de
protenas. La mielinizacin comienza, en la rata, aproximadamente una semana despus del nacimiento, siendo ms activa a la tercera semana postnatal declinando despus progresivamente. En el hombre, el proceso de mielinizacin abarca desde las 25 semanas de gestacin hasta los 20 aos de edad (Bourre, 1989; Gould, 1985; Martnez, 1989). La mielinizacin requiere la interaccin entre los axones y las membranas plasmticas de los oligodendrocitos. Parece que la produccin de mielina por los oligodendrocitos empieza cuando los axones alcanzan un cierto dametro. Cronolgicamente la mielinizacin coincide en parte, con el proceso de sinaptognesis. Se ha sugerido que las neuronas estimulan la diferenciacin de los oligodendrocitos y su capacidad para formar mielina (Vernadakis, 1988). No obstante, parece que los oligodendrocitos estn intrnsicamente programados para formar membranas mielinizantes, aunque este proceso se estimula por las neuronas (Lopes-Cardozo, 1989).
Los oligodendrocitos diferenciados presentan como marcadores los galactocerebrsidos y la protena bsica de mielina (MBP). Asimismo, durante la diferenciacin de los oligodendrocitos aumentan las actividades de la glicerol-3-fosfato deshidrogenasa (EC 1.1.1.8) y de la fosfodiesterasa (EC 3.1.4.1). Probablemente, estas enzimas estn implicadas en la mielognesis (Saneto, 1985). Los glucocorticoides favorecen la direnciacin de los oligodendrocitos y la mielinizacin, ya que inducen la expresin de la MBP, de la protena proteolipdica y de la glicerol-3-fosfato deshidrogenasa (Kumar, 1989). Asimismo, las hormonas tiroideas favorecen la mielinizacin (Dussault y Ruel, 1987; Ferreiro y col., 1990), mientras que la insulina y el factor de crecimiento insulnico estimulan el desarrollo de los oligodendrocitos en cultivo, favoreciendo la expresin de la glicerol-3-fosfato deshidrogenasa (Lopes-Cardozo, 1989).
Las microglias son clulas representantes del sistema inmunolgico en el SNC. Si bien pueden permanecer en estado quiesciente durante largos periodos de tiempo, pueden modificar su comportamiento en respuesta a diversas seales provenientes del entorno celular. La transformacin desde un estado inactivo hasta macrfagos fagocticos cerebrales, est estrctamente controlada y acompaada por la produccin de varios productos de secrecin. stos incluyen citokinas, aminocidos excitatorios, y radicales libres por medio de los cuales las microglias activadas se comunican con otras clulas del cerebro y del sistema inmunolgico. De ste modo, representan una defensa esencial del husped, tambin un sistema de reparacin, pero pueden ser responsables de la destruccin de tejidos y de la muerte neuronal, segn cul sea el balance entre seales activadoras e inhibitorias. Por esta razn, los macrfagos cerebrales son considerados hoy, como un elemento importante en la patogenia de neuropatologas agudas, crnicas y neurodegenerativas. Adems, representan un sitio posible de accin de futuros frmacos neuroprotectores.
3.2.3.Biologa de las microglias y los macrofagos cerebrales
patolgicas.
Activacin de la microglias en dife ren tes con dici one s
Se reconoce que las microglias tienen origen en los monocitos sanguneos e invaden el cerebro muy tempranamente durante el desarrollo, constituyendo el 20% de la poblacin de clulas gliales en roedores. Luego, en la etapa postnatal cambian su morfologa y se diferencian en clulas altamente ramificadas con poca actividad fagoctica y enzimtica. La funcin de stas microglias residentes en cerebros sanos es desconocida. Cuando sobreviene un estmulo fisiolgico o patolgico, las microglias se activan constituyendo macrfagos cerebrales. Este proceso de activacin se caracteriza por proliferacin, aumento en la expresin de molculas propias de los macrfagos (por ejemplo del nmero de antgenos del complejo de histocompatibilidad (MHC), y finalmente, por cambios morfolgicos (adoptando un fenotipo similar a los macrfagos ameboides con propiedades fagocticas y migratorias). Las microglias activadas cumplen un rol clave en los procesos inmunolgicos del SNC; actan como clulas fagocticas, pueden presentar antgenos a linfocitos-T y tienen capacidades citotxicas que se llevan a cabo por varios mecanismos . La activacin de microglias en el SNC puede ser estimulada experimentalmente, in vivo, en respuesta a lesiones isqumicas, inflamatorias, qumicas y mecnicas. Finalmente, la activacin ha sido comprobada en diversos trastornos neurolgicos humanos, incluyendo daos agudos (trauma e isquemia cerebral), y enfermedades crnicas, (Esclerosis mltiple, encefalopata por HIV, Enfermedad de Alzheimer y Enfermedad de Parkinson). Las relaciones entre microglias y enfermedades neurodegenerativas son complejas pus incluyen signos de activacin y toxicidad de macrofagos cerebrales en regiones del cerebro pero tambin la potencialidad de que las microglias puedan cumplir funciones de sostn trfico para neuronas. Similitud entre los macrfagos cerebrales y los monocitos que invaden el parnquima del SNC. En la mayor parte de los estudios experimentales, las microglias residentes se activan, y los monocitos provenientes de la sangre invaden el parnquima cerebral. La contribucin individual de los dos tipos de clulas en la respuesta inflamatoria no se conoce con certeza. Usando quimeras de mdula sea irradiada , se comprob que no slo los monocitos sanguneos responden a la inflamacin inducida por virus, sino tambin las microglias residentes. En ambos casos, aumenta la expresin del receptor C3 del complemento, el receptor CD4 y los antgenos MHC de clase I. Las microglias son los principales fagocitos cuando el grado de dao tisular es menor y cuando no hay destruccin de la organizacin parenquimal. Cuando el dao es masivo, las microglias residentes son asistidas por un aflujo de monocitos sanguneos, los cuales adoptan rpidamente un fenotipo microglial cuando penetran en el parnquuima del SNC. De sta forma, no es posible descriminar las microglias activadas de los monocitos sanguneos, en base a su morfologa o propiedades inmunocitoqumicas.
Mecanismos de la activacin de las microglias.
De una manera general, las clulas microgliales se activan en respuesta al dao
celular y estn involucradas en procesos autoinmunes del sistema nervioso mediados por clulas T. La reaccin microglial se puede observar incluso si la lesin inicial es lejana (como por ejemplo en el sistema nervioso perifrico) y es de inicio rpido (luego de algunas horas del dao cerebral). Los cambios estructurales observados en el parnquima cerebral en todos los modelos son precedidos por alteraciones moleculares tempranas, tal como la induccin de la expresin de antgeno MHC. En estadios ms tardos de la enfermedad, la respuesta microglial es mantenida debido a la presencia de detritos celulares relacionados a la degeneracin axonal y la desmielinizacin. La activacin microglial parece ser independiente de la forma del estmulo patolgico, ya que en todos los modelos, ocurren cambos uniformes, incluyendo: 1. Proliferacin 2. Transformacin en clulas fagocticas con morfologa macrofgica 3. Estimulacin de la expresin de molculas de la superficie celular, tales como el receptor C3 para el complemento o el determinante MUC102 ; o los antgenos MHC.
Es de inters observar el hecho de que un aumento en la expresin de antgenos MHC indica un estado general de activacin microglial y no significa de por s que se est llevando a cabo una respuesta inmune en el tejido. El rol de la expresin del antgeno MHC clase I (Ia) en las funciones no inmunes no est claro. Sin embargo, diversos estudios han sugerido que la molcula Ia puede sealizar la activacin, a travs de la proten-quinasa C, dando lugar a la proliferacin y diferenciacin. El ligando natural para la sealizacin Ia en rutas no inmunes en el cerebro permanece sin identificar.Microglias en lesiones
traumticas del SNC.
Una barrera hematoenceflica intacta tiende a favorecer la participacin de las microglias, mientras que la ruptura de la misma favorece la invasin de derivados monocticos. Por ejemplo, una herida penetrante del SNC que cause un dao directo de los vasos sanguneos con ruptura de la barrera hematoenceflica y destruccin neuronal aguda, resulta en la diferenciacin de las microglias en un fenotipo activado y en una activacin en la expresin de molculas antignicas de superficie, (CD4 y antgeno MHC clase I). En cierto modo, la respuesta inflamatoria aguda frente a un dao focal traumtico es similar al observado en otros tejidos, con reclutamiento de neutrfilos y monocitos en los bordes de la herida. Sin embargo, comparado con el sistema nervioso perifrico y otros tejidos corporales, el nmero de clulas reclutadas en las lesiones del SNC es mucho menor, y la activacin microglial es ms retardada. Esta diferencia, que se observa luego del dao en el nervio ptico comparado con el nervio citico y en la degeneracin Walleriana luego de una axotoma, puede atribuirse a diferencias en la barrera endotelial y a diferentes seales quimiotcticas involucradas. La degeneracin retrgrada de los cuerpos neuronales que transmiten el trauma a sus axones es una forma comn de muerte neuronal. Un modelo estudiado por Kreutzberg y colegas es la respuesta de las motoneuronas frente a un dao en el nervio facial. Como los cuerpos celulares de las motoneuronas en el ncleo facial estn sometidas a cromatolisis, las microglias residentes proliferan rpidamente y se activan. stas ltimas se localizan muy cerca de las neuronas comprometidas y se ha sugerido que estn involucradas en la eliminacin de las sinapsis. Participacin de las microglias en las enfermedades autoinmunes Debido a que son clulas que presentan antgenos de superficie, las microglias tienen muchas posibilidades
de participar activamente en la patognesis de las enfermedades autoinmunes del cerebro. En ratas sometidas a encefalopatas alrgicas experimentales (EAE), un modelo para enfermedades desmielinizantes, la inyeccin intravenosa de clulas T dirigidas contra de la protena bsica de la mielina, da por resultado la inflamacin del parnquima cerebral. En el infiltrado celular que se produce como consecuencia se encuentran macrfagos, linfocitos T y algunos linfocitos B. El proceso se iniciara por la liberacin de citokinas provenientes de clulas T, incluyendo interferon g (IFN-" ) con capacidad de activar in vitro las microglias induciendo la expresin de antgeno MHC clase I y II. Por tanto, las clulas microgliales interactan con clulas T de diferentes maneras, pudiendo adoptar diferentes fenotipos. El papel central de las clulas macrofgicas en la EAE est evidenciada en que la respuesta inflamatoria desaparece cuando se eliminan los macrfagos. En las neuritis alrgicas experimentales del PNS, el contacto directo de clulas microgliales con clulas T invasoras no tiene lugar. Sin embargo, se observa una activacin temprana de las clulas microgliales que rodean las motoneuronas en el SNC. Esto sugiere que la respuesta de las microglias centrales en las enfermedades autoinmunes est mediada por clulas T. Las microglias en la isquemia focal del cerebro. En la isquemia cerebral focal , la activacin microglial ocurre incluso cuando no hay infiltracin de linfocitos T. En algunas regiones cerebrales suceptibles al dao celular, la aparicin de microglias activadas parece ser un proceso rpido, que precede incluso la degeneracin inminente de las neuronas, para lo cual la presencia de la microglias pueden representar un maracador sensible y temprano. En otras regiones cerebrales, como las regiones CA3 del hipocampo, la reaccin microglial se observa incluso en ausencia de dao neuronal concomitante luego de una isquemia transitoria. Debido a que los aminocidos excitatorios juegan un papel crucial en la toxicidad neuronal, es interesante el hecho de que los agonistas del glutamato, el cido Kanico) o el cido Ibotnico inducen la activacin microglial cuando son administrados dentro del parnquima cerebral.
Seales de activacin de las microglias
El interfern-" (IFN-1). Aunque poco se sabe acerca de la regulacin in vivo de la proliferacin y activacin microglial, tanto experimentos in vivo como in vitro sugieren la participacin de citokinas en ste proceso. El IFN-" derivado de las clulas T es la citokina ms ampliamente utilizada para activar las microglias. La larga lista de eventos que ocurren luego del tratamiento con IFN-" incluyen la produccin de intermediarios reactivos del oxgeno (radicales libres), aumento en la expresin de antgenos MHC clase II, y la sntesis de componentes del complemento. Factores estimulantes de colonias (CSF). De acuerdo con el concepto de que las microglias tienen un origen monoctico, los factores estimulantes de colonias (CSF) han sido identificados como potentes mediadores de activacin para las clulas microgliales. Los astrocitos pueden ser inducidos a expresar (M-CSF) de macrfagos, (G-CSF) de granulocitos y (GM-CSF) de granulocitos y macrfagos (9,28). Adems, las neuronas secretan in vitro (M-CSF). Esto permite al SNC controlar la expansin de las clulas microgliales por medio de un camino independiente del sistema inmune. Adems de su efecto promotor del
crecimiento, GM-CSF y M-CSF potencian varias funciones de los macrfagos, tal como sus actividades fagocticas, citotxicas y microbicidas y, la expresin de antgeno MHC clase II. La importancia funcional de la activacin microglial in vivo mediada por M-CSF se muestra en ratones deficientes de M-CSF, los cuales carecen de proliferacin microglial postraumtica. Qimiokinas. Los efectos quimiotcticos en microglias residentes y en monocitos sanguneos son ejercidos por TGF-# y quimiokinas-beta, un grupo de protenas de 8-10 kDa que presentan cistenas ligadas a enlaces disulfuro altamente conservadas. Las infecciones virales provocan la produccin del IP-10 humano, el cual tiene efectos quimiotcticos sobre linfocitos y monocitos y fue detectado en astrocitos que lo expresan en EAE. Otras quimiocinas-# , como la protena-1 qimioatrayente de monocitos (MCP-1/JE) o la protena-1a inflamatoria de macrfagos (MIP-1 ! ) son producidas por astrocitos activados IL-1# y y por clulas microgliales TNF-! activadas. Pptido # -amiloide. Tambin estn involucrados en la activacin microglial un gran nmero de polipptidos provenientes del cerebro incluyendo el pptido # -amiloide y el leucotrieno B4, el cual se demostr que es producido por astrocitos en cultivo. La protena # -amiloide, un fragmento del protena precursora del # -amiloide, acta como un potente factor quimiotctico para fagocitos mononucleares y activa directamente las microglias residentes in vitro como lo sugiere el brusco incremento en la actividad respiratoria y la produccin de xido ntrico (NO) y TNF-! . Otros estmulos. Sin embargo, en la isquemia, parecen operar otros caminos estimulantes ms rpidos precedentes al dao neuronal y a la respuesta inmune. Alteraciones metablicas y ultraestrucurales tempranas, incluyendo la desintegracin de protenas del citoesqueleto o cambios sinpticos en las membranas, disminucin en la sntesis proteica, y/o metabolismo alterado de poliaminas han sido propuestos como estimulos determinantes para la activacin microglial. An antes de stos cambios, la liberacin de potasio por parte de neuronas comprometidas eleva las concentraciones de potasio en el espacio intercelular, lo cual puede depolarizar las microglias por medio de un canal de potasio entrante. Debido a que carecen de corrientes salientes rectificadoras, incluso una pequea corriente entrante conduce a la despolarizacin de la membrana con consecuencias metablicas desconocidas.
Participacin de las microglias activadas en la reparacin e injuria.
En el tejido cerebral, las clulas microgliales activadas representan un sistema de defensa del husped esencial, fagocitando y matando las bacterias, parsitos y hongos. Este proceso es potenciado por la citokina IFN-! derivada del linfocito T, la cual permite que las microglias acten como clulas presentadoras de antgenos. La supervivencia y expansin de los linfocitos T y B en el SNC depende de la produccin de interleukina 1 (IL-1) e IL-6 por parte de las clulas microgliales luego de la estimulacin, ya sea por infeccin de las clulas por el virus o por los restos neuronales debido a la lisis por efectos citopticos causados por virus neurotrpicos. IL-6 acta en clulas B y promueve la diferenciacin de las mismas en clulas plasmticas secretoras de inmunnoglobulinas. La produccin de anticuerpos antivirales desencadenda por la IL-6 puede ser esencial para la liberacin de los virus en las neuronas afectadas. La dependencia de las clulas microgliales y linfocitos en seales de activacin permite una reaccin inmune espacialmente especfica y temporalmente controlada, lo cual limita la reaccin economizando lo mximo posible el sistema neuronal vital.
Citokinas y reparacin del SNC.
La produccin elevada de ciertas citokinas estara tambin potencialmente involucrada en la reparacin de tejidos. Esta hipotsis es apoyada por descubrimientos de que la IL-1, IL-6 y TGF-# potencian la sntesis in vivo e in vitro del mRNA para el NGF. IL-1 y TNF-! tambin regulan positivamente la expresin de molculas de adhesin (ICAM-1, VCAM-1) y molcula-1 asociada al funcionamiento leucocitario (LFA-1) en microglias activadas, las cuales junto con las integrinas # 1 y # 2 y antgenos tardos (VLA) potencian la interaccin de las clulas cerebrales con la matriz extracelular y leucocitos.
Microglias y gliosis reactiva.
Los astrocitos responden vigorosamente frente a una infeccin y frente a enfermedades del SNC mediadas inmunolgicamente. Aumentan en nmero y en tamao y expresan nuevas molculas indetectables en astroglas inactivas, que incluyen antgeno MHC clase I. Adems de los astrocitos reactivos, tanto las microglias activadas como los monocitos sanguneos estn presentes en gran nmero en el tejido glial del SNC. Existen evidencias de que la gliosis resulta de la comunicacin entre astrocitos y microglias por medio de factores solubles. Los astrocitos provenientes del cerebro humano y de roedores en cultivo secretan G-, GM-CSF, y IL-8, los cuales producen una extensin y aumento en la funcin de las clulas microgliales. Por otra parte, las clulas microgliales secretan IL-1, TNF-! , y TGF-# los cuales activan por s mismos la proliferacin y diferenciacin de astrocitos. Esta interaccin da por resultado astrocitos completamente armados que destoxifican aminocidos excitatorios; producen antioxidantes, tal como superxido dismutasa; y producen factores neurotrficos, incluyendo (NGF).
Mecanismos de la toxicidad.
La comprobacin que la inhibicin del proceso de multiplicacin de monocitos por medio de la irradiacin corporal o inactivacin de macrfagos con colchicina o cloroquina, reduce la muerte celular (o neuronal) que se observa en la isquemia y en el dao cerebral inducido por excitotoxinas, ha llevado a postular que las microglias participan en los mecanismos de muerte neuronal. En algunas circunstancias patolgicas las microglias pueden ser capaces de liberar diversas molculas citotxicas, incluyendo citokinas, NO, radicales libres del oxgeno, los aminocidos citotxicos glutamato y cido quinolnico, y factores de complemento. Cuando son activadas con endotoxinas, las microglias producen TNF-! , el cual se encuentra en niveles altos en EAE. Debido a que los oligodendrocitos son vulnerables a los efectos citotxicos provocados por el TNF! provenientes de las microglias, se ha sugerido que las microglias activadas tendran un papel patognico en las enfermedades desmielinizantes, incluyendo esclerosis mltiple y encefalitis viral. Las microglias activadas tienen la capacidad de generar diferentes especies reactivas del oxgeno, como radical superxido, perxido de hidrgeno, NO, y en forma indirecta el radical hidroxilo. La liberacin de superxido al espacio extracelular, por la actividad de la enzima de membrana NADPH oxidasa, parece estar bajo el control de citokinas: M-CSF aumenta y TGF-# suprime la activacin de esta enzima. La produccin de NO en microglias activadas est a cargo de la enzima NOS. Hay dos tipos de NOS: constitutiva e inducible. Esta ltima se encuentra en clulas fagocticas y puede ser inducida por varias endotoxinas y citokinas. El NO reacciona con superxido, generando peroxinitrito, el cual tiene la capacidad de reaccionar directa o indirectamente a pH fisiolgico con aminocidos, protenas, desoxinuclesidos, desoxinucletidos, ADN intacto, etc. Las propiedades txicas de estas especies han sido observadas en mltiples tipos celulares incluyendo oligodendrocitos y neuronas. Los activadores de la protena quinasa C, tal como PMA, las cuales se unen a receptores del complemento, pueden aumentar adems la liberacin de radicales libres del oxgeno, sugiriendo una contribucin significante a la citotoxicidad
microglial in vivo. La toxicidad del O2- proviene fundamentalmente de su conversin espontnea a perxido de hidrgeno el cual da origen al radical hidroxilo por medio de la reaccin HaberWeiss catalizada por hierro. Los radicales peroxinitrito e hidroxilo son conocidos por iniciar mltiples lesiones celulares, que incluyen peroxidaciones de los lpidos de la membrana, ruptura de la hebra de DNA, alteraciones proteicas, inactivacin de enzimas las cuales pueden conducir al la muerte celular. En trminos generales, los radicales libres juegan un papel central en la patogenia de la hinchazn (swelling) cerebral y en la muerte neuronal inducida por isquemia. Sin embargo, la causa primaria de toxicidad de las microglias activadas sobre las clulas granos del cerebelo que expresan el receptor NMDA para el glutamato, es la estimulacin por las excitotoxinas liberadas y no por los radicales libres. Por tanto, en cocultivos de ambos tipos celulares el glutamato es un producto de secrecin de la microglia e interacciona con los receptores NMDA neuronales provocando la muerte neuronal, la que es bloqueada a su vez por antagonistas para ste receptor. Estos datos indican un papel impotante de la microglia en el dao cerebral mediado por receptores NMDA en la enfermedad cerebrovascular y traumtica. La liberacin de citotoxinas por las celulas microgliales puede jugar tambin un papel importante en el desarrollo de la demencia asociada al SIDA. Los macrfagos afectados por el virus HIV secretan neurotoxinas incluyendo glutamato, que actan sinrgicamente con la protena viral gp120-# provocando neurotoxicidad. Este efecto puede ser bloqueado por antagonistas NMDA.
Inhibicin de la activacin de las microglias.
Adems de los mecanismos de activacin descritas ms arriba, tambin existen circuitos qumicos y metablicos de carcter autcrino y parcrino que inactivan los macrfagos. Las citokinas pueden inhibir la activacin, la liberacin de radicales libres y la expresin de antgenos MHC clase II. El TGF-# tambin disminuye la produccin de NO. In vivo se puede observar que la administracin de TGF-# atena el dao cerebrovascular y el edema cerebral que se observa en la meningitis por neumococo. En ste modelo los corticoides tienen el mismo efecto posiblemente reduciendo la produccin de glutamato . La citokina IL-13 suprime el desarrollo de la EAE. La interleukina-6 disminuye la desmielinizacin que se observa en la encefalomielitis viral de roedores.
Importancia de las microglias activadas en patologa humana.
Como se indica ms arriba, existen evidencias que sugieren que las microglias activadas juegan un papel crucial en la patognesis de las lesiones cerebrales agudas y crnicas. En las enfermedades humanas, la relacin causal entre la activacin microglial y las neurotoxicidad todava no ha sido demostrada formalmente. Claramente, la activacin y diferenciacin de las microglias en macrfagos es un proceso notorio en las enfermedades inflamatorias del SNC, tanto agudas (meningoencefalitis) como crnicas (enfermedades desmielinizantes y encefalopata del SIDA). Mientras que en las meningitis bacterianas la citokinas detectadas en el LCR provienen principalmente de los macrfagos y leucocitos meningeos es claro que las citokinas detectadas en el LCR en las encefalitis provienen del parnquima cerebral. En la esclerosis mltiple, las microglias y los monocitos estn localizados en los bordes de las placas. Ellos expresan el antgeno de MHC clase II y son capaces de producir NO y TNF-! con capacidad de daar los oligodendrocitos y fagocitar mielina. El dao cerebral en neuro-SIDA
incluye caractersticas de encefalitis, leucoencefalopata y mielitis. Como la microglia es el lugar primario de la infeccin del retrovirus, sus formas activadas estan diseminadas a lo largo de la sustancia gris y blanca. La anatoma patolgica muestra que la encefalitis por HIV est caracterizada por la formacin de ndulos microgliales (en la sustancia blanca y sustancia gris profunda), y por la presencia de clulas gigantes multinucleadas. El dao neuronal se atribuye a protenas virales y tambin a toxinas derivadas de las microglias (glutamato y cido quinolnico), que se encuentran elevados en el LCR de los pacientes infectados con HIV. En las enfermedades neurodegenerativas como la enfermedad de Alzheimer, ALS, enfermedad de Parkinson, es posible observar una respuesta inflamatoria estrechamente asociada al sitio de degeneracin neuronal, en dnde participan los tipos celulares mononucleares fagoctico, macrfagos y microglias. Esta activacin se acompaa de un aumento en la expresin de receptores de superficie CD43, FC-receptores, antgenos MHC clase I y II y E-integrinas # 2. En la enfermedad de Alzheimer las microglias no slo se acumulan alrededor de los depsitos amiloides, sino que tambin pueden ser responsables de la secrecin del mismo. En suma, el balance entre los efectos benficos y destructivos de las microglias depende del grado de activacin y de la efectividad de los mecanismos de desactivacin. Cuando stos mecanismos regulatorios estn alterados, por ejemplo la recaptura de glutamato por los astrocitos, puede llevar a que los mecanismos efectores de los macrfagos sean neurotxicos an cuando exista un grado de activacin de menor importancia. Revisin preparada por Luis Barbeito en base a los trabajos de Spranger & Fontana (1996) Activation of microglia: a dangerous interlude in inmune function in the brain The neuroscientist; 2: 293-299 y Mc Geer et al. (1993) Microglia in degenerative neurological disease Glia; 7: 8492.http://www.chasque.apc.org/gunn/exp/microgl.htm
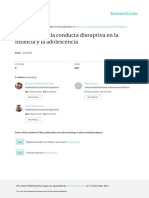
Pathways in neurons, astrocytes and microglia that are implicated in -amyloid toxicity. The figure serves to illustrate the idea that many cellular elements are involved in more than one function or pathway, and are dynamic in that their use in one direction might have an impact on other functions. The development of models of this type, with an ever-increasing degree of sophistication, will foster our understanding of brain function as a dynamic process. See Ref. 9 for details of the elements included in this model of -amyloid toxicity. Reproduced with permission from Ref. 8 2001 Macmillan Magazines Ltd. http://www.nature.com/nrn/journal/v3/n4/slideshow/nrn787_F2.html
Você também pode gostar
- Plan de Intervención Pacientes Con TBCDocumento12 páginasPlan de Intervención Pacientes Con TBCMelissa Balbuena100% (2)
- Nutricion: Guía de Alimentación SaludableDocumento105 páginasNutricion: Guía de Alimentación SaludableAna100% (29)
- Taller de IridologiaDocumento116 páginasTaller de Iridologiagarbomix100% (9)
- CAP.11 - Tratamiento TX Conducta Disruptiva Niños y Adolesc 2 LIBRO SALUD MENTAL Y MED PSICOLOGICA 2da Edición 2014Documento12 páginasCAP.11 - Tratamiento TX Conducta Disruptiva Niños y Adolesc 2 LIBRO SALUD MENTAL Y MED PSICOLOGICA 2da Edición 2014ana cecilia francoAinda não há avaliações
- Diagrama EscaleraDocumento28 páginasDiagrama EscaleraEmmanuel BeltramoAinda não há avaliações
- Manual DIACOM-NLSDocumento47 páginasManual DIACOM-NLSAnonymous GmVJSCS100% (1)
- Normas de EnfermeríaDocumento3 páginasNormas de EnfermeríaMickel Novas100% (2)
- Razas de Carne Bos Tauros 5Documento98 páginasRazas de Carne Bos Tauros 5exodiaferAinda não há avaliações
- Análisis de la película Claro Oscuro sobre la vida de David HelfgottDocumento2 páginasAnálisis de la película Claro Oscuro sobre la vida de David HelfgottJardo Edgar Reymundo75% (4)
- Tratamiento Digital de Señales - Problemas y Ejercicios Resueltos, 2003Documento476 páginasTratamiento Digital de Señales - Problemas y Ejercicios Resueltos, 2003M Elena Gonzalez100% (1)
- Película XXY analiza identidad de género intersexualDocumento3 páginasPelícula XXY analiza identidad de género intersexualxxherecomesthesunxxAinda não há avaliações
- Ease Guidelines June2014 SpanishDocumento16 páginasEase Guidelines June2014 Spanishjovi0Ainda não há avaliações
- InfoPLC Net Conocimientos vISIONARTIFICIALDocumento28 páginasInfoPLC Net Conocimientos vISIONARTIFICIALjovi0Ainda não há avaliações
- Presentacion VISION PDFDocumento11 páginasPresentacion VISION PDFjovi0Ainda não há avaliações
- InfoPLC Net Conocimientos vISIONARTIFICIALDocumento28 páginasInfoPLC Net Conocimientos vISIONARTIFICIALjovi0Ainda não há avaliações
- Machine Vision AplicacionesDocumento34 páginasMachine Vision Aplicacionesjovi0Ainda não há avaliações
- Visión artificial aplicada a la industria: componentes y tendenciasDocumento28 páginasVisión artificial aplicada a la industria: componentes y tendenciasjovi0Ainda não há avaliações
- Cap 1 Intro VADocumento22 páginasCap 1 Intro VAFernando_Argel_9937Ainda não há avaliações
- Disenos Cuasi 1 WOP PDocumento72 páginasDisenos Cuasi 1 WOP PGustav PerlsAinda não há avaliações
- Machine Vision AplicacionesDocumento34 páginasMachine Vision Aplicacionesjovi0Ainda não há avaliações
- Tutorial de EFTDocumento45 páginasTutorial de EFTEntenados De Stanislavsky TeatroAinda não há avaliações
- Clase F85-Transduccion Sensitiva en La RetinaDocumento40 páginasClase F85-Transduccion Sensitiva en La Retinajovi0Ainda não há avaliações
- EA Tema3 3 01 2hDocumento35 páginasEA Tema3 3 01 2hjovi0Ainda não há avaliações
- Guía Roja y Verde de Alimentos Transgénicos.Documento16 páginasGuía Roja y Verde de Alimentos Transgénicos.jsegura28100% (6)
- Introduccion A Los DSPDocumento66 páginasIntroduccion A Los DSPAnonymous 7t2BOJbAinda não há avaliações
- Semiología QuirúrgicaDocumento44 páginasSemiología QuirúrgicaYaira Then FerrerasAinda não há avaliações
- Complejo Mayor de Histocompatibilidad - Docbymatias-SamaDocumento12 páginasComplejo Mayor de Histocompatibilidad - Docbymatias-SamaTamara Andrea Acuña CastroAinda não há avaliações
- Diapositivas de AlzheimerDocumento7 páginasDiapositivas de Alzheimercarlos perezAinda não há avaliações
- Sistema nervioso: evaluación sumativaDocumento8 páginasSistema nervioso: evaluación sumativaRomy ContrerasAinda não há avaliações
- Mejoramiento Genético 4A1 - Informe 2Documento4 páginasMejoramiento Genético 4A1 - Informe 2Gerardo Huaytalla CanoAinda não há avaliações
- Test de La CasaDocumento4 páginasTest de La CasaCommunicactionsSoporteTecnicoAinda não há avaliações
- Hibridacion in SituDocumento10 páginasHibridacion in SituErick EncisoAinda não há avaliações
- Aalisis Clínico II - Líquidos BiologicosDocumento18 páginasAalisis Clínico II - Líquidos BiologicosJessica Benavides BermudezAinda não há avaliações
- Desarrollo Psicosocial en La Niñez IntermediaDocumento4 páginasDesarrollo Psicosocial en La Niñez Intermediapsicodes201186% (7)
- 2ndo Congreso de La Sociedad Ecuatoriana de Emergencias y Cuidados Criticos Veterinarios, 2010Documento172 páginas2ndo Congreso de La Sociedad Ecuatoriana de Emergencias y Cuidados Criticos Veterinarios, 2010Miguel FernandoAinda não há avaliações
- Interveciones Farmacologicas Que Mejoren La Cognicion y El Funcionamiento Adaptativo en El Sindrome de DownDocumento10 páginasInterveciones Farmacologicas Que Mejoren La Cognicion y El Funcionamiento Adaptativo en El Sindrome de DownVladimir Herrera AlvaAinda não há avaliações
- Informe # 11 Meiosis - HerenciaDocumento3 páginasInforme # 11 Meiosis - HerenciaMishellAlvarez100% (1)
- 9° Cuadernillo Noveno Primer Periodo 2021Documento106 páginas9° Cuadernillo Noveno Primer Periodo 2021santiago martinezAinda não há avaliações
- Neurología: LXIV Reunión Anual de La Sociedad Española de NeurologíaDocumento158 páginasNeurología: LXIV Reunión Anual de La Sociedad Española de NeurologíaJosehp Millares TolaAinda não há avaliações
- Orígenes de La Biología Celular y MolecularDocumento38 páginasOrígenes de La Biología Celular y MolecularmasterukiAinda não há avaliações
- TubérculosisDocumento16 páginasTubérculosisAntonioAinda não há avaliações
- Fajas LumbaresDocumento22 páginasFajas Lumbaresovelasquez1160Ainda não há avaliações
- Heridas Por Arma de FuegoDocumento4 páginasHeridas Por Arma de FuegoIbone Ledesma100% (1)
- Importancia de La Recreacion y Esparcimiento en El Desarrollo HumanoDocumento14 páginasImportancia de La Recreacion y Esparcimiento en El Desarrollo HumanoMaria DeicyAinda não há avaliações
- Tipos de ImpactosDocumento14 páginasTipos de ImpactosWilber Marcelo Apaz ArancibiaAinda não há avaliações
- Factores Asociados A Insuficiencia Renal en Pacientes de La Clinica 42 Del ImssDocumento27 páginasFactores Asociados A Insuficiencia Renal en Pacientes de La Clinica 42 Del ImssRosa Mistica Ramirez ArreguinAinda não há avaliações
- Celulitis PeriorbitariaDocumento4 páginasCelulitis PeriorbitariaDiego Pinto Colicheo100% (1)