Escolar Documentos
Profissional Documentos
Cultura Documentos
Difusão de componentes orgânicos no ar
Enviado por
Moisés JúniorTítulo original
Direitos autorais
Formatos disponíveis
Compartilhar este documento
Compartilhar ou incorporar documento
Você considera este documento útil?
Este conteúdo é inapropriado?
Denunciar este documentoDireitos autorais:
Formatos disponíveis
Difusão de componentes orgânicos no ar
Enviado por
Moisés JúniorDireitos autorais:
Formatos disponíveis
1
Instituto Federal de Educao, Cincia e Tecnologia da Bahia
CAMPUS SALVADOR
FENMENO DE TRANSPORTE DE DIFUSO GASOSA DE
COMPONENTES ORGNICOS NO AR
DOCENTE: Lin Kan
DISCENTES: Maria Gorethe Oliveira B. Santos
Moiss Rodrigues Lima Jnior
Monyque Rosa Costa Leal
CURSO: Engenharia Qumica
DISCIPLINA: Laboratrio de Engenharia Qumica 2
SALVADOR
Fevereiro de 2014
2
1. OBJETIVO
Estudar e analisar o fenmeno de transporte de transferncia de massa buscando
determinar o coeficiente de difuso mssica dos solventes em ar utilizando os modelos
matemticos de difuso pseudo-estacionrio atravs de um filme estagnado. Tambm faz
parte deste relatrio comparar os valores empricos calculados com os valores descritos na
literatura.
2. INTRODUO
Num sentido amplo, a transferncia de massa pode ser compreendida como o
movimento espacial da matria. Em um sentido mais especfico refere-se ao movimento de
um componente especfico (A, B,...) em um determinado sistema que possui vrios outros
componentes. Por definio de gradientes de concentrao, existem regies com diferentes
concentraes, logo, o fenmeno de transferncia de massa ocorre quando um constituinte
possui uma concentrao maior numa regio e tende a ocupar a regio onde o constituinte
possui menor concentrao. Sendo que esse transporte pode ocorrer atravs do mecanismo da
difuso molecular ou da conveco.
comum que a difusividade mssica seja mais elevada nos gases do que em
substncias nos estados lquido e slido da matria, assim como maior nos lquidos do que
nos slidos. Tambm h de se notar que, normalmente, espcies qumicas diferentes
apresentam uma difusividade mssica diferente quando submetidas a uma mesma temperatura
e presso constantes. Entretanto, quando h alterao das variveis de estado constantemente,
como a temperatura e a presso, ento haver uma alterao na difusividade da substncia em
estudo.
No experimento realizado pela equipe utilizaram-se tubos de ensaio nos quais foram
introduzidos solventes relativamente mais volteis do que a gua. As substncias introduzidas
no capilar dos tubos de ensaio foram: acetona P.A, ter etlico comercial e etanol. Essas
substncias foram adicionadas at um nvel determinado por uma escala milimtrica adaptado
aos tubos de ensaio. Aps determinados espaos de tempo foi possvel registrar e observar
que a altura de nvel diminua evidenciando a evaporao dos componentes volteis, o que
permite o clculo do coeficiente de difuso mssica dos solventes no ar, alm de
identificarmos quais substncias possuem maiores resistncias transferncia de massa.
3
destaque informar nesta introduo que o solvente ter etlico no estava
especificado, e isso promoveu um comportamento fora do comum como poder ser observado
nas discusses e resultados.
3. FUNDAMENTAO TERICA
3.1 A PRIMEIRA LEI DE FICK
Com o objetivo de analisar o fenmeno da difuso em gases, sero primeiramente
pressupostas molculas gasosas de baixa densidade, de modo que no desprezvel a
considerao de que existem interaes com outras molculas ao redor, e monoatmicas.
Tambm monoatmicas, alm de considera-las esfricas e da mesma espcie qumica,
portanto com o mesmo dimetro d. A energia cintica associada a cada uma das espcies a
proveniente de seu movimento de translao por um eixo fictcio. Devido a esse movimento,
ser admitida a validade do movimento circular uniforme.
Numa primeira aproximao haver colises entre duas molculas, caso estejam
distanciadas entre si centro a centro (Figura 1). Supondo que o choque seja elstico, as duas
iro traas trajetrias aleatrias, desencadeando sucessivos choques populao molecular.
Figura 1 Coliso elstica entre duas molculas
FONTE: Cremasco, 2007
As molculas que migraro para quaisquer sentidos ou direes tendero a ocupar
novos espaos, nos quais a sua populao menor, como pode ser observado na Figura 2.
Esses espaos sero definidos como planos, para efeito da modelagem matemtica do
fenmeno de difuso. A diferena entre essas concentraes possibilita o fluxo de matrias,
em suma, este o gradiente de concentrao.
4
Figura 2 Tendncia das molculas ocuparem maiores espaos
FONTE: http://pt.wikipedia.org/wiki/Difus%C3%A3o_molecular. Acesso em 18/02/2014
Define-se que as concentraes da espcie estudada nos planos A e B so
respectivamente:
E que C
A
representa a concentrao molar da espcie A;
a concentrao molar de
A no plano A;
, a concentrao molar de A no plano B; e
, a concentrao molar de A
no plano O. O parmetro
indica a concentrao da matria a ser ganha no plano B ou
perdida no plano A para que o sistema entre em equilbrio termodinmico. A Figura 3
representa os planos descritos aqui.
5
Figura 3 Fluxo lquido da populao molecular
FONTE: Cremasco, 2007 (p.33)
Com o intuito de obter o fluxo de matria, associaremos o fluxo de A que passa pelo
plano O, na direo z, concentrao
; enquanto no plano A teremos
, no plano B teremos
. Agora para obter CA* utilizar-se-:
A aproximao () ser uma igualdade se, e somente se, a funo C
A
(z) vier a ser
linear no intervalo considerado. Admitindo a linearidade para a funo em estudo, pode-se
descrever:
Substituindo a equao (3.5) nas equaes (3.1) e (3.2), tem-se:
6
Por se tratar de uma populao molecular de mesma espcie, ser considerada uma
velocidade mdia molecular da espcie A igual a . O fluxo lquido da espcie A que passa
por um determinado plano i, no sentido z+, ser definido como
, sendo obtido pelo
produto da velocidade mdia molecular com o valor da concentrao de A contida no plano i,
. No espao tridimensional as molculas fluem em qualquer sentido e direo (seis ao
total), logo:
Representa o fluxo da espcie A no plano i e na direo z.
O fluxo lquido que atravessa o plano A :
Trazendo as expresses (3.6) e (3.7) para a equao (3.9), teremos:
]
O fluxo lquido em qualquer plano situado entre os planos A e B oriundo do seguinte
balano global:
(fluxo lquido) = (fluxo que entra) (fluxo que sai)
Ou
Para a obteno do fluxo lquido de A que atravessa qualquer plano, necessrio levar
em considerao as equaes (3.10), (3.11) e (3.12):
7
]
Do que resulta:
Definindo:
E substituindo na expresso (3.14), tem-se que:
Essa equao denominada primeira lei de Fick. Lei que nasceu historicamente
atravs de observaes empricas. O sinal negativo indica decrscimo da concentrao da
espcie A com o sentido do fluxo, e caminho livre mdio; J
A,z
fluxo difusivo da espcie
A na direo z.
A primeira Lei de Fick aplica-se, empiricamente, ao fenmeno de difuso em qualquer
estado da matria. O coeficiente de difuso pode ser descrito pela equao (3.17), que nasce
da interao soluto-meio para qualquer meio fsico, distinto ou no do soluto.
D
AA
o coeficiente de difuso, neste caso em especfico autodifuso, visto que A
difunde-se num meio constitudo dela prpria.
8
Tabela 1 Coeficientes de difuso binria em gases
Sistema T (K) D
AB
.P (cm
2
. atm/s)
Ar/etanol 299 0,132
Ar/ter etlico 293 0,0896
Ar/acetona 293 0,1242*
*valor obtido na literatura (Faghri & Zhang, 2006) e corrigido para as condies de
temperatura e presso atravs da correlao de Fuller et al. (1966)
3.2 COEFICIENTES DE DIFUSO
Os coeficientes de difuso representam a velocidade com que gradientes de
concentrao so dissipados dentro de uma soluo.
O coeficiente de difuso espontneo de um componente em soluo mede a velocidade
com que este componente se difunde na ausncia de um gradiente de concentrao e est
intimamente ligada a sua natureza qumica.
Nos primeiros estudos realizados pelos cientistas sobre o coeficiente de difuso das
substncias foi abordada de maneira simplificada a teoria cintica dos gases que envolvem:
velocidade relativa das molculas gasosas que esto em contnuo movimento, s posies
onde duas molculas encontram-se na iminncia da coliso; o dimetro eficaz de coliso ou
dimetro de choque; a frequncia das colises; o caminho livre mdio, que tambm pode ser
definido como a distncia mdia entre duas molculas na iminncia de coliso.
Ao passar dos anos e com o avano do conhecimento foram realizados mais estudos
empricos e atravs destes conseguiu-se expressar com maior qualidade o fenmeno de
transporte das molculas num determinado meio. Exemplo disso est presente na equao de
Chapman-Enskog, nas correlaes de Fuller, Schetter e Giddings. A anlise dos efeitos da
polaridade na difuso dos gases atravs de Brokaw (1969). E tambm o estudo da difuso de
um soluto em uma mistura gasosa estagnada de multi componentes atravs da relao
proposta por Wilke (1950).
A correlao de Fuller, Schetter e Giddings remete formulao da equao (3.18),
corrigindo-a em termos da temperatura de acordo com a seguinte expresso:
9
Sendo o fator do denominador,
, o dimetro molecular ou eficaz do choque, e deve
ser calculado atravs de tabelas seguindo a expresso:
()
()
3.3 VELOCIDADE
Considera-se o escoamento de uma soluo com n espcies qumicas. No muito
complicado imaginar que diferentes espcies escoaro com diferentes velocidades.
importante atentar para o fato de que qualquer propriedade em um meio contnuo conhecida
por uma mdia. Quando mencionada velocidade, esta no ser apenas de uma molcula da
espcie i, mas a mdia de n molculas dessa espcie contida em um elemento de volume.
Como a soluo uma mistura de distintas espcies qumicas, a velocidade com a qual
escoa dada pela velocidade mdia mssica:
Ou pela velocidade mdia molar:
Sendo
i
a massa de uma espcie qumica i por unidade de volume da soluo e C
i
a
quantidade de matria (mols) de espcie i por unidade de volume da soluo.
Observa-se que a velocidade local com que a massa da soluo atravessa uma
seo unitria colocada perpendicularmente velocidade . A mesma situao se aplica para
quantidade de matria substituindo por C e por
.
10
necessrio destacar que a velocidade
absoluta e diz respeito espcie qumica i.
Essa velocidade pode estar referenciada a outro tipo de velocidade:
I. A de eixos estacionrios
II. A da soluo (para velocidade mssica)
III. A da soluo (para velocidade molar)
O resultado oriundo das diferenas das proposies (II) e (III) denomina-se velocidade
de difuso.
3.4 FLUXO
Sabe-se que a definio clssica de fluxo :
(Fluxo) = (velocidade) x (concentrao)
Sendo que a unidade de fluxo : [
].
Tambm, sabe-se que conceitual dizer que:
(
) (
) (
)
Se quisermos explicitar o fluxo de uma espcie qumica A em termos de sua
concentrao molar, velocidade absoluta de A e velocidade mdia molar local da soluo,
teremos:
Como consequncia da manipulao algbrica da equao (3.23), teremos que:
O fluxo
posto dessa forma denominado fluxo absoluto molar da espcie A. A
parcela correspondente contribuio difusiva :
)
Sendo reescrita segundo a primeira lei de Fick:
11
Sabendo que o operador
o vetor gradiente de concentrao da espcie A nas trs
direes:
3.5 EQUAO DA CONTINUIDADE MOLAR DE UM SOLUTO A
A equao da continuidade de um soluto A nasce do balano de taxa de matria, o qual
flui atravs das fronteiras de um elemento de volume escolhido no meio contnuo e daquela
taxa que varia no interior desse volume de controle. O balano material para uma dada
espcie qumica A atravs de um volume de controle apropriado :
(
) (
) (
) (
)
Em termos molares a tambm pode ser escrita como:
4. METODOLOGIA
O experimento era para ser realizado semelhante clula de Arnold, que tem como
objetivo analisar o fenmeno de transferncia de massa por difuso em um meio estagnado.
Como o laboratrio no possui esse equipamento foi utilizado o seguinte material:
3 tubos de ensaio com graduados;
Suporte para tubos de ensaio;
Ventilador (OBS: nas trs primeiras horas do experimento);
Soluo de acetona P.A (99,5 %, PM = 58,08);
Soluo de ter comercial;
12
Soluo de lcool etlico - etanol (93 %).
Os dados necessrios para a anlise e os clculos dos modelos do fenmeno de
transferncia de massa foram:
Comprimento do caminho de difuso (cm);
Altura inicial do nvel de lquido (cm);
Altura final do nvel de lquido (cm);
Tempo decorrido da difusividade para o ar (min.);
Temperatura atribuda ao sistema (C).
Presso de vapor dos solventes analisados (atm);
Massa molar dos solventes analisados;
Presso total do sistema (presso ambiente = 1 atm)
Constante dos gases ideais (
).
5. RESULTADOS E DISCUSSES
A partir dos fundamentos tericos apresentados referentes ao fenmeno de
transferncia em um processo de difuso de um gs em um meio utilizou-se a equao do
perfil de concentrao atravs da equao diferencial de transferncia de massa:
Na qual, por medidas de hipteses, foram realizadas algumas aproximaes
pertinentes ao sistema real:
A primeira hiptese foi considerar o regime de difuso em estado estacionrio, logo:
A segunda hiptese que no sistema no ocorre reao qumica, portanto:
13
Substituindo as hipteses 1) e 2) na equao (5.1), teremos que:
Considerando o fluxo unidirecional em z, os termos que esto nas coordenadas x e y
sero desprezados e iguais a zero. Logo:
importante destacar que o fluxo no sentido dos eixos x e y foram desprezados
considerando que o dimetro do tubo de ensaio pequeno.
Sendo assim, a equao global do fluxo molar do solvente para o ar pode ser expressa
da seguinte forma:
Considerando que o ar est estagnado, a velocidade instantnea do ar e o fluxo do
mesmo podem ser considerados iguais a zero.
Ento:
Considerando tambm que no h variao brusca de temperatura e presso durante o
experimento, logo, o coeficiente de difuso e a concentrao do solvente sero ditos
constantes.
14
Sendo assim, pode-se integrar a equao (5.5) e teremos:
)
Como:
Sendo que M
A
a massa molar da substncia A (g/mol) e
A
(g/cm), neste caso, a
massa especfica do solvente utilizado. A frao de gs na interface lquida do solvente y
A,2
e a frao de gs j na iminncia de sair do tubo y
A,1
.
Igualando as equaes (5.8) e (5.7), teremos:
)
Integrando a equao (5.9) encontraremos a seguinte expresso:
)
(
No experimento foi possvel coletar os dados referentes ao tempo e a altura do nvel
(z) do lquido inicial e final. Atravs da equao (5.10) e dos dados empricos obtidos
possvel construir um grfico e assim determinar experimentalmente o valor de
.
Considerando que a mistura gasosa ideal:
15
A frao molar de A para fase gasosa ideal est relacionada com a sua presso parcial
segundo a lei de Dalton:
No caso em que essa fase seja lquida, a condio numa dada fronteira, para uma
soluo ideal, advm lei de Raoult:
A presso de vapor pode ser obtida atravs da equao de Antoine:
)
Tabela 2 Constantes da Equao de Antoine para Presses de Vapor de Espcies Puras
Substncia Frmula Parmetro: A Parmetro: B Parmetro: C
Faixa de
Temperatura
Acetona C
3
H
6
O 14,3145 2756,22 228,060 -26 a 77 C
ter Etlico C
4
H
10
O 14,0735 2511,29 231,200 -43 a 55 C
Etanol C
2
H
6
O 16,8658 3795,17 230,918 3 a 96 C
FONTE: Poling, B. E., Prausnitz, J. M. e OConnell, J. P., The Properties of Gases and Liquids (2001)
Na hiptese de equilbrio termodinmico na interface entre a fase lquida e gasosa,
considerando-as ideais, as equaes (5.12) e (5.13) so igualadas, resultando na equao de
Raoult-Dalton:
Supondo a fase lquida constituda somente da espcie qumica A, a equao (5.15)
escrita como:
16
Observando que o clculo da presso de vapor foi realizado admitindo a temperatura
ambiente de 26 C e presso atmosfrica de 1 atm.
Tabela 3 Presso de Vapor das substncias calculadas atravs da eq. (3.38) 26 C
Substncia Presso de Vapor (kPa) Presso de Vapor (atm)
Acetona 32,00 0,32
ter Etlico 74,41 0,73
Etanol 8,12 0,08
Ao conferir a literatura foi constatado que os valores da Tabela 3 so prximos aos
valores padronizados 20 C. Como o ambiente experimental no laboratrio foi de 26 C foi
possvel perceber valores mais elevados de presso de vapor.
Os dados experimentais esto na Tabela 4.
17
Tabela 4 Dados experimentais coletados no laboratrio de Engenharia Qumica
Horrio de Coleta de Amostra t (s) ACETONA [(z
f
) - (z
0
)]/2 TER [(z
f
) - (z
0
)]/2 ETANOL [(z
f
) - (z
0
)]/2
29/1/14 17:16 0,00 16,00 0,00 16,00 0,00 16,00 0,00
29/1/14 17:36 1200,00 16,15 2,41 16,10 1,61 16,00 0,00
29/1/14 17:56 2400,00 16,20 3,22 16,20 3,22 16,05 0,80
29/1/14 18:16 3600,00 16,30 4,85 16,30 4,85 16,10 1,61
29/1/14 18:36 4800,00 16,35 5,66 16,40 6,48 16,10 1,61
29/1/14 18:56 6000,00 16,40 6,48 16,50 8,13 16,10 1,61
29/1/14 19:16 7200,00 16,45 7,30 16,60 9,78 16,15 2,41
29/1/14 19:36 8400,00 16,50 8,13 16,70 11,45 16,20 3,22
29/1/14 19:56 9600,00 16,60 9,78 16,80 13,12 16,25 4,03
29/1/14 20:16 10800,00 16,70 11,45 16,90 14,81 16,30 4,85
30/1/14 20:20 97440,00 18,20 37,62 18,40 41,28 16,60 9,78
31/1/14 12:20 155040,00 19,00 52,50 19,00 52,50 16,75 12,28
31/1/14 20:20 183840,00 19,45 61,15 19,30 58,25 16,90 14,81
3/2/14 10:20 234240,00 21,95 112,90 20,55 83,15 17,50 25,13
3/2/14 20:30 270840,00 22,30 120,65 20,70 86,25 17,60 26,88
4/2/14 10:20 320640,00 22,80 131,92 20,80 88,32 17,75 29,53
4/2/14 20:20 356640,00 23,15 139,96 21,00 92,50 17,90 32,21
5/2/14 11:00 395040,00 23,60 150,48 21,10 94,61 18,00 34,00
5/2/14 20:20 428640,00 23,95 158,80 21,10 94,61 18,10 35,81
18
Utilizando os dados da Tabela 4, foram construdos os grficos com base na equao
(3.34) para encontrar os coeficientes angulares, e assim calcular o coeficiente de difuso
(D
AB
) experimental para cada solvente estudado.
Grfico 1 Dados experimentais: Acetona
Grfico 2 Dados experimentais: ter etlico**
Grfico 3 Dados experimentais: Etanol
y = 0,0004x + 3,6505
R = 0,9844
0,00
50,00
100,00
150,00
200,00
0,00 100000,00 200000,00 300000,00 400000,00 500000,00
(cm)
tempo (s)
Acetona
y = 0,0002x + 8,7419
R = 0,9528
0,00
20,00
40,00
60,00
80,00
100,00
120,00
0,00 100000,00 200000,00 300000,00 400000,00 500000,00
(cm)
tempo (s)
ter Etlico
y = 8E-05x + 1,5445
R = 0,9834
0,00
5,00
10,00
15,00
20,00
25,00
30,00
35,00
40,00
0,00 100000,00 200000,00 300000,00 400000,00 500000,00
(cm)
tempo (s)
Etanol
19
Atravs da observao dos grficos obtidos, percebe-se que o modelo tende a formar
uma linha reta de tendncia. Quanto maior o R significa que os resultados aproximaram-se
mais da normalidade permitindo algum comentrio fsico sobre o fenmeno.
Para calcular o valor de D
AB
foi realizada uma conta atravs da equao (3.34), sendo
que o coeficiente angular pode ser expresso como:
)
Logo, D
AB
sendo isolado, teremos:
Destaque para y
A,2
igual a zero. Pois, considera-se que o fluxo de ar no tubo carrega
toda quantidade do componente gasoso que se encontra na borda do tubo, sendo que a
velocidade do ar foi mantida, durante quase todo o tempo do experimento, baixa, justificando
o meio estagnado.
Ento, para o experimento realizado, os resultados obtidos nos clculos foram
expressos atravs da Tabela 5:
Tabela 5 Resultados obtidos no clculo do coeficiente de difuso dos solventes em ar
Acetona ter etlico Etanol
Massa Molar (g/mol) 58,080 74,120 46,060
Massa especfica (g/cm) 0,790 0,710 0,789
Concentrao (mol/cm) 0,00004074 0,00004074 0,00004074
Presso de Vapor (atm) 0,31583659 0,73433410 0,08010277
Coeficiente Angular 0,000400 0,000200 0,000080
y
A,1
0,3158 0,7343 0,0801
y
A,2
0,0000 0,0000 0,0000
ln[(1-y
A,2
)/(1-y
A,1
)] 0,3796 1,3255 0,0835
D
AB
.P (cm.atm/s) 0,3519 0,0355 0,4029
Para realizar uma comparao com uma correlao fundamentada no fenmeno
estudado, no tpico (3.2) deste relatrio foram realizados clculos para o coeficiente de
20
difuso molecular atravs das equaes (3.19) e (3.20) que foram retiradas da literatura de
Cremasco, 2007. O resultado est exposto na Tabela 6.
Tabela 6 Clculo dos D
AB
para cada solvente do experimento atravs da correlao de Fuller et al (1966)
Sistema T (K) D
AB
.P (cm
2
. atm/s)
Ar/etanol 299 0,1289
Ar/ter etlico 299 0,0935
Ar/acetona 299 0,1104
Diante dos resultados calculados para o estudo do fenmeno de difuso das molculas
dos solventes no ar foi possvel realizar uma anlise de erros envolvendo o experimento em si
e as prprias correlaes utilizadas em literaturas diferentes. Os resultados desses clculos
foram expressos na Tabela 7.
Tabela 7 Resultados e erros experimentais e das correlaes utilizadas
Substncias: Acetona ter etlico Etanol
D
AB
(cm/s) 0,3519 0,0355 0,4029
D
AB
(cm/s) - correlao 0,1289 0,0935 0,1104
D
AB
(cm/s) - correlao (lit.) 0,132 0,0896 0,1242
Erro experimental 172,99% 62,05% 264,96%
Erro em relao literatura 2,35% 4,35% 11,11%
De acordo com a Tabela 7 podemos observar que as condies experimentais foram
repletas de erros, o que gerou uma propagao de erros muito significante ao ponto de
alcanar a faixa de 200 a 260%, como pode ser visto. Esse erro relativo ao experimento foi
calculado atravs da seguinte expresso:
[
De modo a continuar analisando os resultados realizamos o clculo do erro
envolvendo uma correlao emprica proposta na literatura com valores encontrados em
literaturas mais avanadas, neste caso especfico, no conceituado livro The properties of gases
& liquids, 1977. Observa-se que para esses dois dados os valores encontrados foram bem
mais prximos do que os valores encontrados no experimento. Fator este que aumenta a
probabilidade de que o experimento tenha sido realizado com sucessivos erros.
21
O primeiro erro pode estar logo presente no sistema utilizado para a realizao do
experimento. Esse tipo de experimento deve ser realizado numa clula de Arnold, na qual o
sistema que contm o solvente fechado do contato com o ar mido em uma tubulao que
contm a montante slica-gel, substncia que retm a umidade do ar que introduzido
foradamente por um ventilador, ou seja, a entrada do fluxo de ar deve ser forada por um
agente impelidor. Outro erro que tambm pode ter se propagado foi a especificao dos
solventes utilizados. Foi observado que, por exemplo, que o ter etlico era misturado com
lcool etlico. Fato que, com certeza, interferiu nos resultados experimentais.
De acordo com os dados da literatura percebeu-se que o solvente que mais voltil, ou
seja, aquele que passa para o estado fsico da matria gasosa mais rapidamente, justamente o
que possui um maior coeficiente de difuso molecular, fato que mostra a validao da teoria,
nesse aspecto, com a prtica realizada. Pois, observa-se que no caso que em os dados de D
AB
para a acetona foram retirados ou de correlaes ou do livro que contm as propriedades dos
gases, os valores so maiores do que para os outros solventes, e respectivamente 0,1289 e
0,1320 cm.atm/s. Considerando tambm que os dados so bastante prximos, mesmo
utilizando fontes da literatura distintas.
6. CONCLUSES
Pode-se concluir que um planejamento experimental um passo fundamental para a
realizao de qualquer experimento num ambiente laboratorial. Pois, de entendimento
acadmico que muitas correlaes da literatura que envolve os fenmenos fsicos e qumicos
de transporte de matria ocorrem sob determinadas condies especficas de operao, as
quais devem ser obedecidas, caso o cientista queira compreender os sistemas de maneira
adequada. A utilizao dos mtodos necessrios para modelar e analisar os dados
experimentais de um sistema de difuso de molculas de solventes em ar no foi satisfatrios
devido a quantidade de falhas no planejamento experimental, esse fato promoveu um
afastamento muito elevado da realidade suscitando erros experimentais relativos de at 260%
em relao aos padres encontrados na literatura.
Tambm podem ser destacados outros erros durante o experimento, como os erros
humanos. Na coleta dos dados experimentais vrios estudantes juntamente com o professor
22
realizaram as coletas dos dados manuseando, talvez at de modo incorreto, os tubos de ensaio.
A equipe est ciente que esse possvel erro no fundamenta dados to afastados da realidade.
Na perspectiva de estudar o fenmeno e investigar os resultados a equipe mostrou
entendimento e maturidade para interpretar, fundamentar, com base na pesquisa exaustiva de
literaturas e das correlaes propostas durante a evoluo emprica dos estudos envolvendo a
transferncia de massa, e concluir as situaes ocorridas durante o perodo experimental.
A equipe tambm concluiu que importante considerar a no repetio do
experimento nos mesmos moldes que foram realizados durante a prtica desse semestre
(2013.2), pois os dados obtidos no foram satisfatrios ao ponto de registrarem aplicao da
prtica na teoria. Sendo que os dados considerados reais foram encontrados aproximadamente
sob as mesmas condies de temperatura e presso no laboratrio de engenharia qumica.
7. REFERNCIAS BIBLIOGRFICAS
SMITH, J. M., VAN NESS, H. C., ABBOTT, M. M. Introduo termodinmica
da engenharia qumica. Rio de Janeiro, LTC, 2007.
CREMASCO, M. A. Fundamentos de transferncia de massa, 2 Edio, Campinas
SP, Editora da Unicamp, 2002.
REID, R. C., PRAUSNITZ, J. M. e SHERWOOD, T. K. The properties of gases and
liquids, 3 Ed., Nova York: McGraw-Hill, 1977.
Você também pode gostar
- Simulação ETA ProSimPlusDocumento5 páginasSimulação ETA ProSimPlusMoisés JúniorAinda não há avaliações
- Análise de Processos - ExercíciosDocumento3 páginasAnálise de Processos - ExercíciosMoisés JúniorAinda não há avaliações
- 144-Texto Do Artigo-173-1-10-20150820Documento5 páginas144-Texto Do Artigo-173-1-10-20150820Moisés JúniorAinda não há avaliações
- Análise da qualidade da água da chuva para uso em caldeiras industriaisDocumento10 páginasAnálise da qualidade da água da chuva para uso em caldeiras industriaisMoisés JúniorAinda não há avaliações
- O Processo de Crescimento e Amadurecimento Espiritual Do CristãoDocumento2 páginasO Processo de Crescimento e Amadurecimento Espiritual Do CristãoMoisés JúniorAinda não há avaliações
- Manual de Análise de ÁguaDocumento147 páginasManual de Análise de ÁguaanaepauloAinda não há avaliações
- Fazer Investimentos 2.0 PDFDocumento42 páginasFazer Investimentos 2.0 PDFMateus AlonsoAinda não há avaliações
- Sistema de resfriamento de água em indústriasDocumento11 páginasSistema de resfriamento de água em indústriasMoisés JúniorAinda não há avaliações
- (Normalizado) Fundamentos para Análise de ÁguaDocumento41 páginas(Normalizado) Fundamentos para Análise de ÁguaMoisés JúniorAinda não há avaliações
- Bem-vindos à nova Hinode 4.0Documento45 páginasBem-vindos à nova Hinode 4.0Renne Coutinho100% (1)
- Como planejar a aposentadoria de forma efetivaDocumento36 páginasComo planejar a aposentadoria de forma efetivadamarisbrunetAinda não há avaliações
- Lugar Das RaízesDocumento32 páginasLugar Das RaízesMoisés JúniorAinda não há avaliações
- Release Preparo para Aposentadoria v3 PDFDocumento5 páginasRelease Preparo para Aposentadoria v3 PDFdamarisbrunetAinda não há avaliações
- Implantação de Aterro Sanitário - Techbios PDFDocumento19 páginasImplantação de Aterro Sanitário - Techbios PDFMoisés JúniorAinda não há avaliações
- Apresentacao-Plano - FINAL 2016Documento33 páginasApresentacao-Plano - FINAL 2016Moisés JúniorAinda não há avaliações
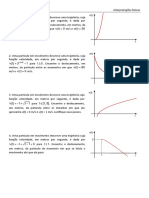
- Interpretacoes Fisicas - Cálculo IIDocumento6 páginasInterpretacoes Fisicas - Cálculo IIMoisés JúniorAinda não há avaliações
- Planilha de Orçamento PessoalDocumento2 páginasPlanilha de Orçamento PessoalMoisés JúniorAinda não há avaliações
- Apostila Curso Matlab Fluxograma BomDocumento31 páginasApostila Curso Matlab Fluxograma BomEduardo Yuji SakuradaAinda não há avaliações
- Mocidade Autoconfrontação 10-05-2015Documento3 páginasMocidade Autoconfrontação 10-05-2015Moisés JúniorAinda não há avaliações
- DTRDocumento1 páginaDTRMoisés JúniorAinda não há avaliações
- Aparelho CISCODocumento3 páginasAparelho CISCOMoisés JúniorAinda não há avaliações
- Relatório 2 - Ferrugem No AçoDocumento6 páginasRelatório 2 - Ferrugem No AçoMoisés JúniorAinda não há avaliações
- Difusão de componentes orgânicos no arDocumento22 páginasDifusão de componentes orgânicos no arMoisés JúniorAinda não há avaliações
- Apostila IV - Tratamento de Água - Versão 02-08Documento11 páginasApostila IV - Tratamento de Água - Versão 02-08Moisés JúniorAinda não há avaliações
- Bloco 1 - Empresa e Gerenciamento de Um EmpreendimentoDocumento17 páginasBloco 1 - Empresa e Gerenciamento de Um EmpreendimentoMoisés JúniorAinda não há avaliações
- Bloco 6 - Analise de SensibilidadeDocumento22 páginasBloco 6 - Analise de SensibilidadeMoisés JúniorAinda não há avaliações
- Bloco 7 - Alavancagem FinanceiraDocumento17 páginasBloco 7 - Alavancagem FinanceiraMoisés JúniorAinda não há avaliações
- Quimica Aplicada - PETROBRASDocumento104 páginasQuimica Aplicada - PETROBRASMateus Guimarães100% (1)
- Conceitos BásicosDocumento38 páginasConceitos BásicosMoisés JúniorAinda não há avaliações
- Isomeria - Exercícios AvançadosDocumento5 páginasIsomeria - Exercícios AvançadosNanda OdebrechtAinda não há avaliações
- Radiação Solar e Movimentos da TerraDocumento12 páginasRadiação Solar e Movimentos da TerraAdjaci Brito100% (2)
- Química 1 Série 2º Sem 2015Documento53 páginasQuímica 1 Série 2º Sem 2015Edvaldo MagalhãesAinda não há avaliações
- 1° Ano - 2B PDFDocumento130 páginas1° Ano - 2B PDFEdilson Junior0% (1)
- Grupos Funcionais 2Documento6 páginasGrupos Funcionais 2Danilo TourinhoAinda não há avaliações
- Resolução de exercícios de Química InorgânicaDocumento24 páginasResolução de exercícios de Química InorgânicaCarmen Paulino100% (2)
- Exercicíos Gerais QUIMICA GERALDocumento13 páginasExercicíos Gerais QUIMICA GERALWylace AndradeAinda não há avaliações
- Forças Intermoleculares: Tipos e PropriedadesDocumento26 páginasForças Intermoleculares: Tipos e PropriedadesjnfjjuniorAinda não há avaliações
- Análise da condutividade iônica de soluções de NaCl e CH3COOHDocumento20 páginasAnálise da condutividade iônica de soluções de NaCl e CH3COOHMadson ZanoniAinda não há avaliações
- GROMACS-Tutorial (Portuguese BR) v.1.2Documento29 páginasGROMACS-Tutorial (Portuguese BR) v.1.2lauramdf100% (3)
- Nanotecnologia Pró-PazDocumento6 páginasNanotecnologia Pró-PazyvessantosAinda não há avaliações
- Quimica - AULA - 02 - Matéria e Suas TransformaçõesDocumento16 páginasQuimica - AULA - 02 - Matéria e Suas Transformaçõesmax_antoniAinda não há avaliações
- Forças IntermolecularesDocumento22 páginasForças IntermolecularesjoabeAinda não há avaliações
- 8-Quimica para Ciencias BiologicasDocumento68 páginas8-Quimica para Ciencias BiologicasciceroAinda não há avaliações
- Compendio de Teosofia - C.W. LeadBeaterDocumento83 páginasCompendio de Teosofia - C.W. LeadBeaterThamos de Tebas75% (4)
- Introducao A Quimica Novo Formato para AlunosDocumento11 páginasIntroducao A Quimica Novo Formato para Alunosfernando lealAinda não há avaliações
- Química - Cadernos Temáticos - BohrDocumento9 páginasQuímica - Cadernos Temáticos - BohrQuimica PasseiAinda não há avaliações
- O Seu Portal de Cursos-13Documento10 páginasO Seu Portal de Cursos-13Jaque MartinsAinda não há avaliações
- Componente Curricular BNCC QuimicaDocumento25 páginasComponente Curricular BNCC QuimicaAnonymous CdTpWVdM7Ainda não há avaliações
- Ligações IntermolecularesDocumento24 páginasLigações IntermolecularesDaniel CamposAinda não há avaliações
- Enem Por AssuntoDocumento224 páginasEnem Por AssuntoCarlos Silva100% (2)
- Avaliação Individual 1 - Química OrgânicaDocumento5 páginasAvaliação Individual 1 - Química OrgânicaEAD - Apoio Curso de QuímicaAinda não há avaliações
- 4 º Bim - LIGAÇÕES QUÍMICA - ExerciciosDocumento2 páginas4 º Bim - LIGAÇÕES QUÍMICA - ExerciciosFernanda Da CostaAinda não há avaliações
- Aula OrbitaismolecularesDocumento21 páginasAula OrbitaismolecularesLeonardo LubeAinda não há avaliações
- Polaridade das Moléculas no 1o BimestreDocumento1 páginaPolaridade das Moléculas no 1o BimestreCassioLucasAinda não há avaliações
- Apostila AAEPPDocumento179 páginasApostila AAEPPRodrigo MelaniAinda não há avaliações
- Química do Ensino Médio: Reações, Elementos e CompostosDocumento4 páginasQuímica do Ensino Médio: Reações, Elementos e CompostosBIAMANINI15Ainda não há avaliações
- Ficha - 3 TLQ - A 2021Documento5 páginasFicha - 3 TLQ - A 2021carolg 0408Ainda não há avaliações
- Quimica de Coordenacao Aula 3Documento26 páginasQuimica de Coordenacao Aula 3Gabriel Bonifacio ViagemAinda não há avaliações
- Tecnologia Dos Materiais - Complementar PDFDocumento97 páginasTecnologia Dos Materiais - Complementar PDFdiego_lcsouzaAinda não há avaliações