Escolar Documentos
Profissional Documentos
Cultura Documentos
Utilização Emn de H 1 Determinação
Enviado por
Prof-Alexsandro FerreiraDireitos autorais
Formatos disponíveis
Compartilhar este documento
Compartilhar ou incorporar documento
Você considera este documento útil?
Este conteúdo é inapropriado?
Denunciar este documentoDireitos autorais:
Formatos disponíveis
Utilização Emn de H 1 Determinação
Enviado por
Prof-Alexsandro FerreiraDireitos autorais:
Formatos disponíveis
Quim. Nova, Vol. 28, No.
6, 1061-1065, 2005
D
i
v
u
l
g
a
o
*e-mail: juceni@ufba.br
UTILIZAO DE RMN DE
1
H NA DETERMINAO DA CONFIGURAO ABSOLUTA DE LCOOIS
Marizeth L. Barreiros e Jorge M. David
Instituto de Qumica, Universidade Federal da Bahia, Campus de Ondina, 40170-290 Salvador - BA
Juceni P. David*
Faculdade de Farmcia, Universidade Federal da Bahia, Campus de Ondina, 40170-290 Salvador - BA
Recebido em 12/7/04; aceito em 17/3/05; publicado na web em 24/8/05
UTILIZATION OF
1
H NMR IN THE DETERMINATION OF ABSOLUTE CONFIGURATION OF ALCOHOLS. This review reports
the determination of absolute configuration of primary and secondary alcohols by
1
H NMR spectroscopy, using the Mosher method.
This method consists in the derivatization of an alcohol possessig unknown absolute configuration with one or both enantiomers
of an auxiliary reagent. The resulting diastereoisomer spectra are registered and compared, and the chemical shift differences (
R,S
=
R
-
S
) are measured. The determination of the absolute configuration of the alcohol molecule is based on the correlation between
its chiral center and the auxiliary reagents chiral center. Therefore, the determination of the absolute configuration depends on
aromatic ring shielding effects on the substituents of the alcohol as evidenced by the
1
H NMR spectrum.
Keywords: absolute configuration; alcohols; Moshers reagent.
INTRODUO
Nas ltimas dcadas houve aumento no desenvolvimento de
mtodos sensveis e confiveis para determinao da configurao
absoluta. Esse aumento deveu-se principalmente ao isolamento de
grande nmero de produtos naturais opticamente ativos e aos re-
centes avanos na rea da sntese assimtrica
1
, uma vez que de
interesse das indstrias farmacuticas e agrcolas a preparao de
enantimeros puros. Neste contexto, a determinao da
estereoqumica tem sido de valiosa importncia para a qumica de
produtos naturais, assim como para a qumica sinttica tendo em
vista que a estrutura de um composto no pode ser considerada
determinada at que sua configurao absoluta seja conhecida.
Alguns mtodos fsicos so utilizados na determinao da
estereoqumica absoluta de compostos orgnicos, tais como a
cristalografia de Raios-X e a excitao de quiralidade
1-3
. A difrao
de raios X o mtodo de maior importncia na elucidao estrutural
de produtos naturais complexos, sendo o nico que permite a deter-
minao da configurao absoluta diretamente. Porm, limitado
pela necessidade da obteno de monocristais adequados. Entre os
mtodos de excitao de quiralidade os mais sensveis so o
Dicrosmo Circular (DC) e a Disperso tica Rotatria (DOR), que
so utilizados na determinao da configurao absoluta de alguns
centros qirais. Estes tambm apresentam limitaes, assim, foram
desenvolvidos outros mtodos para auxiliar na determinao da con-
figurao absoluta de compostos orgnicos, tais como aqueles reali-
zados atravs de reaes qumicas, como o mtodo de Harada e
Nakanishi, bem como o mtodo de Horeau, utilizados para determi-
nar configurao absoluta de lcoois
1,2,4
. Estes ltimos so baseados
na anlise do Dicrosmo Circular (DC). Outro mtodo muito utiliza-
do para determinao da configurao absoluta o mtodo de Mosher.
Inicialmente foi introduzido por Raban e Mislow, tendo sido poste-
riormente adaptado por Mosher, Trost e Dale, entre outros pesquisa-
dores
5
. O mtodo adaptado por Mosher utiliza reagentes de
derivatizao quiral (RDQ) e posterior anlise por RMN de
1
H. O
interesse despertado por este mtodo baseia-se tanto na possibilida-
de de trabalhar com amostras em pequenas quantidades, quanto de-
vido a sua simplicidade. Entretanto, este mtodo requer a presena
de grupos funcionais especficos na molcula, tais como -CO
2
H, -
NH
2
e OH, necessrios para ligar o substrato ao reagente. Portanto,
mostra-se til apenas para lcoois primrios e secundrios, aminas
primrias e secundrias e para cidos carboxlicos. Vrios reagentes
auxiliares tm sido descritos na literatura com essa finalidade
2,4,6
,
dentre estes os mais utilizados so cido -metoxi--trifluorometil
fenil actico MTPA (1), cido -metoxi-fenil actico MPA (2), ci-
do l-naftil--metoxi actico 1-NMA (3) , cido 2-naftil--metoxi
actico 2-NMA (4), cido 9-antranil--metoxi actico 9-AMA (5) e
cido 2-antranil--metoxi actico 2-AMA (6) (Figura 1).
O MTODO
O mtodo de Mosher baseado na dupla derivatizao ou na
simples derivatizao. A dupla derivatizao consiste na esterificao
do lcool de configurao absoluta desconhecida com os dois
Figura 1. Reagentes de derivatizao quiral
1062 Quim. Nova Barreiros et al.
enantimeros (R) e (S) do reagente auxiliar quiral, enquanto que a
simples derivatizao consiste na esterificao do lcool com ape-
nas um dos enantimeros do reagente auxiliar, (R) ou (S). Nos dois
mtodos, so registrados os espectros dos dois diasteroismeros re-
sultantes da reao e comparados, sendo realizada a medida da dife-
rena dos deslocamentos qumicos
R, S
. A determinao da confi-
gurao R/S no centro quiral do lcool feita atravs da correlao
entre esse centro e o centro quiral do reagente auxiliar que de
configurao absoluta conhecida, de acordo com o efeito de prote-
o e/ou desproteo que o grupo aromtico do reagente auxiliar
produzir nos hidrognios dos substituintes L
1
e L
2
do lcool.
O reagente auxiliar deve possuir algumas caractersticas estru-
turais especiais, tais como a presena de um grupo (Z = grupos
carboxilatos, hidroxlicos ou cloretos) capaz de ligar o lcool ao
reagente atravs desse grupo e tambm de um grupo (Y= anel aro-
mtico ou grupo insaturado) com forte efeito anisotrpico para pro-
duzir efeito de proteo ou desproteo nos substituintes L
1
/L
2
do
lcool. Finalmente, deve possuir um grupo polar (R
1
e R
2
) necess-
rio para auxiliar a fixao da molcula na conformao preferida
7
.
Alguns critrios devem ser levados em considerao para que o
mtodo possa ser aplicado. Entre estes, o espectro de RMN de
1
H
deve apresentar, claramente, sinais distinguveis e identificveis de
hidrognio nos dois substituintes L
1
/L
2
do lcool. Deste modo, nor-
malmente utiliza-se equipamentos de campo maior (> 7,05 Tesla).
Outra caracterstica requerida estabelece que o lcool deve apresen-
tar hidrognio nos dois substituintes L
1
/L
2
, e que os sinais de deslo-
camento qumicos ()
nos substituintes L
1
/L
2
sejam opostos. Deste
modo, espera-se que todos os deslocamentos dos hidrognios de L
1
apresentem mesmo sinal de , e todos os deslocamentos dos hidro-
gnios de L
2
tambm apresentem mesmo sinal de .
REAGENTES
O reagente MTPA
O reagente de Mosher MTPA (1) foi introduzido por Mosher
8
em 1969. Este encontrado comercialmente como cido ou cloreto
de cido em ambas as formas enantiomericamente puras. um dos
reagentes auxiliares mais populares para reconhecimento da
estereoqumica absoluta de lcoois secundrios e aminas primri-
as, ambos -substitudos
7,9
.
Os steres de MTPA, de acordo com clculos semiempricos,
so constitudos de trs confrmeros principais
10,11
de baixa ener-
gia em equilbrio e com populaes similares dos confrmeros sp
1
,
sp
2
e ap
1
independentemente da estrutura do lcool que so gera-
dos pelas rotaes em torno das ligaes C-C=O e C-Ph.
Conforme pode ser observado na Figura 2, em alguns
confrmeros o anel aromtico produz proteo e em outros,
desproteo. Assim, nos steres de (R)-MTPA o grupo L
1
est lo-
calizado na regio de desproteo do anel aromtico no confrmero
ap
1
, e no afetado nos confrmeros sp
1
e sp
2
. Entretanto, o grupo
em L
2
est localizado na regio de proteo do anel aromtico no
confrmero sp
1
e na regio de desproteo do confrmero sp
2
, no
sendo afetado no confrmero ap
1
(Figura 2a). Nos steres de (S)-
MTPA o substituinte L
1
est localizado na rea de proteo do anel
aromtico no confrmero sp
1
e na regio de desproteo no
confrmero sp
2
, no sendo afetado no confrmero ap
1
. Enquanto
que, nestes steres, o substituinte L
2
est na regio de desproteo
do anel aromtico no confrmero ap
1
, no sendo afetado nos
confrmeros sp
1
e sp
2
, respectivamente (Figura 2b). Neste caso, os
efeitos anisotrpicos de proteo e desproteo do anel aromtico
nos confrmeros sp
1
e sp
2
so cancelados mutuamente. Portanto, o
efeito mais acentuado no espectro de RMN de
1
H ser aquele do
confrmero ap
1
, que de desproteo. Os valores de
R,S
so cal-
culados de acordo com as frmulas:
R, S
L
1
= (
R
L
1
-
S
L
1
) e
R,S
L
2
= (
R
L
2
-
S
L
2
). Tendo em vista que nos steres de MTPA
o confrmero ap
1
predomina, o substituinte L
1
mais desprotegido
nos steres do ismero (R)-MTPA, significando que (
R, S
L
1
> 0),
enquanto que o substituinte L
2
mais desprotegido nos steres do
ismero (S)-MTPA que no ismero (R)-MTPA, de modo que
R,S
L
2
< 0.
O reagente MPA
O reagente MPA (2) foi introduzido por Raban e Mislow
12
e,
assim como o reagente de Mosher, comercialmente encontrado
na forma de cido ou cloreto de cido nas duas configuraes
enantiomericamente puras, sendo tambm um dos reagentes mais
utilizados para determinao da configurao absoluta de lcoois
secundrios--substitudos
2,7,10,12,13
.
Diferentemente dos steres de MTPA, os steres de MPA de
acordo com clculos semiempricos
2,10,13
so constitudos de 2
confrmeros principais de baixa energia independentemente da
estrutura do lcool: sp e ap. Estes so gerados pelas rotaes em
torno das ligaes C-C=O e C-Ph, sendo o confrmero sp mais
estvel (Figura 3).
De acordo com estes resultados nos steres de (R)-MPA, o gru-
po L
1
est na regio de proteo do anel aromtico no confrmero
sp e no afetado no confrmero ap, enquanto que o grupo L
2
protegido no confrmero ap e no est sendo afetado no confrmero
sp (Figura 3a). Por outro lado, nos steres de (S)-MPA o grupo L
2
est na regio de proteo do anel aromtico no confrmero sp e
no afetado no confrmero ap, enquanto que o grupo L
1
est na
zona de proteo do anel aromtico no confrmero ap e no est
sendo afetado no confrmero sp (Figura 3b). Alternativamente, nos
steres de MPA o confrmero predominante sp. Deste modo, o
grupo L
1
mais protegido nos steres de (R)-MPA que nos steres
do enantimero (S)-MPA. Assim
R, S
L
1
< 0, enquanto que o grupo
L
2
est mais protegido nos steres do enantimero (S)-MPA, de
modo que
R, S
L
2
> 0.
Comparao entre os reagentes MTPA e MPA
Pode-se observar que entre os steres de MTPA (1) e MPA (2),
os steres derivados de MTPA apresentam comportamento
Figura 2. Principais confrmeros dos steres de MTPA (1)
1063 Utilizao de RMN DE
1
H na Determinao da Configurao Absoluta de lcoois Vol. 28, No. 6
conformacional mais complexo em torno da ligao C-Ph. Nes-
ses steres derivados de MTPA, o anel aromtico apresenta trs
orientaes e no exerce forte preferncia conformacional por ne-
nhuma delas. Observa-se leve predominncia do confrmero ap
1
,
que exerce efeito de desproteo, tanto sobre o grupo L
1
quanto L
2
,
devido ao cancelamento mtuo dos outros dois confrmeros sp
1
e
sp
2
, enquanto que nos steres de MPA o anel aromtico tem prefe-
rncia conformacional, sendo o confrmero sp o principal. Esse
exerce efeito de proteo, de forma que se observam maiores valo-
res de deslocamentos qumicos
R,S
. Isso possibilita que o MPA
seja melhor escolha de reagente para a determinao da configura-
o absoluta de lcoois secundrios que o MTPA.
Os reagentes AMAA
Os derivados aril metoxilados do cido actico (AMAA) 1-
NMA (3), 2-NMA (4), 9-AMA (5) e 2-AMA (6) so utilizados
para determinao da configurao absoluta de lcoois secundri-
os--substitudos
2,14
e lcoois primrios--substitudos
15
. Estas subs-
tncias foram desenvolvidas para melhorar os valores da variao
dos deslocamentos qumicos
R, S
obtidos com MPA e MTPA. Este
efeito pode ser obtido atravs da substituio do grupo fenila do
MPA por outro grupo com sistema aromtico mais eficiente, como
naftila e antranila, capaz de produzir deslocamentos qumicos cer-
ca de 3 vezes maiores que aqueles obtidos com MPA
2,14
(Tabela 1).
A eficincia destes grupos principalmente devida ao aumen-
to de tamanho do anel aromtico que, conseqentemente, aumenta
a rea do cone de proteo do sistema aromtico e, por outro lado,
devido a fatores estricos, onde a conformao mais estvel
favorecida. Assim, observa-se o aumento na populao relativa deste
confrmero produzindo aumento nos valores de
R,S
. Os reagentes
1-NMA (3) e 9-AMA (5) so utilizados para determinao da con-
figurao absoluta principalmente de lcoois cclicos, enquan-
to que os reagentes 2-NMA (4) e 2-AMA (6) so empregados para
lcoois lineares de cadeia longa
14
.
Dentre estes reagentes, o 9-AMA (5) e o 2-AMA (6) so os mais
eficientes para determinao da configurao absoluta de lcoois pri-
mrios
15
, pois apresentam rea do cone magntico maior, tendo con-
seqentemente, uma rea de maior alcance. Nos lcoois primrios, a
distncia entre o centro assimtrico do lcool e o anel aromtico do
reagente auxiliar maior que em lcoois secundrios. Deste modo, os
valores de
R,S
em lcoois primrios so maiores e mais confiveis
com o 9-AMA (5), que com aqueles obtidos com os outros reagentes
que tm um grupo fenila. Estes reagentes apresentam comportamento
conformacional igual ao MPA (2) apresentando 2 confrmeros princi-
pais sp e ap, onde o confrmero sp o mais estvel.
Este mtodo pode ser aplicado tanto para lcoois secundrios--
substitudos quanto para lcoois primrios--substitudos, com grande
variedade de grupos e substituies como os exemplos do Quadro 1.
Porm, este no confivel para lcoois primrios altamente impe-
didos, tais como os exemplificados em 8-10. Isto devido s dificul-
dades destes adotarem a conformao ideal, levando a valores de
R,S
muito baixos. Ele tambm no pode ser aplicado para lcoois
primrios--substitudos, ou seja, com o centro quiral distante de
duas ligaes, tais como em 11 e 12. A partir destes dois exemplos
pode-se observar uma distribuio irregular nos sinais. Este fato pode
ser atribudo, principalmente, tanto a fatores estricos quanto dis-
tncia entre o centro assimtrico do lcool e o anel aromtico do
reagente auxiliar, haja vista que o efeito de proteo do anel arom-
tico diminui com a distncia. No exemplo 11 todos os valores de
R,S
para os substituintes L
1
/L
2
so positivos e, no exemplo 12 em
um dos substituintes verifica-se valor positivo e negativo de
R,S
do
mesmo lado, invalidando o mtodo.
Outra maneira de aumentar os valores da variao dos desloca-
mentos qumicos
R,S
daqueles obtidos com MPA atravs da
diminuio da temperatura no probe do RMN.
O primeiro passo a ser seguido a modificao da diferena de
energia entre os dois confrmeros, atravs da variao da tempera-
tura. De acordo com a equao de Boltzman, o decrscimo de 100
C no caso dos steres de MPA leva ao aumento em cerca de 10% na
populao relativa do confrmero sp, o que corresponde ao au-
mento de, no mnimo, 33% no valor
2,15
de
R,S
.
Estudos realizados sobre a variao de
R,S
com a temperatura
para os steres de MPA (2) e para os steres dos outros AMAA (2-
NMA (4) e 9-AMA (5) mostraram que os valores de
R,S
destes
ltimos reagentes so similares queles obtidos com os steres de
MPA (2). Isto provavelmente ocorre devido a fatores estricos que
impedem a desestabilizao do equilbrio, fazendo com que os va-
Tabela 1. Valores de para os steres dos AMAA.: 9-AMA(5), 1-NMA(3), 2-NMA(4), MTPA(1).
R, S
Reagente lcool CH
3
(1) CH
2
(2) CH
2
(3) CH
2
(4) CH(5)
MTPA 0,07 0,11 0,04 -0,07 -0,13
1-NMA 0,23 0,31 0,13 -0,15 -0,27
2-NMA 13 (Quadro 1) 0,37 0,55 0,22 -0,23 -0,47
9-AMA 0,59 0,90 0,35 -0,36 -0,37
CH
3
(8) CH
3
(9) CH
3
(10)
MTPA -0,17 -0,04 0,07
1-NMA 6 (Quadro1) -0,52 -0,065 0,11
2-NMA -0,36 -0,35 0,04
9-AMA -0,79 -0,75 0,19
Figura 3. Principais confrmeros dos steres de MPA (2)
1064 Quim. Nova Barreiros et al.
lores de
R,S
no cresam na mesma proporo que quando usa-
do o MPA (2) (Figura 4). Melhores resultados so observados so-
mente com o MPA (2). Desta forma, com o aumento da populao
do confrmero sp o substituinte L
1
deslocado no ster do
enantimero (R)-MPA para campo de proteo, enquanto o
substituinte L
2
deslocado para campo de desproteo. Assim
T1,T2
L
1
> 0 e
T1,T2
L
2
< 0, respectivamente. Ao contrrio, com o ster
do enantimero (S)-MPA o grupo L
1
deslocado para campo de
desproteo e o grupo L
2
deslocado para campo de proteo. Sendo
assim,
T1,T2
L
1
< 0 e
T1,T2
L
2
> 0, respectivamente.
Condies experimentais para registro dos espectros dos
derivados
Dupla derivatizao
As condies operacionais de RMN devem ser temperatura
ambiente e usar como solvente, CDCl
3.
Os espectros de RMN dos
dois enantimeros devem ser registrados na mesma temperatura,
concentrao e solvente. Alm disso, importante utilizar a mes-
ma referncia interna para ajustar os valores de deslocamentos.
A determinao da configurao absoluta atravs da dupla
derivatizao requer ambos os enantimeros, e o assinalamento da
configurao R/S deve-se seguir as etapas como determinadas na Fi-
gura 5: esterificao do lcool com os enantimeros (R) e o (S) do
reagente auxiliar, registro dos espectros de RMN de
1
H dos dois
diasteroismeros; em seguida, deve-se escolher arbitrariamente os
substituintes L
1
e L
2
e atribuir corretamente os valores de RMN de
1
H
destes grupos L
1
e L
2
nos dois diastermeros (R) e (S). Assim, compa-
ram-se os valores de deslocamento qumicos destes substituintes L
1
e
L
2
em ambos os derivados e calculam-se as diferenas de
R,S
. Os
parmetros de clculo da diferena de
R,S
so definidos como os
valores de deslocamento qumico para o hidrognio do substituinte L
1
no derivado auxiliar-R menos o deslocamento qumico do mesmo hi-
drognio do grupo L
1
do derivado auxiliar-S, tal como nas equaes
R,S
L
1
=
R
L
1
-
S
L
1
e
R,S
L
2
=
R
L
2
-
S
L
2
. Assim, tem-se como
resultado a determinao da configurao R/S baseada na correlao
entre a estereoqumica no centro quiral do reagente auxiliar e os des-
locamentos qumicos dos substituintes L
1
e L
2
nos dois diasteroismeros
resultantes da reao. Deste modo, o assinalamento da configurao
depende do efeito de proteo que o grupo aromtico do reagente
auxiliar produz nos hidrognios dos substituintes L
1
e L
2
do lcool. Se
os valores de do substituinte L
1
ou do substituinte L
2
so deslocados
para campo de proteo significa que este grupo est localizado no
mesmo lado do plano do anel aromtico.
Simples derivatizao
As condies de RMN devem contemplar baixa temperatura
(-70 C) e uso do solvente CS
2
/CD
2
Cl
2
(4:1). A determinao da confi-
gurao absoluta requer o uso de apenas um dos enantimeros. Desse
modo, o assinalamento da configurao R ou S realizado a partir da
esterificao do lcool com um dos enantimeros (R) ou (S) do reagente
auxiliar MPA (2)
16
(Figura 6) e, registro do espectro de RMN de
1
H do
diasteroismero a temperatura ambiente T
1
e do espectro baixa tem-
peratura T
2
. O parmetro para clculo da diferena de
T1,T2
defini-
do como o valor de deslocamento qumico para o hidrognio do
substituinte L
1
no derivado temperatura ambiente T
1
subtraindo-se o
valor do deslocamento qumico do mesmo hidrognio deste derivado
a baixas temperaturas T
2
, tal como dado na equao
T1,T2
L
1
=
T1
L
1
Quadro 1. Exemplos de lcoois secundrios e lcoois primrios. Reproduzido
das refs. 14 e 15, com permisso da Elsevier
Figura 4. Grfico do aumento proporcional para os valores de
R,S
para o
grupo metila dos AMAA, 2 (MPA), 4 (2-NMA), 5 (9-AMA) e 7 com o decrscimo
da temperatura no probe. Reproduzido da ref. 15, com permisso da Elsevier
1065 Utilizao de RMN DE
1
H na Determinao da Configurao Absoluta de lcoois Vol. 28, No. 6
-
T2
L
1
e
T1,T2
L
2
=
T1
L
2
-
T2
L
2
. O assinalamento da configurao R/
S idntico ao de lcoois na dupla derivatizao.
CONCLUSES
A tcnica de RMN apresenta vantagens em relao a outras tcni-
cas para determinao da configurao devido a sua simplicidade, alm
da possibilidade de trabalhar com pequenas quantidades de amostra.
O mtodo de Mosher confivel para determinao da configu-
rao absoluta de lcoois primrios e secundrios, tanto cclicos como
acclicos, desde que obedeam os parmetros conforme indicados
no Mtodo para que a tcnica possa ser aplicada. Porm, no
confivel para determinao da configurao absoluta de molculas
de estruturas muito complexas e com vrios grupos hidroxlicos.
O melhor reagente auxiliar para determinao da configurao
absoluta de lcoois secundrios--substitudos o MPA (2) e para
lcoois primrios--substitudos o 9-AMA.
REFERNCIAS
1. Rinaldi, P. L.; Prog. Nucl. Magn. Reson. Spectrosc. 1982, 15, 291.
2. Seco, J. M.; Latypov, S. K.; Quio, E.; Riguera, R.; Tetrahedron 1997,
53, 8541.
3. Ohtani, I.; Kusumi, T.; Kashman, Y.; Kakisawa, H.; J. Am. Chem. Soc. 1991,
113, 4092.
4. Eliel, E. L.; Wilen, S. H.; Mander, L. N.; Stereochemistry of Organic
Compounds, New York, 1994, p. 140.
5. Latypov, S. K.; Ferreiro, M. J.; Quio, E.; Riguera, R.; J. Am. Chem. Soc.
1998, 120, 877; Seco, J. M.; Latypov, S. K.; Quio, E.; Riguera, R.;
Tetrahedron: Asymmetry 1995, 6, 107.
6. Seco, J. M.; Quio, E.; Riguera, R.; Tetrahedron: Asymmetry 2001, 12,
2915; Fukushi, Y.; Yajima, C.; Mizutani, J.; Tetrahedron Lett. 1994, 35, 599.
7. Seco, J. M.; Quio, E.; Riguera, R.; J. Org. Chem. 1999, 64, 4669.
8. Parker, D.; Chem. Rev. 1991, 91, 1441.
9. Chataigner, I.; Lebreton, J.; Durand, D.; Guingant, A.; Villiras, J.;
Tetrahedron Lett. 1998, 39, 1759; Kusumi, T.; Fujita, Y.; Ohtani, I.;
Kakisawa, H.; Tetrahedron Lett. 1991, 32, 2923; Velten, R.; Steglich, W.;
Anke, T.; Tetrahedron: Asymmetry 1994, 5, 1229; Kouda, K.; Ooi T.;
Kusumi, T.; Tetrahedron Lett. 1999, 40, 3005; Ohtani, I.; Kusumi, T.;
Kashman, Y.; Kakisawa, H.; J. Org. Chem. 1991, 56, 1296.
10. Latypov, S. K.; Seco, J. M.; Quio, E.; Riguera, R.; J. Org. Chem. 1996 ,
61, 8569.
11. Harada, K.; Shimizu, Y.; Kawakami, A.; Kiyonaga, F.; Tetrahedron Lett.
1999, 40, 9081.
12. Trost, B. M.; Belletire, J. L.; Godleski, S.; McDougal, P. G.; Balkovec, J.
M.; J. Org. Chem. 1986, 51, 2370.
13. Latypov, S. K.; Seco, J. M.; Quio, E.; Riguera, R.; J. Org. Chem. 1995,
60, 504.
14. Kouda, K.; Kusumi, T.; Ping, X.; Kan, Y.; Hashimoto, T.; Asakawa, Y.;
Tetrahedron Lett. 1996, 37, 4541; Seco, J. M.; Latypov, S. K.; Quio, E.;
Riguera, R.; Tetrahedron Lett. 1994, 35, 2921; Kusumi, T.; Takahashi, H.;
Xu, P.; Fukushima, T.; Asakawa, Y.; Hashimoto, T.; Kan, Y.; Inouye, Y.;
Tetrahedron Lett. 1994, 35, 4397; Takahashi, H.; Kusumi, T.; Tetrahedron
Lett. 1996, 36, 7087; Takahashi, H.; Iwashima, M.; Iguchi, K.; Tetrahedron
Lett. 1999, 40, 333.
15. Latypov, S. K.; Ferreiro, M. J.; Quio, E.; Riguera, R.; J. Am. Chem. Soc.
1998, 120, 4741; Ferreiro, M. J.; Latypov, S. K.; Quio, E.; Riguera, R.;
Tetrahedron: Asymmetry 1996, 7, 2195.
16. Ward, D. E.; Rhee, C. K.; Tetrahedron Lett. 1991, 32, 7165.
Figura 5. Procedimentos para determinao da configurao do (R)-2-
pentanol. Reproduzido da ref. 6, com permisso da Elsevier
Figura 6. Procedimentos para assinalamento da configurao do (R)-2-
butanol. Reproduzido da ref. 5, com permisso da Elsevier
Você também pode gostar
- Ponto S Cranio Met RicosDocumento3 páginasPonto S Cranio Met RicosCesar Odilon PereiraAinda não há avaliações
- EducaçãoDocumento2 páginasEducaçãoProf-Alexsandro FerreiraAinda não há avaliações
- Sistema Muscular X Atividade Física PDFDocumento4 páginasSistema Muscular X Atividade Física PDFProf-Alexsandro FerreiraAinda não há avaliações
- Bio1 Parte 10 PDFDocumento4 páginasBio1 Parte 10 PDFVictor BorgesAinda não há avaliações
- Informações Sobre o PETDocumento5 páginasInformações Sobre o PETProf-Alexsandro FerreiraAinda não há avaliações
- BIODIVERSIDADE COMO Fonte de MedicamentosDocumento3 páginasBIODIVERSIDADE COMO Fonte de MedicamentosToxinologiaAinda não há avaliações
- Pop Da Clinica FortimagemDocumento31 páginasPop Da Clinica FortimagemProf-Alexsandro FerreiraAinda não há avaliações
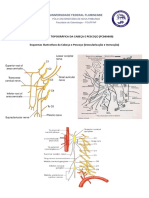
- Esquemascabecaepescoco PDFDocumento3 páginasEsquemascabecaepescoco PDFProf-Alexsandro FerreiraAinda não há avaliações
- Sistema Muscular HumanoDocumento9 páginasSistema Muscular HumanoProf-Alexsandro FerreiraAinda não há avaliações
- Exposição Ocupacional em Intervencionismo: Problemas e SoluçõesDocumento20 páginasExposição Ocupacional em Intervencionismo: Problemas e SoluçõesProf-Alexsandro FerreiraAinda não há avaliações
- Hidrogenação de Óleos e suas Aplicações IndustriaisDocumento16 páginasHidrogenação de Óleos e suas Aplicações IndustriaisProf-Alexsandro FerreiraAinda não há avaliações
- PET CecilDocumento9 páginasPET Cecilrad_rickAinda não há avaliações
- Programas de garantia da qualidade em mamografiaDocumento28 páginasProgramas de garantia da qualidade em mamografiaProf-Alexsandro Ferreira100% (1)
- Racionalidade de MedicamentosDocumento4 páginasRacionalidade de MedicamentosProf-Alexsandro FerreiraAinda não há avaliações
- Desenvolvimento da Radiologia IntervencionistaDocumento3 páginasDesenvolvimento da Radiologia IntervencionistaProf-Alexsandro FerreiraAinda não há avaliações
- Procedimentos de Radiologia Intervencionista CardíacaDocumento69 páginasProcedimentos de Radiologia Intervencionista CardíacaSamuel DutraAinda não há avaliações
- Radioatividade (Exercícios) - Com GabaritoDocumento23 páginasRadioatividade (Exercícios) - Com GabaritoJosimar Lima FerreiraAinda não há avaliações
- QC Radiodiagnostic 05 ThomazDocumento72 páginasQC Radiodiagnostic 05 ThomazRicardo SantosAinda não há avaliações
- Apostila Pratica Quimica ComputacionalDocumento88 páginasApostila Pratica Quimica ComputacionalRafael GomesAinda não há avaliações
- Medicamentos Antimitóticos Com Atuação No Sítio de Ligação Colchicina - Artigos de Farmácia - Portal EducaçãoDocumento16 páginasMedicamentos Antimitóticos Com Atuação No Sítio de Ligação Colchicina - Artigos de Farmácia - Portal EducaçãoProf-Alexsandro FerreiraAinda não há avaliações
- Cap 1Documento10 páginasCap 1robsonnogueiraAinda não há avaliações
- Questões para EstudoDocumento2 páginasQuestões para EstudoProf-Alexsandro FerreiraAinda não há avaliações
- Resolução de Problemas - Fisica MedicaDocumento10 páginasResolução de Problemas - Fisica MedicaProf-Alexsandro FerreiraAinda não há avaliações
- Elementos de EstatísticaDocumento105 páginasElementos de EstatísticaProf-Alexsandro FerreiraAinda não há avaliações
- Funções OrganicasDocumento2 páginasFunções OrganicasBruno Gossler SchmidtAinda não há avaliações
- Bioquimica e Quimica OrganicaDocumento23 páginasBioquimica e Quimica OrganicaProf-Alexsandro FerreiraAinda não há avaliações
- Coeficiente de PartiçãoDocumento1 páginaCoeficiente de PartiçãoDiogo CoelhoAinda não há avaliações
- Estereoisomeria - A Interface Da Tecnologia Industrial de Medicamentos E Da Racionalização TerapêuticaDocumento9 páginasEstereoisomeria - A Interface Da Tecnologia Industrial de Medicamentos E Da Racionalização TerapêuticaProf-Alexsandro FerreiraAinda não há avaliações
- Isomeria OpticaDocumento4 páginasIsomeria OpticaProf-Alexsandro Ferreira0% (1)
- RMN 2D: técnicas de detecção indireta e gradiente de campoDocumento6 páginasRMN 2D: técnicas de detecção indireta e gradiente de campoProf-Alexsandro FerreiraAinda não há avaliações
- CONCEITOS BÁSICOS DE HIDROLOGIA E DRENAGEM PARA PROJETOS RODOVIÁRIOS - Exercício Avaliativo - Módulo 4 - Revisão Da TentativaDocumento3 páginasCONCEITOS BÁSICOS DE HIDROLOGIA E DRENAGEM PARA PROJETOS RODOVIÁRIOS - Exercício Avaliativo - Módulo 4 - Revisão Da TentativaRanieri Carvalho67% (3)
- The Scum Villains Self Saving SystemDocumento1.445 páginasThe Scum Villains Self Saving SystemAlex60% (5)
- Manual Google AgendaDocumento8 páginasManual Google AgendaFellipe Costa PedrosaAinda não há avaliações
- Fispq Sumatane Comp BDocumento13 páginasFispq Sumatane Comp BClara trabalhos extraAinda não há avaliações
- AD - Direito AeronáuticoDocumento4 páginasAD - Direito AeronáuticoÍcaro Marcolin SampaioAinda não há avaliações
- HFC História e Filosofia CiênciaDocumento3 páginasHFC História e Filosofia CiênciaCarlos NássaroAinda não há avaliações
- Periurbano en Bahia BlancaDocumento17 páginasPeriurbano en Bahia Blancaarvillamdp8704Ainda não há avaliações
- Erros Lava e Seca SamsungDocumento4 páginasErros Lava e Seca SamsungPriscila Oliveira75% (8)
- Cinema Militante - TeseDocumento393 páginasCinema Militante - TeseLuiz Gustavo P S CorreiaAinda não há avaliações
- LGPD MapeamentoDocumento20 páginasLGPD MapeamentoSurubimAinda não há avaliações
- Cópia de Shamata e Vipashyana - Tulku UrgyenDocumento8 páginasCópia de Shamata e Vipashyana - Tulku UrgyenAtha IddhiAinda não há avaliações
- Tabela de Calor Específico Da ÁguaDocumento2 páginasTabela de Calor Específico Da ÁguaNilson PalmeirimAinda não há avaliações
- Atividade Mapa Materiais e RevestimentosDocumento3 páginasAtividade Mapa Materiais e RevestimentosAline VieiraAinda não há avaliações
- Contagens, números e ordens no 4o anoDocumento139 páginasContagens, números e ordens no 4o anojulianagsramosAinda não há avaliações
- Métodos de Avaliaçãod e RiscosDocumento108 páginasMétodos de Avaliaçãod e RiscosGabriel Gaspar100% (1)
- Bobone Foto RadiografiasDocumento54 páginasBobone Foto RadiografiasMargaridaMedeiros100% (1)
- A representação do negro na literatura infantil de LobatoDocumento7 páginasA representação do negro na literatura infantil de LobatothisbeAinda não há avaliações
- Contabilidade Geral - Exercícios - Aula01 Princípios Fund ContabDocumento28 páginasContabilidade Geral - Exercícios - Aula01 Princípios Fund ContabDebiticia100% (3)
- Ficha de Trabalho de Português sobre o Sonho Espacial de um MeninoDocumento5 páginasFicha de Trabalho de Português sobre o Sonho Espacial de um MeninoVera AfonsoAinda não há avaliações
- Crie Seu Pendrive de BootDocumento5 páginasCrie Seu Pendrive de BootNhynguyka Almeida100% (2)
- Metais de Engenharia Níquel Titânio ZircônioDocumento6 páginasMetais de Engenharia Níquel Titânio ZircônioRuiter SantosAinda não há avaliações
- Questionwords E Três Atividades de Verificação Da AprendizagemDocumento13 páginasQuestionwords E Três Atividades de Verificação Da AprendizagemMarilia Andreia Jekel de FreitasAinda não há avaliações
- D7 (3 Série - EM - Mat.) - Blog Do Prof. WarlesDocumento4 páginasD7 (3 Série - EM - Mat.) - Blog Do Prof. WarlesANTONIA OLIVEIRA DA SILVAAinda não há avaliações
- Pesquisa Quantitativa Descritiva Sobre A Rede Hoteleira de CampinasDocumento18 páginasPesquisa Quantitativa Descritiva Sobre A Rede Hoteleira de Campinasgeorgia_novaesAinda não há avaliações
- LANTEKDocumento4 páginasLANTEKSatel SoaresAinda não há avaliações
- De Profundis (Oscar Wilde) (Z-Library)Documento168 páginasDe Profundis (Oscar Wilde) (Z-Library)Robson Demetrio0% (1)
- Gestão do Escopo do Projeto: EAP e os 10 MandamentosDocumento18 páginasGestão do Escopo do Projeto: EAP e os 10 MandamentosMaclei AllvesAinda não há avaliações
- Anexo 01 Manual Do UsuarioDocumento89 páginasAnexo 01 Manual Do Usuariojimison francoAinda não há avaliações
- prt7 m15Documento9 páginasprt7 m15Margarida InácioAinda não há avaliações
- Apostila USCSDocumento117 páginasApostila USCSMarcus Vinicius Sousa SousaAinda não há avaliações