Escolar Documentos
Profissional Documentos
Cultura Documentos
SDRA en Ventilaciòn Mecanica
Enviado por
Estefa Tavera VelezDireitos autorais
Formatos disponíveis
Compartilhar este documento
Compartilhar ou incorporar documento
Você considera este documento útil?
Este conteúdo é inapropriado?
Denunciar este documentoDireitos autorais:
Formatos disponíveis
SDRA en Ventilaciòn Mecanica
Enviado por
Estefa Tavera VelezDireitos autorais:
Formatos disponíveis
Redalyc
Sistema de Informacin Cientfica
Red de Revistas Cientficas de Amrica Latina, el Caribe, Espaa y Portugal
Gonzlez, Silvia B.
Sndrome de distrs respiratorio agudo (SDRA) y Ventilacin Mecnica (VM)
Bioqumica y Patologa Clnica, Vol. 72, Nm. 1, 2008, pp. 21-31
Asociacin Bioqumica Argentina
Argentina
Disponible en: http://redalyc.uaemex.mx/src/inicio/ArtPdfRed.jsp?iCve=65112135003
Bioqumica y Patologa Clnica
ISSN (Versin impresa): 1515-6761
info@aba-online.org.ar
Asociacin Bioqumica Argentina
Argentina
Cmo citar?
Nmero completo
Ms informacin del artculo
Pgina de la revista
www.redalyc.org
Proyecto acadmico sin fines de lucro, desarrollado bajo la iniciativa de acceso abierto
REVISTA BIOQUIMICA Y PATOLOGIA CLINICA VOL 72 N 1 2008
Trabajo: pgs 21 | 31
Pg | 21
Sndrome de distrs respiratorio agudo (SDRA)
y Ventilacin Mecnica (VM)
Silvia B. Gonzlez
RESUMEN
Bioqumica especialista en Qca. Clnica.
Orientacin Medio Interno y Gases
Jefe de laboratorio: Hospital de
Rehabilitacin Respiratoria Mara Ferrer .
Ciudad Autnoma de Bs. As.
Es un cuadro clnico con comienzo agudo, dinmico y explosivo que aparece
como resultado de una reaccin inamatoria difusa y severa del parnquima pulmonar. El dao ocurre a nivel de la membrana alveolar (unidad alvolo-capilar)
ocasionado por una alteracin de la permeabilidad capilar, con la formacin de
un edema exudativo rico en protenas.
Es una condicin clnica, que pese a los avances tecnolgicos, contina teniendo
alta mortalidad. El tratamiento sigue siendo, fundamentalmente, de soporte,
por lo que la ventilacin mecnica es la herramienta ms importante para tratar
a los pacientes con SDRA.
Lugar de trabajo:
Hospital de Rehabilitacin Respiratoria
Mara Ferrer . Ciudad Autnoma de Bs. As.
Contacto:
Paraguay N 3007 Dto. 21 A (1425)
Ciudad Autnoma de Bs. As.
e-mail: silbgonzalez@bertel.com.ar
Revista ByPC. Incorporada al Latindex.
ISSN 1515-6761 Cdigo Bibliogrco: RByPC
Trabajo Recibido: 14-02-08 Aceptado: 01-04-08
SUMMARY
Acute respiratory distress syndrome (ARDS) AND Mechanical ventilation (MV)
ARDS is a clinical condition with an acute, dynamic and explosive onset that
appears as a result of a diffuse and severe inammatory reaction of the lung
parenchyma. Damage occurs at the alveolar membrane level (alveolar-capillary
unit) and is caused by a capillary permeability alteration that leads to a proteinrich exudative edema.
Despite technological progresses, this condition leads to a high mortality rate.
Treatment still involves primarily supportive care, so mechanical ventilation is
the most important tool in the treatment of patients with ARDS.
Sndrome de distrs respiratorio agudo (SDRA) y ventilacin mecnica (VM)
DESARROLLO
SDRA: fue descrito por Ashbaugh y Petty en 19671. Es un
cuadro clnico con comienzo agudo, dinmico y explosivo
como resultado de una reaccin inamatoria difusa y severa del parnquima pulmonar. El dao ocurre a nivel de
la membrana alveolar (unidad alvolo-capilar) ocasionado
por una alteracin de la permeabilidad capilar, con la formacin de un edema exudativo, rico en protenas
Se caracterriza por:
1 Shunt intrapulmonar e hipoxemia refractaria al
O2 a pesar de altas concentraciones de oxgeno
suplementario
2 Disminucin progresiva de la compliance pulmonar
3 Inltrado pulmonar difuso con expresin radiolgica
4 Ausencia de insuciencia cardiaca congestiva
5 Antecedentes causales
5) Transporte gaseoso: mecanismo de transporte del oxgeno y
del anhdrido carbnico en la sangre hacia y desde los tejidos.
6) Mecnica de la respiracin: mecanismo que mueve al
pulmn y la pared torcica. Intervienen los msculos respiratorios. Son de importancia las propiedades elsticas y las
resistencias que se deben vencer para asegurar la buena
mecnica respiratoria.
7) Control de la ventilacin: Este proceso siolgico de intercambio requiere de la interaccin armoniosa de todos los
componentes que forman parte del sistema respiratorio:
pulmones, sistema nervioso central, vasos pulmonares, va
area superior e inferior, caja torcica y msculos. Finalmente, el sistema respiratorio interacciona con el sistema
cardiovascular para el transporte de estos gases hacia y
desde la clula. De esta manera se obtiene y transporta el
oxgeno necesario para la produccin de energa a nivel mitocondrial y se remueve el dixido de carbono producto del
metabolismo celular.
Aparato respiratorio
Es una condicin clnica con alta mortalidad pese a los
avances tecnolgicos. El tratamiento contina siendo fundamentalmente de soporte siendo la ventilacin mecnica (VM) la herramienta ms importante en el tratamiento
de pacientes con SDRA.
El SDRA se caracteriza en su comienzo, como se ha dicho,
por un dao agudo de la membrana alvolo capilar con aumento de la permeabilidad vascular. De esta forma, la alteracin inicial consiste en la ocupacin alveolar por un lquido rico en protenas. Esta ocupacin reduce la supercie
alveolar disponible para el intercambio gaseoso. A medida
que el SDRA progresa, se producen fenmenos vasculares
que alteran signicativamente el intercambio gaseoso. La
situacin se agrava por la aparicin de zonas con nula ventilacin debido al desarrollo de atelectasias en diferentes
reas del pulmn y, en denitiva al shunt intrapulmonar.
Todos estos factores conguran el cuadro de hipoxemia
refractaria al aumento de la fraccin inspirada de oxgeno
(FiO2) caracterstica de esta entidad clnica.
INTRODUCCIN A LA ANATOMOFISIOLOGA DEL APARATO
RESPIRATORIO
Intercambio gaseoso normal
La funcin respiratoria puede ser dividida en siete componentes estrechamente relacionados entre s:
1) Ventilacin: mecanismo a travs del cual el aire inspirado
llega a los alvolos y el aire alveolar llega a la atmsfera.
La ventilacin alveolar es la porcin del aire ambiente que
realiza intercambio gaseoso con la sangre del pulmn.
2) Difusin: mecanismo por el cual los gases atraviesan las
paredes alveolares, siguiendo la Ley de Fick.
3) Perfusin: mecanismo a travs del cual la sangre retira el
oxgeno del pulmn y libera en l el anhdrido carbnico
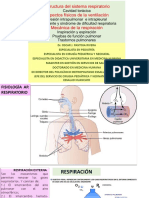
Fig 1.El aire inhalado pasa a travs de la traquea, que
se divide en dos tubos denominados bronquios. Dentro
de los pulmones los bronquios dan la los conductos
alveolares stos terminan en los alvolos.
Musculo bronquiolar
Cavidad nasal
Cavidad oral
Laringe
Traquea
Alveolo
Conducto alveoral
Broquio
Bronquiolos
Pulmon
El pulmn permite que un volumen determinado de aire se
ponga en contacto de manera transitoria e intermitente con
la supercie de intercambio gaseoso. Para cumplir con esta
funcin, posee dos caractersticas fundamentales: una gran
facilidad para deformarse (distensibilidad) y una gran capacidad para recuperar su forma inicial (elasticidad). En virtud
de estas dos caractersticas y por accin de los msculos, el
pulmn permite que un volumen determinado de aire lo distienda, entrando desde la atmsfera hasta el alvolo para
ponerse en contacto con la supercie de intercambio gaseoso. Luego, al suspenderse el estmulo inspiratorio y gracias
a sus propiedades elsticas, el pulmn recupera su forma
inicial expulsando el aire que lo distenda hacia la atmsfera. ste fenmeno de entrada y salida de aire conforman el
ciclo respiratorio o el ciclo de inspiracin-espiracin que se
repite alrededor de 12 a 16 veces cada minuto en el sujeto
adulto normal (frecuencia respiratoria).
Pg | 23
REVISTA BIOQUIMICA Y PATOLOGIA CLINICA VOL 72 N 1 2008
Trabajo: pgs 21 | 31
La distensibilidad pulmonar, conocida como compliance
est determinada por tres factores principales:
1.- El volumen pulmonar, siendo inversamente proporcional
a ste, es decir, cuanto ms volumen tenga el pulmn ms
difcil ser expandirlo y viceversa.
2.- La presencia del surfactante pulmonar que logra disminuir la tensin supercial en el interior del alvolo y de esta
manera evita la tendencia natural de ste hacia el colapso.
3.- La disposicin geomtrica de las bras de elastina.
Compliance: se reere a la facilidad con que se expanden
los pulmones y el trax durante los movimientos respiratorios. Se pueden calcular por separado la compliance de la
caja torcica y de los pulmones y est determinada por el
volumen y la elasticidad pulmonar.
Una compliance elevada indica falta de recuperacin elstica de los pulmones, como ocurre en el ensema; una compliance disminuida supone que es necesaria una mayor
presin para producir cambios de volumen, como ocurre en
la brosis pulmonar, el edema o la ausencia de surfactante.
Alvolos pulmonares:
El alvolo es la parte nal del rbol respiratorio y acta como
unidad primaria de intercambio gaseoso. La barrera gassangre entre el espacio alveolar y los capilares pulmonares
es extremadamente na, permitiendo un rpido intercambio
gaseoso. Para alcanzar la sangre, el O2 debe difundir a travs
del epitelio alveolar, el no espacio intersticial, y el endotelio
capilar. El CO2 sigue el camino inverso para llegar al alvolo.
Fig 1. El pulmn humano adulto posee una gran supercie
para el intercambio gaseoso, ya que est formado por ms
de 300 millones de alvolos y 100 millones de capilares
dispuestos en una red tridimensional.
Los neumocitos tipo II son ms compactas y son las responsables de producir surfactante, un fosfolpido que cubre los
alvolos y sirve para reducir sensiblemente la tensin supercial contribuyendo a la estabilidad alveolar.
Adems, se encuentran los macrfagos alveolares que son
fagocitos errantes que retiran las partculas diminutas de
polvo y otros desechos del espacio alveolar.
Alrededor de los alvolos, hay una red de capilares proveniente de las arteriolas y vnulas del lobulillo; estos capilares tienen una pared de una sola capa de clulas endoteliales.
La barrera alveolo-capilar que separa el espacio areo de la
sangre capilar es de slo 0,5 micras de grosor, lo que permite un eciente intercambio gaseoso, siempre que la ventilacin sea adecuada.
El intercambio de O2 y de CO2 entre los espacios alveolares
de los pulmones y la sangre ocurre por difusin a travs de
las paredes alveolares y capilares. Se produce gracias al
acoplamiento entre la ventilacin y la perfusin3.
Composicin del aire alveolar
Gas
Aire ambiente
Gas alveolar
N2
78.62 %
74.90 %
O2
20.84 %
13,60 % (104 mmHg)
CO2
0.04 %
5.30 % (40 mmHg)
H2O
0.5 %
6,20 % (47 mmHg)
TOTAL
100 %
100 %
Volmenes pulmonares
En reposo, la ventilacin alveolar, es decir, la ventilacin minuto menos la ventilacin del espacio muerto, es de aproximadamente 5.250 ml/minuto y coincide, aproximadamente, con el valor del gasto cardaco. Dado que todo el gasto
cardaco pasa por los pulmones, la relacin entre ventilacin y perfusin (V/Q) del sistema cardiopulmonar global es
aproximadamente = 1
Volmenes Pulmonares
Ventilacin Alveolar ( VA)
VA = (500-150) X 15 = 5.250 ml/min
Volumen Corriente: 500 ml
Frecuencia: 15/min.
La membrana alveolar: sitio del intercambio gaseoso
Existen dos tipos de clulas epiteliales alveolares:
Los neumocitos tipo I, clulas epiteliales planas simples
que forman un revestimiento de la pared alveolar y son el
sitio de intercambio gaseoso.
Ventilacin Total ( VT)
VT= 500 X 15 = 7.500 ml/min
Espacio muerto anatmico
VD : 150 ml
Sndrome de distrs respiratorio agudo (SDRA) y ventilacin mecnica (VM)
Unidades alvolo capilares: Distribucin de la ventilacin
(V) en relacin con la perfusin (Q)
Tanto la ventilacin como la perfusin que recibe el pulmn
debe distribuirse de manera uniforme entre los millones de
unidades alvolo-capilares para asegurar un correcto intercambio gaseoso.
La relacin V/Q normal debera ser = 1 (por cada ml de aire
las unidades recibiran 1 ml de sangre).
Cuando la unidad alvolo-capilar recibe ms aire que sangre
V/Q ser mayor que 1.
Cuando predomina la perfusin sobre la ventilacin la relacin V/Q ser menor que 1.
En un pulmn sano la mayora de las unidades conservan
un balance entre ventilacin y perfusin. Sin embargo V y Q
no se distribuyen de manera uniforme a travs del pulmn
y esas diferencias se explican por los efectos de gravedad y
por la elasticidad del parnquima pulmonar.
V/Q es menor que 1 en la base pulmonar y alcanza valores
de 3 en el pice.
La heterogeneidad de los cocientes V/Q aumenta con la
edad y durante las patologas pulmonares, ya sea por alteracin de la ventilacin, de la perfusin, o de ambas.
Las reas de elevado cociente V/Q causan ventilacin inecaz. Su extremo mximo (cuando tiende a innito) se denomina efecto espacio muerto.
El desequilibrio extremo de las relaciones V/Q, con abolicin
completa de la ventilacin alveolar en una serie de unidades
pulmonares se denomina efecto shunt Estas unidades
mantienen ntegra su perfusin capilar (V/Q =0).
El SDRA se caracteriza por la presencia de shunt.
Este tipo de shunt (intrapulmonar) debe distinguirse desde el punto de vista anatmico del shunt intracardaco (extrapulmonar), con paso directo de sangre venosa hacia la
circulacin arterial sistmica (comunicacin interauricular,
comunicacin interventricular, etc.). Sin embargo, sus consecuencias funcionales son idnticas: hipoxemia arterial
grave acompaada, en general, de hipocapnia debido a que
la hiperventilacin compensadora del resto del parnquima pulmonar sano consigue restaurar la cifra de pCO2 a la
normalidad. No sucede lo mismo con la pO2, ya que debido
a la forma sigmoidea de la curva de disociacin de la oxihemoglobina, la sangre que pasa por las unidades alveolares
hiperventiladas no aportan oxgeno adicional, de forma que
no evita la presencia de hipoxemia arterial 4.
Una caracterstica fundamental del shunt como factor intrapulmonar de intercambio de gases inecaz, es su falta de
respuesta a la oxigenoterapia.
La paO2 es un indicador de la oxigenacin de la sangre
arterial y monitorea la captacin pulmonar de O2.
Saturacin fraccional de O2 (OxiHb% )
Valores de referencia:
Adultos y nios: 96%
Gama aceptable: 94- 98%
Gradiente alvolo arterial de O2
a/A: paO2/pAO2
pAO2 = FiO2 X (PB - 47) paCO2/ R
R: cociente respiratorio; PB: Presin baromtrica
Valores de referencia:
a/A: 0.85 - 0.95
a/A: Indica que porcentaje del aire alveolar ha llegado a la
arteria.
PaFi: Indice pO2/FiO2
Valores de referencia:
Normales > 350 - 400 mmHg
Hipoxemia moderada:
Valores entre 150 y 300 mmHg
Hipoxemia severa < 150 mmHg
Parmetros habituales para monitorear la captacin
pulmonar de O2
paO2: Presin parcial de O2 en sangre arterial
Valores de referencia:
Adultos y nios: 97 mmHg
Gama aceptable: > 85 mmHg
Tercera edad: pO2 = 103.5 - (0.4 edad)
Las causas precipitantes pueden dividirse en: dao pulmonar directo o dao pulmonar secundario a una lesin en otro
rgano (dao indirecto)
Algunos autores 6 sugieren diferencias en la siopatologa y
la mecnica pulmonar segn la etiologa del SDRA. Sin embargo, el pronstico en relacin con la mortalidad est inuido en los primeros 3 das por la severidad de la enfermedad
SDRA: SINDROME DE DISTRES RESPIRATORIO AGUDO: En el
SDRA ocurre un cuadro de edema pulmonar por aumento de
la permeabilidad capilar. Debido a esto, la alteracin inicial
consiste en una ocupacin de los alvolos por un lquido rico
en protenas. El edema reduce la supercie alveolar disponible para el intercambio gaseoso, incrementando las reas
pulmonares con pobre o nula ventilacin. A medida que el
SDRA progresa, se producen fenmenos vasculares que
afectan de forma diferente al intercambio gaseoso, dando
lugar a heterogeneidad en los valores de la relacin V/Q.
Esta situacin se agrava por la aparicin de zonas con nula
ventilacin en relacin con la aparicin de atelectasias en
distintas zonas del pulmn. Todos estos factores conguran el cuadro de hipoxemia refractaria al O2, a pesar de los
aumentos en la fraccin inspirada de oxgeno5.
Antecedentes causales de SDRA
Dao pulmonar directo
Neumona
Aspiracin gstrica
Contusin pulmonar
Edema pulmonar por reperfusin
Ahogamiento
Dao pulmonar indirecto
Sepsis
Trauma severo
Fracturas mltiples
Postoperatorio de ciruga
cardiovascular
Pancreatitis
Sobredosis de drogas
ntoxicaciones
REVISTA BIOQUIMICA Y PATOLOGIA CLINICA VOL 72 N 1 2008
Trabajo: pgs 21 | 31
inicial, y despus por la presencia de complicaciones.
Es una condicin clnica de alta mortalidad que ha disminuido en la ltima dcada. La mejora se vincula al tratamiento
de soporte ms que a una mejora especca del dao pulmonar 7.
Percent of ARDS
Patients Dying
Fig 5
Year
Fisiopatologa de SDRA:
El pulmn supone una gran supercie para el intercambio
gaseoso, y por lo tanto est equipado de amplia serie de
mecanismos de defensa frente a las diversas agresiones a
las que se ve expuesto (patgenos, txicos, estmulos mecnicos, etc.)8.
La lesin pulmonar en el SDRA puede producirse como consecuencia de alteraciones pulmonares y extrapulmonares
y su siopatologa es el resultado de una compleja interaccin de mediadores humorales y celulares.
La patognesis de la lesin pulmonar aguda se sustenta en
4 pilares fundamentales: a) dao endotelial y epitelial; b)
activacin de clulas inamatorias; c) balance entre citoquinas pro y antiinamatorias; d) necrosis y apoptosis.
A la compleja interaccin entre estos mecanismos se aade
una quinta va de lesin, producida por el estrs mecnico
que supone la ventilacin mecnica.
a) El dao de las supercies endoteliales y epiteliales interrumpe la funcin de barrera del pulmn. Los espacios alveolares se llenan con membranas hialinas y con lquido de
edema abundante en protenas y clulas inamatorias. Los
espacios intersticiales, los conductos alveolares, los vasos
pequeos y los capilares tambin contienen macrfagos,
neutrlos y eritrocitos. Hay inactivacin del surfactante,
e inamacin 9.
Todo esto conduce a las anormalidades en el intercambio
gaseoso y la prdida de la distensibilidad pulmonar.
Los eventos ocurridos se reejan en la presencia de inltrados bilaterales. La tomografa computarizada del trax
demuestra con frecuencia reas heterogneas de consolidacin y de atelectasias, aunque puede haber inamacin
incluso en reas aparentemente conservadas.
b) La activacin de clulas inamatorias est, en gran medida, mediada por el acmulo de neutrlos en los capilares
alveolares. No est demasiado claro si son causa o conse-
Pg | 25
cuencia del dao pulmonar agudo10.
La interaccin entre las clulas endoteliales y los leucocitos
es un proceso fundamental en el desarrollo de SDRA, en tanto que constituye el primer paso en la migracin de dichos
leucocitos desde los capilares hacia el parnquima pulmonar y la subsiguiente respuesta inamatoria.
c) El balance entre citoquinas pro y antiinamatorias determinar tambin el desarrollo de esta patologa.
Un complejo grupo de citoquinas y otros factores proinamatorios inician y amplican la respuesta inamatoria en
la lesin pulmonar aguda y el SDRA. Asimismo, en el alvolo
se encuentran inhibidores endgenos de estas citoquinas
proinamatorias. 11
d) Necrosis y apoptosis
La agresin (microbiolgica, qumica o mecnica) a las clulas del epitelio alveolar puede desencadenar fenmenos
de necrosis, caracterizada por un fallo global de todas las
estructuras celulares, prdida de la integridad de membrana y liberacin del contenido celular.
Todo esto desencadena una respuesta inamatoria alrededor de la clula necrosada.
En el SDRA puede agravarse por la presencia de neutrlos
que liberan proteasas y radicales libres.
La neutrolia caracterstica del SDRA puede deberse a una
alteracin en la migracin, a un exceso de activacin o a un
descenso en la apoptosis de los neutrlos. Los mediadores
inamatorios como citoquinas, la hipoxia y la acidosis activan a los neutrlos y retrasan su apoptosis. No se conocen
completamente los mecanismos que producen la inamacin alveolar en el SDRA, pero la disminucin de la apoptosis
de los neutrlos podra ser un factor importante ya que
normalmente funciona como un mecanismo regulador, permitiendo la eliminacin de los neutrlos del rea afectada
con un mnimo dao pulmonar12
Es importante destacar que la fase aguda se puede resolver
o progresar hacia otra brosa (brosis con depsito de colgeno), con hipoxemia persistente, incremento del espacio
muerto, hipertensin pulmonar y prdida adicional de la distensibilidad pulmonar.
Alteraciones del Intercambio gaseoso en el SDRA
Luego de la ocupacin alveolar por edema rico en protenas se reduce la supercie disponible para el intercambio
gaseoso. La sangre venosa que llega al pulmn para su oxigenacin se encuentra con alvolos llenos de lquido, esto
conllevar un aumento de las reas con relacin V/Q baja o
nula (shunt). Ante esta alteracin y la hipoxemia acompaante, el sistema respiratorio responde con un aumento de
la ventilacin minuto. No obstante, debido a la ocupacin
fsica de los alvolos, este aumento de la ventilacin se dirige a las zonas ya previamente aireadas, de forma que slo
consigue hiperventilar zonas preservadas, sin modicar las
zonas con efecto shunt. Por ello, la gasometra mostrar hipoxemia, con hipocapnia y alcalosis en esta fase inicial13.
Uno de los factores ms importantes en el SDRA es el au-
Sndrome de distrs respiratorio agudo (SDRA) y ventilacin mecnica (VM)
mento del gasto cardaco, por lo tanto, aumenta la perfusin
de las zonas no ventiladas, al tiempo que recluta capilares
previamente cerrados. Esto empeora el efecto shunt y la
hipoxemia. Por otra parte, si coexiste hipoperfusin perifrica, la presin venosa de O2 (pvO2) puede ser baja, con lo
que la sangre no oxigenada a su paso por el pulmn estar
an ms hipxica y contribuir a una mayor hipoxemia de la
sangre arterial.
Los mediadores inamatorios liberados pueden afectar de
forma muy diversa al intercambio gaseoso: mientras que
unos producen broncoconstriccin que aumentar las desigualdades V/Q, otros producen vasoconstriccin pulmonar
que aumentar la velocidad del ujo sanguneo a travs de
los pulmones, con reduccin del tiempo para el intercambio
de gases en el alvolo. Si esta vasoconstriccin pulmonar
afecta mayoritariamente al esfnter precapilar, se reducir
el aujo sanguneo pulmonar, lo que podra reducir la produccin de edema pulmonar. Aquellos mediadores que afecten mayoritariamente el esfnter postcapilar conllevarn a
mayor estasis capilar pulmonar, con aumento de la presin
capilar y del edema pulmonar. Por ltimo, si la vasoconstriccin pulmonar llega a ser severa encontraremos fallo
ventricular derecho por cor pulmonale agudo, y puede agravarse el deterioro de la pvO2 y su efecto secundario sobre la
hipoxemia.
A medida que el SDRA progresa, se producen fenmenos
vasculares que afectan de forma diferente al intercambio
gaseoso. Por una parte, las zonas mal ventiladas por la ocupacin alveolar reaccionan a la hipoxia local con vasoconstriccin localizada, reduciendo el aporte de ujo sanguneo
a estas zonas y redirigindolo hacia las zonas bien ventiladas. Algo ms tarde, ocurren fenmenos de microtrombosis
de pequeos vasos pulmonares que producen zonas de espacio muerto y que aumentan los desequilibrios V/Q. Esto
explicara la frecuente evolucin hacia un estado de hipercapnia progresiva (aumento de la pCO2 arterial) a pesar del
aumento de la ventilacin minuto lograda con la ventilacin
mecnica.
Un factor adicional en el empeoramiento del intercambio gaseoso progresivo del SDRA es la formacin de atelectasias
en las zonas declives. stas se ven favorecidas por el decbito supino prolongado, la sedacin profunda con o sin parlisis muscular, la ausencia de contraccin activa diafragmtica y, por ltimo, la reabsorcin del gas inspirado cuando
se emplean concentraciones elevadas de oxgeno, lo que
se conoce como atelectasias por desnitrogenizacin. Estas
zonas de muy bajo o nulo V/Q se aaden a las que existen,
congurando el cuadro de hipoxemia refractaria al aumento
del oxgeno inspirado.
En las fases ms evolucionadas del SDRA el intercambio
gaseoso se ve afectado por nuevos factores. Por un lado, la
ventilacin mecnica que provoca hiperinsuacin. Se producen dilataciones de los sacos alveolares con destruccin
de paredes alveolares, como en el ensema, con un efecto
aditivo de mayor espacio muerto, que empeora las relacio-
nes V/Q, al incrementar las reas de V/Q muy elevado.
Un factor no claramente establecido es la afectacin de la
capacidad de difusin a travs de la membrana alveolocapilar, que se producira a partir de la primera semana de
evolucin del SDRA, debido a los procesos de formacin de
membranas hialinas y, posteriormente, de brosis pulmonar que ocurren.
Fig 6. En la gura se puede ver con claridad la
destruccin de la arquitectura pulmonar que ocurre en
los pacientes con SDRA.
Parnquima normal
Parnquima SDRA
Resumen de los mltiples eventos ocurridos en el SDRA
Proceso inamatorio: da lugar a que solo un pequeo
volumen pulmonar est ventilado
Incremento de la permeabilidad capilar: mayor formacin de edema y lquido rico en protenas.
Depresin del surfactante y protenas asociadas
Colapso alveolar y lisis de clulas epiteliales
Fibrosis con depsito de colgeno
Disminucin de la compliance.
Aumento de la resistencia vascular pulmonar con hipertensin
Incremento del trabajo respiratorio
Aumento de los shunts pasando ms sangre desoxigenada por los alvolos no ventilados.
Hipoxemia refractaria al O2
REVISTA BIOQUIMICA Y PATOLOGIA CLINICA VOL 72 N 1 2008
Trabajo: pgs 21 | 31
Pg | 27
Gases en sangre arterial en la fase inicial: hipoxemia, con
hipocapnia y alcalosis respiratoria.
La ocupacin alveolar por edema rico en protenas, reduce
la supercie alveolar disponible para el intercambio gaseoso: Desequilibrio V/Q.
Ante esta alteracin y la hipoxemia, el sistema respiratorio
responde hiperventilando
sangre mientras se realizan las maniobras teraputicas a
los pacientes.
Un breve diccionario sobre la ventilacin mecnica nos permitir entender mejor este tipo de tratamiento y los resultados obtenidos en nuestras determinaciones.
La VM es una herramienta de soporte en el tratamiento de
pacientes con Insuciencia respiratoria severa.
Gases en sangre en pacientes con anormalidades severas:
Hipercapnia y acidosis respiratoria.
La eliminacin del CO2 se encuentra alterada por microtrombosis de pequeos vasos que producen zonas de espacio
muerto. Tambin se genera espacio muerto qumico creado
por la inhibicin de la anhidrasa carbnica producida por la
elastasa de los PMN .Todo lleva a que aumentan los desequilibrios V/Q.
Es importante destacar que dado la gravedad de estos pacientes las alteraciones en el equilibrio cido base pueden ser multifactoriales. En la gran mayora de los casos se
observan disturbios mixtos. Por lo tanto, a las alteraciones
respiratorias se suman las metablicas: acidosis metablica y/o alcalosis metablica.
El concepto clave es ciclo respiratorio, constituido por la inspiracin y la espiracin
El ciclo respiratorio depende de las siguientes variables: volumen, presin, ujo o tiempo.
Resumen de las causas de la hipoxemia
Pulmonares:
Shunt (puede ser > 20%)
Alteraciones V/Q
Aumento del espacio muerto
Extrapulmonares:
pvO2 baja.
La Conferencia de Consenso de las Sociedades Europea y
Americana (The American-European Consensus Comit)14
eligi en 1994 como marcador de la captacin pulmonar de
O2 al ndice PAFI, considerando los siguientes valores:
ALI..PAFI 300 mmHg
SDRA......... PAFI 200 mmHg
Los expertos consideraron que el trmino SDRA se reserve
para pacientes con anormalidades severas del intercambio
gaseoso y dene un grupo nuevo de pacientes con anormalidades menos severas del intercambio gaseoso. Este ltimo grupo se ha denominado injuria pulmonar aguda (ALI).
Son pacientes caracterizados por inamacin e incremento
de la permeabilidad alveolar.
Pero la severidad inicial de la hipoxemia tiene poco efecto en
el pronstico nal de los pacientes.
Tratamiento del SDRA: Ventilacin mecnica.
Como se mencion al principio el tratamiento del SDRA contina siendo fundamentalmente de soporte siendo la ventilacin mecnica la herramienta ms importante.
El idioma utilizado por mdicos y kinesilogos cuando ventilan un paciente, muchas veces resulta incomprensible para
los bioqumicos que esperamos las muestras de gases en
Volumen: volumen corriente o volumen tidal (VC): es la cantidad
de aire que el respirador enva al paciente en cada inspiracin.
Volumen minuto: se obtiene multiplicando la frecuencia
respiratoria por el volumen corriente de cada inspiracin.
Presin: en VM es la fuerza por unidad de supercie necesaria para desplazar un volumen corriente y se expresa en
cm de H2O.
Presin pico: es el valor en cm H2O obtenido al nal de la inspiracin.
Presin positiva al nal de la espiracin (PEEP): La presin
al nal de la espiracin debe ser cero, pero de una forma teraputica o derivado de la situacin clnica puede volverse
positiva, permite la reapertura alveolar y el reclutamiento
de reas colapsadas.
Generalmente se utilizan valores entre 5 y 20 cm de H2O.
Flujo: es la velocidad con la que el aire entra, depende del
volumen corriente y del tiempo en el que se quiere que pase,
llamado tiempo inspiratorio.
Fraccin inspirada de Oxigeno (FiO2): depende de la cantidad de O2 suministrada. Toma valores de 0.21 a 1.0
La VM se adapta a la situacin siopatolgica del paciente,
es decir, permite hacer una sustitucin completa o parcial
de la funcin respiratoria hasta la completa mejora.
La VM puede ser invasiva o no invasiva, dependiendo del
aislamiento de la va area. Es no invasiva si se utiliza
mascarilla facial, nasal, pas nasales o tubo endotraqueal
en la faringe. Es invasiva si se utiliza tubo endotraqueal o
traqueotoma. Una vez elegido cual es el tipo de ventilacin
mecnica necesitamos un respirador y las tubuladuras, que
unen al paciente y a la mquina entre si.
Tradicionalmente el tratamiento de la insuciencia respiratoria aguda y el SDRA se bas en la utilizacin en VM invasiva
con elevados volmenes corrientes, ya que este abordaje
se asociaba con mejor oxigenacin. Junto con una frecuencia respiratoria ajustada, el concepto se completaba con
el mantenimiento del pH y la PCO2 en valores cercanos a la
normalidad.
La PEEP se utilizaba para mantener la oxigenacin arterial y
sistmica evitando las FiO2 txicas. La idea era que la mejor
PEEP era la menor PEEP 15.
Sndrome de distrs respiratorio agudo (SDRA) y ventilacin mecnica (VM)
Este paradigma de ventilacin mecnica normxica - normocpnica con alto volumen corriente y la menor PEEP posible
fue aplicado a la mayora de los pacientes crticos.
Objetivo de la VM: promover un adecuado intercambio gaseoso, aliviar la dicultad respiratoria dando tiempo a que
el tratamiento de la enfermedad y los mecanismos de reparacin pulmonar permitan la mejora del paciente y evitar
complicaciones.
Uno de los cambios conceptuales, en el manejo de los pacientes crticos, es que la propia VM puede daar al pulmn e inducir o perpetuar la situacin de lesin pulmonar
aguda. Este fenmeno se produce tanto en los pulmones
sanos, como en aquellos ya previamente daados, pero es
de mucha mayor intensidad, tanto in vivo como en modelos
experimentales, en aquellos pulmones con lesin pulmonar
aguda preexistente16.
Son varios los mecanismos por los que la ventilacin mecnica puede ocasionar una lesin pulmonar inducida por el
respirador (VILI).
1. Barotrauma: es una lesin que se produce por cambios
de presin.
Fue demostrada por Webb y col 18, empleando un modelo
de ratas ventiladas durante 1 hora y utilizando diferentes
niveles de presin en su va area, con y sin PEEP. Los animales que fueron ventilados con presiones pico de 14 cm de
H2O no presentaron ningn cambio histolgico en el pulmn,
mientras que aquellos ventilados con alta presin (entre 30
y 45 cm de H2O) presentaron lesiones consistentes en un
importante edema tanto perivascular como alveolar.
2. Volutrauma: sobredistensin del tejido pulmonar, provocado por el efecto de volumen.
Kolobow y col19, estudiaron dos grupos de ovejas sanas
anestesiadas y ventiladas con un volumen
corriente (Vt) de 10 ml/kg y el otro grupo con un volumen
corriente de 50-70 ml/kg. Fueron observadas en un periodo
de 48 horas. Las de mayor volumen circulante desarrollaron
un dao pulmonar agudo caracterizado por la alteracin progresiva de la mecnica pulmonar y el deterioro del intercambio gaseoso, sin que existiera barotrauma.
3. Atelectrauma: Tambin existe evidencia que el uso de bajo
volumen corriente, puede originar injuria alveolar, conocido
como atelectrauma. Se produce por el mecanismo de cierre
y reapertura cclico de las unidades alveolares cerradas y da
lugar a fenmenos de carcter inamatorio (fenmeno de
reclutamiento/ desreclutamiento)20.
Otro mecanismo posible de dao por bajo Vt sera por inhibicin de la produccin de surfactante, contribuyendo a la atelectasia y al aumento de la permeabilidad microvascular.
Estas lesiones pueden corregirse con aumento de PEEP, que
recluta alvolos y los mantiene abiertos, estabilizndolos y
provocando un aumento de la compliance.
PEEP ejerce un efecto favorable sobre la integridad alveolar,
disminuyendo la ltracin de agua y solutos y secundariamente preservando al surfactante.
4. Biotrauma: El efecto de la ventilacin mecnica sobre la
respuesta inamatoria se ha denominado biotrauma 21.
Los resultados obtenidos en grandes ensayos clnicos en
los que se monitoriz una serie de citoquinas en pacientes
sometidos a volmenes tidal bajos o elevados demostraron
de manera sistemtica un aumento de citoquinas proinamatorias en el grupo de volumen tidal elevado. A pesar de
los resultados, a veces contradictorios en modelos experimentales, es innegable que la ventilacin mecnica puede
modular la respuesta inamatoria sistmica.
5. Toxicidad por el oxgeno: La oxigenoterapia es una medida
esencial para combatir la hipoxemia, pero el uso de altas
concentraciones de O2, sobre todo en un pulmn previamente lesionado, origina gran cantidad de radicales libres, los
cuales empeoran el dao pulmonar.
La toxicidad por el oxgeno depende del tiempo de exposicin y de la fraccin inspirada de O2 (a > FiO2 y a > tiempo de
exposicin > dao).
La causa de dao pulmonar inducido por el empleo de elevadas FiO2 puede ser el estrs oxidativo. Este dao se produce
mediante la produccin de diferentes agentes reactivos con
propiedades oxidantes, como el perxido de hidrgeno, los
radicales hidroxilos y los aniones superxido, que en modelos experimentales inducen fenmenos de apoptosis del
epitelio alveolar, adems de alteraciones de las funciones
celulares, fundamentalmente a nivel mitocondrial 17.
La cascada inamatoria que de manera global precede y acompaa el SDRA, origina una serie de cambios humorales, sistmicos y pulmonares, dentro de los cuales podemos mencionar:
activacin del complemento, amplia produccin de citoquinas,
activacin de la Foslipasa A2 y de la xido ntrico sintetasa
en su forma inducible y muchos otros cambios celulares. Sin
embargo, la amplia produccin de radicales libres de oxgeno,
la deplecin pulmonar de sustratos antioxidantes (alteracin
del balance oxidante-antioxidante) y el desequilibrio proteasas-antiproteasas se consideran como los elementos de gran
importancia en el desarrollo y severidad del SDRA 22 y 23.
Segn la Conferencia de Consenso sobre Ventilacin Mecnica 24 de 1993 la FiO2 utilizada debe ser la menor posible,
compatible con una adecuada saturacin de la sangre arterial, mayor o igual al 90%, y con una pO2 mayor o igual a 60
mmHg. Utilizando FiO2 inferiores al 50% no existen evidencia de toxicidad por el O2.
SDRA: Ventilacin mecnica con hipercapnia permisiva (HPC)
Permite una paCO2 alta manteniendo un pH > 7.20
La preocupacin por los efectos adversos de la ventilacin
mecnica fue aumentando con los aos. Tambin fue creciendo la experiencia en el uso de nuevas estrategias de VM
denominadas estrategias protectoras del pulmn. La hipercapnia es una consecuencia frecuente de estas estrategias.
Recordemos que la ventilacin mecnica normxica - normocpnica con alto volumen corriente y bajo PEEP fue el
utilizada tradicionalmente. Nuevos conocimientos fueron
cambiando esta modalidad teraputica utilizada por aos.
Pg | 29
REVISTA BIOQUIMICA Y PATOLOGIA CLINICA VOL 72 N 1 2008
Trabajo: pgs 21 | 31
Estudios clnicos:
El trabajo pionero fue realizado en 1990 por Hickling 25. Describe 50 pacientes con SDRA a quienes ventil limitando las
presiones de la va area y utilizando volmenes corrientes
bajos, cercanos a 5 ml/Kg. En esta serie la paCO2 alcanz valores promedios de 62 mmHg (rango 30-79 mmHg) y el pH
promedio fue de 7.29 (rango de 7.02 - 7.38), ambos hechos
revolucionarios para entonces.
La mortalidad obtenida por Hickling con el uso de hipercapnia permisiva fue de16%, bastante menor a las cifras reportadas de 40 a 60% para pacientes con SDRA.
En los ltimos dos aos, han aparecido cuatro estudios randomizados y prospectivos que comparan dos estrategias
ventilatorias: una ventilacin mecnica convencional con
volmenes corrientes superiores a 10 ml/Kg y una estrategia ventilatoria protectora que consiste, fundamentalmente, en limitar los volmenes y las presiones aplicadas sobre
la va area y permitir hipercapnia moderada.
Cuadro comparativo
Autor
N de pacientes
paCO2 mmHg (media)
pH (media)
Mortalidad % *
Referencia
Amato
29
58.2
7.19
38 vs 71
26
Brochard
58
59.5
7.28
47 vs 38
27
Brower
26
50.3
7.34
50 vs 46
28
Stewart
60
54.4
7.29
50 vs 47
29
* Mortalidad: VM con HPC vs VM tradicional
De ellos, slo el estudio de Amato mostr una disminucin
en la mortalidad con la estrategia protectora y los llev a terminar anticipadamente el estudio.
Cmo explicar estos resultados tan dispares? La respuesta
parece estar en la forma de aplicacin de la PEEP. Mientras los
otros estudios utilizaban niveles similares de PEEP en ambos
grupos de acuerdo a un algoritmo secuencial, Amato j la
PEEP sobre el punto de inexin en la curva presin-volumen,
de modo que su grupo en estudio recibi 16 cm de H2O de PEEP
mientras el grupo control slo 9. De este modo, el optimizar el
reclutamiento alveolar con un adecuado nivel de PEEP parece
ser mucho ms importante que evitar la sobredistensin producida por el uso de volmenes corrientes elevados.
La American Thoracic Society (ATS) mostr en el ao 2000
los resultados de un estudio prospectivo, randomizado y
multicntrico patrocinado por el National Heart, Lung &
Blood Institute (NHLBI), que fue suspendido al evaluar los
primeros 800 pacientes ya que la mortalidad disminuy en
un 25% (de 31 vs 40 %) al aplicar un Vt de 6 ml/Kg con relacin a un grupo VM tradicional con Vt de 12 ml/Kg 30.
El trabajo fue planteado para mantener un pH arterial entre
7.30-7.45
Comparando los resultados del primer da de VM
Bajo Volumen tidal (6 ml/kg): pH: 7.38 0.08 paCO2: 40
10 mmHg
Alto Volumen tidal (12 ml/kg): pH: 7.41 0.07 paCO2: 35
8 mmHg
Las diferencias estudiadas fueron estadsticamente signicativas (p< 0.05)
Estas investigaciones, sin duda alguna, han generado nuevas interrogantes y perspectivas en trminos de soporte
ventilatorio.
Existen casos de contraindicacin de la hipercapnia permisiva:
Contraindicacin absoluta de la Hipercapnia Permisiva: hipertensin endocraneana.
Contraindicaciones relativas de la Hipercapnia Permisiva:
cardiopata isqumica.
En sujetos normales el gasto cardiaco aumenta durante la
hipercapnia como resultado del incremento de la actividad
simptica, la liberacin de catecolaminas y el aumento en
la contractilidad del miocardio. Se produce aumento del ujo esplcnico y renal. La presin en la arteria pulmonar slo
aumenta ligeramente.
El pH intracelular se compensa ms rpidamente que el pH
extracelular durante la hipercapnia.
Adems, la inadecuada perfusin tisular se asocia con una
marcada acidosis intracelular hipercpnica que no se reeja
en la sangre arterial, por esta razn puede considerarse que
el pH arterial no reeja el pH intracelular, especialmente durante la hipercapnia de comienzo gradual.
Se considera que la acidosis puede resultar beneciosa en
ciertas circunstancias y que su correccin mediante el uso
de bicarbonato puede ser perjudicial ya que la acidosis puede facilitar la liberacin tisular de oxgeno al desviar hacia la
derecha la curva de disociacin HbO2.
Est bien demostrado, que la acidosis intracelular, resulta
citoprotectora durante la anoxia tisular y las investigaciones sugieren que las enzimas degradativas como las fosfolipasas y las proteasas (que se activan durante la deplecin
de ATP), resultan inactivadas por el pH cido. La utilizacin
de cidos jos para generar acidosis de reperfusin, aumentan la recuperacin del miocardio tras la reperfusin. Este
efecto qued demostrado en la acidosis por hipercapnia y
no se apreci en la acidosis metablica.
La HPC previene el aumento de la permeabilidad capilar que
sigue al dao pulmonar agudo, y se ha demostrado que inhibe in vitro la actividad de la xantina oxidasa, una enzima
pivote en la injuria por reperfusin isqumica.
RESUMEN
1) La hipercapnia permisiva en el SDRA, puede potenciar
la oxigenacin tisular, mediante el aumento del gasto cardiaco, adems de facilitar la liberacin tisular de oxgeno al
desviar hacia la derecha la curva de disociacin HbO2.
2) La HPC resulta altamente protectora en modelos experimentales de injuria por reperfusin de pulmones, cerebro
y corazn.
3) La hipercapnia puede alterar la regulacin del ujo sanguneo microvascular y la distribucin del ujo sanguneo entre
Sndrome de distrs respiratorio agudo (SDRA) y ventilacin mecnica (VM)
los rganos, por efectos directos o por estmulos simpticos.
El objetivo tradicional de mantener normales los gases en
sangre arterial durante la VM puede llevar al VILI.
Si bien, existe gran controversia sobre el tema, el uso de HPC
como estrategia de la ventilacin parece ser un avance importante en el tratamiento de los pacientes con SDRA.
El conocimiento adquirido sugiere: reducir el Vt a 5-6 ml /kg
para tolerar la inevitable hipercapnia, adems del uso de
PEEP elevado, que tambin se sumara al efecto protector
del pulmn.
Otras consideraciones: sedacin y decbito prono
En el tratamiento universalmente aplicado a los pacientes
con SDRA en su forma de ventilacin con presin positiva
y de forma invasiva, debemos recordar que la intubacin
requiere sedacin con o sin parlisis muscular. Adems el
decbito supino, asociado a la ausencia de tono de la musculatura respiratoria, conlleva a una reduccin del volumen
intrapulmonar Esto provoca una reduccin del V/Q en zonas
normales, y las zonas con V/Q bajo, llegan al shunt por colapso alveolar.
Putensen y colaboradores 31, compararon pacientes con insuciencia respiratoria ventilados con un nivel de sedacin
continua que abola la respiracin espontnea, con otros a
los que un nivel de sedacin menor que permita mantenerla. Los pacientes que mantenan respiracin espontnea
presentaron mayor PAFI (275 frente a 175 mmHg), y menor shunt, sin modicaciones en la paCO2 ni en el espacio
muerto.
Un aspecto novedoso en la manipulacin de pacientes con
SDRA es el decbito prono, que ha demostrado consistentemente su capacidad para mejorar en una gran proporcin
de pacientes la hipoxemia refractaria. Los mecanismos por
los que mejorara el intercambio gaseoso son complejos y
algunos no claramente demostrados, pero principalmente
se deben a la redistribucin del ujo sanguneo hacia zonas
no colapsadas.
Otros tratamientos en SDRA y adyuvantes de la VM.
Existen otras medidas potenciales de tratamiento en SDRA,
tales como reposicin continua de surfactante, inmunoterapia, inhibidores de la ciclooxigenasa, antagonistas de citoquinas proinamatorias, etc. Pero en todos los casos los
resultados son controvertidos. Solo se ha demostrado que
los corticoesteroides pueden ser de utilidad en la fase broproliferativa, pero no al comienzo del proceso.
De todos los adyuvantes de la VM, la inhalacin de vasodilatadores pulmonares y la posicin de decbito prono son los
ms utilizados en la medicina actual.
Consideraciones nales:
El SDRA se mantiene vigente en la literatura mdica mundial
teniendo en cuenta la morbilidad y mortalidad que se producen por su alta agresividad, lo cual se traduce en mltiples
esfuerzos experimentales y clnicos.
Existen an innumerables criterios contradictorios basados
en los datos obtenidos por cada grupo de trabajo.
Los objetivos de la ventilacin mecnica en el sndrome de
distrs respiratorio agudo incluyen el mantenimiento adecuado del intercambio gaseoso hasta que el edema y la
inamacin disminuyan sin provocar lesiones pulmonares
asociadas con la ventilacin.
La medida de la pO2 con el electrodo de Clark y de la paCO2
con el electrodo de Severinghuaus, junto con las medidas
de pH y bicarbonato resultaron durante aos el mejor diagnstico y la indicacin ms precisa de VM. Esto sigue siendo
considerado en la actualidad. Es por eso la importancia del
laboratorio en el diagnstico y seguimiento de los pacientes con SDRA. Hoy sumamos oximetra, electrolitos, metabolitos como glucemia y lactato junto a un amplio men de
determinaciones.
La Terapia Intensiva y la VM ingresaron a nuestro pas en el ao
1956 cuando el Dr. Aquiles Roncoroni organiz el Centro Respiratorio Mara Ferrer durante la epidemia de poliomielitis.
A partir de 1960 se diversic el tipo de pacientes asistidos
y se incorporaron los respiradores con presin positiva. A nes de la dcada del 60 se describi el SDRA y comenz a
utilizarse la PEEP.
La utilizacin de la VM sigue aumentando, debido al aumento
de la edad de la poblacin y a la incidencia de las patologas.
Bibliografa
01 Ashbaugh DG, Bigelow DB, Petty TL, Levine BE. Acute
respiratory distress in adults. Lancet. 1967;2:319-23
02 Ana D. Lamas vila. Sndrome de dicultad respiratoria
del adulto. Medisan 1998 (Esp);1:5-29
03 West JB. Pulmonary Pathophysiologyy- the essentials
4th ed Willams &Wilkins, Baltimore 1992
04 Dollery C, West J, Wilcken D, Goodwin J, Hugh-Jones P.
Regional pulmonary blood ow in patients with circulatory
shunts. Br Heart J 1961; 23: 225-235.
05 Ware LB, Matthay MA. The acute respiratory distress
syndrome. N Engl J Med. 2000;342:1334-49
06 Gattinioni L, Pelosi P, Suter PM, et al. Acute respiratory
distress syndrome caused by pulmonary and extrapulmonary disease. Am J Respir Crit Care Med 1998; 158:3-11
07 Leonard D. Hudson, MD, FCCP and Kenneth P. Steinberg,
MD, FCCP. Epidemiology of Acute Lung Injury and ARDS
Chest 1999;116:74S-82S
08 Strieter RM, Belperio JA, Keane MP. Cytokines in innate
host defense in the lung. J Clin Invest. 2002;109:699-705.
09 Orfanos SE, Mavrommati I, Korovesi I, Roussos C. Pulmonary endothelium in acute lung injury: from basic science to
the critically ill. Intensive Care Med. 2004;30:1702-14.
10 Bachofen M, Weibel ER. Structural alterations of lung
parenchyma in the adult respiratory distress syndrome.
Clin Chest Med. 1982;3:35-56
11 Pittet JF, Mackersie RC, Martin TR, Matthay MA. Biologi-
REVISTA BIOQUIMICA Y PATOLOGIA CLINICA VOL 72 N 1 2008
Trabajo: pgs 21 | 31
cal markers of acute lung injury: prognostic and pathogenetic
signicance. Am J Respir Crit Care Med. 1997;155:1187-205
12 Abraham E.. Neutrophils and acute lung injury. Crit Care
Med 2003;31:S195-9.
13 Piantadosi CA, Schwartz DA. The acute respiratory distress syndrome. Ann Intern Med. 2004;141:460-70
14 Bernard GR, Artigas A, Brigham KL, Carlet J, Falke K,
Hudson L, et al. The American-European Consensus Conference on ARDS. Denitions, mechanisms, relevant outcomes,
and clinical trial coordination. Am J Respir Crit Care Med.
1994;149: 818-24.
15 Marini JJ: Evolving concepts in the ventilatory management of acute respiratory distress syndrome. Clin Chest
Med 1996 ; 17:555
16 Parker J, Hernndez L, Peevy K. Mechanisms of ventilator-induced lung injury. Crit Care Med. 1993;21:131-43.
17 Chabot F, Mitchell JA, and Gutteridge JM. Reactive oxygen
species in acute lung injury. Eur Respir J 1998; 11: 745-757
18 Webb HH, Tierney DF. Experimental pulmonary edema
due to intermittent positive pressure ventilation with high
ination pressures. Protection by positive end-expiratory
pressure. Am Rev Respir Dis 1974; 110: 556-565
19 Kolobow T, Moretti MP, Fumagalli R, Mascheroni D, Prato
P, Chen V, Joris M. Severe impairment in lung function induced by high peak airway pressure during mechanical
ventilation. An experimental study. Am Rev Respir Dis 1987;
135: 312-315.
20 Muscedere JG, Mullen JB, Gan K, et al. Tidal ventilation
at low lung volumes augments lung injury. Am J Respir Crit
Care Med 1994 ; 1327-34
21 Slutsky AS. Ventilator-induced lung injury: from barotrauma to biotrauma. Respir Care. 2005;50:646-59
22 Deneke SM, Fanburg BL. Normobaric oxigen toxicity of
the lung. N Engl J Med 1980; 303:76-80.
23 Sessler CN. Mechanical ventilation of patients with
Acute Lung Injury. Crit Care Clin. 1998;14:707-29.
24 Slusky S. Arthur. ACCP Consensus Conference. Mechanical Ventilation. Chest 1993 ; 104: 833-59.
25 Hickling K G,Henderson S J, Jackson R. Low mortality associated with low volume pressure limited ventilation with
permissive hypercapnia in severe adult respiratory distress
syndrome. Intensive Care Med 1990:16:372-377.
26 Amato MB, Barbas CS, Medeiros DM, et al. Effect of a protective-ventilation strategy on mortality in the acute respiratory distress syndrome. N Engl J Med 1998; 338: 347-354.
27 Brochard L, Roudot-Thoraval F, Roupie E, et al. Tidal volume reduction for prevention of ventilator induced lung injury in acute respiratory distress syndrome. Am J Respir Crit
Care Med 1998; 158: 1831-1838.
28 Brower RG, Shanholtz CB, Fessler HE, et al. Prospective,
randomized controlled clinical trial comparing traditional versus reduced tidal volume ventilation in acute respiratory distress syndrome patients. Crit Care Med 1999; 27: 1492-1498.
29 Stewart TE, Meade MO, Cook DJ, et al. Evaluation of a
ventilation strategy to prevent barotrauma in patients at
Pg | 31
high risk for acute respiratory distress syndrome: pressure
and volume limited ventilation strategy group. N Engl J Med
1998; 338: 355-361.
30 The Acute Respiratory Distress Syndrome Network. Ventilation with lower tidal volumes as compared with traditional
tidal volumes for acute lung injury and the acute respiratory
distress syndrome. N Engl J Med 2000;342:1301-1308.
31 Putensen C, Zech S, Wrigge H, Zinserling J, Stuber F,
Spiegel TV, et al. Long-term effects of spontaneous breathing during ventilatory support in patients with acute lung
injury. Am J Respir Crit Care Med. 2001;164:43-9
Você também pode gostar
- Ultrasonido pulmonar focalizado: Serie Ultrasonido focalizado en urgencias y cuidado críticoNo EverandUltrasonido pulmonar focalizado: Serie Ultrasonido focalizado en urgencias y cuidado críticoAinda não há avaliações
- Alergias y asma. Diferentes tipos de alergias y cómo combatirlas eficazmenteNo EverandAlergias y asma. Diferentes tipos de alergias y cómo combatirlas eficazmenteAinda não há avaliações
- Mecánica Respiratoria - BiofisicaDocumento18 páginasMecánica Respiratoria - BiofisicaronaldchoquehuancaAinda não há avaliações
- Ventilacion MecanicaDocumento16 páginasVentilacion MecanicaCarlos Alberto Solorzano SuriagaAinda não há avaliações
- Ventilacion Mecanica Basica Final-VfDocumento94 páginasVentilacion Mecanica Basica Final-VfRufo Vera SalinasAinda não há avaliações
- Insuficiencia RespiratoriaDocumento44 páginasInsuficiencia RespiratoriaMary Melo YepezAinda não há avaliações
- Ventilacionmecanica 111212120133 Phpapp01Documento73 páginasVentilacionmecanica 111212120133 Phpapp01Daniel VillaAinda não há avaliações
- Introduccinalaparatorespiratorio Ago 2019Documento16 páginasIntroduccinalaparatorespiratorio Ago 2019MARICARMEN CURAY VALLESAinda não há avaliações
- VENTILACIÓN MECÁNICA - MDDocumento8 páginasVENTILACIÓN MECÁNICA - MDOsnaider Andrés Cuello TorresAinda não há avaliações
- Fisiopatologia Tema 13Documento21 páginasFisiopatologia Tema 13Paula OteroAinda não há avaliações
- PlaceDocumento30 páginasPlaceFarid Aguilar67% (3)
- Ventilo Terapia Tipos de Respiradores - GruposDocumento12 páginasVentilo Terapia Tipos de Respiradores - GruposMaria Alvarez CamargoAinda não há avaliações
- Síntesis ClinicaDocumento8 páginasSíntesis ClinicaMaria Monica FabraAinda não há avaliações
- EPOC Seminario Medicina InternaaDocumento17 páginasEPOC Seminario Medicina InternaaClaudia LeónAinda não há avaliações
- Fisioterapia Respiratoria en Pediatria 2017Documento53 páginasFisioterapia Respiratoria en Pediatria 2017Ezequiel SainzAinda não há avaliações
- Ventilacion Mecanica - 5 Alteraciones de La VentilacionDocumento33 páginasVentilacion Mecanica - 5 Alteraciones de La VentilacionGerlin Lastre CabreraAinda não há avaliações
- FisiopatologiaDocumento9 páginasFisiopatologiaJoseVelezAinda não há avaliações
- Vent Mecanic Princ BasicDocumento40 páginasVent Mecanic Princ BasicMaribel ChugáAinda não há avaliações
- PULMONESDocumento8 páginasPULMONESDomenica CristinaAinda não há avaliações
- Mecanica PulmonarDocumento19 páginasMecanica PulmonarJean Claude C. HernandezAinda não há avaliações
- Ventilacion MecanicaDocumento11 páginasVentilacion MecanicaBARTH2005Ainda não há avaliações
- EspiroallDocumento9 páginasEspiroallAlexander Grimaldi E.Ainda não há avaliações
- Formato Detrabajo Autonomo - Tarea 12Documento10 páginasFormato Detrabajo Autonomo - Tarea 12Paula PiconAinda não há avaliações
- Trabajo de Enfermeria Del Adulto, Marisol AnguloDocumento7 páginasTrabajo de Enfermeria Del Adulto, Marisol AnguloALONDRAAinda não há avaliações
- Principios de FuncionamientoDocumento8 páginasPrincipios de FuncionamientoJosé Andrés Affont GAinda não há avaliações
- Fisiología Respiratoria BásicaDocumento26 páginasFisiología Respiratoria BásicaPeter Amaya-QuiñonesAinda não há avaliações
- Sistema RespiratorioDocumento7 páginasSistema RespiratorioMaria Danitza Salguero FigueroaAinda não há avaliações
- Icf - Semana 11 - 14 - Mayo - 23.Documento53 páginasIcf - Semana 11 - 14 - Mayo - 23.Ronald Alfonso Rivera VanegasAinda não há avaliações
- 4Documento14 páginas4Manuel López TkdAinda não há avaliações
- Ventiladores MecanicosDocumento19 páginasVentiladores MecanicosNeira PertuzAinda não há avaliações
- Fisiopatología Sistema RespiratorioDocumento29 páginasFisiopatología Sistema RespiratorioIsidora DonosoAinda não há avaliações
- Diestres Respiratorio AgudoDocumento11 páginasDiestres Respiratorio Agudojose luis sepulveda ortizAinda não há avaliações
- Resumen de Clinica Respiratorio PatologiasDocumento169 páginasResumen de Clinica Respiratorio Patologiasadryp14Ainda não há avaliações
- Intercambio Gaseoso y Transporte de O2 y CO2Documento9 páginasIntercambio Gaseoso y Transporte de O2 y CO2Patocornio Supremo EspacialAinda não há avaliações
- Semana 12 Biofisica Fisiologia RespiratoriaDocumento21 páginasSemana 12 Biofisica Fisiologia RespiratoriaMaria Jose Barcos MonserrateAinda não há avaliações
- Medicina - Semiologia. SDRADocumento42 páginasMedicina - Semiologia. SDRAfluke_1Ainda não há avaliações
- Insuf. Respiratoria NeonatalDocumento11 páginasInsuf. Respiratoria NeonatalJoshua FaudoaAinda não há avaliações
- Capitulo 1. Fisiología RespiratoriaDocumento24 páginasCapitulo 1. Fisiología Respiratoriaange.mbl96Ainda não há avaliações
- Fiología RespiratoriaDocumento10 páginasFiología RespiratoriaIngrid VarelaAinda não há avaliações
- OXIGENOTERAPIADocumento8 páginasOXIGENOTERAPIAPaola Rodriguez0% (1)
- Fisiología RespiratoriaDocumento20 páginasFisiología RespiratoriaAvril VillalbaAinda não há avaliações
- RespiratorioDocumento11 páginasRespiratorioPaola Garcia SauraAinda não há avaliações
- Clase 1 Respiratorio.Documento28 páginasClase 1 Respiratorio.Saul Flores OcampoAinda não há avaliações
- INTRODUCCIÓNDocumento9 páginasINTRODUCCIÓNAllison Darvin Navarro MelendezAinda não há avaliações
- EspirometriaDocumento29 páginasEspirometrialeonardo marcaAinda não há avaliações
- Fisiologia RespiratoriaDocumento27 páginasFisiologia RespiratoriaLaura MoralesAinda não há avaliações
- Cuestionario - 2Documento15 páginasCuestionario - 2Jhamil LopezAinda não há avaliações
- Clase 9 Fisiologia RespiratoriaDocumento53 páginasClase 9 Fisiologia RespiratoriaMARIAFERNANDA RAFAEL LOPEZAinda não há avaliações
- PDF 20230323 065539 0000 PDFDocumento87 páginasPDF 20230323 065539 0000 PDFErika RivasAinda não há avaliações
- Anatomia y Fisiologia RespiratoriaDocumento46 páginasAnatomia y Fisiologia RespiratoriaAndreina Fatima Herrera BejaranoAinda não há avaliações
- Anatomia Pulmonar, NeumoniaDocumento9 páginasAnatomia Pulmonar, NeumoniaYetzabeth RebolledoAinda não há avaliações
- Guia de Ventilacion Mecanica Urgencia EnfDocumento15 páginasGuia de Ventilacion Mecanica Urgencia EnfConnie FrangipaneAinda não há avaliações
- Antomia y Fisiologia de La VentilacionDocumento36 páginasAntomia y Fisiologia de La VentilacionSaeed DiazAinda não há avaliações
- Esquema General de La Funcion PulmonarDocumento45 páginasEsquema General de La Funcion PulmonarmitosmatyAinda não há avaliações
- Artículo MédicoDocumento4 páginasArtículo MédicovickyAinda não há avaliações
- Esquema General de La Funcion PulmonarDocumento34 páginasEsquema General de La Funcion Pulmonaryessy32lAinda não há avaliações
- TALLER de CARDIO, Ventilacion MecacnicaDocumento8 páginasTALLER de CARDIO, Ventilacion MecacnicaSergio Andres CrespoAinda não há avaliações
- Necesidades de OxigenaciónDocumento27 páginasNecesidades de OxigenaciónNAYELIAinda não há avaliações