Escolar Documentos
Profissional Documentos
Cultura Documentos
Sintesis de Un Halogenuro A Partir de Un Alcohol en El Laboratorio
Enviado por
Sam TorresTítulo original
Direitos autorais
Formatos disponíveis
Compartilhar este documento
Compartilhar ou incorporar documento
Você considera este documento útil?
Este conteúdo é inapropriado?
Denunciar este documentoDireitos autorais:
Formatos disponíveis
Sintesis de Un Halogenuro A Partir de Un Alcohol en El Laboratorio
Enviado por
Sam TorresDireitos autorais:
Formatos disponíveis
SINTESIS DE UN HALOGENURO DE ALQUILO A PARTIR DE UN ALCOHOL PRIMARIO POR MEDIO DE UNA SN2.
Resumen: Las reacciones que ocurren comnmente en qumica orgnica se pueden clasificar entre reacciones de
eliminacin y sustitucin. En este laboratorio se obtendr un halogenuro de alquilo a partir de un alcohol primario como el
n-butanol, teniendo en cuenta que es una reaccin de sustitucin nucleoflica de segundo tipo. Se toma como referencia
de pureza la medida del punto de ebullicin dando como resultado 97C.
Palabras Clave: Punto de Ebullicin, SN2, 1-Bromobutano, laboratorio de orgnica
Abstract: the reactions that commonly happen in organic chemistry can be classified between elimination or substitution
reactions. In this laboratory we obtain an alkyl halide from a primary alcohol like n-butanol, taking into account that it is a
nucleophilic substitution reaction of second type. We take as reference purity the measure of Boiling point, resulting in
79C.
KEY WORDS: Boiling Point, SN2, 1 - Bromobutane, organic laboratory.
INTRODUCCION
En una sustitucin nucleoflica, un nuclefilo
(Nuc:-) reemplaza a un grupo saliente (X -) de un tomo
de carbono, utilizando un par de electrones no
enlazados para formar un nuevo enlace con el tomo de
carbono.
En toda reaccin qumica se establece una relacin
directa entre la velocidad de reaccin y las
concentraciones de los reactivos. Cuando se mide esta
relacin se establece la cintica:
2. Se va con el par de electrones que lo unan al tomo
de carbono electroflico.
Para realizar estas funciones, un buen grupo saliente
debe ser:
1 .Un aceptor de electrones para polarizar al tomo de
carbono,
2 .Estable (no una base fuerte) una vez que ha salido, y
3. Polarizable para estabilizar el estado de transicin.
REACCION SN1:
Velocidad = k * [RX] * [Nu: - ].
REACCION SN2:
1. El nuclefilo usa su par de electrones sin compartir
para atacar al carbono del halogenuro de alquilo, a 180
del halgeno que sale. Esto origina un estado de
transicin con un enlace C Nu: - parcialmente formado
y un enlace C Halgeno semirroto.
El mecanismo SN1 es un proceso de mltiples pasos. El
primer paso es una ionizacin lenta para formar un
carbocatin. La segunda es un ataque rpido sobre el
carbocatin por parte de un nuclefilo. El carbocatin es
un electrfilo fuerte; reacciona muy rpido con los
nuclefilos, incluso con los nuclefilos dbiles.[5]
2. La estereoqumica en el carbono se invierte cuando
se establece por completo el enlace C Nu: - y sale el
ion halogenuro con el par de electrones del enlace C
Halgeno anterior. La velocidad depende de ambos:
Velocidad = k * [RX] * [Nu: - ] (Reaccion de 2 orden). [6]
Imag
en 2: Mecanismo SN1
sta es una reaccin de primer orden. La concentracin
del nuclefilo no aparece en la ecuacin de velocidad:
I
magen 1: Mecanismo SN2
Un grupo saliente tiene dos funciones en la reaccin
Sn2:
1. Polariza el enlace CX, lo que vuelve electroflico al
tomo de carbono.
Velocidad = k * [RX] (Reaccin de 1er. orden).
Muchas reacciones orgnicas son relativamente
complicadas y se llevan a cabo en etapas sucesivas.
Uno de estos pasos suele ser menor que los dems y se
llama paso limitante de velocidad.
1. La disociacin espontnea del halogenuro de alquilo
se efecta en el paso lento, que limita la velocidad, y
genera un carbocatin intermediario (hibridacin sp2,
geometra trigonal plana) y un ion halogenuro.
sustitucin nucleoflica y eliminacin con frecuencia
compiten entre s. [4]
2. El carbocatin intermediario reacciona con el
nuclefilo en un paso rpido y forma el compuesto
protonado.
En un baln de fondo plano se colocaron 6 g de bromuro
de sodio, 5 mL de agua y 6 mL de n-butanol. Se mezcl,
con agitacin magntica y Se realiz un reflujo. Se enfri
el matraz en un bao de hielo-agua y pasados unos
minutos se adicion por la boca del condensador 10 mL
de cido sulfrico concentrado en porciones de 2 mL.
Luego, se coloc el matraz del bao de hielo-agua y se
realiz una trampa de hidrxido de sodio en lentejas y
solucin al 5 % (25 mL). Calentamos con agitacin
constantemente hasta obtener un reflujo moderado. Con
las dos fases, siendo la superior la que contiene el
bromuro de n-butilo luego de 30 minutos Se suspende el
calentamiento, se enfra ligeramente se destila hasta
que el destilado es claro y no contenga gotas aceitosas.
El destilado se pasa a un embudo de separacin y se
lava sucesivamente con: 2,5 mL de agua (el bromuro es
la fase inferior); 2,5 mL de H2SO4 concentrado enfriado
a 5 C (el bromuro es la fase superior) agitando
cuidadosamente; 2,5 mL de agua (el bromuro es la fase
inferior); 2,5 mL de solucin de NaOH al 5 % (el bromuro
es la fase inferior); 2,5 mL de agua (el bromuro es la
fase inferior). Se transfiere el bromuro de n-butilo
hmedo a un erlenmeyer y se seca con sulfato de sodio
anhidro; Se decanta y se destila. Se colecta la fraccin
que destila entre 80-90 C en un recipiente previamente
pesado. Se determina el punto de ebullicin de la
muestra obtenida y se tiene posteriormente como criterio
de pureza.[2]
3. La prdida de un protn del compuesto protonado
intermediario da como resultado el compuesto neutro,
producto final. El paso de la reaccin que registre una
mayor diferencia de energa es el paso limitante [1]
Im
agen 3: Diagramas de energa en la sustitucin
nucleoflica.
En este tipo de reaccin, un ncleofilo, es una especie
con un par de electrones no compartido, reacciona con
un haluro de alquilo (llamado sustrato) sustituyendo al
halgeno. Se lleva a cabo una reaccin de sustitucin, y
el halgeno sustituyente, llamado grupo saliente, se
desprende como ion haluro. Como la reaccin de
sustitucin se inicia por medio de un nuclefilo, se llama
reaccin de sustitucin nuclefilica. [1]
Los haluros de alquilo se convierten fcilmente en
muchos otros grupos funcionales. El tomo del halgeno
puede salir con su par de electrones de enlace para
formar un ion haluro estable; decimos que un haluro es
un buen grupo saliente. Cuando otro tomo reemplaza
al ion haluro, la reaccin es de Sustitucin nucleoflica.
Cuando el ion haluro parte junto con otro tomo o ion
(con frecuencia H+), la reaccin es de eliminacin. En
muchas eliminaciones, se pierde una molcula de HX
del haluro de alquilo para generar un alqueno. Estas
eliminaciones
se
conocen
como
des
hidrohalogenaciones, ya que se elimina un haluro de
hidrgeno del haluro de alquilo. Las reacciones de
PROCEDIMIENTO
RESULTADOS Y ANALISIS.
Luego de realizar todos los pasos propuestos en la
metodologa, se obtuvo una sustancia aceitosa la cual
se considera que es la sustancia que contiene el
halogenuro de alquilo. Obtuvimos muy poca muestra,
con lo que no nos permiti realizar una destilacin del
producto para tener un criterio de pureza fijo, pero an
as se realiz la toma del punto de ebullicin dando
como resultado 97C. Con respecto al valor terico del
punto de ebullicin de este, se encuentra que es el
102C a 1atm. Podemos decir que el producto obtenido
se acerca mucho al valor de sta propiedad fsica.
Aunque es evidente el grado de impurezas que
presenta.
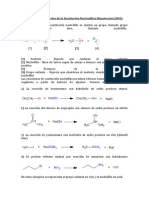
El mecanismo de reaccin que nos describe el proceso
es el siguiente:
Imagen 4: Mecanismo de reaccin.
Por lo anterior este mecanismo es una sustitucin
nucleoflica 2. Al ser un alcohol primario se favorece la
SN2, desplazando fcilmente grupo saliente por el
nuclefilo. El cido proporciona una protonacin en el
oxgeno para el desprendimiento de agua y as
generando la interaccin necesaria para que el ion
bromuro entre a favorecer un nuevo enlace estable
Cabono-Bromo. Como consecuencia los productos
finales son: el bromuro de n-butilo, sulfato de sodio y
agua.
sencillas para halogenuros de alquilo como la prueba de
Beilstein y la de yoduro de sodio en acetona.
COCLUSIONES
[3]Cruz S; Lpez C; Haro C; Barba C. (2012).
Manual de Prcticas de Laboratorio Qumica
Orgnica I. Mxico D.F: Ed Universidad Autnoma
de Metropolitana Unidad Iztapalapa.
Esta sntesis fue una sustitucin nucleoflica de segundo
tipo, debido a que no hay una formacin precisa del
carbocation. Adems, el bromo acta especficamente
para la consolidacin de un estado de transicin en la
que la carga est distribuida entre el nuclefilo que llega
y el grupo del nuclefilo que sale. Mientras mayor sea el
grado de estabilizacin de carga del grupo saliente,
menos energa tendr el estado de transicin y la
reaccin ser ms rpida.[3]. Se debe tener mucho
cuidado con las fases que se generan en el lavado, ya
que seguramente ah es donde se pierde gran cantidad
de muestra. Se propone que adicional del punto de
ebullicin, para consolidar que si fue una formacin
exitosa del producto, se podran realizar pruebas
BIBLIOGRAFA
[1]
Morrison T; Boyd N. (1987). Qiumica
Orgnica. Mxico D.F: Pearson.
[2] Wade L.G. (2011). Qumica Orgnica. Mxido
D.F: Pearson.
[4]Acua A. (2006). Qumica Orgnica. San Jos:
Editorial Universidad Estatal a Distancia.
[5] Beyer H; Wolfgang W. (1987). Manual de
qumica orgnica. Barcelona: Editorial Revert.
[6] Universidad Autnoma de Mxico
(http://depa.fquim.unam.mx/~fercor/RESUME
NSN.pdf)
Você também pode gostar
- Preparacion de Bromulo de ButiloDocumento7 páginasPreparacion de Bromulo de ButiloAngelAinda não há avaliações
- Practica2obtencionden BromobutiloDocumento5 páginasPractica2obtencionden BromobutiloJonatan Estevez JacomeAinda não há avaliações
- Sintesis de NbutiloDocumento6 páginasSintesis de NbutiloJose murciaAinda não há avaliações
- INFORME - IV - ORGANICA - II20191009 111634 1pz9nwb With Cover Page v2Documento7 páginasINFORME - IV - ORGANICA - II20191009 111634 1pz9nwb With Cover Page v2jhoinermauricio martinezmuñozAinda não há avaliações
- Informe Organica Lab 3Documento4 páginasInforme Organica Lab 3MAPSI SASAinda não há avaliações
- Mecanismo de La SN1Documento6 páginasMecanismo de La SN1Jose ArturoAinda não há avaliações
- Reporte 1 Orga 2Documento21 páginasReporte 1 Orga 2Jose Roberto CastañedaAinda não há avaliações
- Informe Organica 2Documento6 páginasInforme Organica 2carmen celenia barrios quirozAinda não há avaliações
- Informe SN2Documento3 páginasInforme SN2lorenaAinda não há avaliações
- 1.) Síntesis de Cloruro de Terc-Butilo Por Reacción SN1Documento8 páginas1.) Síntesis de Cloruro de Terc-Butilo Por Reacción SN1Walter Alvarez OspinoAinda não há avaliações
- Obtención Del Cloruro de TerbutiloDocumento7 páginasObtención Del Cloruro de TerbutiloLaura Fernanda100% (1)
- Practica de Organica 09Documento15 páginasPractica de Organica 09EDITA HUERTAS QUIROZAinda não há avaliações
- Informe SUSTITUCIÓN NUCLEOFÍLICA SN1Documento11 páginasInforme SUSTITUCIÓN NUCLEOFÍLICA SN1Jhon Fuentes GallegoAinda não há avaliações
- Lab Síntesis de Bromuro de N-ButiloDocumento3 páginasLab Síntesis de Bromuro de N-ButiloAndrés JimenezAinda não há avaliações
- SN1 Lab QuímicaDocumento7 páginasSN1 Lab QuímicaDiana Marcela MartinezAinda não há avaliações
- Producción de 1-Bromobutano A Partir Del Alcohol N ButanolDocumento6 páginasProducción de 1-Bromobutano A Partir Del Alcohol N ButanolSebastian Barbosa AvellanedaAinda não há avaliações
- Reacción de Sustituciòn Nucleofìlica UnimolecularDocumento8 páginasReacción de Sustituciòn Nucleofìlica UnimolecularLaura FernandaAinda não há avaliações
- Halogenuros de HidrogenoDocumento38 páginasHalogenuros de HidrogenoJaquelin Solis0% (1)
- Práctica 2 QO2Documento14 páginasPráctica 2 QO2Enrique DelgadoAinda não há avaliações
- Síntesis de Bromuro de N-Butilo Por Reacción Sn2Documento4 páginasSíntesis de Bromuro de N-Butilo Por Reacción Sn2JorgeJiménez0% (1)
- Síntesis de Haluros de AlquiloDocumento8 páginasSíntesis de Haluros de AlquiloDiana PachecoAinda não há avaliações
- Mecanismo Sn2Documento5 páginasMecanismo Sn2GregoriCañasAinda não há avaliações
- 1 Sintesis Bromuro de N ButiloDocumento6 páginas1 Sintesis Bromuro de N ButiloQf Jhon Donado0% (1)
- Haluros de Alquilo - Omarambi - 2013Documento104 páginasHaluros de Alquilo - Omarambi - 2013Oscar G. MarambioAinda não há avaliações
- Reacciones QuímicasDocumento6 páginasReacciones QuímicasJavier GarciaAinda não há avaliações
- Sintesis de Cloruro de Terbutil InformeDocumento6 páginasSintesis de Cloruro de Terbutil InformeMaria Jose Fabregas AnguloAinda não há avaliações
- Preguntas Informe Org2Documento10 páginasPreguntas Informe Org2Ela PachecoAinda não há avaliações
- Informe Sistesis Del 2-Cloro-2-Metilpropano - Luis Guerrero - CorregidoDocumento6 páginasInforme Sistesis Del 2-Cloro-2-Metilpropano - Luis Guerrero - CorregidoLUIS ANDRES GUERRERO CARDONAAinda não há avaliações
- Sintesis de CloruroDocumento4 páginasSintesis de CloruroKelly ArrietaAinda não há avaliações
- Síntesis de Ciclo Hexeno A Partir de Ciclohexanol .Documento5 páginasSíntesis de Ciclo Hexeno A Partir de Ciclohexanol .WILLIAM NICOLAS BACCA NOVOAAinda não há avaliações
- Informe 1 Grupo C3 Haluros Orgánicos Video LqoiiDocumento10 páginasInforme 1 Grupo C3 Haluros Orgánicos Video LqoiiAnais Lucero Zambrano PortillaAinda não há avaliações
- Sintesis de Bromuro SN2Documento6 páginasSintesis de Bromuro SN2SHIRLEY PAOLA BARRERA BARRIOSAinda não há avaliações
- Informe Obtencion de Bromuro de N-ButiloDocumento6 páginasInforme Obtencion de Bromuro de N-ButiloEmiliano LopezAinda não há avaliações
- Informe de Práctica N 9 Química OrgánicaDocumento11 páginasInforme de Práctica N 9 Química OrgánicaPercy Paucar100% (1)
- Reacción de Sustitución NucleofílicaDocumento7 páginasReacción de Sustitución NucleofílicaluciaortegaAinda não há avaliações
- Aldehídos y Cetonas 2022Documento18 páginasAldehídos y Cetonas 2022eliana vegaAinda não há avaliações
- Rporte 10 OrganicaDocumento11 páginasRporte 10 OrganicaLizette AngelAinda não há avaliações
- Práctica 3. OBTENCIÓN DEL BROMURO DE n-BUTILODocumento6 páginasPráctica 3. OBTENCIÓN DEL BROMURO DE n-BUTILOLeidy Laura HRAinda não há avaliações
- Preparacion Del 2 Cloro 2 Metilpropano VDocumento6 páginasPreparacion Del 2 Cloro 2 Metilpropano VandresAinda não há avaliações
- Reacciones Sn1 Y Sn2Documento19 páginasReacciones Sn1 Y Sn2Héctor Jafet Candelario DíazAinda não há avaliações
- INFORME 1 - Síntesis de Bromuro de N-ButiloDocumento5 páginasINFORME 1 - Síntesis de Bromuro de N-ButiloALEXANDRA CABALLERO TURIZOAinda não há avaliações
- Mecanismo SN1Documento5 páginasMecanismo SN1Johanna GalanAinda não há avaliações
- Sustitución Nucleofílica Reacción SN2 y Reacción SN1Documento23 páginasSustitución Nucleofílica Reacción SN2 y Reacción SN1Alfonso Dominguez GonzalezAinda não há avaliações
- Practica Numero 9 OBTENCION DE N-BUTILO.Documento6 páginasPractica Numero 9 OBTENCION DE N-BUTILO.Fco YañezAinda não há avaliações
- Practica 2. Obtencion de Bromuro de N-ButiloDocumento4 páginasPractica 2. Obtencion de Bromuro de N-ButiloKai100% (1)
- Síntesis de Bromuro de T-Butilo Por Reacción SN1 PDFDocumento7 páginasSíntesis de Bromuro de T-Butilo Por Reacción SN1 PDFJairo Cuervo GámezAinda não há avaliações
- 8-Sustitucion Nucleofilica 1 (SN1) .Documento11 páginas8-Sustitucion Nucleofilica 1 (SN1) .fernandoluisAinda não há avaliações
- OBTENCIÓN DE BROMURO DE n-BUTILODocumento5 páginasOBTENCIÓN DE BROMURO DE n-BUTILOPau FlurscheimAinda não há avaliações
- Lab #2 Terc-ButiloDocumento6 páginasLab #2 Terc-ButiloEliana picoAinda não há avaliações
- Reacciones de Sustitucion en H. SaturadosDocumento7 páginasReacciones de Sustitucion en H. SaturadosFrank RodgersAinda não há avaliações
- 14 Haluros de Alquilo IQ-2Documento63 páginas14 Haluros de Alquilo IQ-2Karly ContrerasAinda não há avaliações
- Documento Sin TítuloDocumento8 páginasDocumento Sin TítuloCristian PatiñoAinda não há avaliações
- Practica 2 Objetivos Marco Teorico y ConclusionesDocumento4 páginasPractica 2 Objetivos Marco Teorico y ConclusioneserizoAinda não há avaliações
- Lab 6Documento17 páginasLab 6Ayrton Jimenez InfantesAinda não há avaliações
- 1.sintesis Bromuro de N-ButiloDocumento6 páginas1.sintesis Bromuro de N-Butilojuancho95400Ainda não há avaliações
- INFORME 1 - Síntesis de Bromuro de N-ButiloDocumento4 páginasINFORME 1 - Síntesis de Bromuro de N-ButiloALEXANDRA CABALLERO TURIZOAinda não há avaliações
- Laboratorio de Química Orgánica Sutitucion NucleofílicaDocumento14 páginasLaboratorio de Química Orgánica Sutitucion NucleofílicaMaría MartínezAinda não há avaliações
- Guion p1Documento4 páginasGuion p1Sam TorresAinda não há avaliações
- Fullerenos y GrafenosDocumento15 páginasFullerenos y GrafenosSam TorresAinda não há avaliações
- CompetenciasDocumento8 páginasCompetenciasSam TorresAinda não há avaliações
- FULLERENOS Y GRAFENOS UltimoDocumento15 páginasFULLERENOS Y GRAFENOS UltimoSam TorresAinda não há avaliações
- Obtención de La Acetoacetato de BencilaminaDocumento6 páginasObtención de La Acetoacetato de BencilaminaSam TorresAinda não há avaliações
- Telomeros y TelomerasaDocumento5 páginasTelomeros y TelomerasaSam TorresAinda não há avaliações
- Practica Social Trabajo ViolenciaDocumento18 páginasPractica Social Trabajo ViolenciaSam TorresAinda não há avaliações
- Taller Nanotecnologia TerminadoDocumento6 páginasTaller Nanotecnologia TerminadoSam TorresAinda não há avaliações
- Violencia-Intrafamiliar y ResilienciaDocumento7 páginasViolencia-Intrafamiliar y ResilienciaSam TorresAinda não há avaliações
- Cuestionario Cromatografia 13 - 16Documento5 páginasCuestionario Cromatografia 13 - 16Sam TorresAinda não há avaliações
- Obtención de Acetato de Isobutilo Mediante La Síntesis de FischerDocumento4 páginasObtención de Acetato de Isobutilo Mediante La Síntesis de FischerSam TorresAinda não há avaliações
- Sintesis Educacion, Su Naturaleza y Su FuncionDocumento3 páginasSintesis Educacion, Su Naturaleza y Su FuncionSam TorresAinda não há avaliações
- Sintesis Educacion, Su Naturaleza y Su FuncionDocumento3 páginasSintesis Educacion, Su Naturaleza y Su FuncionSam TorresAinda não há avaliações
- SN1 SN2Documento19 páginasSN1 SN2Federico Matias Fernandez0% (1)
- Sintesis de Cloruro de TerbutiloDocumento8 páginasSintesis de Cloruro de TerbutiloclaudiaAinda não há avaliações
- Alcanos, Alquenos y AlquinosDocumento7 páginasAlcanos, Alquenos y AlquinosLuis carlos Renteria menaAinda não há avaliações
- Comparacion Sn1 y Sn2Documento2 páginasComparacion Sn1 y Sn2Mary helen Molina siancas100% (1)
- Informe Síntesis de Cloruro de Terc Butilo Por Reaccion SN1Documento6 páginasInforme Síntesis de Cloruro de Terc Butilo Por Reaccion SN1Juanita BeltranAinda não há avaliações
- Reacciones Analíticas de Haluros Orgánicos-Análisis Funcional OrgánicoDocumento17 páginasReacciones Analíticas de Haluros Orgánicos-Análisis Funcional Orgánicoraul taya perezAinda não há avaliações
- Clase 5 Haluros y SN1 SN2Documento23 páginasClase 5 Haluros y SN1 SN2RACHELL SANTIBÁÑEZ NÚÑEZAinda não há avaliações
- 09 - 10 y 11 Clase TEQO 2021Documento9 páginas09 - 10 y 11 Clase TEQO 2021Torrez HamiltonAinda não há avaliações
- Informe Síntesis de Cloruro de TerbutiloDocumento5 páginasInforme Síntesis de Cloruro de TerbutiloAnaAinda não há avaliações
- Reporte y Examen Práctica 2Documento7 páginasReporte y Examen Práctica 2Fanny MartínezAinda não há avaliações
- Informe de Organica Felix VelizDocumento13 páginasInforme de Organica Felix VelizYeni PaucarAinda não há avaliações
- Practica 2. Obtencion de Bromuro de N-ButiloDocumento4 páginasPractica 2. Obtencion de Bromuro de N-ButiloKai100% (1)
- Química Orgánica Diapositivas de ReaccionesDocumento21 páginasQuímica Orgánica Diapositivas de ReaccionesXiomara PerezAinda não há avaliações
- 12 Mecanismos de ReacciónDocumento107 páginas12 Mecanismos de ReacciónEmanuel Chacon rodriguezAinda não há avaliações
- Lab #2 Terc-ButiloDocumento6 páginasLab #2 Terc-ButiloEliana picoAinda não há avaliações
- Manual Organica 2Documento86 páginasManual Organica 2FelipeMarinAinda não há avaliações
- Capítulo 6-Haluros de AlquiloDocumento24 páginasCapítulo 6-Haluros de AlquiloOscarAinda não há avaliações
- Sustitución Nucleofílica - Sn1: Msc. Max J. Carlos SDocumento21 páginasSustitución Nucleofílica - Sn1: Msc. Max J. Carlos SBERNI ABEL CONDORI FLORESAinda não há avaliações
- HaloalcanosDocumento15 páginasHaloalcanosFranco BorgatelloAinda não há avaliações
- Química Orgánica 2Documento96 páginasQuímica Orgánica 2Mirthza Aguilar YeAinda não há avaliações
- PREVIO NUMERO 9 OBTENCIÓN DE BROMURO DE n-BUTILODocumento9 páginasPREVIO NUMERO 9 OBTENCIÓN DE BROMURO DE n-BUTILOJose Antonio Martinez MorenoAinda não há avaliações
- Quimica Cap 10Documento65 páginasQuimica Cap 10Mark CastilloAinda não há avaliações
- Experimentos Basicos Organica 2 PDFDocumento94 páginasExperimentos Basicos Organica 2 PDFDiegAinda não há avaliações
- Grupos Funcionales Chapter 1Documento63 páginasGrupos Funcionales Chapter 1Meliza AlvarezAinda não há avaliações
- Sintesis de Cloruro de TerbutiloDocumento4 páginasSintesis de Cloruro de TerbutiloRobinho Sullca Cerron100% (3)
- Mecanismos SN1, SN2, E1 y E2Documento36 páginasMecanismos SN1, SN2, E1 y E2FannyLuna88% (17)
- Sustitución NucleofílicaDocumento27 páginasSustitución NucleofílicaAlfredo Benjamin Fuentes OrtizAinda não há avaliações
- Inf. 8 y 9 Haluros de Alquilo y MentonaDocumento15 páginasInf. 8 y 9 Haluros de Alquilo y MentonaNoe RechnitzerAinda não há avaliações
- Síntesis de Bromuro de T-Butilo Por Reacción SN1Documento8 páginasSíntesis de Bromuro de T-Butilo Por Reacción SN1Kiara GomezAinda não há avaliações
- Reactividad de Grupos Funcionales Alcoholes y AminasDocumento6 páginasReactividad de Grupos Funcionales Alcoholes y AminasMakhiiss VegaAinda não há avaliações