Escolar Documentos
Profissional Documentos
Cultura Documentos
Phenomenes de Corrosion4
Enviado por
KharbiMohamedDireitos autorais
Formatos disponíveis
Compartilhar este documento
Compartilhar ou incorporar documento
Você considera este documento útil?
Este conteúdo é inapropriado?
Denunciar este documentoDireitos autorais:
Formatos disponíveis
Phenomenes de Corrosion4
Enviado por
KharbiMohamedDireitos autorais:
Formatos disponíveis
PHNOMNES DE CORROSION
I. Nature de la corrosion
I.1. Dfinition
La corrosion d'un mtal est l'oxydation de cet lment l'tat d'ion mtallique : il s'agit donc d'une raction
d'oxydo - rduction. Si le mtal M est oxyd l'tat de cation Mn+, il se produit donc : M = M n+ + ne
Cette raction lectrochimique exige la prsence d'un oxydant Ox susceptible de capter les lectrons, soit :
Ox + n e = Red nLa raction de corrosion du mtal se traduit donc par le bilan : M + Ox M n+ + Red nRemarque : l'oxydation d'un mtal peut avoir lieu dans une atmosphre sche par exemple avec O2 ou Cl2
(corrosion sche) ou en prsence d'humidit (corrosion humide).
I.2. Facteurs de la corrosion humide
On peut les classer en deux catgories :
- les facteurs extrieurs :
- air oxydant (O2, CO2)
- vapeur d'eau atmosphrique (H2O)
- pluie (H2O, H+)
- contact eau de mer (H2O, sels divers NaCl)
- les facteurs lis au matriau :
- htrognit de surface (dfauts, rayures)
- htrognit de composition (impurets, alliage, contact avec un autre mtal, soudure)
- htrognit de temprature
- htrognit de concentration du milieu son contact (dilution diffrentielle, aration diffrentielle)
I.3. Corrosion uniforme ou diffrentielle
1/ Corrosion uniforme
Cela suppose que le mtal ait une surface parfaitement homogne et que le mlange ractionnel son contact
soit lui aussi parfaitement homogne. Il y a corrosion uniforme si toute la surface du mtal est attaque de la
mme faon et s'il n'y a pas de circulation d'lectrons au sein du mtal. C'est cas par exemple d'une tige de fer
pur totalement immerge dans l'eau acidule et parfaitement agite. Il y a transfert direct du rducteur Fe
l'oxydant H+ : Fe(s) + 2 H +(aq) Fe2+(aq) + H2(g)
La corrosion est dite chimique.
2/ Corrosion diffrentielle
Cela suppose une htrognit quelconque. Il y a corrosion diffrentielle lorsque l'attaque s'exerce de faon
diffrente en deux zones de la surface du mtal. Il y a ncessairement circulation d'lectrons au sein du mtal
pour relier ces deux zones. Cette corrosion est dite aussi lectrochimique pour traduire la participation des
lectrons de conduction du mtal.
Exemples : - cas d'une canalisation en cuivre amenant l'eau au contact d'un radiateur en fer : le fer rouille au
niveau de la jonction.
- cas d'une canalisation en fer enterre dans deux sols de nature diffrente (argileux faible
teneur en O2 et sablonneux forte teneur en O2) : le fer rouille dans la zone argileuse.
II. Etude thermodynamique : E - pH de corrosion
II.1. Trac des diagrammes E-pH
L'tude thermodynamique de la corrosion humide seffectue avec les diagrammes E-pH, tracs avec :
- les concentrations des espces solubles tant prises gales 10-6 mol.L-1(concentration faible pour traduire
l'apparition de corrosion)
- les phases condenses (hydroxydes, oxydes) envisages tant les plus stables et assurent une protection du
mtal contre l'agression de la solution aqueuse
II.2. Les trois domaines du diagramme
On peut mettre en vidence trois domaines :
- domaine de la corrosion : c'est la rgion E-pH o le mtal se
trouve sous forme ionique ( la concentration de 10-6 mol.L-1). Il
y a eu oxydation du mtal et donc corrosion pour donner une
espce soluble.
- domaine d'immunit : c'est le domaine de stabilit
thermodynamique du mtal. La corrosion tant impossible
thermodynamiquement ne peut donc pas se produire (la cintique
n'intervient pas dans ce cas).
- domaine de passivit : c'est le domaine o se trouvent les
diffrentes phases condenses (en gnral des oxydes et des
hydroxydes) qui recouvrent le mtal et le protgent d'une attaque
ultrieure. Le mtal a donc t oxyd en surface, mais cette
pellicule le protge d'une attaque en profondeur. On voit l tout
l'intrt d'une couche protectrice trs stable, compacte et
fortement lie au mtal.
II.3. Diagramme E-pH du fer
On retrouve les trois domaines (voir le diagramme ci-contre):
- corrosion : elle a lieu surtout en milieu acide ou neutre, le fer tant oxyd en Fe2+ ou Fe3+
- immunit : domaine de stabilit du mtal pour des potentiels ngatifs
- passivation : elle rsulte de la formation d'une couche d'oxyde ferrique protectrice pour des pH neutre ou
basique.
III. Etude cintique
La corrosion si elle est thermodynamiquement possible est conditionne par une cintique favorable. Cette
cintique est apprhende grce aux courbes intensit - potentiel.
III.1. Piles avec lectrodes diffrentes
1/ Aspect exprimental
Trs souvent dans l'industrie, des pices mtalliques sont constitues de
mtaux diffrents lis entre eux : il suffit que ces mtaux soient en contact
avec de l'eau pour raliser une pile. On considre deux lectrodes courtcircuites, l'une de fer et l'autre de cuivre, qui plongent dans une solution
aqueuse pralablement dsare de NaCl 1 mol.L-1 environ (milieu
simulant l'eau de mer). On ajoute quelques gouttes d'orthophnantroline.
E(Cu2+/Cu) = 0,34 V
E(Fe2+/Fe) = - 0,44 V
Au bout de quelques minutes, on constate un rosissement de la solution
traduisant la prsence d'ions Fe2+ qui donne avec l'orthophnantroline un
complexe rose. A l'anode, il y a eu oxydation (corrosion) du fer :
Fe = Fe2+ + 2e
A la cathode de cuivre, il y a eu rduction :
2 H2O(l) + 2 e = H2(g) + 2HO (aq)
D'autre part, grce la phnolphtaline, on peut montrer que la solution devient
basique au voisinage du cuivre. Le bilan est donc :
Fe(s) + 2 H2O(l) = Fe2+(aq) + H2(g) + 2 HO (aq)
Des deux mtaux en contact, c'est le plus lectropositif, donc le plus rducteur,qui est oxyd : seuls Fe2+ et
Cu(s) peuvent coexister (domaine commun). Lorsque deux mtaux constituent une pile de corrosion, c'est le
plus lectropositif (celui qui a le plus petit E) qui se corrode. On a ainsi mis en vidence une mthode pour
protger un mtal de la corrosion : le relier un autre mtal plus lectropositif que lui.
2/ Aspect cintique : potentiel mixte
Les courbes intensit-potentiel sur chaque lectrode sont donnes ci-contre :
Les deux lectrodes tant en contact ont le mme potentiel E. par ailleurs, le courant d'oxydation (1)
est gal au courant de rduction (2) en valeur absolue. Il en rsulte que le point M de fonctionnement est tel
que : iox=-ired
Le potentiel M est appel potentiel mixte : c'est le potentiel commun des deux mtaux en contact. On l'appelle
galement potentiel de corrosion.
III.2. Vitesse de corrosion
1/ Loi de Tafel
On peut montrer thoriquement (quations de Butler-Volmer) que l'intensit i varie exponentiellement avec le
potentiel E : i = Ae B. E i = AeBE A et B constantes.
On peut aussi crire le rsultat connu sous le nom de loi de Tafel : E = a + b log i
Le choix de la valeur absolue de i permet d'tudier de mme la rduction cathodique (pour laquelle i <0)
2/ Diagramme d'Evans
Un mtal M est corrod si sa courbe d'oxydation anodique i = f(E) admet
des valeurs de E communes avec une courbe de rduction sur un autre
mtal, soit existence d'un potentiel mixte. On utilise alors la reprsentation
des courbes i =f(E) en prenant les coordonnes semi logarithmiques,
log iet E lies la loi de Tafel. On obtient alors le diagramme
d'Evans.
Les deux droites se coupent en un point M dont les coordonnes sont :
- Em potentiel mixte ou potentiel de corrosion
- log |icor| qui permet d'atteindre le courant de corrosion icor et donc la
vitesse de corrosion
III.3. Piles avec lectrodes identiques
1/ Pile de concentration
On considre la pile dans laquelle deux lectrodes identiques
(fer) plongent dans deux solutions diffrentes de Fe2+, l'une
concentre droite, et l'autre dilue gauche. Ce systme ne
peut pas tre en quilibre car les concentrations ne sont pas les
mmes :
Le retour l'quilibre va entraner l'galit des potentiels, donc
des concentrations, ce qui suppose :
- dans (2), une rduction cathodique : Fe2+(aq) + 2 e = Fe(s)
- dans (1), une oxydation anodique : Fe(s) = Fe2+(aq) + 2 e
Il y a donc corrosion dans la solution la plus dilue.
2/ Pile d'Evans : aration diffrentielle
La solution de gauche (1) a t porte bullition pour chasser
l'air alors que l'on fait barboter de l'air dans la solution de droite
(2). Grce l'orthophnantroline, on met en vidence la
formation d'ions Fe2+(aq) dans le compartiment de
gauche suivant la raction : Fe(s) = Fe2+(aq) + 2 e .
Dans le compartiment de droite, le dioxygne est donc rduit au
contact du fer : O2(g) + 2 H2O + 4e = 4 HO(aq)
L'quation - bilan s'crit donc :
2 Fe(s) + O2(g) + 2 H2O = 2 Fe2+(aq) + 4 HO(aq)
On constate que c'est dans la zone la moins oxygne que le fer se
corrode. Ce phnomne est trs gnral et correspond une aration
diffrentielle (la concentration en O2 est diffrente d'une rgion
l'autre). Dans l'autre zone, le dioxygne est consomm ce qui tend
diminuer le diffrentiel d'aration. Ainsi, si une pice en fer prsente
une fissure, c'est dans la partie la plus profonde de la fissure, donc la
moins are, que se produit la corrosion : celle-ci se poursuit en
profondeur pouvant entraner la perforation s'il s'agit d'une plaque.
IV. Mthodes de protection du fer
IV.1. Protection physique
On peut isoler le fer du milieu corrosif en le recouvrant d'une pellicule de peinture.
Exemples : peintures anti-rouille base de minium Pb3O4(s). De mme, on peut dposer sur le fer un
revtement plastique permettant de raliser des cltures (grillage plastifi).
IV.2. Protection chimique
La couche protectrice peut tre cre par une raction chimique : la pice de fer est plonge dans un bain
chaud de phosphate de zinc provoquant la formation d'une couche de phosphate de fer impermable
(parkrisation dans l'industrie automobile).
IV.3. Protection mtallique en surface
On peut protger le fer par une couche protectrice de zinc
(lui-mme passiv). En cas d'raflure du mtal protecteur,
le fer est mis en contact avec le milieu corrosif : on
ralise alors une pile de corrosion dans laquelle c'est le
mtal le plus lectropositif qui s'oxyde, c'est--dire le
zinc. Cet accident n'entrane donc pas la corrosion du fer.
Exemples : galvanisation ou lectrozingage
IV.4. Protection lectrochimique
Le fer est reli lectriquement du zinc par exemple (ou un autre
mtal plus lectropositif que lui comme Mg ou Al). On a ainsi
ralis une pile de corrosion dans laquelle :
- le fer est la cathode, sige d'une raction de rduction :
2 H2O(l) + 2 e = H2(g) + 2 HO(aq)
- le zinc est l'anode, sige d'une raction d'oxydation :
Zn(s) = Zn2+(aq) + 2 e
On constate qu'il y a consommation de l'anode en zinc : on parle d'anode sacrificielle.
La vitesse de corrosion du zinc peut tre dtermine grce au diagramme d'Evans.
Bien entendu, la protection du fer cesse lorsque l'anode en zinc est entirement consomme.
Applications : coques des navires, pipelines, cuves en acier enterres ou immerges.
Você também pode gostar
- Coloration GramDocumento6 páginasColoration GramFatmazohra RAHILAinda não há avaliações
- Chapitre - 1 PH201Documento15 páginasChapitre - 1 PH201FanxyvAinda não há avaliações
- AVENTURE DE L'ELECTRICITE - C'est Pas Sorcier Spécial Enseignant - Yoshi37Documento2 páginasAVENTURE DE L'ELECTRICITE - C'est Pas Sorcier Spécial Enseignant - Yoshi37BarbaraAinda não há avaliações
- Ecoconso - Que Signifient Les Nouveaux Pictogrammes de Danger - 2023-02-01Documento4 páginasEcoconso - Que Signifient Les Nouveaux Pictogrammes de Danger - 2023-02-01Dieudonné NofodjiAinda não há avaliações
- TD ExternesDocumento24 páginasTD ExternesDoria OuahraniAinda não há avaliações
- Get File PDFDocumento28 páginasGet File PDFHichemAinda não há avaliações
- Comprendre La SchizophrénieDocumento25 páginasComprendre La SchizophrénieMontada DjazaironaAinda não há avaliações
- Diabete Gestationnel SynthDocumento12 páginasDiabete Gestationnel SynthDumas Tchibozo100% (1)
- Les Biomarqueurs de L'infarctus Du Myocarde: ChapitreDocumento8 páginasLes Biomarqueurs de L'infarctus Du Myocarde: ChapitreTarek SayhiAinda não há avaliações
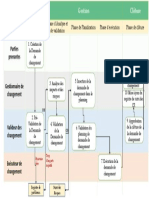
- 25 - Workflow Demande de ModificationDocumento1 página25 - Workflow Demande de ModificationSerge VolpiAinda não há avaliações
- Protocole Reherche 15 Sept 2023Documento78 páginasProtocole Reherche 15 Sept 2023Ali AIT-MOHANDAinda não há avaliações
- Programme AidesoignantfinalDocumento63 páginasProgramme AidesoignantfinalAbdelghni LachhabAinda não há avaliações
- B 800 Cbe 59Documento2 páginasB 800 Cbe 59mahdi elmayAinda não há avaliações
- Dosage de La Vitamine CDocumento10 páginasDosage de La Vitamine CalexisbradAinda não há avaliações
- TD BetonDocumento10 páginasTD BetonAggoun YounesAinda não há avaliações
- SN5 Corrige3 VFDocumento23 páginasSN5 Corrige3 VFSimrat KaurAinda não há avaliações
- Abord Premier de L'artère Mésentérique Supérieure Au Cours de La Duodénopancréatectomie CéphaliqueDocumento3 páginasAbord Premier de L'artère Mésentérique Supérieure Au Cours de La Duodénopancréatectomie CéphaliquefdroooAinda não há avaliações
- Mesures Anthropométriques Pour L'évaluation de L'état Nutritionnel D'un Individu & La Situation Dans Une CommunautéDocumento67 páginasMesures Anthropométriques Pour L'évaluation de L'état Nutritionnel D'un Individu & La Situation Dans Une CommunautéIbrahim HamadouAinda não há avaliações
- 2015 04 17 - Business Plan 2015 2017 - FRDocumento88 páginas2015 04 17 - Business Plan 2015 2017 - FRfohi2009Ainda não há avaliações
- FIT Manioc 2014Documento2 páginasFIT Manioc 2014Williams Koffi100% (1)
- Cours 21-26 (Unite 6 +7)Documento54 páginasCours 21-26 (Unite 6 +7)Maria SimotaAinda não há avaliações
- Graniscel S55Documento2 páginasGraniscel S55Aîda hajriAinda não há avaliações
- Vedette Matiére RAMEAU CORRIGEDocumento5 páginasVedette Matiére RAMEAU CORRIGEBob Cavallo HBAinda não há avaliações
- CND SRDocumento2 páginasCND SRFethi BELOUISAinda não há avaliações
- Brochure Charte Audit Interne 2015def22x23def16pages Corrig2e 1Documento16 páginasBrochure Charte Audit Interne 2015def22x23def16pages Corrig2e 1ʚïɞ Fi Fi ʚïɞAinda não há avaliações
- TP Projet D'arch 2è CibDocumento12 páginasTP Projet D'arch 2è CibAMALI BlaiseAinda não há avaliações
- Colchicine Dans La Goutte Usage Et MésusageDocumento6 páginasColchicine Dans La Goutte Usage Et MésusageAmine DounaneAinda não há avaliações
- MemoireDocumento120 páginasMemoireabdelndam904Ainda não há avaliações
- Tchekhov Les Trois SoeursDocumento28 páginasTchekhov Les Trois SoeursCristina MiaAinda não há avaliações
- 01-03 - Dec10 - Philippe Dozoul - AFNOR - FDX50-252 - Francais PDFDocumento24 páginas01-03 - Dec10 - Philippe Dozoul - AFNOR - FDX50-252 - Francais PDFNassima Bendjeddou100% (1)