Escolar Documentos
Profissional Documentos
Cultura Documentos
Preparação e Identificação de Vidrarias de Laboratório
Enviado por
Denison VictorTítulo original
Direitos autorais
Formatos disponíveis
Compartilhar este documento
Compartilhar ou incorporar documento
Você considera este documento útil?
Este conteúdo é inapropriado?
Denunciar este documentoDireitos autorais:
Formatos disponíveis
Preparação e Identificação de Vidrarias de Laboratório
Enviado por
Denison VictorDireitos autorais:
Formatos disponíveis
UNIVERSIDADE FEDERAL RURAL DO RIO DE JANEIRO
INSTITUTO DE BIOLOGIA
DEPARTAMENTO DE CINCIAS FISIOLGICAS
DISCIPLINA: IB 302 Biofsica
PROFESSORES: Jairo Pinheiro, Michelle Marassi e Norma Almeida.
ROTEIRO DE AULA PRTICA
ASSUNTO: Vidrarias
A rotina de um profissional da rea Biomdica requer a preparao de solues de
caractersticas e usos variados, indo desde a preparao de solues de lcool e formol para
preservao de espcimes at a preparao de medicamentos injetveis. Por esta razo
necessrio conhecer os diferentes tipos de vidrarias para preparar as mais variadas solues,
assim como os procedimentos envolvidos na sua preparao.
MATERIAL: pipeta graduada pipeta volumtrica micropipeta ponteiras para
micropipetas tubos de ensaio tubo de ensaio com tampa de rosca pegador de
tubos tubos de centrfuga tubos Eppendorf pissete balo volumtrico
basto de vidro funil de vidro proveta bquer graduado bquer sem
graduao erlenmeyer graduado erlenmeyer sem graduao esptula - placa de
Petri vidro de relgio.
PROCEDIMENTO:
Identificar corretamente todas as vidrarias e materiais apresentados durante a aula.
Saber a funo de cada vidraria e material de laboratrio.
Comparar a preciso das diferentes vidrarias.
UNIVERSIDADE FEDERAL RURAL DO RIO DE JANEIRO
INSTITUTO DE BIOLOGIA
DEPARTAMENTO DE CINCIAS FISIOLGICAS
DISCIPLINA: IB 302 Biofsica
PROFESSORES: Jairo Pinheiro, Michelle Marassi e Norma Almeida.
ROTEIRO DE AULA PRTICA
ASSUNTO: Preparao de solues I
FUNDAMENTO TERICO
Definio: Misturas homogneas de 2 ou mais substncias puras onde o componente em
maior quantidade o solvente e o que est em menor quantidade o soluto.
Recordando alguns conceitos:
Mol ou molcula grama = PM em gramas.
Nmero de moles (ou de molculas) = massa da substncia (g)/Mol
Expresses da concentrao das solues:
Porcentagem em peso (%p/p) gramas de soluto em 100g de soluo.
Porcentagem em volume (%v/v) mililitros de soluto em 100ml de soluo.
Porcentagem em peso por volume (%p/v) gramas de soluto em 100ml de soluo.
Molaridade nmero de moles de soluto em 1 litro de soluo.
M = massa/Mol
1litro
M = massa/PM(g)
1litro
M = massa/ PM(g)
V(l)
M = massa
PM(g) x V(l)
PROCEDIMENTO PRTICO
Material necessrio: gua destilada, NaCl, sacarose, balana analtica, vidro de relgio,
esptulas, 2 bqueres de 250ml, 2 bales volumtricos de 100ml, 1 balo volumtrico de
250ml, 1 proveta de 250ml, 1 basto de vidro, 1 pipeta graduada de 10ml.
Procedimento:
1. Preparar 100ml de uma soluo 6% de NaCl (PM=58,5).
2. A partir da soluo acima, preparar 100ml de uma soluo 0,6% de NaCl.
3. Preparar 250ml de uma soluo 0,3% de sacarose (PM=342).
UNIVERSIDADE FEDERAL RURAL DO RIO DE JANEIRO
INSTITUTO DE BIOLOGIA
DEPARTAMENTO DE CINCIAS FISIOLGICAS
DISCIPLINA: IB 302 Biofsica
PROFESSORES: Jairo Pinheiro, Michelle Marassi e Norma Almeida.
ROTEIRO DE AULA PRTICA
ASSUNTO: Preparao de solues II
FUNDAMENTO TERICO
Definio: Misturas homogneas de 2 ou mais substncias puras onde o componente em
maior quantidade o solvente e o que est em menor quantidade o soluto.
Recordando alguns conceitos:
Mol ou molcula grama = PM em gramas.
Nmero de moles (ou de molculas) = massa da substncia (g)/Mol
Expresses da concentrao das solues:
Porcentagem em peso (%p/p) gramas de soluto em 100g de soluo.
Porcentagem em volume (%v/v) mililitros de soluto em 100ml de soluo.
Porcentagem em peso por volume (%p/v) gramas de soluto em 100ml de soluo.
Molaridade nmero de moles de soluto em 1 litro de soluo.
M = massa/Mol
1litro
M = massa/PM(g)
1litro
M = massa/ PM(g)
V(l)
M = massa
PM(g) x V(l)
PROCEDIMENTO PRTICO
Material necessrio: gua destilada, NaCl, sacarose, Balana analtica, Folha de alumnio,
esptulas, 2 bqueres de 250ml, 2 bales volumtricos de 100ml, 1 balo volumtrico de
500ml, 1 proveta de 250ml, 1 basto de vidro, 1 pipeta graduada de 5ml, 2 pipetas
graduadas de 10ml
Procedimento:
1. Preparar 100ml de uma soluo 0,3M de NaCl (PM=58,5).
2. A partir da soluo acima, preparar 100ml de uma soluo 0,03M de NaCl.
3. Preparar 500ml de uma soluo 0,1M de sacarose (PM=342).
UNIVERSIDADE FEDERAL RURAL DO RIO DE JANEIRO
INSTITUTO DE BIOLOGIA
DEPARTAMENTO DE CINCIAS FISIOLGICAS
DISCIPLINA: IB 302 Biofsica
PROFESSORES: Jairo Pinheiro, Michelle Marassi e Norma Almeida.
ROTEIRO DE AULA PRTICA
ASSUNTO: Osmose
As clulas biolgicas quando colocadas em solues de diferentes concentraes,
podem sofrer perturbaes osmticas, permanecendo com seu volume inalterado, inchar at
arrebentar ou murcharem por compresso.
De acordo com o comportamento das clulas, o meio onde estas so colocadas
ento classificado em hipotnico, isotnico ou hipertnico.
MATERIAL: sangue tubos de ensaio pipetas graduadas solues de NaCl 0,9% e
NaCl 4% - gua destilada tubos de centrfuga centrfuga de bancada.
PROCEDIMENTO:
Tubos
1
2
3
gua dest. NaCl 0,9%
10 ml
10 ml
-
NaCl 4%
10 ml
-
Sangue
0,5 ml
0,5 ml
0,5 ml
1 Misturar o contedo de cada tubo por uma inverso suave e esperar 10 minutos.
2 Centrifugar os tubos a 4000 rpm.
3 Decantar o contedo de cada tubo e observar as caractersticas do precipitado.
UNIVERSIDADE FEDERAL RURAL DO RIO DE JANEIRO
INSTITUTO DE BIOLOGIA
DEPARTAMENTO DE CINCIAS FISIOLGICAS
DISCIPLINA: IB 302 Biofsica
PROFESSORES: Jairo Pinheiro, Michelle Marassi e Norma Almeida.
ROTEIRO DE AULA PRTICA
ASSUNTO: Dilise
Membranas semipermeveis podem separar concentraes distintas de um mesmo
soluto ou de solutos diferentes, neste caso normalmente um soluto no difusvel, ou no
dialisvel naquele sistema de transporte.
O processo de dilise ocorre nos sistemas biolgicos, sendo de extrema importncia.
o que observamos, por exemplo, nos capilares que compem o glomrulo renal, onde
pequenas partculas, como sdio, potssio, uria e gua, conseguem atravessar livremente a
membrana do capilar, passando para o interior da cpsula de Bowman, porm as
macromolculas, como as protenas plasmticas no conseguem atravessar a membrana dos
capilares. Neste exemplo, a seleo se d predominantemente pelo tamanho da espcie a
ser transportada, mas outros fatores, como gradientes de presso e eltrico, presena de
carga na espcie a ser transportada e nos canais, temperatura, tempo e forma da partcula
podem influenciar o processo de dilise.
MATERIAL: soluo de AgNO3 (5%) soluo de amido soluo de NaCl (5%)
soluo de Lugol papel celofane pipetas tubos de ensaio bquer
de 500 ml barbantes.
PROCEDIMENTO:
1 Umedecer previamente o papel celofane em gua destilada.
2 Fazer, com o papel celofane, um saquinho, amarrando-o na extremidade inferior da
pipeta de 10 ml. Esvaziar o saquinho e verificar se h vazamentos.
3 Adicionar, atravs da extremidade livre da pipeta, 10 ml de soluo de NaCl e 10 ml da
soluo de amido.
4 Colocar gua destilada no bquer em quantidade suficiente para cobrir a parte do saco
de celofane que contm a mistura das duas solues.
5 Deixar o sistema em repouso por 15 min. e proceder de acordo com o quadro abaixo.
Reagentes/Tubos
1
2
3
4
5
6
gua
1 ml
1 ml
Sol. amido
1 ml
Sol. NaCl
1 ml
gua do bquer
1 ml
1ml
Lugol
1 gota
1 gota
1 gota
AgNO3
1 gota
1 gota
1 gota
6- Interpretar os resultados obtidos.
UNIVERSIDADE FEDERAL RURAL DO RIO DE JANEIRO
INSTITUTO DE BIOLOGIA
DEPARTAMENTO DE CINCIAS FISIOLGICAS
DISCIPLINA: IB 302 Biofsica
PROFESSORES: Jairo Pinheiro, Michelle Marassi e Norma Almeida.
ROTEIRO DE AULA PRTICA
ASSUNTO: Determinao de pH
O termo pH foi proposto por Srensen para designar o potencial de hidrognio inico em
um determinado meio, sendo matematicamente expresso por uma funo logartmica devido aos
baixos valores da concentrao de on hidrognio, quando comparado com outros ons.
H diferentes mtodos para determinao do pH em um meio, variando a sua praticidade e
preciso, o que os torna mais ou menos adequados a diferentes situaes, dependendo de nosso
objetivo.
MATERIAL: solues de pH desconhecido pipetas graduadas estantes para tubos
tubos de ensaio papel indicador de pH indicador universal de Bgen
potencimetro tampes de calibrao pH 4,0 e 7,0.
PROCEDIMENTO:
1 Enumerar os tubos de ensaio.
2 Transferir 1 ml da soluo 1 para o tubo 1, 1 ml da soluo 2 para o tubo 2 e 1 ml da soluo 3
para o tubo 3.
3 Acrescentar 1 gota do indicador universal de Bgen em cada tubo.
4 Observar a colorao desenvolvida em cada tubo e comparar com a tabela abaixo para
determinar o pH de cada soluo e anote no quadro abaixo.
INDICADOR UNIVERSAL DE BGEN
Cor
Reao
pH aproximado
Vermelho
Muito cida
2
Alaranjado
cida
4
Amarela
Fracamente cida
6
Verde
Fracamente alcalina
8
Azul
Alcalina
10
5 Com o auxlio do papel indicador, determinar o pH das solues 1, 2 e 3, contidas em cada um
dos tubos e anote no quadro abaixo.
6 Determinar o pH das solues 1, 2 e 3 contidas em cada tubo com o auxlio do potencimetro e
anotar os valores observados no quadro abaixo.
7 Comparar os resultados.
pH
Amostra Indicador universal
Papel indicador Potencimetro
1
2
3
UNIVERSIDADE FEDERAL RURAL DO RIO DE JANEIRO
INSTITUTO DE BIOLOGIA
DEPARTAMENTO DE CINCIAS FISIOLGICAS
DISCIPLINA: IB 302 Biofsica
PROFESSORES: Jairo Pinheiro, Michelle Marassi e Norma Almeida.
ROTEIRO DE AULA PRTICA
ASSUNTO: Capacidade Tamponante dos Lquidos Biolgicos
Os seres vivos so extremamente sensveis s variaes do pH do seu meio interno.
O controle fsico do pH feito atravs de misturas reguladoras chamadas Tampes. O
tampo recolhe prtons quando h excesso ou fornece prtons quando h falta. O tampo
no impede mudanas de pH, mas atenua consideravelmente essas mudanas.
MATERIAL: solues de HCl e NaOH pipetas graduadas basto de vidro
bquer - papel indicador de pH gua destilada urina
PROCEDIMENTO:
1 Identificar 1 bquer para gua destilada e outro para urina.
2 Pipetar 25ml de gua destilada e 25ml de urina no bquer identificado.
3 Medir o pH da gua e da urina utilizando a fita indicadora de pH.
4 Pipetar volumes crescentes (0,5; 1; 1,5 ml) de HCl e NaOH no bquer com gua
destilada e com urina. Cada grupo ficar responsvel por um volume.
5 Misturar com o basto de vidro.
6 Medir o pH com a fita indicadora de pH e anotar no quadro abaixo.
7 Construir um grfico com a curva da gua e da urina. Analisar e discutir os resultados.
pH da gua destilada =
25 ml
Grupo 1
Grupo 2
Grupo 3
Grupo 4
Grupo 5
Grupo 6
pH da urina =
HCl
NaOH
gua destilada
Urina
gua destilada
Urina
gua destilada
Urina
0,5 ml
0,5 ml
1 ml
1 ml
1,5 ml
1,5 ml
gua destilada
Urina
gua destilada
Urina
gua destilada
Urina
0,5 ml
0,5 ml
1 ml
1 ml
1,5 ml
1,5 ml
pH
UNIVERSIDADE FEDERAL RURAL DO RIO DE JANEIRO
INSTITUTO DE BIOLOGIA
DEPARTAMENTO DE CINCIAS FISIOLGICAS
DISCIPLINA: IB 302 Biofsica
PROFESSORES: Jairo Pinheiro, Michelle Marassi e Norma Almeida.
ROTEIRO DE AULA PRTICA
ASSUNTO: Medida indireta da presso arterial
A medida da presso arterial sistmica pode ser realizada por mtodo direto ou
indireto. A medida direta da presso arterial obtida de forma invasiva, mediante a
introduo de um cateter em artria perifrica, o que permite sua quantificao
continuamente, batimento a batimento. A medida indireta da presso arterial pode ser
efetuada, utilizando-se diversas tcnicas, sendo aquela realizada com o esfigmomanmetro
de coluna de mercrio ou aneride, a mais utilizada na prtica clnica diria. Este
equipamento foi desenvolvido, inicialmente, pelo mdico italiano Riva Rocci, em 1896, e
aperfeioado, no que tange ao mtodo de medida, por Nikolas Korotkoff, no incio do
sculo XX. A padronizao da tcnica de medida, ento estabelecida, permanece
praticamente inalterada desde ento. Este autor verificou que, ao desinflar o manguito que
oclua totalmente a artria, diferentes tipos de sons eram perceptveis com o estetoscpio, o
que correspondia a diferentes graus de obstruo parcial da artria.
Os rudos ou fases de Korotkoff podem ser detectados na maioria dos indivduos se
o procedimento de medida for executado dentro do rigor estabelecido para tal tcnica. So
cinco as fases:
Fase I- Corresponde ao aparecimento do primeiro som, ao qual se seguem batidas
progressivamente mais fortes, bem distintas e de alta frequncia. Correlaciona-se com o
nvel da presso sistlica.
Fase II- Neste momento, o som adquire caracterstica de zumbido e sopro, podendo
ocorrer sons de baixa frequncia, que eventualmente determinam o hiato auscultatrio.
Fase III- Sons ntidos e intensos.
Fase IV- Abafamento dos sons, correspondendo ao momento prximo ao
desaparecimento deles.
Fase V- Desaparecimento total dos sons. Correlaciona-se com a presso diastlica.
MATERIAL: Manguito esfigmomanmetro estetoscpio algodo lcool.
PROCEDIMENTO:
A medida da presso arterial tem sua tcnica padronizada e publicada em diversas
diretrizes internacionais. No Brasil, foi publicada, mais recentemente, como parte do III
Consenso Brasileiro de Hipertenso Arterial. Abaixo est transcrita a sequncia de passos a
serem executados para uma medida adequada da presso arterial.
8
1) Explicar o procedimento ao paciente.
2) Certificar-se de que o paciente: no est com a bexiga cheia; no praticou exerccios
fsicos; no ingeriu bebidas alcolicas, caf, alimentos, ou fumou at 30 min antes da
medida.
3) Deixar o paciente descansar por 5 a 10min em ambiente calmo, com temperatura
agradvel.
4) Localizar a artria braquial por palpao.
5) Colocar o manguito firmemente cerca de 2cm a 3cm acima da fossa antecubital,
centralizando a bolsa de borracha sobre a artria braquial. A largura da bolsa de borracha
do manguito deve corresponder a 40% da circunferncia do brao, e seu comprimento
envolver, pelo menos, 80% do brao. Assim, a largura do manguito a ser utilizado estar na
dependncia da circunferncia do brao do paciente.
6) Manter o brao do paciente na altura do corao.
7) Posicionar os olhos no mesmo nvel da coluna de mercrio ou do mostrador do
manmetro aneride.
8) Palpar o pulso radial e inflar o manguito at seu desaparecimento, para a estimativa do
nvel da presso sistlica, desinflar rapidamente e aguardar de 15 a30 seg antes de inflar
novamente.
9) Colocar o estetoscpio nos ouvidos, com a curvatura voltada para a frente.
10) Posicionar a campnula do estetoscpio, suavemente, sobre a artria braquial, na fossa
antecubital, evitando compresso excessiva.
11) Solicitar ao paciente que no fale durante o procedimento de medio.
12) Inflar rapidamente, de 10 mmHg em 10 mmHg, at 10 a 20 mmHg acima do nvel
estimado da presso arterial.
13) Proceder deflao, com velocidade constante inicial de 2 mmHg a 4 mmHg por
segundo, evitando congesto venosa e desconforto para o paciente.
14) Determinar a presso sistlica no momento do aparecimento do primeiro som (fase I de
Korotkoff), que se intensifica com o aumento da velocidade de deflao.
15) Determinar a presso diastlica no desaparecimento do som (fase V de Korotkoff),
exceto em condies especiais. Auscultar cerca de 20 mmHg a 30 mmHg abaixo do ltimo
som, para confirmar seu desaparecimento e, depois, proceder deflao rpida e completa.
Quando os batimentos persistirem at o nvel zero, determinar a presso diastlica no
abafamento dos sons (fase IV de Korotkoff) e anotar o valor final de zero, por exemplo,
136/78/0.
16) Registrar os valores das presses sistlica e diastlica, complementando com a posio
do paciente, o tamanho do manguito e o brao em que foi feita a mensurao. Dever ser
registrado sempre o valor da presso, obtido na escala do manmetro, que varia de 2 mmHg
em 2 mmHg, evitando-se arredondamentos.
17) Esperar 1 a 2 min antes de realizar novas medidas.
18) O paciente deve ser informado sobre os valores da presso arterial e a possvel
necessidade de acompanhamento.
Em caso de dificuldade para auscultar os rudos de Korotkoff, pode-se lanar mo
de uma manobra simples: fechar e abrir a mo do membro em que a presso est sendo
medida, durante alguns segundos.
Você também pode gostar
- Unidade 1 - Solução Tampão PDFDocumento20 páginasUnidade 1 - Solução Tampão PDFLEE MARX100% (1)
- Aula 04 DOENÇAS CAUSADAS POR VÍRUS Caxumba, Raiva, Meningite, GripesDocumento23 páginasAula 04 DOENÇAS CAUSADAS POR VÍRUS Caxumba, Raiva, Meningite, GripeslidiaAinda não há avaliações
- 2 Aula Prática Fisiologia HumanaDocumento18 páginas2 Aula Prática Fisiologia HumanaAntónio Netto100% (1)
- Enemem100dias Apostila BiologiaDocumento218 páginasEnemem100dias Apostila Biologiapaulo100% (1)
- Origem da Vida: Teorias sobre como surgiram os primeiros seres vivos na TerraDocumento53 páginasOrigem da Vida: Teorias sobre como surgiram os primeiros seres vivos na TerraIvan Barbosa100% (1)
- Procedimento Operacional Padrao Capela de Exaustao Com Lavador de GasesDocumento6 páginasProcedimento Operacional Padrao Capela de Exaustao Com Lavador de GasesPdindin100% (1)
- Introdução À BioquímicaDocumento43 páginasIntrodução À BioquímicaUallase VenturiniAinda não há avaliações
- 04 Biofísica Da CirculaçãoDocumento41 páginas04 Biofísica Da CirculaçãoTatiane ValeAinda não há avaliações
- Origem Do UniversoDocumento147 páginasOrigem Do UniversoJoão Victor LadislauAinda não há avaliações
- Aula 8 - nr-32Documento70 páginasAula 8 - nr-32André HenriqueAinda não há avaliações
- Aula - 2 Busca de Evidências CientíficasDocumento25 páginasAula - 2 Busca de Evidências CientíficasRodrigo RodriguesAinda não há avaliações
- PPT5 - Obtenção de Matéria (Seres Heterotróficos) - Membrana PlasmáticaDocumento28 páginasPPT5 - Obtenção de Matéria (Seres Heterotróficos) - Membrana PlasmáticablacksmokerAinda não há avaliações
- A Célula: Unidade Básica e FuncionalDocumento9 páginasA Célula: Unidade Básica e FuncionalVerónica MartinsAinda não há avaliações
- Roteiro Rato Virtual Sistema EndócrinoDocumento6 páginasRoteiro Rato Virtual Sistema EndócrinoHeberson SantosAinda não há avaliações
- Acidez e Basicidade em Compostos OrgânicosDocumento8 páginasAcidez e Basicidade em Compostos OrgânicosRayanne Silva100% (1)
- Resultados análise ácido-baseDocumento7 páginasResultados análise ácido-baseMineiraPereira100% (1)
- 11 Biofisica Da RespiracaoDocumento36 páginas11 Biofisica Da RespiracaoAna Katarine Pordeus LisboaAinda não há avaliações
- Elementos Da Função RenalDocumento29 páginasElementos Da Função RenalRosimere Brito100% (1)
- Aula 1 de Citologia, Histologia e EmbriologiaDocumento27 páginasAula 1 de Citologia, Histologia e EmbriologiaElyarlan FabioAinda não há avaliações
- Características Gerais Da Célula e Suas EstruturasDocumento37 páginasCaracterísticas Gerais Da Célula e Suas EstruturasRobert BrennerAinda não há avaliações
- Estudo Dirigido Proliferação CelularDocumento12 páginasEstudo Dirigido Proliferação CelularFernando Granzotto100% (1)
- Sistema respiratório: funções e anatomiaDocumento53 páginasSistema respiratório: funções e anatomiaELOIZI DOS PASSOS100% (1)
- Vírus: vida, estrutura e infecçãoDocumento19 páginasVírus: vida, estrutura e infecçãoBruno Tiago100% (1)
- POP 50 - DETERMINAÇÃO DO PHDocumento4 páginasPOP 50 - DETERMINAÇÃO DO PHMAGALI MURROAinda não há avaliações
- Formacao Pedagogica de Preceptores Do Ensino em Saude PDFDocumento126 páginasFormacao Pedagogica de Preceptores Do Ensino em Saude PDFfabioconstancio335311100% (1)
- Doenças protozoáriasDocumento16 páginasDoenças protozoáriasRenato GessingerAinda não há avaliações
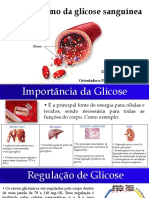
- Regulação da glicose sanguíneaDocumento18 páginasRegulação da glicose sanguíneadebora machado fonseca100% (1)
- Regulação da Temperatura Corporal e Alterações como Febre e HipotermiaDocumento45 páginasRegulação da Temperatura Corporal e Alterações como Febre e Hipotermiapereira_wilker9835Ainda não há avaliações
- Avaliano o Aprendizado - Anatomia Do Aparelho Locomotor 2018.2Documento2 páginasAvaliano o Aprendizado - Anatomia Do Aparelho Locomotor 2018.2Marcelly Elizabeth100% (1)
- Métodos de Contracepção QuímicosDocumento32 páginasMétodos de Contracepção Químicosescapesest100% (1)
- Lista Exerc BioquimicaDocumento9 páginasLista Exerc BioquimicaCamille FlexaAinda não há avaliações
- Sistema muscular: componentes, tipos e classificaçãoDocumento44 páginasSistema muscular: componentes, tipos e classificaçãogerasanthi100% (2)
- Os principais métodos contraceptivos: naturais, não naturais e de emergênciaDocumento20 páginasOs principais métodos contraceptivos: naturais, não naturais e de emergênciaWanda MagalhãesAinda não há avaliações
- Metodos ContraceptivosDocumento17 páginasMetodos Contraceptivosvanessaluis100% (9)
- Perguntas de AnatomiaDocumento13 páginasPerguntas de AnatomiaBeatrizBarbosaAinda não há avaliações
- Elemento Radioativo PolônioDocumento2 páginasElemento Radioativo PolôniowozikAinda não há avaliações
- ProtozoáriosDocumento26 páginasProtozoáriosThiago Almeida de Carvalho100% (1)
- Biologia PPT - Sistema Digestivo IDocumento11 páginasBiologia PPT - Sistema Digestivo IBiologia ppt100% (5)
- Exercícios - Sistemas Nervoso e EndócrinoDocumento3 páginasExercícios - Sistemas Nervoso e EndócrinoKelley Cristiny PiresAinda não há avaliações
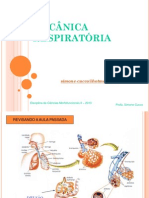
- Mecânica Respiratória - Ciências Morfofuncionais II - Simone Cucco - UNIMEDocumento56 páginasMecânica Respiratória - Ciências Morfofuncionais II - Simone Cucco - UNIMEEtcy TalAinda não há avaliações
- Interações EcologicasDocumento29 páginasInterações EcologicasArianne FabresAinda não há avaliações
- Aminoácidos para atletasDocumento2 páginasAminoácidos para atletashandreymAinda não há avaliações
- Aula 1 - IntroduçãoDocumento41 páginasAula 1 - IntroduçãoLeticia RodriguesAinda não há avaliações
- Aula 7º Ano Anelideos Platelmintos e NematelmintosDocumento24 páginasAula 7º Ano Anelideos Platelmintos e NematelmintosteresaAinda não há avaliações
- ANATOMIA HUMANA PLANOS E ESTRUTURASDocumento24 páginasANATOMIA HUMANA PLANOS E ESTRUTURASgutoaragaoAinda não há avaliações
- 05 Traumatismos Exame Neurológico em Trauma VertebralDocumento18 páginas05 Traumatismos Exame Neurológico em Trauma VertebralManfroi GregoriAinda não há avaliações
- Aula 2 - Biofísica Da AguaDocumento18 páginasAula 2 - Biofísica Da AguaLudymilla Barbosa100% (1)
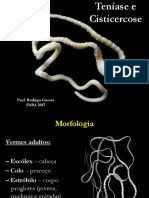
- Teníase e Cisticercose: Morfologia, Ciclo Biológico e DiagnósticoDocumento16 páginasTeníase e Cisticercose: Morfologia, Ciclo Biológico e DiagnósticoAllana CristinaAinda não há avaliações
- EF Ke08 AsPopulacoeseoAmbienteDocumento17 páginasEF Ke08 AsPopulacoeseoAmbienteeng civil Paulo Vitor MedeirosAinda não há avaliações
- Plano de Ação Escolar - Diagnóstico e IndicadoresDocumento12 páginasPlano de Ação Escolar - Diagnóstico e IndicadoresEREM SÃO SEBASTIÃOAinda não há avaliações
- Roteiro 1 Ano R6Documento8 páginasRoteiro 1 Ano R6Fernanda CruzAinda não há avaliações
- FungosDocumento48 páginasFungosThayane MaytcheleAinda não há avaliações
- Iatrogenia na prática geriátricaDocumento33 páginasIatrogenia na prática geriátricaAnanda DomingosAinda não há avaliações
- Trilha BIOLOGIA 2 Série Semana04Documento6 páginasTrilha BIOLOGIA 2 Série Semana04Daiane NicoliAinda não há avaliações
- Aula NeuroanatomiaDocumento32 páginasAula NeuroanatomiaNavegantes Silva de OliveiraAinda não há avaliações
- Concurso CEFET Química/RJ provê cargos de professorDocumento14 páginasConcurso CEFET Química/RJ provê cargos de professorThyago MotaAinda não há avaliações
- Biorremediação de solos - técnicas e aplicaçõesDocumento9 páginasBiorremediação de solos - técnicas e aplicaçõesdennyele0% (1)
- Mutações e cromossomopatiasDocumento72 páginasMutações e cromossomopatiasChristian Lenk de souza100% (1)
- Formas e Estruturas BacterianasDocumento36 páginasFormas e Estruturas BacterianasSophia GambardelloAinda não há avaliações
- No caminho certo após uma cirurgia cardíaca: Um guia completo com orientações e recomendações para o pós-operatórioNo EverandNo caminho certo após uma cirurgia cardíaca: Um guia completo com orientações e recomendações para o pós-operatórioAinda não há avaliações
- Lista12 - ED Ordem Sup, Variação de Parametros PDFDocumento2 páginasLista12 - ED Ordem Sup, Variação de Parametros PDFDenison VictorAinda não há avaliações
- 1 Lista de Exercicios ResolucaoDocumento4 páginas1 Lista de Exercicios ResolucaoDenison VictorAinda não há avaliações
- Os ElementaisDocumento9 páginasOs ElementaisDenison VictorAinda não há avaliações
- SAFASFSAFASFDocumento4 páginasSAFASFSAFASFDenison VictorAinda não há avaliações
- Derivada 1 PDFDocumento28 páginasDerivada 1 PDFDenison VictorAinda não há avaliações
- Algebra Linear Ead Livro 1 PDFDocumento197 páginasAlgebra Linear Ead Livro 1 PDFSimone Santana100% (1)
- Teorema Fundamental Do CalculoDocumento5 páginasTeorema Fundamental Do CalculoDenison VictorAinda não há avaliações
- As muitas funções de um time de Xadrez PokémonDocumento4 páginasAs muitas funções de um time de Xadrez PokémonDenison VictorAinda não há avaliações
- 3d&t - Manual Das Vantagens Alpha - Versão 1.6Documento138 páginas3d&t - Manual Das Vantagens Alpha - Versão 1.6andre_alcantaraAinda não há avaliações
- As Proteínas Apresentam Solubilidades Variadas emDocumento3 páginasAs Proteínas Apresentam Solubilidades Variadas emLauraAinda não há avaliações
- Brix manualDocumento96 páginasBrix manualDébora DamianiAinda não há avaliações
- Determination CL For MohrDocumento8 páginasDetermination CL For MohrRicardo BrunoAinda não há avaliações
- Prova32 Tecnico em Quimica de PetroleoDocumento15 páginasProva32 Tecnico em Quimica de PetroleoAlexandre BarbosaAinda não há avaliações
- Artigo FinalDocumento20 páginasArtigo Finalmariane carneiroAinda não há avaliações
- Fundamentacao Teorica para IontoforeseDocumento8 páginasFundamentacao Teorica para IontoforeseThiago Botacin PanettoAinda não há avaliações
- Rebolo Orgânico: Instruções de SegurançaDocumento10 páginasRebolo Orgânico: Instruções de Segurançarsantos356Ainda não há avaliações
- O equilíbrio ácido-alcalino e a importância da alcalinidade para a saúdeDocumento5 páginasO equilíbrio ácido-alcalino e a importância da alcalinidade para a saúdeviviane custodioAinda não há avaliações
- Apostila PráticaDocumento36 páginasApostila Práticamarcoslouro.medicinaAinda não há avaliações
- Métodos para Análise Microbiológica de Produtos de Origem Animal e ÁguaDocumento76 páginasMétodos para Análise Microbiológica de Produtos de Origem Animal e ÁguaSoane SoucarAinda não há avaliações
- Determinação de acidez e basicidade por diferentes métodosDocumento17 páginasDeterminação de acidez e basicidade por diferentes métodosVinicius SalomãoAinda não há avaliações
- Coletânea de provas resolvidas de químicaDocumento88 páginasColetânea de provas resolvidas de químicaLouis PhiAinda não há avaliações
- Experimento de PHDocumento8 páginasExperimento de PHJanioPauloEleoterioFerreiraFerreiraAinda não há avaliações
- Aquifero BambuíDocumento11 páginasAquifero BambuíPaulo HenriqueAinda não há avaliações
- Resumo - Portaria GMMS #888 de 4 de Maio de 2021Documento9 páginasResumo - Portaria GMMS #888 de 4 de Maio de 2021Síntia MacêdoAinda não há avaliações
- Inseticida NaturaisDocumento15 páginasInseticida Naturaismcbneto5470Ainda não há avaliações
- Ácidos & Bases Do Meu Dia - Uma Sequência Didática para o Ensino de QuímicaDocumento9 páginasÁcidos & Bases Do Meu Dia - Uma Sequência Didática para o Ensino de QuímicaGil VaneteAinda não há avaliações
- Relatório 4 - QA - Separação de Cátions Do Grupo IIIADocumento5 páginasRelatório 4 - QA - Separação de Cátions Do Grupo IIIAEmílioDosSantosAinda não há avaliações
- Relatório Condutividade de Soluções EletroliticasDocumento9 páginasRelatório Condutividade de Soluções Eletroliticasmarcos5513Ainda não há avaliações
- Lista de Exercícios - LogaritmoDocumento3 páginasLista de Exercícios - LogaritmoRicardo cardosoAinda não há avaliações
- Artigo Lauren Zauza - Eugenia UnifloraDocumento13 páginasArtigo Lauren Zauza - Eugenia UnifloraLauren ZauzaAinda não há avaliações
- Lição Nº. 9 e 10 - para 11 Classe - CópiaDocumento4 páginasLição Nº. 9 e 10 - para 11 Classe - CópiaKivangui AguiarAinda não há avaliações
- 17 PH e pOHDocumento6 páginas17 PH e pOHRodrigo CarneiroAinda não há avaliações
- Relatório Anin - PhmetriaDocumento7 páginasRelatório Anin - PhmetriaDaniel CoelhoAinda não há avaliações
- Lista 3 Produto Ionico Da Água - GabaritoDocumento6 páginasLista 3 Produto Ionico Da Água - GabaritomateusAinda não há avaliações