Escolar Documentos
Profissional Documentos
Cultura Documentos
Química - Caderno de Resoluções - Apostila Volume 1 - Pré-Universitário - Quim3 Aula02
Enviado por
Química Caderno de ResoluçõesTítulo original
Direitos autorais
Formatos disponíveis
Compartilhar este documento
Compartilhar ou incorporar documento
Você considera este documento útil?
Este conteúdo é inapropriado?
Denunciar este documentoDireitos autorais:
Formatos disponíveis
Química - Caderno de Resoluções - Apostila Volume 1 - Pré-Universitário - Quim3 Aula02
Enviado por
Química Caderno de ResoluçõesDireitos autorais:
Formatos disponíveis
Química 3 aula 2 2.
( F ) Os gases não são bons condutores de corrente elé-
COMENTÁRIOS – ATIVIDADES PARA SALA trica
(V)
1. O modelo atômico de Thomson considera partículas (V)
subatômicas. (V)
(V)
Resposta correta: B (V)
Resposta correta: F, V, V, V, V, V
2. Caracteriza a descoberta dos elétrons.
Resposta correta: E 3. Há cem anos, acredita-se que o átomo era o menor
3. O sal de Urânio, usado por Becquerel conseguia impres- constituinte da matéria, que era indivisível, mas com a
sionar chapas fotográficas, pelo fato de o próprio Urânio descoberta do elétron em 1847, pode-se concluir que o
ser radioativo e emitir partículas, que hoje conhecemos átomo é divisível. Hoje sabemos que existem partículas
como partículas α, β e γ. E não pelo fato da fluorescên- menores “os elétrons”.
cia.
Resposta correta: B
Resposta correta: D
4. Na visão de Thomson, o átomo seria uma esfera de
4. Nos primeiro experimento, Thomson pôde averiguar massa uniforme e de carga positiva, espalhada pela es-
que os raios catódicos eram desviados por um campo fera uniformemente. E que na esfera, existiriam partícu-
elétrico e magnético concluindo que os raios catódicos las incrustadas. Os elétrons, de carga negativa, o que
são constituídos de partículas com carga elétrica e pelo tornaria o átomo eletricamente neutro.
desvio concluiu que eram partículas eletricamente nega-
tivas (menor que zero). Resposta correta: B
No segundo experimento, os raios catódicos são inter-
ceptados por um molinete, verificando que este entra
em movimento de rotação pôde concluir que os raios 5. Thomson elaborou seu modelo atômico baseado em
catódicos apresentam massa diferente de zero, ou seja, uma série de observações e resultados experimentais,
são corpusculares. como a descoberta dos íons, a descoberta dos raios ca-
nais, a descoberta da radioatividade e a descoberta dos
Resposta correta: D raios catódicos. A descoberta da quantização da energia
não foi utilizada por Thomson.
5. Dalton desconhecia os elementos isótopos. Resposta correta: E
Resposta correta: C
6. Ao receber o prêmio Nobel, Pierre Curie deixa claro que
novas descobertas nas mãos de pessoas certas trazem
mais benefícios à humanidade que prejuízos.
Resposta correta: E
COMENTÁRIOS – ATIVIDADES PROPOSTAS
1. O físico americano Robert Andrews Millikan mediu a
7. O modelo de Thompson propôs que o átomo seria for-
carga de um elétron e assim possibilitou o cálculo de sua
mado por um esfera de carga positiva contendo, em sua
massa. Millikan usou um aparelho, onde injeta-se uma
superfície, elétrons incrustados, possuidores de carga
nuvem de gotículas de óleo na câmara, as moléculas de
negativa.
gás na câmara são ionizadas por um feixe de raios x. Os
elétrons aderem às gotículas de óleo, e algumas ficam
com um elétron, outras com dois, e assim por diante, es- Resposta correta: D
sas gotas de óleo com carga negativa caem sob a ação
da gravidade numa região entre duas placas carregadas
eletricamente. Pelo ajuste cuidadoso da voltagem entre 8. O próton apresenta massa de 1,672623 x 10–24g e carga
as placas, a força da gravidade é exatamente contraba- +1. O elétrons apresenta massa de 9,109389 x 10–28g e
lanceada pela atração que a placa superior, positiva carga –1.
exerce sobre a gota. A análise dessas forças leva ao va-
lor da carga do elétron. Resposta correta: C
Resposta correta: A
3ª SÉRIE E EXTENSIVO | VOLUME 1 | QUÍMICA 3 1
9. Característica do modelo de Thomson.
Resposta correta: E
10.
( F ) Os raios anódicos caminham em direção contrária
ao ânodo.
(V)
(V)
( F ) A massa dos raios catódicos é 1.836 vezes menor
que a massa dos raios canais.
(V)
Resposta correta: F, V, V, F, V
2 3ª SÉRIE E EXTENSIVO | VOLUME 1 | QUÍMICA 3
Você também pode gostar
- Apostila Química Cnen - Radiações IonizantesDocumento42 páginasApostila Química Cnen - Radiações IonizantesQuímica Caderno de Resoluções100% (2)
- Química - Pré-Vestibular Dom Bosco - Gab-Qui2-Ex2Documento7 páginasQuímica - Pré-Vestibular Dom Bosco - Gab-Qui2-Ex2Química Caderno de Resoluções100% (4)
- Apostila Química Cnen - Radioatividade IIDocumento19 páginasApostila Química Cnen - Radioatividade IIQuímica Caderno de Resoluções100% (1)
- Apostila Química Cnen - Radioatividade IDocumento50 páginasApostila Química Cnen - Radioatividade IQuímica Caderno de Resoluções100% (3)
- Química - Pré-Vestibular Dom Bosco - Gab-Qui1-Se2Documento6 páginasQuímica - Pré-Vestibular Dom Bosco - Gab-Qui1-Se2Química Caderno de Resoluções100% (2)
- Química - CEESVO - Apostila2Documento50 páginasQuímica - CEESVO - Apostila2Química Caderno de Resoluções100% (3)
- Apostila Química Cnen - Aplicações Da Energia NuclearDocumento18 páginasApostila Química Cnen - Aplicações Da Energia NuclearQuímica Caderno de Resoluções100% (12)
- Apostila Química Cnen - Energia Nuclear HistóriaDocumento20 páginasApostila Química Cnen - Energia Nuclear HistóriaQuímica Caderno de Resoluções100% (2)
- Apostila Química Cnen - Energia NuclearDocumento29 páginasApostila Química Cnen - Energia NuclearQuímica Caderno de Resoluções100% (1)
- Química - CEESVO - Apostila1Documento73 páginasQuímica - CEESVO - Apostila1Vestibular Apostilas100% (5)
- Química - CuriosidadesDocumento2 páginasQuímica - CuriosidadesQuímica Caderno de ResoluçõesAinda não há avaliações
- Química - Pré-Vestibular Dom Bosco - Gab-Qui1-Ex4Documento6 páginasQuímica - Pré-Vestibular Dom Bosco - Gab-Qui1-Ex4Química Caderno de ResoluçõesAinda não há avaliações
- Ligação QuímicaDocumento7 páginasLigação QuímicaJosé António Araújo Gonçalves100% (6)
- Química - CEESVO - Apostila3Documento58 páginasQuímica - CEESVO - Apostila3Vestibular Apostilas100% (4)
- Química - Pré-Vestibular Dom Bosco - Gab-Qui2-Se4Documento9 páginasQuímica - Pré-Vestibular Dom Bosco - Gab-Qui2-Se4Química Caderno de ResoluçõesAinda não há avaliações
- Química - Pré-Vestibular Dom Bosco - Gab-Qui2-Se2Documento7 páginasQuímica - Pré-Vestibular Dom Bosco - Gab-Qui2-Se2Química Caderno de ResoluçõesAinda não há avaliações
- Química - Apostila 6 - Artigos para Leitura ComplementarDocumento5 páginasQuímica - Apostila 6 - Artigos para Leitura ComplementarQuímica Caderno de ResoluçõesAinda não há avaliações
- Química - Pré-Vestibular Dom Bosco - Gab-Qui2-Ex3Documento7 páginasQuímica - Pré-Vestibular Dom Bosco - Gab-Qui2-Ex3Química Caderno de Resoluções100% (1)
- Química - Apostila 2 - Artigos para Leitura ComplementarDocumento8 páginasQuímica - Apostila 2 - Artigos para Leitura ComplementarQuímica Caderno de Resoluções100% (1)
- Química - Apostila 3 - Artigos para Leitura ComplementarDocumento9 páginasQuímica - Apostila 3 - Artigos para Leitura ComplementarQuímica Caderno de Resoluções33% (3)
- Química - Pré-Vestibular Dom Bosco - Gab-Qui1-Ex1Documento5 páginasQuímica - Pré-Vestibular Dom Bosco - Gab-Qui1-Ex1Química Caderno de Resoluções100% (3)
- Química - Pré-Vestibular Dom Bosco - Gab-Qui1-Ex3Documento7 páginasQuímica - Pré-Vestibular Dom Bosco - Gab-Qui1-Ex3Química Caderno de Resoluções100% (1)
- Química - Pré-Vestibular Dom Bosco - Equilíbrio Químico-2008Documento8 páginasQuímica - Pré-Vestibular Dom Bosco - Equilíbrio Químico-2008Química Caderno de Resoluções100% (2)
- Química - Apostila 1 - Artigos para Leitura ComplementarDocumento10 páginasQuímica - Apostila 1 - Artigos para Leitura ComplementarQuímica Caderno de Resoluções100% (3)
- Química Orgânica - CASD Vestibulares - Simulado 03Documento2 páginasQuímica Orgânica - CASD Vestibulares - Simulado 03Química Caderno de ResoluçõesAinda não há avaliações
- Química Orgânica - CASD Vestibulares - Simulado 04Documento2 páginasQuímica Orgânica - CASD Vestibulares - Simulado 04Química Caderno de ResoluçõesAinda não há avaliações
- Química Orgânica - CASD Vestibulares - Simulado 02Documento2 páginasQuímica Orgânica - CASD Vestibulares - Simulado 02Química Caderno de Resoluções0% (2)
- Química Orgânica - CASD - Aula14 Reações de Substituição II RespostasDocumento3 páginasQuímica Orgânica - CASD - Aula14 Reações de Substituição II RespostasQuímica Caderno de ResoluçõesAinda não há avaliações
- Química Orgânica - CASD Vestibulares - Simulado 01Documento2 páginasQuímica Orgânica - CASD Vestibulares - Simulado 01Química Caderno de Resoluções100% (1)
- Química Orgânica - CASD - Aula13 Reações de Substituição I RespostasDocumento1 páginaQuímica Orgânica - CASD - Aula13 Reações de Substituição I RespostasQuímica Caderno de Resoluções75% (4)
- Dark Wood 011102033Documento90 páginasDark Wood 011102033jandersondtdAinda não há avaliações
- Nema11 Manual U1 Res PDFDocumento59 páginasNema11 Manual U1 Res PDFJaime FonsecaAinda não há avaliações
- Manual UFCD 8598Documento209 páginasManual UFCD 8598marianampmartinss_69Ainda não há avaliações
- Estácio - Alunos PDFDocumento4 páginasEstácio - Alunos PDFMauricio Lucas AlbertiAinda não há avaliações
- Prova de HistoriaDocumento2 páginasProva de HistoriaBruna SantanaAinda não há avaliações
- Vim20 Ti P339 07 PortuguesDocumento9 páginasVim20 Ti P339 07 PortuguesAndreAinda não há avaliações
- Cartilha Informativa - Síndrome de BurnoutDocumento10 páginasCartilha Informativa - Síndrome de BurnoutIsabela SouzaAinda não há avaliações
- Fiscal de TributosDocumento12 páginasFiscal de TributosFrancisco carpegeano Felix da silvaAinda não há avaliações
- PHDA transição cuidados adultosDocumento11 páginasPHDA transição cuidados adultosFilipa FreitasAinda não há avaliações
- Os Movimentos Espíritas (Ou A Hidra de Lerna Espírita)Documento8 páginasOs Movimentos Espíritas (Ou A Hidra de Lerna Espírita)Antonio BuenoAinda não há avaliações
- Bojana Cvejić - Notas para Uma Sociedade Da Performance - Sobre Dança, Esportes, Museus e Seus UsosDocumento17 páginasBojana Cvejić - Notas para Uma Sociedade Da Performance - Sobre Dança, Esportes, Museus e Seus UsosJbrt OueAinda não há avaliações
- Genealogia ConstelacoesDocumento50 páginasGenealogia Constelacoesraviresck100% (1)
- Sistema Da OrdoDocumento13 páginasSistema Da OrdoJoão100% (1)
- Ajudante de Produção-ServenteDocumento1 páginaAjudante de Produção-ServenteElisaldo SilvaAinda não há avaliações
- História Da Língua PortuguesaDocumento3 páginasHistória Da Língua PortuguesaJOHnnY dAiNAinda não há avaliações
- Importância da sexualidade no casamentoDocumento3 páginasImportância da sexualidade no casamentoIsaac AngeloAinda não há avaliações
- Estaca hélice contínua monitoradaDocumento35 páginasEstaca hélice contínua monitoradapressottiAinda não há avaliações
- Serra Talhada Pereiras e CarvalhoDocumento149 páginasSerra Talhada Pereiras e CarvalhoKraus Diniz CoelhoAinda não há avaliações
- As Grandes Profecias Relativas Aos Gentios - G. H. PemberDocumento406 páginasAs Grandes Profecias Relativas Aos Gentios - G. H. PemberEDGAR DE PAULO SilvaAinda não há avaliações
- Anatomia TireoideeparatireoideDocumento38 páginasAnatomia TireoideeparatireoidethiagomedruasAinda não há avaliações
- As quatro sugestões para mudançaDocumento3 páginasAs quatro sugestões para mudançaRegina CoeliAinda não há avaliações
- Resultado Manaus - Distribuição de Bolsas PIBIC2021 - 1cham.Documento76 páginasResultado Manaus - Distribuição de Bolsas PIBIC2021 - 1cham.Luiz Carlos Martins de SouzaAinda não há avaliações
- Arte 7 AnoDocumento2 páginasArte 7 AnoMárcia BarrosAinda não há avaliações
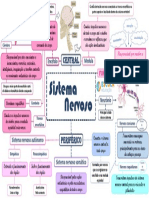
- Sistema nervoso: estrutura e funções principaisDocumento1 páginaSistema nervoso: estrutura e funções principaisGabriela PiresAinda não há avaliações
- 38fatorial, Permutações E Arranjos SimplesDocumento40 páginas38fatorial, Permutações E Arranjos SimplesZé OtávioAinda não há avaliações
- Direito a 1/3 hora-atividade para todos os profissionais da educaçãoDocumento7 páginasDireito a 1/3 hora-atividade para todos os profissionais da educaçãoTiago TondinelliAinda não há avaliações
- Redação Suspensão A ArDocumento1 páginaRedação Suspensão A ArMateus FerreiraAinda não há avaliações
- Eixo Tematico PreconceitoDocumento2 páginasEixo Tematico PreconceitoFelipe CavalcanteAinda não há avaliações
- Análise de riscos de escavaçãoDocumento5 páginasAnálise de riscos de escavaçãoAna Carolina NascimentoAinda não há avaliações
- Aula2 MhsDocumento24 páginasAula2 MhsFelipe MorganAinda não há avaliações