Escolar Documentos
Profissional Documentos
Cultura Documentos
Screening Phytochimiques Des Plantes Medecinales
Enviado por
HarounBio-technologieTítulo original
Direitos autorais
Formatos disponíveis
Compartilhar este documento
Compartilhar ou incorporar documento
Você considera este documento útil?
Este conteúdo é inapropriado?
Denunciar este documentoDireitos autorais:
Formatos disponíveis
Screening Phytochimiques Des Plantes Medecinales
Enviado por
HarounBio-technologieDireitos autorais:
Formatos disponíveis
Afrique SCIENCE 10(3) (2014) 316 - 328 316
ISSN 1813-548X, http://www.afriquescience.info
Screening phytochimique et identification spectroscopique des flavonodes
dAsteriscusgraveolenssubsp. odorus
Hakim ALILOU 1 *, Bouchaib BENCHARKI 1, Lalla Mina Idrissi HASSANI 2 et Noureddine BARKA 3
1
Laboratoire dAgroalimentaire et Sant, Facult des Sciences et Techniques, Universit Hassan 1er,
Casablanca, Maroc
2
Laboratoire de Biotechnologie Vgtale, Facult des Sciences, BP 28/S, Universit Ibn Zohr Agadir, Maroc
3
Universit Hassan 1er, Laboratoire des Sciences des Matriaux, des Milieux et de la Modlisation (LS3M),
Facult Polydisciplinaire de Khouribga, BP. 145 Khouribga, Morocco
________________
*Correspondance, courriel : alilouhakim@gmail.com
Rsum
Ce travail sintresse ltude phytochimique dune espce du Sud du Maroc appartenant la famille des
Asteraceae : Asteriscusgraveolenssubsp. odorus. Le screening phytochimique des feuilles et des fleurs de cette
plante, effectue pour la premire fois, a rvl la prsence des alcalodes, des flavonodes, des tanins
catchiques, des terpnes, des coumarines et des composs cyanogntiques. Quant aux saponines et les
quinones libres, ils sont prsents chez les fleurs et absents chez les feuilles. La caractrisation des molcules
par spectrophotomtrie UV a rvl la prsence de lacide cafique, nvadensine, lutoline et artemtine dans
les feuilles dAsteriscus graveolens subsp. odorus.
Mots-cls : analyse spectrophotomtrique, screening phytochimique, asteriscus graveolens subsp. odorus.
Abstract
Phytochemical screening and spectroscopic identification of flavonoids of
Asteriscusgraveolens sub sp. odorus
This work concern the study of phytochemical of a species of southern Morocco belonging to the Asteraceae
family : Asteriscus graveolens subsp. odorus. The phytochemical screening of the leaves and flowers of this
plant, performed for the first time, reavealed the presence of alkaloids, flavonoids, catechintanins, terpenes,
coumarins and cyagenetic compounds. While the quinones and saponins are present in the flowers and absent in
the leaves. The identification of molecules using UV spectrophotometry showed the presence of caffeic acid,
nevadensine, luteolin and artemetin in leaves of Asteriscus graveolens subsp. odorus.
Keywords : spectrophotometry analysis, phytochemical screening, steriscus graveolens subsp. odorus.
Hakim ALILOU et al.
317 Afrique SCIENCE 10(3) (2014) 316 - 328
1. Introduction
De nos jours, les produits naturels sont une source importante pour la recherche de nouveaux composs actifs
contre de nombreuses maladies. Lutilisation thrapeutique des plantes fait partie intgrante des traditions de
toutes les cultures. La valorisation mdicinale de ces pratiques passe notamment par lisolement et
lidentification de nouvelles molcules. Dans le but de rechercher les diffrentes classes des substances
secondaires dans les extraits dAsteriscus graveolens subsp. odorus, nous avons effectu un screening
phytochimique par la mise en place dun ensemble de ractions de caractrisation de diffrents composs
chimiques savoir : les flavonodes, les saponines, les tanins, les alcalodes, les anthocyanes, les terpnes et
les composs cyanogntiques.
Cette plante constitue un patrimoine local floristique trs important qui nest en grande partie dcrit que dun
point de vue botanique, sauf quelques tudes portant sur lidentification des lactones sesquiterpniques [1] et
dautres sur lactivit antifongique des extraits de cette plante [2,3]. Le screening phytochimique, effectu pour
la premire fois, a port sur les feuilles et les fleurs des deux plantes afin didentifier le maximum de
composs phnoliques en utilisant le spectrophotomtre UV ainsi que diffrentes techniques danalyse. De plus,
une tude qualitative et quantitative (aglycones, anthocyanes et flavonodes totaux) ayant pour but principal de
dfinir les types des polyphnols existant dans les feuilles dAsteriscus graveolens subsp. odorus a t effectue.
2. Matriel et mthodes
2-1. Matriel vgtal
Les feuilles et les fleurs dAsteriscus graveolens subsp. odorus ont t rcoltes de la rgion dAgadir (Sud du
Maroc) durant le mois dAvril (2004) de manire alatoire. Cette plante a t identifie par le Professeur
Ouyahya A. l'Institut Scientifique (Rabat, Maroc). Un spcimen a t dpos l'herbier de la Facult des
Sciences dAgadir (Universit Ibn Zohr, Agadir, Maroc). Une partie du matriel vgtal a t conserve 4C
quelques heures aprs la rcolte pour lanalyse des composs cyanogntiques et pour dventuelles tudes
ultrieures. Lautre partie a t sche lombre, labri de lhumidit et stocke soigneusement. La plante a
t ensuite broye au moulin lectrique jusqu' obtention dune poudre.
2-2. Screening phytochimique et caractrisation spectroscopique des mtabolites secondaires
dAsteriscus graveolens subsp. odorus
2-2-1. Les alcalodes
La prsence des alcalodes a t mise en vidence par trois tests diffrents [4] :
Test d'Iodoplatinate : L'extrait tester est dpos sur couche mince (plaque de silice) le
chromatogramme est dvelopp dans le solvant suivant : (AcEt / MeOH / NH4OH) (9/1/1), puis sch
sous la hotte. Les bandes de migration sont repres et dlimites sous lumire UV
365nm.L'application du ractif d'Iodoplatinate par pulvrisation permet de rvler la prsence
d'alcalodes. Ceux-ci se rvlent par une couleur bleue sur le chromatogramme.
Test de Mayer : A une quantit de 0,5 g du matriel vgtal sec broy, on ajoute 15 mL dthanol
(70%) suivi dune sonication pendant 15 mn. Ensuite, les extraits sont laisss en agitation magntique
pendant toute la nuit, dcants et filtrs. L'extrait est vapor sec dans le rotavapor. Le rsidu
rcupr dans quelques mL de HCl (50%) est ensuite transvas dans deux tubes essai ; l'un est utilis
comme tmoin et l'autre on ajoute le ractif de Mayer. L'apparition de prcipit blanc traduit la
prsence des alcalodes.
Hakim ALILOU et al.
Afrique SCIENCE 10(3) (2014) 316 - 328 318
Test de Dragendorff : Il repose sur le mme principe que le test d'Iodoplatinate sauf que la
rvlation se fait par la pulvrisation au ractif de Dragendorff. La prsence d'alcalodes se rvle par
une couleur orange vive sur le chromatogramme.
2-2-2. Les coumarines
Les coumarines sont dtectes par deux tests diffrents :
Premier test : Une quantit de 2 g de matriel vgtal sec broy est plac dans 10 mL de CH 2Cl2. Le
tout est chauff pendant quelques minutes puis filtr. La migration de cette solution a t faite sur
couche mince dans le solvant : tolune /actate dthyle (93/7). Aprs un schage sous hotte ventile,
la rvlation a t faite laide de NH3 sous UV 365nm [5].
Deuxime test: On pse 1 g de matriel vgtal sec broy et on le place dans un tube essai,
couvert par du papier filtre imbib avec NaOH dilu. Le tube est ensuite plac dans un bain marie
bouillant pendant quelques minutes. Le papier filtre est ensuite examin sous lumire UV. Une
fluorescence jaune indique la prsence des coumarines [6].
2-2-3. Les saponosides
Dans un bcher, on ajoute 100 mL deau distille a une quantit de 2 g de matriel vgtal sec, puis la solution
est porte bullition pendant 30 min. Aprs refroidissement, on filtre la solution, et on ajuste le filtrat 100
mL avec de l'eau distille. Une srie de 1 10 mL de filtrat est place dans 10 tubes essai et additionne de
10 mL deau distille. Une agitation violente et horizontale a t faite pendant 15 secondes pour chaque tube.
Aprs 15 mn de repos on mesure la hauteur de mousse rsiduelle (en cm) dans chaque tube.La prsence des
saponines est indique par un indice de mousse suprieur 100. Ce dernier est calcul selon la relation (1) :
I = La hauteur de la mousse dans le 9me tube x 10/0,09 (1)
On note que Saponaria officinalis est utilise comme tmoin positif.
2-2-4. Les tanins
Une quantit de 1,5 g du matriel vgtal sec a t place dans 10 mL de mthanol 80% est agite durant 15
mn puis filtre. On ajoute quelques gouttes du chlorure ferrique (FeCl3) 1% l'extrait mthanolique dj
prpar. En prsence de tanins galliques et ellagiques, on observe une coloration bleue noire, alors qu'en
prsence de tanins catchiques cette coloration est brune verdtre [6].
2-2-5. Les terpnodes
A une quantit de 1 g du matriel vgtal broy on ajoute 5 mL d'hexane, puis une sonication pendant
quelques minutes a t faite. Aprs une agitation de 30 min et une filtration, la migration du filtrat a t
effectue sur une plaque prparative de gel de silice, le solvant utilis est le benzne. Aprs migration, la
plaque est pulvrise avec le chlorure d'antimoine puis mise l'tuve 110C pendant 10 min. Toute
fluorescence dcele aprs ce traitement prouve que le matriel test contient des terpnodes [4].
2-2-6. Les composs cyanogntiques
Une quantit de 1 g de matriel vgtal frais est mouill avec quelques gouttes de CHCl 3 dans un tube essai
o est insre une bandelette de papier filtre imprgne avec du picrate de sodium. L'ensemble est chauff
dans un bain marie 35C pendant 3 heures. Le papier vire au rouge aprs production de HCN tmoignant de la
prsence des composs cyanogntiques [7].
Hakim ALILOU et al.
319 Afrique SCIENCE 10(3) (2014) 316 - 328
2-2-7. Les quinones libres
Une quantit de 0,5 g du matriel vgtal sec est plac dans 5 mL d'ther de ptrole. Aprs quelques minutes
d'agitation, le mlange est laiss au repos pendant toute la journe. Aprs la filtration de ce mlange, il est
concentr au rotavapor. Le virage de la couleur de la phase aqueuse au jaune, rouge ou violet aprs ajout de
quelques gouttes de NaOH (1/10), tmoigne de la prsence des quinones [5].
2-2-8. Les flavonodes
2-2-8-1. Dosage des flavonodes totaux
A 1 g du matriel vgtal sec sont ajouts 100 mL de mthanol 80%. L'ensemble est agit pendant 15 mn, puis
port au sonicateur durant 15 mn. La quantification des flavonodes dans les parties ariennes par
spectrophotomtrie est ralise en mlangeant 2 mL de cet extrait mthanolique avec 100 l du ractif de
(2 aminothyl-diphnylborate (NEU) 1% dans le mthanol). La lecture des rsultats a t faite 409 nm.
L'absorption de l'extrait a t compare celle de la querctine (0,05 mg/mL) traite avec le mme ractif dans
les mmes conditions. Les flavonodes totaux sont calculs selon la formule (2) [8] :
F%= Aext 0,05 100 / Aq Cext (2)
Aext : Absorption de l'extrait, Aq: Absorption de la querctine ( concentration de 0,05 mg/mL) et Cext :
Concentration de l'extrait en mg/mL.
2-2-8-2. Extraction des aglycones et anthocyanes
- Hydrolyse acide : 2 g de poudre de matriel vgtal ont t ajouts 200 mL de HCl 2N froid, puis ports au
bain marie bouillant pendant 40 mn avec insufflation d'air et agitation rgulire toutes les 10 minutes. Aprs
refroidissement et filtration, la solution acide est transfre en ampoule dcanter. L'hydrolyse acide permet
la transformation des proanthocyannes en anthocyanes et la libration des aglycones de flavonodes de leurs
formes O-htrosidiques.
- Extraction : Elle se fait successivement [9] :
- Par l'ther thylique (2 fois 20 mL) : les composs phnoliques, sauf les anthocyanes et les C-
glucosides quittent l'hypophase acide au profit de l'piphase thre. Les extraits runis et vapors sous
hotte ventile sont repris par 10 mL d'thanol 95;
- Par le n-butanol (2 fois 20 mL) : cette phase extrait les anthocyanes et les C-glycoflavones. Ce solvant
entrane les anthocyanes colors en rouge provenant de l'oxydation des proanthocyanes.
2-2-8-3. Examen chromatographique
Aprs rcupration des aglycones par 10 mL dthanol 95 dans une fiole jauge de 10 mL, la sparation des
molcules est effectue laide dune chromatographie sur papier Whatman n1. Le solvant utilis est lacide
actique 2% qui permet la migration des acides phnols vers le front. Les chromatogrammes sont ensuite
examins sous UV (356 nm) et les bandes observes ont t entoures. La couleur des bandes sous UV est note
et le front servira pour calculer lerapport frontal (Rf).Les bandes observes sont dcoupes et lues dans le
mthanol afin de les identifier au spectrophotomtre UV-visible (HP Vectra, programme Chemstation software).
Les mesures sont effectues entre les longueurs dondes 260 et 600 nm. Quant aux flavonodes, la migration
est effectue dans lacide actique 60% pour la sparation des molcules et une chromatographie sur papier
Wattman n1 est effectue pour leur purification.
Hakim ALILOU et al.
Afrique SCIENCE 10(3) (2014) 316 - 328 320
2-2-8-4. Dosage des flavones-flavonols
Le dosage diffrentiel des flavones et flavonols est bas sur la chlation spcifique des flavonodes par les ions
Al3+. Dans la cuve de rfrence est place la solution alcoolique convenablement dilue. Dans la cuve de
mesure est place la solution alcoolique amene la mme dilution mais avec une solution alcoolique d'AlCl3
1%. Aprs 10 mn de contact, le spectre est enregistr au spectrophotomtre UV-visible entre 380 et 460 nm
pour les aglycones. La prsence des flavonols est indique par un pic entre 420 et 440 nm et celle des flavones
par un maximum d'absorption entre 390 nm et 415 nm. La hauteur du pic diffrentiel est proportionnelle la
concentration en aglycones flavoniques[10]. Ainsi la teneur en aglycones exprime comme querctine
(flavonol tmoin) est calcule selon la formule suivante :
T aglycones = (DO / ). M. V. d / p (3)
Avec : T aglycones : teneur en aglycones (en % ou en mg/g ; DO : Densit optique du pic diffrentiel;
: Coefficient d'absorption molaire de la querctine (= 23000) ; M : Masse molaire de la querctine (= 302) ;
V : Volume de la solution thanolique d'aglycones ; d : Facteur de dilution ; p : Poids sec de matriel vgtal
hydrolys.
Pour les anthocyanes, la phase aqueuse acide rsiduelle est extraite 2 fois par le n-butanol. Ce solvant entrane
les anthocyanes colors en rouge provenant de l'oxydation des proanthocyanes. Ces anthocyanes sont doss
par spectrophotomtrie entre 480 et 600 nm [9,11]. La teneur en proanthocyanes (le rendement de la
transformation des proanthocyanes en anthocyanes tant pratiquement constant dans des conditions
standardises) exprime comme procyanidine est donne par la formule suivante :
T anthocyanes = (DO / ). M. V. d / p (4)
Avec : T anthocyanes : teneur en anthocyanes (en % ou en mg/g) ; DO : Densit optique la longueur d'onde
d'absorption maximale ; : Coefficient d'absorption molaire de la cyanidine (=34700) ; M : Masse molaire de la
procyanidine (=306) ; V : Volume de la solution butanolique ; d : Facteur de dilution ; p : Poids sec de matriel
vgtal hydrolys.
2-2-8-5. Analyse par Chromatographie sur couches minces (CCM)
Nous avons utilis le papier Wathman n1 pour la sparation des aglycones flavoniques dans les solvants acide
actique 2 % et 60 %. Les flavonols et flavones sont visibles sous UV, ce qui permet d'en relever les Rf. Les
spots sont rcuprs et lus par le MeOH. Des cochromatographies avec des substances tmoins sont
ralises. Les comportements chromatographiques nots pour lidentification des molcules majoritaires des
feuilles dAsteriscus graveolens subsp. odorus sont les fluorescences visualises lil nu, aprs pulvrisation
par le NEU et sous lumire ultra violette (UV).Les relevs de Rf, ont t faits sur papier Whatman n1 et sur gel
de silice. Lidentification a ncessit une comparaison avec les donnes de la littrature.
3. Rsultats et discussion
3-1. Screening phytochimique des extraits des feuilles et des fleurs dAsteriscus graveolens
subsp. odorus
Le screening phytochimique des feuilles et des fleurs dAsteriscus graveolens subsp. odorus a montr la
prsence des alcalodes aprs les trois tests positifs de Iodoplatinate, Dragendorf et Mayer. Le mme rsultat a
t confirm pour les coumarines.
Hakim ALILOU et al.
321 Afrique SCIENCE 10(3) (2014) 316 - 328
Quant aux saponines, ils sont prsent chez les fleurs et absent chez les feuilles dAsteriscus graveolens subsp.
odorus. Le test des tanins a montr la prsence dune coloration brune verdtre, ce qui signifie que les feuilles
et les fleurs de cette plante contiennent les tanins catchiques. Pour le test des composs cyanogntiques et
en comparaison avec des extraits de graines dabricots qui sont de bons tmoins riches en composs
cyanogntiques, on a constat lapparition dune coloration rouge sur le papier filtre. Les parties de la plante
tudie sest rvl contenir ce type de composs avec des quantits variables selon lorgane analys. Le test
des terpnes a montr leurs prsence dans les feuilles et les fleurs aprs pulvrisation de la plaque CCM au
chlorure dantimoine et chauffage ltuve (110C/10 min) et obtention dune fluorescence bleue ciel. Pour les
quinones libres, le virage de la couleur au jaune de la phase aqueuse rvle la prsence de ces composs dans
les fleurs dAsteriscus graveolens subsp. odorus. Quant aux feuilles, les quinones libres ne sont pas dtectes.
Cette tude a t effectue pour la premire fois afin de prospecter les diffrents mtabolites secondaires
existants chez ces deux plantes caractrisant le Sud du Maroc. Dans des tudes antrieures, les flavonodes
jouent un rle important dans la coloration des vgtaux [5]. Ils sont utiliss dans la chimiotaxonomie vgtale
[12,13]. Ils jouent le rle des marqueurs de la maturation des fruits [14]. Les polyphnols ont aussi le rle de la
protection contre les agressions biotiques et abiotiques, de lactivit antifongique [15], de lactivit antivirale
[16], de lactivit anti-oxydante [17-19] et de lactivit anti-inflammatoire [20].La prsence des alcalodes peut
expliquer des activits biologiques diverses [21]. Quant aux terpnes, ils servent comme des additifs dans les
industries alimentaires et cosmtiques [22] et plusieurs dentre eux possdent des activits biologiques:
antimicrobienne, insecticide, anti-carcinognique, anti-inflammatoire [23], anesthsique et antihistaminique
(des mono et sesquiterpnes), diurtique (-eudesmol) [24,25], neuroprotective (-terpinne, -terpinne, et
trans-caryophyllne) [26]. On peut citer galement les proprits anti-tumorales et cytotoxiques des diterpnes
(taxol), et des activits anti-oxydantes attribues surtout aux diterpnes phnoliques [27]. La prsence des
coumarines explique leffet antifongique [28], antibactrien [29], antiviral [30], antimalarial [31], anti-
inflammatoire [20-32], anti-tumoral [33,34] et anticoagulant [35].
3-2. Dosage et caractrisation spectroscopique des flavonodes des extraits des feuilles
dAsteriscus graveolens subsp. odorus
3-2-1. Dosage des flavonodes totaux, des aglycones flavoniques et des anthocyanes
Le dosage de diffrents composs phnoliques des feuilles Asteriscus graveolens subsp. odorus a rvl une
teneur importante en aglycones flavoniques estime 3,34 mg/g. Quant aux flavonodes, elles reprsentent
uniquement 1,62 mg/g de lextrait des feuilles de cette plante. Quant aux anthocyanes, elles prsentent une
trs faible teneur.
3-2-2. Fractionnement de lextrait thr et caractrisation des acides phnols et des
flavonodes aglycones des feuilles dAsteriscus graveolens subsp. odorus
Ltude qualitative a permis de caractriser les principaux composs phnoliques des feuilles d Asteriscus
graveolens subsp. odorus. En effet, une diversit du pool phnolique a t observe. Pour cette raison, une
tude spectrophotomtrique base sur les caractristiques spectrales et chromatographiques a t ncessaire
pour lidentification des diffrentes molcules phnoliques. Deux grandes familles des composs phnoliques
ont t mises en vidence : les acides phnols et les aglycones flavoniques en utilisant les solvants : acide
actique 2% et 60%. Les analyses effectues ont montr diffrentes fluorescences sous UV correspondant
des htrosides flavoniques, entre autres les flavones et les acides phnols. En prsence des tmoins on
pourrait caractriser les fractions obtenues, et ce en comparant leur comportements chromatographiques.
Hakim ALILOU et al.
Afrique SCIENCE 10(3) (2014) 316 - 328 322
3-2-2-1. Groupe des acides phnols
Aprs une premire sparation par CCM de lextrait thr dans lacide actique 2%, les bandes ont t
dcoupes et mises dans le mthanol. Un seul compos a t isol (B1). Une chromatographie bidimensionnelle
a t ncessaire pour la vrification de la puret des fractions. Ce compos est incolore lil nu, il se prsente
sur le chromatogramme sous forme dune tache bleue sous UV, dune couleur jaune verdtre aprs
pulvrisation par le NEU, son Rf est de 0,30 et son spectre dabsorption correspond une longueur donde max
de : 234nm-298nm-325nm (Figure 1). Daprs la littrature [9, 36, 10, 12, 37], les donnes du compos B1 sont
les mmes que celle de lacide cafique (Figure 2).
Des tudes [38,39] ont montrs que le groupe des acides phnols a un rle trs important dans la pigmentation
des fleurs et des fruits et la protection des plantes contre les herbivores et les radiations UV. Dailleurs, lacide
cafique est connu pour son grand pouvoir antifongique [40]. Dautres auteures [41,42] ont montr que les
phnols simples et les acides phnoliques possdent des proprits anti-inflammatoires et antihmorragiques,
des proprits antibactriennes et antifongiques, en particulier lgard des organismes phytopathognes.
325
298
1.2
234
1
A bs or banc e ( A U)
0.8
0.6
263
0.4
0.2
430
485
250 300 350 400 450 500 Wavelength (nm)
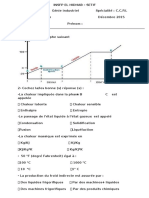
Figure 1: Spectre dabsorption du compos B1 isol de lextrait dAsteriscusgraveolenssubsp. Odorus
Figure 2 : Structure de lacide cafique
Hakim ALILOU et al.
323 Afrique SCIENCE 10(3) (2014) 316 - 328
3-2-2-2. Groupe des aglycones flavoniques
Dans notre tude, la purification des aglycones flavoniques sur papier Whatman n1 en utilisant comme solvant de
migration : lacide actique 60%nous a permis disoler diffrentes molcules. Ainsi, en comparant leurs diffrentes
proprits physiques et spectroscopiques avec celles de la littrature, nous avons pu identifier trois flavones. La
bande B1 correspondrait la nvadensine (Figure 3) avec une longueur donde de max : 286nm-328nm
(Figure 4), incolore lil nu, de couleur mauve sous UV et un Rf= 0,74. La bande B2 correspondrait la lutoline
(Figure 5) avec une longueur donde de max : 254nm-267nm-347nm (Figure 6), incolore lil nu, de couleur
brune fonce sous UV et un Rf= 0,59. Quant la bande B3, il reprsenterait lartemtine (Figure 7) avec un
max : 274nm-339nm (Figure 8), de couleur jaune claire lil nu et brune sous UV et un Rf= 0,69. Des CCM
bidimensionnelles ont montr que les bandes migrent en un seul spot : les molcules sont supposes tre pures. On
note que les feuilles dAsteriscus graveolens subsp. odorus sont dpourvues des proanthocyanes. Cela est confirm
par labsence de cette famille des composs secondaires lors du dosage de cette plante par le spectrophotomtre UV.
Figure 3 : Structure de nvadensine (5,7-dihydroxy-6,8,4'-mthoxy)
0.8
286
328
0.7
A bs or banc e ( A U)
308
0.6
0.5
261
0.4
0.3
0.2
0.1
487
250 300 350 400 450 500 Wavelength (nm)
Figure 4 : Spectre dabsorption du compos B1 de lextrait Asteriscus graveolens subsp. Odorus
Hakim ALILOU et al.
Afrique SCIENCE 10(3) (2014) 316 - 328 324
Figure 5 : Structure de lutoline (Ttr-5,7,3',4'-hydroxy-3',4',5'-mthoxy)
2.25
2
347
254
1.75
A bs or banc e ( A U)
267
1.5
1.25
1
0.75
0.5
0.25
588
578
582
0
250 300 350 400 450 500 Wavelength (nm)
Figure 6 : Spectre dabsorption du compos B2 de lextrait dAsteriscus graveolens subsp. Odorus
Figure 7 : Structure dartemtine (5-hydroxy-3,3',4',6,7-pentamethoxy)
Hakim ALILOU et al.
325 Afrique SCIENCE 10(3) (2014) 316 - 328
0.16
0.14
A bs or banc e ( A U)
0.12
0.1
274
339
0.08
0.06
0.04
581
583
590
0.02
488
0
250 300 350 400 450 500 Wavelength (nm)
Figure 8 : Spectre dabsorption du compos B3 de lextrait dAsteriscus graveolens subsp. odorus
Daprs la littrature, la lutoline est une substance antibactrienne importante [43] et elle pourrait aussi tre
responsable de leffet antioxydant [44]. Elle est reconnue aussi pour sa capacit de stimuler certaines hormones
estrognes [45], dinhiber la croissance des cellules cancreuses [46] et la tumorognse [47] et galement de
piger laction nocive des radicaux libre au niveau de lADN [49]. Quant la nvadensine, elle prsente aussi
une large activit biologique. En effet, elle a t connue par son activit antioxydante [49], antitumorale [50],
anticancereuse, antiinflammatoire [51], Hypotensive [52] et antimicrobienne [53]. Pour lartemtine, une tude
prsente par [54] a montr que cette molcule isole de Cordiacurassavica (Boraginaceae) et teste chez les
souris mles, presente une importante activit antieodematogenique.
4. Conclusion
Malgr limportance biologique et mdicinale dAsteriscus graveolens subsp. odorus, cette espce nest
auparavant t tudies que du point de vue botanique et cologique. Pourtant, la prsente tude a dmontr
la grande richesse de la plante en polyphnols, produits naturels intrt considrable dans le domaine
pharmacologique. Ce travail apporte, donc, une contribution phytochimique la connaissance dAsteriscus
graveolens subsp. odorus et permet ainsi, de mieux comprendre les proprits pharmacodynamiques des
extraits de cette plante. Il serait, donc, trs intressant dexploiter ces extraits pour la recherche de leurs
principes actifs, responsables de leurs proprits pharmacologiques.Le screening phytochimique a montr la
prsence des alcalodes, des coumarines, des tanins, des terpnes et des composs cyanogntiques. En outre,
les saponines et les quinones libres sont prsentes chez les fleurs et absentes chez les feuilles dAsteriscus
graveolens subsp. odorus. Quant ltude spectrophotomtrique de la fraction thre, elle nous a permis
didentifier les diffrents composs phytochimiques savoir : un acide phnol (acide cafique) et trois flavones
(nvadensine, lutoline et artemtine) chez les feuilles dAsteriscus graveolens subsp. odorus.
Hakim ALILOU et al.
Afrique SCIENCE 10(3) (2014) 316 - 328 326
Rfrences
[1] - H. Akssira, F. Mellouki, A. Salhi, H. Alilou, A. Saouf, F. El Hanbali, J. F. Arteaga et AF. Barrero,
Naupliolide, a sesquiterpene lactone with a novel tetracyclic skeleton from Nauplius graveolens
subsp. odorus, Tetrahedron Letters, 47, (2006) 6719-6721.
[2] - H. Alilou, J. Talbi et L. M. Idrissi Hassani, Activit antifongique des extraits de quatre plantes du Sud du
Maroc : Asteriscus imbricatum (CAV.) DC., Asteriscus graveolens subsp. Odorus (Schousb.) Greuter,
Cladanthus arabicus (L.) Cass. et Kleinia antheuphorbium (L.) Haw. Science Lib, 5, (2013) 1-9.
[3] - H. Alilou, R. Rouhi, L. M. Idrissi Hassani et M. Akssira, Activit antifongique de Bubonium odorum
(Asteraces) sur des champignons pathognes d'agrumes, Reviews in Biology and Biotechnology.,
6(1), (2007) 20-24.
[4] - K. Randerath, Chromatographie sur couches minces, Paris : dition Gauthier-Villars, (1971) 337-339.
[5] - J. Ribreau-Gayon et E. Peynaud, Les composs phnoliques des vgtaux, Trait dnologie, Paris
: dition Dunod, (1968) 254 p.
[6] - A. M. Rizk, Constituents of plants growing in Qatar, Fitoterapia, 52 (2), (1982) 35-42.
[7] - M. A. Al-Yahya, Phytochemical studies of the plants used in traditional medicine of Saudi Arabia.
Fitoterapia, 57 (3), (1986) 179-182.
[8] - E. B. Hariri, G. Salleet, C. Andary, Involvement of flavonoids in the resistance of two poplar
cultivars to mistletoe (Viscum album L.), Protoplasma, 162, (1991) 20-26.
[9] - P. H. Lebreton, M. Jay, B. Voirin et M. P. Bouchez, Sur lanalyse qualitative et quantitative des
flavondes, Chim. Anal, Fr., 49, (1967) 175-383.
[10] - M. Jay, J. F. Gonnet, E. Wollenweber et B. Voirin, Sur lanalyse qualitative des aglycones
flavoniques dans une optique chimiotaxinomique, Phytochemistry., 14, (1975) 1605-1612.
[11] - N. Porter, Essential oils and their production, Crop et Food Research, (2001) 39.
[12] - L. M. Idrissi Hassani, Etude de la variabilit flavonique chez deux conifres mditerranennes : Le
pin maritime Pinus pinaster Ait. et le genvrier thurifire Juniperus thurifera L, Thse de Doctorat
de 3 cycle, Universit Claude Bernard Lyon I, France, (1985) 171 p.
[13] - P. Lebreton et G. Meneret, Elements de chimiotaxonomie bonatique. I. Gnralits ; notion despce
biochimique ; cas des flavonoides chez Humuluslupulus, L Bull. Soc. Bot., 111, (1964) 70-80.
[14] - J. J. Macheix et A. Fleuriet, Phenolics in fruit products: progress and prospects in Polyphenolic
Phenomena, Ed. A. Scalbert, INRA Paris, (1993) 157-163.
[15] - Q. Kanwal, I. Hussain, H. Latif Siddiqui et A. Javaid, Antifungal activity of flavonoids isolated from
mango (Mangifera indica L.) leaves. Nat Prod Res., 24(20), (2010) 1907-14.
[16] - K. Ono, H. Nakane, M. Fukushima, JC. Chermann et F. Barre-sinoussi, Differential inhibitory effects
of various flavonoids on the activities of reverses transcriptase and cellular DNA and RNA
polymerases, Eur. J. Biochem., 190, (1990) 469-476.
[17] - A. K. Rahmat, Evaluation of flavonoids and diverse antioxidant activities of Sonchus arvensis,
Chemistry Central Journal., (2012), 6:126.
[18] - MC. Silva et SR. Paiva, Antioxidant activity and flavonoid content of Clusia fluminensis Planch. &
Triana. An Acad Bras Cienc., 84(3), (2012) 609-16.
[19] - N. Amessis-Ouchemoukh, I. M. Abu-Reidah, R. Quirantes-Pin, K. Madani, et A. Segura-Carretero.
Phytochemical profiling, in vitro evaluation of total phenolic contents and antioxidant properties of
Marrubium vulgare (horehound) leaves of plants growing in Algeria, Industrial Crops and Products.,
61, (2014) 120-129.
[20] - A. Hiermann, H. W. Schramm et S. Laufer, Antiinflammatory activity of myricitin-3-o-beta-D-
glucuronide and related compounds, Inflamm. Res., 47, (1998) 421-427.
Hakim ALILOU et al.
327 Afrique SCIENCE 10(3) (2014) 316 - 328
[21] - R. Milcent etF. Chau, Chimie organique htrocyclique : Structure fondamentale, chimie et biochimie
des principaux composs naturels, (2003) EDP sciences.
[22] - R. Tsao et J. R. Coats, Starting from nature to make better insecticides. Chemtech., 25, (1995) 23-28.
[23] - A. Murakami, T. Tanaka, J. Y. Lee, Y. J. Surch, H. W.Kim, K. Kawabata, Y.Akamura, S. Jiwajinda et H.
Ohigashi, Zerumbone, a sesquiterpene en subtropical ginger, suppresses skin tumor initiation and
promotion stages in ICR mice, International journal of cancer., 110, (2004) 481-490.
[24] - A. S. Velickovic, M. S. Ristic, D. T.Velickovic, S.Ilic et N. D.Mitic, The possibilities of the application of
some species of sage (Salvia L.) as auxiliaries in the treatmentof some diseases, J.Serb. Chem.
Soc., 68 (6), (2003) 435-445.
[25] - Y. D. Hsiou, W.Yang-ch et L. Hang-ch, Journal of the Chinese Chemical Society., 47, (2000) 561-566.
[26] - J. Hyun, J. K. Hyun et S. C.Hyang, Quntitative structure activity relationship (QSAR) for
neuroprotective activity of terpenoids, Life Sciences., 80, (2007) 835-841.
[27] - R. A. Hill, In the chemistry of natural products, 2nd edition (Ed.R.H.Thomson), Blackie, Glasgow.,
(1993) 124 p.
[28] - N. Kandaswamy et N. Raveendiran, Synthesis, Characterization and Antifungal activity of Coumarin
based random copolyester, American Journal of Research, 4 (3), (2014) 704-707.
[29] - A. B. Mashooq, M. A. Al-Omar et N. Siddiqui, Antimicrobial activity of Schiff bases of coumarin-
incorporated 1,3,4-oxadiazole derivatives: an in vitro evaluation, Medicinal Chemistry Research.,
22 (9) (2013) 4455-4458.
[30] - R. W. Fuller, H. R. Bokesch, K. R. Gustafson, T. C. Mckee, J. H. Cradellina, J. B. Mcmhon, G. M. Cragg,
D. Sojaerto et M. R. Boyd, Bioorg. Med. Chem. Lett., 4 (16), (1994) 1961-1964.
[31] - Y. Z. Yang, A.Ranz, H. Z. Pan, Z. N. Zhang, X. B. Lin et S. R.Meshnich, Daphnetin : a novel
antimalarial agent with in vitro and in vivo activity, Am. J. Trop. Med. Hyg., 46 (1), (1992) 15-20.
[32] - A. N. Garcia-argaez, T. O. R. Apan, HP. Delgado, G. Velazquez et M. Martinez-Vazquez,
PlantaMedica., 66, (2000) 279-281.
[33] - C. Kofinas, I.Chinou, A.Loukis, C.Harvala, C.Roussakis, M. Maillard et K.Hostettmann, Cytotoxic
coumarins from the aerial parts of Tordyliumapulum and their effects on a non-small-cell bronchial
carcinoma line, Planta Medica., 64, (1998) 174-176.
[34] - T. Fujioka, K. Furumi, H. Fujii, K. Mihashi, Y. Nakano, H. Matsunaga, M. Ktano et M. Mori,
Antiproliferative constituents from Umbelliferae plants. V. A new furanocoumarin and
falcarindiolfuranocoumarin ethers from the root of Angelica japonica, Chem. Pharm. Bull., 47(1),
(1999) 96-100.
[35] - D. Egan, R. Okennedy, E. Moran, D. Cox, E. Prosser et D. Thornes, Drug. Metabolism Reviews., 22
(5), (1990) 503-529.
[36] - B. Voirin, UV spectral differentiation of 5-hydroxy and 3-mythoxyflavones with mono-(4), di-(3, 4)
or tri-(3, 4, 5)-substitued rings, Phytochemistry., 22 (10), (1983) 2107-2145.
[37] - D. Touati, Contribution la connaissance du profil biochimique des dicotyldones buissonnantes et
arbustives de mditerrane. Thse de Doctorat de troisime cycle, Universit Claude Bernard, Lyon
I, (1985) 155 p.
[38] - S. F. Asad, S. Singh, A. Ahmad etS. M.Hadi, Flavonoids : antioxidants in diet and potentiel anticancer
agents,Medical Science Research., 26, (1998) 273-728.
[39] - G. Di Carlo, N. Mascolo, A. A. Izzo et F. Capasso, Flavonoids : old and new aspects of class of
natural therapeitic drugs, Life Sciences., 65, (1999) 337-353.
[40] - M. M. Cowan, Plants products as antimicrobial agents, Clinical Microbiology Reviews., 12 (4), (1999)
564-582.
[41] - J. Bruneton, Pharmacognosie, phytochimie, plantes mdicinales, 3me Edition, Editeur technique et
Hakim ALILOU et al.
Afrique SCIENCE 10(3) (2014) 316 - 328 328
documentation, Paris, (1999) 1120 p.
[42] - V. A. Kurkin, Phenylpropanoids from medicinal plants: distribution, classification, structural
analysis, and biological activity. Chemistry of Natural Compounds., (2003) 39 (2).
[43] - Q.Wang, M. Xie, Antibacterial activity and mechanism of luteolin on Staphylococcus aureus. Acta
Microbiologica Sinica., 50(9), (2010) 1180-4.
[44] - YC. Zhang, FF. Gan, SB. Shelar, KY. Ng et EH. Chew, Antioxidant and Nrf2 inducing activities of
luteolin, a flavonoid constituent in Ixeris sonchifolia Hance, provide neuroprotective effects against
ischemia-induced cellular injury. Food Chem Toxicol., 59, (2013) 272-80.
[45] - R. S. Zand, D. J. A. Jenkins et E. Diamandis, Steroid hormone activity of flavonoids and related
compounds. Breast Cancer Res. Treat., 62, (2000) 35-49.
[46] - Y. Matsukawa, N. Marui, T. Sakai, Y. Satomi, M. Yoshida et K. Matsumoto, Genistein arrests cell
cycle progression at G2-M, Cancer Res., 53, (1993) 1328-1331.
[47] - V. Elangovan, N.Sekar, S.Govindasamy, Chemopreventive potential of dietary bioflavonoids against
20-methylcholanthrene-induced tumorigenesis. Cancer Lett., 87, (1994) 107-113.
[48] - C. Qiuyin, O. R. Ronald et Z. Ruiwen, Dietary flavonoids, quercetin, luteolin and genistein, reduce oxidative
DNA damage and lipid peroxidation and quench free radicals, Cancer Lett., 119, (1997) 99-107.
[49] - S. Ganapaty, V. M.Chandrashekhar, H. R.Chitme et M.LakashmiNarsu, Free radical scavenging activity
of gossypin and nevadensin : An in vitro evaluation, Indian J Pharmacol., 39 (6), (2008) 281-283.
[50] - C. J. Chung et R. L.Geahlen, Protein-tyrosine kinase inhibition: Mexchanism-based discovery of
antitumor agents, J Nat Prod., 55, (1992) 1529-1560.
[51] - G. B. Reddy, A. B.Melkhani, G. A.Kalyani, J. V.Rao, A. Shirwaikar et M. Kotian, Chemical and
pharmacological investigation of Limnophila conferta and Limnophila heterophylla, Int J
Pharmacog., 29, (1991) 145-53.
[52] - J. Y. Song, X. Z. He, X. F. Chen, J. Y. Hu, G. Y. Luo et Y. Z. Mo, Hypotensive effect of nevadensin, Acta
Pharmacol Sin., 6, (1985) 99-102.
[53] - G. Brahmachari, Limnophila (Scrophulariaceae): Chemical and pharmaceutical aspects, Open Nat
Prod J., 1, (2008) 34-43.
[54] - M. C. Bayeux, A. T. Fernandes, M. A. Foglio et J. E. Carvalho, Evaluation of the antiedematogenic
activity of artemetin isolated from Cordiacurassavica DC, Brazilian Journal of Medical and
Biological Research., 35, (2002) 1229-1232.
Hakim ALILOU et al.
Você também pode gostar
- Le Jardin Du CroyantDocumento153 páginasLe Jardin Du CroyantLegendaryManAinda não há avaliações
- Cours Botanique NomenclatureDocumento23 páginasCours Botanique NomenclaturePaul FatheadAinda não há avaliações
- TSTL - Bioch.Cours .Chap.4.Metabolisme.I.Le - Metabolisme.energetiqueDocumento8 páginasTSTL - Bioch.Cours .Chap.4.Metabolisme.I.Le - Metabolisme.energetiquekotobindenie0% (1)
- BiocatalyseDocumento23 páginasBiocatalysemohamed benlaragueAinda não há avaliações
- Technologies de L'énergie Propre, Moins Connues, Faible Coût, Et Liées À L'évolution Des ApplicationsDocumento388 páginasTechnologies de L'énergie Propre, Moins Connues, Faible Coût, Et Liées À L'évolution Des ApplicationsBen RusuisiakAinda não há avaliações
- Rapport BroyageDocumento59 páginasRapport BroyageIhsan Afriad75% (4)
- Polyphénols Et Antioxydants de Graines de Voandzou (Vigna Subterranea)Documento11 páginasPolyphénols Et Antioxydants de Graines de Voandzou (Vigna Subterranea)univouaga100% (2)
- Screening PhytochimiqueDocumento15 páginasScreening PhytochimiqueMissimawu Houessionon Jr.Ainda não há avaliações
- Des Plantes À L'agricultureDocumento0 páginaDes Plantes À L'agriculturemekaekAinda não há avaliações
- Defenses Des Vegetaux Contre Les Facteurs AbiotiquesDocumento43 páginasDefenses Des Vegetaux Contre Les Facteurs Abiotiquesmekaek50% (2)
- Plantes Et Chpg. ToxiquesDocumento52 páginasPlantes Et Chpg. ToxiquesAnwar SalamaAinda não há avaliações
- Plantes Emmenagogues en Cote D'ivoireDocumento23 páginasPlantes Emmenagogues en Cote D'ivoirepenseesauvageAinda não há avaliações
- Les Plantes Et L EauDocumento49 páginasLes Plantes Et L Eaulile aichaAinda não há avaliações
- These: République Algérienne Démocratique Et PopulaireDocumento109 páginasThese: République Algérienne Démocratique Et PopulaireLÿ DîeAinda não há avaliações
- Etude Phytochimique Et Evaluation de L'activité Antioxydante de Romarin (Rosmarinus Officinalis)Documento85 páginasEtude Phytochimique Et Evaluation de L'activité Antioxydante de Romarin (Rosmarinus Officinalis)Rou MaissaAinda não há avaliações
- Activité AntimicrobienneDocumento18 páginasActivité Antimicrobiennekhitriwalid100% (1)
- Lutte Biologique Intégrée: Plaquette de Présentation (Aficar)Documento2 páginasLutte Biologique Intégrée: Plaquette de Présentation (Aficar)benefred100% (1)
- Etude de L'importance de La Mycorhization Dans La Synthèse Des Composés Phénoliques Chez Le Maïs en Condition de Stress HydriqueDocumento7 páginasEtude de L'importance de La Mycorhization Dans La Synthèse Des Composés Phénoliques Chez Le Maïs en Condition de Stress HydriqueinventyAinda não há avaliações
- Programme Scientifique Congrès CISNEM Taza 2014Documento36 páginasProgramme Scientifique Congrès CISNEM Taza 2014Reda RraaAinda não há avaliações
- Atlas Des Plantes de France T2Documento203 páginasAtlas Des Plantes de France T2albundAinda não há avaliações
- Etude Activite Biologie Extrait Fruit PDFDocumento88 páginasEtude Activite Biologie Extrait Fruit PDFalphonse1988100% (1)
- These de Doctorat Unique: OBAME ENGONGA Louis ClémentDocumento277 páginasThese de Doctorat Unique: OBAME ENGONGA Louis ClémentSoussou PerlaAinda não há avaliações
- PharmacognosieDocumento29 páginasPharmacognosieLatifa HammadAinda não há avaliações
- Tableaux de PlantesDocumento1 páginaTableaux de Plantesiteration615Ainda não há avaliações
- Mesurer La Capacite AntioxydanteDocumento1 páginaMesurer La Capacite AntioxydanteJasmine BioAinda não há avaliações
- Téchnique D'extrac Et Dosage Des PolyphénolsDocumento5 páginasTéchnique D'extrac Et Dosage Des Polyphénolsdj48100% (2)
- 2 RemerciementDocumento30 páginas2 RemerciementChawki MokademAinda não há avaliações
- Schleiermacher Le Projet D Une Hermeneutique Materielle 1Documento13 páginasSchleiermacher Le Projet D Une Hermeneutique Materielle 1flapinniAinda não há avaliações
- Propriétés Antioxydantes de L'huile Essentielle Des FeuillesDocumento5 páginasPropriétés Antioxydantes de L'huile Essentielle Des FeuillesmekaekAinda não há avaliações
- Livre Physio 2023Documento49 páginasLivre Physio 2023talakibadebalaki56Ainda não há avaliações
- Biologie Vegetale-2Documento18 páginasBiologie Vegetale-2Carely AngelAinda não há avaliações
- Les Plantes M2dicinale PDFDocumento115 páginasLes Plantes M2dicinale PDFemmanuel drogonAinda não há avaliações
- Les Plantes Endémiques Médicinales en AlgérieDocumento127 páginasLes Plantes Endémiques Médicinales en AlgérieKhamed OussamaAinda não há avaliações
- Biodiversité Et Valeur Des Plantes Médicinales Dans La Phytothérapie Cas de La Région deDocumento95 páginasBiodiversité Et Valeur Des Plantes Médicinales Dans La Phytothérapie Cas de La Région dekasouana_40254947Ainda não há avaliações
- Evaluation de La Contamination Microbienne Des Smartphones Et Efficacité Des Techniques Courantes de Désinfection Synthése BibliographiqueDocumento91 páginasEvaluation de La Contamination Microbienne Des Smartphones Et Efficacité Des Techniques Courantes de Désinfection Synthése BibliographiqueOmar ZouguaghAinda não há avaliações
- OliveDocumento35 páginasOliveclauclau7Ainda não há avaliações
- Organographie Végétale, Appareil Reproducteur (Fruits, Sans Coordonnées), 2021-2022Documento51 páginasOrganographie Végétale, Appareil Reproducteur (Fruits, Sans Coordonnées), 2021-2022hughAinda não há avaliações
- Caractérisation Et Comparaison Du Contenu PolyphénoliqueDocumento116 páginasCaractérisation Et Comparaison Du Contenu PolyphénoliqueSabrin Amani50% (2)
- Le Danger Des PlantesDocumento24 páginasLe Danger Des PlantesMichael DorsanAinda não há avaliações
- Akr 4668Documento97 páginasAkr 4668Jojo JolieAinda não há avaliações
- Screening Phytochimique Etude ToxicologiDocumento23 páginasScreening Phytochimique Etude ToxicologiEL Hassania EL HERRADIAinda não há avaliações
- MycorhizesDocumento67 páginasMycorhizesMáñ ØûAinda não há avaliações
- Botanique: Corrigé Du Devoir N°5Documento12 páginasBotanique: Corrigé Du Devoir N°5Fraust Kashuki BokekAinda não há avaliações
- RosidéesDocumento8 páginasRosidéesعبد الله0% (1)
- Propriétés Thérapeutiques Des Plantes À Tanins Du Burkina FasoPlantes À Tanin Du Burkina FaasoDocumento9 páginasPropriétés Thérapeutiques Des Plantes À Tanins Du Burkina FasoPlantes À Tanin Du Burkina Faasounivouaga100% (1)
- Ovules, Forme GaléniqueDocumento14 páginasOvules, Forme GaléniqueMohamed Taieb BakoucheAinda não há avaliações
- 284 - Enscm - 2012 - Nguemtchouin Mbouga PDFDocumento293 páginas284 - Enscm - 2012 - Nguemtchouin Mbouga PDFDjamel AnteurAinda não há avaliações
- Drogues A Huiles EssentiellesDocumento34 páginasDrogues A Huiles EssentiellesAicha MrizigAinda não há avaliações
- Abts DPPH PDFDocumento68 páginasAbts DPPH PDFSiham OurouadiAinda não há avaliações
- Cours de PhytosociologieDocumento23 páginasCours de PhytosociologieXaviers SHOMARIAinda não há avaliações
- Drogues À SaponosidesDocumento10 páginasDrogues À SaponosidesKomla Edem Dieudonné AdjonyoAinda não há avaliações
- Les PtéridophytesDocumento7 páginasLes Ptéridophytesعلى الله متوكلAinda não há avaliações
- Stress Hydrique EdeeDocumento114 páginasStress Hydrique Edeekhiati asmaAinda não há avaliações
- BotaniqueDocumento4 páginasBotaniqueHtnb0Ainda não há avaliações
- Formation Botanique 2012 - Pples Familles PDFDocumento14 páginasFormation Botanique 2012 - Pples Familles PDFRADIDADIAinda não há avaliações
- Cours 1 Historique de L'amélioration Des PlantesDocumento5 páginasCours 1 Historique de L'amélioration Des PlantesButter FlyAinda não há avaliações
- Le guide de la flore de Tlemcen (Algérie): Tome IINo EverandLe guide de la flore de Tlemcen (Algérie): Tome IIAinda não há avaliações
- Développement végétal: Les Grands Articles d'UniversalisNo EverandDéveloppement végétal: Les Grands Articles d'UniversalisAinda não há avaliações
- Directives d’application volontaire pour la conservation et l’utilisation durable des variétés des agriculteurs/variétés localesNo EverandDirectives d’application volontaire pour la conservation et l’utilisation durable des variétés des agriculteurs/variétés localesAinda não há avaliações
- Déserts: Les Grands Articles d'UniversalisNo EverandDéserts: Les Grands Articles d'UniversalisAinda não há avaliações
- Polymorphisme en biologie: Les Grands Articles d'UniversalisNo EverandPolymorphisme en biologie: Les Grands Articles d'UniversalisAinda não há avaliações
- Toxicologie Alimentaire Controle de Qualité S1Documento11 páginasToxicologie Alimentaire Controle de Qualité S1HarounBio-technologie67% (3)
- Protocole Effet InhibiteurDocumento9 páginasProtocole Effet InhibiteurHarounBio-technologieAinda não há avaliações
- Guide LMDDocumento72 páginasGuide LMDKarim Kemih100% (1)
- Examen ToxicologieDocumento2 páginasExamen ToxicologieHarounBio-technologieAinda não há avaliações
- Examen Suynthèse Juin 2015Documento2 páginasExamen Suynthèse Juin 2015HarounBio-technologieAinda não há avaliações
- Corrigé ToxicologieDocumento1 páginaCorrigé ToxicologieHarounBio-technologieAinda não há avaliações
- Avant ProjetDocumento6 páginasAvant ProjetHafidElgraaAinda não há avaliações
- Nutrition NutrimentsDocumento23 páginasNutrition NutrimentsHarounBio-technologieAinda não há avaliações
- Contrôles Des Corps GrasDocumento11 páginasContrôles Des Corps GrasHarounBio-technologie100% (1)
- Economie Politique 2009-2010Documento1 páginaEconomie Politique 2009-2010HarounBio-technologieAinda não há avaliações
- Controles Divers NutritionDocumento12 páginasControles Divers NutritionHarounBio-technologieAinda não há avaliações
- Cursus Des Modules INATAADocumento3 páginasCursus Des Modules INATAAHarounBio-technologieAinda não há avaliações
- Cours - Zoologie Générale 2009-2010Documento49 páginasCours - Zoologie Générale 2009-2010HarounBio-technologieAinda não há avaliações
- Cours - Physiologie Animale 2009-2010Documento39 páginasCours - Physiologie Animale 2009-2010HarounBio-technologie100% (2)
- Les Hépatites Virales Chroniques Et La NutritionDocumento11 páginasLes Hépatites Virales Chroniques Et La NutritionHarounBio-technologieAinda não há avaliações
- Convention de FormationDocumento11 páginasConvention de FormationHarounBio-technologieAinda não há avaliações
- Béjaia Rachitisme Carentiel (Cours S5)Documento44 páginasBéjaia Rachitisme Carentiel (Cours S5)HarounBio-technologie100% (2)
- Appréciation de Deux Variétés de BLEDocumento66 páginasAppréciation de Deux Variétés de BLEHarounBio-technologieAinda não há avaliações
- Techniques D'EchantillonnageDocumento19 páginasTechniques D'EchantillonnageHarounBio-technologieAinda não há avaliações
- Achat de FormationDocumento8 páginasAchat de FormationHarounBio-technologieAinda não há avaliações
- Examen HodnaDocumento2 páginasExamen HodnaHarounBio-technologieAinda não há avaliações
- Cours Contrôle Des Sucres, Des Produits Sucrés Et Du Miel 2011Documento4 páginasCours Contrôle Des Sucres, Des Produits Sucrés Et Du Miel 2011HarounBio-technologie100% (2)
- Aspects EnvironnementauxDocumento25 páginasAspects EnvironnementauxHarounBio-technologieAinda não há avaliações
- Chapitre 1 Generalité Sur Le LaitDocumento6 páginasChapitre 1 Generalité Sur Le LaitHarounBio-technologie100% (2)
- HH - Malinf Infnoso Epidemio PDFDocumento37 páginasHH - Malinf Infnoso Epidemio PDFAlina BraisAinda não há avaliações
- BoissonsDocumento44 páginasBoissonsHarounBio-technologie100% (1)
- Code TravailDocumento294 páginasCode TravailHakim Maacha100% (2)
- Coagulation FloculationDocumento8 páginasCoagulation FloculationHarounBio-technologieAinda não há avaliações
- 04 Annabel Bourde PDFDocumento21 páginas04 Annabel Bourde PDFAmine LoyalAinda não há avaliações
- Mod4 Corrige ch8 Partie2Documento8 páginasMod4 Corrige ch8 Partie2api-278378684100% (1)
- Application Des Méthodes Expérimentales Dans Des Structures en B.ADocumento25 páginasApplication Des Méthodes Expérimentales Dans Des Structures en B.ANazim KASSABAinda não há avaliações
- 32examen National Physique Chimie Sciences Maths 2018 Rattrapage CorrigeDocumento4 páginas32examen National Physique Chimie Sciences Maths 2018 Rattrapage CorrigeAssia OunkhirAinda não há avaliações
- TD 3 Et CorrectionDocumento10 páginasTD 3 Et CorrectionCǿêûr Ðê PîirâtêAinda não há avaliações
- Leçon N6 Reactions Les Solutions Avec Les MetauxDocumento3 páginasLeçon N6 Reactions Les Solutions Avec Les MetauxAgnaou MohamedAinda não há avaliações
- EFFICACITE ENERGETIQUE - Processus de Fabrication de Sucre (La Cosumar)Documento21 páginasEFFICACITE ENERGETIQUE - Processus de Fabrication de Sucre (La Cosumar)Abdellah Samadi100% (3)
- Freitapox SR 215 NFDocumento2 páginasFreitapox SR 215 NFmarine MAinda não há avaliações
- Aniosyme Pla IiDocumento8 páginasAniosyme Pla IiAbdelAinda não há avaliações
- Analyse TGADocumento20 páginasAnalyse TGAzhor El hallaoui100% (1)
- N2016SM PDFDocumento8 páginasN2016SM PDFmjidooooAinda não há avaliações
- T1 C1A2 COURS Evolution AtmosphèreDocumento1 páginaT1 C1A2 COURS Evolution AtmosphèresimousseeAinda não há avaliações
- Chap 1Documento15 páginasChap 1Anonymous f5yW3N0jSAinda não há avaliações
- MANSOURI Fatima-Converti - 3Documento97 páginasMANSOURI Fatima-Converti - 3Ouail gueAinda não há avaliações
- Biology Paper 1 TZ1 HLDocumento16 páginasBiology Paper 1 TZ1 HLyara hazemAinda não há avaliações
- Ads TPDocumento6 páginasAds TPcélia ferAinda não há avaliações
- Devoir de Synthèse N°1 - Sciences Physiques - 3ème Mathématiques (2015-2016) Mme Grissa HafidhaDocumento3 páginasDevoir de Synthèse N°1 - Sciences Physiques - 3ème Mathématiques (2015-2016) Mme Grissa HafidhaaliAinda não há avaliações
- 10 SD FRDocumento4 páginas10 SD FRabbes ben hemanaAinda não há avaliações
- BP Chap2 PDFDocumento15 páginasBP Chap2 PDFHamedGamaounAinda não há avaliações
- TDPermDocumento4 páginasTDPermAmine HeddoubAinda não há avaliações
- Criteres D'acceptation API 1104Documento1 páginaCriteres D'acceptation API 1104Had Rayane100% (2)
- Fup FRDocumento16 páginasFup FRMohamed ChelfatAinda não há avaliações
- Les Structures PoreusesDocumento9 páginasLes Structures PoreusesSeddik hAinda não há avaliações
- Extraction Solide Liquide Sur Pilote de GraineDocumento78 páginasExtraction Solide Liquide Sur Pilote de GraineMaryem Ben SalemAinda não há avaliações
- Chapitre 2-0-Pliage Des TolesDocumento32 páginasChapitre 2-0-Pliage Des TolesHamza Liberados80% (5)
- Mémo Thermochimie Chap 1 MP 22Documento3 páginasMémo Thermochimie Chap 1 MP 22emilian ghaniAinda não há avaliações
- Amelioration de La Disponibili - Safae JTITE - 4630Documento151 páginasAmelioration de La Disponibili - Safae JTITE - 4630Zineddine El Mehdi MustaphaAinda não há avaliações
- Exp RaffinageDocumento15 páginasExp RaffinageNøü ĐaAinda não há avaliações
- La Gaine de Câble À Fibre Optique ++++Documento1 páginaLa Gaine de Câble À Fibre Optique ++++Abdelhamid SammoudiAinda não há avaliações