Escolar Documentos
Profissional Documentos
Cultura Documentos
Aulão Gabriel
Enviado por
Gabriel MessiasDireitos autorais
Formatos disponíveis
Compartilhar este documento
Compartilhar ou incorporar documento
Você considera este documento útil?
Este conteúdo é inapropriado?
Denunciar este documentoDireitos autorais:
Formatos disponíveis
Aulão Gabriel
Enviado por
Gabriel MessiasDireitos autorais:
Formatos disponíveis
QUESTES segundo ano
01) - (UFSC)A gua potvel proveniente de estaes de tratamento resulta de um conjunto de
procedimentos fsicos e qumicos que so aplicados na gua para que esta fique em condies
adequadas para o consumo. Esta separao necessria uma vez que a gua de rios ou lagoas
apresenta muitos resduos slidos, por isso tem que passar por uma srie de etapas para que esses
resduos sejam removidos. Neste processo de tratamento a gua fica livre tambm de qualquer tipo
de contaminao, evitando a transmisso de doenas.
Em uma ETA (estao de tratamento de gua) tpica, a gua passa pelas seguintes etapas:
coagulao, floculao, decantao, filtrao, desinfeco, fluoretao e correo de pH.
Assinale a(s) proposio(es) correta(s).
1) Fluoretao: quando se adiciona flor na gua, cuja finalidade prevenir a formao de
crie dentria em crianas.
2) Floculao: ocorre em tanques de concreto, logo aps a coagulao. Com a gua em
movimento, as partculas slidas se aglutinam em flocos maiores.
4) Decantao: nesta etapa, que posterior coagulao e floculao, por ao da gravidade,
os flocos com as impurezas e partculas ficam depositados no fundo de outros tanques, separando-se
da gua. A etapa da decantao pode ser considerada um fenmeno fsico.
8) Filtrao: a etapa em que a gua passa por filtros formados por carvo, areia e pedras de
diversos tamanhos. Nesta etapa, as impurezas de tamanho pequeno ficam retidas no filtro. A etapa
da filtrao pode ser considerada como um fenmeno qumico.
16) Coagulao: a etapa em que a gua, na sua forma bruta, entra na ETA. Ela recebe, nos
tanques, uma determinada quantidade de cloreto de sdio. Esta substncia serve para aglomerar
partculas slidas que se encontram na gua como, por exemplo, a argila.
32) Desinfeco: a etapa em que cloro ou oznio aplicado na gua para eliminar
microorganismos causadores de doenas.
64) Correo de pH: esse procedimento serve para corrigir o pH da gua e preservar a rede de
encanamentos de distribuio. Se a gua est bsica, aplicada certa quantidade de cal hidratada ou
de carbonato de sdio.
(UFSM-RS) Considere o grfico:
Curvas de solubilidade de KNO3 e de Na2SO4 em 100 g de gua
Indique a alternativa correta:
a) No intervalo de temperatura de 0 C a 30 C, h diminuio da solubilidade do nitrato
de potssio.
b) A solubilidade do sulfato de sdio diminui a partir de 20 C.
c) Na temperatura de 40 C, o nitrato de potssio mais solvel que o sulfato de sdio.
d) Na temperatura de 60 C, o sulfato de sdio mais solvel que o nitrato de potssio.
e) No intervalo de temperatura de 30 C a 100 C, h diminuio da solubilidade do sulfato
de sdio.
. 3) - (UEM) Considere duas solues A e B. A soluo A constituda de 1,0 L de A2(SO4)3(aq)
0,15 mol/L e a soluo B constituda de 1,0 L de Ba(NO3)2(aq) 0,15 mol/L. Sabendo-se que os
sais esto 100% ionizados nas solues e que ambas esto ao nvel do mar, assinale o que for
correto. 01) A soluo A possui menor temperatura de congelao do que a soluo B.
02) A soluo B entra em ebulio a uma temperatura menor do que a soluo A.
04) A soluo A possui maior presso osmtica que a soluo B.
08) Misturando-se as duas solues, a concentrao de ons Ba +2 de 0,30 mol/L.
16) Uma soluo de glicose 0,15 mol/L apresentar efeito coligativo superior ao da soluo A.
32) Crioscopia a propriedade coligativa que corresponde diminuio da presso de vapor de um
lquido.
04) (UEM) Foram preparadas trs solues de um mesmo soluto em gua pura. A primeira uma
soluo de 1 L a 10 g/L, a segunda uma soluo de 500 mL a 25 g/L, a terceira uma soluo de
1,5 L a 15 g/L. Sabendo que as trs solues so mantidas a 25 o C e que o coeficiente de
solubilidade da substncia em questo de 40 g/L a essa temperatura, assinale o que for correto.
01) Considerando que o acrscimo de soluto no altera significativamente o volume da soluo,
necessrio acrescentar 7,5 g de soluto para que a segunda soluo fique saturada.
02) Se, a 15 o C, o coeficiente de solubilidade do soluto utilizado diminui 30 %, nenhuma das
solues apresentar precipitado a essa temperatura.
04) Se as trs solues forem completamente misturadas em um recipiente com capacidade para trs
litros, a concentrao da soluo resultante ser de 15 g/L.
08) Essas solues so exemplos de sistemas heterogneos com trs fases cada.
16) A soluo com a maior massa de soluto dissolvida a segunda.
5. (Uepg 2013) A respeito dos conceitos relacionados a disperses e a solues, assinale o que for
correto.
01) Disperses so misturas de duas ou mais substncias onde a substncia em menor quantidade
recebe o nome de disperso.
02) Uma soluo pode ser ao mesmo tempo diluda e saturada.
04) Quando um volume de 20 mL de uma soluo de cido sulfrico 0,05 mol L diludo para um
volume final de 100 mL, a concentrao torna-se igual a 0,01mol L.
08) Em uma soluo com densidade igual a 3 1,1g cm , cada 100 mL tem massa igual a 110 g.
16) A reao entre os solutos na mistura de duas solues poder ocorrer com excesso de um dos
solutos.
GABARITO:
01: 39
02: E
03: 07
04: 07
05: 31
Questes Primeiro ano
01)Considere as reaes abaixo e assinale a(s) alternativa(s) correta(s).
I) SO3 + H2O H2SO4
II) H2SO4 + CaCO3 CaSO4 + H2CO3
III) CaSO4 + NaOH Ca(OH)2 + Na2SO4
01) A reao I uma reao de adio.
02) A reao III uma reao de neutralizao.
04) Todas as reaes apresentadas acima esto balanceadas.
08) Carbonato de clcio um exemplo de sal insolvel em gua.
16) O cido carbnico formado na reao II um cido fraco, instvel e se decompe formando
gua e dixido de carbono
02)Assinale a(s) alternativa(s) correta(s).
01) Na combusto da gasolina (C8H18), que reage com O2(g) produzindo CO2 (g), H2O (l) e
energia, o volume de gs oxignio gasto na queima de 2 litros deste combustvel nas CNTP de
aproximadamente 3920 litros. Dado: densidade da gasolina = 0,8 grama/cm3 .
02) Na combusto da gasolina (C8H18), que reage com O2(g) produzindo CO2 (g), H2O (l) e
energia, a quantidade de dixido de carbono gerado na queima de 2 litros deste combustvel nas
CNTP de aproximadamente 5,0 kg. Dado: densidade da gasolina = 0,8 grama/cm 3.
04) Considere a reao cido-base HNO3 + KOH KNO3 + H2O. Fazendo-se reagir 20 gramas
de KOH com 20 gramas de HNO3, haver um excesso de aproximadamente 2,2 gramas de KOH.
08) Considere que uma amostra contendo 90% de Al2O3 reage com HCl em excesso formando 65
gramas de AlCl3 segundo a reao 1Al2O3 + 6HCl 2AlCl3 + 3H2O. Calculando-se a proporo
em massa de cada componente, possvel inferir que a massa da amostra contendo Al2O3
aproximadamente 28 gramas.
16) A soma dos coeficientes estequiomtricos da reao abaixo (a, b, c e d) balanceada com os
menores nmeros inteiros possveis igual a 14. aAl(OH)3 + bH2SO4 cAl2(SO4)3 + dH2O
24. (Uem) Aps fazer o balanceamento das reaes a seguir, nos casos necessrios, assinale o que
for correto.
01) A reao balanceada que representa a produo de carbonato de clcio slido e gs acetileno, a
partir de carbeto de clcio slido, gs carbnico e gua lquida
02) Considerando-se um rendimento de 100% para qualquer uma das reaes apresentadas no
enunciado, (I), (II) ou (III), a sntese de 2 kg de CaCO3(s) requer 1,4 kg de CaO.
04) Na reao (I), no sentido da reao direta, enquanto alguns tomos de C(s) sofrem oxidao
outros devem sofrer reduo.
08) Nas reaes (I), (II) e (III) pode-se encontrar o tomo de carbono com os Nox -2, -1, 0, +2 e +4.
16) A reao (II) pode ser classificada como uma reao de adio.
4 Assinale o que for correto.
01) Na queima de uma vela, no esto envolvidas transformaes qumicas, apenas fsicas.
02) O reflexo da luz solar em um lago um exemplo de um fenmeno fsico.
04) Em uma salina, a evaporao da gua para a produo do NaCl um exemplo de transformao
qumica.
08) A formao da ferrugem em uma estrutura metlica um exemplo de transformao qumica.
16) O derretimento do gelo um exemplo de fenmeno fsico.
5 Assinale o que for correto.
01) Cl2, S8 e O3 so exemplos de substncias simples.
02) O KMnO4 composto por trs elementos e seis tomos.
04) O ato de acender o farol de um automvel envolve fenmenos de transformao de energia
qumica em energia eltrica que, por sua vez, transforma-se em energia luminosa.
08) Um tomo que possui, em uma camada, somente os subnveis s e p possui, no mximo, oito
eltrons nessa camada.
16) O nmero de nutrons de um tomo de potssio 39 19 ( K) em seu estado neutro maior que o
nmero de nutrons de um on positivo de potssio (K1+).
Gabarito
01: 25
02 :15
03: 05
04: 26
05: 15
Você também pode gostar
- Avaliação da maturidade e vitalidade fetalDocumento4 páginasAvaliação da maturidade e vitalidade fetalGabriel MessiasAinda não há avaliações
- 2015 Aula Curso NUTRI SPok - 2 - 2Documento65 páginas2015 Aula Curso NUTRI SPok - 2 - 2Gabriel MessiasAinda não há avaliações
- Lesão Celular na Patologia GeralDocumento39 páginasLesão Celular na Patologia GeralGabriel MessiasAinda não há avaliações
- DefesaDocumento46 páginasDefesaGabriel MessiasAinda não há avaliações
- Tomografia Computadorizada OkDocumento51 páginasTomografia Computadorizada OkGabriel MessiasAinda não há avaliações
- Controle de Microrganismos Fis e QuimDocumento57 páginasControle de Microrganismos Fis e QuimGabriel MessiasAinda não há avaliações
- Semiologia - PulsosDocumento27 páginasSemiologia - PulsosGabriel MessiasAinda não há avaliações
- 06 Aula Hemodinamicos 1Documento47 páginas06 Aula Hemodinamicos 1Gabriel MessiasAinda não há avaliações
- 14a Aula Funções Motoras Da Medula EspinalDocumento32 páginas14a Aula Funções Motoras Da Medula EspinalGabriel MessiasAinda não há avaliações
- Aula 7 - Síndrome Do Intestino IrritávelDocumento25 páginasAula 7 - Síndrome Do Intestino IrritávelsanthiagoschneiderAinda não há avaliações
- Revisão Simplificada Da Fisiologia CardiovascularDocumento37 páginasRevisão Simplificada Da Fisiologia CardiovascularRuy LimaAinda não há avaliações
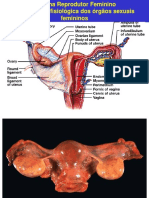
- Reprodutor FemininoDocumento19 páginasReprodutor FemininoGabriel MessiasAinda não há avaliações
- 2-Anatomia e Fisiologia Do Coracao NormalDocumento60 páginas2-Anatomia e Fisiologia Do Coracao NormalAlfredo JuniorAinda não há avaliações
- PsicopatologiaDocumento66 páginasPsicopatologiaGabriel Messias100% (2)
- 1) Acesso VenosoDocumento3 páginas1) Acesso VenosoGabriel MessiasAinda não há avaliações
- Amebas de Vida LivreDocumento1 páginaAmebas de Vida LivreGabriel Messias0% (1)
- Dicionario de DermatologiaDocumento438 páginasDicionario de DermatologianeiaoutAinda não há avaliações
- Sinapses: tipos de comunicação celularDocumento83 páginasSinapses: tipos de comunicação celularGabriel Messias100% (1)
- 05 Infecção em CirurgiaDocumento4 páginas05 Infecção em CirurgiaGabriel MessiasAinda não há avaliações
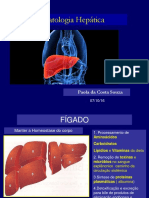
- 05 Patologia Hepática VB e Pancreas 2016Documento109 páginas05 Patologia Hepática VB e Pancreas 2016Gabriel Messias100% (1)
- Apostila Fisiologia Da DORDocumento12 páginasApostila Fisiologia Da DORGabriel Messias100% (1)
- Patologias dos Intestinos Delgado e GrossoDocumento110 páginasPatologias dos Intestinos Delgado e GrossoGabriel MessiasAinda não há avaliações
- Patologia Circulatória: Distúrbios da CirculaçãoDocumento46 páginasPatologia Circulatória: Distúrbios da CirculaçãoGabriel Messias100% (1)
- Patologia do Estômago: Gastrites, Úlceras e NeoplasiasDocumento81 páginasPatologia do Estômago: Gastrites, Úlceras e NeoplasiasGabriel MessiasAinda não há avaliações
- Amebíase PDFDocumento2 páginasAmebíase PDFGabriel Messias100% (1)
- Ácidos e Sais 2003Documento46 páginasÁcidos e Sais 2003Gabriel MessiasAinda não há avaliações
- Aulas interdisciplinares de matemática e físicaDocumento3 páginasAulas interdisciplinares de matemática e físicaGabriel MessiasAinda não há avaliações
- Sistema Limbico SilviaDocumento55 páginasSistema Limbico SilviaJuliana ToledoAinda não há avaliações
- Aula 7 - Síndrome Do Intestino IrritávelDocumento25 páginasAula 7 - Síndrome Do Intestino IrritávelsanthiagoschneiderAinda não há avaliações
- Meningite GraduaçãoDocumento60 páginasMeningite GraduaçãoGabriel MessiasAinda não há avaliações
- Higienização bananas máscara facialDocumento2 páginasHigienização bananas máscara facialEDUARDA APARECIDA SANTOSAinda não há avaliações
- Ouvindo o Planeta TerraDocumento217 páginasOuvindo o Planeta TerraRodrigo Carneiro Babazinho100% (1)
- Exercícios termoquímicaDocumento22 páginasExercícios termoquímicaSérgio ViroliAinda não há avaliações
- 03 Espec°ficosDocumento1.498 páginas03 Espec°ficosJessica RodriguesAinda não há avaliações
- Manual - Aditivos - VEDACITDocumento86 páginasManual - Aditivos - VEDACITLeonardo SantanaAinda não há avaliações
- 1 Aula Tratamento de Efluentes - 2018Documento53 páginas1 Aula Tratamento de Efluentes - 2018Talissa NamiasAinda não há avaliações
- Classificação, propriedades e aplicações de álcooisDocumento59 páginasClassificação, propriedades e aplicações de álcooisJoao ClaytonAinda não há avaliações
- Atividade Avaliativa Agroecologia - 4 AnoDocumento2 páginasAtividade Avaliativa Agroecologia - 4 AnoNinna SantiniAinda não há avaliações
- APOSTILA BPF Completa 1Documento76 páginasAPOSTILA BPF Completa 1Priscilla Botelho100% (2)
- APOSTILA DE PNEUMÁTICA UERJ FATDocumento72 páginasAPOSTILA DE PNEUMÁTICA UERJ FATenge2209100% (1)
- Avaliação 1oBimestre de Química com questões sobre transformações químicas e físicasDocumento3 páginasAvaliação 1oBimestre de Química com questões sobre transformações químicas e físicasClésio O de SouzaAinda não há avaliações
- Apostila Agroecologia e Horta Organica 2010Documento30 páginasApostila Agroecologia e Horta Organica 2010Marcelo Nardin100% (1)
- Sub-Bacia Do Córrego Olhos D'águaDocumento54 páginasSub-Bacia Do Córrego Olhos D'águaAna Clara MottaAinda não há avaliações
- Recursos Naturais e Meio Ambiente 26-01-22Documento20 páginasRecursos Naturais e Meio Ambiente 26-01-22Anthony RodriguesAinda não há avaliações
- Fotossíntese: tipos de plantas C3, C4 e CAMDocumento3 páginasFotossíntese: tipos de plantas C3, C4 e CAMAlane AquinoAinda não há avaliações
- Monitoramento AquapônicoDocumento95 páginasMonitoramento AquapônicoindioAinda não há avaliações
- Chuveiro automático controlado por sensorDocumento81 páginasChuveiro automático controlado por sensorAlessandro SilvaAinda não há avaliações
- A Alegria No CasamentoDocumento3 páginasA Alegria No CasamentoCasa do PaiAinda não há avaliações
- Inspeção de caldeiras: aspectos termodinâmicos e tiposDocumento196 páginasInspeção de caldeiras: aspectos termodinâmicos e tiposPedroDiazAinda não há avaliações
- Análises Bromatológicas - AVADocumento79 páginasAnálises Bromatológicas - AVAJéssica TussiAinda não há avaliações
- MaxxForce 4.3 - 6.5Documento66 páginasMaxxForce 4.3 - 6.5FR0% (1)
- Medição de vazão em cursos d'água com vertedoresDocumento32 páginasMedição de vazão em cursos d'água com vertedoresdoug9douglasAinda não há avaliações
- 05 - Sanitariedade Na Indústria AlimentíciaDocumento208 páginas05 - Sanitariedade Na Indústria AlimentíciaGestão Qualidade RSAinda não há avaliações
- Livro Conservacao Pescado PDFDocumento117 páginasLivro Conservacao Pescado PDFCarlos CavalcanteAinda não há avaliações
- Curso de Jardinagem Básica OnlineDocumento35 páginasCurso de Jardinagem Básica OnlineKesia OliveiraAinda não há avaliações
- Como fazer brotos em casaDocumento42 páginasComo fazer brotos em casag.tiger@ig.com.br100% (1)
- Gestão sustentável de recursos florestaisDocumento17 páginasGestão sustentável de recursos florestaiseulario86% (7)
- Como tratar piscinas com hipoclorito de sódioDocumento25 páginasComo tratar piscinas com hipoclorito de sódioFernanda FernandesAinda não há avaliações
- Ácido Sulfúrico e Fertilizantes FosfatadosDocumento57 páginasÁcido Sulfúrico e Fertilizantes FosfatadosFelipe Guedes Pucci100% (2)
- Processo de polpação química alcalinaDocumento117 páginasProcesso de polpação química alcalinaValdir OliveiraAinda não há avaliações