Escolar Documentos
Profissional Documentos
Cultura Documentos
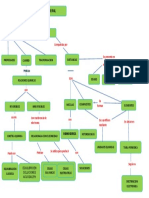
Cuadro Comparativo Modelos Atomicos
Enviado por
Andres Cano0 notas0% acharam este documento útil (0 voto)
135 visualizações3 páginasTítulo original
cuadro comparativo modelos atomicos..docx
Direitos autorais
© © All Rights Reserved
Formatos disponíveis
DOCX, PDF, TXT ou leia online no Scribd
Compartilhar este documento
Compartilhar ou incorporar documento
Você considera este documento útil?
Este conteúdo é inapropriado?
Denunciar este documentoDireitos autorais:
© All Rights Reserved
Formatos disponíveis
Baixe no formato DOCX, PDF, TXT ou leia online no Scribd
0 notas0% acharam este documento útil (0 voto)
135 visualizações3 páginasCuadro Comparativo Modelos Atomicos
Enviado por
Andres CanoDireitos autorais:
© All Rights Reserved
Formatos disponíveis
Baixe no formato DOCX, PDF, TXT ou leia online no Scribd
Você está na página 1de 3
cientfico aportacin Modelo atomico
Demcrito desarroll la teora atmica del
(Filosofo) universo, Los tomos son
partculas
eternas, indivisibles, homogneos,
incompresibles e invisibles, se
diferencian solo en forma y
tamao, pero no por cualidades
internas, a su vez establecio que
las propiedades de la materia Las
varan segn el agrupamiento de
los tomos.
John Dalton Debido a sus investigaciones entre
1803 y 1807, naci la teora
atmica qumica, y estableci 4
postulados sobre los tomos
Cada elemento se compone de
partculas extremadamente
pequeas llamadas tomos
Todos los tomos de un elemento
dado son idnticos; los tomos de
elementos diferentes son
diferentes y tienen propiedades
distintas (incluida la masa), Los
tomos de un elemento no se
transforman en tomos diferentes
durante las reacciones qumicas;
los tomos no se crean ni se
destruyen en las reacciones
qumicas, Cuando se combinan
tomos de ms de un elemento se
forman compuestos; un
compuesto dado siempre tiene el
mismo nmero relativo de la
misma clase de tomos.
J.J Descubri por su experimento de
Thomson rayos catdicos la presencia de
partculas cargadas negativamente
en los tomos, como los
electrones constituyen una
fraccin muy
pequea de la masa de un tomo,
probablemente haba una relacin
con el tamao del tomo, y
propuso que el tomo consista en
una esfera uniforme de materia
positiva
en la que estaban incrustados los
electrones, a este modelo se le
denomin el pudin de pasas de
Thomson.
Ernest Gracias a sus experimentos de
Rutherford dispersin de partculas (con
carga positiva, protones) dio pie al
modelo nuclear del tomo, en el
cual exista en un ncleo cargado
positivamente y electrones
girando alrededor de este.
Niels Bohr el primer modelo atmico en el
que se introduce
una cuantizacin a partir de
ciertos postulados. Fue propuesto
en 1913 por el fsico dans Niels
Bohr, para explicar cmo
los electrones pueden
tener rbitas estables alrededor
del ncleo. En este modelo los
electrones giran en
rbitas circulares alrededor del
ncleo, ocupando la rbita de
menor energa posible, o la rbita
ms cercana posible al ncleo. El
electromagnetismo clsico
predeca que una partcula
cargada movindose de forma
circular emitira energa por lo que
los electrones deberan colapsar
sobre el ncleo en breves
instantes de tiempo. Para superar
este problema Bohr supuso que
los electrones solamente se
podan mover en rbitas
especficas, cada una de las cuales
caracterizada por su nivel
energtico. Cada rbita puede
entonces identificarse mediante
un nmero entero n que toma
valores desde 1 en adelante. Este
nmero "n" recibe el nombre
de nmero cuntico principal.
James confirm la existencia de otra
Chadwick partcula subatmica de la que se
tenan mltiples sospechas:
el neutrn. Los neutrones son
partculas subatmicas que no
tienen carga elctrica, y cuya masa
es casi igual a la de los protones. El
neutrn es una partcula
subatmica que no tiene carga
elctrica. Su masa es casi igual a la
del protn. Determin mediante el
estudio de reacciones nucleares la
masa del Neutrn, el cual no posee
carga
Werner Este modelo matemtico no
Heisenberg expresa claramente la posicin de
y Erwin los electrones esta basado en los
Schrdinger estudios de Mecnica Cuntica en
la cual se plantea que los
electrones se encuentran en
determinadas regiones
denominadas orbitales de tal
manera que en esta regin la
probabilidad de localizar un
electrn es mxima. Este modelo
se basa en la dualidad de la
materia que se comporta como
onda y partcula y en el principio
de incertidumbre de Heisenberg
que nos dice que es imposible
determinar la velocidad y la
posicin de un electrn al mismo
tiempo en un instante
determinado. Segn este modelo,
los tomos metlicos ceden sus
electrones de valencia a una "nube
electrnica" que comprende todos
los tomos del metal. Entonces el
enlace metlico resulta de las
atracciones electrostticas entre
los restos positivos y los electrones
mviles que pertenecen en su
conjunto a la red metlica.
Você também pode gostar
- Historia de La Genética PDFDocumento7 páginasHistoria de La Genética PDFDanielAinda não há avaliações
- Mapas Conceptuales Enlaces QuimicosDocumento5 páginasMapas Conceptuales Enlaces QuimicosAnonymous u7auloU7K0% (1)
- Mapa Mental Del AtomoDocumento1 páginaMapa Mental Del AtomoAlejandroAinda não há avaliações
- Cuadro Comparativo ModelosDocumento5 páginasCuadro Comparativo ModelosDaniel Jose Ruiz GutierrezAinda não há avaliações
- Cuadro Comparativo de Modelos AtómicosDocumento10 páginasCuadro Comparativo de Modelos AtómicosBaeta Jesus0% (1)
- Factores Fisicos y Ambientales de VenezuelaDocumento5 páginasFactores Fisicos y Ambientales de VenezuelaEdwardAlcheAinda não há avaliações
- Niveles y Subniveles de La Energia de La Configuracion ElectronicaDocumento6 páginasNiveles y Subniveles de La Energia de La Configuracion ElectronicaFernanda RamirezAinda não há avaliações
- Mandala Del Origen de El Sistema SolarDocumento4 páginasMandala Del Origen de El Sistema SolarAngelaGarcia100% (1)
- Tabla de AcontecimientosDocumento3 páginasTabla de AcontecimientosDANNA NAVARRO GUZMANAinda não há avaliações
- DemocritoDocumento5 páginasDemocritoSamanda Suselly Franco100% (1)
- Cuadro Comparativos de Los Modelos AtomicosDocumento1 páginaCuadro Comparativos de Los Modelos AtomicosJuan Cruz EmmaAinda não há avaliações
- Trabajo Mapa Conceptual Enlaces QuimicosDocumento3 páginasTrabajo Mapa Conceptual Enlaces QuimicosAmyl JensAinda não há avaliações
- Estructura Atómica y Estructura de Las Cargas Eléctricas.Documento3 páginasEstructura Atómica y Estructura de Las Cargas Eléctricas.Ingrid D. ReyesAinda não há avaliações
- Cuadro Comparativo 7Documento2 páginasCuadro Comparativo 7Juan jose Avila GomezAinda não há avaliações
- Fallas corteza terrestreDocumento8 páginasFallas corteza terrestreDilson Loaiza CruzAinda não há avaliações
- Elementos que conforman el sistema solarDocumento6 páginasElementos que conforman el sistema solarWilder Magdiel Lopez HernandezAinda não há avaliações
- Mapa Conceptual, BiologiaDocumento1 páginaMapa Conceptual, BiologiaGerardo RodriguezAinda não há avaliações
- Biologia Mapa Conceptual NeuronasDocumento1 páginaBiologia Mapa Conceptual NeuronasNelson Alemán SánchezAinda não há avaliações
- Linea de Tiempo Aportaciones en El Modelo AtomicoDocumento5 páginasLinea de Tiempo Aportaciones en El Modelo AtomicoJuan PabloAinda não há avaliações
- Mapa Conceptual Historia Del MundoDocumento1 páginaMapa Conceptual Historia Del MundoFernando GutiérrezAinda não há avaliações
- Materiales TerrestresDocumento27 páginasMateriales TerrestresLinero CandyAinda não há avaliações
- Mapa Conceptual FisicaDocumento2 páginasMapa Conceptual FisicaYepes Marquez80% (10)
- Clases Sociales VenezolanasDocumento8 páginasClases Sociales VenezolanasframanvideoAinda não há avaliações
- Flujo de Energía en Los EcosistemasDocumento6 páginasFlujo de Energía en Los EcosistemasLaura Carolina Alvarez100% (1)
- Metales y No MetalesDocumento12 páginasMetales y No MetalesCiber San JuditasAinda não há avaliações
- Mapas ConceptualesDocumento1 páginaMapas ConceptualesAdrián ZarateAinda não há avaliações
- Origen y Diversificacion de La VidaDocumento8 páginasOrigen y Diversificacion de La VidaNicolas Patricio Sitja100% (6)
- Dinámica poblacional Venezuela 1926-1985Documento14 páginasDinámica poblacional Venezuela 1926-1985Pedro Muro MorenoAinda não há avaliações
- Trabajo de Castellano CUADRO DE LIRICADocumento7 páginasTrabajo de Castellano CUADRO DE LIRICAmerlyAinda não há avaliações
- Examen FinalDocumento5 páginasExamen FinalManuel Jose Sandoval UrízarAinda não há avaliações
- CLASE 13 La Transmisión de Los Caracteres Hereditarios.Documento28 páginasCLASE 13 La Transmisión de Los Caracteres Hereditarios.jose miguelAinda não há avaliações
- Ley Periódica PDFDocumento1 páginaLey Periódica PDFSantiago SanchezAinda não há avaliações
- Clase de Familia DerivadaDocumento14 páginasClase de Familia DerivadaGilsonFiguera100% (2)
- Himno Liceo Andrés Bello caracteresDocumento1 páginaHimno Liceo Andrés Bello caracteresRoberto Vasquez0% (1)
- Historia de La QuimicaaDocumento2 páginasHistoria de La QuimicaaJatziri RiosAinda não há avaliações
- Infogracia IndependenciaDocumento1 páginaInfogracia IndependenciaDavid Alberto Arias ZavalaAinda não há avaliações
- La Materia y Sus Estados Con Cuadro ComparativoDocumento11 páginasLa Materia y Sus Estados Con Cuadro ComparativoCarlosRober7o100% (4)
- Qué es un ecosistemaDocumento3 páginasQué es un ecosistemavladimir sAinda não há avaliações
- Lenguaje Quimico DonadoDocumento28 páginasLenguaje Quimico DonadoGalaxia Marcano SandovalAinda não há avaliações
- 2.-Aislamiento Reproductivo-1Documento23 páginas2.-Aislamiento Reproductivo-1Steve MedinaAinda não há avaliações
- Biografía de Carlos NogueraDocumento2 páginasBiografía de Carlos NogueraRobertoAinda não há avaliações
- Triptico FSNDocumento3 páginasTriptico FSNEddimag BriceñoAinda não há avaliações
- ELECTROSTÁTICADocumento7 páginasELECTROSTÁTICARafael Flores YabarAinda não há avaliações
- Mapa Mixto Reacciones QuimicasDocumento1 páginaMapa Mixto Reacciones QuimicasServideskOffice Accm100% (1)
- Estructura de La Materia y Teoría Atómica.Documento1 páginaEstructura de La Materia y Teoría Atómica.Stephany 03042001100% (1)
- El Efecto de Los Electronico en La Quimica OrganicaDocumento9 páginasEl Efecto de Los Electronico en La Quimica OrganicaRoxelis Manzano50% (4)
- ElectrostáticaDocumento4 páginasElectrostáticaJesus GomezAinda não há avaliações
- Ciclo viral en 4 fasesDocumento2 páginasCiclo viral en 4 fasesKarla OsorioAinda não há avaliações
- Q10° Teoría Atómica 1Documento18 páginasQ10° Teoría Atómica 1Luis Hernando López LozanoAinda não há avaliações
- OvogénesisDocumento4 páginasOvogénesisNando FloresAinda não há avaliações
- Electricidad: Fenómeno y AplicacionesDocumento14 páginasElectricidad: Fenómeno y Aplicacionesrichard_17dAinda não há avaliações
- Mapa Conceptual de Las Sustancias PurasDocumento2 páginasMapa Conceptual de Las Sustancias PurasUrquizo Mendoza Nicolás MatiasAinda não há avaliações
- Evolución de los modelos atómicos desde Demócrito hasta HeisenbergDocumento2 páginasEvolución de los modelos atómicos desde Demócrito hasta HeisenbergMario NoleAinda não há avaliações
- 20 Asociación de ResistenciasDocumento6 páginas20 Asociación de ResistenciasROY FERNANDOAinda não há avaliações
- Tarea 2 - Caída de TenochtitlánDocumento2 páginasTarea 2 - Caída de TenochtitlánOmar Arturo Pineda ReyesAinda não há avaliações
- PRONOMBRES INTERROGATIVOS y DIALOGOSDocumento1 páginaPRONOMBRES INTERROGATIVOS y DIALOGOSNarda CzabanyiAinda não há avaliações
- Modelos AtómicosDocumento4 páginasModelos AtómicosSaranndonga100% (1)
- Modelos AtómicosDocumento4 páginasModelos AtómicosSaranndongaAinda não há avaliações
- Historia de Modelos AtómicosDocumento7 páginasHistoria de Modelos AtómicosAndrea Jezabel López GonzálezAinda não há avaliações
- El ÁtomoDocumento16 páginasEl ÁtomoDaniel OrtuñoAinda não há avaliações
- Actividad 2 Quimica GeneralDocumento4 páginasActividad 2 Quimica GeneralAndres CanoAinda não há avaliações
- Ciclo de Vida D Ela TecnologiaDocumento4 páginasCiclo de Vida D Ela TecnologiaAndres CanoAinda não há avaliações
- Cuadro Comparativo Modelos Atomicos.Documento3 páginasCuadro Comparativo Modelos Atomicos.Andres CanoAinda não há avaliações
- Matriz de Respuestas Caso Del Toque Magico de SonyDocumento3 páginasMatriz de Respuestas Caso Del Toque Magico de SonyAndres CanoAinda não há avaliações
- Congelacion Por InmersiónDocumento14 páginasCongelacion Por InmersiónAndres CanoAinda não há avaliações
- Alejandro Dolina Dijo Una VezDocumento1 páginaAlejandro Dolina Dijo Una VezAndres CanoAinda não há avaliações
- En 1884 El Doctor Christian Gram Desarrolló La Tinción Más Famosa y Utilizada en Los Laboratorios de BacteriologíaDocumento2 páginasEn 1884 El Doctor Christian Gram Desarrolló La Tinción Más Famosa y Utilizada en Los Laboratorios de BacteriologíaAndres CanoAinda não há avaliações
- Diagrama Flujo BasicoDocumento2 páginasDiagrama Flujo BasicoAndres CanoAinda não há avaliações
- Ejercicio 1 Quimica GeneralDocumento2 páginasEjercicio 1 Quimica GeneralAndres CanoAinda não há avaliações
- Receta polcanes YucatánDocumento1 páginaReceta polcanes YucatánAndres CanoAinda não há avaliações
- ZanahoriaDocumento50 páginasZanahoriaRicardo AceroAinda não há avaliações
- Fundamentos de Transferencia de MasaDocumento98 páginasFundamentos de Transferencia de MasaAndres CanoAinda não há avaliações
- Ahumado de pescadoDocumento2 páginasAhumado de pescadoAndres CanoAinda não há avaliações
- ADA 1 Ecuaciones DiferencialesDocumento2 páginasADA 1 Ecuaciones DiferencialesAndres CanoAinda não há avaliações
- Ejercicios - Resueltos de CengelDocumento11 páginasEjercicios - Resueltos de CengelGonzález NickovAinda não há avaliações
- Aminas BiogenicasDocumento23 páginasAminas BiogenicasAndres CanoAinda não há avaliações
- Expo Flujo Casi Final 2Documento36 páginasExpo Flujo Casi Final 2Andres CanoAinda não há avaliações
- Evaluación de Los Programas Pre Requisitos Del Plan HACCPDocumento29 páginasEvaluación de Los Programas Pre Requisitos Del Plan HACCPAndres CanoAinda não há avaliações
- El PrecioDocumento15 páginasEl PrecioAndres CanoAinda não há avaliações
- Educación Integral HumanistaDocumento4 páginasEducación Integral HumanistaAndres CanoAinda não há avaliações
- Aditivos Usados en Jugos y NéctaresDocumento7 páginasAditivos Usados en Jugos y NéctaresAndres CanoAinda não há avaliações
- Expo Flujo Casi Final 2Documento36 páginasExpo Flujo Casi Final 2Andres CanoAinda não há avaliações
- Β-oxidación de Ácidos GrasosDocumento7 páginasΒ-oxidación de Ácidos GrasosAndres CanoAinda não há avaliações
- Educación Integral HumanistaDocumento4 páginasEducación Integral HumanistaAndres CanoAinda não há avaliações
- Ejercicio 1-Actividad 1Documento2 páginasEjercicio 1-Actividad 1Andres CanoAinda não há avaliações
- Β-oxidación de Ácidos GrasosDocumento7 páginasΒ-oxidación de Ácidos GrasosAndres CanoAinda não há avaliações
- CaramelizacionDocumento6 páginasCaramelizacionAndres CanoAinda não há avaliações
- Esteroides y TerpenosDocumento20 páginasEsteroides y TerpenosAndres CanoAinda não há avaliações
- Cinetica y PontencialDocumento4 páginasCinetica y PontencialAndres CanoAinda não há avaliações
- Lab de QuimicaDocumento13 páginasLab de Quimicadocsofi60% (5)
- Cargas puncher y corte de tuberías en operaciones especialesDocumento32 páginasCargas puncher y corte de tuberías en operaciones especialesKellys Paola Lanza Gil100% (1)
- Cortes y grabados láserDocumento36 páginasCortes y grabados láserJoseJoseAinda não há avaliações
- Circuitos capacitivos ACDocumento3 páginasCircuitos capacitivos ACRafael LaraAinda não há avaliações
- Especificaciones Técnicas CITEmaderaDocumento124 páginasEspecificaciones Técnicas CITEmaderaArmando Nilo Ramos SilvaAinda não há avaliações
- Masa VariableDocumento83 páginasMasa Variableedco01Ainda não há avaliações
- Ecuaciones y funciones polinómicasDocumento4 páginasEcuaciones y funciones polinómicaselmer1987-1Ainda não há avaliações
- LarelaticdDocumento22 páginasLarelaticdleandrole0% (1)
- Ingenieria de Metodos II Cl09 2011 0Documento13 páginasIngenieria de Metodos II Cl09 2011 0Paul Tello RojasAinda não há avaliações
- 1470-15 GSI170-TA9 Rev0 ESDocumento245 páginas1470-15 GSI170-TA9 Rev0 ESSergioAinda não há avaliações
- ODI Operador GrúaDocumento3 páginasODI Operador GrúaManuel Mora M.Ainda não há avaliações
- Informe Real Energia MecanicaDocumento3 páginasInforme Real Energia MecanicaAlejandro AlejandroAinda não há avaliações
- 04 - Difracción Rendija y RejillaDocumento7 páginas04 - Difracción Rendija y RejillaRom Kno SanAinda não há avaliações
- Poleas, máquinas simples para elevar cargasDocumento7 páginasPoleas, máquinas simples para elevar cargaseddie2166Ainda não há avaliações
- Desigualdad de BooleDocumento5 páginasDesigualdad de BooleEduardo Andres Lorca CastilloAinda não há avaliações
- Trogo Auto EgocráticoDocumento2 páginasTrogo Auto Egocráticociensiano100% (1)
- Cromatografía PlanaDocumento4 páginasCromatografía PlanaAlberto Junior Quispe YayaAinda não há avaliações
- Instrumentos de Medición 1.0Documento29 páginasInstrumentos de Medición 1.0Juan David Comas CabralesAinda não há avaliações
- Cálculo de TransformadorDocumento20 páginasCálculo de TransformadorRandyAinda não há avaliações
- Grúas Giratorias Fijas.Documento60 páginasGrúas Giratorias Fijas.Anonymous PAd5e7LaXY100% (1)
- CinemaDocumento17 páginasCinemamablozadaAinda não há avaliações
- Circuitos en Ingenieria Electrica - SkillingDocumento378 páginasCircuitos en Ingenieria Electrica - SkillingRenzo NobileAinda não há avaliações
- El teodolito: definición, centraje, nivelación y usosDocumento39 páginasEl teodolito: definición, centraje, nivelación y usosCristian VallejoAinda não há avaliações
- 1era Practica de Movimiento Vertical de Caida LibreDocumento2 páginas1era Practica de Movimiento Vertical de Caida Libreshagy ticonaAinda não há avaliações
- El Ácido SalicílicoDocumento49 páginasEl Ácido SalicílicoCristian Joaquin ZegarraAinda não há avaliações
- Sujetadores de Pasador y Anillos de RetenciónDocumento24 páginasSujetadores de Pasador y Anillos de RetenciónCalvin ClaneAinda não há avaliações
- Thatquiz AP TrigDocumento5 páginasThatquiz AP TrigISABEL100% (1)
- Maquina de Vapor GeneralidadesDocumento12 páginasMaquina de Vapor GeneralidadesReynolds HansAinda não há avaliações
- Tipos de PoleaDocumento15 páginasTipos de PoleaRonald PalominoAinda não há avaliações
- Sistemas No Lineales y Metodo de LinealizacionDocumento19 páginasSistemas No Lineales y Metodo de LinealizacionMafer Ruiz EstudilloAinda não há avaliações