Escolar Documentos
Profissional Documentos
Cultura Documentos
Cuadro Comparativo de Propiedades de Los Enlaces Quimicos
Enviado por
Jorge Lopez GomezDireitos autorais
Formatos disponíveis
Compartilhar este documento
Compartilhar ou incorporar documento
Você considera este documento útil?
Este conteúdo é inapropriado?
Denunciar este documentoDireitos autorais:
Formatos disponíveis
Cuadro Comparativo de Propiedades de Los Enlaces Quimicos
Enviado por
Jorge Lopez GomezDireitos autorais:
Formatos disponíveis
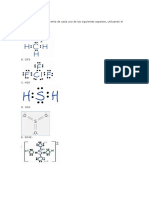
Propiedades Enlace Inico Enlace Covalente Enlace Metlico
Comportamiento de los electrones Transferencia Electrnica Comparticin de Electrones Liberacin de Electrones
Diferencia de electronegatividad Se establece en tomos con diferencias La diferencia de electronegatividades Es el enlace que se da entre elementos
marcadas en sus electronegatividades y se entre los tomos no es de electronegatividades bajas y muy
debe a la interaccin electrosttica entre suficientemente grande como para parecidas, en estos casos ninguno de los
los iones que pueden formarse por la que se efecte una transferencia de tomos tiene ms posibilidades que el
transferencia de uno o ms electrones de electrones. De esta forma, los dos otro de perder o ganar los electrones
un tomo o grupo atmico a otro. tomos comparten uno o ms pares
electrnicos en un nuevo tipo de
orbital, denominado orbital molecular.
Los enlaces covalentes se suelen
producir entre elementos gaseosos
no metales.
Elementos qumicos que lo Este tipo de enlace suele darse entre Este tipo de enlace se produce entre Este tipo de enlace se produce entre
conforman elementos que estn a un extremo y a otro elementos muy electronegativos (no elementos poco electronegativos
de la tabla peridica. O sea, el enlace se metales) (metales)
produce entre elementos muy
electronegativos (no metales) y elementos
poco electronegativos (metales)
Estado fsico a temperatura Todos los compuestos inicos puros son A temperatura ambiente algunos son Son slidos a temperatura ambiente
ambiente slidos a temperatura ambiente. slidos, lquidos o gases (excepto el mercurio que es lquido).
Partculas que lo forman Cationes y Aniones Molculas Cationes
tomos
Tipo de estructura Red inica Molculas simples Estructuras Cristalinas compactas: cbica
Molculas gigantes centrada en el espacio (cce), cbica
compacta (cc) y hexagonal compacta (hc)
Puntos de fusin Por lo general 400 C Por lo general 300 C Temperaturas de fusin elevadas
Puntos de ebullicin Encima de los 1500 C Las temperaturas de ebullicin son Temperaturas de ebullicin elevadas
bajas
Deformabilidad del slido Se forman redes cristalinas (ordenadas). Tenemos molculas como tales en el La aleacin de dos metales es de gran
Por tanto, los iones que se forman con este caso de las sustancias moleculares. importancia ya que es una de las
enlace no forman molculas aisladas sino Si los tomos que se unen con enlace principales formas de modificar las
que se agrupan de forma ordenada en covalente forman 'slidos covalentes' propiedades de los elementos metlicos
redes en las que el nmero de cargas o 'redes covalentes', no tendremos puros.
positivas es igual al de cargas negativas, molculas como tales entidades que
compuesto es neutro. se puedan aislar
Conductividad elctrica En estado slido no conducen la corriente Los compuestos lquidos o fundidos Buenos conductores de la electricidad
elctrica debido a que los iones estn no conducen la electricidad. (nube de electrones deslocalizada) y del
demasiados juntos. Al fundir estas sales los Las soluciones acuosas suelen ser calor (facilidad de movimiento de
iones se separan y pueden moverse dentro malas conductoras de la electricidad electrones y de vibracin de los restos
de un campo elctrico y por lo tanto porque no contienen partculas con atmicos positivos)
conducen la corriente elctrica en solucin. carga.
Solubilidad Son solubles en disolventes polares Muchos de ellos son insolubles en Solubles en otro metal fundido
(Como el agua) debido a que sus iones se disolventes polares. (aleaciones)
separan por atracciones electrostticas. La mayora es soluble en disolventes
no polares, como el hexano.
Você também pode gostar
- SUCESIONES Y SERIES DE FUNCIONES Basado en Los Libros Granville y LeitholdDocumento6 páginasSUCESIONES Y SERIES DE FUNCIONES Basado en Los Libros Granville y LeitholdChristian Gonzalo Pinargote Garcia0% (1)
- Actividad 5 Enlaces Químicos e Interacción MolecularDocumento8 páginasActividad 5 Enlaces Químicos e Interacción MolecularBrayan Arley100% (1)
- Cuadro Comparativo de Propiedades de Los Enlaces QuimicosDocumento2 páginasCuadro Comparativo de Propiedades de Los Enlaces QuimicosCeledonio Hernandez Sanchez79% (78)
- Expediente Tecnico de Reparacion de Sardineles y PavimentosDocumento32 páginasExpediente Tecnico de Reparacion de Sardineles y PavimentosDavid RodriguezAinda não há avaliações
- Medidas de Tendencia CentralDocumento4 páginasMedidas de Tendencia CentraledwinAinda não há avaliações
- Cómo Fabricar AerogelDocumento28 páginasCómo Fabricar AerogelclaudioAinda não há avaliações
- 03 Números Reales DiapositivasDocumento52 páginas03 Números Reales DiapositivasRicardo EmilioAinda não há avaliações
- Selectividad Movimiento Armonico SimpleDocumento6 páginasSelectividad Movimiento Armonico SimpleAna Belen GrañaAinda não há avaliações
- Tetraedro de La Ciencia e Ingenieria de MaterialesDocumento5 páginasTetraedro de La Ciencia e Ingenieria de MaterialesPaul Alejandro100% (2)
- Mapa Conceptual (Imperfecciones Cristalinas)Documento2 páginasMapa Conceptual (Imperfecciones Cristalinas)Socrates JavierAinda não há avaliações
- Respuesta 3,4,5 Materilaes1Documento3 páginasRespuesta 3,4,5 Materilaes1Marlene ArgelAinda não há avaliações
- U2 Diapos Isomeria OrganicaDocumento50 páginasU2 Diapos Isomeria OrganicaAbril Gutierrez LuqueAinda não há avaliações
- EstructuraDocumento13 páginasEstructuraIvan Dario Pineda PatiñoAinda não há avaliações
- Taller 2 Actividad Formativa 2 2020 2Documento5 páginasTaller 2 Actividad Formativa 2 2020 2Maria Jose Von BerchemAinda não há avaliações
- Teoria Global Del Universo SpaxiumDocumento138 páginasTeoria Global Del Universo SpaxiumLuis Jimenez Precoma0% (1)
- Mate ProyectDocumento4 páginasMate ProyectGilliam CastellanosAinda não há avaliações
- Direcciones de Celda - T3.2Documento5 páginasDirecciones de Celda - T3.2Miguel ÃngelAinda não há avaliações
- Ejercicios Conduccion de Los MetalesDocumento2 páginasEjercicios Conduccion de Los MetalesNéstor Galeano ArenasAinda não há avaliações
- Laboratorio Estructuras3 PDFDocumento6 páginasLaboratorio Estructuras3 PDFBrando Acuña VelasquezAinda não há avaliações
- Ciencia de Los Materiales FzaDocumento6 páginasCiencia de Los Materiales FzaChristian Marisol ClementinaAinda não há avaliações
- Taller 3 - Átomo y Modelos AtómicosDocumento3 páginasTaller 3 - Átomo y Modelos Atómicoskatherin vargasAinda não há avaliações
- Mapa Conceptual Practica 9Documento1 páginaMapa Conceptual Practica 9Isaac VillamaresAinda não há avaliações
- Corrección ExamenDocumento8 páginasCorrección ExamenDomenica CoralAinda não há avaliações
- Resumen Materiales I - AskelandDocumento109 páginasResumen Materiales I - AskelandAtilioPanizziAinda não há avaliações
- Índices de Miller-ExpoDocumento5 páginasÍndices de Miller-ExpoRober RoqueAinda não há avaliações
- Informe Numero 3Documento13 páginasInforme Numero 3Brandon EspinozaAinda não há avaliações
- T3 CienciasDocumento6 páginasT3 CienciasJosh FuentesAinda não há avaliações
- T1 Estructura Materiales EjerciciosDocumento5 páginasT1 Estructura Materiales EjerciciosJoaquin G. MarreroAinda não há avaliações
- Serie Tecnología de MaterialesDocumento42 páginasSerie Tecnología de MaterialesMauricio Antonio Olvera LuqueAinda não há avaliações
- Enunciados Ejercicios Enlace Quimico QuimitubeDocumento14 páginasEnunciados Ejercicios Enlace Quimico QuimitubePonchito GrajalesAinda não há avaliações
- Linea Del Tiempo Del Desarrollo de La Teoria Cuantica y Estructura Atomica Equipo 1Documento4 páginasLinea Del Tiempo Del Desarrollo de La Teoria Cuantica y Estructura Atomica Equipo 1Alonso Conti MelissaAinda não há avaliações
- Dibujo y Diseno en Ingenieria Edicion 6-17-23 PDFDocumento7 páginasDibujo y Diseno en Ingenieria Edicion 6-17-23 PDFahernandez0623Ainda não há avaliações
- Lab Fissica Lineas EquipotencialesDocumento9 páginasLab Fissica Lineas Equipotencialessantiago sierraAinda não há avaliações
- Ley de AmpèreDocumento11 páginasLey de AmpèreSofia Sabogal AvellaAinda não há avaliações
- Resistencias en SerieDocumento3 páginasResistencias en Seriejohan ramirezAinda não há avaliações
- Laboratorio #02 Fisica IIDocumento7 páginasLaboratorio #02 Fisica IIYonatanZavaletaAinda não há avaliações
- Tema 7. Solicitaciones CompuestasDocumento13 páginasTema 7. Solicitaciones Compuestasmaria0% (1)
- X Tan (X) DX: Integrar Por PartesDocumento1 páginaX Tan (X) DX: Integrar Por PartesEsteven SolanoAinda não há avaliações
- Teoría de BandasDocumento13 páginasTeoría de BandasEdu HGAinda não há avaliações
- Informe 9-Circuito Divisor de Corriente EléctricaDocumento6 páginasInforme 9-Circuito Divisor de Corriente EléctricaMishu EstefyAinda não há avaliações
- Ejercicios ResistenciasDocumento3 páginasEjercicios ResistenciasTateAinda não há avaliações
- 298 Capítulo 4 Integral Definida e IntegraciónDocumento1 página298 Capítulo 4 Integral Definida e IntegraciónJhonnatan ChicoAinda não há avaliações
- 03 Sistema Periodico SolucionarioDocumento10 páginas03 Sistema Periodico SolucionarioCristina FernandezAinda não há avaliações
- Trabajo de La CatapultaDocumento10 páginasTrabajo de La CatapultaKaren Yudith De La Cruz GuillenAinda não há avaliações
- 01 Magnitudes, Analisis Dimensional y Conversión de UnidadesDocumento37 páginas01 Magnitudes, Analisis Dimensional y Conversión de UnidadesYerick Blanco SalazarAinda não há avaliações
- Circuitos Corriente Directa y Leyes de Kirchhoff PDF FreeDocumento3 páginasCircuitos Corriente Directa y Leyes de Kirchhoff PDF FreeMarcelo Marques AraujoAinda não há avaliações
- Hoja 7 - Dinámica 1Documento50 páginasHoja 7 - Dinámica 1Jorman Sebastian ChuquerAinda não há avaliações
- Hoja de Problemas de Clase 7Documento2 páginasHoja de Problemas de Clase 7José Antonio Marín ArcasAinda não há avaliações
- CEM4042 Cap 1-2 - Análisis Vectorial Sadiku-2014Documento19 páginasCEM4042 Cap 1-2 - Análisis Vectorial Sadiku-2014Hector VergaraAinda não há avaliações
- Maquina de AtwoodDocumento3 páginasMaquina de AtwooddeadpoolAinda não há avaliações
- Atomo ResueltosDocumento45 páginasAtomo ResueltosJorge PibaqueAinda não há avaliações
- Efecto Túnel A Través de Una Barrera de Energía PotencialDocumento12 páginasEfecto Túnel A Través de Una Barrera de Energía PotencialRonal Antonio Zeballos Quispe100% (1)
- Energia ReticularDocumento3 páginasEnergia ReticularAndres F. VelasquezAinda não há avaliações
- Puntos 4-6Documento4 páginasPuntos 4-6alejo uribeAinda não há avaliações
- Fundamento Conceptual Nº1Documento3 páginasFundamento Conceptual Nº1Christian ChazoAinda não há avaliações
- Estructura Cristalina Parte 2Documento38 páginasEstructura Cristalina Parte 2Neiver Castro JulioAinda não há avaliações
- IEE Tema3 MaquinasElectricasDocumento21 páginasIEE Tema3 MaquinasElectricasChristian FernandezAinda não há avaliações
- COMPENDIO Unidad 1Documento34 páginasCOMPENDIO Unidad 1Luis Alberto Barragán VillacresesAinda não há avaliações
- Diaz Visitacion Guia 1ra-SemanaDocumento24 páginasDiaz Visitacion Guia 1ra-SemanaJuan Carlos Diaz Visitacion100% (1)
- 05-Teoría de Conjuntos (RESPUESTAS)Documento14 páginas05-Teoría de Conjuntos (RESPUESTAS)drivers SoporteAinda não há avaliações
- Cuadro Comparativo Enlaces QuimicosDocumento2 páginasCuadro Comparativo Enlaces QuimicosPedro Antonio RT100% (6)
- Cuadro Comparativo de Propiedades de Los Enlaces QuimicosDocumento2 páginasCuadro Comparativo de Propiedades de Los Enlaces QuimicosJose Enrique Toledo FelipeAinda não há avaliações
- Enlace QuimicoDocumento6 páginasEnlace QuimicoJeferson rodriguez lozanoAinda não há avaliações
- Queso PanelaDocumento13 páginasQueso Paneladavidem07Ainda não há avaliações
- Formulario Quimica Comun Psu 2018 FinalDocumento18 páginasFormulario Quimica Comun Psu 2018 FinalLuis EspinosaAinda não há avaliações
- Ciclohexanona PrácticaDocumento6 páginasCiclohexanona PrácticaSain Bear RAinda não há avaliações
- Medios de Cultivo Preparación y EsterilizaciónDocumento3 páginasMedios de Cultivo Preparación y EsterilizaciónAnthony GuevaraAinda não há avaliações
- Reporte 1 - Introduccion Al LaboratorioDocumento6 páginasReporte 1 - Introduccion Al LaboratorioFranyel Perez MendezAinda não há avaliações
- DeberDocumento6 páginasDeberIbeth CajoAinda não há avaliações
- Grupo 232005 1 Tarea 2Documento23 páginasGrupo 232005 1 Tarea 2Julian DavidAinda não há avaliações
- Visita Técnica Realizada A La Mina HuaratoDocumento4 páginasVisita Técnica Realizada A La Mina HuaratoFredy Solano PimentelAinda não há avaliações
- Fluidos-Giancoli - PDF Fisicaaaaaaaaaaaaaaaaaa PDFDocumento5 páginasFluidos-Giancoli - PDF Fisicaaaaaaaaaaaaaaaaaa PDFAnonymous 0iuLGhqPKaAinda não há avaliações
- 5.3 Ejemplo para Plan de Lección - Filtro CaseroDocumento2 páginas5.3 Ejemplo para Plan de Lección - Filtro CaseroGerardo IvanAinda não há avaliações
- Guia de Laboratorio 2023-IDocumento65 páginasGuia de Laboratorio 2023-Isergiolastra80Ainda não há avaliações
- Separacion de Mo Por Centrifugacion FiltracionDocumento27 páginasSeparacion de Mo Por Centrifugacion FiltracionLuis De Jesus Toro RojasAinda não há avaliações
- Mantenimiento de Sistemas HidraulicosDocumento13 páginasMantenimiento de Sistemas HidraulicosVictor Gaytan RuizAinda não há avaliações
- Cuestionario Previo 5Documento5 páginasCuestionario Previo 5Elias Cruz JimenezAinda não há avaliações
- Tipos de ResistenciasDocumento2 páginasTipos de ResistenciasGabriela FloresAinda não há avaliações
- OxicorteDocumento4 páginasOxicorteMauricio Ariel Almoancid AgueroAinda não há avaliações
- 210 - FT Rifampicina 300mg Cap Dura - Colmed - Caja X 20 Capsulas - 300000802Documento2 páginas210 - FT Rifampicina 300mg Cap Dura - Colmed - Caja X 20 Capsulas - 300000802ing.andrescubillosAinda não há avaliações
- Aditivos QsiDocumento6 páginasAditivos QsijamilqhAinda não há avaliações
- El Huerto MedicinalDocumento80 páginasEl Huerto Medicinalfcuevaspr1Ainda não há avaliações
- Lipidos Informe LabDocumento4 páginasLipidos Informe LabSilvina Ostojich Saavedra100% (1)
- Formato de Examen Parcial IiDocumento2 páginasFormato de Examen Parcial Iidavid chapoñan ayalaAinda não há avaliações
- Manual General para Lavadoras Samsung PDFDocumento12 páginasManual General para Lavadoras Samsung PDFAlbert GTAinda não há avaliações
- 1.protocolo Administracion de MedicamentosDocumento34 páginas1.protocolo Administracion de MedicamentosJUAN ESTEBANAinda não há avaliações
- Guia de Practica PDFDocumento14 páginasGuia de Practica PDFJharitza Jimenez VasquezAinda não há avaliações
- La FERMENTACIÓN LÁCTICA Es Un Proceso Celular Anaeróbico Donde Se Utiliza GLUCOSA para Obtener ENERGÍA y Donde El Producto de Desecho Es El ÁCIDO LÁCTICODocumento4 páginasLa FERMENTACIÓN LÁCTICA Es Un Proceso Celular Anaeróbico Donde Se Utiliza GLUCOSA para Obtener ENERGÍA y Donde El Producto de Desecho Es El ÁCIDO LÁCTICOGabriela V. OchoaAinda não há avaliações
- Pg-sgc-07 - Procemiento de Instalacion de Ductos de Fierro Negro para Extraccion de HumosDocumento8 páginasPg-sgc-07 - Procemiento de Instalacion de Ductos de Fierro Negro para Extraccion de HumosDaniel Menejes MontesinosAinda não há avaliações
- PVC Contra PvaDocumento3 páginasPVC Contra PvaAle MuakAinda não há avaliações