Escolar Documentos
Profissional Documentos
Cultura Documentos
Feyman
Enviado por
donreyrdDireitos autorais
Formatos disponíveis
Compartilhar este documento
Compartilhar ou incorporar documento
Você considera este documento útil?
Este conteúdo é inapropriado?
Denunciar este documentoDireitos autorais:
Formatos disponíveis
Feyman
Enviado por
donreyrdDireitos autorais:
Formatos disponíveis
Volume I
Lição I - Átomos em movimento
1-1. Introdução (a própria natureza da ciência física nos impõem preterir certas
abordagens pedagógicas)
- Leis básicas: por que aprendeŕ Física em quatro anos ao invés de quatro minutos?;
1. Ainda não conhecemos todas as leis básicas;
2. Tais leis físicas em sua forma mais precisa conhecida atualmente são
absurdamente complexas;
- O princípio da Ciência: o teste de todo o conhecimento é o experimento;
- Um experimento pode estar errado?
1. Motivo trivial;
2. Sendo imprecisos, i.e., as leis que os pautam são más aproximações;
Ex. Lei da massa constante e relatividade restrita;
1-2. A matéria é feita de átomos (Descrição dos gases, sólidos e líquidos)
- Um conhecimento a ser guardado:
Def. (Hip./ Fato atômico). que todas as coisas são feitas
de átomos – pequenas partículas que se movem em constante movimento, atraindo-
se umas às outras quando separadas por pequenas distâncias, mas repelindo-se ao
serem comprimidas umas sobre as outras.
- Ampliando a gota d'água (2000x2000x250), uma visão simplificada das moléculas
d'água;
Falhas:
1. Moléculas com bordas bem definidas;
2. Arranjo bidimensional;
3. Imagem estática;
4. Atração e repulsão entre as moléculas;
- O tamanho de um átomo: Angstrons e o exemplo da maçã e da Terra;
- Conclusão da Hipótese Atômica: a água não desaparecerá devido a atração entre as
moléculas d'água;
- IntDef. (Calor). Movimento das moléculas;
- Conclusão da Hipótese Atômica: a água transforma-se em vapor ao aumentarmos a
temperatura,
pois quando o movimento das moléculas torna-se demasiado intenso, a força de
atranção entre elas não é suficiente para
mantê-las unidas;
- A representação do vapor através da figura 1-2 e suas falhas:
1. Muitas moléculas num quadro muito pequeno;
2. Simplificação do ângulo entre as moléculas;
- Conclusão da hipótese atômica: existência e explicação da pressão;
- IneDef. Pressão: a ideia de 'empurrão médio' e o exemplo das bolas de Tênis
contra a parede;
- Conclusão da hipótese atômica: a força necessária para manter o pistão imóvel é
proprocional a área;
- Conclusão da hipótese atômica: é uma boa aproximação para densidades baixas que a
pressão seja proporcional à densidade;
Por que é aproximação:
1. Há diminuição na pressão, pois há mais átomos exercendo força;
2. Há um aumento na pressão, pois os átomos possuem volume não nulo;
- Conclusão da hipótese atômica: se aumentarmos a temperatura sem mudar a densidade
do gás, a pressão aumenta;
- IntDef. (Gelo). Nova estrutura formada quando a temperatura está muito baixa;
Falha do diagra: bidimensional;
- Rede cristalina, a diferença entre o sólido e o líquido: a posição das partículas
nessa nova estrutura está bem definida em contraste ao que acontece com a água,
na qual há liberdade para as moléculas se movimentarem;
Conclusões:
- o formato hexagonal dos flocos de gelo;
- o encolhimento do gelo ao derreter-se em oposição ao que acontece à maioria
das moléculas;
- Refinando o modelo anterior: o gelo possui calor;
Conclusões:
- as moléculas permanecem em movimento em torno de sua posição na rede
crsitalina;
- Conclusão da hipótese atômica: existêcia e explicação do derretimento;
- IntDef. (Derretimento). Quando aumentamos a temperatura, a oscilação das
moléculas na rede cristalina aumenta em amplitude a ponto de elas se desprenderem
dessa estrutura;
- O zero absoluto: existe uma quantidade mínima de vibração que os átomos podem
ter. Esse quantidade, entretanto, é não nula;
- O hélio é o único elemento que permanece gasoso mesmo no zero absoluto. Para dar
conta do recado, é necessário aumentarmos a temperatura;
1-3. Processos atômicos
- Constituição dos gases atmosféricos;
- Conclusão da hipótese atômica: formação do vapor d'água;
- Diferença entre os equilíbrios dinâmicos do vapor quando o recipiente está aberto
e quando está fechado;
Ex. Aumentar a velocidade de evaporação usando um ventilador;
- Consequência da hipótese atômica: 'Assim, quando elas saem levam calor embora e
quando elas voltam geram calor.';
Exemplos:
- a temperatura é mantida se são houver rede de evaporação;
- o porquê da sopa esfriar quando a sopramos;
- Eventos do equilíbio água-atmosfera que omitimos;
Exemplo: descompressão;
- IntDef. (Íons)
- Mais um (par) equilíbrio dinâmico: dissolução/ cristalização do sal em água;
- O próprio modelo de molécula é, em si, uma aproximação;
- O efeito do aumento de temperatura sobre o equilíbrio solução-precipitação;
1-4. Reações químicas
- DefInt (Reação química Vs. Reação física);
- Não há uma distinção formal entre os dois tipos de reação acima;
- Obs. É possível queimar diamante em ar;
- A combustão incompleta e por que ela é exotérmica;
Ex. Por que ocorre combustão incompleta no motor de um automóvel;
- O trabalhos dos químicos:
1. Descobrindo a composição das moléculas;
2. Nomeando-as;
Exemplos:
- aroma das violetas;
- De volta À hipótese atômica: como sabemos que existem átomos?
1. Chutamos e verificamos se os resultados condizem com a nossa hipótese;
2. Coloides e o Movimento Browniano;
3. Análise de raios X de cristais;
Você também pode gostar
- Atualização Do Sistema Brasileiro de Classificação de Solos - 2003Documento56 páginasAtualização Do Sistema Brasileiro de Classificação de Solos - 2003Iziquiel CecchinAinda não há avaliações
- Diálogos Sobre Pré-História - Mente, Cultura e Sociedade - Volume 2Documento250 páginasDiálogos Sobre Pré-História - Mente, Cultura e Sociedade - Volume 2Larissa MikaelyAinda não há avaliações
- Curso EFNTDocumento152 páginasCurso EFNTalvarogodoiAinda não há avaliações
- LTCAT relatório de condições ambientaisDocumento15 páginasLTCAT relatório de condições ambientaisThamires MouraAinda não há avaliações
- Transmissão de Calor - NoiteDocumento3 páginasTransmissão de Calor - NoiteNuricel Villalonga AguileraAinda não há avaliações
- Autorização para intervenção em APPDocumento2 páginasAutorização para intervenção em APPMelvinAinda não há avaliações
- Own DocumentDocumento2 páginasOwn DocumentdonreyrdAinda não há avaliações
- Own Document 2Documento2 páginasOwn Document 2donreyrdAinda não há avaliações
- Own DocumentDocumento2 páginasOwn DocumentdonreyrdAinda não há avaliações
- B 2 L 1Documento12 páginasB 2 L 1donreyrdAinda não há avaliações
- Own DocumentDocumento2 páginasOwn DocumentdonreyrdAinda não há avaliações
- Own DocumentDocumento1 páginaOwn DocumentdonreyrdAinda não há avaliações
- Own DocumentDocumento2 páginasOwn DocumentdonreyrdAinda não há avaliações
- Own DocumentDocumento2 páginasOwn DocumentdonreyrdAinda não há avaliações
- Own DocumentDocumento1 páginaOwn DocumentdonreyrdAinda não há avaliações
- Own DocumentDocumento2 páginasOwn DocumentdonreyrdAinda não há avaliações
- Own DocumentDocumento1 páginaOwn DocumentdonreyrdAinda não há avaliações
- Own DocumentDocumento2 páginasOwn DocumentdonreyrdAinda não há avaliações
- Own DocumentDocumento1 páginaOwn DocumentdonreyrdAinda não há avaliações
- AnkiDocumento6 páginasAnkidonreyrdAinda não há avaliações
- Calc2 2008 1 p1 Gabarito PDFDocumento4 páginasCalc2 2008 1 p1 Gabarito PDFdonreyrd0% (1)
- Passagens - A NascenteDocumento11 páginasPassagens - A NascentedonreyrdAinda não há avaliações
- Untitled 1dfbvczDocumento1 páginaUntitled 1dfbvczdonreyrdAinda não há avaliações
- Own DocDocumento1 páginaOwn DocdonreyrdAinda não há avaliações
- Mar Salgado - Das PoëmDocumento1 páginaMar Salgado - Das PoëmdonreyrdAinda não há avaliações
- Passagens - A NascenteDocumento11 páginasPassagens - A NascentedonreyrdAinda não há avaliações
- Passagens - A NascenteDocumento11 páginasPassagens - A NascentedonreyrdAinda não há avaliações
- PoemaDocumento1 páginaPoemadonreyrdAinda não há avaliações
- Novo Documento de Texto6785Documento1 páginaNovo Documento de Texto6785donreyrdAinda não há avaliações
- Passagens - A NascenteDocumento11 páginasPassagens - A NascentedonreyrdAinda não há avaliações
- 10 Músicas Do Exalta - CifrasDocumento13 páginas10 Músicas Do Exalta - CifrasdonreyrdAinda não há avaliações
- Poema 2.0Documento1 páginaPoema 2.0donreyrdAinda não há avaliações
- TalvezDocumento1 páginaTalvezdonreyrdAinda não há avaliações
- Novo Documento de Texto678Documento1 páginaNovo Documento de Texto678donreyrdAinda não há avaliações
- Novo Documento de TextoDocumento1 páginaNovo Documento de TextodonreyrdAinda não há avaliações
- Química Geral IEQ614 Lista1Documento3 páginasQuímica Geral IEQ614 Lista1Anderson Flavio 080% (1)
- Opolítica Dos Recursos Naturais - Minérios e Minerais Energéticos PDFDocumento38 páginasOpolítica Dos Recursos Naturais - Minérios e Minerais Energéticos PDFRicardo Ogusku100% (3)
- Química Verde - ResumoDocumento13 páginasQuímica Verde - ResumoMartim L FAinda não há avaliações
- O estudo das propriedades da matériaDocumento84 páginasO estudo das propriedades da matériaGabrieli LagoooAinda não há avaliações
- Ebook NR 9 NR 15 NR 16 e NR 24Documento22 páginasEbook NR 9 NR 15 NR 16 e NR 24Andreia AzevedoAinda não há avaliações
- 3 - AdsorçãoDocumento8 páginas3 - AdsorçãoMarcos GarcezAinda não há avaliações
- Densidade RelatórioDocumento9 páginasDensidade RelatórioTATIANE DE OMENA LIMAAinda não há avaliações
- Lista 1 Propriedades Dos Fluidos Plano de Carga e ManometriaDocumento21 páginasLista 1 Propriedades Dos Fluidos Plano de Carga e ManometriaThiago LoboAinda não há avaliações
- Relatório 1 Química InorgânicaDocumento7 páginasRelatório 1 Química InorgânicaPriscila Guardia IanhezAinda não há avaliações
- Oficina Temática Uma Proposta Metodológica para o Ensino Do Modelo Atômico de BohrDocumento15 páginasOficina Temática Uma Proposta Metodológica para o Ensino Do Modelo Atômico de BohrGiovanna StefanelloAinda não há avaliações
- 3 Exercícios de Índices FísicosDocumento5 páginas3 Exercícios de Índices FísicosFernando Aguiar0% (1)
- Universidade Federal Do Pará Instituto de Geociências Programa de Pós-Graduação em Geologia E GeoquímicaDocumento130 páginasUniversidade Federal Do Pará Instituto de Geociências Programa de Pós-Graduação em Geologia E GeoquímicaTiago PereiraAinda não há avaliações
- Fenômenos de Transporte ListaDocumento4 páginasFenômenos de Transporte ListaEduardo PizzaniAinda não há avaliações
- Estrutura Atômica: Lista de Exercícios de Química InorgânicaDocumento10 páginasEstrutura Atômica: Lista de Exercícios de Química InorgânicaFabiano SantosAinda não há avaliações
- Planeta Terra: Tempo Geológico e Histórico. O TempoDocumento7 páginasPlaneta Terra: Tempo Geológico e Histórico. O TempobeccaAinda não há avaliações
- Proteção da camada de ozono e efeitos da sua destruiçãoDocumento3 páginasProteção da camada de ozono e efeitos da sua destruiçãoCristina MarquesAinda não há avaliações
- Degradação e Conservação AmbientalDocumento59 páginasDegradação e Conservação AmbientalAnderson Basílio100% (1)
- Atividades 2° AnoDocumento3 páginasAtividades 2° AnoanalaurademoraissilvaAinda não há avaliações
- Desenvolvimento sustentável cuida recursos futurosDocumento3 páginasDesenvolvimento sustentável cuida recursos futurosjrfrAinda não há avaliações
- TDS - PT MACMAT R1 8127GN - Rev.24 20211104Documento1 páginaTDS - PT MACMAT R1 8127GN - Rev.24 20211104almirante_andreAinda não há avaliações
- Re82133 Fa11 Teste1Documento6 páginasRe82133 Fa11 Teste1Ana 2005Ainda não há avaliações
- Fisica - 12a Classe - 2019-2a EpocaDocumento5 páginasFisica - 12a Classe - 2019-2a EpocaAnildaAinda não há avaliações
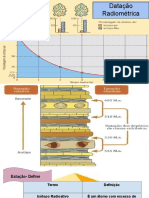
- Datação RadiometricaDocumento32 páginasDatação RadiometricazecaAinda não há avaliações