Escolar Documentos
Profissional Documentos
Cultura Documentos
EXERCÍCIOS DE FÍSICO-QUÍMICA – PROPRIEDADES COLIGATIVAS
Enviado por
rsantini40 notas0% acharam este documento útil (0 voto)
127 visualizações2 páginasExercícios - Diagrama de Fases
Título original
Exercícios Propriedades Coligativas 09-2015
Direitos autorais
© © All Rights Reserved
Formatos disponíveis
PDF, TXT ou leia online no Scribd
Compartilhar este documento
Compartilhar ou incorporar documento
Você considera este documento útil?
Este conteúdo é inapropriado?
Denunciar este documentoExercícios - Diagrama de Fases
Direitos autorais:
© All Rights Reserved
Formatos disponíveis
Baixe no formato PDF, TXT ou leia online no Scribd
0 notas0% acharam este documento útil (0 voto)
127 visualizações2 páginasEXERCÍCIOS DE FÍSICO-QUÍMICA – PROPRIEDADES COLIGATIVAS
Enviado por
rsantini4Exercícios - Diagrama de Fases
Direitos autorais:
© All Rights Reserved
Formatos disponíveis
Baixe no formato PDF, TXT ou leia online no Scribd
Você está na página 1de 2
MINISTÉRIO DA EDUCAÇÃO
SECRETARIA DE EDUCAÇÃO PROFISSIONAL E TECNOLÓGICA
INSTITUTO FEDERAL DE EDUCAÇÃO, CIÊNCIA E TECNOLOGIA DE SANTA CATARINA
CÂMPUS LAGES
CURSO TÉCNICO EM ANÁLISES QUÍMICAS
EXERCÍCIOS DE FÍSICO-QUÍMICA – PROPRIEDADES COLIGATIVAS
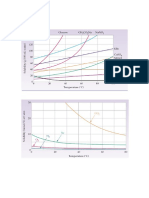
1) Observe o diagrama de fase mostrado a seguir. 4)
5)Observe diagrama de fases da substância X,
representado abaixo:
Pode-se concluir, corretamente, que uma
substância que passou pelo processo de sublimação
segue a trajetória
a) X ou Y.
b) Y ou U.
c) U ou V.
d) V ou X.
2)
a) Em que estado físico a substância X se encontra
em condições ambientes (pressão de 1 atm e
temperatura de 25 °C)?
b) Se essa mesma substância for aquecida na pressão
de 1 atm, em que temperatura, aproximadamente,
sofrerá fusão?
c) Qual é o ponto de ebulição da substância X à
pressão de 0,5 atm?
d) Se abaixarmos a pressão para 0,2 atm, a
substância X ainda poderá entrar em ebulição?
Explique.
6) Sabe-se que por osmose o solvente de uma
solução mais diluída atravessa uma membrana
semipermeável em direção da solução mais
concentrada. Sabe-se, também, que um peixe de água
doce é hipertônico em relação a água do rio e
hipotônico a água do mar. Se um peixe de água doce
for colocado na água do mar ele:
a) morre porque entra água do mar no seu corpo.
b) morre porque sai água do seu corpo.
c) morre porque entra sal no seu corpo.
d) morre porque sai sal do seu corpo.
3) e) sobrevive normalmente.
7) À temperatura de 27 °C, 500 mL de uma solução
aquosa contém 34,2 g de açúcar (sacarose,
C12H22O11). Qual é a pressão osmótica dessa solução?
8) 36 g de glicose (C6H12O6) foram dissolvidos em 500
g de água.
a) Sabendo-se que a pressão de vapor da água a
20 °C é igual a 0,023 atm, calcule a pressão de vapor
da solução.
b) Calcule a temperatura de congelamento da solução,
sabendo que a constante crioscópica da água é igual
a 1,853 K.kg.mol-1.
c) Se no lugar de glicose adicionássemos a mesma
quantidade, em mols, de cloreto de sódio, o efeito
causado seria o mesmo? Explique.
9)
10) Foi observado que o cozimento de meio quilo de
batatas em 1 litro de água é mais rápido
se adicionarmos 200g de sal à água do
cozimento. Considere as seguintes possíveis
explicações para o fato:
I. A adição de sal provoca um aumento da
temperatura de ebulição da água.
II. A adição de sal provoca um aumento da
pressão de vapor.
III. O sal adicionado não altera a temperatura
de ebulição da água, mas reage com o
amido das batatas.
Está(ao) correta(s) a(s) explicação(ões):
a) I apenas.
b) II apenas.
c) III apenas.
d) I e II apenas.
e) I, II e III.
11) Das soluções aquosas abaixo, qual terá a mesma
temperatura de ebulição que uma solução aquosa de
cloreto de sódio (NaCl) 0,1 mol/L?
a) sulfato de cobre (CuSO4) 0,2 mol/L.
b) cloreto de cálcio (CaCl 2) 0,1 mol/L.
c) bicarbonato de sódio (NaHCO 3) 0,3 mol/L.
d) glicose (C6H12O6) 0,1 mol/L.
e) iodeto de potássio (KI) 0,1 mol/L.
Você também pode gostar
- 05-Separações de MisturaDocumento6 páginas05-Separações de Misturanv77vnmAinda não há avaliações
- Propriedades Coligativas 2 AnoDocumento31 páginasPropriedades Coligativas 2 AnoJúnior FerreiraAinda não há avaliações
- Questo-Es - Propriedades ColigativasDocumento18 páginasQuesto-Es - Propriedades ColigativasSergio NweyAinda não há avaliações
- Quím 2o EM P1 1o BimDocumento4 páginasQuím 2o EM P1 1o Bimalambique51100% (1)
- Exercício Propriedades ColigativasDocumento3 páginasExercício Propriedades ColigativasÉrica LimaAinda não há avaliações
- 2012 - TMedicina - Quimica - Borges - Exercícios de Solubilidade - SiteDocumento12 páginas2012 - TMedicina - Quimica - Borges - Exercícios de Solubilidade - SiteDhieniffer FerreiraAinda não há avaliações
- Solubilidade da lactose e cristalizaçãoDocumento12 páginasSolubilidade da lactose e cristalizaçãoTiago RodriguesAinda não há avaliações
- PDF - Lista 41 - Propriedades ColigativasDocumento4 páginasPDF - Lista 41 - Propriedades ColigativasLucas AmorimjsAinda não há avaliações
- Soluções: tipos, concentração e solubilidadeDocumento8 páginasSoluções: tipos, concentração e solubilidadeVitóriaAinda não há avaliações
- Cbae4ae1 Db5c 4fc9 8184 5115d78789b8 Fisico QuimicaDocumento79 páginasCbae4ae1 Db5c 4fc9 8184 5115d78789b8 Fisico QuimicaNina Bob Brown100% (1)
- Pressão Osmótica em BiomedicinaDocumento2 páginasPressão Osmótica em BiomedicinaAlbertoAlecio100% (1)
- Atividade Recuperativa 1 Bim - 2° AnoDocumento2 páginasAtividade Recuperativa 1 Bim - 2° Anorubens.costaAinda não há avaliações
- Atividades Propriedades ColigativasDocumento4 páginasAtividades Propriedades ColigativasJocimara MonsaniAinda não há avaliações
- 1 Ano 1bimestreaDocumento2 páginas1 Ano 1bimestreaRonan BarrosAinda não há avaliações
- Estudo das SoluçõesDocumento5 páginasEstudo das SoluçõesKyuraKingAinda não há avaliações
- Lista Propriedades ColigativasDocumento4 páginasLista Propriedades ColigativasAdriele SchaurichAinda não há avaliações
- PropColigDocumento13 páginasPropColigAparecida BatistaAinda não há avaliações
- Química - Pressão de vapor, diagramas de fases e propriedades coligativasDocumento29 páginasQuímica - Pressão de vapor, diagramas de fases e propriedades coligativasRicardo AlvesAinda não há avaliações
- 31-Soluções e SolubilidadeDocumento4 páginas31-Soluções e Solubilidadenv77vnm100% (2)
- Química FBDocumento3 páginasQuímica FBANNA KARIENINAAinda não há avaliações
- Equilíbrio Químico e Transporte de OxigênioDocumento29 páginasEquilíbrio Químico e Transporte de OxigênioFernandes YoshimotoAinda não há avaliações
- Exercicios de SolubilidadeDocumento6 páginasExercicios de Solubilidadesua mae de 4Ainda não há avaliações
- Solubilidade de sais e açúcares: curvas e fatores que influenciamDocumento22 páginasSolubilidade de sais e açúcares: curvas e fatores que influenciamRebecaAinda não há avaliações
- Lista de Exerccios de QuímicaDocumento3 páginasLista de Exerccios de QuímicaJoão PedroAinda não há avaliações
- Arquivo de Soluções Do Prof° VieiraDocumento9 páginasArquivo de Soluções Do Prof° VieiravieirasalesAinda não há avaliações
- Exercícios de OsmometriaDocumento2 páginasExercícios de Osmometriamujers7_Ainda não há avaliações
- 19 20mudan C3 A7as 20de 20estados 20f C3 ADsicos 20e 20diagramasDocumento20 páginas19 20mudan C3 A7as 20de 20estados 20f C3 ADsicos 20e 20diagramasMicaelaNeivaAinda não há avaliações
- Exercicios Propriedades Coligativas (Ultimos 3 Resolvidos)Documento4 páginasExercicios Propriedades Coligativas (Ultimos 3 Resolvidos)Tainara SantosAinda não há avaliações
- Propriedades dos materiaisDocumento4 páginasPropriedades dos materiaisElisa BeteAinda não há avaliações
- Propriedades Coligativas Soluções Química GeralDocumento7 páginasPropriedades Coligativas Soluções Química GeralIsaias Silva0% (1)
- Exercícios Físico-Química SolubilidadeDocumento3 páginasExercícios Físico-Química SolubilidadeAlfredo Sahade VespaAinda não há avaliações
- OSMOSE (Pressão OsmóticaDocumento25 páginasOSMOSE (Pressão OsmóticaGleisonAinda não há avaliações
- Calor latente e mudanças de estado físico da águaDocumento2 páginasCalor latente e mudanças de estado físico da águaJardel Del RosaAinda não há avaliações
- Propriedades coligativas de soluçõesDocumento6 páginasPropriedades coligativas de soluçõesLucas CamargoAinda não há avaliações
- Exercícios de coligativasDocumento2 páginasExercícios de coligativasVr BettiolAinda não há avaliações
- Revisao Unidade 2 e 3Documento6 páginasRevisao Unidade 2 e 3UEVERTON CARLOS DO CARMO DA SILVAAinda não há avaliações
- Avaliação A3 - 2 Etapa - Química e Química Aplicada - Turma 321 - Adaptada 2023Documento5 páginasAvaliação A3 - 2 Etapa - Química e Química Aplicada - Turma 321 - Adaptada 2023Saulo LeiteAinda não há avaliações
- 1 Ano 1bimestrebDocumento2 páginas1 Ano 1bimestrebRonan BarrosAinda não há avaliações
- Curvas de solubilidade - Lista de exercíciosDocumento2 páginasCurvas de solubilidade - Lista de exercíciosMax NunesAinda não há avaliações
- Prop Coligativas Slides ExercíciosDocumento9 páginasProp Coligativas Slides ExercíciosPedro Lucas Ferreira RodriguesAinda não há avaliações
- Exercicio 1 - 2º AnoDocumento1 páginaExercicio 1 - 2º Anoanaduarte181993Ainda não há avaliações
- Densidades de refrigerantes e comportamento de garrafas em tanqueDocumento2 páginasDensidades de refrigerantes e comportamento de garrafas em tanqueGeiziane OliveiraAinda não há avaliações
- Questoes Quimica - Estados, Misturas e SubstanciasDocumento6 páginasQuestoes Quimica - Estados, Misturas e SubstanciasLarissa PortellaAinda não há avaliações
- Gab - gb22 Lrp3b.qui 2emaeb 3bimDocumento3 páginasGab - gb22 Lrp3b.qui 2emaeb 3bimabidabugaAinda não há avaliações
- Trabalho 3: QuímicaDocumento2 páginasTrabalho 3: QuímicaBruna AlvarengaAinda não há avaliações
- Exercício - Eureka QuímicaDocumento1 páginaExercício - Eureka QuímicaJosé AllisonAinda não há avaliações
- Equilíbrio Iônico e pHDocumento5 páginasEquilíbrio Iônico e pHedfloydAinda não há avaliações
- PropriedadescoligativasDocumento6 páginasPropriedadescoligativasCatiele DCAinda não há avaliações
- Recuperação de Física Segunda Série 2º TrimestreDocumento11 páginasRecuperação de Física Segunda Série 2º TrimestreMarguiené BragaAinda não há avaliações
- DL 50Documento11 páginasDL 50Rita Sofia Ramos MesquitaAinda não há avaliações
- Química CEFET-MGDocumento3 páginasQuímica CEFET-MGFelipe AugustoAinda não há avaliações
- Química - Lista de Exercícios de Soluções e SolubilidadeDocumento2 páginasQuímica - Lista de Exercícios de Soluções e SolubilidadeCELI ANTONIA DE DEUSAinda não há avaliações
- Propriedades físicas da matériaDocumento21 páginasPropriedades físicas da matériaNanda OdebrechtAinda não há avaliações
- Lista 01Documento7 páginasLista 01Edson CardosoAinda não há avaliações
- EXERCÍCIOSDocumento4 páginasEXERCÍCIOSjosilucaAinda não há avaliações
- Química Prof. Durval Exercícios Corrigidos 02.03 2º AnoDocumento3 páginasQuímica Prof. Durval Exercícios Corrigidos 02.03 2º Anothomasbarreto213Ainda não há avaliações
- Propriedades ColigativasDocumento2 páginasPropriedades ColigativasLEVI LOPES DA SILVAAinda não há avaliações
- Apostila Química Orgânica: Terpenos E Rotas De SínteseNo EverandApostila Química Orgânica: Terpenos E Rotas De SínteseAinda não há avaliações
- Água Viva - Nutriente Nº 1 No Corpo | Artigo ProfundoNo EverandÁgua Viva - Nutriente Nº 1 No Corpo | Artigo ProfundoAinda não há avaliações
- Matemática - 9°ano - 1° TrimestreDocumento132 páginasMatemática - 9°ano - 1° Trimestrersantini4100% (1)
- Material Do Mec - ÁguaDocumento22 páginasMaterial Do Mec - Águagilbertoazevedo5345Ainda não há avaliações
- 1ºano P1 3ºbimDocumento4 páginas1ºano P1 3ºbimrsantini4Ainda não há avaliações
- Prova 2ºano 1ºtrimDocumento3 páginasProva 2ºano 1ºtrimrsantini4Ainda não há avaliações
- Teste 2ºtrim 1º QuimDocumento3 páginasTeste 2ºtrim 1º Quimrsantini4Ainda não há avaliações
- Rec 1º PDFDocumento2 páginasRec 1º PDFrsantini4Ainda não há avaliações
- 1ºano P2 PDFDocumento3 páginas1ºano P2 PDFrsantini4Ainda não há avaliações
- Prova 3ºano 1ºtrimDocumento3 páginasProva 3ºano 1ºtrimrsantini4Ainda não há avaliações
- Educação inclusiva: da antiguidade à proteção dos direitos humanosDocumento46 páginasEducação inclusiva: da antiguidade à proteção dos direitos humanosrsantini4Ainda não há avaliações
- Prova 1ºano 1ºtrimDocumento3 páginasProva 1ºano 1ºtrimrsantini4Ainda não há avaliações
- 1ºano P2Documento3 páginas1ºano P2rsantini4Ainda não há avaliações
- Ligação iônica e covalenteDocumento2 páginasLigação iônica e covalentersantini4Ainda não há avaliações
- pRINCÍPIOS DA qUÍMICA aNALÍTICA PDFDocumento9 páginaspRINCÍPIOS DA qUÍMICA aNALÍTICA PDFrsantini4Ainda não há avaliações
- Análise Do Panorama Energético Mundial e Perspectivas para As Fontes Renováveis Na Paraíba2Documento10 páginasAnálise Do Panorama Energético Mundial e Perspectivas para As Fontes Renováveis Na Paraíba2rsantini4Ainda não há avaliações
- Tabela Periódica ExeDocumento2 páginasTabela Periódica Exersantini4100% (1)
- AD1-Rosa Maria Santini Prado-Licenciatura em Química - OdtDocumento4 páginasAD1-Rosa Maria Santini Prado-Licenciatura em Química - Odtrsantini4Ainda não há avaliações
- Ensino da Tabela Periódica por meio de jogo e TICDocumento8 páginasEnsino da Tabela Periódica por meio de jogo e TICrsantini4Ainda não há avaliações
- Curiosidades Químicas 4 - O Eteno e o Amadurecimento de Frutas PDFDocumento1 páginaCuriosidades Químicas 4 - O Eteno e o Amadurecimento de Frutas PDFrsantini4Ainda não há avaliações
- Prática 1 - 2013Documento7 páginasPrática 1 - 2013rsantini4100% (1)
- Relatório IDocumento4 páginasRelatório Irsantini4Ainda não há avaliações
- Análise Térmica Aplicada À CosmetologiaDocumento10 páginasAnálise Térmica Aplicada À Cosmetologiapapitoo_manAinda não há avaliações
- URPA Cuidados pós-anestésicosDocumento57 páginasURPA Cuidados pós-anestésicosIhone TeixeiraAinda não há avaliações
- PGRSS PrencherDocumento13 páginasPGRSS Prencherroone45 45Ainda não há avaliações
- Pibic Pivic Resultado FinalDocumento58 páginasPibic Pivic Resultado FinalhaglfwkhseAinda não há avaliações
- TCC CláudioDocumento20 páginasTCC CláudioThiago MonteiroAinda não há avaliações
- Aula 6 (Unidade 3) - Sistemas de CusteioDocumento7 páginasAula 6 (Unidade 3) - Sistemas de CusteioHerminio JuvenalsAinda não há avaliações
- Como monitorar esterilização com indicadoresDocumento29 páginasComo monitorar esterilização com indicadoresNeocamargoAinda não há avaliações
- 3ºem Lingagensp1203Documento20 páginas3ºem Lingagensp1203GuiAinda não há avaliações
- APS - Gestão em EnfermagemDocumento4 páginasAPS - Gestão em EnfermagemLucas FelipeAinda não há avaliações
- Anamnese Criança AdolescenteDocumento5 páginasAnamnese Criança AdolescenteEliziana De Paula Lucas85% (13)
- Membrana Plasmática e A PermeabilidadeDocumento39 páginasMembrana Plasmática e A PermeabilidadeWesleyJúniorAinda não há avaliações
- Controle microbiológico na bovinocultura leiteiraDocumento7 páginasControle microbiológico na bovinocultura leiteiraAna Clara NevesAinda não há avaliações
- Concurso Admissão 2021 - Área do CandidatoDocumento3 páginasConcurso Admissão 2021 - Área do CandidatoCarlos AlbertoAinda não há avaliações
- Pessoas Com DeficiênciaDocumento7 páginasPessoas Com DeficiênciaHelena LibardiAinda não há avaliações
- Resolvendo problemas com unidades de medidaDocumento4 páginasResolvendo problemas com unidades de medidaDionaldo DuarteAinda não há avaliações
- UFCD 3564 FT1 CorrigendaDocumento3 páginasUFCD 3564 FT1 CorrigendaMartaMatos100% (1)
- Validação embalagens alimentosDocumento25 páginasValidação embalagens alimentosCassilda CarvalhoAinda não há avaliações
- A Água Ocupa A Maior Parte Do PlanetaDocumento3 páginasA Água Ocupa A Maior Parte Do PlanetaLariissa StefanyAinda não há avaliações
- Receita de Danoninho Caseiro - TudogostosoDocumento4 páginasReceita de Danoninho Caseiro - TudogostosoIvete AlmeidaAinda não há avaliações
- Terapia Cognitiva EsquemasDocumento4 páginasTerapia Cognitiva EsquemasMariana SousaAinda não há avaliações
- Use of Drones For ResearchDocumento194 páginasUse of Drones For ResearchMatheus GrandeAinda não há avaliações
- Carboidratos e LipídiosDocumento14 páginasCarboidratos e LipídiosArizonaAinda não há avaliações
- Livro de Receitas Tia Nastacia CulinariaDocumento16 páginasLivro de Receitas Tia Nastacia CulinarianastaciadositioAinda não há avaliações
- Maquinas 172 Online PDFDocumento52 páginasMaquinas 172 Online PDFMarcondes PereiraAinda não há avaliações
- Montreal Tabela AplicaçãoDocumento1 páginaMontreal Tabela AplicaçãojokekaAinda não há avaliações
- ?? Noticias 20220525 @O JornalDocumento40 páginas?? Noticias 20220525 @O JornalJPhil NacaAinda não há avaliações
- Gabinete Do Deputado Roosevelt Vilela - Gab. 14Documento6 páginasGabinete Do Deputado Roosevelt Vilela - Gab. 14Mandato InterativoAinda não há avaliações
- Microsoft Word - Manual PatologiasDocumento122 páginasMicrosoft Word - Manual Patologiassoares.nguerra8634Ainda não há avaliações
- Homeopatia na Medicina VeterináriaDocumento21 páginasHomeopatia na Medicina Veterinárianatalia100% (3)
- Plano Alimentar - Denise Careli de MeloDocumento18 páginasPlano Alimentar - Denise Careli de MeloMarialina CarvalhoAinda não há avaliações