Escolar Documentos
Profissional Documentos
Cultura Documentos
Apoio Às Atividades Laboratoriais
Enviado por
anitadiogoTítulo original
Direitos autorais
Formatos disponíveis
Compartilhar este documento
Compartilhar ou incorporar documento
Você considera este documento útil?
Este conteúdo é inapropriado?
Denunciar este documentoDireitos autorais:
Formatos disponíveis
Apoio Às Atividades Laboratoriais
Enviado por
anitadiogoDireitos autorais:
Formatos disponíveis
6 Apoio às Atividades Laboratoriais
No Domínio 1 estão previstas três aulas de índole laboratorial (de três tempos cada). Nestas aulas
realizar-se-ão três atividades experimentais.
No Domínio 2 estão previstas quatro aulas de índole laboratorial (de três tempos cada). Nestas
aulas realizar-se-ão quatro atividades experimentais.
AL 1.1 Volume e número de moléculas de uma gota de água (CAL pp. 15-17)
Deve iniciar-se esta atividade com alguns conceitos sobre medição, questionando os alunos sobre
um processo de medir a massa e o volume de uma gota de água, orientando a discussão de forma
que concluam que a medição deve fazer-se a partir da massa e do volume de um número elevado de
gotas. Propõe-se que se determine a massa e o volume de 300 gotas de água.
Os alunos podem ser questionados acerca de qual das grandezas medidas (massa e volume) deve
ser usada para determinar o número de moléculas de água numa gota.
Resolução das questões teórico-práticas da AL 1.1
1. Afirmações verdadeiras: (B); (D); (F). Afirmações falsas: (A); (C); (E); (G).
2.
2.1 Aluno A. Os valores obtidos estão mais próximos uns dos outros do que os obtidos pelo aluno B.
2.2 Aluno B. O valor médio dos resultados obtidos pelo aluno A é 2,038 e o dos obtidos pelo aluno B
é 2,033, que é igual ao valor real da massa da amostra.
3. Aluno A. O algarismo do número que corresponde à menor divisão da escala ainda é algarismo
exato. Neste caso, é o primeiro zero. Como o resultado deve ainda apresentar um algarismo
aproximado, será 15,00 mL.
0,1
Incerteza da medição = 2
= 0,05 mL.
4. Opção (B).
10,001 – 9,999
5. 𝑚 = 10,001 g; Incerteza relativa = 10,001
× 100 ⇔ Incerteza relativa = 0,020%;
𝑚água = 10,001 ± 0,020%.
6.
6.1 𝑚H2 O = 28,50 – 25,02 ⇔ 𝑚H2 O = 3,48 g.
6.2 ± 0,01 g.
0,01
6.3 Incerteza relativa = × 100 ⇔ Incerteza relativa = 0,29%.
3,48
3,48
6.4 𝑚1 gota = 100
⇔ 𝑚1 gota = 3,48 × 10–2 g;
𝑚 3,48 × 10–2
𝑀(H2 O) = 18,02 g mol−1 ; 𝑛 = 𝑀
→𝑛= 18,02
⇔ 𝑛 = 1,93 × 10−3 mol H2 O;
𝑁 = 𝑛 × 𝑁A → 𝑁 = 1,93 × 10−3 × 6,02 × 10 23
⇔ 𝑁 = 1,93 × 1020 moléculas de H2 O.
Editável e fotocopiável © Texto | Novo Jogo de Partículas 10 131
AL 1.2 Teste de chama (CAL pp. 18-19)
Nesta atividade propõem-se dois procedimentos alternativos. Cabe ao professor selecionar o
procedimento. Em relação aos sais metálicos, os exemplos indicados podem ser substituídos por
outros de catiões desconhecidos. Neste caso, esta atividade pode adquirir um caráter de pesquisa
laboratorial. Se forem usados anéis de cromo-níquel, deve planear-se a atividade de modo que o
mesmo anel seja sempre utilizado na mesma amostra para evitar, o mais possível, o recurso a ácido
clorídrico concentrado para limpeza dos anéis.
Devem ser referidos os aspetos de segurança em relação a fontes de aquecimento e à
manipulação de reagentes.
Resolução das questões teórico-práticas da AL 1.2
1. Sim. Cada metal (catião metálico) tem uma cor de chama própria. A sua análise espetral revelará,
em qualquer situação, as riscas características do elemento.
2. A cor da chama depende do catião metálico presente no sal e não da cor deste. Catiões diferentes
apresentam cores diferentes.
3. O teste de chama terá de ser sempre complementado com a análise espetral, porque existem metais
(catiões metálicos) cujas chamas têm colorações parecidas.
4. Devido à presença de catiões metálicos no material de combustão.
5. A cor das auroras boreais depende do tipo de partículas que sofrem as excitações e as desexci-
tações.
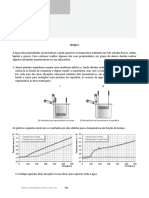
AL 1.3 Densidade relativa de metais (CAL pp. 20-21)
As amostras metálicas devem ser escolhidas tendo em conta a sua existência no laboratório da
escola. Poderão ser de metais como o cobre, o alumínio ou o chumbo, na forma de grãos, fios de
pequena dimensão ou lâminas cujo tamanho seja apropriado às dimensões do colo do picnómetro.
Devem discutir-se erros aleatórios e sistemáticos ligados à influência da temperatura, devidos à
formação de bolhas de ar no interior do picnómetro, a uma secagem inadequada do picnómetro ou à
presença de impurezas no metal em estudo.
Deve introduzir-se o erro percentual associado a um resultado experimental quando há um valor
de referência e a sua relação com a exatidão do resultado.
Resolução das questões teórico-práticas da AL 1.3
1.
1.1 ± 0,01 g.
1.2 𝑚água deslocada = 91,69 – 91,65 ⇔ 𝑚água deslocada = 0,04 g.
𝑚esferas 0,34
1.3 𝑑 = 𝑚água deslocada
→ 𝑑= 0,04
⇔ 𝑑 = 8,5.
3 –3
1.4 𝜌 = 8,5 × 10 kg m .
1.5 Cobre.
132 Editável e fotocopiável © Texto | Novo Jogo de Partículas 10
1.6 Erros de medição nas leituras e possível existência de impurezas no metal.
2. O volume de água deslocado por um corpo mergulhado nessa água corresponde ao volume do corpo.
A massa de água deslocada é:
𝑚 = 𝜌água × 𝑉água deslocada.
Sendo 𝜌água , a 4 °C, igual a 1,0 g cm–3 , 𝑚 = 𝑉corpo .
AL 2.1 Miscibilidade de líquidos (CAL pp. 22-24)
Os líquidos propostos são os indicados no programa. No entanto, poderão ser utilizados outros
líquidos com as características adequadas ao objetivo do trabalho.
Antes de iniciar o procedimento experimental, pode-se sugerir aos alunos que formulem hipóteses
sobre a miscibilidade dos líquidos propostos, com base nas respetivas fórmulas de estrutura.
Devem ser tomadas medidas para lidar com riscos associados à manipulação de alguns líquidos.
Resolução das questões teórico-práticas da AL 2.1
1.
1.1 As moléculas de bromo e de tetracloreto de carbono são apolares. A molécula de água é polar.
1.2
1.2.1 Não miscíveis.
1.2.2 Não miscíveis.
1.2.3 Miscíveis.
2. Uma substância é tanto mais miscível com outra quanto maior for a semelhança das ligações
intermoleculares de cada uma delas.
3. Opção (B). A ureia e a água são substâncias polares com ligações de hidrogénio. Na água são as
ligações O–H e na ureia são as ligações N–H. A ureia não se dissolve em tetracloreto de carbono
porque esta é uma substância apolar.
AL 2.2 Soluções a partir de solutos sólidos (CAL pp. 25-27)
O soluto escolhido deve estar devidamente rotulado para que se possa fazer a necessária
avaliação de riscos. Podem ser utilizados outros sais que originem soluções coradas, atendendo aos
custos e à poluição eventual que poderão causar nas águas dos rios e do mar. Não se devem usar sais
que contenham catiões de metais pesados como chumbo, cromo, cobalto ou níquel.
Uma vez preparadas, as soluções devem ser devidamente guardadas e rotuladas de modo a
poderem ser utilizadas em trabalhos posteriores.
Devem ser discutidos os erros aleatórios e sistemáticos.
Resolução das questões teórico-práticas da AL 2.2
1.
1.1 ± 0,01 g.
Editável e fotocopiável © Texto | Novo Jogo de Partículas 10 133
1.2 𝑀(KMnO4 ) = 158,04 g mol–1;
𝑚 7,90
𝑛 = → 𝑛 = ⇔ 𝑛 = 5,0 × 10–2 mol KMnO4
𝑀 158,04
𝑛 5,0 × 10–2
1.3 Opção (B). 𝑐 = 𝑉
→ 𝑐 = 0,200
⇔ 𝑐 = 0,250 mol dm–3.
1.4 A fórmula iónica de KMnO4 é K + MnO− 4 .
1 mol KMnO4 5,0 × 10–2 mol KMnO4
2 mol de iões
= 𝑥
⇔ 𝑥 = 1,0 × 10–1 mol de iões;
−1 23
𝑁 = 1,0 × 10 × 6,02 × 10 ⇔ 𝑁 = 6,02 × 1022 iões.
2.
2.1
2.1.1 249,85 mL ≤ 𝑉 ≤ 250,15 mL.
2.1.2 Opção (D).
2.2 𝑀(CuSO4 . 5H2 O) = 249,69 g mol−1;
𝑛 = 𝑐 × 𝑉 → 𝑛 = 7,5 × 10–3 mol CuSO4 . 5H2 O;
𝑚 = 𝑛 × 𝑀 → 𝑚 = 7,5 × 10−3 × 249,69 ⇔ 𝑚 = 1,88 g CuSO4 . 5H2 O.
AL 2.3 Diluição de soluções (CAL pp. 28-29)
Os alunos poderão treinar a medição de volumes com pipetas e respetiva pompete, começando
por utilizar água. As pipetas deverão ser da mesma classe, para que os alunos possam comparar as
respetivas incertezas de leitura. Nesta atividade propõe-se que a solução a diluir seja a preparada na
atividade laboratorial anterior e que os fatores de diluição das soluções diluídas a preparar sejam de
2, 4 e 5. Poderão ser utilizados outros fatores de diluição, selecionando balões volumétricos e pipetas
adequadas.
A solução preparada poderá ser armazenada depois de convenientemente rotulada.
Resolução das questões teórico-práticas da AL 2.3
1.
𝑉f 250
1.1 Opção (B). 𝑓 = 𝑉i
→ 5 = 𝑉i
⇔ 𝑉i = 50 mL.
𝑐i 0,5
1.2 𝑓 = → 5 = ⇔ 𝑐f = 0,10 mol dm–3.
𝑐f 𝑐f
1.3
1.3.1 Retiraram-se 50 mL da primeira solução. A quantidade de cloreto de potássio presente neste
volume é:
𝑛 = 𝑐 × 𝑉 → 𝑛 = 0,5 × 0,050 ⇔ 𝑛 = 2,5 × 10–2 mol KCℓ.
𝑛 0,025
1.3.2 𝑐 = 𝑉 → 𝑐 = 0,500 ⇔ 𝑐 = 5,0 × 10–2 mol dm–3;
𝑐m = 𝑐 × 𝑀, sendo 𝑀(KCℓ) 74,55 g mol–1;
𝑐m = 5,0 × 10–2 × 74,55 ⇔ 𝑐m = 3,7 g dm–3 .
2.
2.1 Opção (B).
2.2 𝑉 = 2,500 × 10−1 dm3.
2.3
2.3.1 𝑛i = 𝑛f → 𝑐i × 𝑉i = 𝑐f × 𝑉f → 5,71 × 𝑉i = 50,0 × 10–3 × 0,23 ⇔ 𝑉i = 2,0 × 10–3 dm3 ou 𝑉i = 2,0 mL.
2.3.2 Balão volumétrico de 50 mL; pipeta graduada de 5 mL e pompete; esguicho com água desionizada.
134 Editável e fotocopiável © Texto | Novo Jogo de Partículas 10
2.3.3 Efetuar os cálculos para determinar o volume de solução a retirar da solução-mãe; retirar da
solução-mãe o volume antes calculado com a pipeta e respetiva pompete; transvasar a solução
para um balão volumétrico de 50 mL de capacidade; adicionar água desionizada até ao traço de
referência; rolhar e homogeneizar a solução; rotular devidamente a solução obtida.
AL 2.4 Reação fotoquímica (CAL pp. 30-32)
Para investigar o efeito da luz sobre o cloreto de prata deve usar-se luz branca, luz azul e luz
vermelha, e usar como termo de comparação uma amostra ao abrigo da luz.
Considerar os cuidados a ter nesta atividade, referidos no procedimento experimental.
Resolução das questões teórico-práticas da AL 2.4
1. Fotossíntese e formação e decomposição do ozono.
2. Devido à formação de vapores de cloro prejudiciais à saúde.
3. Para se ver o precipitado de cloreto de prata são necessárias, apenas, pequenas quantidades de
reagentes. Além disso, o nitrato de prata é um reagente de custo elevado.
4. 2 AgBr (aq) → 2 Ag (s) + Br2 (g)
Editável e fotocopiável © Texto | Novo Jogo de Partículas 10 135
Você também pode gostar
- Novo11Q - (Teste 3 - Mai18)Documento5 páginasNovo11Q - (Teste 3 - Mai18)Isabel Vilhena FerreiraAinda não há avaliações
- 1 Ae q11 Teste5 v1Documento14 páginas1 Ae q11 Teste5 v1Luísa CarmoAinda não há avaliações
- Queda LivreDocumento10 páginasQueda LivreVânia Faria100% (1)
- Ae q11 Fich Form 1Documento5 páginasAe q11 Fich Form 1carla50% (2)
- Física 11o exercícios 1o unidadeDocumento33 páginasFísica 11o exercícios 1o unidadeDiana Castro100% (1)
- Soluções Químicas: Preparação e DiluiçãoDocumento5 páginasSoluções Químicas: Preparação e DiluiçãoZélia CoelhoAinda não há avaliações
- AL1.2 Teste N.º 1 - Soluções 07-12Documento3 páginasAL1.2 Teste N.º 1 - Soluções 07-12Stéphanie Pinto0% (1)
- Energia de ionização e propriedades periódicasDocumento19 páginasEnergia de ionização e propriedades periódicasSuuurmAinda não há avaliações
- Física e Química - Movimento MecânicoDocumento5 páginasFísica e Química - Movimento Mecânicoyuki sanAinda não há avaliações
- Apoio Às Atividades Laboratoriais (Word)Documento58 páginasApoio Às Atividades Laboratoriais (Word)Paula FernandesAinda não há avaliações
- Relatório AL 1.1Documento5 páginasRelatório AL 1.1sgbrodrigues33% (3)
- Ef10 Questão Aula Energia Fenomenos Eletricos ResolucaoDocumento3 páginasEf10 Questão Aula Energia Fenomenos Eletricos ResolucaoSara PereiraAinda não há avaliações
- Variação Energia Cinética Carrinho RampaDocumento23 páginasVariação Energia Cinética Carrinho RampaSara Raquel Costa PintoAinda não há avaliações
- AL 3.2 Capacidade Termica Sol Manual 2021Documento3 páginasAL 3.2 Capacidade Termica Sol Manual 2021lara felgueirasAinda não há avaliações
- AL 2.2 - Soluções A Partir de Solutos SólidosDocumento2 páginasAL 2.2 - Soluções A Partir de Solutos SólidosZélia CoelhoAinda não há avaliações
- Solubilidade de sais e iões na água do marDocumento7 páginasSolubilidade de sais e iões na água do marOrlando Meireles0% (1)
- Teste 1 - Tema 1 - VERSÃO 1Documento12 páginasTeste 1 - Tema 1 - VERSÃO 1Lina SimoesAinda não há avaliações
- Teste 1 (2018-2019)Documento9 páginasTeste 1 (2018-2019)Luísa CarmoAinda não há avaliações
- Oxigénio e crescimento de insetos: um estudo experimentalDocumento8 páginasOxigénio e crescimento de insetos: um estudo experimentalElisabete Soares100% (2)
- 11oqui Mica FT Apoio No2Documento4 páginas11oqui Mica FT Apoio No2milenerato224050% (2)
- Ae rq10 Teste 2Documento9 páginasAe rq10 Teste 2zava0% (1)
- Ficha 2 - Estrutura e Dinâmica Da GeosferaDocumento9 páginasFicha 2 - Estrutura e Dinâmica Da Geosferaofélia_silva_10% (1)
- Ae rf10 Teste Resol 2Documento6 páginasAe rf10 Teste Resol 2Francisco JesusAinda não há avaliações
- Registos vulcânicos em núcleos de gelo antárticosDocumento8 páginasRegistos vulcânicos em núcleos de gelo antárticosFlavia RoxoAinda não há avaliações
- Solução Questão de AulaDocumento3 páginasSolução Questão de AulaSandra AndradeAinda não há avaliações
- Química 11: Equilíbrio e reaçõesDocumento9 páginasQuímica 11: Equilíbrio e reaçõesGuilherme CunhaAinda não há avaliações
- FA 6 COM CCsDocumento11 páginasFA 6 COM CCsteresamartins100% (2)
- Como avaliar argumentos lógicosDocumento4 páginasComo avaliar argumentos lógicosAluno Rodrigo Calhau FriasAinda não há avaliações
- 11f NL (Teste1 CC)Documento3 páginas11f NL (Teste1 CC)Catarina AlmeidaAinda não há avaliações
- Biogeo10!19!20 Teste2 CorrecaoDocumento2 páginasBiogeo10!19!20 Teste2 Correcaoandregafanha100% (1)
- 3º Teste 10ºA 2014 V1Documento12 páginas3º Teste 10ºA 2014 V1Susana Lopes0% (1)
- Ef11 Em2 Cad Lab Exploracao Al 1 1Documento5 páginasEf11 Em2 Cad Lab Exploracao Al 1 1MiguelAinda não há avaliações
- Recur SoDocumento18 páginasRecur SoSonia CoelhoAinda não há avaliações
- Atividade Laboratorial: Metas TransversaisDocumento7 páginasAtividade Laboratorial: Metas TransversaisAfonso RomualdoAinda não há avaliações
- Física e Química A | 11oano - Gráficos de posição, velocidade e tempoDocumento4 páginasFísica e Química A | 11oano - Gráficos de posição, velocidade e tempoRicardo GonçalvesAinda não há avaliações
- Avaliação da resistência de calcários ao nevoeiro salinoDocumento7 páginasAvaliação da resistência de calcários ao nevoeiro salinoJoão SantosAinda não há avaliações
- Física e Química - Forças que atuam sobre um balãoDocumento6 páginasFísica e Química - Forças que atuam sobre um balãoJoao MAchadoAinda não há avaliações
- 11 Ano Teste de FQDocumento8 páginas11 Ano Teste de FQPedro Carvalho100% (1)
- Aef11 Teste Ava 3Documento7 páginasAef11 Teste Ava 3Sandra SilvestreAinda não há avaliações
- Teste Global de FísicaDocumento14 páginasTeste Global de FísicaAna 2005100% (1)
- Relatório Capacidade Termica MassicaDocumento11 páginasRelatório Capacidade Termica Massicamaria_santos3616119Ainda não há avaliações
- Aef11 Fich Form 1Documento6 páginasAef11 Fich Form 1adivinhoeuAinda não há avaliações
- Fichas - Dominio 2Documento38 páginasFichas - Dominio 2Francisco MendesAinda não há avaliações
- Teste de Avaliacao Texto Ed.Documento5 páginasTeste de Avaliacao Texto Ed.Luis Ribeiro100% (3)
- Ae q11 Sol TestesDocumento5 páginasAe q11 Sol TestesGabriela SaraivaAinda não há avaliações
- Ae Fqa11 Quimica11 em RevistaDocumento36 páginasAe Fqa11 Quimica11 em RevistaMariliaPacAinda não há avaliações
- Biogeo10!19!20 Teste2 CorrecaoDocumento2 páginasBiogeo10!19!20 Teste2 CorrecaoandregafanhaAinda não há avaliações
- Densidade relativa de metais: determinação experimentalDocumento15 páginasDensidade relativa de metais: determinação experimentalLyana AlexandraAinda não há avaliações
- Aef11 Teste Ava 3Documento7 páginasAef11 Teste Ava 3Beatriz SilvaAinda não há avaliações
- Apoio Às Atividades LaboratoriaisDocumento10 páginasApoio Às Atividades LaboratoriaisAna FerreiraAinda não há avaliações
- Aef11 Teste Ava 1Documento5 páginasAef11 Teste Ava 1TeresaVaraoAinda não há avaliações
- Minificha 4 Versao 2 11o Ano 2020Documento4 páginasMinificha 4 Versao 2 11o Ano 2020Tiago Sousa0% (1)
- Ficha Fenómenos Térmicos + ResoluçãoDocumento16 páginasFicha Fenómenos Térmicos + ResoluçãoCatarina Jesus100% (1)
- BioGeo 10 Teste Pratico 4-2021Documento7 páginasBioGeo 10 Teste Pratico 4-2021Maria Graça RochaAinda não há avaliações
- Aef11 Ques Aulalab 2Documento2 páginasAef11 Ques Aulalab 2Narcisa Alexandra Filipe100% (1)
- Apoio Às Atividades LaboratoriaisDocumento10 páginasApoio Às Atividades LaboratoriaisEdite BrandãoAinda não há avaliações
- ResoluçõesDocumento37 páginasResoluçõesHugo MartinsAinda não há avaliações
- Ft-9a-Fqa11 Revisoes Q10 ResolucaoDocumento5 páginasFt-9a-Fqa11 Revisoes Q10 Resolucaopedro bandarraAinda não há avaliações
- Inbound 6378397766959620845Documento10 páginasInbound 6378397766959620845alexandreoliveira2827Ainda não há avaliações
- Resolução Ficha Formativa Quantidade Química TEDocumento3 páginasResolução Ficha Formativa Quantidade Química TEMiguel Angélico GonçalvesAinda não há avaliações
- Santillana CN5 Teste de Avaliacao 2ADocumento5 páginasSantillana CN5 Teste de Avaliacao 2AMónica Seabra100% (1)
- Reflexão do Som e EcoDocumento16 páginasReflexão do Som e EcoanitadiogoAinda não há avaliações
- Teste 3Documento5 páginasTeste 3anitadiogoAinda não há avaliações
- Santillana Cn5 Teste de Avaliacao 5aDocumento5 páginasSantillana Cn5 Teste de Avaliacao 5aFunny centerAinda não há avaliações
- 22 Outros fenómenos acústicosDocumento15 páginas22 Outros fenómenos acústicosanitadiogoAinda não há avaliações
- Teste 4 - Teste GlobalDocumento8 páginasTeste 4 - Teste GlobalanitadiogoAinda não há avaliações
- Tv5 em Ficha Avaliacao 1aDocumento5 páginasTv5 em Ficha Avaliacao 1aLuis FerreiraAinda não há avaliações
- FrancêsDocumento1 páginaFrancêsanitadiogoAinda não há avaliações
- Tv5 em Ficha Avaliacao 1a SolDocumento1 páginaTv5 em Ficha Avaliacao 1a SolLuis FerreiraAinda não há avaliações
- Teste 3Documento8 páginasTeste 3anitadiogoAinda não há avaliações
- Segunda Lei Newton aceleração forçasDocumento13 páginasSegunda Lei Newton aceleração forçasanitadiogoAinda não há avaliações
- 23 Características das ondas eletromagnéticasDocumento17 páginas23 Características das ondas eletromagnéticasanitadiogoAinda não há avaliações
- Teste Diagnóstico de Ciências da NaturezaDocumento5 páginasTeste Diagnóstico de Ciências da NaturezaanitadiogoAinda não há avaliações
- Primeira Lei Newton movimento repousoDocumento8 páginasPrimeira Lei Newton movimento repousoGonçalo PinhoAinda não há avaliações
- Teste 2Documento7 páginasTeste 2Susana FigueiredoAinda não há avaliações
- Teste 1Documento6 páginasTeste 1anitadiogoAinda não há avaliações
- Exp8 Apresentacao 27Documento20 páginasExp8 Apresentacao 27anitadiogoAinda não há avaliações
- Audição Humana 20 CaracterísticasDocumento18 páginasAudição Humana 20 CaracterísticasanitadiogoAinda não há avaliações
- Como vemos as coresDocumento20 páginasComo vemos as coresanitadiogoAinda não há avaliações
- Exp8 Apresentacao 28Documento22 páginasExp8 Apresentacao 28Rúben SousaAinda não há avaliações
- Exp8 Apresentacao 25Documento19 páginasExp8 Apresentacao 25anitadiogoAinda não há avaliações
- Exp8 Apresentacao 24Documento15 páginasExp8 Apresentacao 24Matilde Pacheco100% (1)
- Exp8 Apresentacao 26Documento17 páginasExp8 Apresentacao 26anitadiogoAinda não há avaliações
- AL - 1.2 - Quimica 2015 1 Parte-Proposta de ResoluçãoDocumento2 páginasAL - 1.2 - Quimica 2015 1 Parte-Proposta de ResoluçãoanitadiogoAinda não há avaliações
- Ae Pfug10 ppt3Documento22 páginasAe Pfug10 ppt3anitadiogoAinda não há avaliações
- A Fada OrianaDocumento17 páginasA Fada OrianaanitadiogoAinda não há avaliações
- Ae Pfug10 ppt2Documento6 páginasAe Pfug10 ppt2anitadiogoAinda não há avaliações
- Ae f1015 Ques Aulalab 2Documento3 páginasAe f1015 Ques Aulalab 2Mafalda NunesAinda não há avaliações
- Ae Pfug10 ppt4Documento36 páginasAe Pfug10 ppt4anitadiogoAinda não há avaliações
- Ae f1015 Ques Aulalab 1Documento3 páginasAe f1015 Ques Aulalab 1Ricardo Dos ReisAinda não há avaliações
- Propriedades coligativas: ebulioscopia e crioscopiaDocumento11 páginasPropriedades coligativas: ebulioscopia e crioscopiaCarlos Silva AlvesAinda não há avaliações
- Execução de paredes e fornecimento de artefactos de construçãoDocumento1 páginaExecução de paredes e fornecimento de artefactos de construçãoJorge MondlaneAinda não há avaliações
- Escolha de fundaçãoDocumento10 páginasEscolha de fundaçãoAbrão JuniorAinda não há avaliações
- Moradia unifamiliar tipo 2 BeiraDocumento6 páginasMoradia unifamiliar tipo 2 BeiraBelmiro40% (5)
- Ligas Ni PDFDocumento55 páginasLigas Ni PDFHenry Shinji JoutiAinda não há avaliações
- Metodologias Utilizadas para Amostragem de Efluentes AtmosféricosDocumento2 páginasMetodologias Utilizadas para Amostragem de Efluentes AtmosféricosRafael PaludoAinda não há avaliações
- Mapa - Mecânica e Resistência Dos Materiais - 52 2023Documento7 páginasMapa - Mecânica e Resistência Dos Materiais - 52 2023Fabio GuimaraesAinda não há avaliações
- Exemplo Caderno de Encargos - CópiaDocumento45 páginasExemplo Caderno de Encargos - CópiajoseAinda não há avaliações
- Publicações - Anais Do 1º Simpósio Internacional Das Engenharias UniDoctumDocumento27 páginasPublicações - Anais Do 1º Simpósio Internacional Das Engenharias UniDoctumAna CruzAinda não há avaliações
- Reforma escolas CametáDocumento50 páginasReforma escolas CametáVictor AndreiAinda não há avaliações
- Descarte de resíduos sólidos e impactos ambientaisDocumento15 páginasDescarte de resíduos sólidos e impactos ambientaisLeonard ZimmerAinda não há avaliações
- Válvulas Blanketing Catalogo - CelticDocumento8 páginasVálvulas Blanketing Catalogo - CelticAnonymous LBwADkNZHAinda não há avaliações
- Manual Do Usuário: Por Favor, Leia Este Manual Com Atenção para Uso Do EquipamentoDocumento39 páginasManual Do Usuário: Por Favor, Leia Este Manual Com Atenção para Uso Do EquipamentoRodrigo DelfinoAinda não há avaliações
- Apostila de Calorimetria 2Documento7 páginasApostila de Calorimetria 2mgalceuAinda não há avaliações
- Ductile iron parametersDocumento1 páginaDuctile iron parametersRonaldo RodriguesAinda não há avaliações
- Tratamento de Água - Caldeira - Daw Power PDFDocumento25 páginasTratamento de Água - Caldeira - Daw Power PDFEvandro VianaAinda não há avaliações
- Manual de OPERACAO CALD AUPDocumento56 páginasManual de OPERACAO CALD AUPYul Ramon Paradas Hernandez100% (1)
- Reações químicas, rendimentos e graus de purezaDocumento2 páginasReações químicas, rendimentos e graus de purezaMarianaAinda não há avaliações
- Catálogo de produtos para banheiro com conjuntos de banheira e armáriosDocumento9 páginasCatálogo de produtos para banheiro com conjuntos de banheira e armáriosVithinhagi GiAinda não há avaliações
- Bujoes - Bucha Cepel Exp DPDocumento5 páginasBujoes - Bucha Cepel Exp DPMarcos SiqueiraAinda não há avaliações
- NBR6118 - 1980 - Projeto e Execução de Obras de Concreto Armado - ProcedimentoDocumento53 páginasNBR6118 - 1980 - Projeto e Execução de Obras de Concreto Armado - ProcedimentoFelipe Fonseca100% (4)
- Cerâmicas: propriedades, processos produtivos e aplicaçõesDocumento9 páginasCerâmicas: propriedades, processos produtivos e aplicaçõesAlex Wiedthauper100% (1)
- Potenciais de redução e pilhasDocumento3 páginasPotenciais de redução e pilhasMaria Luiza Souza SoutoAinda não há avaliações
- Tabela de preços de produtos químicos para 2011Documento2 páginasTabela de preços de produtos químicos para 201168santos6806Ainda não há avaliações
- Nexans 26968Documento2 páginasNexans 26968eduardasotrabalhoAinda não há avaliações
- Aditivos para Produtos de PetroleoDocumento14 páginasAditivos para Produtos de PetroleoJefferson T. GiraoAinda não há avaliações
- Ácidos de Arrhenius: classificação e propriedadesDocumento10 páginasÁcidos de Arrhenius: classificação e propriedadesCaio De Paula ColnagoAinda não há avaliações
- Avaliação Parcial II QuimicaDocumento14 páginasAvaliação Parcial II QuimicaLuizFabianoAinda não há avaliações
- Trabalho Ibracon FinalDocumento7 páginasTrabalho Ibracon Finalfabricio.fontenelleAinda não há avaliações