Escolar Documentos
Profissional Documentos
Cultura Documentos
Halogenação de Aromáticos
Enviado por
Júlio César LimaTítulo original
Direitos autorais
Formatos disponíveis
Compartilhar este documento
Compartilhar ou incorporar documento
Você considera este documento útil?
Este conteúdo é inapropriado?
Denunciar este documentoDireitos autorais:
Formatos disponíveis
Halogenação de Aromáticos
Enviado por
Júlio César LimaDireitos autorais:
Formatos disponíveis
Série mecanismos de Orgânica Número 3
INFORME-SE SOBRE A QUÍMICA
Tito Peruzzo e Eduardo Canto
Autores de Química na Abordagem do Cotidiano – Editora Moderna
Halogenação de aromáticos
Equação da reação global:
H Br
FeBr3
+ Br2 + HBr
(catalisador)
Mecanismo:
1a_ etapa — Reação entre Br2 e FeBr3, formando um complexo.
Uma seta como a Br Br
mostrada em azul é + –
usada para indicar a Br Br + Fe Br Br Br Fe Br
movimentação de um
© 2008 Francisco (Tito) Miragaia Peruzzo e Eduardo Leite do Canto (www.professorcanto.com.br) – Venda proibida
par eletrônico para Br Br
estabelecer ligação com
Br2 atua como FeBr3 atua como Indicações de
outro átomo ou para
base de Lewis ácido de Lewis carga formal
um rearranjo das
(doa par (recebe par (veja Informe-se sobre a
ligações em uma
eletrônico) eletrônico) Química, edição para o
molécula
professor, número 3)
2a_ etapa — Ataque eletrófilo (filo = amigo) do complexo ao anel benzênico. Essa etapa equivale ao ataque
eletrófilo de um íon Br+ ao anel aromático.
H Br H Br
+ – Br –
+ Br Br Fe Br + Br Fe Br
+
Br Br
–
No ataque eletrófilo ao anel, Cátion Ânion FeBr4
um par eletrônico do anel é intermediário intermediário
usado para fazer ligação da reação
com o átomo de bromo
3a_ etapa — O cátion intermediário perde próton (H+), que se liga ao bromo formando HBr.
H Br
–
Br + Br FeBr3 + H Br + FeBr3
+
Observação 1: Note que a soma das etapas fornece a equação global. O catalisador, FeBr3, não é efetiva-
mente consumido.
Observação 2: O FeBr3, apesar de ser formado por metal e ametal, tem acentuado caráter molecular
porque a diferença de eletronegatividade entre ferro e bromo não é grande o suficiente para
que a ligação seja iônica.
Observação 3: Na cloração do benzeno, o catalisador usado é AlCl3, ou FeCl3. O ânion intermediário,
nesse caso, é AlCl4–, ou FeCl4–.
Você também pode gostar
- Química Orgânica - Parte 1 - AulaDocumento25 páginasQuímica Orgânica - Parte 1 - AulaQuímica com o RastaAinda não há avaliações
- Reacoes OrganicasDocumento13 páginasReacoes OrganicasTamires CostaAinda não há avaliações
- Introdução a Química orgânica PDFDocumento3 páginasIntrodução a Química orgânica PDFantoniojr2811Ainda não há avaliações
- Reacoes AromaticosDocumento59 páginasReacoes AromaticosGuilherme PereiraAinda não há avaliações
- QMC AP Hidrocarbonetos HidrocarbonetosDocumento6 páginasQMC AP Hidrocarbonetos HidrocarbonetosMellissa dlucasAinda não há avaliações
- Exercícios sobre ligações químicasDocumento2 páginasExercícios sobre ligações químicasMax Nunes BarretoAinda não há avaliações
- Ligações Químicas e Teorias de Valência e Orbitais MolecularesDocumento34 páginasLigações Químicas e Teorias de Valência e Orbitais MolecularesLucas Roniery100% (1)
- Lista 1 Boro QI-II-EQ2012-gabarito PDFDocumento10 páginasLista 1 Boro QI-II-EQ2012-gabarito PDFHelio JuniorAinda não há avaliações
- Reações Orgânicas: Cisões e ReagentesDocumento12 páginasReações Orgânicas: Cisões e Reagentesandre_7_souza501Ainda não há avaliações
- Mod 06 - Propriedades PeriódicasDocumento8 páginasMod 06 - Propriedades PeriódicasDaiane Santos FilgueirasAinda não há avaliações
- Química - Caderno de Resoluções - Apostila Volume 3 - Pré-Universitário - Quim3 Aula15Documento1 páginaQuímica - Caderno de Resoluções - Apostila Volume 3 - Pré-Universitário - Quim3 Aula15Química Caderno de ResoluçõesAinda não há avaliações
- Átomos e suas cargas: cátions, ânions e neutrosDocumento2 páginasÁtomos e suas cargas: cátions, ânions e neutrosRafael BritoAinda não há avaliações
- Aula 3 - O Átomo de CarbonoDocumento41 páginasAula 3 - O Átomo de CarbononathaliamoraesdejesusAinda não há avaliações
- Lista Exercícios - Interações IntermolecularesDocumento2 páginasLista Exercícios - Interações IntermolecularesalexchacalAinda não há avaliações
- Aprofundamento-Química-Ligação Covalente - Fórmulas e Geometria Molecular-27-03-2023Documento10 páginasAprofundamento-Química-Ligação Covalente - Fórmulas e Geometria Molecular-27-03-2023Camilla RequiãoAinda não há avaliações
- Ficha Suplementar - Tabela Periodica - CorreccaoDocumento2 páginasFicha Suplementar - Tabela Periodica - CorreccaoDiana FeiteiraAinda não há avaliações
- 01 - Introdução À Química OrgânicaDocumento5 páginas01 - Introdução À Química OrgânicaProf. Ricardo FrazãoAinda não há avaliações
- 08-03 - Ofbm - QuimDocumento3 páginas08-03 - Ofbm - Quimmarciohcs2003Ainda não há avaliações
- Estruturas de Lewis e HibridizaçãoDocumento49 páginasEstruturas de Lewis e HibridizaçãoISABELLE HAYASHI FUGIKAVAAinda não há avaliações
- Intro Química OrgânicaDocumento4 páginasIntro Química Orgânicaregiquimico100% (1)
- Quadruple Bonding Between Iron and Boron in The BFDocumento7 páginasQuadruple Bonding Between Iron and Boron in The BFCarlos EduardoAinda não há avaliações
- Reações de Adição Eletrofílica A AlquenosDocumento44 páginasReações de Adição Eletrofílica A AlquenosIgor BarretoAinda não há avaliações
- Teoria e ExercciosDocumento32 páginasTeoria e Exercciosyves raphaelAinda não há avaliações
- Atividades 04-04Documento3 páginasAtividades 04-04bininha89Ainda não há avaliações
- CLASSIFICAÇÃO DO CARBONO - 9 A 13 DE AGOSTO 2021Documento2 páginasCLASSIFICAÇÃO DO CARBONO - 9 A 13 DE AGOSTO 2021matheus8oliveira-44Ainda não há avaliações
- 10FQA Ficha Trab Ini Q2.1 - N.º 2Documento5 páginas10FQA Ficha Trab Ini Q2.1 - N.º 2paulamanuela140366Ainda não há avaliações
- Qi ManualDocumento94 páginasQi ManualdavidAinda não há avaliações
- Função de Proteínas Mioglobina e HemoglobinaDocumento35 páginasFunção de Proteínas Mioglobina e HemoglobinaEder SouzaAinda não há avaliações
- Aula08BioqI Funà à oProteà Nas PDFDocumento35 páginasAula08BioqI Funà à oProteà Nas PDFAbdul Laura CondulaAinda não há avaliações
- Exercicíos Gerais QUIMICA GERALDocumento13 páginasExercicíos Gerais QUIMICA GERALWylace AndradeAinda não há avaliações
- Química Orgânica-Ligação Covalente e Hibridização Do CarbonoDocumento32 páginasQuímica Orgânica-Ligação Covalente e Hibridização Do CarbonoMárlon SantosAinda não há avaliações
- QuímicaDocumento126 páginasQuímicaAlessandra AzevedoAinda não há avaliações
- Atividades Ligações QuímicasDocumento6 páginasAtividades Ligações QuímicasVagner Fortes RosadoAinda não há avaliações
- Forcas Intermoleculares Solido SolucoesDocumento8 páginasForcas Intermoleculares Solido SolucoesEricson SousaAinda não há avaliações
- Química - Pré-Vestibular Impacto - Ligação CovalenteDocumento2 páginasQuímica - Pré-Vestibular Impacto - Ligação CovalenteQuímica Qui100% (1)
- Teoria da Ligação de Valência e HibridizaçãoDocumento21 páginasTeoria da Ligação de Valência e HibridizaçãojoabeAinda não há avaliações
- Capítulo 5Documento6 páginasCapítulo 5Selma MeloAinda não há avaliações
- Reações Orgânicas e MecanismosDocumento7 páginasReações Orgânicas e MecanismosWisley NascimentoAinda não há avaliações
- Prova de QuímicaDocumento3 páginasProva de QuímicaKayro FantuchiAinda não há avaliações
- Atomística - Já Caiu Na FUVESTDocumento7 páginasAtomística - Já Caiu Na FUVESTpaulo robertoAinda não há avaliações
- 1 Lista de Exerci Cios - Estruturaato Mica e Ligac o EsquimicasDocumento3 páginas1 Lista de Exerci Cios - Estruturaato Mica e Ligac o EsquimicasNilbon RichardsAinda não há avaliações
- 4 Aula Geometria2010Documento3 páginas4 Aula Geometria2010luciano77araujoAinda não há avaliações
- Ligacoes QuimicasDocumento5 páginasLigacoes QuimicasJamirJamirJamirAinda não há avaliações
- Parte 2 - Valencia HibridaoDocumento19 páginasParte 2 - Valencia HibridaoAnonymous UYDJtUnAinda não há avaliações
- Propriedades Periódicas e Ligação Química 1o EMDocumento57 páginasPropriedades Periódicas e Ligação Química 1o EMAna Elisa FonsecaAinda não há avaliações
- Estrutura AtômicaDocumento12 páginasEstrutura AtômicaLucas AraújoAinda não há avaliações
- Número de Oxidação - Semana 5Documento11 páginasNúmero de Oxidação - Semana 5IsaqueAinda não há avaliações
- SIMULADO 2 - Farias Brito - 2º DiaDocumento20 páginasSIMULADO 2 - Farias Brito - 2º DiaLuana DiasAinda não há avaliações
- Introdução à Química OrgânicaDocumento8 páginasIntrodução à Química OrgânicaAgostinho Carrara100% (1)
- Revisao PF Em1 2022Documento18 páginasRevisao PF Em1 2022Anna CarolinaAinda não há avaliações
- Alista 08 - Hibridizacao de Orbitais AtomicosDocumento4 páginasAlista 08 - Hibridizacao de Orbitais AtomicosHeitorAinda não há avaliações
- Reações de Adição, Eliminação e Substituição RevisadaDocumento80 páginasReações de Adição, Eliminação e Substituição RevisadaRailson MoreiraAinda não há avaliações
- Azdoc - Tips Exercicios Resolvidos de QuimicaDocumento140 páginasAzdoc - Tips Exercicios Resolvidos de QuimicaBreno FariasAinda não há avaliações
- 10FQA Ficha Trab Ini Q2.1 - N.º 2Documento4 páginas10FQA Ficha Trab Ini Q2.1 - N.º 2Tiago SousaAinda não há avaliações
- Hemoglobina e MioglobinaDocumento45 páginasHemoglobina e MioglobinaMiguel TuriniAinda não há avaliações
- Prova de Química - 1º Ano PreenchidoDocumento2 páginasProva de Química - 1º Ano Preenchidojosielebraz5Ainda não há avaliações
- Química - Slides Cap13 - Espectrometria de Massa e Espectroscopia No InfravermelhoDocumento49 páginasQuímica - Slides Cap13 - Espectrometria de Massa e Espectroscopia No InfravermelhodiegoarimateiaAinda não há avaliações
- Introducao Quimica OrganicaDocumento21 páginasIntroducao Quimica OrganicaArthur A. NaiverthAinda não há avaliações
- Apostila Química Orgânica: Carbono, Dienos E AromáticosNo EverandApostila Química Orgânica: Carbono, Dienos E AromáticosAinda não há avaliações
- Cubo Mágico - SoluçãoDocumento8 páginasCubo Mágico - Soluçãoleandrocs1310Ainda não há avaliações
- Matemática - Circuitos Elétricos Métodos de Resolução de Malhas MúltiplasDocumento20 páginasMatemática - Circuitos Elétricos Métodos de Resolução de Malhas MúltiplasCaderno_Vestibular100% (7)
- Quimica CFG 2008Documento4 páginasQuimica CFG 2008Júlio César LimaAinda não há avaliações
- Performance de Torres de Resfriamento de Circulação NaturalDocumento74 páginasPerformance de Torres de Resfriamento de Circulação NaturalJúlio César LimaAinda não há avaliações
- Indice de Viscosidade PDFDocumento2 páginasIndice de Viscosidade PDFMarcos Inácio67% (3)
- Leptons e QuarksDocumento6 páginasLeptons e QuarksPaulAinda não há avaliações
- Mens Health - 25 - Maio-2008Documento126 páginasMens Health - 25 - Maio-2008Júlio César Lima0% (1)
- Local Provas Etapa2 2019 10 14Documento1 páginaLocal Provas Etapa2 2019 10 14Júlio César LimaAinda não há avaliações
- Mens Health - Julho-2008Documento105 páginasMens Health - Julho-2008Júlio César Lima100% (2)
- Mens Health - Junho-2008Documento107 páginasMens Health - Junho-2008Júlio César LimaAinda não há avaliações
- Reações de EliminaçãoDocumento12 páginasReações de EliminaçãoJúlio César LimaAinda não há avaliações
- Lista de Doenças ProfissionaisDocumento50 páginasLista de Doenças ProfissionaisJúlio César LimaAinda não há avaliações
- Química - Aula 04 - Tabela Periódica PDFDocumento12 páginasQuímica - Aula 04 - Tabela Periódica PDFDJNUNESAinda não há avaliações
- An Elise de Circuitos 79Documento0 páginaAn Elise de Circuitos 79lecosmonauteAinda não há avaliações
- Gradiene, Derivada Direcional, Rotacional, LaplacianoDocumento6 páginasGradiene, Derivada Direcional, Rotacional, LaplacianoluizclaudioventuraAinda não há avaliações
- RenatoBrito MomentoAngularDocumento18 páginasRenatoBrito MomentoAngularEldervixAinda não há avaliações
- Empuxos não-arquimedianosDocumento2 páginasEmpuxos não-arquimedianosjesusemanuelAinda não há avaliações
- Lista Algebra LinearDocumento3 páginasLista Algebra LinearJúlio César LimaAinda não há avaliações
- Lista4 08Documento2 páginasLista4 08Júlio César LimaAinda não há avaliações
- Analise de OrsatDocumento10 páginasAnalise de OrsatJúlio César LimaAinda não há avaliações
- Inglês - Aula 01 - Frases BásicasDocumento9 páginasInglês - Aula 01 - Frases BásicasBbook One100% (24)
- Exercícios Química TermodinâmicaDocumento14 páginasExercícios Química TermodinâmicaAdrianoDSAinda não há avaliações
- Relatorio de Sustentabilidade 2013 PetrobrasDocumento73 páginasRelatorio de Sustentabilidade 2013 PetrobrasJúlio César LimaAinda não há avaliações
- Matemática - Aula 01 - Potenciação PDFDocumento6 páginasMatemática - Aula 01 - Potenciação PDFVanessa Batista Bispo SilvaAinda não há avaliações
- Determinacao Do Coeficiente de Arrasto Na Posicao Inicial e Final Da Bracada Subaquatica de BrucosDocumento54 páginasDeterminacao Do Coeficiente de Arrasto Na Posicao Inicial e Final Da Bracada Subaquatica de BrucosJúlio César LimaAinda não há avaliações
- Prova Selecao2007 2Documento4 páginasProva Selecao2007 2Júlio César LimaAinda não há avaliações
- FisicaBasicaVol - I - Livro Baixado InternetDocumento205 páginasFisicaBasicaVol - I - Livro Baixado InternetTatiana BendoAinda não há avaliações
- A Origem e História Da AlquimiaDocumento4 páginasA Origem e História Da AlquimiaRodrigo MedeirosAinda não há avaliações
- Result Disc Vidraria Aula 1 Rot 1 17 09Documento7 páginasResult Disc Vidraria Aula 1 Rot 1 17 09Iria DominguesAinda não há avaliações
- FISPQ - Detergente CleanDocumento7 páginasFISPQ - Detergente Cleanjulio cesarAinda não há avaliações
- Aplicação Eslastron TanquesDocumento3 páginasAplicação Eslastron TanquesFabiano TeixeiraAinda não há avaliações
- Química analítica qualitativa: Hidrólise salinaDocumento7 páginasQuímica analítica qualitativa: Hidrólise salinaElmar Damasceno Damasceno JúniorAinda não há avaliações
- Mod Sim Proc Quim QRCodeDocumento51 páginasMod Sim Proc Quim QRCodeMarcelo SouzaAinda não há avaliações
- Manual de Instruções: Modificação Data PORDocumento8 páginasManual de Instruções: Modificação Data PORSergino InohueAinda não há avaliações
- Quimica de Alimentos - Escurecimento Nao EnzimaticoDocumento27 páginasQuimica de Alimentos - Escurecimento Nao EnzimaticoGabrieli Bernardi0% (2)
- Relatório 2 - Cromatografia em Camada Delgada (CCD)Documento6 páginasRelatório 2 - Cromatografia em Camada Delgada (CCD)Monsenhor D'AmatoAinda não há avaliações
- Limite microbiológico para produtos farmacêuticosDocumento12 páginasLimite microbiológico para produtos farmacêuticosKeise XavierAinda não há avaliações
- Quadro de esquadrias e portasDocumento1 páginaQuadro de esquadrias e portasJoão Pereira de SouzaAinda não há avaliações
- Relatório sobre soluções e suspensõesDocumento35 páginasRelatório sobre soluções e suspensõesMikele PereiraAinda não há avaliações
- ManualMaxpneumatic Bomba DiafragmaDocumento40 páginasManualMaxpneumatic Bomba DiafragmaVicente Aparecido Pineda Ferrari Jr.Ainda não há avaliações
- Simulado Ciclo 1 - 2 Dia EnemDocumento34 páginasSimulado Ciclo 1 - 2 Dia EnemLucas VerasAinda não há avaliações
- 1 - Polímeros Biodegradáveis - ApresentaçãoDocumento27 páginas1 - Polímeros Biodegradáveis - ApresentaçãoLeandro FrigoAinda não há avaliações
- Dos EspiritosDocumento4 páginasDos EspiritosvanessaAinda não há avaliações
- Po Gasomatria 221Documento14 páginasPo Gasomatria 221CAETANO SCOMBATI JUNIORAinda não há avaliações
- 1 +químicaDocumento161 páginas1 +químicacamila.gomes296Ainda não há avaliações
- Concreluz Mix Indianopolis MG - FISPQ - Aditivo Muraplast FK 230 - MC BauchemieDocumento6 páginasConcreluz Mix Indianopolis MG - FISPQ - Aditivo Muraplast FK 230 - MC BauchemieAlexandra VignoliAinda não há avaliações
- FISPQ OxylavfreshDocumento6 páginasFISPQ OxylavfreshVendas Clean PremiereAinda não há avaliações
- Compostos inorgânicos: óxidosDocumento4 páginasCompostos inorgânicos: óxidosIdiamine Da Alzira SKAinda não há avaliações
- Atividade1 ModeloDocumento5 páginasAtividade1 ModeloCarlos Roberto de SouzaAinda não há avaliações
- Sistema Duplex: Vantagens da pintura sobre aço galvanizadoDocumento22 páginasSistema Duplex: Vantagens da pintura sobre aço galvanizadoRenan BergamimAinda não há avaliações
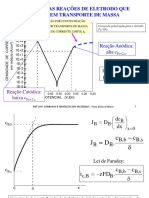
- Cinética de eletrodo com transporte de massaDocumento10 páginasCinética de eletrodo com transporte de massaMarcos Lapa BritoAinda não há avaliações
- Modelo Atividade1Documento4 páginasModelo Atividade1Marcelo RobertoAinda não há avaliações
- Exercícios Op. Unitárias II - IFSCDocumento28 páginasExercícios Op. Unitárias II - IFSCmarcelodalboAinda não há avaliações
- Impermeabilização de Reservatórios ElevadosDocumento3 páginasImpermeabilização de Reservatórios ElevadosGláuber LucasAinda não há avaliações
- Acabamento para Junta de DilatacaoDocumento7 páginasAcabamento para Junta de DilatacaoEduardo Rampanelli TosettoAinda não há avaliações
- (2.1) JogoParticulas10 - CAP - (FichaDiagnostico)Documento6 páginas(2.1) JogoParticulas10 - CAP - (FichaDiagnostico)Sara NaveAinda não há avaliações
- FTQ (2) - S..Documento2 páginasFTQ (2) - S..Nelson FernandesAinda não há avaliações