Escolar Documentos
Profissional Documentos
Cultura Documentos
DETERMINACION DE PH Y PREPARACION DE SOLUCIONES AMORTIGUADORAS
Enviado por
fercho80120 notas0% acharam este documento útil (0 voto)
15K visualizações7 páginasTítulo original
DETERMINACION DE pH Y PREPARACION DE SOLUCIONES AMORTIGUADORAS
Direitos autorais
© Attribution Non-Commercial (BY-NC)
Formatos disponíveis
DOCX, PDF, TXT ou leia online no Scribd
Compartilhar este documento
Compartilhar ou incorporar documento
Você considera este documento útil?
Este conteúdo é inapropriado?
Denunciar este documentoDireitos autorais:
Attribution Non-Commercial (BY-NC)
Formatos disponíveis
Baixe no formato DOCX, PDF, TXT ou leia online no Scribd
0 notas0% acharam este documento útil (0 voto)
15K visualizações7 páginasDETERMINACION DE PH Y PREPARACION DE SOLUCIONES AMORTIGUADORAS
Enviado por
fercho8012Direitos autorais:
Attribution Non-Commercial (BY-NC)
Formatos disponíveis
Baixe no formato DOCX, PDF, TXT ou leia online no Scribd
Você está na página 1de 7
DETERMINACION DE pH Y PREPARACION DE SOLUCIONES AMORTIGUADORAS
Carol Ibarra, Andrés Rosero
Laboratorio de Bioquímica I
Programa de Química, Facultad de Ciencias Exactas y Naturales
Universidad de Nariño, Ciudad Universitaria Torobajo, AA 1157
San Juan de Pasto.
RESUMEN: Se prepararon 3 soluciones a partir de soluciones con concentración conocida;
se mezclaron cantidades diferentes de estas en 6 tubos de ensayo a los cuales se les
agrego indicador creando una escala de pH de 3 a 5. Luego se tomaron 10 tubos de ensayo
a los cuales se les agrego soluciones diferentes con concentración conocida, se agrego un
indicador y se procedió a medir el pH patrón basándose en la escala anterior, se les midió el
pH con papel tornasol, con el pH metro y se calculo el pH teórico; como siguiente paso se
midió el pH de diferentes sustancias, luego se preparo la solución buffer y se le realizando
diferentes pruebas para medir la variación de pH, por último se realizaron diferentes cálculos
para preparara una solución amortiguadora problema de fosfato 0.5 M a un pH de 7,5.
PALABRAS CLAVE: Indicador, Concentración, Variación de pH, soluciones amortiguadores
INTRODUCCION El ion acetato es la base conjugada del
acido acético y el ion amonio es el acido
Según la definición de Bronsted (1879– conjugado del amoniaco.
1947) y Thomas Lowry (1874–1936) en
1923 un acido está definido como una La acidez y la alcalinidad de una solución
molécula que cede protones (H+) y una se la expresa por medio del logaritmo
base como la molécula que acepta el negativo de la concentración (mol / L) de
protón. El ejemplo más claro es la los iones H+ presentes en ella; al valor
molécula de agua ya que ella es obtenido se le llama pH de la solución.
anfiprotica ósea se comporta como un
acido liberando el protón y formando el
Ion hidroxilo.
Ahora si se conoce el valor de la
Cuando se comporta como una base, concentración de iones hidronio (H3O+) se
acepta un protón para formal el ion puede calcular el valor de la concentración
hidronio (H3O+). de iones hidroxilo (OH) utilizando la
Cuando un ácido y una base reaccionan, siguiente ecuación
los productos son un nuevo ácido y base,
los cuales respectivamente se les llama
acido y base conjugados.
Por ejemplo:
Donde en soluciones acuosas KW se
conoce como el producto iónico del agua
el cual es de 1x10-14 a 250C.
Las soluciones amortiguadoras son ejemplo, el pH de la sangre es alrededor
soluciones de ácidos, HA, o bases débiles de 7.4, en tanto que el jugo gástrico
con sales, NaA, de estos electrolitos, que humano es alrededor de 1.5. En la mayor
tienen un ion común y poseen la parte de los casos, estos valores de pH
propiedad de mantener el pH de las que son críticos para el funcionamiento
soluciones más o menos constantes a adecuado de las enzimas y del balance de
pesar de adiciones de cantidades la presión osmótica, se mantienen gracias
pequeñas de ácidos o bases fuertes. a las disoluciones.
El equilibrio involucrado es el del ácido o Una disolución amortiguadora debe
la base débil, en donde la concentración contener una concentración relativamente
del anion común A, proviene casi grande de ácido para reaccionar con los
exclusivamente de la sal, NaA. iones OH- que se añadan; y también debe
contener una concentración semejante de
HA= H+ + AKa = [H+] x [ HCO3-] base para que reaccione con la cantidad
[HA] de iones H+ que se añadan. Además, los
[H+] = Ka [HA] componentes ácidos y básicos del
[A-] amortiguador no deben consumirse el uno
Ka = [ ácido ] al otro en una reacción de neutralización.
[ sal ] Estos requerimientos se satisfacen con un
par ácido-base conjugado, por ejemplo, un
Ka es un valor constante y, se conoce el ácido débil y su base conjugada
pH de la solución sacando el logaritmo a (suministrada por una sal) o una base
la ecuación que esta igualada a [H] y débil y su ácido conjugado (suministrada
queda así: por una sal).
pH = pKa + log [A+] La medición de pH se efectúa ya sea por
[HA] un método calorimétrico, por un
(Ec de Henderson Hasselbalch) electrométrico o por cálculos analíticos.
Para este último, se usa el pHmetro.
Cada vez que se adiciona cierto número
de moles de ácido fuerte se observa un El método calorimétrico se basa en el uso
aumento de la [H+] y el equilibrio se de colorantes orgánicos complejos que
rompe momentáneamente. El sistema cambian de color de acuerdo al valor del
trata de restablecer el equilibrio, tratando pH de una soluciona acuosa. Estas
de disminuir la [H+] aumentada, para lo substancias se conocen como
cual se desplaza en el sentido inverso, indicadores. Para la mayoría de los casos,
aumentando la cantidad de ácido HA y aquellos requieren de un rango de pH
disminuyendo los iones de A-, entre 4.0 y 8.4. El método potenciometrico
manteniendo el pH más o menos utiliza el sistema del electrodo que
constante. consiste de un sensor cuyo voltaje varia
proporcionalmente a la actividad de iones
Si estas mismas moles de ácido fuerte se hidrogeno de la solución y un electrodo de
agregan al agua el pH cambia referencia que proporciona un voltaje de
bruscamente. Las disoluciones referencia constante y estable.
amortiguadoras o tampón son muy
importantes en los sistemas químicos y MATERIALES Y REACTIVOS
biológicos. El pH en el cuerpo humano
varía mucho de un fluido a otro; por Reactivos:
– pH metro 5.0 5.0 5.55 0.45
– Papel indicador
– Sln HCl 0.1 M
– Sln CH3COOH 0.1 M 2. Se tomo 10 tubos de ensayo y se
– Sln NH4OH 0.1 M agrego a cada uno 6 ml de sustancias
– Sln NH4Cl 0.1 M con concentración conocida
– Acetato de amonio 0.1 M
preparadas en laboratorio a las cuales
– Fosfato di acido de sodio 1M
– Fosfato acido de sodio 1M se les determino el pH teórico, pH
– Indicador azul de bromofenol patrón y pH potenciometrico. Las
sustancias preparadas en el
Materiales: laboratorio se muestran en la tabla 2.
– Probeta: 100ml Tabla 2.
– 8 beakers: 250ml
tubo Sustancia(12 Concentración
– Pipeta: 1ml, 5ml, 10ml
– 16 tubos de ensayo ml) (N)
– Balón volumétrico: 100ml, 25ml
1 Agua destilada ---------------------
METODOLOGÍA 2 Agua de la llave ---------------------
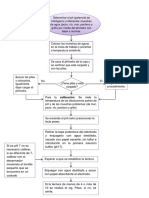
1. Se realizaron los cálculos para 3 HCl 0.1 M
preparar las siguientes soluciones:
4 HCl 0.01 M
– 50 ml de HCL 0.1 N a partir de HCL 5 HCl 0.001 M
0.5N
– 50 ml de NaOH 0.1 N a partir de 6 HCl 0.0001 M
NaOH 0.5 N
7 CH3COOH 0.1 M
– 0.5 ml de CH3COOH 0.1 N
8 NH4OH 0.1 M
1. Se preparo una escala coloreada de
pH en 6 tubos numerados de 3 a 5 con 9 NH4Cl 0.1 M
unidades de 0.4 en 0.4, a los cuales se
10 Acetato de 0.1 M
les agrego 3 gotas de indicador azul
amonio
de bromofenol. En cada tubo se
mezclo diferentes volúmenes de las
soluciones anteriormente preparada A las anteriores soluciones preparadas a
de CH3COOH, NaOH y agua destilada partir de soluciones de laboratorio se les
como se muestra en la tabla 1: determino los siguientes valores:
Tabla 1. a. A cada tubo de ensayo se le agrego 3
gotas de azul de bromofenol y se
pH CH3COOH ml NaOH ml H2O ml busco el equivalente más cercano de
acuerdo a la escala de pH que ya se
3.0 5.0 0.7 5.83
había elaborado anteriormente, siendo
3.4 5.0 0.42 5.58 este el pH patrón.
b. A las soluciones se les determino el
3.8 5.0 1.0 5.0 pH por medio del papel tornasol
4.2 5.0 2.15 3.85 siendo esta valoración el pH de papel.
4.6 5.0 4.1 1.9
c. A las soluciones se les determino el Este procedimiento se aplica para prepara
pH por medio del pHmetro, siendo las soluciones del primer punto y para
este valor el pH potenciometrico. preparar las soluciones utilizadas para
hacer la escala del pH de la tabla 1 y las
d. Por último se calculo teóricamente el soluciones utilizadas para la
pH de cada solución, siendo este el pH determinación del pH de la tabla 2.
calculado.
2. Preparación de la escala coloreada
6. Se rotularon 6 beakers (A – F), en A se
colocaron 20 ml de acido acético 0.5M, en Con la combinación de los volúmenes de
b se colocaron 20ml de acetato de sodio, acido acético, hidróxido de sodio y agua
se midió el pH, luego se mezclaron especificados en la tabla 1. Se obtuvo una
midiendo el nuevo pH. En C se coloco escala de pH como se muestra en la
20ml de agua destilada + 2ml de HCl figura 1:
0.5M, se mido el pH. En D se colocaron
20 ml de agua destilada + 3ml de NaOH Figura 1.
0.5M, se tomo el pH. A los beaker E y F
se les coloco 20 ml de la solución
resultante de A y B, al beaker E se le
adiciono 2 ml de HCl 0.5M y a F se le
adiciono 2 ml de NaOH 0.5M, se midió el pH 3 pH 5
pH a cada una de ellas.
El azul de bromofenol es un indicador
Por último se realizo los cálculos para orgánico de formula C19H10O5SBr4,
preparar un amortiguador de fosfato 0.5M tiene un olor característico este tiene un
Intervalo de transición visual: pH 3.0
a pH 7,5 y se midió su efectividad
(amarillo) - pH 4.6 (azul violeta o púrpura),
agregándole a este acido y base por es irritante y poco nocivo, su estructura
separado para medir el pH observando así molecular se muestra en la figura 2:
la capacidad amortiguadora.
Fig 2.
ANALISIS DE RESULTADOS
1. Preparación de soluciones:
Las soluciones iníciales fueron preparadas
utilizando la ley de la disolución la cual se
expresa de la siguiente ecuación:
Ec 1. Este es un compuesto orgánico cuya
C1V1 = C2V2 forma no disociada tiene un color
diferente al de su acido o base
conjugados. La disociación del indicador
Despejando V1 se tiene: (Ec 3).se acompaña de cambios en su
estructura interna y concominante cambio
Ec 2. de color
V1 = C2V2 / C1
Ec 3.
In + H2O ↔ LnH+ + OH-
Se procede a remplazar los valores:
V1 = 0.1 x 6 / 0.5 = 1.2 ml 3. Determinación de pH por diferentes
métodos:
Para el cloruro de amonio:
Se determino el pH de las 10 soluciones
que están descritas en la tabla 2. Ec 7.
Obteniendo los valores (tabla 3.):
pH = ½ pkw – ½ pKB + ½ log [NH4Cl]
Tabla 3.
tubo pH pH pH pH – El pH patrón corresponde a los valores
de pH aproximados obtenidos de la
papel Potencio teorico Patron
escala que se realizo con las
1 5 6.45 7 4 variaciones de color del indicador azul
de bromofenol con los valores de la
2 6 --------- ------- 4 tabla 1.
3 1 1.03 1 3 – El valor potenciometrico corresponde
a los valores de pH medidos en el
4 2 2.04 2 3.2
pHmetro.
5 3 2.096 3 3.4
6 4 3.97 4 3.6
7 3 3.74 2.86 3.2
1. Preparación de una solución
8 11 11.02 11.13 5 amortiguadora:
Tabla 4.
9 5 5.15 5.12 3.8 Beaker pH medido
10 9 8.94 7 4 A 10 ml ac acético 2,68
B 10 ml acetato de sodio 8.34
Solución A + B 4.57
– El pH teórico de la tabla 3 se cálculo C + D + 20 ml de agua 5.80
de la siguiente forma:
C+ 2mL de HCl 1.83
Para el agua no se calcula el pH porque D + 2mL de NaOH 11.98
se supone que es neutra E (A + B)+ 2mL de HCl 4.57
F (A + B)+ 2mL de 4.42
Para las diferentes concentraciones de NaOH
HCl el cual es acido fuerte se dice que:
2. Preparación de una solución buffer
Ec 4.
de fosfato 0.5 M y pH 7.5:
pH = -Log (H+)
pKa: 7.20
Para el acido acético: pH: 7.5
Concentración: 0.5 M
Ec 5.
Aplicamos la formula de Henderson–
pH = ½ pKA- ½ log [CH3COOH]
Hasselbalch:
Para el hidróxido de amonio: pH = pKa + log [A+]
[HA]
Ec 6.
7.5 – 7.20 = log [A+]
pH = pkw – ½ pKB + ½ log [NH4OH] [HA]
Antilog 0.3 = [A+] 633 ml 1L
[HA] X 0.1L X = 63.3 ml
1.995 = [A+] Volumen de acido:
[HA] 332 ml 1L
X 0.1L X = 33.2 ml
Relación (Base) 1.995
(Acido) 1 Por lo anterior podemos decir que se
necesitan 33.2 ml de fosfato acido mas
Parte total: 1.995 + 1 = 2.995 aprox = 3 63.3 ml de fosfato bibásico; el pH teórico
es de 7.5 y el pH experimental es de 7.06,
Para la base: se le agrego unas gotas de NaOH hasta
3 100% alcanzar el pH de 7.5 y se lo aforo.
1.99 X X = 66.33 % Base
Como la relación de porcentaje supera la
Para el acido: mitad, se calcula el volumen para cada
3 100% uno de los componentes determinando las
1 X X = 33.33 % Acido cantidades de acido y de base para
Moles de la base: preparar la solución buffer.
100 mol 63.33
0.5 mol X Para observar la variación de pH se le
X = 0.3166 mol de la base agrego al buffer obtenido inicialmente 1 ml
de HCl y 1ml de NaOH obteniendo el
Moles del acido: siguiente resultado: ( Tabla 5.)
100 mol 33.33
0.5 mol X Tabla 5.
X = 0.1666 mol del acido Sln (buffer pH 7.06) pH
Concentración para preparar un litro de de Buffrer + 1ml de HCl 0.1 M 6.57
solución:
Buffre + 1 ml de NaOH 0.1 M 7.08
Para la base:
M = 0.3166 mol = 0.3166 M
1L sln En la tabla 1 se observa que no hay una
variación significativa de pH lo cual puede
Para el acido: ser porque el agua tenía un grado de
M = 0.1666mol = 0.1666 M acidez bajo (medido: 6.02); este es
1L sln diferente al teórico por las impurezas que
Se calculas los volúmenes de acido y de el agua puede contener.
base con la formula de las disoluciones
(Ec 1): Con respecto a los valores obtenidos con
el pHmetro (Tabla 2) se puede decir que
– V1 para la base = 0.633 L (633 ml) estos como son de uso general no
– V1 para el acido = 0.332 L (332 ml) estaban correctamente calibrados lo cual
se evidencia en lo que ellos tardan en dar
Se calculan los volúmenes para preparar un valor estable dando origen a un error.
100ml: Los recubrimientos del electrodo, los
posibles cambios en la energía eléctrica
Volumen de base: también pueden ser factores de
interferencia además de esto igualmente unidad de pH a un litro del
también puede influir el medio de trabajo y amortiguador. Esta premisa es de
la limpieza del material. suma importancia en las ciencias ya
que un cambio brusco de pH en un
Los datos de la tabal 2 explican los sistema biológico puede causar
cambios que se dan cuando agregamos al perjuicios que afecten la integridad del
medio una cantidad de acido o base fuerte humano.
reflejándose este en la gran variación de
pH ya que aumentan o disminuyen la BIBLIOGRAFIA
cantidad de iones hidronio en el medio
1. SKOOG, West, Holler. Química
que se está trabajando.
Analítica. Ed Mc Graw Hill, Colombia
1998 Séptima edición
En la preparación del buffer de fosfato 0.5
M a pH 7.5 el pH calculado fue muy
2. Bohinski R. Bioquímica, quinta edición,
cercano al calculado. Cuando se realizo la
editorial Adisson Westey, México
prueba de amortiguamiento se observo
1998.
que la variación de pH fue muy pequeña
lo cual nos confirma la capacidad de
3. MURRAY RK et al. Bioquímica de
amortiguamiento de la solución ya que
Harper, 16° edición, 2004
mantuvo un rango del pH.
4. McKEE y McKEEE J. Bioquímica.
CONCLUSIONES
McGraw-Hill-Interamericana,
1. Los amortiguadores se usan en todos México 2003
los tipos de reacciones químicas en
las que se desean mantener el pH de
una solución a un nivel relativamente
constante
2. Para preparar una disolución
amortiguadora a un pH especifico, se
seleccionara un ácido débil cuyo pKa
sea parecido al pH deseado. esta
selección no solo da el valor de pH
correcto del sistema amortiguador sino
que asegura que tengan cantidades
comparables del ácido y su base
conjugada de la disolución; que son
prerrequisitos para el sistema
amortiguador funcione con eficacia.
3. La capacidad amortiguadora de una
solución se define como el número de
moles de un ácido o de una base
fuerte que ocasiona un cambio de una
Você também pode gostar
- Informe de Laboratorio PH y Soluciones AmortiguadorasDocumento7 páginasInforme de Laboratorio PH y Soluciones AmortiguadorasJuan FernandezAinda não há avaliações
- 8 Soluciones BufferDocumento18 páginas8 Soluciones BufferNicolas Patricio SitjaAinda não há avaliações
- Equipos para Medir La AWDocumento4 páginasEquipos para Medir La AWIvan FrancoAinda não há avaliações
- Práctica #1 ToxicologiaDocumento4 páginasPráctica #1 Toxicologiacristian david hurtado peña0% (1)
- Identificacion de AminoacidosDocumento6 páginasIdentificacion de AminoacidosJonathan Gavilanes LópezAinda não há avaliações
- Informe 2 de Lab. BioquimicaDocumento11 páginasInforme 2 de Lab. BioquimicaSoraida Brigitte100% (6)
- Informe 8-1Documento10 páginasInforme 8-1nico_recarAinda não há avaliações
- Amarillo de AlizarinaDocumento1 páginaAmarillo de AlizarinaHenrry R. GutierrezAinda não há avaliações
- Laboratorio 7Documento10 páginasLaboratorio 7Jessica Beltrán100% (1)
- Proyecto Microbiologia de AlimentosDocumento6 páginasProyecto Microbiologia de AlimentosYöhana Flörëz100% (1)
- Elaboracion de Nectar de FresaDocumento8 páginasElaboracion de Nectar de Fresaviviana RodriguezAinda não há avaliações
- Grasa y Aceites BROMATOLOGÍADocumento47 páginasGrasa y Aceites BROMATOLOGÍANadia Auzsa100% (1)
- Práctica DuraznoDocumento5 páginasPráctica DuraznoScS JuanAinda não há avaliações
- Guía #2 Preparación de Soluciones para Biología MolecularDocumento3 páginasGuía #2 Preparación de Soluciones para Biología MolecularSharick Ramos0% (1)
- Obtención de Pectina Con Estándares Mínimos de Calidad Mediante Extracción Por Hidrólisis Ácida DDocumento30 páginasObtención de Pectina Con Estándares Mínimos de Calidad Mediante Extracción Por Hidrólisis Ácida DCristian Marín50% (2)
- Discusion PH y Acidez.Documento2 páginasDiscusion PH y Acidez.Aubry Galindo BravoAinda não há avaliações
- Montelongo PHDocumento2 páginasMontelongo PHOscar0% (1)
- Reporte Titulación Del Ácido Fuerte y Base FuerteDocumento9 páginasReporte Titulación Del Ácido Fuerte y Base FuerteErnesto Sanchez Soberane50% (2)
- Técnicas de Tinción Simple InformeDocumento4 páginasTécnicas de Tinción Simple InformeAnonymous fYkno9aXQL100% (1)
- Titulación: Determinación concentraciónDocumento3 páginasTitulación: Determinación concentraciónGaby NarväezAinda não há avaliações
- PFGE Metarhizium 2005.en - EsDocumento6 páginasPFGE Metarhizium 2005.en - EsDayana LizcanoAinda não há avaliações
- Informe 1 de ApaDocumento4 páginasInforme 1 de ApaxxxelyxxxAinda não há avaliações
- P HMETRIADocumento11 páginasP HMETRIAcaritoo0% (1)
- Practica EnterobacteriasDocumento7 páginasPractica EnterobacteriasSelene Ruiz MoriAinda não há avaliações
- Practica 7Documento9 páginasPractica 7Ysmael BarrientosAinda não há avaliações
- 03 Toxicidad en AlimentosDocumento22 páginas03 Toxicidad en AlimentosElizabeth VargasAinda não há avaliações
- Determinación de Acidez Titulable - LiliDocumento3 páginasDeterminación de Acidez Titulable - LiliPatricia RettoAinda não há avaliações
- 15 - Soluciones AmortiguadorasDocumento17 páginas15 - Soluciones AmortiguadorasConi SchnohrAinda não há avaliações
- Informe 1 Determinación de CarbohidratosDocumento12 páginasInforme 1 Determinación de CarbohidratosMica BetancourtAinda não há avaliações
- Calor de neutralizaciónDocumento9 páginasCalor de neutralizaciónCamilo SanchezAinda não há avaliações
- Análisis Del VinagreDocumento7 páginasAnálisis Del Vinagrelibra257Ainda não há avaliações
- Mohos y LevadurasDocumento8 páginasMohos y LevadurasRoss M. CazónAinda não há avaliações
- Aw Agua Libre y LigadaDocumento1 páginaAw Agua Libre y LigadaJomy Chaguay DuarteAinda não há avaliações
- Determinacion de PHDocumento9 páginasDeterminacion de PHnilquier benitoAinda não há avaliações
- Soluciones Ideales - Ley de Raoult - Ley de HenryDocumento12 páginasSoluciones Ideales - Ley de Raoult - Ley de HenryBeto Ugarte MedinaAinda não há avaliações
- Informe de Bioquimica PH de Los AlimentosDocumento4 páginasInforme de Bioquimica PH de Los AlimentosJohnnyHingaAinda não há avaliações
- Reacciones de Reconocimiento de CarbohidratosDocumento6 páginasReacciones de Reconocimiento de Carbohidratoskaritho sanchezAinda não há avaliações
- Secador de lecho estáticoDocumento2 páginasSecador de lecho estáticoFer Ramirez0% (1)
- Balanza analíticaDocumento3 páginasBalanza analíticapolo1526Ainda não há avaliações
- Informe Del ArrozDocumento3 páginasInforme Del ArrozYohana Cano NoyaAinda não há avaliações
- Determinación de Vitamina CDocumento7 páginasDeterminación de Vitamina CCarlos Vásquez UruetaAinda não há avaliações
- CargaBacterianaDocumento36 páginasCargaBacterianaOswaldo MendozaAinda não há avaliações
- Preparación soluciones laboratorioDocumento11 páginasPreparación soluciones laboratorioYessica Quisbert GutierrezAinda não há avaliações
- PROTEÍNASDocumento7 páginasPROTEÍNASFernando Sk50% (2)
- Determinaciones Analiticas en Leche FrescaDocumento10 páginasDeterminaciones Analiticas en Leche FrescaCristian R. RoldánAinda não há avaliações
- Reactivo de FehlingDocumento8 páginasReactivo de FehlingEdith HSAinda não há avaliações
- 1.3.2 FermentacionesDocumento21 páginas1.3.2 FermentacionesSonia Herrera MonroyAinda não há avaliações
- Elaboracion de ChucrutDocumento4 páginasElaboracion de ChucrutpapaquitoAinda não há avaliações
- Técnica. Agar CLEDDocumento2 páginasTécnica. Agar CLEDMarifer ArzolaAinda não há avaliações
- T. Sup y OxidacionDocumento13 páginasT. Sup y OxidacionROXANA QUISPE MAMANIAinda não há avaliações
- Practica Soluciones AmortiguadoresDocumento12 páginasPractica Soluciones AmortiguadoresJuan Carlos Castillo ZamoraAinda não há avaliações
- Diluciones y HidrolisisDocumento8 páginasDiluciones y HidrolisisAliss NatarenoAinda não há avaliações
- Determinación de Grasas en Los AlimentosDocumento24 páginasDeterminación de Grasas en Los AlimentosMiiLenaKariiNaAinda não há avaliações
- AcidimetriaDocumento10 páginasAcidimetriaFreddyAinda não há avaliações
- Resultados y DiscusionesDocumento14 páginasResultados y DiscusionesMariaRitaAinda não há avaliações
- Lab 3 - 4Documento4 páginasLab 3 - 4Laura VillamilAinda não há avaliações
- Practica 16 Calculo Teorico y Experimental de PH de Disoluciones de Acidos Bases y Sales Disoluciones ReguladorasDocumento7 páginasPractica 16 Calculo Teorico y Experimental de PH de Disoluciones de Acidos Bases y Sales Disoluciones ReguladorasJosh Emg100% (1)
- Resume NDocumento42 páginasResume NKlenny EstefanyAinda não há avaliações
- 2-Preparación de Soluciones AmortiguadorasDocumento6 páginas2-Preparación de Soluciones AmortiguadorasVanessaAinda não há avaliações
- Info 1 Mediciones de PHDocumento7 páginasInfo 1 Mediciones de PHdidy861Ainda não há avaliações
- Plan de Clases Biologia Ciclo IvDocumento2 páginasPlan de Clases Biologia Ciclo Ivfercho8012Ainda não há avaliações
- Taller Nomenclatura InorganicaDocumento4 páginasTaller Nomenclatura Inorganicafercho8012Ainda não há avaliações
- Reproduccion Humana Guia 9Documento5 páginasReproduccion Humana Guia 9fercho8012Ainda não há avaliações
- Reproduccion en Plantas Guia 7Documento5 páginasReproduccion en Plantas Guia 7fercho8012Ainda não há avaliações
- Taller EstequiometriaDocumento4 páginasTaller Estequiometriafercho8012Ainda não há avaliações
- Cuadro-Comparativo Teorias AprendizajeDocumento1 páginaCuadro-Comparativo Teorias AprendizajeYolanda Arteaga0% (1)
- Ejercicios de Repaso Ingenierias ItpDocumento4 páginasEjercicios de Repaso Ingenierias Itpfercho8012Ainda não há avaliações
- Evaluacion Tercer Periodo DecimoDocumento2 páginasEvaluacion Tercer Periodo Decimofercho8012100% (1)
- Plan de Clase Física Grado Undécimo I Periodo 2020Documento4 páginasPlan de Clase Física Grado Undécimo I Periodo 2020fercho8012Ainda não há avaliações
- Lineamientos para La Vigilancia Por Laboratorio VIHDocumento61 páginasLineamientos para La Vigilancia Por Laboratorio VIHfercho8012Ainda não há avaliações
- PEI Proyecto Educativo InstitucionalDocumento39 páginasPEI Proyecto Educativo Institucionalfercho8012100% (1)
- Guia 6 AlcanosDocumento7 páginasGuia 6 Alcanosfercho8012Ainda não há avaliações
- Prueba Diagnostica Quimica Grado DecimoDocumento3 páginasPrueba Diagnostica Quimica Grado Decimofercho8012Ainda não há avaliações
- 186568000567-Isce-Ie Alvernia-2018Documento10 páginas186568000567-Isce-Ie Alvernia-2018fercho8012Ainda não há avaliações
- SENA - Seguridad y salud en el trabajoDocumento1 páginaSENA - Seguridad y salud en el trabajofercho8012Ainda não há avaliações
- Guia de Aprendizaje 1Documento8 páginasGuia de Aprendizaje 1fercho8012Ainda não há avaliações
- Genetica Basica Guia 1 NovenoDocumento8 páginasGenetica Basica Guia 1 Novenofercho8012Ainda não há avaliações
- Desarrollo Guia 1 CucigramaDocumento9 páginasDesarrollo Guia 1 Cucigramafercho8012Ainda não há avaliações
- Guia 11 Acidos CarboxilicosDocumento4 páginasGuia 11 Acidos Carboxilicosfercho8012Ainda não há avaliações
- Recuperacion FinalDocumento2 páginasRecuperacion Finalfercho8012Ainda não há avaliações
- Analisis Obra Doce Cuentos PeregrinosDocumento17 páginasAnalisis Obra Doce Cuentos Peregrinosfercho801267% (3)
- Planeador de Clases-Ciclo 5abcde FisicaDocumento11 páginasPlaneador de Clases-Ciclo 5abcde Fisicafercho8012Ainda não há avaliações
- Identificación de especies vegetales y animales en el colegio Fidel de MontclarDocumento4 páginasIdentificación de especies vegetales y animales en el colegio Fidel de Montclarfercho8012Ainda não há avaliações
- Propiedades de Los GasesDocumento5 páginasPropiedades de Los Gasesfercho8012Ainda não há avaliações
- Ejercicios de Genetica (Buenos)Documento8 páginasEjercicios de Genetica (Buenos)fercho8012100% (1)
- Consulta Caracol AfricanoDocumento4 páginasConsulta Caracol Africanofercho8012Ainda não há avaliações
- Proyecto Lecto - Escritor Funes y LinaresDocumento32 páginasProyecto Lecto - Escritor Funes y Linaresfercho8012Ainda não há avaliações
- Guia 1 Unidades de Medida y Facores de ConversionDocumento5 páginasGuia 1 Unidades de Medida y Facores de Conversionfercho8012Ainda não há avaliações
- Evaluacion Segundo Periodo Grado OnceDocumento3 páginasEvaluacion Segundo Periodo Grado Oncefercho8012Ainda não há avaliações
- Matriz Uno y Dos Completas Grado Octavo 2014 - 2015Documento3 páginasMatriz Uno y Dos Completas Grado Octavo 2014 - 2015fercho8012Ainda não há avaliações
- Algo Mas Que Palabras - Darlis StefanyDocumento864 páginasAlgo Mas Que Palabras - Darlis StefanyYomahira DiazAinda não há avaliações
- Taller 1 Unid II Analisi Derecho de VíaDocumento4 páginasTaller 1 Unid II Analisi Derecho de VíaLeonela GrandaAinda não há avaliações
- Simbolos Electricos Electronicos BasicosDocumento5 páginasSimbolos Electricos Electronicos BasicosAntonioAinda não há avaliações
- Fase 4 Trabajo Colaborativo Unidad 2 Grupo311Documento9 páginasFase 4 Trabajo Colaborativo Unidad 2 Grupo311steventorres7404Ainda não há avaliações
- ¿Cuántos Géneros Musicales Existen Tipos de Música. Estilos MusicalesDocumento40 páginas¿Cuántos Géneros Musicales Existen Tipos de Música. Estilos MusicalesEnrique Salazar AliagaAinda não há avaliações
- Educacion en Chile, Revision Politicas Nacionales, 2017, OECDDocumento308 páginasEducacion en Chile, Revision Politicas Nacionales, 2017, OECDFabiola HenAinda não há avaliações
- El KerógenoDocumento20 páginasEl KerógenoLuis Alberto Tupa CoilaAinda não há avaliações
- Cualidades Estèticas de La QuinchaDocumento6 páginasCualidades Estèticas de La QuinchaNicoll RodriguezAinda não há avaliações
- I Simposio de BibliografiaDocumento28 páginasI Simposio de BibliografiaNahama MGAinda não há avaliações
- Elman BackpropagationDocumento2 páginasElman BackpropagationgianAinda não há avaliações
- PNL I Nivel 2022-2 InicialDocumento5 páginasPNL I Nivel 2022-2 Inicialluis cruzAinda não há avaliações
- El Mundo Era Tan Reciente, Que Muchas Cosas Carecían de Nombre, y para Mencionarlas Había Que Señarlarlas Con El Dedo.-Cien Años de Soledad de Gabriel García Marquez.Documento2 páginasEl Mundo Era Tan Reciente, Que Muchas Cosas Carecían de Nombre, y para Mencionarlas Había Que Señarlarlas Con El Dedo.-Cien Años de Soledad de Gabriel García Marquez.Ross GallegosAinda não há avaliações
- Bianco 2 ESPAÑOL 6 GRADODocumento19 páginasBianco 2 ESPAÑOL 6 GRADOBolivar Concepcion PrescottAinda não há avaliações
- Diagrama de Flujo de Proceso de Produccion de Un LapizDocumento1 páginaDiagrama de Flujo de Proceso de Produccion de Un LapizadrianAinda não há avaliações
- Cultivo de Stevia RebaudianaDocumento37 páginasCultivo de Stevia Rebaudianarijo123Ainda não há avaliações
- 1 Seminario MasaDocumento1 página1 Seminario MasaMarcos Condorí PacoAinda não há avaliações
- Tarta de arándanos y frambuesaDocumento4 páginasTarta de arándanos y frambuesaSamantha CorralAinda não há avaliações
- Foro Semana 6 Sistema de Gestion de Seguridad y Salud LaboralDocumento3 páginasForo Semana 6 Sistema de Gestion de Seguridad y Salud LaboralMARCOS GUZMANAinda não há avaliações
- UnidadDocumento5 páginasUnidadjos22miguel2moreno2cAinda não há avaliações
- Temario UNSAAC Primera Opción Grupo ADocumento3 páginasTemario UNSAAC Primera Opción Grupo AAlexito TorresAinda não há avaliações
- Manual Inmunizaciones API2017 Print4abr2017-3Documento348 páginasManual Inmunizaciones API2017 Print4abr2017-3Marcos Quispe KapaAinda não há avaliações
- Calculos Renales TratamientoDocumento3 páginasCalculos Renales TratamientotratamieerAinda não há avaliações
- Guia Ciclo Iii Unidades de Longitud - MetroDocumento4 páginasGuia Ciclo Iii Unidades de Longitud - MetrowilsonAinda não há avaliações
- Mcdonald Cultura OrganizacionalDocumento2 páginasMcdonald Cultura OrganizacionalJhon Campoverde20% (5)
- Informe Acueducto San Juan de AramaDocumento38 páginasInforme Acueducto San Juan de AramaDaniel MartínAinda não há avaliações
- Psilocibes ThemushroomsDocumento255 páginasPsilocibes Themushroomsfred sanAinda não há avaliações
- Aws Academy Cloud OperationDocumento3 páginasAws Academy Cloud OperationneonaviAinda não há avaliações
- Punta lógica TTLDocumento2 páginasPunta lógica TTLCristian Daniel Gonzalez RodriguezAinda não há avaliações
- Plan financiero empresa Amarilis rentabilidad 15Documento3 páginasPlan financiero empresa Amarilis rentabilidad 15Marcos Alberto Jimenez MonagoAinda não há avaliações
- Farmacologia Insulinas PDFDocumento29 páginasFarmacologia Insulinas PDFJhon GomezAinda não há avaliações