Escolar Documentos
Profissional Documentos
Cultura Documentos
Estrutura e metabolismo do colesterol
Enviado por
Felipe GonzalezTítulo original
Direitos autorais
Formatos disponíveis
Compartilhar este documento
Compartilhar ou incorporar documento
Você considera este documento útil?
Este conteúdo é inapropriado?
Denunciar este documentoDireitos autorais:
Formatos disponíveis
Estrutura e metabolismo do colesterol
Enviado por
Felipe GonzalezDireitos autorais:
Formatos disponíveis
BIOQUÍMICA – FELIPE GONZALEZ ESTRUTURA DO COLESTEROL
METABOLISMO DO COLESTEROL E LIPOPROTEÍNAS • Composto altamente hidrofóbico
• Consiste em quatro anéis de hidrocarbonetos fundidos
O colesterol é o esteroide característico dos tecidos humanos, (A,B,C e D à núcleos esteroides)
desempenhando várias funções esssenicais no organismo. • Presença de uma cadeia ramificada de hidrocarbonetos
Como: de 8 carbonos ligada ao C-17 do anel D.
• Composição das membranas plasmáticas à modulador • Anel A tem uma hidroxila no C-3
de fluidez • Anel B apresenta uma ligação dupla entre C-5 e C-6
• Precursor de ácidos biliares
• Precursor de hormônios esteroides ESTERÓIS à Os esteroides apresentam de 8 a 10 carbonos na
• Precursor da vitamina D cadeia lateral ligada ao C-17 e um grupo hidroxila no C-3.
• Esteróides vegetais são pouco absorvidos em humanos,
Níveis adequados de colesterol devem ser mantidos no visto que são transportados ativamente de volta ao lúmen
organismo para garantir a homeostase à garantir um intestinal ao entrar nos enterócitos.
suprimento contínuo de Colesterol. • Juntamente a esse processo ocorre também o transpote
de parte do colesterol de volta ao lúmen intestinal
Para manutenção dos níveis de Colesterol estão envolvidos • Baseado nessa premissa, a ingestão diária de ésteres de
complexos sistemas de transporte, biossíntese e regulação. esteroides de plantas é uma estratégia dietética para
• Fígado à papel central na regulação da homeostasia do redução dos níveis plasmáticos de Colesterol.
Colesterol.
• Pelo fígado, passam moléculas de Colesterol de ÉSTERES DE COLESTEROL à Maior parte do colesterol
diferentes fontes como: plasmático está na forma de éster
o Dieta (colesterol exógeno) • Molécula ainda mais hidrofóbica que o colesterol livre.
o Síntese de Novo em tecidos extra-hepáticos • Não ocorrem nas membranas celulares, estando
o Síntese Local presentes em pequenas quantidades na maioria das
• Pelo fígado, o colesterol pode ser encaminhado para os células.
tecidos periféricos como componente das lipoproteínas • Devido ao seu caráter altamente hidrofóbico, o colesterol
plasmáticas OU e seus ésteres devem ser transportados associados a
o pode ser eliminado através da bile proteínas à componentes de partículas de lipoproteínas
• Nos humanos, nosso organismo não possui mecanismos o Ou podem ser solubilizados por fosfolipídeos e
reguladores do influxo/efluxo de colesterol. Com isso, sais biliares na bile.
excedentes do colesterol acabam depositando-se
gradualmente nos tecidos.
o Formação de placas à Aterosclerose
SÍNTESE DO COLESTEROL
Obs: A HMG-COA redutase é uma proteína intrínseca da
• Sintetizado por quase todos os tecidos humanos membrana do retículo endoplasmático.
o Fígado, Intestino, Córtex Adrenal e Tecidos
Reprodutivos à Maiores produtores
• Síntese ocorre no citoplasma
o Participação de enzimas citoplasmáticas e
enzimas do retículo endoplasmático
• A energia da síntese é garantida pela hidrólise das
ligações tio éster da acetil-Coenzima A (COA) e das
ligações de fosfatos terminais do ATP.
• A velocidade das reações dessa rota são respondem
diretamente a mudanças na concentração de Colesterol
o Mecanismos que regulam a síntese endógena em
função da quantidade de colesterol excretado
o Desquilíbrios nessa regulação podem elevar os
níveis de colesterol plasmático na circulação,
com potencial risco de doença arterial
coronariana.
A rota de síntese do colesterol apresenta as seguintes
reações:
1. Síntese de HMG-COA a partir do acetoacetil-COA.
2. Síntese do Mevalonato a partir do HMG-COA
3. Síntese do Colesterol a partir de uma série de 8 reações
mais específicas iniciadas pelo Mevalonato.
OBS: As duas primeiras reações da via de síntese do
colesterol são similares às que produzem os corpos
cetônicos.
SÍNTESE DE HMG-COA
• Síntese de Acetoacetil-COA a partir de 2 moléculas de
ACetil-COA com liberação do grupamento COA.
o Enzima Tiolase
• Síntese de HMG-COA a partir da reação do Acetoacetil-
COA com outra molécula de Acetil-COA, havendo
liberação de grupamento COA.
o Enzima HMG-COA sintase
Obs: O parênquima hepático apresenta duas isoformas da
HMG-COA sintase.
• HMG-COA sintase citosólica à Síntese de Colesterol
• HMG-COA sintase mitocondrial à Síntese de corpos
• cetônicos
SÍNTESE DE ÁCIDO MEVALÔNICO (MEVALONATO)
• Reação de redução do HMG-COA à doação de íons pelo
NADPH + liberação de grupamento COA
• Etapa limitante da velocidade e o passo regulador da
síntese de colesterol
A seguir, uma série de 8 reações mais específicas irão
• Ocorre no citosol usando duas moléculas de NADPH como
ocorrer, tomando o Mevalonato como substrato para,
agente redutor + liberação de COA.
posteriormente, haver-se a formação do colesterol.
• Reação Irreversível.
• Reação catalisada pela enzima HMG-COA redutase
Elas encontram-se descritas no página a seguir:
o Sua expressão é inibida por Colesterol
REGULAÇÃO DA SÍNTESE DO COLESTEROL b) Aceleração esterol-dependente da degradação enzimática
• Quando os níveis de colesterol estiverem muito altos, a
HMG-COA redutase à Enzima limitante da velocidade da HMG-COA redutase irá ligar-se a proteínas que irão
reação de síntese do colesterol promover sua ubiquitinzação e degradação proteossomal.
• Essa regulação está sujeita a diversos tipos de controle • Logo, Colesterol = Degradação da HMG-COA redutase
metabólico como:
o Regulação esterol-dependente da expressão c) Fosforilação/desfosforilação independente de esteróis
gênica • A atividade da HMG-Coa redutase é controlada por
o Aceleração esterol-dependente da degradação alterações covalentes produzidas por ação da ptn cinase
enzimática ativada por AMP ou AMPk.
o Fosforilação/desfosforilação independente de • HMG-COA fosforilada à Inativa
esteróis • HMG-COA desfosforilada à Ativa
o Regulação hormonal
d) Regulação Hormonal
a) Regulação esterol-dependente da expressão gênica • Aumento de Insulina à Aumento da concentração do gene
• A expressão do gene da HMG-COA reutase é controlada da HMG-COA redutase
por fatores transcricionais que irão estimular o aumento • Aumento do Glucagon à Redução da expressão do gene
da síntese do HMG-COA quando os níveis de colesterol da HMG-COA redutase
estiverem baixos.
• Se os níveis de Colesterol estiverem altos, tais fatores
transcricionais irão cessar o estímulo para a síntese da
HMG-COA redutase.
Obs: Inibição por fármacos à As Estatinas são análogos Tamanho e Densidade (ptns = densidade)
estruturais da HMG-COA e atuam diretamente como • Quilomícrons à menor densidade e maior tamanho
inibidores competitivos e reversíveis da HMG-COA redutase. o Contém maior porcentagem de lipídeos e menor
• Uso para diminuir os níveis plasmáticos de colesterol em de ptns
pacientes com hipercolesterolemia. • VLDLs e LDLs à densidade reduzida pois ainda carregam
bastante lipídeos
DEGRADAÇÃO DO COLESTEROL • HDL à Partículas mais densas
Em humanos, o colesterol devido a sua estrutura cíclica não Apolipoproteínas à Partículas associadas as vesículas
pode ser degradado até CO2 e H2O. lipoproteicas que execem funções diversas, como:
• Núcleo esterol é eliminado intacto pela sua conversão em • Fornecem sítios de reconhecimento para receptores nas
ácidos e sais biliares, que são excretados nas fezes, superfícies celulares
o Ou o colesterol pode ser eliminado sem • Atuam como ativadoras ou coenzimas para enzimas
metabolização prévia diretamente na bile, que é envolvidas no metabolismo das lipoproteínas
transportada até o Intestino para eliminação. • Algumas são componentes estruturais essenciais das
• No Intestino, parte do colesterol é modificada por lipoproteínas, não podendo ser removidas.
bactérias antes da excreção. o Outras já podem ser transferidas livremente
entre as lipoproteínas
LIPOPROTEÍNAS PLASMÁTICAS
• São classificadas pela sua estrutura e sua função em 5
As liproteínas plasmáticas são complexos macromoleculares classes principais à A, B, C, D e E.
esféricos de lipídeos e proteínas específicas (apolipoproteínas • As diferentes classes podem ainda ser divididas em
ou apoproteínas). Dentre elas incluem-se: subclasses (ex: apolipoproteína A-I e apo-CII).
• vLDL à lipoproteínas de densidade muito baixa
• LDL à Lipoproteínas de densidade baixa
• ILDLs à Lipoproteínas de densidade intermediária
• HDLs à Lipoproteínas de alta densidade
As lipoproteína diferem-se na sua composição lipídica e
proteica, em seu tamanho, densidade e em seu sítio de origem.
FUNÇÃO à Tentar manter solúveis os componentes lipídicos
de modo a transportá-los de forma eficaz pelo plasma
sanguíneo.
• Constituem um eficiente mecanismo de transporte de
lipídeos entre os tecidos!
Nos humanos, esse transporte é menos perfeito do que em
outros animais.
• Com isso, pode acontecer uma deposição gradual de
lipídeos – especialmente do coleseterol – nos tecidos.
o Potencial fator de risco à estreitamento de
vasos sanguíneos (aterosclerose)
COMPOSIÇÃO DAS LIPOPROTEÍNAS PLASMÁTICAS
As lipoproteínas são constituídas por um núcleo de lipídeos
neutros (triacilglicerois e ésteres de colesterol) envolvido por
uma camada anfipática de apolipoproteínas, fosfolipídeos e
colesterol livre.
• A camada anfipática direciona seus componentes polares
na superfície da lipoproteína de modo a torna-la solúvel
em meio aquoso.
• Os triacilgliceróis e o colesterol carregados pelas
lipoptns são obtidos da dieta (fonte exógena) ou via
síntese de novo (fonte endógena)
• As diferentes lipoptns trocam constantemente de lipídeos
e apolipoproteínas umas com as outras, logo sua
composição é variável.
Degradação dos triacilgliceróis pela lipase liproteica à A
lipase lipoproteica é uma enzima extracelular ancorada por
heparan sulfato na parede dos capilares da maioria dos
tecidos.
• Predominante nos tecidos adiposo, cardíaco e muscular
esquelético (fígado adulto não tem essa enzima)
• Ela é ativada pela apolipoproteína C-II
• Irá atuar hidrlisando os triacilgliceróis, formando ácidos
graxos livres e glicerol.
• Os ácidos graxos serão armazenados pelos adipócitos ou
serão utilizados pelo musculo esquelético e cardíaco para
produção de energia.
• Se não forem utilizados imediatamente, os ácidos graxos
livres serão ligados a albumina sérica e transportados até
que sua captação ocorra.
• Glicerol à Utilizado pelo fígado na síntese de lipídeos,
glicólise ou gliconeogênese.
Obs: A lipase hepática é encontrada na superfície das células
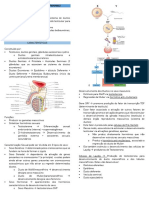
METABOLISMO DOS QUILOMÍCRONS
endoteliais do fígado.
Os quilomícrons são formados nas células da mucosa • Ela não ataca os triacilgliceróis do quilomícron ou das
intestinal e transportam para os tecidos periféricos: vLDLS.
• Triacilgliceróis (90% da composição do quilomícron) • Sua atuação centra-se no metabolismo do HDL.
• Colesterol
• Vitaminas Lipossolúveis Obs 2: Hiperlipoproteínemia do tipo I/deficiência familiar de
• Ésterers de colesterol da dieta lipase lipoproteica
• Lipídeos sintetizados pelos enterócitos • Quadros em que o indivíduo terá deficiência ou da lipase
liproproteica ou de APO-CII.
Síntese das apoproteínas à APO B-48 (exclusiva do
• Estes indívudos apresentarão grande acúmulo de
quilomícron)
quilomícron mesmo em jejum, que não será metabolizado.
• Começa a aser sintetizada no RER, sendo glicosilada a
passar por ele e pelo complexo de Golgi.
Regulação da atividade da lipase lipoproteica
Montagem dos quilimícrons à As enzimas envolvidas na • INSULINA à Regula a síntese da lipase lipoproteica e sua
síntese dos triacilgliceróis, do colesterol e dos fosfolipídeos transferência para a superfície luminal dos capilares.
estão localizadas no REL.
• A organização das apoliproteínas e dos lipídeos para • Influência do Km à Quanto maior o Km da lipase
formar o quilomícron depende da ptn microssomal lipoproteica maior deverá ser a concentração de
transferidora de triacilgliceróis triacilgliceróis nos sangue para que ela possa atuar.
• Essa ptn irá ligar a apo-B48 aos lipídeos o Lipase lipoproteica do tecido adiposo à Km alto
o Isso ocorre antes da transição do RE para o § Só consegue remover os ácidos graxos
aparelho de Golgi, onde as partícula são das lipoproteínas circulantes quando
acondicionadas em vesículas secretórias. sua concentração plasmática estiver
o Ocorre a fusão dessas vesículas com a elevada.
membrana plasmática, havendo a liberação das o Lipase lipoproteica do músculo cardíaco à Km
lipoproteínas no sistema linfático e dele para o baixo
sangue. § Possui acesso contínuo aos
Modificação dos Quilomícrons nascentes à A partícula combustíveis circulantes
liberada pelas células da mucosa intestinal é chamada de § Consegue remover os ácidos graxos
quilomícron nascente que é funcionalmente incompleta. mesmo quando estes estão em
• Ao alcanár o plasma, ela será rapidamente modficada concentrações reduzidas
recebendo a apo E e as apoproteínas C cedidas pelo HDL
circulante. Formação dos remanescentes dos quilomícrons à Quando
o Apo E à é reconhecida pelos receptores mais de 90% dos triacilgliceróis do quilimomícron já forma
hepáticos degradados pela lipase lipoproteica, a partícula irá diminuir de
o Apo C-II à necessária para ativação da lipase tamanho e aumentar em densidade.
liproteica • Apoproteínas C apenas (mas não a APO E) irá retornar
§ Degrada os triacilgliceróis do para o HDL.
quilomícron • Partícula do quilomícron remanescente será rapidamente
removida da circulação pelo fígado.
o Células hepáticas apresentem receptores para
lipoproteínas que reconhecem a APO-E.
• Estes remanescentes serão capturados pelos hepatócitos via fagocitose.
• Em seguida, ocorre a fusão da vesícula endocitada com lisossomos, havendo a degradação das apolipoproteínas, dos ésteres
de colesterol e outros componentes, gerando:
o Ácidos graxos
o Aminoácidos o Reciclagem de receptor
o Colesterol Livre
METABOLISMO DAS VLDLS Obs: Abetalipoproteínemia à Tipo raro de hipoliproteinemia
causada por um defeito na ptn microssomal transferidora de
• As vLDLs são produzidas pelo fígado triacigliceróis, que impede o carregamento da apo B com
• Compostas predominantemente por triacilgliceróis (60%) lipídeos.
• Função à carregar os triacigliceróis do fígado para • Com isso não há a formação de quilomícrons ou vLDLs
tecidos periféricos (colesterol endógeno) causando acúmulo de triacilgliceróis no fígado e Intestino.
o Sofrerão degradação pela lipase liproteica, assim
como os quilimícrons MODIFICAÇÃO DAS VLDL CIRCULANTES à A medida que o
vLDL passa pela circulação o triacigliceról será degradado
Obs: Esteatose Hepática à Quadro que ocorre em condições pela lipase liproteica, tornando o vLDL menor e mais denso.
de desequilíbrio entre a síntese hepática dos triacilgliceróis e • Apoproteínas C e E retornam para os HDLs, enquanto que
a secreção de vLDL. a apo B-100 é retida.
• Excesso e deposição de triacilgliceróis no fígado • Triacigliceróis serão transferidos das vLDLs para as
• Associada a quadros como obesidade, diabetes mellitus HDLs em uma reação de troca.
não controlada e ingestão crôncia de Etanol. o HDL por sua vez transfere ésteres de colesterol
para as vLDLs.
Liberação das vLDLs à As vLDLs são secretadas no sangue o Troca mediada pela ptn trocadora de ésteres de
pelo fígado como partículas de vLDL nascentes contendo colesterol
apenas apo-B100.
• Na circulação elas obtém apo C-II e apo E derivada da HDL
circulante.
• Dentro da célula os receptores da LDL serão reciclados,
enquanto que as liproteínas remanescente nas vesículas
serão transferidas para lisossomos, sendo degradadas
por enzimas liberando:
o Colesterol Livre
o Aminoácidos
o Ácidos graxos
o Fosfolipídeos
Efeitos Do Colesterol Endocitado sobre a Homeostasia celular
à O colesterol originário dos remanescentes de quilomícron,
das IDL e das LDLs afetam o conteúdo celular de várias
maneiras. Como:
• Colesterol à Inibição da HMG-Coa redutase
o Redução da síntese de novo de colesterol
• Ausência de necessidade imediata de colesterol para
Produção de LDL a partir de vLDL do plasma à Com as
funções estruturais ou síntese de derivados de colesterol
modificações descritas anteriormente as vLDLs são
o Esterrificação do colesterol pela ACAT (acilCOA
convertidas no plasma em LDL.
colesterol-aciltransferase)
• Antes de formar-se o LDL, temos a formação do IDL
o Produção de ésteres de colesterol que serão
(remanescente do vLDL) à fase de transição
armazenados na célula
• As IDLs também podem ser captadas pelas células por
o Colesterol intracelular à ACAT ativada
meio de endocitose mediada por receptor, usando a apo E
• Colesterol à Redução da síntese de receptores
como ligante.
proteicos de LDL
METABOLISMO DAS LDLs o Limitação da entrada de colesterol LDL nas
células
As LDLs contém muito menos TAGs que suas precursoras
o Aumento da entrada de colesterol na célula induz
vLDLs.
um mecanismo de feedback negativo sobre o
• Apresentam alta concentração de colesterol/ésteres de
gene do receptor de LDL
colesterol.
§ Redução da expressão desse gene e da
Principal função à Prover colesterol para os tecidos síntese de receptores, de modo a barrar
periféricos a entrada de excedentes de colesterol
dentro da célula
Endocitose mediada por receptores à As LDLs devem ligar-
§ Excedente de colesterol permanecerá
se na superífice da membrana celular para prover colesterol
circulante no sangue, gerando uma
para as células dislipidemia.
• Receptores devem reconhecer sua APO B-100.
Captação das LDLs quimicamente modificadas por receptores • A FCCAT liga-se às HDLs nascentes, sendo ativada pela
removedores de macrófagos APO-1, fazendo com que elas acumulem ésteres de
• As LDLs podem também ser capturadas por macrófagos colesterol.
que possuem altos níveis de receptores removedores o Formação de HDL-3 à pobre em ésteres de
classe A (RR-A) colesterol
• Eles reconhecem principalmente LDLs quimicamente o Em seguida, de HDL-2 à ricas em ésteres de
modificadas, cujos componentes lipídicos ou a apo-B colesterol, que o transportam para o fígaod.
estão oxidados. • Os ésteres de colesterol presentes no HDL irão ser
• A expressão do receptor RR-A não é regulada a nível de armazenados posteriormente no fígado, sendo
expressão gênica pelo aumento das concentrações transportados pelo próprio HDL ou sendo transferidas
intracelulares de colesterol para os vLDLs.
o Assim, mesmo havendo um excedente de • Proteína transferidora de ésteres de Colesterol à irá
colesterol no macrófago, a expressão dos fazer a transferência destes ésteres de colesterol
receptores removedores não será inibida! carregados pelo HDL para as VLDLs em troca de TAGs.
o Logo, eles continuarão absorvendo as LDLs o Uma vez que as vLDLs são catabolizadas a LDLs,
quimicamente modificadas. os ésteres de colesterol terminam sendo
• Com isso, os ésteres de colesterol continuarão capturados pelo fígado.
acumulando-se nos macrófagos causando sua
transformação em células espumosas que patticipam da Obs: A Lipase Hepática participa da conversão das HDL2 em
formação de placas ateroscleróticas. HDL3.
• Ademais, ela degrada tanto triacilgliceróis quando
METABOLISMO DAS HDLs fosfolipídeos.
As HDLs são uma família heterogênea de liproteínas com Transporte Reverso do Colesterol à Consiste na
metabolismo complexo. transferência seletiva do Colesterol dos tecidos periféricos
• São formadas no sangue a paritr da adição de lipídeos à para as HDLs e das HDLs para o fígado e ou tecidso
APO-1 (produzida pelo fígado e pelo Intestino e secretada esteroidogêncios.
no sangue) • Tal processo é essencial para a homeostasia do
• APO-1 à Compreende 70% das apoproteínas das HDLs. colesterol.
• No fígado à Colesterol pode ser convertido em ácidos
Funções da HDL: biliares ou excretado pela Bile.
• Reservatório de apolipoproteínas • Nos tecidos esteroidogêncios à Pode servir de substrato
• Captação de Colesterol não-esterificado para síntese de hormônios.
• Esterificação do Colesterol • O transporte reverso é responsável pela reação inversa
• Transporte Reverso do Colesterol existente entre a concentração plasmática de HDL e a
aterosclerose
Reservatório de apolipoproteínas à As HDLs servem como o HDL designada como uma “boa transportadora do
um reservatório circulante de apo C-II e de apo-E. colesterol.
• Relembrando... o HDL à ¯ Risco para Aterosclerose
o Apo C-II à ativadora da lipase lipoproteica
(quilomícrons e vLDLs) Em suma, o transporte reverso envolve:
o Apo E à endocitose mediada por receptor das • Efluxo de colesterol dos tecidos periféricos para as HDLs
IDLs e remanescentes de quilomícron • Esterificação do colesterol pela FCCAT
• Ligação das HDLs ricas em colesterol (HDL2) às células
hepáticas e células de tecidso esteroidogênicos
Captação de Colesterol não-esterificado à As partícula de o Transferência seletiva dos ésteres de colesterol
HDLs nascentes têm formato discoide contendo para essas células
principalmente fosfolipídeos e apoliproteínas A, C e E. • Liberação das HDLs depletadas/livres desse lip’dieo
• Elas podem rapidamente converter seu formato discoide (HDL3)
em um formato esférico ao acumularem colesterol não
esterificado derivado de outras lipoproteínas e das O efluxo de colesterol da células periféricas é mediado pela
membranas celulares. proteína transportadora ABCA1.
• Elas são excelentes aceptoras de colesterol não
esterificado por serem ricas em fosfolipídeos que Já a captação de ésteres de colesterol pelo fígado é mediado
solubilizam o colesterol. por receptores RR-B1 que ligam-se às HDLs.
Esterificação do Colesterol à Quando o Colesterol é captado
pelas HDLs ele é imediatamente esterficado pela enzima
FCCAT (fosfatidilcolina colesterol-aciltransferase)
• Tal enzima é sintetizada pelo fígado
LP(a) à LIPOPROTEÍNA A Metabolismo de colesterol à é extremamente regulado à seu
acúmulo na célula não é normal!
Lp(a) à Partícula que em grandes qtdes no plama está
associada ao aumento do risco de doença coronariana. • Doença inflamatória caracterizada pela deposição de
• Sua estrutura é quase idêntica a uma patícula de LDL, mas colesterol na túnica íntima dos vasos de grande e médio
apresenta uma apoliproteína adicional – apo(a). calibre
o A apo(A) liga-se covalentemente a um sítio na • Atenção a quantidade e a qualidade dos lipídeos ingeridos
apo-b100, o que permite a diferenciação das duas na dieta à este penetram na barreira endotelial e
lipoproteínas. invadem a íntima dos vasos à Lesão endotelial
Os níveis circulantes de Lp(a) são determinados
geneticamente, contudo alguns fatores podem também alterar Processo de Invasão
sua concentração. 1. Aumento dos espaços interendoteliais à Penetração dos
• Ácidos graxos trans (gorduras trans) à Lp(a) lipídeos na túnica íntima
• Estrógenos à ¯ LDL ¯ Lp(a)
2. Adesão e Agregação Plaquetária
Há grande homologia entre a Lp(a) e o plasmionogênio –
precursor da protease sanguínea cujo substrato é a fibrina, 3. LDL oxidada vai estimular as células endoteliais a
principal ptn dos coágulos sanguíneos. sintetizarem moléculas de adesão + quimiocinas/citocinas
• É provável que a concentração elevada de Lp(a) torne atrativas para monócitos
mais lenta a degradação de coágulos sanguíneos
• Lp(a) irá competir com o plasminogênio para ligação na 4. Diapedese dos monócitos para a Íntima à Transformam-se
fibrina. em macrófagos e capturam a LDL presente na íntima
• O acúmulo destes coágulos pode causar ataques • Tornam-se células espumosas
cardíacos e outros distúrbios cardiovasculares.
5. Macrófagos ativados vão produzir mais citocinas e
ATEROSCLEROSE quimiocinas estimuladoras da atividade da célula endotelial -
que também produzirá essas substâncias atraindo mais
Doença Multifatorial à Diversos fatores de risco monócitos e linfócitos para a Íntima
• Obesidade .
• Sedentarismo 6. Monócitos+Linfócitos+Plaquetas à liberam outros fatores
• Tabagismo de crescimento e outros mediadores que induzem a migração
• Hipertensão Arterial de células musculares da camada média para a íntima.
• Diabetes Induzem também a neoformação de vasos.
• Células musculares também capturam o LDL e tornam-
Patogênese à Temos uma dislipidemia que se caracteriza se células espumosas.
pela degradação de lipídeos mais complexos, com formação
excessiva de ácidos graxos livres e colesterol. 7. Células Musculares diferenciam-se em Miofibroblastos à
passam a sintetizar matiz extracelular fibrosa
• Contribuem para formar a capa fibrosa que envolve o
núcleo lipídico.
Você também pode gostar
- Regulação do Colesterol emDocumento12 páginasRegulação do Colesterol emRenato Torres Moul50% (2)
- Metabolismo Do Colesterol e Sais BiliaresDocumento8 páginasMetabolismo Do Colesterol e Sais BiliaresErika BennaiaAinda não há avaliações
- Roseli unip farmáciaDocumento7 páginasRoseli unip farmáciawemillynobreAinda não há avaliações
- BiossínteseDocumento48 páginasBiossínteseJosé Eduardo AdornoAinda não há avaliações
- 15 - Biossíntese Do Colesterol PDFDocumento5 páginas15 - Biossíntese Do Colesterol PDFIvone Pires PortoAinda não há avaliações
- Hormonios Resumida 2023 E-Disciplinas02Documento50 páginasHormonios Resumida 2023 E-Disciplinas02adrianasoaresyuriAinda não há avaliações
- Metabolismo dos LipídeosDocumento68 páginasMetabolismo dos LipídeosLetícia CabralAinda não há avaliações
- Metabolismo Do ColesterolDocumento13 páginasMetabolismo Do ColesterolIhury JhonsonAinda não há avaliações
- Regulação Metab EnzimasDocumento14 páginasRegulação Metab EnzimasMarcelo MorettoAinda não há avaliações
- Metabolismo Do Colesterol e Sais BiliaresDocumento9 páginasMetabolismo Do Colesterol e Sais BiliaresErika BennaiaAinda não há avaliações
- Regulação Do Metabolismo - HORMÔNIOS 2023Documento42 páginasRegulação Do Metabolismo - HORMÔNIOS 2023Nádia SousaAinda não há avaliações
- Metabolismo em Jejum - Colunistas - Sanar MedicinaDocumento8 páginasMetabolismo em Jejum - Colunistas - Sanar MedicinaHelder,s Evolution DesignerAinda não há avaliações
- Distúrbios Metabólicos em RuminantesDocumento101 páginasDistúrbios Metabólicos em RuminantesFlávio Moreno100% (2)
- Síntese de Ácidos Graxos e ColesterolDocumento49 páginasSíntese de Ácidos Graxos e ColesterollouisecdmAinda não há avaliações
- Regulação do metabolismo e perfis metabólicos dos principais órgãosDocumento2 páginasRegulação do metabolismo e perfis metabólicos dos principais órgãosPATRICIA AMORIMAinda não há avaliações
- Esteatose Hepática: Causas e Aspectos MorfológicosDocumento75 páginasEsteatose Hepática: Causas e Aspectos MorfológicosAna Cristina DuqueAinda não há avaliações
- Uma Panorâmica Geral Das Vias Metabólicas AvançadissimoDocumento4 páginasUma Panorâmica Geral Das Vias Metabólicas AvançadissimoallanfradiqueAinda não há avaliações
- Aula 2 (DCV) e 3 (PUFA)Documento71 páginasAula 2 (DCV) e 3 (PUFA)camilobt100% (1)
- Sistema de EndomembranasDocumento37 páginasSistema de EndomembranasRose Meire Costa BrancalhãoAinda não há avaliações
- #Anti-Inflamatórios Esteroides (Aie)Documento7 páginas#Anti-Inflamatórios Esteroides (Aie)CarolWolfMachadoAinda não há avaliações
- Metabolismo de Lipídeos Aula 2Documento26 páginasMetabolismo de Lipídeos Aula 2Brunno PinhoAinda não há avaliações
- Resolução Lista BioquimicaDocumento16 páginasResolução Lista BioquimicaVitor SouzaAinda não há avaliações
- Fisiologia Hepática PDFDocumento5 páginasFisiologia Hepática PDFRenata Lima de FreitasAinda não há avaliações
- Bio - Metabolismo HepáticoDocumento4 páginasBio - Metabolismo HepáticoCaique André100% (1)
- Glicocorticoides 2007Documento8 páginasGlicocorticoides 2007elizasalesAinda não há avaliações
- Metabolismo de carboidratos: glicólise, ciclo de Krebs e gliconeogêneseDocumento41 páginasMetabolismo de carboidratos: glicólise, ciclo de Krebs e gliconeogêneseRosiane Gomes Silva Oliveira100% (1)
- DislipidemiaDocumento58 páginasDislipidemiaTaís MaiaAinda não há avaliações
- Antiinflamatórios esteroidais e córtex adrenalDocumento2 páginasAntiinflamatórios esteroidais e córtex adrenalAndressa NevesAinda não há avaliações
- Digestão e absorção de macromoléculasDocumento110 páginasDigestão e absorção de macromoléculasAndre GuimaraesAinda não há avaliações
- Metabolismo Do Colesterol - ResumidoDocumento5 páginasMetabolismo Do Colesterol - ResumidoDianaAinda não há avaliações
- Módulo 6 - Oxidação de Ácidos GraxosDocumento17 páginasMódulo 6 - Oxidação de Ácidos GraxosBeatriz De Sousa CoelhoAinda não há avaliações
- Estudo de CasoDocumento20 páginasEstudo de CasoEng.Civil Andre ́ de JesusAinda não há avaliações
- Regulação hormonal do metabolismo energéticoDocumento52 páginasRegulação hormonal do metabolismo energéticoLeandro CastilhaAinda não há avaliações
- Anotações Conferencia Biocel 2Documento3 páginasAnotações Conferencia Biocel 2Ana Laura MartinsAinda não há avaliações
- Aula 6 Lipídeos, Lipoproteínas e ApolipoproteínasDocumento50 páginasAula 6 Lipídeos, Lipoproteínas e ApolipoproteínasLídia Rosa100% (1)
- Metabolismo de Lipídeos: Formação de Corpos Cetônicos e ColesterolDocumento26 páginasMetabolismo de Lipídeos: Formação de Corpos Cetônicos e ColesterolLorena HenriquesAinda não há avaliações
- Problema 03 11Documento20 páginasProblema 03 11Ricardo Vitor Mesquita BedettiAinda não há avaliações
- Aula 10 - Lipídios Na Nutrição AnimalDocumento48 páginasAula 10 - Lipídios Na Nutrição Animaleriksilva4587Ainda não há avaliações
- Bioquímica Esportiva Macroeconomia Do Metabolismo EnergéticoDocumento19 páginasBioquímica Esportiva Macroeconomia Do Metabolismo EnergéticoFranck Jose Poravoski TolfoAinda não há avaliações
- Diarrei CronicaDocumento19 páginasDiarrei CronicaMarisa Vilaverde NarcisoAinda não há avaliações
- Perfil Lipidico e GlicemicoDocumento21 páginasPerfil Lipidico e GlicemicoAurilane Oliveira da SilvaAinda não há avaliações
- Uma Panorâmica Geral Das Vias MetabólicasDocumento4 páginasUma Panorâmica Geral Das Vias Metabólicaskk da quimicaAinda não há avaliações
- Aula Lipidios Partes II e IIIDocumento28 páginasAula Lipidios Partes II e IIIGabriel NobregaAinda não há avaliações
- Regulação e Integração Metabólica QuímicaDocumento106 páginasRegulação e Integração Metabólica QuímicaKimberly FreitasAinda não há avaliações
- Dislipidemias e Aterosclerose: Aspectos GeraisDocumento74 páginasDislipidemias e Aterosclerose: Aspectos Geraispatricia torkaski100% (1)
- Ligações Glicosídicas, Enzimas e Digestão de CarboidratosDocumento9 páginasLigações Glicosídicas, Enzimas e Digestão de CarboidratosLadina_Ainda não há avaliações
- Fisiologia HepáticaDocumento3 páginasFisiologia HepáticaNusia MotaAinda não há avaliações
- Aula+02+Bioquímica.+Introdução+à+Bioquímica.+Substratos+energéticos.+Água.Documento37 páginasAula+02+Bioquímica.+Introdução+à+Bioquímica.+Substratos+energéticos.+Água.ThiagoSoaresAinda não há avaliações
- Metabolismo Do ColesterolDocumento4 páginasMetabolismo Do ColesterolFlávia Duarte100% (1)
- Bioenergética aplicada à Atividade Física e EsporteDocumento46 páginasBioenergética aplicada à Atividade Física e EsporteMarilia TarragoAinda não há avaliações
- Lipídios: funções, classificação e metabolismoDocumento82 páginasLipídios: funções, classificação e metabolismokaline cardosoAinda não há avaliações
- Digestão e absorção de lipídios: da dieta às célulasDocumento42 páginasDigestão e absorção de lipídios: da dieta às célulasLívia Born100% (1)
- Dislipidemia - Aula SanarDocumento5 páginasDislipidemia - Aula SanarRodolfo CabralAinda não há avaliações
- Prova Bioquímica com questões sobre desidratação, diabetes e tampõesDocumento3 páginasProva Bioquímica com questões sobre desidratação, diabetes e tampõesthamiAinda não há avaliações
- Aulas Metabolismo Parte 1 N3 - Bioquímica PDFDocumento63 páginasAulas Metabolismo Parte 1 N3 - Bioquímica PDFWillian FerrudaAinda não há avaliações
- Lipidios, Apolipos e LipoproteinasDocumento105 páginasLipidios, Apolipos e LipoproteinasMarval Fone100% (1)
- Aula Função HepáticaDocumento33 páginasAula Função HepáticaMel DanielleAinda não há avaliações
- Controle hormonal e neural do metabolismoDocumento7 páginasControle hormonal e neural do metabolismoKeyla Silva100% (1)
- Rejuvenescer Com O Plasma Sanguíneo Dos JovensNo EverandRejuvenescer Com O Plasma Sanguíneo Dos JovensAinda não há avaliações
- Histologia - S Reprodutor MasculinoDocumento18 páginasHistologia - S Reprodutor MasculinoFelipe GonzalezAinda não há avaliações
- Imunidade de MucosasDocumento4 páginasImunidade de MucosasFelipe GonzalezAinda não há avaliações
- Fisiologia Renal emDocumento26 páginasFisiologia Renal emFelipe GonzalezAinda não há avaliações
- Sistema imune: imunidade inata e adaptativaDocumento8 páginasSistema imune: imunidade inata e adaptativaFelipe GonzalezAinda não há avaliações
- Fisiologia Das Hemácias1Documento8 páginasFisiologia Das Hemácias1Felipe GonzalezAinda não há avaliações
- Parasitos PDFDocumento156 páginasParasitos PDFAlison MartinsAinda não há avaliações
- Homeostase e Coagulação SanguíneaDocumento8 páginasHomeostase e Coagulação SanguíneaFelipe GonzalezAinda não há avaliações
- Sistema imune: imunidade inata e adaptativaDocumento8 páginasSistema imune: imunidade inata e adaptativaFelipe GonzalezAinda não há avaliações
- Funções das células T CD4+ efetoras na eliminação de microrganismosDocumento9 páginasFunções das células T CD4+ efetoras na eliminação de microrganismosFelipe GonzalezAinda não há avaliações
- Fisiologia Sangue Abo e RHDocumento4 páginasFisiologia Sangue Abo e RHFelipe GonzalezAinda não há avaliações
- Fisiologia Das Hemácias1Documento8 páginasFisiologia Das Hemácias1Felipe GonzalezAinda não há avaliações
- Metabolismo de LipídeosDocumento12 páginasMetabolismo de LipídeosFelipe GonzalezAinda não há avaliações
- AMEBÍASE E GIARDIASE: ASPECTOS CLÍNICOS, CICLO DE VIDA E PROFILAXIADocumento8 páginasAMEBÍASE E GIARDIASE: ASPECTOS CLÍNICOS, CICLO DE VIDA E PROFILAXIAFelipe GonzalezAinda não há avaliações
- Mecanismos-chave da tolerância e autoimunidadeDocumento8 páginasMecanismos-chave da tolerância e autoimunidadeFelipe GonzalezAinda não há avaliações
- FEBRE HEMORRÁGICA DA DENGUE FisiopatologiaDocumento4 páginasFEBRE HEMORRÁGICA DA DENGUE FisiopatologiaLukas MadeiraAinda não há avaliações
- A Linguagem e A Construção Do Real Pela Criança: Contrapontos Entre Lev S.vygotsky e Jean PiagetDocumento15 páginasA Linguagem e A Construção Do Real Pela Criança: Contrapontos Entre Lev S.vygotsky e Jean PiagetRevista Olhar de ProfessorAinda não há avaliações
- Ensino Fundamental - Ciências - Atividade de acompanhamento da aprendizagem escolarDocumento3 páginasEnsino Fundamental - Ciências - Atividade de acompanhamento da aprendizagem escolarOcilia dos Santos BromenchenkelAinda não há avaliações
- Dissertação FINAL para DepositoDocumento94 páginasDissertação FINAL para DepositoPH Ph GnsoAinda não há avaliações
- Mecanismo de Acao Dos Herbicidas Parte 1Documento25 páginasMecanismo de Acao Dos Herbicidas Parte 1Leandro Dos santos paivaAinda não há avaliações
- Cronograma EnfermagemDocumento3 páginasCronograma EnfermagemangeloAinda não há avaliações
- Efeito Da Acupuntura No Tratamento Da Plaquetopenia FinalDocumento30 páginasEfeito Da Acupuntura No Tratamento Da Plaquetopenia FinalramaralAinda não há avaliações
- Tanatologia forense - Estudo da morte e perícia médico-legalDocumento147 páginasTanatologia forense - Estudo da morte e perícia médico-legalMarcos Soar100% (2)
- A importância da luz solar para a vidaDocumento1 páginaA importância da luz solar para a vidaIsabel Cristina Barbosa BernardiAinda não há avaliações
- Fuvest - 1 Fase - ResoluçãoDocumento91 páginasFuvest - 1 Fase - ResoluçãoAntonia NunesAinda não há avaliações
- Livro Unico PDFDocumento192 páginasLivro Unico PDFandreia pereiraAinda não há avaliações
- 10-Ciclos de VidasDocumento75 páginas10-Ciclos de VidasmanuelafonsecaAinda não há avaliações
- Proporção genotípica F2 cruzamento di-híbridoDocumento4 páginasProporção genotípica F2 cruzamento di-híbridoChiara Cristina Marafon CorreiaAinda não há avaliações
- Aula Prática 3Documento6 páginasAula Prática 3jessica souzaAinda não há avaliações
- Mutação e Reparo Do DNADocumento32 páginasMutação e Reparo Do DNALUIZROBERTOBIOLOGO1387Ainda não há avaliações
- PP30 Hetrotrofia e Membrana PlasmáticaDocumento43 páginasPP30 Hetrotrofia e Membrana PlasmáticaGustavo LapoAinda não há avaliações
- Farmacologia Endócrina Do PâncreasDocumento17 páginasFarmacologia Endócrina Do PâncreasRodrigo Santos100% (2)
- Décio Sena - Coleção Provas Comentadas - Português FCC - 3º Edição - Ano 2010Documento448 páginasDécio Sena - Coleção Provas Comentadas - Português FCC - 3º Edição - Ano 2010Ricardo AndradeAinda não há avaliações
- A Importância Do Selênio Nos Níveis Dos Anticorpos Antiperoxidase Na Tireoidite de HashimotoDocumento8 páginasA Importância Do Selênio Nos Níveis Dos Anticorpos Antiperoxidase Na Tireoidite de HashimotoRicardo NovaisAinda não há avaliações
- Tratamento Da Amebiase TraduçãoDocumento14 páginasTratamento Da Amebiase TraduçãoVanessa OliveiraAinda não há avaliações
- Cardiovascular Fitness: Tips for Creating an Exercise RoutineDocumento19 páginasCardiovascular Fitness: Tips for Creating an Exercise RoutinePriscilla LimaAinda não há avaliações
- Alfa-Amilase - Fisiologia VegetalDocumento7 páginasAlfa-Amilase - Fisiologia VegetalFCiênciasAinda não há avaliações
- Apontamentos - Primeiro - Miniteste - Pratico 1 PDFDocumento107 páginasApontamentos - Primeiro - Miniteste - Pratico 1 PDFBeatriz TeixeiraAinda não há avaliações
- Matriz Curricular Medicina Veterinária PDFDocumento1 páginaMatriz Curricular Medicina Veterinária PDFJaime GonçalvesAinda não há avaliações
- Aula sobre a composição química da célula e suas principais moléculasDocumento4 páginasAula sobre a composição química da célula e suas principais moléculasNathan Goodwin100% (1)
- QUESTÕES VACINAS AtualizadasDocumento12 páginasQUESTÕES VACINAS AtualizadasRoberta Souza De BarrosAinda não há avaliações
- Programa de Saude 2013 Saude e Doencas - CancerDocumento62 páginasPrograma de Saude 2013 Saude e Doencas - CancerjoseAinda não há avaliações
- Relatório de Estágio em Analises ClínicasDocumento20 páginasRelatório de Estágio em Analises ClínicasAna Caroline Silva90% (10)
- Microbiologia - Microorganismos IndicadoresDocumento22 páginasMicrobiologia - Microorganismos IndicadoresJose Fernando Solanilla Duque0% (1)
- Principais escolas psicológicasDocumento16 páginasPrincipais escolas psicológicasGraça Martins Martins100% (1)