Escolar Documentos
Profissional Documentos
Cultura Documentos
Ciclo de Vida Pilas
Enviado por
Peke1128Direitos autorais
Formatos disponíveis
Compartilhar este documento
Compartilhar ou incorporar documento
Você considera este documento útil?
Este conteúdo é inapropriado?
Denunciar este documentoDireitos autorais:
Formatos disponíveis
Ciclo de Vida Pilas
Enviado por
Peke1128Direitos autorais:
Formatos disponíveis
INTRODUCCION
Electroqumica. Es una rama de la qumica que trata los procesos qumicos producidos por el pasaje de la corriente elctrica y la produccin de la energa elctrica a partir de energa puesta en libertad en una reaccin qumica. Tambin es una disciplina cientfica que estudia y valora las relaciones existentes entre las reacciones qumicas y fenmenos elctricos. Aplicacin de la Electroqumica. Es muy usado en diversos campos debido a que no produce contaminacin del ambiente. Hoy en da se emplean procedimientos Electrolticos para obtener metales alcalinos y alcalinotrreos como el magnesio a partir de sus sales fundidas. Tambin se utilizan en la industria de electro recubrimiento, ya sea de tipo anticorrosivo o de naturaleza decorativa. La electrlisis constituye la base terica y prctica de la construccin de pilas y acumuladores de corriente continua, tambin cuentan con un amplsimo nmero de usos en la industria qumica y de materiales de construccin. Unidades y Ecuaciones Fundamentales.
La intensidad de una corriente que pasa por un conductor se expresa en amperios (A). La diferencia potencial en los puntos extremos de un conductor se expresa en voltios (V). La cantidad de energa transportada est dada en coulomb (COUL). Otra unidad de cantidad de energa que se emplea con frecuencia es el Faraday (F), que equivale a 96500 coulomb. La cantidad de electricidad transportada en la intensidad (I) Amperios en un tiempo (+) de + segundos, es igual a 9=I.T Proceso de la Electrlisis. Reaccin qumica producida por medio de la corriente elctrica que proviene de electrodos, descomponiendo los compuestos qumicos y desasindolos en iones. Reacciones de Oxido Reduccin. Son aquellas reacciones qumicas en las cuales un tomo se oxida y otro se reduce. La cantidad de electrones perdidos (tomos que se oxidan) es igual a la cantidad de electrones ganados (tomos que se reducen). Para determinar cul es el tomo que se oxido y cul es el que se produce, se utiliza lo que se conoce como numero de oxidacin. Importancia Industrial de los Procesos de Oxido Reduccin. Los procesos de Oxido Reduccin tienen aplicacin industrial con la finalidad de purificar y encontrar sustancias. Entre otros casos, la electrlisis puede aplicarse por cubrir ciertos materiales electrolticamente con aluminio y con cobre, una aplicacin industrial de los procesos de oxido DESARROLLO SUSTENTABLE CICLO DE VIDA DE LAS PILAS Y SU IMPACTO AMBIENTAL
reduccin que permite obtener cloro, hidrogeno e hidrxido de sodio es la electrlisis de una solucin de cloruro de sodio, para ello se agranda en una cuba electroltica, provisto de electrodos redes y conectados en una fuente de energa elctrica. Cuando se cierre el circuito se observa el desprendimiento del gas hidrogeno en ctodo y el cloro en el nodo. La solucin que queda como residuo es el hidrxido de sodio, todas estas sustancias tienen aplicacin industrial. Leyes de Faraday. Entre 18001830 Michael Faraday fsico y qumico ingles, realiz estudios cuantitativos referente a la relacin entre la cantidad de electricidad que pasa por una solucin y resultado de sus investigaciones las enuncio entre los aos 18331834 en las leyes que tienen su nombre. La primera ley de Faraday seala que la masa de una sustancia involucrada en la reaccin de cualquier electrodo es directamente proporcional a la cantidad de electricidad que pasa por una solucin. La segunda Ley, seala que las masas de las diferentes sustancias producidas por el paso de la misma cantidad de electricidad son directamente proporcionales a sus equivalentes en gramos. Electrlisis de Agua Acidulada. El agua solo conduce muy dbilmente la electricidad, si se le agrega una pequea cantidad de cido sulfrico (agua acidulada solucin de H2SO4 al 10%, se hace ms conductora y experimenta el proceso de electrlisis ms rpidamente. El proceso se realiza utilizando unos aparatos llamados voltmetros que poseen ramas laterales graduados en milmetros que permiten los volmenes de los gases desprendidos. El proceso consiste en llenar el voltmetro con agua acidulada cuidando que no quede aire en las ramas laterales y se conecta en una fuente de energa continua (una pila). Cuando se cierre el circuito, se observa un desprendimiento de gas en cada rama, cuando finaliza el proceso se puede observar que el gas desprendido en el electrodo negativo es el doble del de otra rama, con esto podemos demostrar que gas de mayor volumen es el hidrogeno y el de menos es el oxigeno. Celda Electroltica Qumica. Es un dispositivo simple de dos electrodos, sumergido en un electrolito capaz de originar energa elctrica por medio de una reaccin qumica. Si se produce una reaccin qumica por el paso de electricidad a travs de ella, tenemos las celdas electrolticas. Cuando se combinan dos o ms celdas en serie o paralelo se obtiene una batera. El acumulador de plomo es una batera constituida por tres celdas conectadas en serie. Celda de Daniell. Est formada de la siguiente forma: Un recipiente que contiene una solucin de sulfato de cobre, en la cual se encuentra introducida una lamina limpio de cobre. En la solucin se sumerge un vaso poroso que contiene una solucin de sulfato de zinc, dentro de la cual contiene una lamina limpia de zinc. Cuando el circuito se cierra usando conductores metlicos se observa un flujo de corriente desde la lmina de zinc hacia la de cobre. En la superficie de la lamina de zinc (se produce la oxidacin como nodo) y en la lamina de cobre se realiza la reduccin (ctodo).
DESARROLLO SUSTENTABLE
CICLO DE VIDA DE LAS PILAS Y SU IMPACTO AMBIENTAL
Notaciones convencionales de la celda. Para describir una celda se utiliza la siguiente notacin: En primer lugar se escribe el material del electrodo negativo utilizando su smbolo qumico, luego se coloca una lnea vertical para separar el electrodo de la solucin de iones de concentracin determinado. Inmediatamente se usa el smbolo II para sealar el puente salino, a continuacin se coloca la segunda solucin inica de concentracin conocida el signo II y por ltimo el signo del metal: 2+ 2+ Zn (.) l Zn (1mol/L) ll Cu (1mol/L) l Cu (.) La electroqumica, rama de la qumica que estudia las interrelaciones entre los procesos qumicos y los procesos elctricos. El flujo de electrones desde un punto a otro se llama corriente elctrica. Cuando la concentracin de electrones se iguala en ambos puntos, cesa la corriente elctrica. El material por el cual fluyen los electrones se denomina conductor. Los conductores pueden ser de dos tipos: conductores electrnicos o metlicos, y los conductores electrolticos. La conduccin tiene lugar por la migracin directa de los electrones a travs del conductor bajo la influencia de un potencial aplicado.
DESARROLLO SUSTENTABLE
CICLO DE VIDA DE LAS PILAS Y SU IMPACTO AMBIENTAL
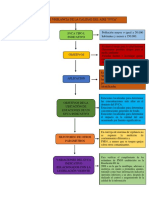
Ciclo de Vida Pilas-Bateras
Las pilas no tiene un buen ciclo de vida, puesto que la mayor cantidad de materia prima usada en su produccin es virgen y los materiales reciclados (metales) que se usan deben ser compensados para adquirir sus propiedades, lo cual requiere de qumicos peligros y nocivos para el medio y la salud, adems, por lo menos 30 por ciento de cada pila est constituida por compuestos txicos, tales como mercurio, plomo, litio, cadmio y nquel.
materia prima: metales y sustancias quimicas
transporte
destino de venta
se tira el hogar, la calle, los rios, suelo abierto,
desechado, eliminacion o reciclado
uso en el hogar, fabrica, etc.
causan deterioro al medio ambiente
algunas son recolectadas
se lleva a cabo un reciclado
tratamiento especial
residuos peligrosos
recuperacion de metales
se tiene un control sobre este poducto
DESARROLLO SUSTENTABLE
CICLO DE VIDA DE LAS PILAS Y SU IMPACTO AMBIENTAL
A pesar de esto, las pilas no reciben el manejo especial que amerita un residuo peligroso sino que van a parar a los tiraderos municipales, donde las carcazas sufren de corrosin debido a la accin climtica y procesos de fermentacin de la basura, con lo que sus compuestos txicos se escurren (lixivian) contaminando suelos y cuerpos de agua. Adems, la mayor parte de las veces, las pilas y bateras terminan siendo quemadas en estos basureros, lo que aumenta la contaminacin por la generacin de sustancias muy peligrosas y cancergenas, como son las dioxinas y los furanos.
DESARROLLO SUSTENTABLE
CICLO DE VIDA DE LAS PILAS Y SU IMPACTO AMBIENTAL
Como se puede observar la produccin de pilas, que conlleva a su uso requiere materia primas vrgenes para su elaboracin, lo cual implica el desperdicio de energa elctrica, sustancias qumicas nocivas y metales que podran tener un mejor uso.
Datos importantes de la pila en Mxico
Por lo menos 30 por ciento de cada pila est constituida por compuestos txicos, tales como mercurio, plomo, litio, cadmio y nquel y se estima que cada mexicano utiliza un promedio de 10 pilas al ao, muchas de ellas piratas.
Fabricar una pila consume 50 veces ms energa de la que sta produce y se calcula que la corriente generada por cada pila es 450 veces ms cara que la generada por la red elctrica. Alrededor del 30% de los materiales contenidos en pilas y bateras son txicos; si se trata de pilas de xido de mercurio su contenido txico es de 50%. Clculos conservadores sealan que usamos alrededor de 10 pilas desechables por ao en Mxico (400 gramos-120 gramos de txicos). Las pilas de carbn-zinc (heavy dutty) duran poco y son de baja toxicidad; las alcalinas (dixido de manganeso y zinc) duran ms y son de toxicidad media. Estas dos clases de pilas son las ms comunes, se utilizan en juguetes, radios, cmaras, etc. Las pilas de botn de mercurio y son altamente txicas, se utilizan en calculadoras,
DESARROLLO SUSTENTABLE CICLO DE VIDA DE LAS PILAS Y SU IMPACTO AMBIENTAL
relojes, aparatos de sordera; las de litio son altamente txicas, utilizadas en equipos de comunicacin, computadoras, celulares, entre Otros. Otras pilas de botn son de zinc-aire y xido de plata. Existen tambin bateras de nquel-cadmio, nquel-metal hidruro, etc. Clculos conservadores sealan que cada ao se tiran, 35, 500,000 kilos de de pilas y bateras. Tienes idea de cuanta agua contamina cada pila? Se calcula que: Una pila de mercurio puede contaminar 600 mil litros de agua; Una de zinc-aire, 12 mil litros; Una de xido de plata, 14 mil litros; Una alcalina, 167 mil litros de agua, Una de carbn-zinc 3 mil litros. Sabes cunto te cuesta utilizar esta energa enlatada, desechable y contaminante? Si usas un walkman 5 horas a la semana durante 1 ao se utilizarn: 38 pilas alcalinas (380 pesos), 116 bateras heavy dutty carbn-zinc (754 pesos) y, menos de una recargable (38 pesos la pila ms costo proporcional del cargador que es de 30 pesos. Qu puedes hacer? Cambia ambientalmente responsable: tus hbitos, consume de manera
A. Exige depsitos adecuados para que pongas tus pilas y bateras cuando ya no las uses. B. Exige a la Secretara de Economa no permitir la importacin ilegal de pilas y bateras. C. No permitas la incineracin de pilas y bateras. Las campaas de recoleccin de pilas en comercios u otros sitios no siempre solucionan el problema, averigua cul ser el destino de las pilas recolectadas. D. Prefiere las pilas recargables, pues pueden sustituir 300 desechables. E. Evita el uso de pilas siempre que sea posible. F. Usa y promueve productos que funcionen con cuerda, energa solar y energa elctrica. G. Prefiere los productos que se pueden conectar a la red elctrica, adems de no contaminar, es ms eficiente desde el punto de vista energtico. H. La mitad de las pilas utilizadas son para esparcimiento, disminuye dicho consumo. I. No compres pilas piratas: es ilegal, duran menos y son ms txicas.
DESARROLLO SUSTENTABLE
CICLO DE VIDA DE LAS PILAS Y SU IMPACTO AMBIENTAL
J. No tires las pilas en la basura, en el campo, en la calle. Evita que lleguen a cuerpos de agua y jams las quemes, pues los metales txicos desprendidos irn a la atmsfera. K. No entierres las pilas, ya que contaminan la tierra, el subsuelo y el agua una vez que se oxide su cubierta de metal. L. Llama a los nmeros 1-800 indicados en los empaques de las pilas y pregunta por las acciones de recoleccin del fabricante. Si declara no tenerlas, dile que la fbrica es responsable de su producto en todo su ciclo de vida y exige que retiren los txicos de las pilas y bateras.
Efectos en la salud El mercurio es un posible cancergeno y es bioacumulable. Una alta exposicin puede daar el cerebro, los riones y al feto, provocando retraso mental, en el andar o el habla, falta de coordinacin, ceguera y convulsiones. El mercurio que se emite en los basureros contamina el agua y la tierra, con lo que puede llegar a la comida pues se acumula en los tejidos de peces. El plomo puede daar el sistema nervioso, los riones y el sistema reproductivo y no se degrada. Cuando se libera al aire puede ser transportado largas distancias antes de sedimentar. Se adhiere a partculas en el suelo y puede pasar a aguas subterrneas. El litio es un neurotxico y txico para el rin. La intoxicacin por litio produce fallas respiratorias, depresin del miocardio, edema pulmonar y estupor profundo. Daa al sistema nervioso, llegando a estado de coma e incluso la muerte. El litio puede lixiviarse fcilmente a los mantos acuferos. El cadmio es una sustancia cancergena que si se respira a altos niveles produce graves lesiones en los pulmones e ingerirlo produce daos a los riones. En dosis altas puede producir la muerte. Ingerir alimentos o tomar agua con cadmio irrita el estmago e induce vmitos y diarrea. El cadmio entra al aire y al agua de fuentes como vertederos y derrames de desechos domsticos y se puede viajar largas distancias. El nquel tiene efectos sobre la piel. Respirar altas cantidades produce bronquitis crnica y cncer del pulmn y de los senos nasales. Se libera a la atmsfera por incineradores de basura. En el aire, se adhiere a partculas de polvo que se depositan en el suelo.
DESARROLLO SUSTENTABLE
CICLO DE VIDA DE LAS PILAS Y SU IMPACTO AMBIENTAL
Você também pode gostar
- Criterio Procedimiento de Medición NOM-013-ENER-2013Documento2 páginasCriterio Procedimiento de Medición NOM-013-ENER-2013Jorge Alberto Delgadillo CarpinteyroAinda não há avaliações
- Plan de Manejo CERRO LA JUDIADocumento2 páginasPlan de Manejo CERRO LA JUDIAJuvia LoxarAinda não há avaliações
- Pep Ingenieria Ambiental y Sanitaria Aguachica PDFDocumento109 páginasPep Ingenieria Ambiental y Sanitaria Aguachica PDFJaner Orozco RodriguezAinda não há avaliações
- Rack 3 GasesDocumento10 páginasRack 3 GasesJuan CuelloAinda não há avaliações
- Biorremediación en EcuadorDocumento2 páginasBiorremediación en EcuadorVictor Van Ronzelen100% (1)
- Fase 4 Modelacion Ambiental en AccionDocumento12 páginasFase 4 Modelacion Ambiental en AccionLuz Suarez100% (1)
- Capacidad de Carga Turistica Parque Nacional Natural AmacayacuDocumento8 páginasCapacidad de Carga Turistica Parque Nacional Natural AmacayacuIvanna DavidAinda não há avaliações
- Svca Tipo IDocumento3 páginasSvca Tipo IcesarAinda não há avaliações
- Ficha Ramsar BluefieldsDocumento31 páginasFicha Ramsar BluefieldsJurgen GuillenAinda não há avaliações
- El Método de Los Costos Evitados o InducidosDocumento3 páginasEl Método de Los Costos Evitados o InducidosCindy Carolina Contreras Castro100% (1)
- Ensayo de RAEEDocumento3 páginasEnsayo de RAEECarlos Ernesto Calderon0% (1)
- Crema Antipañalitis TerminadoDocumento70 páginasCrema Antipañalitis Terminadojesusernesto ramirez castañedaAinda não há avaliações
- El Páramo de Paja Blanca 1Documento4 páginasEl Páramo de Paja Blanca 1EdissonAinda não há avaliações
- Benceno EnsayoDocumento4 páginasBenceno EnsayoChristopher EstevezAinda não há avaliações
- Topografia y La Ing. AmbientalDocumento2 páginasTopografia y La Ing. AmbientalJUDITH HUAMAN TAPIA100% (1)
- Tarea 2 - Fundamentación - Desarrollo Legal NormativoDocumento8 páginasTarea 2 - Fundamentación - Desarrollo Legal NormativoyolandaAinda não há avaliações
- Matriz Med Panela PDFDocumento2 páginasMatriz Med Panela PDFjuan jose herrera ortizAinda não há avaliações
- Anteproyecto PasantiaDocumento40 páginasAnteproyecto PasantiaJUAN BERNARDOAinda não há avaliações
- Doc Acuerdo Inter 001 El Acuerdo Interministerial N. 001 entre el Ministerio del Ambiente y de Recursos Naturales No Renovables, compensación por afectaciones socioambientales y los problemas de implementaciónDocumento22 páginasDoc Acuerdo Inter 001 El Acuerdo Interministerial N. 001 entre el Ministerio del Ambiente y de Recursos Naturales No Renovables, compensación por afectaciones socioambientales y los problemas de implementaciónBolívar Amón0% (2)
- Taller de Hallazgos 18 Enero 2021 - SSODocumento1 páginaTaller de Hallazgos 18 Enero 2021 - SSOCristhian Gabriel MaciasAinda não há avaliações
- La Investigacion en El Centro Forestal Tropical Del Bajo CalimaDocumento33 páginasLa Investigacion en El Centro Forestal Tropical Del Bajo CalimaDanielaAinda não há avaliações
- Suelos EstérileDocumento2 páginasSuelos Estérilealbertoros100% (3)
- Olores OfensivosDocumento26 páginasOlores OfensivosOscar Diaz GarciaAinda não há avaliações
- Abasteccimeinto de Agua Fase 4Documento17 páginasAbasteccimeinto de Agua Fase 4Alejandra Rojas100% (1)
- Emisión de Gases Contaminación en La Ciudad de Cuenca EcuadorDocumento12 páginasEmisión de Gases Contaminación en La Ciudad de Cuenca EcuadorBryanStivenMaRevillaAinda não há avaliações
- Plantilla de Respuestas - Paso 2Documento18 páginasPlantilla de Respuestas - Paso 2GILDARDO GUISAOAinda não há avaliações
- Trabajo AspiDocumento2 páginasTrabajo AspiJosé ArrietaAinda não há avaliações
- Canaleta ParshallDocumento9 páginasCanaleta ParshallIsabel MerchanAinda não há avaliações
- Manual Tecnico Iraps MultisectorDocumento280 páginasManual Tecnico Iraps MultisectorRosalva Angulo ReyesAinda não há avaliações
- Conceptos PuearDocumento3 páginasConceptos PuearHulyAinda não há avaliações
- Fase 2 - Revisar El Aprovechamiento y Valorización de Residuos Sólidos ConvencionalesDocumento8 páginasFase 2 - Revisar El Aprovechamiento y Valorización de Residuos Sólidos Convencionaleshenry fernandezAinda não há avaliações
- Gastos Actuales y PotencialesDocumento17 páginasGastos Actuales y PotencialesSofia Sánchez CárdenasAinda não há avaliações
- Praes Humedal Maria CamilaDocumento19 páginasPraes Humedal Maria CamilaCristian JimenezAinda não há avaliações
- Informe de Generación Per Capita de Residuos en El Hogar y Su ComposiciónDocumento8 páginasInforme de Generación Per Capita de Residuos en El Hogar y Su ComposiciónAnahi Sosaya GuzmanAinda não há avaliações
- Segundo Parcial Profundizacion 2021Documento4 páginasSegundo Parcial Profundizacion 2021Sebastian SalcedoAinda não há avaliações
- Anexo 1 - Fase 3 Agua - 2021 - 2Documento2 páginasAnexo 1 - Fase 3 Agua - 2021 - 2sandra virviescasAinda não há avaliações
- Casos de Estudio en AguasDocumento4 páginasCasos de Estudio en AguasGenesis QuezadaAinda não há avaliações
- Análisis de Matriz Leopold Del EIA-sdDocumento2 páginasAnálisis de Matriz Leopold Del EIA-sdAaronAinda não há avaliações
- BaygonDocumento7 páginasBaygonSebastián Guevara Warthon100% (1)
- EL PROBLEMA DE LAS AGUAS CONTAMINADAS - Por Cristian FrersDocumento5 páginasEL PROBLEMA DE LAS AGUAS CONTAMINADAS - Por Cristian FrersADN CreadoreS100% (1)
- Entrevista Al GerenteDocumento2 páginasEntrevista Al Gerente1191mlAinda não há avaliações
- Guía de Actividades y Rubrica de Evaluación - Unidad 1 - Paso 2 - Origen de La Diversidad GenéticaDocumento12 páginasGuía de Actividades y Rubrica de Evaluación - Unidad 1 - Paso 2 - Origen de La Diversidad GenéticaLORENA ALVAREZ MONROYAinda não há avaliações
- PMA Parque Ecologico Humedal CoroncoroDocumento52 páginasPMA Parque Ecologico Humedal CoroncoroAlejandra Sierra FandiñoAinda não há avaliações
- Tarea 4 Elaborar Una Propuesta de Valoración Económica Ambiental AplicadaDocumento4 páginasTarea 4 Elaborar Una Propuesta de Valoración Económica Ambiental AplicadaConambiente S.A.SAinda não há avaliações
- Diagrama de RedesDocumento1 páginaDiagrama de RedesChennen Chavez DAinda não há avaliações
- Recipe - CML Baseline 20000Documento5 páginasRecipe - CML Baseline 20000rosmary charris100% (1)
- Construccion de Indicadores Ambientales Fase 2Documento10 páginasConstruccion de Indicadores Ambientales Fase 2Javier Mauricio Valencia ChacueAinda não há avaliações
- CONPES 3530 de 2008Documento45 páginasCONPES 3530 de 2008Cata Fracica100% (2)
- Procedimiento para Toma de muestrasCDMB PDFDocumento19 páginasProcedimiento para Toma de muestrasCDMB PDFYamil CastilloAinda não há avaliações
- Fase 2 Trabajo Colaborativo - Definición de Indicadores AmbientalesDocumento8 páginasFase 2 Trabajo Colaborativo - Definición de Indicadores Ambientaleseliza100% (1)
- Caracterizacion de Contaminantes Atmosfericos Evaluaciones UnadDocumento65 páginasCaracterizacion de Contaminantes Atmosfericos Evaluaciones Unadmuber800% (2)
- Compuestos Organoclorados en El PapelDocumento3 páginasCompuestos Organoclorados en El PapelA Zuu ArAinda não há avaliações
- Horizontes DiagnosticoDocumento33 páginasHorizontes DiagnosticoNancy Carolaim VelandiaAinda não há avaliações
- Decreto 475 de 1998 PDFDocumento23 páginasDecreto 475 de 1998 PDFFrank Solarte MosqueraAinda não há avaliações
- Tarea 5 - BIORREMEDIACIÓNDocumento8 páginasTarea 5 - BIORREMEDIACIÓNMilena LealAinda não há avaliações
- Oleoducto Porvenir. Monterrey - CasanareDocumento27 páginasOleoducto Porvenir. Monterrey - CasanareGean Carlo Ospina FrancoAinda não há avaliações
- Analisis Quimico para IMPRIMIRIIDocumento40 páginasAnalisis Quimico para IMPRIMIRIIgaby181107Ainda não há avaliações
- ElectroquímicaDocumento9 páginasElectroquímicacarlosAinda não há avaliações
- Practica 3Documento10 páginasPractica 3Vane ParamoAinda não há avaliações
- Actividad3 - Calculo DiferencialeintegralDocumento8 páginasActividad3 - Calculo DiferencialeintegralAlonso Gomez Luis AlbertoAinda não há avaliações
- Manual Draga Aumund Oem48374 (1) KZB-Q 1Documento638 páginasManual Draga Aumund Oem48374 (1) KZB-Q 1jkanclaAinda não há avaliações
- Taller 1 Presion Grupo 1 SJ NaukaryDocumento3 páginasTaller 1 Presion Grupo 1 SJ Naukaryjoluvasi58819Ainda não há avaliações
- Facultad de Ciencias Humanas Programa Curricular de Psicología Fundamentos Del ConductismoDocumento4 páginasFacultad de Ciencias Humanas Programa Curricular de Psicología Fundamentos Del ConductismoVivian Samantha Palacios PachonAinda não há avaliações
- Percepcion VisualDocumento4 páginasPercepcion VisualLu' CastrillonAinda não há avaliações
- Tarea 1 - John SamaniegoDocumento4 páginasTarea 1 - John Samaniegojohn reyesAinda não há avaliações
- Plan Global LenguajeDocumento6 páginasPlan Global Lenguajejuariey1Ainda não há avaliações
- Embarazo PrecozDocumento2 páginasEmbarazo PrecozRuggery LeonAinda não há avaliações
- Reporte de Conductividad de AbrasivosDocumento1 páginaReporte de Conductividad de Abrasivosjuniuni18Ainda não há avaliações
- Existencialismo LatinoamericanoDocumento4 páginasExistencialismo LatinoamericanoFrancisco Fernando FrigeriAinda não há avaliações
- Características de Los Equipos de Trabajo PDFDocumento4 páginasCaracterísticas de Los Equipos de Trabajo PDFVale RivasAinda não há avaliações
- Material de Pseudo A JavaDocumento19 páginasMaterial de Pseudo A JavaZuLeika ALezones CamposAinda não há avaliações
- CRM (CR-01 y 02)Documento37 páginasCRM (CR-01 y 02)Fred LimaAinda não há avaliações
- 30 Versachem Mega GreyDocumento8 páginas30 Versachem Mega GreyConnie Elanie KimAinda não há avaliações
- Clase 4 - ESCUELA 2 - Bárbara BacioccoDocumento3 páginasClase 4 - ESCUELA 2 - Bárbara BacioccoBarbi BacioccoAinda não há avaliações
- Proyecto de Inversion para Comercializacion de Jugo de CañaDocumento10 páginasProyecto de Inversion para Comercializacion de Jugo de CañaJulio Cesar Urquidi BarbozaAinda não há avaliações
- Practica 4Documento2 páginasPractica 4Cielo Karina (Sky)Ainda não há avaliações
- Agregados CristalinosDocumento2 páginasAgregados CristalinosEstip Esnaider Cahuana Maron100% (1)
- El NitrógenoDocumento2 páginasEl NitrógenoRonald Nilson CAAinda não há avaliações
- Estudio Habitos y Valores Ores Tiendas de Barrio CaliDocumento20 páginasEstudio Habitos y Valores Ores Tiendas de Barrio CaliJulián Garcés DíazAinda não há avaliações
- T5 CTVDocumento9 páginasT5 CTVJefferson ChipantizaAinda não há avaliações
- BNFDocumento2 páginasBNFChristian Emanuel Gallardo DelgadilloAinda não há avaliações
- Flexibilidad Verbal y RendimientoDocumento5 páginasFlexibilidad Verbal y RendimientopmartinrAinda não há avaliações
- Discurso Pilar ZamoraDocumento7 páginasDiscurso Pilar ZamoraCrisol De Ciudad RealAinda não há avaliações
- Contabildad de Costo Unid 1Documento12 páginasContabildad de Costo Unid 1Edwin MedranoAinda não há avaliações
- Filipenses Tarea 1Documento8 páginasFilipenses Tarea 1Eddy MPAinda não há avaliações
- Dioses MayasDocumento6 páginasDioses MayasCyber TeenAinda não há avaliações
- Monica K.. KidadultDocumento29 páginasMonica K.. KidadultCatalina ZapataAinda não há avaliações
- Tarea 3-Gestion de OperacionesDocumento35 páginasTarea 3-Gestion de OperacionespaolaAinda não há avaliações
- Epistemologia EnsayoDocumento3 páginasEpistemologia EnsayoÁngela PoloAinda não há avaliações