Escolar Documentos
Profissional Documentos
Cultura Documentos
TM Franco Gonzales Del Valle Zúñiga
Enviado por
marcos antonio0 notas0% acharam este documento útil (0 voto)
44 visualizações12 páginasColoracion paz. Es un método para detectar polisacáridos en los tejidos. Tanto glucógeno como muco polisacáridos
Título original
567
Direitos autorais
© © All Rights Reserved
Formatos disponíveis
PPTX, PDF, TXT ou leia online no Scribd
Compartilhar este documento
Compartilhar ou incorporar documento
Você considera este documento útil?
Este conteúdo é inapropriado?
Denunciar este documentoColoracion paz. Es un método para detectar polisacáridos en los tejidos. Tanto glucógeno como muco polisacáridos
Direitos autorais:
© All Rights Reserved
Formatos disponíveis
Baixe no formato PPTX, PDF, TXT ou leia online no Scribd
0 notas0% acharam este documento útil (0 voto)
44 visualizações12 páginasTM Franco Gonzales Del Valle Zúñiga
Enviado por
marcos antonioColoracion paz. Es un método para detectar polisacáridos en los tejidos. Tanto glucógeno como muco polisacáridos
Direitos autorais:
© All Rights Reserved
Formatos disponíveis
Baixe no formato PPTX, PDF, TXT ou leia online no Scribd
Você está na página 1de 12
TM FRANCO GONZALES DEL VALLE ZÚÑIGA
COLORACIÓN PAS Y HEMATOXILINA
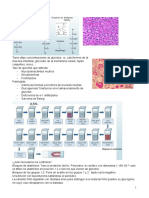
Este método de tinción se emplea para detectar polisacáridos en los tejidos, tanto
glucógeno como mucopolisacáridos. También es una buena tinción para membranas
basales y cartílago. Cualquier fijador es apropiado para esta técnica.
El mecanismo de coloración de la tinción de PAS no es sólo por afinidad eléctrica, como los
colorantes habituales, sino que es una tinción histoquímica, es decir, se realiza una
modificación química del tejido previa a la coloración. Es el ácido peryódico quien lleva a
cabo esta reacción.
PROCEDIMIENTO
Partimos de muestras que han sido fijadas e incluidas en parafina. Estas muestras se han cortado en
secciones de unas 8 µm y adheridas a portaobjetos recubiertos con gelatina.
1.- 2x10 min en xileno para desparafinar
2.- 2x10 min en etanol 100º
3.- 10 min en etanol 96º
4.- 10 min en etanol 80º
5.- 10 min en etanol 50º
6.- 5 min en H2O destilada
7.- Ácido peryódico al 0.5 % durante 5 min. Se oxidan las uniones carbono-carbono de los azúcares para
formar grupos aldehídos.
8.- varios lavados en H2O destilada
9.- Reactivo de Schiff durante 30 min en oscuridad (el tiempo depende de la temperatura). Los grupos
aldehídos reaccionan con el reactivo de Schiff (ácido sulfuroso con fucsina) resultando en un color rojo
fucsia. Las secciones quedan de un color rosado intenso.
Se puede dar un paso con una solución de metabisulfito potásico (o sódico) durante 2 minutos para eliminar los residuos
de reactivo de Schiff de la muestra.
10.- 5 min en agua corriente
11.- Varios lavados en H2O destilada
12.- 5 min en hematoxilina de Mayer
13.- 15 min en agua corriente
14.- 20 seg en H2O destilada
15.- 5 min en etanol 80º
16.- 5 min en etanol 96º
17.- 2x10 min en etanol 100º
18.- 2x10 min en xileno
19.- Montado con medio de montaje
RESULTADOS
Glúcidos: rosa intenso a fucsia
Núcleos: azul oscuro (en realidad se tiñe sólo la cromatina)
CONSEJOS
• El tiempo en reactivo de Schiff depende de la temperatura. Incluso se puede teñir
en microondas durante menos de un minuto.
• El reactivo de Schiff puede reutilizarse pero ha de conservarse en nevera y
llevarlo a la temperatura deseada antes de su uso.
• El reactivo de Schiff debe conservar un color amarillento y hay que descartarlo si
se vuelve de color rosado. Si aparece precipitado blanco en el fondo del bote de
reactivo se puede disolver de nuevo.
COLORACIÓN PAS Y AZUL ALCIÁN
Este método de tinción se emplea para detectar polisacáridos en tejidos, tanto glucógeno como
mucopolisacáridos. También es una buena tinción para membranas basales y cartílago. Cualquier
fijador es apropiado para esta técnica.
La combinación del PAS con el azul alcián nos permite distinguir a los mucopolisacáridos ácidos,
teñidos con el azul alcián, del resto de mucopolisacáridos. Todos los mucopolisacáridos se tiñen con
el PAS.
PROCEDIMIENTO
Partimos de muestras que han sido fijadas e incluidas en parafina. Estas muestras se han cortado en secciones de unas 8 µm y adheridas a
portaobjetos recubiertos con gelatina.
1.- Xileno para desparafinar, 2x10 min.
2.- Etanol 100º, 2x10 min.
3.- Etanol 96º, 10 min.
4.- Etanol 80º, 10 min.
5.- Etanol 50º, 10 min.
6.- H2O destilada, 5 min.
7.- Azul alcián al 1 %, 30 min.
Azul alcián:
1 g de azul alcián (C.I. 74240)
3 ml de ácido acético
97 ml de agua destilada
8.- H2O corriente, 3 min.
9.- Ácido peryódico al 0.5 % en H2O destilada, 10 min.
10.- H2O destilada, 3x1m.
11.- Reactivo de Schiff durante 30 min en oscuridad (el tiempo depende de la temperatura y del propio
reactivo; puede ser incluso 10 min). Los grupos aldehídos reaccionan con el reactivo de Schiff (ácido
sulfuroso con fucsina) resultando en un color rojo fucsia. Las secciones quedan de un color rosado.
Se puede dar un paso con una solución de metabisulfito potásico (o sódico) al 0.5 % durante 2 minutos
para eliminar los residuos de reactivo de Schiff de la muestra.
12.- H2O corriente, 5 min.
13.- H2O destilada, varios lavados.
14.- Hematoxilina de Mayer, 5 min (es opcional).
15.- H2O corriente, 5 min (es opcional).
16.- H2O destilada, 20s (es opcional).
17.- Etanol 80º, 5 min.
18.- Etanol 96º, 5 min.
19.- Etanol 100º, 2x10 min.
20.- Xileno, 2x10 min.
21.- Montado con medio de montaje
RESULTADOS
Glúcidos: rosa intenso a fucsia
Mucopolisacáridos ácidos: azul
CONSEJOS
• El tiempo en reactivo de Schiff depende de la temperatura y de las condiciones
en las que se encuentre el propio reactivo. Incluso se puede teñir en microondas
durante menos de un minuto.
• El reactivo de Schiff puede reutilizarse pero ha de conservarse en nevera y
llevarlo a la temperatura deseada antes de su uso.
• El reactivo de Schiff debe conservar un color amarillento y hay que descartarlo si
se vuelve de color rosado. Si aparece precipitado blanco en el fondo del bote de
reactivo se puede disolver de nuevo.
Você também pode gostar
- TINCIONESDocumento9 páginasTINCIONESDaya BolañosAinda não há avaliações
- PDF Tincion Tricromica de Masson - CompressDocumento3 páginasPDF Tincion Tricromica de Masson - CompressGemma LizethAinda não há avaliações
- Tinción PASDocumento4 páginasTinción PASJhoao Mejia Parra75% (4)
- Expo de CitologiaDocumento24 páginasExpo de Citologiajhon_4548Ainda não há avaliações
- Grupo 5 - Analisis de CarbohidratosDocumento25 páginasGrupo 5 - Analisis de CarbohidratosCristian ACAinda não há avaliações
- Tecnicas para La Demostración de La MielinaDocumento8 páginasTecnicas para La Demostración de La MielinaPaulina MaliqueoAinda não há avaliações
- Azul de PrusiaDocumento5 páginasAzul de PrusiaDaya BolañosAinda não há avaliações
- TINCIONESDocumento4 páginasTINCIONESAndrea Flores RiosAinda não há avaliações
- Coloración PasDocumento21 páginasColoración PasVicttoryaAinda não há avaliações
- TINCIONDocumento14 páginasTINCIONvillarroelgeorgeAinda não há avaliações
- Analisis de Polisacaridos y AlmidonesDocumento7 páginasAnalisis de Polisacaridos y Almidonestefa13137495Ainda não há avaliações
- Unidad 5 PDFDocumento12 páginasUnidad 5 PDFJudith Capel OrtegaAinda não há avaliações
- Flujograma Tinciones EspecialesDocumento1 páginaFlujograma Tinciones EspecialesMichelleSánchez100% (1)
- PeroxidasaDocumento6 páginasPeroxidasadanko_3000Ainda não há avaliações
- Técnicas HistoquímicasDocumento26 páginasTécnicas HistoquímicasLaura Salgado ManriqueAinda não há avaliações
- ENZIMOLOGIA Protocolo de Extracción de La Enzima Ą AmilazaDocumento8 páginasENZIMOLOGIA Protocolo de Extracción de La Enzima Ą AmilazaCreteys ValeraAinda não há avaliações
- Microtecnicas BotanicasDocumento7 páginasMicrotecnicas BotanicasJaquiAinda não há avaliações
- 6º InformeDocumento6 páginas6º InformeDayana GamboaAinda não há avaliações
- TincionesDocumento17 páginasTincionesLetty EAinda não há avaliações
- Coloraciones MicrobiologiaDocumento30 páginasColoraciones MicrobiologiaGabrielAlencarAinda não há avaliações
- Método para Fijar y Cortar Muestras de Médula Espinal de RoedorDocumento8 páginasMétodo para Fijar y Cortar Muestras de Médula Espinal de RoedorcaradeperrierAinda não há avaliações
- Portada Practicas HistologiaDocumento5 páginasPortada Practicas Histologiaanon_711769378Ainda não há avaliações
- Guía PanelasDocumento8 páginasGuía PanelasValentina VanegasAinda não há avaliações
- Determinación de PeroxidasasDocumento6 páginasDeterminación de PeroxidasasGabriela Vargas GonzálezAinda não há avaliações
- Tincion de AmebasDocumento3 páginasTincion de AmebasJonathan Medina MarroquinAinda não há avaliações
- Tinción Con Hematoxilina y EosinaDocumento2 páginasTinción Con Hematoxilina y EosinaFabiana PérezAinda não há avaliações
- Manual de Laboratorio de Nutricion AnimalDocumento22 páginasManual de Laboratorio de Nutricion AnimalMARCOS ALEJANDRO CHAMORRO TRUJILLOAinda não há avaliações
- Protocolo 1 Obtencion de Adn de Bacterias Patogenas PDFDocumento6 páginasProtocolo 1 Obtencion de Adn de Bacterias Patogenas PDFGonzalo Bravo JimenezAinda não há avaliações
- Hidrólisis Del Almidon Del MaizDocumento4 páginasHidrólisis Del Almidon Del MaizJimmy SimpsonAinda não há avaliações
- K-Lmal-116a - Data EspDocumento16 páginasK-Lmal-116a - Data EspNepropac acuamarketAinda não há avaliações
- Patas de PolloDocumento31 páginasPatas de PolloAnonymous AcvCtVAinda não há avaliações
- Act 5Documento7 páginasAct 5ibqa20.agonzalezcAinda não há avaliações
- T 4 y 5 PCYT Imprimir 2Documento9 páginasT 4 y 5 PCYT Imprimir 2anonimo282093Ainda não há avaliações
- Tinciones Especiales para HistologiaDocumento8 páginasTinciones Especiales para HistologiaFernanda Razo100% (1)
- Coloraciones CarbohidratosDocumento6 páginasColoraciones CarbohidratosYeixandra PerezAinda não há avaliações
- Process y TecnicaDocumento6 páginasProcess y TecnicaYadira JayaAinda não há avaliações
- Tinción PAPANICOLAOUDocumento2 páginasTinción PAPANICOLAOUFanny CastellanosAinda não há avaliações
- 3 Tincion de PapanicolaouDocumento8 páginas3 Tincion de Papanicolaouunocero411Ainda não há avaliações
- Tinciones EspecialesDocumento13 páginasTinciones EspecialesVivis Allauca CarrilloAinda não há avaliações
- Tecnica de GomorriDocumento7 páginasTecnica de GomorriSonaly Coyla BarredaAinda não há avaliações
- Tinción Tricrómico de Van GiesonDocumento13 páginasTinción Tricrómico de Van GiesonSonaly Coyla BarredaAinda não há avaliações
- Exposicion-Caracteristicas Tintoriales de Los HongosDocumento45 páginasExposicion-Caracteristicas Tintoriales de Los HongosJonathan Urbina100% (1)
- Protocolo de Extracción de Adn de Plantas Basado en CtabDocumento4 páginasProtocolo de Extracción de Adn de Plantas Basado en CtabCesar Tolentino MasgoAinda não há avaliações
- Extracción de Adn Vegetal - Protocolo Con CtabDocumento2 páginasExtracción de Adn Vegetal - Protocolo Con Ctabvalenciabasto100% (1)
- Laminillas ProtozoariosDocumento7 páginasLaminillas ProtozoariospaulinahhaAinda não há avaliações
- Practica 13parasitologiaDocumento5 páginasPractica 13parasitologiaDavid Espinosa CamachoAinda não há avaliações
- Protocolo FOSFATASA ÁCIDA LEUCOCITARIAokDocumento3 páginasProtocolo FOSFATASA ÁCIDA LEUCOCITARIAokAdrian Dominguez SantanaAinda não há avaliações
- Tinción de PapanicolaouDocumento22 páginasTinción de PapanicolaouDarla Milagros Choque EstradaAinda não há avaliações
- Extracción, Detección y Cuantificación de Compuestos FenólicosDocumento6 páginasExtracción, Detección y Cuantificación de Compuestos FenólicosTeo SuazoAinda não há avaliações
- Guía Cromatografia de Gases - Perfil de AGDocumento3 páginasGuía Cromatografia de Gases - Perfil de AGMilena EscamillaAinda não há avaliações
- PROMEFA - Guía de Procedimientos 2021 - v14 (2021 Feb 20)Documento78 páginasPROMEFA - Guía de Procedimientos 2021 - v14 (2021 Feb 20)Martin BoninfanteAinda não há avaliações
- Practica No. 3 y 4Documento4 páginasPractica No. 3 y 4Gaby BlancoAinda não há avaliações
- Guia de Laboratorio AzucaresDocumento39 páginasGuia de Laboratorio AzucaresAlejandro Saravia AlcócerAinda não há avaliações
- Almidón ExtracciónDocumento4 páginasAlmidón ExtracciónEvelyn Rengifo Escobar100% (3)
- COMETA Protocolo TerminadoDocumento5 páginasCOMETA Protocolo TerminadoOwen Alejandro Villatoro AguilarAinda não há avaliações
- Purificación de La G6PDHDocumento16 páginasPurificación de La G6PDHMercedes MartínezAinda não há avaliações
- Tincion PLATADocumento2 páginasTincion PLATASaul Dominguez VegaAinda não há avaliações
- Apendice ADocumento18 páginasApendice AChristian LopezAinda não há avaliações
- Tinciones MicrobiológicasDocumento29 páginasTinciones MicrobiológicasXimena PineloAinda não há avaliações
- Diagnostico de Saneamiento AmbientalesDocumento19 páginasDiagnostico de Saneamiento Ambientalesmarcos antonioAinda não há avaliações
- 567 PDFDocumento109 páginas567 PDFmarcos antonioAinda não há avaliações
- 08 Polimorfismo GeneticoDocumento32 páginas08 Polimorfismo Geneticomarcos antonioAinda não há avaliações
- 10 Sitios FragilesDocumento23 páginas10 Sitios Fragilesmarcos antonioAinda não há avaliações
- Introducción AgitacionDocumento24 páginasIntroducción AgitacionKathycitha HuizaAinda não há avaliações
- S05 - Estructura Atómica y Tabla PeriódicaDocumento11 páginasS05 - Estructura Atómica y Tabla PeriódicaFrank FarfanAinda não há avaliações
- Tipos de SeguidoresDocumento28 páginasTipos de SeguidoresMiguel Castro100% (1)
- Informe CobreDocumento6 páginasInforme CobreLizett Sofia Garcia MaldonadoAinda não há avaliações
- 1 Generadores ElectromecánicosDocumento16 páginas1 Generadores ElectromecánicosJorgeCampos100% (2)
- Merged PDFDocumento480 páginasMerged PDFCristhyan Edwin Mita CharaAinda não há avaliações
- Nanoparticulas Metalicas PDFDocumento156 páginasNanoparticulas Metalicas PDFpajoderAinda não há avaliações
- Informe de Carlos Gonzales Completamente ListoDocumento60 páginasInforme de Carlos Gonzales Completamente ListoAngelCegarra100% (1)
- Tesis Victoria Elena Meza Ochoa PDFDocumento113 páginasTesis Victoria Elena Meza Ochoa PDFTavo Suarez CAinda não há avaliações
- Incol Sas - PQR Smaw 001 Asme Ix-23-12-20Documento8 páginasIncol Sas - PQR Smaw 001 Asme Ix-23-12-20Maritza HernandezAinda não há avaliações
- TESISDocumento255 páginasTESISJose Andre Flores ChiaAinda não há avaliações
- Evolucion 2021Documento226 páginasEvolucion 2021Erick jose Salas ChacónAinda não há avaliações
- Materialismo Sistemico Emergentista.... 1Documento8 páginasMaterialismo Sistemico Emergentista.... 1Claudio CondoriAinda não há avaliações
- Semana 13Documento2 páginasSemana 13Philly Ross Sinarahua RengifoAinda não há avaliações
- Fase 4 - Señales y Sistemas - Final - Alexis PedrozaDocumento24 páginasFase 4 - Señales y Sistemas - Final - Alexis Pedrozaalexis pedrozaAinda não há avaliações
- Bali SticaDocumento18 páginasBali SticaInfanteria de MarinaAinda não há avaliações
- PDF Diseo de Cimentacion de Tanque Elevado 250m3 - CompressDocumento15 páginasPDF Diseo de Cimentacion de Tanque Elevado 250m3 - Compressxavier moraAinda não há avaliações
- Aspectos Técnicos Cartas ElectronicasDocumento13 páginasAspectos Técnicos Cartas ElectronicasErnestoDomAinda não há avaliações
- Limpia TodoDocumento5 páginasLimpia TodoPaul Christian Rojas FloresAinda não há avaliações
- Syllabus Acústica y Vibraciones 2008ultima VersionDocumento16 páginasSyllabus Acústica y Vibraciones 2008ultima VersionedutintaAinda não há avaliações
- 01 Tejas Asfalticas Manual Instalacion PDFDocumento46 páginas01 Tejas Asfalticas Manual Instalacion PDFJomasemaAinda não há avaliações
- Ensayo de MolineteDocumento9 páginasEnsayo de MolineteEnzo Delgado MuñozAinda não há avaliações
- INFORMEDocumento30 páginasINFORMEjhonAinda não há avaliações
- Trabajo de Ventilacion 2.0Documento13 páginasTrabajo de Ventilacion 2.0Duran UCAinda não há avaliações
- Informe S7 - Reacciones QuímicasDocumento25 páginasInforme S7 - Reacciones QuímicasMaricela Alcantara MuchaAinda não há avaliações
- CodigosDocumento5 páginasCodigosLeo GallardoAinda não há avaliações
- Electro CardioDocumento10 páginasElectro CardioRenzo Zuñiga CastilloAinda não há avaliações
- Tema 1 Quimica AnaliticaDocumento45 páginasTema 1 Quimica AnaliticaDavid Ballejos ArriolaAinda não há avaliações
- Sem 3 Matriz JacobianaDocumento6 páginasSem 3 Matriz JacobianaRenzo TuestasAinda não há avaliações
- Procesos de PerforacionDocumento26 páginasProcesos de PerforacionJ-Luis RodriguezAinda não há avaliações