Escolar Documentos
Profissional Documentos
Cultura Documentos
Quimica Geral I - Atividade Ii - Módulo Ii
Enviado por
Ana Karen Albuquerque0 notas0% acharam este documento útil (0 voto)
20 visualizações2 páginasO documento apresenta uma atividade sobre química geral com 10 questões sobre estruturas de ressonância, tipos de ligação química, geometria molecular e teoria da ligação de valência. Os tópicos incluem representações de íons, análise de polaridade em moléculas, demonstração teórica da inexistência de hélio diatômico e explicação da geometria do difluoreto de xenônio.
Descrição original:
Título original
QUIMICA GERAL I - ATIVIDADE II - MÓDULO II
Direitos autorais
© © All Rights Reserved
Formatos disponíveis
DOCX, PDF, TXT ou leia online no Scribd
Compartilhar este documento
Compartilhar ou incorporar documento
Você considera este documento útil?
Este conteúdo é inapropriado?
Denunciar este documentoO documento apresenta uma atividade sobre química geral com 10 questões sobre estruturas de ressonância, tipos de ligação química, geometria molecular e teoria da ligação de valência. Os tópicos incluem representações de íons, análise de polaridade em moléculas, demonstração teórica da inexistência de hélio diatômico e explicação da geometria do difluoreto de xenônio.
Direitos autorais:
© All Rights Reserved
Formatos disponíveis
Baixe no formato DOCX, PDF, TXT ou leia online no Scribd
0 notas0% acharam este documento útil (0 voto)
20 visualizações2 páginasQuimica Geral I - Atividade Ii - Módulo Ii
Enviado por
Ana Karen AlbuquerqueO documento apresenta uma atividade sobre química geral com 10 questões sobre estruturas de ressonância, tipos de ligação química, geometria molecular e teoria da ligação de valência. Os tópicos incluem representações de íons, análise de polaridade em moléculas, demonstração teórica da inexistência de hélio diatômico e explicação da geometria do difluoreto de xenônio.
Direitos autorais:
© All Rights Reserved
Formatos disponíveis
Baixe no formato DOCX, PDF, TXT ou leia online no Scribd
Você está na página 1de 2
UNIVERSIDADE ESTADUAL DO CEARÁ
CENTRO DE CIÊNCIAS E TECNOLOGIA
CURSO DE LICENCIATURA EM QUÍMICA
DISCIPLINA: QUÍMICA GERAL I
PROFESSOR________________
Nome__________________________________________________________________________________
ATIVIDADE II
1. Represente através de um número adequado de formas de ressonância o SO 42- e
diga qual é a ordem da ligação enxofre-oxigênio.
2. A acroleína, usada na fabricação de plásticos, pode ser obtida através da reação
entre etileno e monóxido de carbono, conforme a equação abaixo:
a) Indique qual é a ligação carbono-carbono mais forte na molécula de acroleína.
Justifique.
b) Indique qual é a ligação carbono-carbono mais longa na molécula de acroleína.
Justifique.
c) As moléculas de etileno e acroleína são apolares? Justifique.
3. O íon cianato, NCO-, possui o átomo menos eletronegativo, C, no centro. O fulminato,
CNO-, tem a mesma fórmula, mas o átomo de N está no centro.
a) Desenhe três possíveis estruturas de ressonância para o CNO - e calcule as cargas
formais.
b) Com base nas cargas formais, decida qual é a estrutura de ressonância com a
distribuição de cargas mais razoável. Justifique.
4. Defina orbital atómico e orbital molecular.
5. Defina os seguintes itens.
a) Ligação iônica
b) Ligação covalente
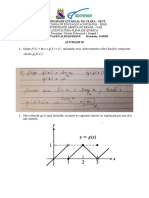
6. Com base no gráfico abaixo discorra sobre ligações químicas.
UECE PROF: LEONARDO SILVA QUÍMICA
7. Com base nos orbitais moleculares demonstre que não existe Hélio diatômico.
8. O xenônio é um dos gases nobres e geralmente é bastante não reativo. De fato,
acreditou-se por muito tempo que todos os gases nobres fossem totalmente
incapazes de formar compostos. Assim, foi com grande surpresa que se descobriu
que alguns compostos poderiam ser produzidos. Um deles é o difluoreto de xenônio.
O que você esperaria como geometria do difluoreto de xenônio — linear ou não
linear?
9. Utilize a teoria da ligação de valência para explicar a ligação na molécula de SF 4.
10. Você espera que a molécula de HCN seja polar ou apolar?
Você também pode gostar
- Lista de Exercícios 2º BimestreDocumento10 páginasLista de Exercícios 2º BimestreprofnonocmmAinda não há avaliações
- Fundamentos de Química: Física Quântica e EletromagnetismoNo EverandFundamentos de Química: Física Quântica e EletromagnetismoAinda não há avaliações
- Lista de Exercicio Com Gabarito de QuimicaDocumento7 páginasLista de Exercicio Com Gabarito de QuimicaJenifer AlvesAinda não há avaliações
- Potenciometria: aspectos teóricos e práticosNo EverandPotenciometria: aspectos teóricos e práticosAinda não há avaliações
- 05 2a Lista de Exercicios Calculo 1Documento2 páginas05 2a Lista de Exercicios Calculo 1Caio SilvaAinda não há avaliações
- TopG-ligcovalente 01 23Documento2 páginasTopG-ligcovalente 01 23Isabelle SantosAinda não há avaliações
- Lista Exercicios 3Documento1 páginaLista Exercicios 3Vanessa RochaAinda não há avaliações
- 10FQA Ficha Trab Ini Q2.1 - N.⺠2Documento4 páginas10FQA Ficha Trab Ini Q2.1 - N.⺠2Joaquina JúliaAinda não há avaliações
- Teste Q2.1 N.º 1 - V1 10-3Documento4 páginasTeste Q2.1 N.º 1 - V1 10-3BiaAinda não há avaliações
- Teste Q2.1 N.º 1 - V1 10-3 CorrDocumento5 páginasTeste Q2.1 N.º 1 - V1 10-3 CorrBia100% (2)
- SimuladoDocumento126 páginasSimuladosantos kAinda não há avaliações
- Unidade 1 - Lista de ExercíciosDocumento3 páginasUnidade 1 - Lista de ExercíciosMaíra Malonn100% (1)
- Teste Q2.1 N.º 2 - V1 10-4 CorrDocumento5 páginasTeste Q2.1 N.º 2 - V1 10-4 CorrBia100% (1)
- Prova de QuimicaDocumento4 páginasProva de QuimicaPedagogico Escola 26 de JunhoAinda não há avaliações
- 10FQA Ficha Trab Ini Q2.1 - N.º 2Documento4 páginas10FQA Ficha Trab Ini Q2.1 - N.º 2Mariana CardosoAinda não há avaliações
- Lista 2 PDFDocumento4 páginasLista 2 PDFJoaog123Ainda não há avaliações
- Prova Mestrado PPGQB 2017.1Documento8 páginasProva Mestrado PPGQB 2017.1André Felippe XavierAinda não há avaliações
- QG1P2Documento15 páginasQG1P2João Pedro MaiaAinda não há avaliações
- FF02 FQDocumento4 páginasFF02 FQAndré MatosAinda não há avaliações
- Covalente Aula 5Documento5 páginasCovalente Aula 5PROFº MARCELO SANTOSAinda não há avaliações
- Teste Q2.1 N.º 2 - V1 10-4Documento4 páginasTeste Q2.1 N.º 2 - V1 10-4BiaAinda não há avaliações
- Atividade Revisional Geometria Molecular e Polaridade Das Ligações.Documento5 páginasAtividade Revisional Geometria Molecular e Polaridade Das Ligações.Abraão MattosAinda não há avaliações
- Lista de Exercícios 1 - CQ124Documento3 páginasLista de Exercícios 1 - CQ124Jacqueline Agatha FerreiraAinda não há avaliações
- Simulado Sobre Interações Atômicas Geometria Molecular Polaridade Da Ligação e Da Molécula Forças Intermoleculares e Número de Oxidação. Concurso Professor de QuímicaDocumento4 páginasSimulado Sobre Interações Atômicas Geometria Molecular Polaridade Da Ligação e Da Molécula Forças Intermoleculares e Número de Oxidação. Concurso Professor de QuímicaAnonymous aPzoIa4Ainda não há avaliações
- 3 Lista QuimicaDocumento8 páginas3 Lista QuimicaPedro AlmeidaAinda não há avaliações
- Lista de Exercicios 01 - 9 AnoDocumento4 páginasLista de Exercicios 01 - 9 AnoLarissa BarbosaAinda não há avaliações
- Ficha Formativa 6-10ºano - Ligação QuímicaDocumento11 páginasFicha Formativa 6-10ºano - Ligação QuímicaviviAinda não há avaliações
- Atividade Online Unidade1Documento6 páginasAtividade Online Unidade1Ismael_Malaquias100% (1)
- Lista de TLVDocumento2 páginasLista de TLVKEVIN CARVALHO ツAinda não há avaliações
- Atividade - Ligações Polaridade e Forças Intermoleculares PDFDocumento2 páginasAtividade - Ligações Polaridade e Forças Intermoleculares PDFBirina DamasioAinda não há avaliações
- Ficha 7 FQDocumento6 páginasFicha 7 FQEmma Oliveira MendesAinda não há avaliações
- 10FQA Ficha Trab Ini Q2.1 - N.º 2Documento4 páginas10FQA Ficha Trab Ini Q2.1 - N.º 2Tiago SousaAinda não há avaliações
- Lista de Exercícios - 01 - 08.09.2022Documento1 páginaLista de Exercícios - 01 - 08.09.2022taynarAinda não há avaliações
- 03 Ligacao CovalenteDocumento8 páginas03 Ligacao CovalenteRubens SantosAinda não há avaliações
- FT 7 RespostasDocumento5 páginasFT 7 RespostasptpbzpwtqdAinda não há avaliações
- FT2 Ligacoesquimicas ForcasintermolecularesDocumento3 páginasFT2 Ligacoesquimicas ForcasintermolecularesAfonso VasconcelosAinda não há avaliações
- Ap - Teoria Dos Orbitais Moleculares (Parte 3 - 3)Documento1 páginaAp - Teoria Dos Orbitais Moleculares (Parte 3 - 3)Geremias Armindo ArmindoAinda não há avaliações
- Geometria e PolaridadeDocumento6 páginasGeometria e Polaridadeanon_855647014Ainda não há avaliações
- Ressonância PDFDocumento8 páginasRessonância PDFRomeuComastriAbdalaAinda não há avaliações
- Exercícios de Estudo de MoléculasDocumento37 páginasExercícios de Estudo de MoléculasyagoAinda não há avaliações
- 10Q - FF4 - Ligação QuímicaDocumento10 páginas10Q - FF4 - Ligação QuímicaAvmiguelAinda não há avaliações
- Provas de MestradoDocumento40 páginasProvas de MestradoEder RaminAinda não há avaliações
- Exercicios P2 - Com Algumas RespostasDocumento10 páginasExercicios P2 - Com Algumas RespostasCaroline CarvalhoAinda não há avaliações
- Lista Exercicios LigaçõesDocumento2 páginasLista Exercicios LigaçõesEric garciaAinda não há avaliações
- Ficha Ligacao QuimicaDocumento8 páginasFicha Ligacao QuimicaSusana Maria Cunha Teixeira100% (1)
- Alfa - Módulo 14Documento11 páginasAlfa - Módulo 14Juliano Abreu PrattiAinda não há avaliações
- Ficha 7Documento7 páginasFicha 7leandromaia123789Ainda não há avaliações
- 2 2022 Qof 1avaDocumento3 páginas2 2022 Qof 1avaLuana SimaoAinda não há avaliações
- 4 FQ 10 Ano Ligacao QuimicaDocumento3 páginas4 FQ 10 Ano Ligacao QuimicajferAinda não há avaliações
- Quimica 1ano v2 AlunoDocumento3 páginasQuimica 1ano v2 AlunoMarcelo GfteamAinda não há avaliações
- Questc3b4es de Quc3admica 3c2ba Ano Com DescritoresDocumento26 páginasQuestc3b4es de Quc3admica 3c2ba Ano Com DescritoresCirlene Oliveira Sousa0% (1)
- Lista 4 - Quimica Geral v2Documento2 páginasLista 4 - Quimica Geral v2Lilian PaesAinda não há avaliações
- 214770-Di Qu A09 WEBDocumento24 páginas214770-Di Qu A09 WEBSarah MenesesAinda não há avaliações
- Geometria e Polaridade MolecularDocumento10 páginasGeometria e Polaridade MolecularFerdinando De CarliAinda não há avaliações
- Lista de Exercicios - Geometria Molec e PolaridadeDocumento8 páginasLista de Exercicios - Geometria Molec e PolaridadeJulio AndradeAinda não há avaliações
- Ficha de Trabalho FQ 9º Ano Ligações QuímicasDocumento9 páginasFicha de Trabalho FQ 9º Ano Ligações QuímicasacpalmamaoAinda não há avaliações
- Aula 10 PDFDocumento41 páginasAula 10 PDFGuilhermeAinda não há avaliações
- Universidade Da Beira Interior Departamento de QuímicaDocumento5 páginasUniversidade Da Beira Interior Departamento de QuímicaBruna LopesAinda não há avaliações
- Exercícios de Revisão para A Prova Bimestral Dissertativa Do 2o BimestreDocumento3 páginasExercícios de Revisão para A Prova Bimestral Dissertativa Do 2o BimestremauoscuroAinda não há avaliações
- Genes Livro PDFDocumento127 páginasGenes Livro PDFAna Karen AlbuquerqueAinda não há avaliações
- Principios Eticos e Manejo - DRFC - USP Curso USPDocumento10 páginasPrincipios Eticos e Manejo - DRFC - USP Curso USPAna Karen AlbuquerqueAinda não há avaliações
- Links YOU TUBEDocumento2 páginasLinks YOU TUBEAna Karen AlbuquerqueAinda não há avaliações
- Atividade I - Cálculo Diferencial e Integral IDocumento5 páginasAtividade I - Cálculo Diferencial e Integral IAna Karen AlbuquerqueAinda não há avaliações
- Atividade II - Cálculo Diferencial e Integral IDocumento7 páginasAtividade II - Cálculo Diferencial e Integral IAna Karen AlbuquerqueAinda não há avaliações
- Guia de Construção de Projetos Como Apresentar Um Plano de Análise e Projetos 1 EdiçãoDocumento36 páginasGuia de Construção de Projetos Como Apresentar Um Plano de Análise e Projetos 1 EdiçãoAna Karen AlbuquerqueAinda não há avaliações
- Amostra - Piano e Teclado - Explicação Detalhada e Ampla PDFDocumento18 páginasAmostra - Piano e Teclado - Explicação Detalhada e Ampla PDFAna Karen AlbuquerqueAinda não há avaliações