Escolar Documentos
Profissional Documentos
Cultura Documentos
Aula 1 - ENEM - Propriedades Dos Materiais PDF
Enviado por
Isabela TeotônioTítulo original
Direitos autorais
Formatos disponíveis
Compartilhar este documento
Compartilhar ou incorporar documento
Você considera este documento útil?
Este conteúdo é inapropriado?
Denunciar este documentoDireitos autorais:
Formatos disponíveis
Aula 1 - ENEM - Propriedades Dos Materiais PDF
Enviado por
Isabela TeotônioDireitos autorais:
Formatos disponíveis
Preparatrio para o ENEM
Curso Preparatrio
Qumica Prof. Isabela Teotnio
Tpico I Introduo Qumica
Tpico II Propriedades dos Materiais
Exerccios de Nivelamento
Conceitue e exemplifique, quando possvel.
a) tomos
b) Estados Fsicos
c) Elemento Qumico, n
atmico e n de massa.
d) Substncia pura
e) Mistura homognea X
heterognea
f) Soluo
g) Ponto de Fuso e Ponto
de Ebulio
h) Processos
endotrmicos X
exotrmicos
i) Densidade
j) Fenmeno fsico X
qumico
k) Reao qumica
l) Balanceamento de
equao qumica: N
2
+
H
2
NH
3
m) Reao de oxirreduo
n) Pilha de Daniell
o) Ligao qumica
p) Interao Qumica (ex:
dipolo induzido- dipolo
induzido, ligao de H)
q) NOX
r) Escala de PH
s) cido
t) Base
u) xido
v) Sal
w) Hidrocarbonetos
x) lcool
y) Fenol
z) ter
aa) Cetona
bb)Aldedo
cc) cido Carboxlico
dd)ster
ee) Amina
ff) Amida
gg) Energia renovvel X
no-renovvel
hh)Calor X Temperatura
Conceitos Bsicos da Qumica
Matria
Tudo o que possui massa e, portanto, ocupa lugar no
espao.
Ex: madeira, ouro, ferro, areia, gua, ar.
Energia no matria!
Ex: luz, som, calor...
Conceitos Bsicos da Qumica
Substncia
Constitui os corpos.
Formada de apenas um tipo
de molcula.
Ex: gua, diamante, cloreto
de sdio.
Se h mais de um tipo de
molcula, chamamos de
Mistura.
Ex: ar (O2, N2, CO2),
petrleo (comp. orgnicos),
soro fisiolgico (H2O e NaCl).
Partculas
1. Molculas: Conjunto de
tomos. Menor parte de
uma substncia que
conserva suas propriedades.
Ex: NaOH, HCl, O2.
2. tomos: Formam as
molculas. Menor parte da
matria.
Ex: Ca, Cl, Na.
Exemplo:
Matria: madeira
Substncias: celulose (molcula: C6H10O5 / tomos: C, H e O); lignina; e gua.
Estados Fsicos da Matria
A matria pode ser encontrada em trs estados fsicos:
slido, lquido e gasoso.
Mudanas de Estado Fsico:
Propriedades da Matria
Propriedades da Matria
Propriedades Organolpticas
Relacionadas aos sentidos.
Cor viso: uma matria pode possuir cor ou no. A
gua incolor . Os alimentos tm cores prprias, e
quando apresentam cor diferente da esperada, esto
em processo de deteriorao.
Aspecto tato.
Cheiro olfato.
Sabor paladar.
Propriedades Fsicas P.F. e P.E.
Ponto de Fuso (S-L): Temperatura na qual uma substncia ou mistura
passa do estado slido para o lquido.
Ponto de Ebulio (L-G): Temperatura na qual uma substncia ou
mistura passa do estado lquido para o gasoso.
Durante os P.F. e P.E. coexistem os dois estados fsicos.
Relao com a Presso: diretamente proporcional.
Propriedades Fsicas P.F. e P.E.
Algumas misturas tm o
comportamento semelhante ao
de substncias puras quando
submetidas ebulio e fuso.
Misturas azeotrpicas: lcool etlico +
gua, acetona + metanol, lcool etlico +
clorofrmio
Misturas eutticas: ligas metlicas em
geral.
Propriedades Fsicas Densidade
Relao entre massa e volume. D (g/cm) = . massa (g) .
volume (cm)
Cada material possui a sua densidade. A densidade da gua 1g/cm.
A densidade de uma mistura sua mdia ponderada.
Afunda ou Flutua ? Dada uma mistura, a substncia mais densa afunda e a
menos densa flutua.
Escala de densidade p um mesma substncia/mistura: slido > lquido > gs.
Exceo: a gua a nica substncia que mais densa lquida do que slida,
e, por isso o gelo flutua. Densidade da gua lquida: 1g/cm. Densidade do
gelo: 0,92 g/cm.
Propriedades Fsicas Solubilidade
Soluo = Solvente: quem dissolve. A gua o solvente universal.
Soluto: dissolvido.
Coeficiente de Solubilidade: quantidade mxima de
soluto, que determinada poro de solvente dissolve, a
uma certa temperatura. Ex: coeficiente de solubilidade
(CS) do NaCl em H2O: 360g/L a 20C.
Soluo insaturada: quantidade de soluto inferior.
Soluo saturada: quantidade mxima de soluto.
Soluo super saturada: quantidade de soluto superior.
Propriedades Fsicas Solubilidade Grficos
Anlise do grfico:
KNO3: quanto maior a temperatura, maior o CS, logo, coeficiente
endotrmico.
NaCl: quanto m maior a temperatura, maior o CS, logo, coeficiente
endotrmico. Pouca variao no CS.
CO2: quanto maior a temperatura, menor o CS, logo, coeficiente
exotrmico.
Classificao da Matria
Substncias e Misturas
Substncia
Constituem-se de apenas
umtipo de molcula.
Critrios de Pureza:
P.F./P.E. e densidade
constantes e definidos.
Mistura
Constituem-se de mais de
umtipo de molcula.
Conceito: Reunio de duas
ou mais substncias sem
que haja reao entre elas.
Substncias
Substncias Simples
Constituem-se de apenas
um elemento qumico.
Substncias Compostas
Constituem-se de dois ou
mais elementos qumicos
Substncias - Alotropia
Um mesmo elemento qumico* capaz de formar
substncias simples diferentes.
*Elemento Qumico: Conjunto de
tomos com o mesmo nmero
atmico.
Substncias Critrios de Pureza
Critrios de pureza so testes, atravs dos quais,
identificamos a pureza de uma substncia.
As substncias puras apresentem P.F. e P.E,
densidade e solubilidade constantes e definidos.
P.F e P.E.
Exemplo gua Destilada
P.F. e P.E: 0 e 100C.
Densidade: 1g/cm
Solubilidade: -
Ateno! Propriedades Fsicas P.F. e P.E.
Algumas misturas tm o
comportamento semelhante ao
de substncias puras quando
submetidas ebulio e fuso.
Misturas azeotrpicas: lcool etlico +
gua, acetona + metanol, lcool etlico +
clorofrmio
Misturas eutticas: ligas metlicas em
geral.
Misturas
Misturas
Heterogneas
Ocorrem quando as
substncias so imiscveis, isto
, no se misturam,
apresentando duas ou mais
fases identificveis.
Ex: gua+areia, lcool+leo.
Importante: o leite e o sangue
so misturas heterogneas.
Polaridade: Semelhante
dissolve semelhante.
Molcula da gua: polar.
Molcula de leos: apolares.
Sabes: Bipolares.
Homogneas
Ocorrem quando as
substncias so miscveis, isto
, se misturam, apresentando
apenas uma fase.
Ex: gases, vinagre, gua + sal.
Sistemas
Sistema uma poro limitada do universo, considerada como
um todo para efeito de estudo.
Sistema homogneo aquele que apresenta as mesmas propriedades
em qualquer parte de sua extenso em que seja examinado.
Sistema heterogneo aquele que no apresenta as mesmas
propriedades em qualquer parte de sua extenso em que seja
examinado.
Processos de Separao de
Misturas Heterogneas
1.Catao: Consiste na identificao visual
dos componentes da mistura. Usada na
separao de sistemas slido-slido. Ex:
catar gros de feijo.
2. Peneirao/Tamisao: Usada quando os
gros que formam a mistura tm tamanhos
diferentes; os gros maiores ficam retidos
na malha da peneira. Separao de
sistemas slido-slido. Ex: peneirar areia e
brita.
Processos de Separao de
Misturas Heterogneas
3. Ventilao: O componente menos denso arrastado por
uma corrente de ar. Usada na separao de sistemas slido-
slido. Ex: separao da casca e do caroo do amendoim.
4. Imantao: Utiliza-se do magnetismo para realizar a
separao. Usada na separao de sistemas slido-slido.
Processos de Separao de
Misturas Heterogneas
6. Levigao: Utiliza-se de um
lquido corrente para fazer a
separao. O componente
menos denso arrastado pelo
lquido, enquanto o mais
denso deposita-se no fundo de
um recipiente. Separao de
sistemas slido-slido. Ex:
lavagem de areia e ouro
(garimpo).
5. Flotao: Utiliza-se de um
lquido com densidade
intermediria para fazer a
separao. Separao de
sistemas slido-slido.
Animao
Processos de Separao de
Misturas Heterogneas
7. Dissoluo fracionada/Extrao por solvente: Utiliza-se de
um lquido para dissolver um dos componentes da mistura.
Separao de sistemas slido-slido. Ex: sal+areia,
acar+cascalho.
Animao
Processos de Separao de
Misturas Heterogneas
8. Filtrao simples: Separao de componentes por meio de
uma superfcie porosa denominada filtro. O filtro retm a fase
slida em sua superfcie, permitindo somente a passagem da
fase lquida ou gasosa. Aplica-se a sistemas slido-lquido ou
slido-gasoso.
1. slido lquido 2. slido gasoso
A mistura lanada sobre um filtro, o qual
permite somente a passagem do
componente gasoso. Ex: aspirador de p.
Animao 1
Processos de Separao de
Misturas Heterogneas
8. Filtrao a vcuo: utilizada para acelerar o processo de
filtrao quando a mistura slido-lquida muito pastosa (como
o caso da mistura gua e farinha de trigo) ou quando o lquido
tem alta viscosidade.
Processos de Separao de
Misturas Heterogneas
9. Decantao: Baseia-se na diferena de densidade. Aplica-se
a sistemas heterogneos slido-lquido, lquido-lquido e slido-
gs. Ao deixarmos a mistura em repouso, lentamente o
componente mais denso, deposita-se no fundo, ocorrendo a
sedimentao. Ex: separar gua e areia, gua e leo, gs e
poeira. 2. lquido lquido
1. slido lquido
Animao 2
Processos de Separao de
Misturas Heterogneas
9. Decantao:
3. slido gs
Cmera de gs: Corresponde a um sistema com duas aberturas
onde a mistura introduzida num sistema em zigue-zague,
onde as partculas slidas ao encontrarem os obstculos
perdem velocidade depositando-se no fundo do recipiente.
Processos de Separao de
Misturas Heterogneas
10. Sifonao: Processo de transporte de um lquido de um
nvel mais alto a outro mais baixo. Voc faz um sifo funcionar
sugando o lquido para o seu interior. O lquido ento flui para o
nvel inferior porque a presso maior na extremidade alta do
que na baixa. um processo aplicado em sistemas slido-
lquido e lquido-lquido.
Animao
Processos de Separao de
Misturas Heterogneas
11. Centrifugao: Decantao acelerada. Aplica-se quando a
diferena de densidade das substncias muito pequena.
feita em uma centrifuga (imagem abaixo). Ex: sangue, parte
slida (hemcias, plaquetas e glbulos brancos) separada da
parte lquida (soro ou plasma).
Processos de Separao de
Misturas Homogneas
1. Evaporao/Cristalizao: O lquido evapora, restando o
slido. Sistemas slido-lquido. Ex: obteno de sal em
salinas.
Processos de Separao de
Misturas Homogneas
2. Destilao simples: Utilizada quando temos um slido
dissolvido em um lquido. Baseia-se na diferena de P.E. A
soluo entra em ebulio no balo, mas somente o lquido
vaporiza-se e caminha pelo condensador. Ao entrar em
contato com as paredes frias, condensa-se, voltando ao
estado lquido.
Animao
Processos de Separao de
Misturas Homogneas
3. Destilao fracionada:
Aplica-se a lquidos miscveis.
Baseada na diferena de PE.
Ex: destilao do petrleo.
Animao
Obs: para separar gases,
liquefazemo-nos.
Exerccios
1. Escolha um material e designe um corpo, um objeto, as substncias, as molculas e
tomos constituintes.
2. Diferencie tomos de molculas. D exemplos.
3. Fale sobre P.F e P.E. Esboce um grfico para substncia pura e um para mistura.
Explique porque so diferentes.
4. Fale sobre densidade.
5. O que uma soluo? De que formada? Quais as suas classificaes?
6. Defina substncia e diferencie de misturas.
7. O que uma substncia pura? Diferencie suas classificaes e d exemplos.
8. O que critrio de pureza? Quais so eles?
9. De que so formadas as misturas? Quais as suas classificaes? Exemplifique.
10. Fale sobre extrao por solvente/dissoluo fracionada.
11. Fale sobre decantao e centrifugao. Que tipos de materiais elas separam?
12. Quais os dois tipos de destilao? Expilque-os. Qual a principal diferena entre
eles?
13. Quais as semelhanas e diferenas entre a evaporao/cristalizao e a destilao
simples?
Você também pode gostar
- Prática - ConcenTração de SoluçõesDocumento5 páginasPrática - ConcenTração de SoluçõesIsabela TeotônioAinda não há avaliações
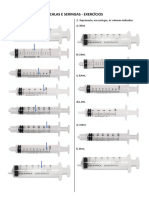
- Escalas e seringas - exercícios de volumeDocumento2 páginasEscalas e seringas - exercícios de volumeIsabela TeotônioAinda não há avaliações
- Exercícios - Concentração de SoluçõesDocumento4 páginasExercícios - Concentração de SoluçõesIsabela TeotônioAinda não há avaliações
- Química IDocumento3 páginasQuímica IIsabela TeotônioAinda não há avaliações
- Exercícios - Ligações e Interações 2018Documento2 páginasExercícios - Ligações e Interações 2018Isabela TeotônioAinda não há avaliações
- Exercícios - Lei de HessDocumento1 páginaExercícios - Lei de HessIsabela TeotônioAinda não há avaliações
- REVISÃO - Exercicios - Tabela - Provas Anteriores PDFDocumento2 páginasREVISÃO - Exercicios - Tabela - Provas Anteriores PDFIsabela TeotônioAinda não há avaliações
- BALANCEAMENTO DE EQUAÇÕESDocumento2 páginasBALANCEAMENTO DE EQUAÇÕESdesinhalove100% (5)
- Pilhas e baterias: funcionamento e tiposDocumento10 páginasPilhas e baterias: funcionamento e tiposIsabela TeotônioAinda não há avaliações
- Aula 4 - Corpo de Bombeiros Militar de Minas GeraisDocumento12 páginasAula 4 - Corpo de Bombeiros Militar de Minas GeraisIsabela TeotônioAinda não há avaliações
- Geo PDFDocumento4 páginasGeo PDFIsabela TeotônioAinda não há avaliações
- Elementos Químicos e Tabela PeriódicaDocumento2 páginasElementos Químicos e Tabela PeriódicaIsabela TeotônioAinda não há avaliações
- Prática de SolubilidadeDocumento6 páginasPrática de Solubilidadegabirodrigues0909Ainda não há avaliações
- Silicato de Sódio LíquidoDocumento15 páginasSilicato de Sódio LíquidoDéboraAinda não há avaliações
- Diagrama ternário água-etanol-acetato de etilaDocumento11 páginasDiagrama ternário água-etanol-acetato de etilaMarcella MantovaniAinda não há avaliações
- 006 Produto de SolubilidadeDocumento11 páginas006 Produto de Solubilidadeulisses7Ainda não há avaliações
- Síntese da Aspirina a partir do Ácido SalicílicoDocumento10 páginasSíntese da Aspirina a partir do Ácido SalicílicoNanda SousaAinda não há avaliações
- Ficha de Segurança Produto Químico YesoDocumento9 páginasFicha de Segurança Produto Químico YesoGabriel “Ftz” RodriguesAinda não há avaliações
- Aula-5 - Sistemas de Reagentes PDFDocumento67 páginasAula-5 - Sistemas de Reagentes PDFNelo DionisioAinda não há avaliações
- Ar atmosférico/Funções Inorgânicas/Estudo de reaçõesDocumento7 páginasAr atmosférico/Funções Inorgânicas/Estudo de reaçõesMarjoliGrandoAinda não há avaliações
- REACOES DE PRECIPTACAO - AlunoDocumento9 páginasREACOES DE PRECIPTACAO - AlunoRoberta Parastchuk100% (1)
- AlginatoDocumento27 páginasAlginatocarina baltazarAinda não há avaliações
- Relatório SulfatoCobreDocumento17 páginasRelatório SulfatoCobreWagnerBertoliniJuniorAinda não há avaliações
- Nalco® 47506Documento8 páginasNalco® 47506Ikarus2903Ainda não há avaliações
- Capitulo (III.1) Soluçoes SolubilidadeDocumento22 páginasCapitulo (III.1) Soluçoes SolubilidadeDauson CuigicjenhiAinda não há avaliações
- Identificação metabólitos secundários folhas sene casca pau-pereiraDocumento6 páginasIdentificação metabólitos secundários folhas sene casca pau-pereiracaroline1303Ainda não há avaliações
- FISPQ MediawebserverDocumento14 páginasFISPQ MediawebserverFlavia Varela de FrançaAinda não há avaliações
- Solubilidade do Hidróxido de CálcioDocumento9 páginasSolubilidade do Hidróxido de CálcioLuisa BiaAinda não há avaliações
- Ficha de Ciências 5º Ano - ÁguaDocumento5 páginasFicha de Ciências 5º Ano - ÁguaAndreia Pais91% (11)
- Reações de Precipitação e Equilíbrio HeterogêneoDocumento72 páginasReações de Precipitação e Equilíbrio HeterogêneoPaulo Alexandre Alves Massa100% (1)
- Solvente Químico: Informações de SegurançaDocumento7 páginasSolvente Químico: Informações de SegurançaCarlos JuniorAinda não há avaliações
- Aula 6 Volumetria de Precipitação Alunos 2011.1Documento28 páginasAula 6 Volumetria de Precipitação Alunos 2011.1robertamarlaAinda não há avaliações
- Introdução ao Controle Químico de Plantas DaninhasDocumento16 páginasIntrodução ao Controle Químico de Plantas DaninhasDiovane AntonowAinda não há avaliações
- 5 - NalcoDocumento14 páginas5 - NalcoJulia Silveira CostaAinda não há avaliações
- FISPQ - Lukscolor - Acrílico Premium Plus PDFDocumento9 páginasFISPQ - Lukscolor - Acrílico Premium Plus PDFKarolAinda não há avaliações
- Relatorio 9Documento11 páginasRelatorio 9Gabriella Hernandez100% (1)
- Ficha de Segurança Graxa LubrificanteDocumento8 páginasFicha de Segurança Graxa LubrificanteLAERCIO ENGEVALEAinda não há avaliações
- Germi Rio FispqDocumento7 páginasGermi Rio FispqRafael CozerAinda não há avaliações
- ANEXO I - Especificações Dos Fertilizantes Minerais SimplesDocumento21 páginasANEXO I - Especificações Dos Fertilizantes Minerais SimplesPaulo Roberto de CarvalhoAinda não há avaliações
- 1a Lista de Exercicios - Reacoes QuimicasDocumento2 páginas1a Lista de Exercicios - Reacoes QuimicasSerena100% (1)
- Apostila de Quimica Aplicada 1Documento26 páginasApostila de Quimica Aplicada 1evolutionfins100% (4)
- Guia rápido de tratamento de água e efluenteDocumento19 páginasGuia rápido de tratamento de água e efluenteAndreAinda não há avaliações