Escolar Documentos
Profissional Documentos
Cultura Documentos
Relatorio - Expansao de Gases - docxTERMODINAMICA.123
Enviado por
Elvis AlvesTítulo original
Direitos autorais
Formatos disponíveis
Compartilhar este documento
Compartilhar ou incorporar documento
Você considera este documento útil?
Este conteúdo é inapropriado?
Denunciar este documentoDireitos autorais:
Formatos disponíveis
Relatorio - Expansao de Gases - docxTERMODINAMICA.123
Enviado por
Elvis AlvesDireitos autorais:
Formatos disponíveis
UNIVERSIDADE TIRADENTES
CURSO DE ENGENHARIA DE PETRLEO
EXPANSO DOS GASES
ELVIS ALVES DOS SNATOS
RENATA EVANGELISTA STRAPPA
STEPHANE CAROLINE SILVA SANTOS
Aracaju/SE
ABRIL/2014
2
ELVIS ALVES DOS SANTOS
RENATA EVANGELISTA STRAPPA
STEPHANE CAROLINE SILVA SANTOS
EXPANSO DOS GASES
Relatrio sobre a experincia Expanso de Gases,
realizada em outubro de 2013, da disciplina de
Termodinmica, ministrada pelo Prof. Cludio Dariva, na
Universidade Tiradentes.
Aracaju/SE
ABRIL/2014
3
NDICE
1 Introduo........................................................................................................... 04
2 Reviso de Literatura .......................................................................................... 04
3 Objetivos............................................................................................................. 05
4 Materiais e Mtodos............................................................................................ 06
5Resultados e Discusses .................................................................................... 07
6 Concluso............................................................................................................ 17
7Referencias ..........................................................................................................17
4
1. INTRODUO
O gs ideal um modelo idealizado no qual o gs se move ao acaso, sendo
que suas molculas se chocam elasticamente, apresentam volume prprio e no
exercem aes mtuas.
2. REVISAO DE LITERATURA
Caractersticas de um gs ideal
composto de partculas puntiformes, ou seja, de tamanho desprezvel;
dessa maneira, elas no podem realizar movimento de rotao.
A fora de interao eltrica entre as partculas devem ser nulas, ou seja, elas
devem estar bem afastadas para que no haja fora eltrica.
H ocorrncia de interao apenas durante as colises, que so
perfeitamente elsticas; e aps esta coliso entre duas partculas, no h perda de
energia na forma de calor.
Ento, para que o gs possa ser dito ideal, deve ter presso baixa (as
partculas devem estar mais afastadas uma das outras) e alta temperatura (as
partculas devem vibrar com mais energia).
O estudo do comportamento dos gases resultou em uma relao entre as
variveis: temperatura, presso, volume e nmero de mols do gs. Essa relao
matemtica conhecida como a Lei dos Gases Ideais. A maioria dos gases reais
se comporta de acordo com esta lei. Apenas em poucas situaes, como prximo de
uma transio de fase ou temperaturas muito baixas, esta lei no obedecida.
A Lei dos gases ideais nos permite determinar o valor de uma das variveis
de estado de um gs se conhecermos as outras trs. Assim, quando o nmero de
mols de um gs permanece constante, a Lei dos Gases Ideais expressa pela
seguinte equao:
P.V=n.R.T
Onde P a presso; V o volume; n o nmero de mols, R a constante
dos gases e T a temperatura. Um gs dito ideal quando obedece Lei dos
5
Gases Ideais. Esta lei a combinao das Leis de Boyle, de Charles e da Lei de
Gay-Lussac e Avogadro.
Quando as medidas de presso, volume molar e temperatura no admitem a
relao prevista pela Equao de Clayperon, dentro da exatido das medidas, o gs
desvia-se da idealidade, ou seja, apresenta um comportamento no ideal. Esses
desvios, em valores absolutos, so pequenos e so observados em gases puros e
em misturas gasosas no reagentes. temperatura ambiente e baixa presso
praticamente no ocorre desvios da idealidade, porm, medida que a presso
aumenta o comportamento desses gases divergem (Castellan, 1978).
Um gs real existe sob a maioria das condies de temperatura e presso e
constitudo por partculas materiais dotadas de movimento catico, sujeitas s foras
de atrao longa distncia e foras de repulso curta distncia (Kauzmann,
1970).
O comportamento de um gs real desvia-se daquele do gsideal, a uma dada
presso e temperatura. Segundo van Wylenet al. (2003), essasinformaes podem
ser esclarecidas a partir do conceito de fator de compressibilidade Z, oqual
definido pela relao:
PV = ZnRT (2)
Verifica-se, por meio da equao (2), que quando se trata de um gs ideal Z =
1,o afastamento de Z, em relao unidade, uma medida do desvio de
comportamentodo gs real em relao ao previsto pela equao (1).
3. OBJETIVOS
- Calibrar volume de tubulaes pela tcnica de gases;
-Calcular o volume de um sistema desconhecido atravs de um volume
conhecido.
6
1. MATERIAIS E MTODOS
3.1. Materiais utilizados
- Cilindro de 1L;
- Conjunto de linhas;
- Transdutor de presso;
-Indicador de presso (Bar).
3.2Procedimento Experimental
1-Encheu-se um cilindro de 1L, com um determinado gs e anotou-se a
presso inicial quando o gs estava somente no cilindro.
2- Abriu-se a vlvula deixando o gs se expandir para o conjunto de linhas e
anotou-se a presso total de todo o sistema.
3- Em seguida, esvaziou-se o gs que estava presente no conjunto de linhas,
anotando a nova presso inicial do cilindro.
4- Repetiu-se o procedimento 2 e 3 vezes.
A Figura 1 apresenta o aparato experimental utilizado durante o
procedimento.
Figura 1: Aparato experimental prtica de Expanso de Gases
7
Figura 2: Aparato experimental prtica de Expanso de Gases
5.RESULTADOS E DISCUSSES
A Tabela 1 apresenta os valores obtidos durante o procedimento
experimental.
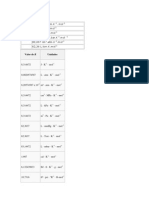
Tabela 1: Dados da prtica de Expanso de Gases
Presso
Inicial
Presso
Total
1 Ensaio 29,00 26,2
2 Ensaio 26,2 24,2
3 Ensaio 24,2 21,7
4 Ensaio 21,7 20,00
Atravs da tabela possvel perceber que medida que o gs se expande
para todo o sistema, ou seja, com o aumento do volume a presso diminui. No
entanto o nmero de molculas permanece o mesmo, mas de um ensaio para o
outro o nmero de molculas diminui.
8
Como a presso uma propriedade Intensivafoi possvel calcular o volume do
conjunto de linhas, atravs de trs mtodos: Gs Ideal, Equao Virial e pela
Teoria do Estados Correspondentes (TEC), como mostrado a seguir, alm disso
sabemos que a temperatura ambiente correspondeu a 20C ou 293K, o gs foi o
CO
2
que a essa temperatura possui o 2 coeficiente do virial correspondente a
-130 cm
3
/mol e fator acntrico igual a 0,224.
1 Ensaio:
- Gs Ideal
Para o Gs Ideal temos Z = 1
- Equao Virial
Para Equao Virial ns teremos
Temos que:
- Teoria dos Estados Correspondentes
Temos que:
(
()
()
)
Para o CO
2
temos e temperatura crtica igual a 304,2K e presso critica igual
a 73,83 bar e w = 0, 224
Nas condies de temperatura 298K e presso 29,0 Bar:
10
VERIFICADO NA TABELA E. 1; VALUES OF Z
()
()
(
()
()
) ( ( )) 0, 8237
Nas condies de temperatura 298K e presso 26,2 Bar:
Para TR
()
= 0,97 -- p=0,2 0,35 0,4 vide tabela
0, 9997 x 0, 8338
0,4 - 0,2 / = 0,35 0,2 /
0, 8338 -0, 9227 x 0, 9227
= -2, 2497. (x 0, 92227) = 0,15
- 2, 2497 x + 2, 075 = 0,15
-2, 2497x = 0,15 2, 075
-2, 2497x = -1, 925
()
X= 0, 8556
Para TR
()
= 0,97 p=0,2 0,35 p= 0,4 vide tabela
-0, 0208 x -0, 0450
0,4 - 0,2 / = 0,35 0,2 /
-0, 0150 + 0, 0208 x + 0, 0208
= -8, 2644. (x + 0, 0, 0208) = 0,15
11
- 8, 2644 x 0, 171 = 0,15
-8, 2644x = 0,15 + 0, 171
-8, 2644x = 0, 321
0, 321/ -8, 2644x
()
X= -0, 0388
(
()
()
) ( ( )) 0, 8469
Temos que:
2 Ensaio:
- Gs Ideal
Para o Gs Ideal temos Z = 1
12
- Equao Virial
Para Equao Virialtemos
Temos que:
13
- Teoria dos Estados Correspondentes
Nas condies de temperatura 298K e presso 26,2 Bar e w = 0, 224:
(
()
()
)
( ( ))
0, 8469
Nas condies de temperatura 298K e presso 24,2 Bar:
()
()
(
()
()
)
( ( ))
0,87
(
()
()
) Substituindo os valores na equao da tec. o
ensaio 1 iremos encontrar: zf = -0,0359
(
()
()
) = 0,8690 + (0,224 x -0,0359) = 0,8609
Temos que:
3 Ensaio:
14
- Gs Ideal
Para o Gs Ideal temos Z = 1
- Equao Virial
Para Equao Virialtemos
Temos que:
15
- Teoria dos Estados Correspondentes
Nas condies de temperatura 298K e presso 24,2 Bar:
(
()
()
)
( ( ))
0, 8690
Na condies de temperatura 298K e presso 21,7 Bar:
()
()
(
()
()
)
( ( ))
0, 8752
Temos que:
16
4 Ensaio:
- Gs Ideal
Para o Gs Ideal temos Z = 1
- Equao Virial
Para Equao Virialtemos
17
Temos que:
- Teoria dos Estados Correspondentes
Nas condies de temperatura 298K e presso 21,7 Bar:
(
()
()
)
( ( ))
0,89
Nas condies de temperatura 293K e presso 20,6 Bar:
()
()
(
()
()
)
( ( ))
0,89
18
Temos que:
2. CONCLUSAO
Atravs da prtica experimental foi possvel verificar que a partir do momento
que se trabalha com um gs real, no caso o CO
2,
as interaes entre suas molculas
devem ser consideradas e esse desvio de comportamento em relao ao gs ideal
foi calculado a partir do conceito de fator de compressibilidade Z.Concluindo que
medida que o valor desse parmetro se afasta de 1,0, valorcaracterstico do gs
ideal, o comportamento do gs real se distancia da idealidade do gs.
Na prtica no houve uma grande discrepncia entre o volume final obtido
considerando a equao de estado do gs ideal eo volumes final obtido
considerando as interaes moleculares, isto ocorreu porque o desvio de idealidade
de um gs mais evidente a altas presses e baixas temperaturas.
Contudo como vimos que a diferena dos valores no foram muito distante a
equao o gs ideal e um modelo para este sistema o que comprova que este
ideal para sistemas com baixa densidade e baixa presso j se as interaes o
sistema fossem fortes este no seria um modelo bom, pois o mesmo s bom para
as interaes fracas, contudo os modelos de tec e viral so bons para calcular as
interaes de mdias a fortes sendo estas duas melhores do que a do gs ideal por
este motivo.
19
REFERENCIAS
Introduo Termodinmica (Apontamentos curso Termodinmica e Estrutura da
Matria) , L.L. Alves, 2006, -
Thermodynamique. Fondements et applications , J.-P. Prez , Dunod, 3 ed.
(2001), ISBN: 2-10-005554-2
CASTELLAN, G. W. Fsico-Qumica; traduo de Luiz Carlos Guimares,
LivrosTcnicos e Cientficos, v1. Rio de Janeiro, 1978.
KAUZMANN, W., Teoria Cintica de los Gases, Editorial Revert, S. A .,
Barcelona,1970.
MAHAN, B.M.; MYERS, R. J. Qumica, um curso universitrio. Traduo da 4
edioamericana. Editora Edgard Blcher Ltda. So Paulo, 2000.
van WYLEN, G.; SONNTAG, R.; BORGNAKKE, C. Fundamentos da Termodinmica
Clssica. Traduo da 4 edio Americana. Editora Edgard Blcher Ltda. SoPaulo,
2003.
I
Você também pode gostar
- Revisão UnB - Química GeralDocumento15 páginasRevisão UnB - Química GeralHASFTAGAinda não há avaliações
- Revisão Estudo Sobre Os GasesDocumento23 páginasRevisão Estudo Sobre Os GasesLuiz Gustavo MartinsAinda não há avaliações
- TermoDocumento19 páginasTermoDanillo BarretoAinda não há avaliações
- Exercícios Gases PerfeitosDocumento13 páginasExercícios Gases PerfeitosJeferson Albino FleckAinda não há avaliações
- Captura de Tela 2023-10-09 À(s) 08.08.26Documento10 páginasCaptura de Tela 2023-10-09 À(s) 08.08.26hremohiAinda não há avaliações
- Exercicio 2 AnoDocumento13 páginasExercicio 2 Anoalmeida amorim almeida100% (1)
- FisicoQuimica IDocumento216 páginasFisicoQuimica IWagner Rodrigues NascimentoAinda não há avaliações
- Cap VI - GasesDocumento6 páginasCap VI - GasesHélder ViegasAinda não há avaliações
- Apostila FísicaDocumento91 páginasApostila FísicaViviane BoulosAinda não há avaliações
- Intensivomedicina-Química-Casos Particulares de Estequiometria - Rendimento, Pureza e Gases Fora Das CNTP-23-08-2019Documento11 páginasIntensivomedicina-Química-Casos Particulares de Estequiometria - Rendimento, Pureza e Gases Fora Das CNTP-23-08-2019Edison SilvaAinda não há avaliações
- 10 Prof (IIº Trimestre)Documento22 páginas10 Prof (IIº Trimestre)jusianeteixeira21Ainda não há avaliações
- Laboratorio de Fisica Termica ApostilaDocumento35 páginasLaboratorio de Fisica Termica ApostilaLucas CoutoAinda não há avaliações
- Termodinamica Aplicada Na RefrigeracaoDocumento94 páginasTermodinamica Aplicada Na RefrigeracaoGuto BelotoAinda não há avaliações
- Picnometria de HélioDocumento5 páginasPicnometria de HélioMichelle LouiAinda não há avaliações
- P2-Quimico Produtos PerigososDocumento16 páginasP2-Quimico Produtos PerigososHugo RidaoAinda não há avaliações
- Aula 17 - TermometriaDocumento40 páginasAula 17 - TermometriaFabricio VigolloAinda não há avaliações
- Logica Matematica 4Documento18 páginasLogica Matematica 4PEDRO FERNANDESAinda não há avaliações
- Cte RDocumento5 páginasCte RPâmela BarbosaAinda não há avaliações
- Aula 3 - 1 Lei Da Termodinâmica 1Documento35 páginasAula 3 - 1 Lei Da Termodinâmica 1SidsambangaAinda não há avaliações
- SeriesDocumento86 páginasSeriesJorge CambindaAinda não há avaliações
- Trabalho em Grupo Mecanica Dos Fluidos RetDocumento16 páginasTrabalho em Grupo Mecanica Dos Fluidos RetMilton ChiluvaneAinda não há avaliações