Escolar Documentos
Profissional Documentos
Cultura Documentos
Espectros Atômicos
Enviado por
Ruan Luz0 notas0% acharam este documento útil (0 voto)
7 visualizações2 páginasEspectros Atômicos
Direitos autorais
© © All Rights Reserved
Formatos disponíveis
PDF, TXT ou leia online no Scribd
Compartilhar este documento
Compartilhar ou incorporar documento
Você considera este documento útil?
Este conteúdo é inapropriado?
Denunciar este documentoEspectros Atômicos
Direitos autorais:
© All Rights Reserved
Formatos disponíveis
Baixe no formato PDF, TXT ou leia online no Scribd
0 notas0% acharam este documento útil (0 voto)
7 visualizações2 páginasEspectros Atômicos
Enviado por
Ruan LuzEspectros Atômicos
Direitos autorais:
© All Rights Reserved
Formatos disponíveis
Baixe no formato PDF, TXT ou leia online no Scribd
Você está na página 1de 2
Instituto Federal de Educação, Ciência e Tecnologia do Pará- Campus
Bragança
Disciplina: Fundamentos de Física
Docente: Msc. Sandro do Nascimento da Costa
Espectros Atômicos
Indicação do comportamento quântico da
matéria tinha sido observada bem antes
da época de Rutherford e Bohr. Uma das
mais notáveis evidências desse
comportamento tinha sido observada na
emissão do espectro eletromagnético por
átomos.
Newton em 1666
Franhoffer em 1814 – luz não contínua
Nota-se que cada átomo tem seu próprio
espectro característico, isto é, tem um
conjunto específico de linhas espectrais.
Em geral, os espectros atômicos são
extremamente complicados, pois podem
conter centenas de linhas. Entretanto o
espectro do átomo de hidrogênio é
relativamente simples, por conter apenas
um elétron.
No final do século XIX foram observados
diversos espectros do átomo de
hidrogênio, sem que nenhuma análise ou
interpretação fosse realizada para
explica-los.
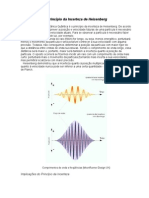
Radiação corpo negro aquecido
A primeira interpretação empírica
“contínuo”
satisfatória para explicar as linhas
Radiação emitida por um átomo
espectrais observadas no hidrogênio na
livre, está concetrada em um
região do visível, foi proposta por J.J.
número discreto de 𝜆.
Balmer.
λ1 λ2 λ3 λ4
A tabela abaixo resume as principais
séries observadas
𝝀𝟏 = 𝟔𝟓𝟔, 𝟐𝒏𝒎 vermelho NOME REGIÃO FÓRMULA
𝝀𝟐 = 𝟒𝟖𝟔, 𝟏𝒏𝒎 azul LYMAN U.V 1 1 1
= 𝑅𝐻 ( 2 − 2 )
𝑛1 = 2,3 𝜆 1 𝑛1
𝟒𝟒𝟎𝒏𝒎
BALMER UV-ViS 1 1
=𝑅 ( − )
1
𝟒𝟏𝟎𝒏𝒎
Violeta
𝐻
𝝀𝟑 = { 𝑛1 = 3,4,5,6 𝜆 22 𝑛12
𝟑𝟗𝟕𝒏𝒎
𝟑𝟖𝟖, 𝟗𝒏𝒎
PASCHEN I.V 1 1 1
= 𝑅𝐻 ( 2 − 2 )
𝑛1 = 4,5,6 𝜆 3 𝑛1
𝝀𝟒 = 𝟑𝟔𝟒, 𝟓𝒏𝒎 Ultra violeta
BRACKETT I.V 1 1 1
= 𝑅𝐻 ( 2 − 2 )
Em 1885, Johann Balmer encontrou uma 𝑛1 = 5,6 𝜆 4 𝑛1
fórmula empírica para determinar o
comprimento de onda no visível das linhas Exemplo 1:
espectrais para o átomo de hidrogênio. Um átomo de Hélio ionizado faz uma
1 1 1
= 𝑅 ( − 2 ) , 𝑛 = 3,4,5,6 transição de um estado 3P para o estado
𝜆 4 𝑛 2S, sendo que as energias são E3P=23,1 eV
Onde 𝑅 = 0,0110𝑛𝑚−1 . e E2S=20,6 eV. Determine o comprimento
A importância da formulação empírica de de onda do fóton.
Balmer é que ele descobriu a regularidade
no espectro. Exemplo 2:
Em 1890, foi obtida pelo físico Sueco Determine todos os comprimentos de onda
Johannes Rydberg um expressão mais possíveis do diagrama de níveis abaixo
geral, interpretando a fórmula de Balmer
como sendo um caso particular desta
expressão mais geral.
n=3 5 eV
1 1 1
= 𝑅𝐻 ( 2 − 2 ) ; 𝑛2 < 𝑛1
𝜆 𝑛2 𝑛1 n=2 3 eV
A introdução do novo índice 𝑛2 < 𝑛1
n=1 0 eV
permitiria descrever outras possíveis
séries de linhas espectrais do hidrogênio,
além do espectro visível 𝑛2 = 2, observada
por Balmer.
Você também pode gostar
- Anatomia Das Valvas CardíacasDocumento28 páginasAnatomia Das Valvas CardíacasRuan Luz100% (1)
- Ecossistemas Amazônicos e Seus ProblemasDocumento92 páginasEcossistemas Amazônicos e Seus ProblemasRuan LuzAinda não há avaliações
- Ecossistemas Amazônicos e Seus ProblemasDocumento92 páginasEcossistemas Amazônicos e Seus ProblemasRuan LuzAinda não há avaliações
- E-Book - CI Encontra BourdieuDocumento469 páginasE-Book - CI Encontra BourdieuKleber Lima100% (3)
- BaladaDocumento59 páginasBaladaRuan LuzAinda não há avaliações
- Ensaio Macrográfico - Infosolda Portal Brasileiro Da SoldagemDocumento5 páginasEnsaio Macrográfico - Infosolda Portal Brasileiro Da SoldagemEduardo de PaulaAinda não há avaliações
- Fisica - Trabalho EI 2 AnoDocumento2 páginasFisica - Trabalho EI 2 AnoSauloNascimentoAinda não há avaliações
- Ficha de Informação de Segurança de Produto Químico: Suvinil Esmalte Premium Cor & Prote Cao Brilhante LaranjaDocumento18 páginasFicha de Informação de Segurança de Produto Químico: Suvinil Esmalte Premium Cor & Prote Cao Brilhante LaranjaDiego ViniciusAinda não há avaliações
- Artigo Hidroxiapatita PDFDocumento5 páginasArtigo Hidroxiapatita PDFJulia M M SantosAinda não há avaliações
- Onc 1fase 9o Ano Nivel A 2017Documento5 páginasOnc 1fase 9o Ano Nivel A 2017Antonio JoséAinda não há avaliações
- Força CentrífugaDocumento3 páginasForça CentrífugaAnonymous yEP1XKvPKAinda não há avaliações
- 1º Ano - 2ºbimestre - QUÍMICADocumento2 páginas1º Ano - 2ºbimestre - QUÍMICAOrlando Oliveira100% (1)
- Lentes 2Documento13 páginasLentes 2Cefas AlmeidaAinda não há avaliações
- Hidrocarbonetos - Alcanos RamificadosDocumento50 páginasHidrocarbonetos - Alcanos RamificadosGustavo HenriqueAinda não há avaliações
- Aeronautica 2010 Afa Aspirante Da Aeronauitca ProvaDocumento21 páginasAeronautica 2010 Afa Aspirante Da Aeronauitca ProvaJvictor SaxAinda não há avaliações
- Aula06 Dipolo EletricoDocumento12 páginasAula06 Dipolo EletricoAline OliveiraAinda não há avaliações
- Trabalho de MetalogeneseDocumento15 páginasTrabalho de MetalogeneseDelito LopesAinda não há avaliações
- AULA 5 Engenharia Quimica Siderurgia 2021Documento74 páginasAULA 5 Engenharia Quimica Siderurgia 2021Iara ChagasAinda não há avaliações
- 8 A SÉRIE 9 o ANO CIÊNCIAS. Caderno Do Aluno Volume 1. Ciências Da Natureza ENSINO FUNDAMENTAL ANOS FINAIS PDFDocumento90 páginas8 A SÉRIE 9 o ANO CIÊNCIAS. Caderno Do Aluno Volume 1. Ciências Da Natureza ENSINO FUNDAMENTAL ANOS FINAIS PDFAngélica dos ReisAinda não há avaliações
- Modulo de Trtac-1Documento85 páginasModulo de Trtac-1vqjmphgp7kAinda não há avaliações
- Gestão de EfluentesDocumento21 páginasGestão de EfluentesArthur VictorAinda não há avaliações
- Filtro Ativo Série Sem Fonte de Tensão Do Lado CC para Compensação de HarmónicosDocumento151 páginasFiltro Ativo Série Sem Fonte de Tensão Do Lado CC para Compensação de HarmónicosjoaoAinda não há avaliações
- Tabela 1: Indicadores Ácido-Base: Indicador Cor Da Forma Ácida Cor Da Forma Básica PH de ViragemDocumento3 páginasTabela 1: Indicadores Ácido-Base: Indicador Cor Da Forma Ácida Cor Da Forma Básica PH de ViragemBeatriz VenturaAinda não há avaliações
- Final - Introdução A Anatomia RadiológicaDocumento5 páginasFinal - Introdução A Anatomia Radiológicaunrealengine25Ainda não há avaliações
- 2º Ano - Sequência - TermoquímicaDocumento9 páginas2º Ano - Sequência - Termoquímicaandre_7_souza501Ainda não há avaliações
- Lista de AtividadeDocumento3 páginasLista de AtividadeGustavo Rossoni RuyAinda não há avaliações
- Enem 2018 NaturezaDocumento15 páginasEnem 2018 NaturezaJACIANE DE 0LIVEIRAAinda não há avaliações
- Análise GravimétricaDocumento5 páginasAnálise GravimétricaJunior FariasAinda não há avaliações
- Termodinâmica I - CAPÍTULO 3Documento31 páginasTermodinâmica I - CAPÍTULO 3Pedro DuarteAinda não há avaliações
- Trabalho Fisica 3 - Principio Da IncertezaDocumento22 páginasTrabalho Fisica 3 - Principio Da IncertezaAngélica Luana LinharesAinda não há avaliações
- 1° Lista CMDocumento4 páginas1° Lista CMValdeci de Pinho Fortes JúniorAinda não há avaliações
- Estequiometria AulaDocumento2 páginasEstequiometria AulagreatinhoAinda não há avaliações
- 6 Sexta Aula Fís Exp I Exercícios Cap 3Documento13 páginas6 Sexta Aula Fís Exp I Exercícios Cap 3Pietra MatosAinda não há avaliações
- BT Esm. Pu Amarelo RK Farben PDFDocumento2 páginasBT Esm. Pu Amarelo RK Farben PDFMuller VendasAinda não há avaliações
- 7451-Acido Glioxilico 50Documento6 páginas7451-Acido Glioxilico 50kitofanecoAinda não há avaliações