Escolar Documentos
Profissional Documentos
Cultura Documentos
Resolução Da Lista de Exercícios de Química Nº 9
Enviado por
João Vitor Santos TostesDescrição original:
Título original
Direitos autorais
Formatos disponíveis
Compartilhar este documento
Compartilhar ou incorporar documento
Você considera este documento útil?
Este conteúdo é inapropriado?
Denunciar este documentoDireitos autorais:
Formatos disponíveis
Resolução Da Lista de Exercícios de Química Nº 9
Enviado por
João Vitor Santos TostesDireitos autorais:
Formatos disponíveis
Nome: _________________________________________________ nº: ________
Bimestre: 2º Ano/série: 3ª série _____ Ensino: Médio
Componente Curricular: Química
Professor: Ricardo Honda
Data: ____ /____ /____
Resolução da Lista de exercícios de Química nº 9
Revisão para a 2ª Avaliação: Princípio de Le Chatelier, Constante de ionização e Lei de Ostwald
01. (UFF 2010) – Considere a reação exotérmica de
formação do trióxido de enxofre, a partir do dióxido:
CO2 + H2O H2CO3
HCO3– + H+
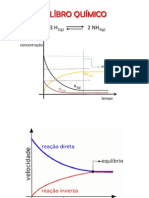
2 SO2 (g) + O2 (g) 2 SO3 (g)
A 900 K, KP = 40,5 e ΔH = –198 kJ. Explique o efeito do aumento de temperatura na
concentração de CO2 dissolvido e no pH do sistema.
a) escreva a expressão de equilíbrio (em função da Com o aumento da temperatura, a concentração de CO2
pressão) para essa reação. no sistema diminui, deslocando o equilíbrio para a
a) KP = pSO32 / (pSO22 · pO2) esquerda. Como consequência, a concentração de H+
b) será o valor da constante de equilíbrio para essa diminui, aumentando o pH do meio.
reação, em temperatura ambiente (300 K), maior, menor
ou igual ao valor da constante de equilíbrio a 900 K? 03. (UNIFESP 2008) – Sob condições experimentais
Justifique sua resposta; adequadas, o gás metano pode ser convertido nos
O valor da constante de equilíbrio a 300 K será maior do gases etano e hidrogênio:
que a 900 K. Essa é uma reação exotérmica. Se
2 CH4 (g) C2H6 (g) + H2 (g)
diminuirmos a temperatura de 900 K para 300 K, o
equilíbrio será deslocado para a direita, liberando calor. Para essa reação, a dependência da constante de
Se mais SO3 é produzido pelo consumo de SO2 e O2, a equilíbrio com a temperatura é dada na tabela.
constante de equilíbrio aumenta.
c) se, enquanto a temperatura é mantida constante, uma Temperatura (K) KC
quantidade a mais de O2, é adicionada ao recipiente que
contém os três gases em estado de equilíbrio, irá o 298 9 × 10–13
número de mols de SO2 aumentar, diminuir ou 400 8 × 10–10
permanecer o mesmo? Justifique sua resposta. 600 6 × 10–7
O número de mols de SO2 irá diminuir. O sistema será
deslocado no sentido de consumir o O 2 adicionado. A reação de conversão do gás metano para etano é
Assim, o equilíbrio é deslocado para direita. O SO 2 será uma reação endotérmica? No sistema em equilíbrio, a
consumido e mais SO3 será formado. concentração de gás metano pode ser aumentada se
houver um aumento de temperatura? Justifique suas
02. (UFRJ 2008) – O gráfico a seguir representa a respostas.
solubilidade de CO2 na água em diferentes A constante de equilíbrio é diretamente proporcional à
temperaturas. concentração dos produtos e, portanto, quanto maior o
valor para essa constante, maior é a concentração de
produtos no equilíbrio. Para a reação indicada, observa-
se que a constante de equilíbrio aumenta conforme a
temperatura sobe, o que indica que a formação dos
produtos é favorecida pelo aumento de temperatura.
Portanto, a conversão de metano a etano é
endotérmica.
04. (UFF 2009) – O processo industrial da síntese da
amônia (NH3) pelo método de Haber envolve a seguinte
reação
N2 (g) + 3 H2 (g) 2 NH3 (g)
Considerando a informação acima, o que acontecerá
com o equilíbrio químico caso a pressão do sistema seja
Após a dissolução, o CO2 reage com a água segundo a duplicada? Justifique sua resposta.
equação:
O aumento da pressão desloca o equilíbrio no sentido com o valor do pH do sangue desse individuo quando
do maior para o menor número de volume de gás. O ele estiver no topo de uma montanha (alta altitude)?
equilíbrio é deslocado para a direita. Justifique sua resposta.
Como o enunciado afirma, em altas altitudes aumenta a
05. (UNIFESP 2010) – O metabolismo humano utiliza frequência respiratória e, consequentemente, há maior
diversos tampões. No plasma sanguíneo, o principal eliminação de gás carbônico, o que faz com que caia
deles é o equilíbrio entre ácido carbônico e íon sua concentração no sangue. Como ocorre diminuição
bicarbonato, representado na equação: de CO2, o equilíbrio equacionado anteriormente é
CO2 (g) + H2O (ℓ) deslocado para a esquerda, já que há retirada de
H2CO3 (aq) H (aq) + HCO3 (aq) produto, e o sistema se desloca de modo a repor parte
+ –
A razão [HCO3–] / [H2CO3] é 20/1. daquilo que foi perdido (Princípio de Le Chatelier).
Considere duas situações: Desse modo há diminuição na concentração de H 3O+ e
I. No indivíduo que se excede na prática de exercícios o sangue fica menos ácido (mais alcalino), ou seja,
físicos, ocorre o acúmulo de ácido lático, que se difunde aumenta o pH sanguíneo.
rapidamente para o sangue, produzindo cansaço e
cãibras. 07. (ENEM 2009) – Sabões são sais de ácidos
II. O aumento da quantidade de ar que ventila os carboxílicos de cadeia longa utilizados com a finalidade
pulmões é conhecido por hiperventilação, que tem como de facilitar, durante processos de lavagem, a remoção
consequência metabólica a hipocapnia, diminuição da de substâncias de baixa solubilidade em água, por
concentração de gás carbônico no sangue. exemplo, óleos e gorduras. A figura a seguir representa
–
a) O que ocorre com a razão [HCO3 ] / [H2CO3] no a estrutura de uma molécula de sabão.
plasma sanguíneo do indivíduo que se excedeu na
prática de exercícios físicos? Justifique. Em solução, os ânions do sabão podem hidrolisar a
A razão [HCO3–]/[H2CO3] no plasma sanguíneo do água e, desse modo, formar o ácido carboxílico
indivíduo que se excedeu na prática de exercícios correspondente. Por exemplo, para o estearato de
físicos tende a diminuir, pois o acúmulo de ácido lático sódio, é estabelecido o seguinte equilíbrio:
desloca o equilíbrio para a esquerda, o que provoca
aumento na concentração de ácido carbônico e CH3(CH2)16COO + H2O
– CH3(CH2)16COOH + OH–
diminuição na concentração de bicarbonato.
Uma vez que o ácido carboxílico formado é pouco
b) O que ocorre com o pH do sangue do indivíduo que
solúvel em água e menos eficiente na remoção de
apresenta hipocapnia? Justifique.
gorduras, o pH do meio deve ser controlado de maneira
A diminuição de gás carbônico, que é um óxido ácido,
a evitar que o equilíbrio acima seja deslocado para a
leva à diminuição da acidez sanguínea, o que acarreta
direita.
aumento do pH do sangue (ou ainda, a diminuição de
Com base nas informações do texto, é correto concluir
gás carbônico faz com que o equilíbrio seja deslocado
+ que os sabões atuam de maneira
para a esquerda, diminuindo a [H ] e,
consequentemente, aumentando o pH do sangue).
a) mais eficiente em pH básico.
06. (UFSCar 2010) – A atmosfera terrestre é constituída b) mais eficiente em pH ácido.
c) mais eficiente em pH neutro.
essencialmente por N2 e O2 gasosos. Com o aumento
d) eficiente em qualquer faixa de pH.
da altitude a pressão parcial e a concentração de O 2 na
e) mais eficiente em pH ácido ou neutro.
atmosfera diminuem. Quando um ser humano está em
Comentário: os sabões serão mais eficientes em meio
altitude elevada, ocorrem várias alterações no seu
básico, pois o aumento da [OH-] faz com que o equilíbrio
organismo para compensar essa diminuição, como, por
seja deslocado para a esquerda.
exemplo, o aumento da velocidade de respiração.
Entretanto, esta alteração na respiração produz também
08. Calcule a concentração em quantidade de matéria
outro efeito, resultando na diminuição da concentração
do ácido sulfídrico, H2S (aq), em uma solução, sabendo-
de CO2 dissolvido no sangue. Sabe-se que o CO2
se que, nessa solução, o ácido apresenta grau de
gerado nos processos metabólicos do organismo e
ionização igual a 0,01% e que a constante de ionização,
removido quase exclusivamente através de um -10
na mesma temperatura, é 7,2 x 10 .
equilíbrio químico que ocorre no sangue, e que é um
dos principais responsáveis pelo controle do seu pH. K = α ∙ ɱ 7,2 ∙ 10 = 0,0001 ∙ ɱ ɱ = 0,072 mol/L
2 -10 2
Esse equilíbrio corresponde a reação, em meio aquoso,
entre o CO2 dissolvido no sangue e a água nele contida, 09. A constante
–10
de ionização de um ácido HA é igual a
produzindo o ânion hidrogenocarbonato e o cátion 3,6 × 10 a 25°C. Calcule:
hidrônio. a) o grau de ionização a 25°C, em solução 0,10mol/L;
K = α2 ∙ ɱ 3,6 ∙ 10-10 = α2 ∙ 0,10 α = 6 ∙ 10-5
a) Escreva a equação química balanceada que b) o grau de ionização a 25°C, em solução 0,0010mol/L.
3,6 ∙ 10-10 = α2 ∙ 0,0010 α = 6 ∙ 10-4
2
representa esse equilíbrio que ocorre no sangue K = α ∙ ɱ
humano.
10. (FGV 2010) – A reação da amônia com a água é
CO2 + 2 H2O HCO3– + H3O+ representada na equação:
b) Sabendo-se que o valor médio do pH sanguíneo de
NH3 (aq) + H2O (l) NH4+ (aq) + OH– (aq)
um individuo normal ao nível do mar é igual a 7,4, e
considerando as informações fornecidas, o que ocorrerá
A constante de equilíbrio a 5 ºC é 1,45 x 10–5 e a 25 ºC
é 1,8 x 10–5.
Considere as seguintes afirmações sobre o sistema em
equilíbrio:
I. a reação química é classificada como reação
exotérmica;
II. o aumento da temperatura resulta em um aumento da
concentração de íons hidroxila;
III. a adição de íons amônio resulta numa redução do pH
do sistema.
São corretas as afirmações
a) I, II e III.
b) I e II, apenas.
c) I e III, apenas.
d) II e III, apenas.
e) III, apenas.
Comentário:
I. Falso, pois um aumento de temperatura provoca um
aumento da constante de equilíbrio, ou seja, o 15. Calcule a concentração hidrogeniônica [H+] existente
aquecimento favorece a reação direta, mas segundo o
em uma solução aquosa 0,01 mol/L de um ácido HX,
princípio de Le Chatelier, aquecimento favorece o
cuja constante de ionização é igual a 9 ⋅ 10–8 a 25 ºC.
sentido endotérmico.
II. Verdadeiro. Como foi discutido na frase anterior, o
aquecimento favorece a reação direta, ou seja, desloca
o equilíbrio químico para a direita fazendo as
concentrações de NH4+ e OH- (hidroxila) aumentarem.
III. Verdadeiro, a adição de íons NH4+ (amônio) faz o
equilíbrio se deslocar para a esquerda, no sentido de
consumir parte desses íons que foram colocados. Com
-
isso diminui a concentração dos íons OH , ou seja, a
solução fica menos alcalina, e o pH diminui.
11. O ácido acetilsalicílico é usado como princípio ativo
em remédios para dores de cabeça. Trata-se de um
monoácido orgânico fraco. Calcule a concentração em
quantidade de matéria de uma solução de ácido
acetilsalicílico que apresenta em determinada
temperatura um grau de dissociação igual a 5,7 x 10 -2.
Dado: O valor de Ki do ácido acetilsalicílico é 3,2 x 10-4.
K = α2 ∙ ɱ 3,2 ∙ 10-4 = 0,0572 ∙ ɱ ɱ = 0,0985 mol/L
12. Um ácido HX apresenta um grau de ionização de
2% em uma solução 1 mol/L. Calcule a sua constante
de ionização.
K = α2 ∙ ɱ K = 0,022 ∙ 1 K = 4 ∙ 10-4.
13. (FEI-SP) – A constante de equilíbrio (Ka) dos ácidos
HA, HB e HC, a 25°C é, respectivamente: 1,8 ⋅ 10–5; 5,7
⋅ 10–8 e 1,8 ⋅ 10–4. Indique a ordem crescente de força
desses ácidos.
HB < HA < HC
14. O ácido acetilsalicílico, mais conhecido como
aspirina, é um ácido orgânico fraco, cuja fórmula será
representada por HAsp. Uma solução aquosa 0,1mol/L
de HAsp apresenta uma concentração de H + igual a
0,004 mol/L. Calcule o Ka da aspirina.
Você também pode gostar
- 2012 - TEmescam - Química - Borges - Deslocamento de EquilíbrioDocumento7 páginas2012 - TEmescam - Química - Borges - Deslocamento de EquilíbrioKlebson Santos da SilvaAinda não há avaliações
- Lista de Exercícios - Deslocamento de EquilíbrioDocumento21 páginasLista de Exercícios - Deslocamento de EquilíbrioAlielson BotelhoAinda não há avaliações
- 82336-Lista de Exercicios de Equilibrio QuimicoDocumento4 páginas82336-Lista de Exercicios de Equilibrio QuimicoYasmin silvaAinda não há avaliações
- 2º ANO - Equilibrio QuimicoDocumento8 páginas2º ANO - Equilibrio Quimicomatheus xexeuAinda não há avaliações
- Lista de Exercícios - Equilíbrio QuímicoDocumento7 páginasLista de Exercícios - Equilíbrio QuímicoIzabelleAinda não há avaliações
- Revisao 2 Serie Quim ADocumento7 páginasRevisao 2 Serie Quim AHenrique CaldasAinda não há avaliações
- Exercícios Deslocamento de EquilíbrioDocumento5 páginasExercícios Deslocamento de EquilíbrioBruna FerreiraAinda não há avaliações
- Cenro Universitário de Sete LagoasDocumento13 páginasCenro Universitário de Sete LagoasElizangela GomesAinda não há avaliações
- Exercícios QuimicaDocumento4 páginasExercícios QuimicaLeonardo PyrrhoAinda não há avaliações
- DF Quimica Ita 5ebbd95959f26Documento7 páginasDF Quimica Ita 5ebbd95959f26Vitor BernardesAinda não há avaliações
- Aula16 Quimica2 ExercíciosDocumento8 páginasAula16 Quimica2 Exercíciosjpturi14Ainda não há avaliações
- Equilíbrio QuímicoDocumento4 páginasEquilíbrio Químicolucas_cmaAinda não há avaliações
- 44.deslocamento de EquilíbrioDocumento23 páginas44.deslocamento de EquilíbrioPaulo VictorAinda não há avaliações
- 410504Documento8 páginas410504anon_312056206Ainda não há avaliações
- 135Documento4 páginas135mailas33Ainda não há avaliações
- Lista de Equilíbrio Químico 22Documento5 páginasLista de Equilíbrio Químico 22TORRES PREPARATÓRIO MILITARAinda não há avaliações
- Segunda Prova de QG - Gabarito - Versão FinalDocumento3 páginasSegunda Prova de QG - Gabarito - Versão FinalThomas JacobsenAinda não há avaliações
- 11quimicapreparaoparaexame11ano 130516092559 Phpapp01 PDFDocumento12 páginas11quimicapreparaoparaexame11ano 130516092559 Phpapp01 PDFanamdAinda não há avaliações
- Fisico Quimica Equilibrio Quimico PDFDocumento20 páginasFisico Quimica Equilibrio Quimico PDFLeonardo PyrrhoAinda não há avaliações
- Fisico Quimica Equilibrio Quimico PDFDocumento20 páginasFisico Quimica Equilibrio Quimico PDFEricson Andre MonteiroAinda não há avaliações
- Equilibrio Quimico 2009Documento47 páginasEquilibrio Quimico 2009Pedro LessaAinda não há avaliações
- Lista Exercicios Deslocamento EquilibrioDocumento2 páginasLista Exercicios Deslocamento EquilibrioRodrigo MacedoAinda não há avaliações
- Equilíbrio QuímicoDocumento2 páginasEquilíbrio QuímicoGerson SilvaAinda não há avaliações
- Equilíbio Químico e Constantes de EquilíbrioDocumento13 páginasEquilíbio Químico e Constantes de EquilíbrioRenato SouzaAinda não há avaliações
- Resolucao Da Lista de Exercicios 8 - Revisao para A 2 Avaliacao - Principio de Le Chatelier - 2 Bimestre 2013 - 3 SeriesDocumento3 páginasResolucao Da Lista de Exercicios 8 - Revisao para A 2 Avaliacao - Principio de Le Chatelier - 2 Bimestre 2013 - 3 SeriesLorran Alves ViannaAinda não há avaliações
- Cap 9 Equilibrio Quimico 2009Documento37 páginasCap 9 Equilibrio Quimico 2009Pedro LessaAinda não há avaliações
- UntitledDocumento4 páginasUntitledGustavo BroedelAinda não há avaliações
- Extensivoenem Química Equilíbrio Químico - KC e KP 12-07-2019Documento9 páginasExtensivoenem Química Equilíbrio Químico - KC e KP 12-07-2019Pedro ManoelAinda não há avaliações
- Livro Equilibrio QuimicoDocumento5 páginasLivro Equilibrio QuimicoNathan Corcino Dos SantosAinda não há avaliações
- Estudo Dirigido - Química - 3° Ano - 1° Bimestre PDFDocumento2 páginasEstudo Dirigido - Química - 3° Ano - 1° Bimestre PDFLaura BeatrizAinda não há avaliações
- Equi Lib Rio CompletoDocumento50 páginasEqui Lib Rio CompletoLeonardo JunglesAinda não há avaliações
- 11quimicapreparaoparaexame11ano 130516092559 Phpapp01Documento12 páginas11quimicapreparaoparaexame11ano 130516092559 Phpapp01malopAinda não há avaliações
- Equilibrios ConstantesDocumento6 páginasEquilibrios ConstantesFred DiasAinda não há avaliações
- 22 TermoquimicaDocumento5 páginas22 TermoquimicaLuma MagnagoAinda não há avaliações
- Lista de Exercícios II - Equilíbrio QuímicoDocumento6 páginasLista de Exercícios II - Equilíbrio QuímicoErenilson SantosAinda não há avaliações
- Cap 8 - Ficha Exercicios-Equilibrio QuimicoDocumento10 páginasCap 8 - Ficha Exercicios-Equilibrio QuimicofersayAinda não há avaliações
- Lista de Exercícios Equilíbrio QuímicoDocumento4 páginasLista de Exercícios Equilíbrio QuímicoSamara CristinyAinda não há avaliações
- Equilíbrio Químico - Já Caiu Na FUVESTDocumento27 páginasEquilíbrio Químico - Já Caiu Na FUVESTpaulo robertoAinda não há avaliações
- Experiência 3 Calor de Reação E Calor de SolidificaçãoDocumento7 páginasExperiência 3 Calor de Reação E Calor de Solidificaçãosocorro silvaAinda não há avaliações
- Deslocamento de Equilibrio Quimica Exercicios GabaritoDocumento29 páginasDeslocamento de Equilibrio Quimica Exercicios GabaritoAdolfo GomesAinda não há avaliações
- FQ - Equilíbrio Químico - Revisão 2019Documento21 páginasFQ - Equilíbrio Químico - Revisão 2019Caio LimmaAinda não há avaliações
- Equilíbrio 388 QuestõesDocumento118 páginasEquilíbrio 388 QuestõesThiago Alonso Rodrigues da Hora100% (2)
- Resolvidas - Equilibrio Quimico IDocumento15 páginasResolvidas - Equilibrio Quimico IMariaAinda não há avaliações
- Gabarito Lista CineticaDocumento3 páginasGabarito Lista CineticasheldonsingAinda não há avaliações
- TeresaDocumento21 páginasTeresaGabriel MattediAinda não há avaliações
- Questionario 02 - Equilibrio Quimico - RESPOSTASDocumento5 páginasQuestionario 02 - Equilibrio Quimico - RESPOSTASmisaelinacioAinda não há avaliações
- Química - Prof. Rafael - Equilíbrio Químico e Deslocamento de EquilíbrioDocumento12 páginasQuímica - Prof. Rafael - Equilíbrio Químico e Deslocamento de EquilíbrioRafael VaristeloAinda não há avaliações
- FichaprinchatDocumento4 páginasFichaprinchatAndrei GalanAinda não há avaliações
- Química Geral 1 e 11Documento71 páginasQuímica Geral 1 e 11Zeferino pedroAinda não há avaliações
- Equilibrio Quimico Questoes ObjetivasDocumento14 páginasEquilibrio Quimico Questoes ObjetivasharoldoalencarAinda não há avaliações
- 5º Teste 3º P 11º A 18-19 v9Documento5 páginas5º Teste 3º P 11º A 18-19 v9sofiaAinda não há avaliações
- Química-2º Trim-2º AnoDocumento8 páginasQuímica-2º Trim-2º AnoThania ArrudaAinda não há avaliações
- A Lei de HessDocumento3 páginasA Lei de HessmarcosFullmetalAinda não há avaliações
- Apostila Química Orgânica: Carbono, Dienos E AromáticosNo EverandApostila Química Orgânica: Carbono, Dienos E AromáticosAinda não há avaliações
- A sociedade do conhecimento e suas tecnologias: estudos em Ciências Exatas e Engenharias - Volume 8No EverandA sociedade do conhecimento e suas tecnologias: estudos em Ciências Exatas e Engenharias - Volume 8Ainda não há avaliações
- Guia de Laboratório Física Experimental AI: Faraday Maxwell AmpereDocumento61 páginasGuia de Laboratório Física Experimental AI: Faraday Maxwell AmpereDaniel MirandaAinda não há avaliações
- A Linguagem VisualDocumento13 páginasA Linguagem VisualJoyceEMarceloDuarteAinda não há avaliações
- Pão de Ló, Bolo Genovês, Receita PetitchefDocumento4 páginasPão de Ló, Bolo Genovês, Receita PetitchefJoanaAinda não há avaliações
- Lista de Exercícios de MULTIPLICAÇÃO E DIVISÃODocumento1 páginaLista de Exercícios de MULTIPLICAÇÃO E DIVISÃOErik Gueiros100% (1)
- 2 - A Importância Da ED Na Vida Do CristãoDocumento4 páginas2 - A Importância Da ED Na Vida Do Cristãocarlos0% (1)
- Beca AprobadaDocumento2 páginasBeca AprobadaKelson MárioAinda não há avaliações
- Características Dos Direitos Humanos RAFADocumento2 páginasCaracterísticas Dos Direitos Humanos RAFAThaiane RibeiroAinda não há avaliações
- Avaliacao NutricionalDocumento4 páginasAvaliacao Nutricionalmagrao80Ainda não há avaliações
- Termo de Compromisso de Estágio - Tce: I IdentificaçãoDocumento3 páginasTermo de Compromisso de Estágio - Tce: I IdentificaçãoLee ToukaAinda não há avaliações
- Detonado God War 2Documento30 páginasDetonado God War 2Márcio BeloAinda não há avaliações
- Slides Da AulaDocumento62 páginasSlides Da AulaICNAinda não há avaliações
- Parnasianismo CsDocumento5 páginasParnasianismo CssaluafayalAinda não há avaliações
- VALIM, Patricia. Mulheres InsurretasDocumento14 páginasVALIM, Patricia. Mulheres InsurretasMarilia AraujoAinda não há avaliações
- Manual Tx417 Tx517Documento39 páginasManual Tx417 Tx517des_mondAinda não há avaliações
- 314-Texto Do Artigo-1294-1-10-20160831Documento40 páginas314-Texto Do Artigo-1294-1-10-20160831Angelo AguirreAinda não há avaliações
- Folha Do PecadoDocumento2 páginasFolha Do PecadoCleide CristinaAinda não há avaliações
- ESCATOLOGIADocumento110 páginasESCATOLOGIAMarcelo Marcos100% (3)
- Teste Séc XiiiDocumento4 páginasTeste Séc XiiiAna Pereira100% (4)
- Linha MelódicaDocumento4 páginasLinha Melódicaoto100% (1)
- Laboratório Emílio Ribas - Exame On-LineDocumento5 páginasLaboratório Emílio Ribas - Exame On-LineVictor Firmino de AraújoAinda não há avaliações
- Como Calcular o Consumo de Energia ElétricaDocumento3 páginasComo Calcular o Consumo de Energia ElétricaWanderson Daiane CarvalhoAinda não há avaliações
- Projeto de ReforçoDocumento3 páginasProjeto de ReforçoAdolpho LisboaAinda não há avaliações
- MEDAUAR, Odete. O Direito Administrativo em Evolução. (P. 23-72)Documento27 páginasMEDAUAR, Odete. O Direito Administrativo em Evolução. (P. 23-72)Jairo OliveiraAinda não há avaliações
- Apr - Retirada de Marimbondo 2023Documento1 páginaApr - Retirada de Marimbondo 2023lerianoAinda não há avaliações
- 100 Histórias Divertidas, Curiosas e Inusitadas Do Futebol AmericanoDocumento14 páginas100 Histórias Divertidas, Curiosas e Inusitadas Do Futebol AmericanoJoão VictorAinda não há avaliações
- 5 - Matematica Financeira e InflacaoDocumento27 páginas5 - Matematica Financeira e InflacaoBruno Soares de CastroAinda não há avaliações
- Poderosa Novena Maria Passa Na FrenteDocumento19 páginasPoderosa Novena Maria Passa Na FrenteMerlen Chiarelotto100% (1)
- Ficha Cadastral PJ - Mo - Dulo Ficha Cadastral Norma - AgrariaDocumento3 páginasFicha Cadastral PJ - Mo - Dulo Ficha Cadastral Norma - AgrariafernandoAinda não há avaliações
- Como Aprendem As CriançasDocumento5 páginasComo Aprendem As CriançasCláudia RosaAinda não há avaliações
- Matematica Do Ensino Basico I Capitulo 03 Introducao As FuncoesDocumento24 páginasMatematica Do Ensino Basico I Capitulo 03 Introducao As Funcoesricardo14231Ainda não há avaliações