Escolar Documentos
Profissional Documentos
Cultura Documentos
QUÍMICA - Resgate
Enviado por
Rodrigues Alves0 notas0% acharam este documento útil (0 voto)
14 visualizações2 páginasDireitos autorais
© © All Rights Reserved
Formatos disponíveis
DOCX, PDF, TXT ou leia online no Scribd
Compartilhar este documento
Compartilhar ou incorporar documento
Você considera este documento útil?
Este conteúdo é inapropriado?
Denunciar este documentoDireitos autorais:
© All Rights Reserved
Formatos disponíveis
Baixe no formato DOCX, PDF, TXT ou leia online no Scribd
0 notas0% acharam este documento útil (0 voto)
14 visualizações2 páginasQUÍMICA - Resgate
Enviado por
Rodrigues AlvesDireitos autorais:
© All Rights Reserved
Formatos disponíveis
Baixe no formato DOCX, PDF, TXT ou leia online no Scribd
Você está na página 1de 2
QUÍMICA – RESGATE
1) Observe a cadeia carbônica do eugenol. Escreva o
número de carbonos primários, secundários e quaternários
que ele possui.
6) Uma das substâncias responsáveis pelo cheiro
agradável de morango pode ser representada de uma
forma simplificada por:
2) Observe a cadeia carbônica abaixo. Como podemos
classifica-la?
Com base na estrutura responda:
a) Quantos átomos de hidrogênio completam corretamente
a estrutura?
b) Escreva sua fórmula molecular.
c) Classifique os carbonos da estrutura abaixo.
7) Uma das substâncias responsáveis pelo mau cheiro das
3) Observe o composto orgânico abaixo e as afirmações a
secreções do gambá tem a seguinte fórmula estrutural:
seu respeito. Classifique-as com V ou F
A cadeia principal dessa substância pode ser classificada
como:
8) (Enem/2013) As moléculas de nanoputians lembram
figuras humanas e foram criadas para estimular o interesse
de jovens na compreensão da linguagem expressa em
( ) É uma cadeia heterogênea fórmulas estruturais, muito usadas em química orgânica.
( ) É uma cadeia ramificada Um exemplo é o NanoKid, representado na figura:
( ) É uma cadeia fechada
( ) Há no total 10 átomos de carbono
4) Observe a estrutura abaixo e responda:
a) Indique a quantidade de átomos de carbono e hidrogênio
b) Classifique todos os átomos de carbono como primários,
secundários, terciários ou quaternários.
5) Uma das substancias responsáveis pelo aroma de rosa é
o 2-feniletanol, cuja estrutura é representada abaixo. a) Em qual parte do NanoKid há carbonos quaternários?
Classifique essa cadeia carbônica: b) Justifique se existe presença de heteroátomo
c) Indique a quantidade de carbonos primários.
9) (Ufac) - Uma reação atinge o equilíbrio químico: e) 1,6 x 10⁻⁴ mol/L
I. Quando não há mais reagentes, somente produtos.
II. Quando as concentrações dos reagentes são iguais às 14) A uma temperatura, a reação 2 HI(g) ⇄ H2(g) + I2(g)
concentrações dos produtos. apresenta as seguintes concentrações no equilíbrio: [HI] =
III. Quando a velocidade da reação direta é igual à 2,2 x 10-2 mol/L [H2] = 1,0 x 10-3 mol/L [I2] = 2,5 x 10-2 mol/L
velocidade da reação inversa. Calcular a constante de equilíbrio, Kc, dessa reação.
IV. Quando as concentrações de reagentes e produtos
tornam-se constantes. 15) a uma dada temperatura 2 mol de H 2 e 1,5 mol de I2
V. Quando não existe mais reação química. foram colocados em um balão de 10 litros estabelecido o
H2(g) + I2(g) ⇄ 2 HI(g) encontra-se no balão 1 mol de HI
As afirmações corretas são: calcular a constante de equilíbrio Kc do sistema.
a) I e II
b) II e III 16) Calcule o pH de uma solução aquosa de um ácido HX
c) III e IV de concentração 0,2 mol/l, cujo Ka = 3,2.10 -4.
d) IV e V
e) III e V 17) Uma solução de HClO apresenta concentração de
ácido igual a 0,2 mol/L. Determine o valor do pH, do pOH e
10) (FAAP – SP) Foi aquecido a 250°C um recipiente de 12 da constante ácida da solução considerando, nas
litros contendo certa quantidade de PCl 5. Sabe-se que, no condições estabelecidas, ácido 0,4% ionizado.
equilíbrio, o recipiente contém 2 mol de PCl 5, 4 mol de PCl3
e 2 mol de Cl2. A constante de equilíbrio, para a 18) 21) Calcule o valor do Kb de uma solução 0,4 mol/L de
dissociação térmica do PCl5, em mol/litro, é: hidróxido de prata (AgOH) cuja base se apresenta 0,5%
dissociada. Determine também pH e pOH.
PCl5(g) → PCl3(g) + Cl2(g)
19) Há dois sistemas gasosos em equilíbrio, cujas
a) 0,4 b) 0,6 c) 2 d) 4 constantes de equilíbrio são dadas pelas expressões (I) e
(II) a seguir:
11) O valor do grau de ionização do ácido HX em uma
solução de concentração 0,4 mol/l cujo Ka = 2,56.10 -5 é
igual a:
a) 0,4% b) 0,6% c) 0,8% d) 8%
12) Determine o valor de Kc no sistema em equilíbrio
Nessas condições, escreva a equação química para cada
quando a concentração de X2 = 20 mol/l; Y2 = 20 mol/l e XY
um dos sistemas em equilíbrio:
= 4 mol/l.
X2 + Y2 ⇆ 2XY. (I) (II)
a) 0,02 b) 0,03 c) 0,04 d) 0,06
20) Um mol de hidrogênio é misturado com um mol de iodo
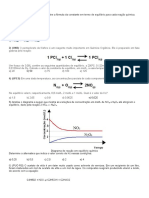
13) A altas temperaturas, N₂, reage com O₂ produzindo num recipiente de um litro a 500°C, no qual se estabelece o
NO, um poluente atmosférico: equilíbrio H2(g) + I2(g) ⇄ 2 HI(g. Se o valor da constante de
equilíbrio (Kc) for 49, a concentração de HI no equilíbrio em
N₂ (g) +O₂(g) ⇄ 2NO (g) mol/litro valerá:
A temperatura de 2000 kelvins, a constante do equilíbrio
acima é igual a 4,0 x 10⁻⁴. Nesta temperatura, se as
concentrações de equilíbrio de N₂ e O₂ forem,
respectivamente, 4,0 x 10⁻³ e 1,0 x 10⁻³ mol/L, qual será a
de NO?
a) 1,6 x 10⁻⁹ mol/L
b) 4,0 x 10⁻⁹ mol/L
c) 1,0 x 10⁻⁵ mol/L
d) 4,0 x 10⁻⁵ mol/L
Você também pode gostar
- Lista de Exerccios 2022Documento18 páginasLista de Exerccios 2022Ralac MajavAinda não há avaliações
- Lista de Exercícios II - Equilíbrio QuímicoDocumento6 páginasLista de Exercícios II - Equilíbrio QuímicoErenilson SantosAinda não há avaliações
- Anhembi 20morumbi 202022 20 - 20medicinaDocumento6 páginasAnhembi 20morumbi 202022 20 - 20medicinaJulia ZanoniAinda não há avaliações
- Lista de Exercícios de Soluções e SolubilidadeDocumento1 páginaLista de Exercícios de Soluções e SolubilidadeCELI ANTONIA DE DEUSAinda não há avaliações
- QuímicaDocumento4 páginasQuímicaflcbAinda não há avaliações
- Química - Prof. Rafael - Equilíbrio Químico e Deslocamento de EquilíbrioDocumento12 páginasQuímica - Prof. Rafael - Equilíbrio Químico e Deslocamento de EquilíbrioRafael VaristeloAinda não há avaliações
- QuiDocumento10 páginasQuiMaria ClaraAinda não há avaliações
- Lista de Exercícios de Química Nº 10: Revisão Dos Principais Tópicos Sobre Equilíbrio Químico Abordados No 1º SemestreDocumento5 páginasLista de Exercícios de Química Nº 10: Revisão Dos Principais Tópicos Sobre Equilíbrio Químico Abordados No 1º SemestreWellington ReisAinda não há avaliações
- Prof. Rafa - Química - Equilíbrio QuímicoDocumento9 páginasProf. Rafa - Química - Equilíbrio QuímicoRafael VaristeloAinda não há avaliações
- Quimica 2010Documento4 páginasQuimica 2010veralucena8224Ainda não há avaliações
- Exercícios CineticaEquilibrioDocumento3 páginasExercícios CineticaEquilibrioVandice75Ainda não há avaliações
- Lista 2Documento2 páginasLista 2Marcilio Santos SilvaAinda não há avaliações
- 1a FichaDocumento4 páginas1a FichaAlexandre DiazAinda não há avaliações
- Lista de Exercícios Equlíbrio QuímicoDocumento2 páginasLista de Exercícios Equlíbrio QuímicoBrandie ThompsonAinda não há avaliações
- Quitec - Aula 5 - Química Tecnológica - EstequiometriaDocumento31 páginasQuitec - Aula 5 - Química Tecnológica - EstequiometriagamalukasAinda não há avaliações
- Alfa - Módulo 43 PDFDocumento31 páginasAlfa - Módulo 43 PDFjparatyAinda não há avaliações
- Lista de Exercícios - Equilíbrio QuímicoDocumento6 páginasLista de Exercícios - Equilíbrio QuímicowalmaedAinda não há avaliações
- 51 20equil C3 ADbrio 20qu C3 ADmico 20ADocumento49 páginas51 20equil C3 ADbrio 20qu C3 ADmico 20AJohn Vieira OliveiraAinda não há avaliações
- CQD - Lista-Livro #39Documento12 páginasCQD - Lista-Livro #39d4ark21Ainda não há avaliações
- Aula 14 - Questões Química IIDocumento3 páginasAula 14 - Questões Química IIestudanteboamorteAinda não há avaliações
- Cálculo Da ConstanteDocumento2 páginasCálculo Da ConstanteArthur FiaminiAinda não há avaliações
- Exercicios Estequio InorganicaDocumento17 páginasExercicios Estequio Inorganicaanon-430322100% (2)
- Exercícios de AplicaçãoDocumento3 páginasExercícios de AplicaçãoDominique NascimentoAinda não há avaliações
- 4a Lista de Exercicios - Equilibrio1Documento2 páginas4a Lista de Exercicios - Equilibrio1Roger GomesAinda não há avaliações
- 4a Lista de Exercicios - EquilibrioDocumento2 páginas4a Lista de Exercicios - EquilibrioSabrina IsabelAinda não há avaliações
- Equilíbrio Químico 3Documento6 páginasEquilíbrio Químico 3Milton LopesAinda não há avaliações
- Exercícios QFL1150Documento9 páginasExercícios QFL1150Renata MullerAinda não há avaliações
- Lista 1 PDFDocumento3 páginasLista 1 PDFThierry RodriguesAinda não há avaliações
- Ficha de Trabalho - Q4Documento4 páginasFicha de Trabalho - Q4Raquel_Daniela100% (1)
- Exercícios de Equilíbrio - Módulo 43Documento31 páginasExercícios de Equilíbrio - Módulo 43frechesAinda não há avaliações
- LISTA DE EXERCI769CIOS To769pico 2Documento3 páginasLISTA DE EXERCI769CIOS To769pico 2Davi Marçal RibeiroAinda não há avaliações
- 1º Lista de Exercícios - Equilibrio 2021-2Documento8 páginas1º Lista de Exercícios - Equilibrio 2021-2bernardo garciaAinda não há avaliações
- Revisão Química 1ºano 2ºbimestreDocumento2 páginasRevisão Química 1ºano 2ºbimestrebernardo bastosAinda não há avaliações
- Revisão de Química 3 MédioDocumento4 páginasRevisão de Química 3 MédioCleilton NascimentoAinda não há avaliações
- 2009 FinalDocumento6 páginas2009 FinaliolaAinda não há avaliações
- Termoquimica - Especifica - 1 - ALUNOSDocumento2 páginasTermoquimica - Especifica - 1 - ALUNOSRaiani gomesAinda não há avaliações
- Medicina Química Termoquímica Mistura Dos Casos Exercícios Específicos 19-07-2018Documento15 páginasMedicina Química Termoquímica Mistura Dos Casos Exercícios Específicos 19-07-2018belinhaAinda não há avaliações
- 2o TRABALHO Ácidos e Bases e Eletroquímica - 2021Documento2 páginas2o TRABALHO Ácidos e Bases e Eletroquímica - 2021Gerald RodriguesAinda não há avaliações
- Lista Sobre Equilíbrio Químico Química Geral PresençaDocumento4 páginasLista Sobre Equilíbrio Químico Química Geral PresençaAriélly RolimAinda não há avaliações
- 11-Gabarito - Quimica DiscursivaDocumento6 páginas11-Gabarito - Quimica DiscursivaMarcosAinda não há avaliações
- Captura de Tela 2022-04-26 À(s) 17.03.23Documento7 páginasCaptura de Tela 2022-04-26 À(s) 17.03.23Marina RodriguesAinda não há avaliações
- EXAME 2ANO QuimicaDocumento3 páginasEXAME 2ANO QuimicaBruna MartinsAinda não há avaliações
- Calculos Das Constantes IntermediarioDocumento2 páginasCalculos Das Constantes Intermediariovmosconta4Ainda não há avaliações
- Calculo-Estequiometrico ExerciciosDocumento13 páginasCalculo-Estequiometrico ExerciciosJúlia Avelar de CastroAinda não há avaliações
- 1 Lista Exercicios Medio 2018Documento5 páginas1 Lista Exercicios Medio 2018Denise Schwantes0% (1)
- Lista de Exercícios - Equilíbrio QuímicoDocumento2 páginasLista de Exercícios - Equilíbrio QuímicoJoão Henrique OzonAinda não há avaliações
- 126 Quimica ITA 89Documento10 páginas126 Quimica ITA 89jbmccavalcantiAinda não há avaliações
- Prova Final em Forma de TrabalhoDocumento5 páginasProva Final em Forma de TrabalhoGabriel VitorAinda não há avaliações
- Resolvidas - Equilibrio Quimico IDocumento15 páginasResolvidas - Equilibrio Quimico IMariaAinda não há avaliações
- Guia de Estudo ACSDocumento9 páginasGuia de Estudo ACSScribdTranslationsAinda não há avaliações
- QUIMDocumento5 páginasQUIMJuma Daude Screed MadeinMoz100% (1)
- 2003 FinalDocumento8 páginas2003 FinaliolaAinda não há avaliações
- Lista Complementar de Exercícios: Ensino Médio 3º AnoDocumento10 páginasLista Complementar de Exercícios: Ensino Médio 3º AnogabezmirandaAinda não há avaliações
- 7 Lista - Equilíbrio IônicoDocumento2 páginas7 Lista - Equilíbrio IônicoClertan Souza Martins de PaulaAinda não há avaliações
- Go Tarefa Semanal 3 Serie e Curso 5e961d9f0ad5fDocumento15 páginasGo Tarefa Semanal 3 Serie e Curso 5e961d9f0ad5fBaptistaAinda não há avaliações
- Exercícios Constante de EquilíbrioDocumento13 páginasExercícios Constante de EquilíbrioPietra LemosAinda não há avaliações
- Estequiometria 1 PDFDocumento5 páginasEstequiometria 1 PDFEwerton LeonardoAinda não há avaliações
- Apostila Química Orgânica: Carbono, Dienos E AromáticosNo EverandApostila Química Orgânica: Carbono, Dienos E AromáticosAinda não há avaliações
- Ácidos e Bases de Brönsted e Lowry: Uma visão aplicada ao meio ambienteNo EverandÁcidos e Bases de Brönsted e Lowry: Uma visão aplicada ao meio ambienteAinda não há avaliações
- Ae q11 Fich Form 2Documento2 páginasAe q11 Fich Form 2carlaAinda não há avaliações
- Princípios Das Principais Provas Bioquímicas BacteriológicasDocumento6 páginasPrincípios Das Principais Provas Bioquímicas BacteriológicasEloi MenezesAinda não há avaliações
- Relatório de Estagio Tec em Quimica - Franciele VenturiniDocumento48 páginasRelatório de Estagio Tec em Quimica - Franciele VenturiniFranciele Venturini BarbosaAinda não há avaliações
- Ácido Linear Alquilbenzeno Sulfônico (LAS) - Revisao - 3Documento8 páginasÁcido Linear Alquilbenzeno Sulfônico (LAS) - Revisao - 3ElidaineAinda não há avaliações
- Aula 7 Introdução A Formulação de Materiais CerâmicosDocumento17 páginasAula 7 Introdução A Formulação de Materiais CerâmicosAdemar Espírito SantoAinda não há avaliações
- Heco B 28Documento3 páginasHeco B 28wetirolesAinda não há avaliações
- Preparação Dos Corpos de Prova para Ensaio MetalográficoDocumento5 páginasPreparação Dos Corpos de Prova para Ensaio MetalográficoJohnMoroniAinda não há avaliações
- Química - Turma 101Documento2 páginasQuímica - Turma 101Tito FerreiraAinda não há avaliações
- Simulação RLCDocumento15 páginasSimulação RLCRoger UnixAinda não há avaliações
- Slides MadeiraDocumento27 páginasSlides MadeiraJonelso Fernandes100% (1)
- Dimensionamento Condutos Livres - ABASTECIMENTODocumento20 páginasDimensionamento Condutos Livres - ABASTECIMENTOSimplícia LuanaAinda não há avaliações
- 15º O Que É OrmusDocumento5 páginas15º O Que É OrmusmarilenaAinda não há avaliações
- WEB Ar at A06Documento20 páginasWEB Ar at A06Albino NunesAinda não há avaliações
- Coifa Lavadora Wash Pull TricapDocumento4 páginasCoifa Lavadora Wash Pull TricapJoaquim PaulinoAinda não há avaliações
- Apostila de MergulhoDocumento10 páginasApostila de MergulhotialililazerAinda não há avaliações
- PROPRIEDADES TÉRMICAS IntroduçãoDocumento14 páginasPROPRIEDADES TÉRMICAS IntroduçãoCandice MartinezAinda não há avaliações
- Gerardo DendocronologiaDocumento0 páginaGerardo DendocronologiaLucas Sousa Neves AndradeAinda não há avaliações
- Acabe Comigo Livro 2 Christina Ross PDFDocumento114 páginasAcabe Comigo Livro 2 Christina Ross PDFIzah57% (7)
- Regulagem 20pressostato PDFDocumento3 páginasRegulagem 20pressostato PDFLuís César MartinsAinda não há avaliações
- Apostila Enologia PDFDocumento26 páginasApostila Enologia PDFFabio Airton BanderoAinda não há avaliações
- Lista 1 AvaliaçãoDocumento5 páginasLista 1 AvaliaçãoAnonymous u6wQm2YXAinda não há avaliações
- Recursos Subsolo II 14-15 - GinaDocumento40 páginasRecursos Subsolo II 14-15 - GinaGina Espenica100% (1)
- Campanha Proteção Das Mãos RevDocumento10 páginasCampanha Proteção Das Mãos RevAdriano Rogerio Santos100% (1)
- Valdo - Princípios Da Climatologia e Hidrologia - D.20231.CDocumento2 páginasValdo - Princípios Da Climatologia e Hidrologia - D.20231.CAna PaulaAinda não há avaliações
- Radiopacidade Dos CIVDocumento5 páginasRadiopacidade Dos CIVMário FerreiraAinda não há avaliações
- Aula 11 - Dissociação e Ionização e Ácidos, Bases e SaisDocumento5 páginasAula 11 - Dissociação e Ionização e Ácidos, Bases e SaisvicfborgesAinda não há avaliações
- Explosivos PrimariosDocumento42 páginasExplosivos PrimariosGabriel NunesAinda não há avaliações
- QUÍMICA. Mudanças de Estado Físico e Densidade ESTADOS FÍSICOS. O Estado Sólido. O Estado Líquido MÓDULO FRENTE. Bernoulli Sistema de EnsinoDocumento12 páginasQUÍMICA. Mudanças de Estado Físico e Densidade ESTADOS FÍSICOS. O Estado Sólido. O Estado Líquido MÓDULO FRENTE. Bernoulli Sistema de EnsinoAdriana Silva100% (1)
- Permissão de Entrada e Trabalho - PET PDFDocumento2 páginasPermissão de Entrada e Trabalho - PET PDFAndréVinícius100% (2)
- 36 Laudo1 PDFDocumento10 páginas36 Laudo1 PDFEderson SouzaAinda não há avaliações