Escolar Documentos
Profissional Documentos
Cultura Documentos
Resposta 1,2 e 5
Resposta 1,2 e 5
Enviado por
Carla Sousa0 notas0% acharam este documento útil (0 voto)
9 visualizações1 páginaO documento descreve duas titulações ácido-base. A primeira determina a concentração de ácido sulfúrico como 0,5M a partir da titulação com NaOH 0,05M. A segunda calcula a concentração de ácido clorídrico como 0,25M a partir da titulação com Mg(OH)2 0,5M no volume de equivalência de 50mL.
Descrição original:
Resposta do livro de fundamentos da matematica
Título original
resposta 1,2 e 5
Direitos autorais
© © All Rights Reserved
Formatos disponíveis
DOCX, PDF, TXT ou leia online no Scribd
Compartilhar este documento
Compartilhar ou incorporar documento
Você considera este documento útil?
Este conteúdo é inapropriado?
Denunciar este documentoO documento descreve duas titulações ácido-base. A primeira determina a concentração de ácido sulfúrico como 0,5M a partir da titulação com NaOH 0,05M. A segunda calcula a concentração de ácido clorídrico como 0,25M a partir da titulação com Mg(OH)2 0,5M no volume de equivalência de 50mL.
Direitos autorais:
© All Rights Reserved
Formatos disponíveis
Baixe no formato DOCX, PDF, TXT ou leia online no Scribd
0 notas0% acharam este documento útil (0 voto)
9 visualizações1 páginaResposta 1,2 e 5
Resposta 1,2 e 5
Enviado por
Carla SousaO documento descreve duas titulações ácido-base. A primeira determina a concentração de ácido sulfúrico como 0,5M a partir da titulação com NaOH 0,05M. A segunda calcula a concentração de ácido clorídrico como 0,25M a partir da titulação com Mg(OH)2 0,5M no volume de equivalência de 50mL.
Direitos autorais:
© All Rights Reserved
Formatos disponíveis
Baixe no formato DOCX, PDF, TXT ou leia online no Scribd
Você está na página 1de 1
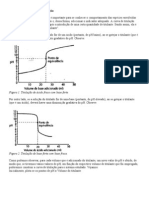
1- Cálculo feito ( está no whatsapp)
No gráfico da titulação apresentado, o salto potenciométrico ocorre no volume de NaOH
de 10 mL, que corresponde a um pH de 7,0.
2- O ponto de equivalência da titulação ocorre no pH 7,0, que é o pH neutro. No ponto de
equivalência o número de mols de ácido sulfúrico (H₂SO₄) é igual ao número de mols de base
(NaOH).
A concentração da solução de NaOH é de 0,05 M, o número de mols de NaOH é igual a:
0,05x20 = 1,0 mol.
Assim, a concentração do analito, que é o ácido sulfúrico é de 1,0 / 2 = 0,5 M.
A concentração do analito será de 0,5 M
5- A questão pede para calcular a concentração do ácido clorídrico (HCl) a partir de uma
titulação com hidróxido de magnésio (Mg(OH)2 a 0,5M.
A curva de titulação mostra que o ponto de equivalência ocorre em um volume de 50 mL de
Mg(OH)2. Nesse ponto, todos os íons H+ do HCl foram neutralizados pelos íons OH- do Mg(OH)2
A partir da equação química da reação temos
HCl + Mg(OH)2 -> MgCl2 + H2O
1 mol de HCl reage com 1 mol de Mg(OH)2.
Portanto, se 50 mL de Mg(OH)2 foram necessários para neutralizar 25 mL de HCl, então a
concentração do HCl é de:
[HCl] = Mg(OH)2 * (V_HCl / V_Mg(OH)2)
[HCl] = 0,5M * (25 mL / 50 mL)
[HCl] = 0,25M
A concentração do ácido clorídrico é de 0,25 mol/L
Uma forma é observar o ponto de equivalência da curva de titulação. Nesse ponto, a
concentração do HCl é igual à concentração da base utilizada na titulação. No caso a
concentração da base é de 0,5M. Portanto, a concentração do HCl também é de 0,5M.
Você também pode gostar
- Operações Com Soluções TitulaçãoDocumento22 páginasOperações Com Soluções TitulaçãoGleison100% (1)
- Gama - Módulo SolucoesDocumento24 páginasGama - Módulo SolucoesAntonio ManuelAinda não há avaliações
- Mistura de Soluções - ExercíciosDocumento2 páginasMistura de Soluções - ExercíciosRandom-songs100% (1)
- Titulação - Módulo 27Documento22 páginasTitulação - Módulo 27Ricardo AlmeidaAinda não há avaliações
- Lista de Exercicios - 01 AnaliticaDocumento3 páginasLista de Exercicios - 01 AnaliticaVitorNoviicAinda não há avaliações
- Lista de Exercícios de Química Analítica IDocumento2 páginasLista de Exercícios de Química Analítica ICaroline BarrosoAinda não há avaliações
- Lista de Exercícios Sobre Mistura de Soluções Com Ocorrência de Reações QuímicasDocumento3 páginasLista de Exercícios Sobre Mistura de Soluções Com Ocorrência de Reações QuímicasEduardo FariaAinda não há avaliações
- Gama - Módulo 27 PDFDocumento22 páginasGama - Módulo 27 PDFThiago Magno Tavares MachadoAinda não há avaliações
- Mistura de Soluções Com Reação Química e TitulaçãoDocumento10 páginasMistura de Soluções Com Reação Química e TitulaçãoCláudio Daniel100% (1)
- Lista de Exercícios 1 - Introdução PDFDocumento3 páginasLista de Exercícios 1 - Introdução PDFBruna FerreiraAinda não há avaliações
- Lista Química OrgânicaDocumento3 páginasLista Química OrgânicaWiliam ColenAinda não há avaliações
- Lista-De-Exercícios-1-2011 Química Analítica PDFDocumento3 páginasLista-De-Exercícios-1-2011 Química Analítica PDFLaysa MaiaAinda não há avaliações
- Construção de Curvas de TitulaçãoDocumento19 páginasConstrução de Curvas de TitulaçãoEliana AlvarengaAinda não há avaliações
- III Lista de Exercícios - CorrigidaDocumento2 páginasIII Lista de Exercícios - CorrigidaRaul Cléverson50% (2)
- Turmadefevereiro-Química-Mistura de Soluções Com Reação Química e Titulação-25-05-2021Documento17 páginasTurmadefevereiro-Química-Mistura de Soluções Com Reação Química e Titulação-25-05-2021raul inacioAinda não há avaliações
- 1a. Lista de Exercicios QAII 2013.1Documento4 páginas1a. Lista de Exercicios QAII 2013.1Luccas X NascimentoAinda não há avaliações
- Resolucao de Exercicios de Acido-BaseDocumento7 páginasResolucao de Exercicios de Acido-BaseviniciusmacielleiteAinda não há avaliações
- Resolucao de Exercicios de Acido-BaseDocumento7 páginasResolucao de Exercicios de Acido-BaseSara e JorgeAinda não há avaliações
- Lista de Exercício Química Analítica Quantitativa PDFDocumento2 páginasLista de Exercício Química Analítica Quantitativa PDFNely Targino67% (3)
- Exercícios Cálculos Titulação ResolvidosDocumento3 páginasExercícios Cálculos Titulação Resolvidoswesley.zanonAinda não há avaliações
- Exercícios Sobre Cálculos Envolvidos Na Titulação. TitulaçãoDocumento3 páginasExercícios Sobre Cálculos Envolvidos Na Titulação. TitulaçãoBoruto A Nova GeraçãoAinda não há avaliações
- Quimica - Analitica QuantoDocumento36 páginasQuimica - Analitica QuantoDih LimaAinda não há avaliações
- RESULTADOS E DISCUSSÕES - Volumetria de NeutralizaçãoDocumento5 páginasRESULTADOS E DISCUSSÕES - Volumetria de NeutralizaçãoGerson Lima100% (1)
- Volumetria Acido-Base 16-04-2022Documento18 páginasVolumetria Acido-Base 16-04-2022Isadora Lima SilvaAinda não há avaliações
- Aprofundamento-química-Mistura de Soluções Com Reação Química e Titulação-05-07-2022Documento12 páginasAprofundamento-química-Mistura de Soluções Com Reação Química e Titulação-05-07-2022Sr. OrthusAinda não há avaliações
- Exercícios de Química Analítica QuantitativaDocumento17 páginasExercícios de Química Analítica QuantitativaMaria Luísa M. Lira100% (1)
- Preparacao e Padronizacao de Solucoes Roteiro 1revisado 2017Documento3 páginasPreparacao e Padronizacao de Solucoes Roteiro 1revisado 2017Tom RibeiroAinda não há avaliações
- Determinação Do Teor de Carbonato e Hidróxido em Uma Amostra de Soda CáusticaDocumento9 páginasDeterminação Do Teor de Carbonato e Hidróxido em Uma Amostra de Soda CáusticaBruen Turazzi100% (1)
- Lista de Exercà - Cios Volum ácido Base PDFDocumento6 páginasLista de Exercà - Cios Volum ácido Base PDFLaila QuaresmaAinda não há avaliações
- Lista 05 PDFDocumento5 páginasLista 05 PDFIlzonRamosAinda não há avaliações
- Equilbrio Exerccios 1226681398676011 9Documento52 páginasEquilbrio Exerccios 1226681398676011 9Carlos CoutoAinda não há avaliações
- Lista de Exercà - Cios - Vol - Acido - BaseDocumento3 páginasLista de Exercà - Cios - Vol - Acido - BaseGEOVANA DE SOUZA ALMEIDAAinda não há avaliações
- Exercícios de Química Analítica QuantitativaDocumento20 páginasExercícios de Química Analítica QuantitativaIsrael NarvastaAinda não há avaliações
- Exercícios Titulação Semana 1Documento1 páginaExercícios Titulação Semana 1João Victor RochaAinda não há avaliações
- Relatório 3Documento7 páginasRelatório 3Milena LimaAinda não há avaliações
- Avaliação2 QuímicaAnalítica EngQuímica GABARITODocumento5 páginasAvaliação2 QuímicaAnalítica EngQuímica GABARITOBruno Carvalho TulmannAinda não há avaliações
- Prova Final em Forma de TrabalhoDocumento5 páginasProva Final em Forma de TrabalhoGabriel VitorAinda não há avaliações
- Determinação Do Teor de MG (OH) 2 em Uma Amostra de Leite de MagnésiaDocumento3 páginasDeterminação Do Teor de MG (OH) 2 em Uma Amostra de Leite de MagnésiaMarcos De Sa MartinsAinda não há avaliações
- LISTA 02 - Volumetria de NeutralizaçãoDocumento5 páginasLISTA 02 - Volumetria de NeutralizaçãoAmanda Matoso VianaAinda não há avaliações
- Relatório - 003Documento9 páginasRelatório - 003Emanuel AmaralAinda não há avaliações
- Química Analitica RetrotitulaçãoDocumento10 páginasQuímica Analitica Retrotitulaçãobiabia3333% (3)
- Relatório 7 - (Volumetria de Precipitação - Volhard)Documento12 páginasRelatório 7 - (Volumetria de Precipitação - Volhard)CleandsonvieiraAinda não há avaliações
- 07 - Quimica Geral Reacoes em Solucoes Aquosas 2, CalculosDocumento36 páginas07 - Quimica Geral Reacoes em Solucoes Aquosas 2, Calculosvanderlanaraujo207Ainda não há avaliações
- Exercicios de Quimica Analitica QuantitativaDocumento21 páginasExercicios de Quimica Analitica QuantitativaSabrina IsabelAinda não há avaliações
- Relatório Quím 3Documento13 páginasRelatório Quím 3Nélio Evandro LemisAinda não há avaliações
- Aula 6 - Físico-Química I - Mistura de Solução Com ReaçãoDocumento12 páginasAula 6 - Físico-Química I - Mistura de Solução Com ReaçãomvfreitasmotaAinda não há avaliações