Escolar Documentos
Profissional Documentos
Cultura Documentos
Liga Coes
Enviado por
Marianne Soares0 notas0% acharam este documento útil (0 voto)
9 visualizações57 páginasDireitos autorais
© © All Rights Reserved
Formatos disponíveis
PPT, PDF, TXT ou leia online no Scribd
Compartilhar este documento
Compartilhar ou incorporar documento
Você considera este documento útil?
Este conteúdo é inapropriado?
Denunciar este documentoDireitos autorais:
© All Rights Reserved
Formatos disponíveis
Baixe no formato PPT, PDF, TXT ou leia online no Scribd
0 notas0% acharam este documento útil (0 voto)
9 visualizações57 páginasLiga Coes
Enviado por
Marianne SoaresDireitos autorais:
© All Rights Reserved
Formatos disponíveis
Baixe no formato PPT, PDF, TXT ou leia online no Scribd
Você está na página 1de 57
GUA AMNIA
Prof. Agamenon Roberto
Se dois tomos combinarem entre si, dizemos
que foi estabelecida entre eles uma
LIGAO QUMICA
Os eltrons mais externos do tomo
so os responsveis pela
ocorrncia da ligao qumica
Prof. Agamenon Roberto
Para ocorrer uma ligao qumica
necessrio que os tomos
percam ou ganhem eltrons, ou, ento,
compartilhem seus eltrons
de sua ltima camada
Na Cl
+
H H
O SDIO PERDEU
ELTRON
O CLORO GANHOU
ELTRON
OS TOMOS DE HIDROGNIO COMPARTILHARAM ELTRONS
Prof. Agamenon Roberto
Na maioria das ligaes, os tomos ligantes possuem
distribuio eletrnica
semelhante de um gs nobre, isto ,
apenas o nvel K, completo, ou, 8 eltrons em
sua ltima camada
Esta idia foi desenvolvida pelos cientistas
Kossel e Lewis
e ficou conhecida como
TEORIA DO OCTETO
Prof. Agamenon Roberto
Um tomo que satisfaz A TEORIA DO OCTETO
estvel e aplicada principalmente
para os elementos do subgrupo A (representativos)
da tabela peridica
H (Z = 1)
He (Z = 2)
F (Z = 9)
Ne (Z = 10)
Na (Z = 11)
1s
1
1s
2
INSTVEL
2s
2
2p
5
1s
2
2s
2
2p
6
1s
2
3s
1
2s
2
2p
6
1s
2
ESTVEL
INSTVEL
ESTVEL
INSTVEL
Prof. Agamenon Roberto
Na maioria das vezes, os tomos que:
Perdem eltrons
so os metais das famlias 1A, 2A e 3A
Recebem eltrons
so ametais das famlias 5A, 6A e 7A
Prof. Agamenon Roberto
01) Os tomos pertencentes famlia dos metais
alcalinos terrosos e dos halognios adquirem
configurao eletrnica de gases nobres quando,
respectivamente, formam ons com nmeros de carga:
a) + 1 e 1.
b) 1 e + 2.
c) + 2 e 1.
d) 2 e 2.
e) + 1 e 2.
ALCALINOS
TERROSOS
HALOGNIOS
FAMLIA 2A
FAMLIA 7A
PERDE
2 ELTRONS
GANHA
1 ELTRONS
+ 2
1
Prof. Agamenon Roberto
02) Um tomo X apresenta 13 prtons e 14 nutrons. A carga
do on estvel formado a partir deste tomo ser:
a) 2.
b) 1.
c) + 1.
d) + 2.
e) + 3.
1s
2
2s
2
2p
6
3s
2
3p
1
LTIMA
CAMADA
3 ELTRONS
PERDE
3 ELTRONS
+ 3
X (Z = 13)
Prof. Agamenon Roberto
LIGAO INICA ou ELETROVALENTE
Esta ligao ocorre devido
ATRAO ELETROSTTICA
entre ons de cargas opostas
Na ligao inica os tomos ligantes apresentam uma
grande
diferena de eletronegatividade ,
isto , um
METAL e o outro AMETAL
Prof. Agamenon Roberto
LIGAO ENTRE O SDIO (Z = 11) E CLORO (Z = 17)
Na (Z = 11) 1s
2
2s
2
2p
6
3s
1
PERDE 1 ELTRON
Cl (Z = 17)
1s
2
2s
2
2p
6
3s
2
3p
5
RECEBE 1 ELTRON
CLORETO DE SDIO
Na Cl
+
Na Cl
+
Prof. Agamenon Roberto
UMA REGRA PRTICA
Para compostos inicos poderemos
usar na obteno da frmula final o
seguinte esquema geral
C A
x y
Prof. Agamenon Roberto
01) A camada mais externa de um elemento X possui 3
eltrons, enquanto a camada mais externa de outro
elemento Y tem 6 eltrons. Uma provvel frmula de
um composto, formado por esses elementos :
a) X
2
Y
3
.
b) X
6
Y.
c) X
3
Y.
d) X
6
Y
3
.
e) XY.
X
Y
perde 3 eltrons
ganha 2 eltrons
X
3+
Y
2
X
Y
2 3
Prof. Agamenon Roberto
02) O composto formado pela combinao do elemento X
(Z = 20) com o elemento Y (Z = 9) provavelmente tem
frmula:
a) XY.
b) XY
2
.
c) X
3
Y.
d) XY
3
.
e) X
2
Y.
X (Z = 20)
4s
2
1s
2
2s
2
2p
6
3s
2
3p
6
Y (Z = 9)
X perde 2 eltrons X
2+
2s
2
2p
5
1s
2
Y
ganha 1 eltron
Y
1
1 2
Y X
Prof. Agamenon Roberto
A principal caracterstica desta ligao o
compartilhamento (formao de pares) de
eltrons entre os dois tomos ligantes
Os tomos que participam da ligao
covalente so
AMETAIS, SEMIMETAIS e o HIDROGNIO
Os pares de eltrons compartilhados so
contados para os dois tomos ligantes
Prof. Agamenon Roberto
quando cada um dos tomos ligantes
contribui com
um eltron para a formao do par
Prof. Agamenon Roberto
Consideremos, como primeiro exemplo, a unio
entre dois tomos do
ELEMENTO HIDROGNIO (H)
para formar a molcula da substncia
SIMPLES HIDROGNIO (H
2
)
H H
H H
FRMULA ELETRNICA
2
H H
FRMULA ESTRUTURAL PLANA
FRMULA MOLECULAR
H (Z = 1) 1s
1
Prof. Agamenon Roberto
Consideremos, como segundo exemplo, a unio entre dois
tomos do ELEMENTO NITROGNIO (N)
para formar a molcula da substncia
SIMPLES NITROGNIO (N
2
)
N (Z = 7)
2s
2
2p
3
1s
2
N N
FRMULA ELETRNICA
N N
FRMULA ESTRUTURAL PLANA
N
2
FRMULA MOLECULAR
Prof. Agamenon Roberto
Consideremos, como terceiro exemplo, a unio
entre dois tomos do ELEMENTO HIDROGNIO e
um tomo do ELEMENTO OXIGNIO para formar a
substncia COMPOSTA GUA (H2O)
H (Z = 1) 1s
1
O (Z = 8)
2s
2
2p
4
1s
2
O
H
H
O
H
H
FRMULA ELETRNICA
FRMULA ESTRUTURAL PLANA
H
2
O
FRMULA MOLECULAR
Prof. Agamenon Roberto
01) Os elementos qumicos N e Cl podem combinar-se
formando a substncia:
Dados: N (Z = 7); Cl (Z = 17)
a) NCl e molecular.
b) NCl
2
e inica.
c) NCl
2
e molecular.
d) NCl
3
e inica.
e) NCl
3
e molecular.
como os dois tomos so AMETAIS a ligao molecular (covalente)
Cl (Z = 17)
1s
2
2s
2
2p
6
3s
2
3p
5
N (Z = 7)
1s
2
2s
2
2p
3
N Cl
Cl
Cl
N Cl
3
Prof. Agamenon Roberto
02) (UESPI) O fosfognio (COCl
2
), um gs incolor, txico, de cheiro penetrante,
utilizado na Primeira Guerra Mundial como gs asfixiante, produzido a
partir da reao:
CO
(g)
+ Cl
2(g)
COCl
2(g)
Sobre a molcula do fosfognio, podemos afirmar que ela apresenta:
a) duas ligaes duplas e duas ligaes simples
b) uma ligao dupla e duas ligaes simples
c) duas ligaes duplas e uma ligao simples
d) uma ligao tripla e uma ligao dupla
e) uma ligao tripla e uma simples
Pg.114
Ex. 02
C O
Cl
Cl
Prof. Agamenon Roberto
03) Observe a estrutura genrica representada abaixo;
Para que o composto esteja corretamente representado, de acordo com as
ligaes qumicas indicadas na estrutura, X dever ser substitudo pelo
seguinte elemento:
a) fsforo
b) enxofre
c) carbono
d) nitrognio
e) cloro
X
H
H
O
O
O C
Prof. Agamenon Roberto
Se apenas um dos tomos contribuir com os dois
eltrons do par, a ligao ser
COVALENTE DATIVA ou COORDENADA
A ligao dativa indicada por uma seta que sai do
tomo que cede os eltrons chegando no tomo que
recebe estes eltrons, atravs do compartilhamento
Prof. Agamenon Roberto
Vamos mostrar a ligao DATIVA, inicialmente, na molcula do
dixido de enxofre (SO2),
onde os tomos de oxignio e enxofre possuem
6 eltrons na camada de valncia
S O
O
S O
O
FRMULA ELETRNICA
FRMULA ESTRUTURAL PLANA
S O
2
FRMULA MOLECULAR
Prof. Agamenon Roberto
01) O gs carbnico (CO2) o principal responsvel pelo efeito estufa, enquanto
o dixido de enxofre (SO2) um dos principais poluentes atmosfricos.
Se considerarmos uma molcula de CO2 e uma molcula de SO2, podemos
afirmar que o nmero total de eltrons compartilhados em cada molcula
respectivamente igual a:
Dados: nmeros atmicos: C = 6; 0 = 8; S = 16.
a) 4 e 3.
b) 2 e 4.
c) 4 e 4.
d) 8 e 4.
e) 8 e 6.
C O
O
O
S O
Prof. Agamenon Roberto
02) Certo tomo pode formar 3 covalncias normais e 1 dativa. Qual
a provvel famlia desse elemento na classificao peridica?
a) 3 A .
b) 4 A .
c) 5 A .
d) 6 A .
e) 7 A .
X
5 A
Prof. Agamenon Roberto
DESOBEDINCIA REGRA DO OCTETO
Hoje so conhecidos compostos que no obedecem
regra do OCTETO
tomos que ficam estveis com menos de 8 eltrons
na camada de valncia
H Be H
O berlio ficou estvel com 4 eltrons
na camada de valncia
H Be H
Prof. Agamenon Roberto
O boro ficou estvel com 6 eltrons
na camada de valncia
B
F
F
F
B
F
F
F
Prof. Agamenon Roberto
tomos que ficam estveis com mais de 8 eltrons
na camada de valncia
S
F
F
F
F
F F
S
F
F
F
F
F F
O enxofre ficou estvel com 12 eltrons
na camada de valncia
Prof. Agamenon Roberto
P
Cl
Cl
Cl
Cl Cl
P
Cl
Cl
Cl
Cl
Cl
O fsforo ficou estvel com 10 eltrons
na camada de valncia
Prof. Agamenon Roberto
tomo que fica estvel com nmero impar de eltrons
na camada de valncia
O nitrognio ficou estvel com 7 eltrons
na camada de valncia.
O N O O N O
Prof. Agamenon Roberto
Compostos dos gases nobres
F Xe F Xe
F F
F F
Recentemente foram produzidos vrios compostos
com os gases nobres
Estes compostos s ocorrem com gases nobres
de tomos grandes, que comportam a camada
expandida de valncia
Prof. Agamenon Roberto
01) (PUC-SP) Qual das seguintes sries contm todos os
compostos covalentes, cuja estabilizao ocorre sem que
atinjam o octeto?
a) BeCl
2
, BF
3
, H
3
BO
3
, PCl
5
.
b) CO, NH
3
, HClO, H
2
SO
3
.
c) CO
2
, NH
4
OH, HClO
2
, H
2
SO
4
.
d) HClO
3
, HNO
3
, H
2
CO
3
, SO
2
.
e) HCl, HNO
3
, HCN, SO
3
.
Prof. Agamenon Roberto
02) (PUC RJ) Observa-se que, exceto o hidrognio, os outros
elementos dos grupos IA a VIIIA da tabela peridica tendem a
formar ligaes qumicas de modo a preencher oito eltrons na
ltima camada. Esta a regra do octeto. Mas, como toda regra
tem exceo, assinale a opo que mostra somente molculas
que no obedecem a esta regra:
BH
3
CH
4
H
2
O HCl XeF
6
I II III IV V
a) I, II e III.
b) II, II e IV.
c) IV e V.
d) I e IV.
e) I e V.
Prof. Agamenon Roberto
A forma geomtrica de uma molcula pode ser
obtida a partir de vrios meios, entre os quais destacamos
as
REGRAS DE HELFERICH,
que podem ser resumidas da seguinte forma:
Prof. Agamenon Roberto
O C O
O
H
H
Estas molculas podem ser LINEARES ou ANGULARES
Se o tomo central A no
possui par de eltrons
disponveis, a molcula
LINEAR
Se o tomo central A
possui um ou mais pares de
eltrons disponveis, a
molcula
ANGULAR
Prof. Agamenon Roberto
B
F
F
F
N
Cl
Cl
Cl
Estas molculas podem ser TRIGONAL PLANA ou PIRAMIDAL
Se o tomo central A
no possui par de eltrons
disponveis a geometria da
molcula ser
TRIGONAL PLANA
Se o tomo central A
possui par de eltrons
disponveis a geometria da
molcula ser
PIRAMIDAL
Prof. Agamenon Roberto
C
Cl
Cl
Cl
Cl
Estas molculas tero uma geometria
TETRADRICA
Prof. Agamenon Roberto
molculas do PCl 5
Estas molculas tero uma geometria
BIPIRMIDE TRIGONAL
Prof. Agamenon Roberto
molculas do SF6
Estas molculas tero uma geometria
OCTADRICA
Prof. Agamenon Roberto
01) Dados os compostos covalentes, com as respectivas estruturas:
I : BeH
2
- linear.
II : CH
4
- tetradrica.
III : H
2
O - linear.
IV : BF
3
- piramidal.
V : NH
3
- trigonal plana.
Pode-se afirmar que esto corretas:
a) apenas I e II.
b) apenas II, IV e V.
c) apenas II, III e IV.
d) apenas I, III e V.
e) todas.
Verdadeiro
Falso
Falso
Verdadeiro
Falso
Prof. Agamenon Roberto
02) As molculas do CH
4
e NH
3
apresentam, as seguintes
respectivamente, as seguintes geometrias:
a) quadrada plana e tetradrica.
b) pirmide trigonal e angular.
c) quadrada plana e triangular plana.
d) pirmide tetragonal e quadrada plana.
e) tetradrica e pirmide triangular.
Estas molculas tero
uma geometria
TETRADRICA
CH4
N
H
H
H
Se o tomo central A
possui par de eltrons
disponveis a
geometria da
molcula ser
PIRAMIDAL
Prof. Agamenon Roberto
Cl H
CLORO
mais eletronegativo que o
HIDROGNIO
d +
d
-
Prof. Agamenon Roberto
H H
Os dois tomos
possuem a mesma
ELETRONEGATIVIDADE
Prof. Agamenon Roberto
A polaridade de uma molcula
que possui mais de dois tomos expressa pelo
VETOR MOMENTO DE DIPOLO RESULTANTE ( )
u
Se ele for NULO, a molcula ser APOLAR;
caso contrrio, POLAR.
Prof. Agamenon Roberto
C O O
A resultante das foras nula
(foras de mesma intensidade, mesma direo
e sentidos opostos)
A molcula do CO
2
APOLAR
Prof. Agamenon Roberto
O
H
H
A resultante das foras
diferente de ZERO
A molcula da gua
POLAR
Prof. Agamenon Roberto
01) Assinale a opo na qual as duas substncias so apolares:
a) NaCl e CCl
4
.
b) HCl e N
2
.
c) H
2
O e O
2
.
d) CH
4
e Cl
2
.
e) CO
2
e HF.
CH
4
e CCl
4
tm geometria TETRADRICA
com todos os ligantes
do carbono iguais, portanto, so
APOLARES
CH4, CCl4,
CO
2
tem geometria LINEAR
com todos os ligantes
do carbono iguais, portanto,
APOLAR
CO2,
N
2
, O
2
e Cl
2
so substncias SIMPLES,
portanto, so
APOLARES
N2, O2, Cl2.
Prof. Agamenon Roberto
02) (UFES) A molcula que apresenta momento dipolar diferente
de zero (molecular polar) :
a) CS
2
.
b) CBr
4
.
c) BCl
3
.
d) BeH
2
.
e) NH
3
.
NH
3
tem geometria
piramidal, portanto, POLAR
Prof. Agamenon Roberto
03) (UFRS) O momento dipolar a medida quantitativa da polaridade de uma
ligao. Em molculas apolares, a resultante dos momentos dipolares
referentes a todas as ligaes apresenta valor igual a zero. Entre as
substncias covalentes abaixo:
I) CH4 II) CS2 III) HBr IV) N2
Quais as que apresentam a resultante do momento dipolar igual a zero?
CH4
Molcula
tetradrica que
so
APOLARES
molculas
LINEARES
com ligantes
iguais so
APOLARES
S C S
Br H
molculas
DIATMICAS
com ligantes
diferentes so
POLARES
N N
molculas
DIATMICAS
com ligantes
iguais so
APOLARES
Prof. Agamenon Roberto
So as ligaes que resultam da interao
ENTRE MOLCULAS, isto ,
mantm unidas molculas de uma substncia
As ligaes INTERMOLECULARES podem ser em:
Dipolo permanente dipolo permanente
Dipolo induzido dipolo induzido ou
foras de disperso de London
Ponte de hidrognio
Prof. Agamenon Roberto
Em uma MOLCULA POLAR sua
extremidade NEGATIVA atrai a extremidade POSITIVA da
molcula vizinha, o mesmo ocorre com sua extremidade positiva
que interage com a parte negativa de outra molcula vizinha
+
+
+
+
+
+
Prof. Agamenon Roberto
Nas molculas APOLARES, uma nuvem
de eltrons se encontra em constante movimento
H H
H H
Se, durante uma frao de segundo, esta nuvem eletrnica
estiver deslocada para um dos extremos da molcula,
pode-se dizer que foi criado um
DIPOLO INDUZIDO,
isto , por um pequeno espao a molcula possui PLOS
Prof. Agamenon Roberto
Um caso extremo de atrao dipolo dipolo ocorre quando
temos o HIDROGNIO ligado a tomos pequenos e
muito eletronegativos, especialmente
o FLOR, o OXIGNIO e o NITROGNIO.
Esta forte atrao chama-se
PONTE DE HIDROGNIO,
sendo verificada nos estados slido e lquido
H
F
H
F
H
F
H
F
Prof. Agamenon Roberto
As pontes de hidrognio so mais intensas que
as foras dipolo dipolo permanente, e estas mais intensas que
as interaes dipolo dipolo induzido
O
H
O
H
O
H
H
O
H
H
O
H
H
H
H
O
H
H
Prof. Agamenon Roberto
01) Compostos de HF, NH
3
e H
2
O apresentam pontos de
fuso e ebulio maiores quando comparados com H
2
S
e HCl, por exemplo, devido s:
a) foras de Van Der Waals.
b) foras de London.
c) pontes de hidrognio.
d) interaes eletrostticas.
e) ligaes inicas.
Prof. Agamenon Roberto
02) (UCDB-DF) O CO
2
no estado slido (gelo seco) passa diretamente
para o estado gasoso em condies ambiente; por outro lado, o
gelo comum derrete nas mesmas condies em gua lquida, a
qual passa para o estado gasoso numa temperatura prxima a
100C. Nas trs mudanas de estados fsicos, respectivamente,
so rompidas:
a) ligaes covalentes, pontes de hidrognio e pontes de
hidrognio.
b) interaes de Van der Waals, ligaes inicas e ligaes
inicas.
c) interaes de Van der Waals, pontes de hidrognio e ligaes
covalentes.
d) interaes de Van der Waals, pontes de hidrognio e pontes
de hidrognio.
e) interaes de Van der Waals, pontes de hidrognio e
interaes de Van der Waals.
Prof. Agamenon Roberto
03) Considere o texto abaixo.
Nos icebergs, as molculas polares da gua associam-se por.................................
No gelo seco, as molculas apolares do dixido de carbono unem-se por
...................................... . Conseqentemente, a 1 atm de presso, possvel
prever que a mudana de estado de agregao do gelo ocorra a uma temperatura
................ do que a do gelo seco.
I
II
III
Para complet-lo corretamente, I, II e III devem ser substitudos,
respectivamente, por:
a) Foras de London, pontes de hidrognio e menor.
b) Pontes de hidrognio, foras de Van der Waals e maior.
c) Foras de Van der Waals, pontes de hidrognio e maior.
d) Foras de Van der Waals, foras de London e menor.
e) Pontes de hidrognio, pontes de hidrognio e maior.
PONTES DE HIDROGNIO
FORAS DE VAN DER WAALS
MAIOR
Prof. Agamenon Roberto
Você também pode gostar
- Divina de Jesus Scarpim - Deus Não Existe e Eu Posso Provar PDFDocumento265 páginasDivina de Jesus Scarpim - Deus Não Existe e Eu Posso Provar PDFLuciano de Oliveira0% (1)
- IFPADocumento7 páginasIFPANelson CardosoAinda não há avaliações
- Preservado para Um PropósitoDocumento8 páginasPreservado para Um Propósitoalanariana2644Ainda não há avaliações
- Material Didatico - Treinamento NR35Documento8 páginasMaterial Didatico - Treinamento NR35FREAKAZOIDEAinda não há avaliações
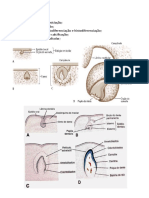
- RESUMO HISTOLOGIA - DentinogeneseDocumento16 páginasRESUMO HISTOLOGIA - DentinogeneseSérgio Henrique Ferreira dos ReisAinda não há avaliações
- Parábolas de Jesus - 2022Documento146 páginasParábolas de Jesus - 2022Hilmar CesarAinda não há avaliações
- Protocolo de Ginecologia Do HC-UFMGDocumento56 páginasProtocolo de Ginecologia Do HC-UFMGSabrina AraújoAinda não há avaliações
- Necessidades Nutricionais Gestantes 2023Documento42 páginasNecessidades Nutricionais Gestantes 2023JuliaAinda não há avaliações
- MP - Sigacom - Importador XMLDocumento10 páginasMP - Sigacom - Importador XMLThaty AnjosAinda não há avaliações
- Apostila Avaliação Psicopedagógica Com Anexos - AtualizadaDocumento32 páginasApostila Avaliação Psicopedagógica Com Anexos - AtualizadaCris Saraiva86% (29)
- Alfred Hitchcock - Historias para Ler No CemiterioDocumento164 páginasAlfred Hitchcock - Historias para Ler No CemiterioMagnoMendesAinda não há avaliações
- 5e - Quintaessência-1Documento101 páginas5e - Quintaessência-1Diego LemosAinda não há avaliações
- (2625) PDFDocumento384 páginas(2625) PDFFabrício SouzaAinda não há avaliações
- Resolution A.960 (23) TraducaoDocumento11 páginasResolution A.960 (23) TraducaoMarco Antonio ToscanoAinda não há avaliações
- Preschool and Kindergarten Behavior Scales - Second Edition (PKBS-2)Documento11 páginasPreschool and Kindergarten Behavior Scales - Second Edition (PKBS-2)Wesley Esdras Santiago100% (1)
- 1.2 Resumo Introdução - AracnídeosDocumento4 páginas1.2 Resumo Introdução - AracnídeosPaloma BaldisseraAinda não há avaliações
- Neomalignas II - 3Documento72 páginasNeomalignas II - 3alessoncavalcanti2013Ainda não há avaliações
- Planificação 11 AnoDocumento4 páginasPlanificação 11 AnoFrederico MarquesAinda não há avaliações
- Estatística e FiabilidadeDocumento54 páginasEstatística e FiabilidadeAnaAinda não há avaliações
- Folder TH Da CTBCDocumento2 páginasFolder TH Da CTBCBruno da CostaAinda não há avaliações
- Lição Completa Tradição e SabedoriaDocumento194 páginasLição Completa Tradição e SabedoriaDaniel GomesAinda não há avaliações
- BG 1944 v1 n11 FevDocumento123 páginasBG 1944 v1 n11 FevCae MartinsAinda não há avaliações
- Chapeuzinho Vermelho - PerraultDocumento103 páginasChapeuzinho Vermelho - PerraultSâmia Sousa100% (1)
- Constitucional - Informativos Importantes STFDocumento48 páginasConstitucional - Informativos Importantes STFRoberta GonçalvesAinda não há avaliações
- Pronomes ÁtonosDocumento14 páginasPronomes ÁtonosElizabeth Palacios chavezAinda não há avaliações
- Fatura Vivo 10-2023Documento3 páginasFatura Vivo 10-2023Paulo FreitasAinda não há avaliações
- Orações Subordinadas AdverbiaisDocumento3 páginasOrações Subordinadas AdverbiaisJéssica Ulbricht100% (3)
- Apostila Vigilante Defesa e ArmamentoDocumento21 páginasApostila Vigilante Defesa e ArmamentoHack Security100% (9)
- Pop Uenc 002Documento12 páginasPop Uenc 002Juliana Coelho100% (1)
- Gileuza - Estágio Supervisionado em Farmácia ComercialDocumento15 páginasGileuza - Estágio Supervisionado em Farmácia ComercialAngelica MartinsAinda não há avaliações