Escolar Documentos
Profissional Documentos
Cultura Documentos
Deslocamento de Equilibrio Quimica Exercicios Gabarito PDF
Deslocamento de Equilibrio Quimica Exercicios Gabarito PDF
Enviado por
Víctor JuliaoTítulo original
Direitos autorais
Formatos disponíveis
Compartilhar este documento
Compartilhar ou incorporar documento
Você considera este documento útil?
Este conteúdo é inapropriado?
Denunciar este documentoDireitos autorais:
Formatos disponíveis
Deslocamento de Equilibrio Quimica Exercicios Gabarito PDF
Deslocamento de Equilibrio Quimica Exercicios Gabarito PDF
Enviado por
Víctor JuliaoDireitos autorais:
Formatos disponíveis
Exerccios sobre Deslocamento de
Equilbrio com Gabarito
1) (Vunesp-2001) No corpo humano, o transporte de
oxignio feito por uma protena chamada hemoglobina.
Cada molcula de hemoglobina contm 4 tomos de ferro.
O transporte de oxignio, dos pulmes para os tecidos,
envolve o equilbrio reversvel:
Mesmo um atleta bem treinado tem seu rendimento fsico Assinale a alternativa que apresenta os sistemas a que o
muito diminudo quando vai competir em localidades de princpio de le Chatelier pode ser aplicado.
altitude muito mais elevada do que a que est habituado. A) I e III.
Aps cerca de duas semanas de treinamento na nova B) I, II e III.
altitude, o rendimento do atleta retorna ao normal. C) I e II.
a) Explique, em termos qumicos, por que o rendimento D) II e III.
fsico inicial do atleta diminui na altitude mais elevada.
b) Explique por que, aps o perodo de adaptao, o
rendimento do atleta retorna ao normal. 4) (Fuvest-1999)
O que ocorre com as reservas originais de ferro do
organismo em conseqncia da adaptao?
2) (Mack-2006) Cientistas descobriram que guas de O esmalte dos dentes , principalmente hidroxiapatita que,
giseres, dentro do Parque Yellowstone (E.U.A.), so sob certas condies, sofre dissoluo (desmineralizao), o
moradia de certos microorganismos. Essas guas, as mais que provoca a crie.
quentes do mundo, so ricas em cido sulfrico. A
descoberta permite supor a existncia de vida em outros Provoca desmineralizao bochechar com
ambientes inspitos, dentro e fora da Terra. I) uma soluo aquosa de hipoclorito de sdio (pH=9);
Considere que, nas guas dos giseres, predomine o II) uma soluo aquosa de cloreto de sdio (soro
equilbrio fisiolgico);
1 III) vinagre diludo em gua.
H1+(aq.) + HSO 4 (aq.) H2SO4(aq.)
e que, numa amostra dessa gua, se tenha verificado que Dessas afirmaes, apenas:
1
[H2SO4] = 0,6mol/L e [HSO 4 ] = 0,2mol/L. O valor da
a) a I correta.
constante de equilbrio, na temperatura em que a
b) a II correta.
experincia foi feita, K = 3,0 101. Assim, o pH da gua c) a III correta.
da amostra analisada d) a I e a II so corretas.
a) 1 e) a II e a III so corretas.
b) 2
c) 3
d) 4 5) (Fuvest-1999) Algumas argilas do solo tm a capacidade
e) 6 de trocar ctions da sua estrutura por ctions de solues
aquosas do solo. A troca inica pode ser representada pelo
3) (UFMG-1999) O princpio de le Chatelier permite prever equilbrio:
os efeitos de perturbaes impostas a sistemas em
equilbrio. R-Na+(s) + NH4+(aq) R-NH4+ (s) + Na+(aq)
O quadro descreve trs sistemas de interesse qumico, bem
como perturbaes impostas a eles. onde R representa parte de uma argila.
Se o solo for regado com uma soluo aquosa de um adubo
contendo NH4NO3, o que ocorre com o equilbrio acima?
a) Desloca-se para o lado do do Na+(aq).
b) Desloca-se para o lado do NH4+(aq).
c) O valor de sua constante aumenta.
d) O valor de sua constante diminui.
e) Permanece inalterado.
1 | Projeto Medicina www.projetomedicina.com.br
uma reao realizada a 400C na presena de um
catalisador? Justifique.
6) (UFSCar-2001) 31. Quando se dissolve cloreto de cobalto
(II) em cido clordrico, HC (aq), ocorre o seguinte
equilbrio:
[Co(H2O)6]2+(aq) + 4 C(aq) [CoC4]2(aq) + 6
H2O() H > 0
rosa azul
temperatura ambiente, a cor dessa soluo violeta.
a) O que acontece com a cor da soluo quando ela
aquecida? Justifique a resposta.
b) O que acontece com a cor da soluo quando se 9) (Vunesp-2001) Leia o seguinte trecho de um dilogo
adiciona mais cido clordrico? Justifique a resposta.
entre Dona Benta e seus netos, extrado de um dos
memorveis livros de Monteiro Lobato, Seres de Dona
Benta:
7) (Mack-2002) ... Toda matria cida tem a propriedade de tornar
vermelho o papel de tornassol.
... A matria bsica no tem gosto cido e nunca faz o
(T constante) papel de tornassol ficar vermelho...
Da reao acima equacionada, pode-se afirmar que o E os sais?
equilbrio: Os sais so o produto da combinao dum cido com
a) desloca-se no sentido 2, se a presso aumentar. uma base. ...
b) desloca-se no sentido 1, se a concentrao do Cl2 E de que cor os sais deixam o tornassol?
aumentar. Sempre da mesma cor. No tm nenhum efeito sobre
c) desloca-se no sentido 1, se for adicionado um catalisador. ele. ...
d) desloca-se no sentido 2, se a concentrao de gs a) Explique como o papel de tornassol fica vermelho em
oxignio diminuir. meio cido, sabendo que o equilbrio para o indicador
e) no se altera, se a presso diminuir. impregnado no papel pode ser representado como:
8) (Unicamp-2000) A revoluo verde, que compreende a
grande utilizao de fertilizantes inorgnicos na agricultura, b) Identifique uma parte do dilogo em que h um conceito
fez surgir a esperana de vida para uma populao mundial qumico errado. Justifique sua resposta.
cada vez mais crescente e, portanto, mais necessitada de
alimentos.
O nitrognio um dos principais constituintes de
fertilizantes sintticos de origem no orgnica. Pode 10) (Unicamp-1994) A reao de transformao do dixido
aparecer na forma de uria, sulfato de amnio, fosfato de de carbono em monxido de carbono, representada pela
amnio etc., produtos cuja produo industrial depende da equao a seguir, muito importante para alguns processos
amnia como reagente inicial. A produo de amnia, por metalrgicos.
sua vez, envolve a reao entre o gs nitrognio e o gs C(s)+CO2(g) 2CO(g) H=174kJ/mol de carbono
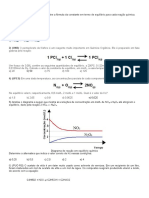
hidrognio. A figura a seguir mostra, aproximadamente, as A constante de equilbrio desta reao pode ser expressa,
porcentagens de amnia em equilbrio com os gases em termos de presses parciais, como: K = p 2(CO)/p(CO2).
nitrognio e hidrognio, na mistura da reao de sntese. Qual o efeito sobre este equilbrio quando:
a)A reao de sntese da amnia um processo a) adiciona-se carbono slido?
endotrmico? Justifique. b) aumenta-se a temperatura?
b)Imagine que uma sntese feita temperatura de 450C e c) introduz-se um catalisador?
presso de 120 atm tenha produzido 50 toneladas de amnia Justifique suas respostas.
at o equilbrio. Se ela tivesse sido feita temperatura de
300C e presso de 100 atm, quantas toneladas a mais de 11) (Unicamp-1997) O processo de dissoluo do oxignio
amnia seriam obtidas? Mostre os clculos. do ar na gua fundamental para a existncia de vida no
c) Na figura, a curva no sinalizada com o valor de planeta. Ele pode ser representado ela seguinte equao
temperatura pode corresponder aos dados de equilbrio para qumica:
O2(g) + H2O(l) = O2(aq); H = -11,7 kJ.mol-1
2 | Projeto Medicina www.projetomedicina.com.br
Observao: o smbolo significa grande quantidade de 16) (UFC-2003) A aplicao do princpio de Le Chatelier
substncia. possibilita o controle da direo e da extenso de uma
a) Considerando que a altitude seja a mesma em que lago determinada reao qumica. Um exemplo tpico o
h mais oxignio dissolvido: em um de guas a 10C ou em equilbrio entre as formas cor de rosa e azul dos ons
outro de guas a 25C? Justifique. cobalto.
b) Considerando uma mesma temperatura, onde h mais [Co(H2O)]2+ (aq) + 4Cl (aq) [CoCl4]2+
oxignio dissolvido, em um lago no alto da cordilheira dos (aq) + 6 H2O (l) ; H = 120cal/mol
Andes ou em outro em sua base? Justifique. cor de rosa azul
Assinale a alternativa que apresenta uma ao sobre o
sistema, que favorece a formao da soluo de cor azul.
12) (Vunesp-1996) Considere o equilbrio que ocorre em A) Diminuio da concentrao de Cl.
fase gasosa a uma certa temperatura: B) Diminuio da temperatura.
SO3 + NOSO2 + NO2 C) Diluio da soluo.
Explique: D) Aumento da concentrao de gua.
a) o efeito no equilbrio provocado pela remoo de NO 2. E) Adio de cloreto de sdio aquoso.
b) por que um aumento de presso sobre o sistema no
influi no equilbrio.
17) (UFSCar-2002) O pH do sangue humano de um
indivduo saudvel situa-se na faixa de 7,35 a 7,45. Para
13) (Vunesp-1996) Em recipiente fechado, temperatura manter essa faixa de pH, o organismo utiliza vrios
constante, ocorre o seguinte equilbrio em fase gasosa: tampes, sendo que o principal tampo do plasma
4NH3 + 3O22N2 + 6H2O sangneo consiste de cido carbnico e on bicarbonato. A
Explique os efeitos que provocam nesse equilbrio: concentrao de ons bicarbonato aproximadamente vinte
a) a adio de N2 gasoso ao recipiente. vezes maior que a concentrao de cido carbnico, com a
b) o aumento da presso sobre o sistema. maior parte do cido na forma de CO2 dissolvido. O
equilbrio qumico desse tampo pode ser representado pela
equao:
14) (UFPE-2002) A solubilidade do dixido de carbono em CO2(g) + H2O(l) H2CO3(aq) H+(aq) + HCO3 (aq)
refrigerantes pode ser representada pelos seguintes
processos: Analise as afirmaes seguintes.
CO2(g) CO2(aq) I. Quando uma pequena quantidade de base entra em
CO2(aq) + H2O(l) H2CO3(aq) contato com uma soluo tampo, os ons hidrxido reagem
H2CO3(aq) HCO3(aq) + H+(aq) Ka = 10-7 com o cido do tampo, no alterando praticamente o pH
Nos refrigerantes o CO2 mantido a presses maiores que a dessa soluo.
atmosfrica, mas aps abertos, a presso entra em equilbrio II. Quando a concentrao de ons bicarbonato no sangue
com a presso atmosfrica, e portanto o pH do refrigerante, aumenta, o pH tambm aumenta.
de acordo com as equaes acima, dever: III. Quando a concentrao de CO2 no sangue aumenta, o
pH diminui.
A) aumentar.
B) diminuir. So corretas as afirmaes:
C) permanecer inalterado. a) I, apenas.
D) tornar-se igual a 107. b) II, apenas.
E) tornar-se igual a 107. c) III, apenas.
d) I e II, apenas.
15) (PUC-MG-2001) A sntese de HI um processo e) I, II e III.
exotrmico que, no equilbrio, pode ser representado pela
equao:
18) (UFPE-2003) O aumento da concentrao de dixido de
H 2( g ) I 2( g ) 2 HI ( g ) carbono na atmosfera tem outras conseqncias alm do
Com relao a esse processo, CORRETO afirmar que: efeito estufa. Analisando-se as principais reaes
envolvidas na formao do esqueleto calcrio dos corais
a) quando abaixarmos a temperatura, o equilbrio (carbonato de clcio),
deslocado para a direita.
b) quando adicionarmos uma pequena quantidade de Ca2+(aq) + CO32-(aq) CaCO3(s)
hidrognio, o equilbrio deslocado para a esquerda. CO32-(aq) + H2O(l) HCO3-(aq) + OH-(aq)
c) quando retirarmos uma parte do iodo, o equilbrio HCO3-(aq) + H2O(l) H2CO3(aq) + OH-(aq)
deslocado para a direita. H2CO3(aq) CO2(g) + H2O(l)
d) quando adicionarmos um catalisador, o equilbrio
deslocado para a direita.
3 | Projeto Medicina www.projetomedicina.com.br
pode-se inferir, a partir do Princpio de Le Chatelier, que o b) Mantidas as demais condies constantes, qual o efeito
aumento da concentrao de dixido de carbono na esperado do aumento da presso sobre a produo do
atmosfera: metanol neste processo? Justifique.
a) causar um aumento na formao do esqueleto dos
corais.
b) causar uma diminuio na formao do esqueleto dos 22) (UFV-2005) A amnia um importante insumo da
corais. indstria de fertilizantes. O processo industrial de sntese
c) no afetar a formao do esqueleto dos corais desse composto, conhecido como Haber-Bosh, baseia-se na
d) aumentar o pH da gua do mar. reao entre o nitrognio e o hidrognio gasosos, como
e) causar um aumento da concentrao de ons hidroxila. representado pela equao:
N2(g) + 3 H2(g) 2 NH3(g) DH = -93 kJ mol-1
Sabendo que, industrialmente, esta sntese realizada na
19) (Vunesp-2004) Uma das substncias responsveis pelo presena de catalisadores e com temperatura e presso
odor desagradvel em banheiros muito utilizados o gs elevadas, assinale a afirmativa INCORRETA relacionada
amnia (NH3), resultante da decomposio da uria com a sntese da amnia.
presente na urina. Este gs dissolvido na gua e reage a) O uso de catalisadores no altera o rendimento da reao.
b) O aumento da temperatura altera a constante de
com ela, produzindo ons amnio (NH 4 ) em soluo.
equilbrio.
a) Escreva a equao qumica para a reao da amnia com
c) O aumento da temperatura e o uso de catalisadores
a gua e informe qual o efeito dessa reao sobre o pH da
aumentam a velocidade da reao.
soluo resultante.
d) O aumento da presso desloca o equilbrio no sentido de
b) Estando disponveis solues aquosas de cido clordrico
formao da amnia.
(HCl), hidrxido de sdio (NaOH) e cloreto de sdio
e) O aumento da presso diminui o rendimento da reao.
(NaCl), qual delas deveria ser utilizada para a diminuio
imediata do odor da amnia? Utilize o Princpio de Le
Chatelier para justificar sua resposta.
23) (Mack-2004) Se, ao equilbrio acima, se adicionar uma
soluo de NaOH,
1
20) (Unicamp-2005) A comunicao que ocorre entre NH 4 (aq.) + OH1 (aq.) NH3(g) + H2O(lq.)
neurnios merece ser destacada. atravs dela que se a) a quantidade de amnia liberada aumenta.
manifestam as nossas sensaes. Dentre as inmeras b) a concentrao do on amnio aumenta.
substncias que participam desse processo, est a 2- c) o pH da soluo em equilbrio diminui.
feniletilamina a qual se atribui o ficar enamorado. d) no h qualquer alterao.
Algumas pessoas acreditam que sua ingesto poderia e) a quantidade de amnia liberada diminui.
estimular o processo do amor mas, de fato, isto no se
verifica. A estrutura da molcula dessa substncia est
abaixo representada. 24) (Mack-2004) Numa churrasqueira, para tornar o carvo
em brasa mais incandescente, hbito abanar ou assoprar o
carvo. Essa prtica funciona bem, pois provoca:
a) o aumento da concentrao de gs nitrognio, que o
reagente principal numa combusto.
a) Considerando que algum ingeriu certa quantidade de 2- b) o aumento da concentrao de gs carbnico, que
feniletilamina, com a inteno de cair de amores, escreva a aumenta a velocidade da reao.
equao que representa o equilbrio cido-base dessa c) a diminuio da concentrao de gs nitrognio,
substncia no estmago. Use frmulas estruturais. favorecendo a combusto do carvo.
b) Em que meio (aquoso) a 2-feniletilamina mais solvel: d) o aumento da concentrao de gs oxignio, que o
bsico, neutro ou cido? Justifique. comburente da reao.
e) o aumento da concentrao de gs oxignio, que o
combustvel da reao.
21) (Vunesp-2005) O metanol um produto com elevada
toxidez, podendo provocar nusea, vmito, perturbao
visual, confuso mental e conduzindo morte em casos
mais graves de intoxicao. Em alguns pases ele 25) (VUNESP-2006) O equilbrio cido bsico do sangue
utilizado como combustvel, em especial em competies pode ser representado como segue:
automobilsticas, e pode ser obtido industrialmente pela CO2 + H2O H2CO3 H+ + HCO 3
reao do monxido de carbono com o hidrognio.
Assinale a alternativa que apresente dois fatores que
a) Escreva a equao qumica para a reao do monxido
combateriam a alcalose respiratria (aumento do pH
de carbono com o hidrognio, produzindo o metanol, e a
sangneo).
expresso para a constante de equilbrio para esta reao no
estado gasoso. A) Aumento da concentrao de CO2 e HCO 3
4 | Projeto Medicina www.projetomedicina.com.br
B) Diminuio da concentrao de CO2 e HCO 3
a) O aumento da presso total aumenta a produo de
C) Diminuio da concentrao de CO2 e aumento da nitrognio.
concentrao de HCO 3 b) A diminuio da presso total aumenta a produo
D) Aumento da concentrao de CO2 e diminuio da de amnia.
c) O aumento da presso total desloca o equilbrio
concentrao de HCO 3 para a direita.
E) Aumento da concentrao de CO2 e diminuio da d) O aumento da presso total desloca o equilbrio
concentrao de H2O. para o lado de maior volume.
e) A presso no exerce nenhuma influncia sobre o
equilbrio da reao.
26) (UNIFESP-2006) Poluentes como xidos de enxofre e de f) A diminuio da presso total desloca o equilbrio
nitrognio presentes na atmosfera formam cidos fortes, para o lado da menor quantidade de mols.
aumentando a acidez da gua da chuva. A chuva cida pode
causar muitos problemas para as plantas, animais, solo,
gua, e tambm s pessoas. O dixido de nitrognio, gs 29) (PUC - PR-2007) Considere a seguinte reao :
castanho, em um recipiente fechado, apresenta-se em 2 SO2 (g) + O2 (g) 2 SO3 (g) + 23,5 kcal
equilbrio qumico com um gs incolor, segundo a equao: Para que o equilbrio possa ser deslocado para a direita
2NO2(g) N2O4(g) poderemos :
Quando esse recipiente colocado em um banho de gua e I. Aumentar a presso
gelo, o gs torna-se incolor. Em relao a esse sistema, so II. Aumentar a temperatura
feitas as seguintes afirmaes: III. Aumentar a concentrao de SO2 (g)
I. A reao no sentido da formao do gs incolor IV. Diminuir a presso
exotrmica. V. Diminuir a temperatura
II. Com o aumento da presso do sistema, a cor castanha Esto corretas as afirmaes:
atenuada. a) I, III e V.
III. Quando o sistema absorve calor, a cor castanha b) I, II e III.
acentuada. c) II, III e IV.
Dentre as afirmaes, as corretas so: d) III, IV e V.
A) I, apenas. e) I, IV e V.
B) III, apenas.
C) I e III, apenas.
D) II e III, apenas. 30) (UFSC-2007)
E) I, II e III. Os catalisadores automotivos so formados por uma
colmia metlica ou cermica, impregnada por uma
27) (UFC-2006) Uma das reaes que podem ocorrer em mistura de paldio-rdio (para veculos a gasolina) ou
uma atmosfera poluda representada pelo equilbrio paldio-molibdnio (para veculos a lcool). Esses
qumico abaixo: dispositivos tm a funo de converter gases nocivos,
2NO (g) + O2 (g) 2NO2 (g) H > 0
dentre eles os xidos de nitrognio (NOx) e o monxido de
carbono (CO), em substncias menos prejudiciais sade
Considerando tratar-se de uma reao simples e elementar,
(CO2 e N2).
analise as afirmativas abaixo e marque aalternativa correta.
Uma das reaes que ocorre nos catalisadores
A) A ordem total da reao 2.
representada pela equao no balanceada:
B) Aumentando-se a presso do sistema, no se altera a
posio do equilbrio.
C) Aumentando-se a temperatura do sistema, o equilbrio
desloca-se para a esquerda. CO(g) + NO(g) CO2(g)
D) A reao de terceira ordem, com relao ao NO, e de + N2(g) H < 0
primeira ordem, com relao ao O2.
E) A reao de segunda ordem, com relao ao NO, e de Considere que num recipiente fechado contendo
primeira ordem, com relao ao O2. inicialmente 3 mol de monxido de carbono e 2 mol de
monxido de nitrognio, o equilbrio foi estabelecido
quando 90% de monxido de nitrognio foi consumido.
28) (UFPB-2006) O estudo da sntese da amnia,
N2 ( g ) + 3H2 ( g ) 2NH3 ( g ) , bem como o seu controle, Com base nas informaes fornecidas e na equao
de fundamental importncia, tendo em vista a crescente balanceada, assinale a(s) proposi-o(es) CORRETA(S).
demanda de fertilizantes base de nitrognio, um nutriente
01. O aumento da temperatura favorece a formao de
essencial ao crescimento dos vegetais.
CO2 e N2.
Com respeito sntese da amnia, correto afirmar:
5 | Projeto Medicina www.projetomedicina.com.br
02. Na reao em questo, o catalisador tem a funo
de alterar a posio do equilbrio.
04. No equilbrio, a quantidade de monxido de
carbono no recipiente de 1,2 mol.
08. A reao favorecida pelo aumento da presso.
16. A expresso da constante de equilbrio, em
termos da concentrao, dada por:
Kc = [CO2]2.[N2]/[CO].[NO]2.
32. A quantidade total de mol de gases, no equilbrio, medida que o gs cloro formado pela perturbao do
igual a 4,1. seguinte equilbrio na fase aquosa Cl- + ClO- + H2O
64. A introduo de N2(g) no equilbrio acarreta uma
Cl2 + 2OH , a fase que contm o hidrocarboneto vai
-
diminuio da concentrao de NO(g).
adquirindo a colorao esverdeada tpica deste halognio.
Considerando que a cada um dos cinco frascos contendo
quantidades idnticas da mesma soluo de hipoclorito de
31) (VUNESP-2008) Dada a reao exotrmica: sdio e de hidrocarboneto lquido, foi adicionada uma das
2 H2O2 (aq) 2 H2O (l) + O2 (g), seguintes solues: cloreto de sdio, hidrxido de sdio,
a alterao que favorece a formao dos produtos a cido actico, cido clordrico e nitrato de amnio, todas
elevao da com as mesmas concentraes molares, haver a maior
a) temperatura. produo de gs cloro no tubo ao qual foi adicionado a
b) presso parcial de O2. soluo de
c) concentrao de H2O. a) Cloreto de sdio.
d) presso. b) Hidrxido de sdio.
e) concentrao de H2O2. c) cido actico.
d) cido clordrico.
e) Nitrato de amnio.
32) (VUNESP-2008) Dois fatores que podem alterar o pH
sanguneo so: a intensidade da respirao (quanto maior a
intensidade, menor o teor de CO2 no sangue) e o teor de
bicarbonato na urina (quanto maior o teor de bicarbonato na 35) (Vunesp-1999)
urina, maior a diminuio de sua concentrao no sangue).
Considerando a equao qumica
CO2(g) + H2O(l) H2CO3(aq) H+(aq) + HCO 3 (aq),
quais os efeitos do aumento da intensidade da respirao e
do aumento do teor em bicarbonato na urina sobre os
valores do pH sangneo?
No estado gasoso, ocorre a reao representada pela
33) (UFC-2009) Considere uma soluo aquosa de cido equao N2 + 3H22NH3
actico, de concentrao qualquer. Com a temperatura
constante, se em determinado volume desta soluo for As porcentagens de converso dos reagentes em NH3, em
adicionado acetato de sdio, ir ocorrer um deslocamento diferentes condies de temperatura e presso, esto
do equilbrio qumico. Com base nessas informaes, resumidas na tabela.
responda o que se pede a seguir.
Em que sentido este equilbrio qumico ser deslocado? a) A reao de sntese da amnia exotrmica ou
Justifique sua resposta ao item A em termos de constante de endotrmica? Justifique a resposta.
equilbrio (Ka).
b) Justifique a relao que existe, a uma dada temperatura,
34) (VUNESP-2010) Uma das etapas finais do tratamento da entre o aumento da presso e a porcentagem de converso
gua envolve o borbulhamento de cloro no efluente para dos reagentes em NH3.
desinfeco. A substncia cloro encontrada como um gs
amarelo-esverdeado a 25 C e 1 atm. Pequenas quantidades
deste gs podem ser geradas em laboratrio de acordo com
o experimento ilustrado: 36) (Fuvest-2002) Galinhas no transpiram e, no vero, a
freqncia de sua respirao aumenta para resfriar seu
corpo. A maior eliminao de gs carbnico, atravs da
respirao, faz com que as cascas de seus ovos, constitudas
principalmente de carbonato de clcio, se tornem mais
finas. Para entender tal fenmeno, considere os seguintes
equilbrios qumicos:
6 | Projeto Medicina www.projetomedicina.com.br
Para que as cascas dos ovos das galinhas no diminuam de
espessura no vero, as galinhas devem ser alimentadas
a) com gua que contenha sal de cozinha.
b) com rao de baixo teor de clcio. 39) (Fuvest-2000)
c) com gua enriquecida de gs carbnico. No sistema aquoso representado acima, existe o seguinte
d) com gua que contenha vinagre. equilbrio qumico:
e) em atmosfera que contenha apenas gs carbnico. Cu2+(aq) + 2I (aq) CuI(s) + 1/2 I2 (s)
Ao balo, foi acrescentado benzeno, que um lquido
incolor, imiscvel com gua, no qual, dentre as espcies do
37) (Vunesp-2002) O esmalte dos dentes formado por equilbrio, somente o iodo muito solvel, conferindo-lhe
hidroxiapatita que, em determinadas condies, pode ser cor vermelha. Como resultado de tal perturbao, aps
dissolvida devido ao equilbrio representado pela equao: agitao e repouso, estabelece-se um novo estado de
Ca10(PO4)6(OH)210Ca2+ + 6PO43- + 2OH- equilbrio. Em relao situao inicial, tm-se agora:
HIDROXIAPATITA a) maior [Cu2+(aq)], maior quantidade de CuI (s), e benzeno
Considere trs pessoas, X, Y e Z, que consomem vermelho.
diariamente os produtos cujos valores de pH esto b) maior [Cu2+(aq)], menor quantidade de CuI (s), e
apresentados na tabela. benzeno incolor.
c) menor [Cu2+(aq)], menor quantidade de CuI (s), e
Pessoas Produtos consumidos pH
benzeno vermelho.
diariamente
d) menor [Cu2+(aq)], menor quantidade de CuI (s), e
X Suco de laranja 3
benzeno incolor.
Y gua com gs 4
e) menor [Cu2+(aq)], maior quantidade de CuI (s), e
Z Leite de magnsia 10 benzeno vermelho.
Considerando somente o efeito do uso continuado destes
trs produtos, ocorrer dissoluo da hidroxiapatita do
40) (Fuvest-2002) O transporte adequado de oxignio para
esmalte dos dentes:
os tecidos de nosso corpo essencial para seu bom
(A) da pessoa X, apenas.
funcionamento. Esse transporte feito atravs de uma
(B) da pessoa Y, apenas.
substncia chamada oxi-hemoglobina, formada pela
(C) das pessoas X e Y, apenas.
combinao de hemoglobina (Hb) e oxignio dissolvidos no
(D) da pessoa Z, apenas.
nosso sangue. Abaixo esto representados, de maneira
(E) das pessoas X e Z, apenas.
simplificada, os equilbrios envolvidos nesse processo: 100
mL de sangue contm por volta de 15 g de hemoglobina e
80 g de gua. Essa massa de hemoglobina (15 g) reage com
38) (Vunesp-2002) Considere os dois sistemas, 1 e 2, cerca de 22,5 mL de oxignio, medidos nas condies
observados por iguais perodos de tempo, em que as partes ambiente de presso e temperatura.
aquosas esto em equilbrio com o ar e com o CO2, Considerando o exposto acima,
respectivamente, temperatura ambiente. So dados os a) calcule a quantidade, em mols, de oxignio que reage
equilbrios: com a massa de hemoglobina contida em 100 mL de
sangue.
b) calcule a massa molar aproximada da hemoglobina.
c) justifique, com base no princpio de Le Chtelier,
aplicado aos equilbrios citados, o fato de o oxignio ser
muito mais solvel no sangue do que na gua.
Dado: volume molar de O2, nas condies ambiente de
CaCO3(s) Ca2+(aq) + CO32(aq) presso e temperatura: 25 L/mol
CO2(g)CO2(aq) + calor
CaCO3(s) + CO2(g) + H2O(l)Ca2+(aq) + 2HCO3(aq) 41) (ITA-2005) A 25C e 1atm, um recipiente aberto contm
a) Explique o motivo pelo qual a solubilizao do carbonato uma soluo aquosa saturada em bicarbonato de sdio em
de clcio no sistema 1 consideravelmente menor do que equilbrio com seu respectivo slido. Este recipiente foi
no sistema 2. aquecido temperatura de ebulio da soluo por 1 hora.
b) Explique por que, se o sistema 2 fosse resfriado, a Considere que o volume de gua perdido por evaporao
quantidade de CaCO3 dissolvida seria maior do que se o foi desprezvel.
sistema fosse mantido temperatura ambiente.
7 | Projeto Medicina www.projetomedicina.com.br
a) Explique, utilizando equaes qumicas, o que ocorre (3) Com o aumento da temperatura, o equilbrio
durante o aquecimento, considerando que ainda se observa alcanado mais rapidamente.
bicarbonato de sdio slido durante todo esse processo. (4) O uso de catalisador no processo propicia um estado de
b) Aps o processo de aquecimento, o contedo do bquer transio energeticamente idntico quele atingido sem o
foi resfriado at 25C. Discuta qual foi a quantidade de uso do mesmo.
slido observada logo aps o resfriamento, em relao
quantidade do mesmo (maior, menor ou igual) antes do
aquecimento. Justifique a sua resposta. 44) (Fuvest-2000) Considere o equilbrio, em fase gasosa,
CO (g) + H2O (g) CO2 (g) + H2 (g)
cuja constante K, temperatura de 430 C, igual a 4.
Em um frasco de 1,0 L, mantido a 430 C, foram
42) (Unifesp-2004) Quando se borbulha Cl2(g) na gua, misturados 1,0 mol de CO, 1,0 mol de H2O, 3,0 mol de CO2
estabelecem-se os seguintes equilbrios: e 3,0 mol de H2. Esperou-se at o equilbrio ser atingido.
Cl2((g) Cl2(aq) a) Em qual sentido, no de formar mais CO ou de consumi-
Cl2(aq) + H2O HClO + H+ + Cl lo, a rapidez da reao maior, at se igualar no equilbrio?
HClO(aq) H+ + ClO Kdissoc = 8 104, a 25C. Justifique.
Analisando-se esses equilbrios, foram feitas as seguintes b) Calcule as concentraes de equilbrio de cada uma das
afirmaes: espcies envolvidas (Lembrete: 4=22).
I. Quanto maior o pH da gua, maior ser a solubilidade do Obs.: Considerou-se que todos os gases envolvidos tm
gs. comportamento de gs ideal.
II. Pode ocorrer desprendimento de Cl2 gasoso se for
adicionado NaCl slido soluo.
III. A constante de dissociao do HClO aumenta se for 45) (Unicamp-2001) Nan responde prontamente; afinal a
adicionado um cido forte soluo, a 25C. danada craque em Qumica. Veja s o experimento e as
Est correto o que se afirma em perguntas que ela prope a Chu:
A) I, apenas. Quando em soluo aquosa, o ction amnio, NH4+ ,
B) II, apenas. dependendo do pH, pode originar cheiro de amnia, em
C) I e II, apenas. intensidades diferentes. Imagine trs tubos de ensaio,
D) II e III, apenas. numerados de 1 a 3, contendo, cada um, pores iguais de
E) I, II e III. uma mesma soluo de NH4Cl. Adiciona-se, no tubo 1 uma
dada quantidade de NaCH3COO e agita-se para que se
dissolva totalmente. No tubo 2, coloca-se a mesma
43) (UnB-2001) No incio do sculo XX, a perspectiva da I quantidade em moles de Na2CO3 e tambm se agita at a
Guerra Mundial gerou uma busca desesperada por dissoluo. Da mesma forma se procede no tubo 3, com a
compostos de nitrognio, uma vez que os nitratos, usados adio de NaHCO3. A hidrlise dos nions considerados
como fertilizantes na agricultura, vinham sendo utilizados pode ser representada pela seguinte equao:
na fabricao de explosivos. Essa demanda esgotou Xn (aq) + H2O(aq) = HX(n 1) (aq) + OH (aq)
rapidamente os depsitos de compostos nitrogenados Os valores das constantes das bases Kb para acetato,
existentes naquela poca. O problema da escassez desses carbonato e bicarbonato so, na seqncia:
compostos foi superado devido ao trabalho do qumico 5,6 1010, 5,6 104 e 2,4 108. A constante Kb da
alemo Fritz Haber, que descobriu um meio econmico amnia 1,8 105.
para aproveitar o gs nitrognio, encontrado em abundncia a) Escreva a equao que representa a liberao de amnia
na atmosfera. Essa descoberta rendeu-lhe o Prmio Nobel a partir de uma soluo aquosa que contm ons amnio.
de Qumica em 1918. O mtodo inventado por Haber, b) Em qual dos tubos de ensaio se percebe cheiro mais
utilizado at os dias atuais, consiste em uma sntese forte de amnia? Justifique.
cataltica de amnia, sob temperatura e presso elevadas, a c) O pH da soluo de cloreto de amnio maior, menor
partir dos gases nitrognio e hidrognio, presentes no ar, ou igual a 7,0? Justifique usando equaes qumicas.
segundo a equao abaixo. Nan, voc est querendo me estourar, mas no vai
N2(g) + 3H2(g) 2NH3(g) conseguir. Lembro-me muito bem das explicaes da nossa
Sabendo que a decomposio de amnia favorecida professora esclarecendo sobre equilbrio em soluo aquosa
termodinamicamente pelo aumento da temperatura, julgue fala Chu.
os itens a seguir, relativos ao processo mencionado no texto
II.
(1) A reao de sntese da amnia pelo processo Haber 46) (Unicamp-2001) Que moleza! Est pensando o qu?
exotrmica. Pergunta a que vou lhe fazer agora! vibra Nan.
(2) A presso elevada, mencionada no texto, utilizada Vamos falar um pouco de respirao.
para deslocar o equilbrio no sentido de formao de Respirao? pergunta Chu. Mas estamos
amnia. estudando Qumica ou Biologia?
8 | Projeto Medicina www.projetomedicina.com.br
Pois , mas os tomos e as molculas no sabem disso, e A) a adio de gs cloro a guas alcalinas pode levar
as reaes qumicas continuam ocorrendo em todos os seres converso indesejada do HOCl em OCl_ .
vivos emenda Nan, continuando: No corpo humano, B) a adio de gs cloro provoca uma diminuio do pH da
por exemplo, o CO2 dos tecidos vai para o sangue e o O2 do gua.
sangue vai para os tecidos. Quando o sangue alcana os C) a condutividade eltrica da gua aumenta aps a adio
pulmes, d-se a troca inversa. O sangue contm, tambm, do Cl2 (g).
substncias que impedem a variao do pH, o que seria D) a formao do HOCl a partir do hipoclorito favorecida
fatal ao indivduo. Mesmo assim, pode ser observada em guas alcalinas.
pequena diferena de pH (da ordem de 0,04) entre o sangue
arterial e o venoso.
a) Utilizando equaes qumicas explique onde se pode 49) (Mack-2001) O principal constituinte dos dentes a
esperar que o pH seja um pouco mais baixo: no sangue hidroxiapatita, cuja destruio acarreta a desmineralizao
arterial ou no venoso? dos dentes. A hidroxiapatita apresenta o seguinte equilbrio:
Puxa! Nessa voc me pegou. Mas vou resolver diz Ca5(PO4)3OH(s) 5Ca2+(aq.) + 3PO43(aq.) + OH1(aq.)
Chu. A fermentao de alimentos, como os carboidratos,
Nan, porm, logo continua: Quando em repouso, aumenta a concentrao de ons H + na boca e, nesse caso, o
liberamos nos pulmes, por minuto, cerca de 200mL de equilbrio:
dixido de carbono oriundo do metabolismo, medida esta a) no se altera.
feita a temperatura ambiente (25C). Voc est comendo b) desloca-se no sentido 2, favorecendo a desmineralizao
po que podemos considerar, numa simplificao, como dos dentes.
sendo apenas um polmero de glicose (C6H12O6). A massa c) desloca-se no sentido 2, aumentando a concentrao de
dessa fatia de aproximadamente 18 gramas. ons OH1.
b) Seguindo esse raciocnio e admitindo, ainda, que a d) desloca-se no sentido 1, favorecendo a desmineralizao
fatia se transforme em CO2 e gua, sendo o dixido de dos dentes.
carbono eliminado totalmente pela respirao, quantos e) desloca-se no sentido 1, diminuindo a concentrao de
minutos sero necessrios para que ela seja queimada ons Ca2+.
no organismo?
50) (UFMG-1999) O princpio de le Chatelier permite prever
os efeitos de perturbaes impostas a sistemas em
equilbrio.
47) (PUC - SP-2000) O processo Haber-Bosch, para a sntese
da amnia, foi desenvolvido no incio desse sculo, sendo O quadro descreve trs sistemas de interesse qumico, bem
largamente utilizado hoje em dia. Nesse processo, a mistura como perturbaes impostas a eles.
de nitrognio e hidrognio gasosos submetida a elevada
presso, na presena de catalisadores em temperatura de SISTEMA DESCRIO PERTURBAO
450 C. A reao pode ser representada a seguir: I gua e vapor, a 100 oC e Aumento da
N2(g) + 3 H2(g) 2 NH3(g) H= -100 kJ/mol presso constante, no presso interna
Com relao ao processo Haber-Bosch incorreto afirmar interior de uma panela de
que: presso fechada
a) a alta temperatura tem como objetivo aumentar a
concentrao de amnia obtida no equilbrio. II Soluo saturada de sal em Adio de mais
b) o uso do catalisador e a alta temperatura permitem que a gua, em contato com gua
reao ocorra em uma velocidade economicamente vivel. excesso de sal slido
c) a alta presso desloca o equilbrio no sentido de produzir
mais amnia. III Oxidao de ferro Aumento da
d) o catalisador no influi na concentrao final de amnia metlico pelo oxignio do temperatura
obtida aps atingido o equilbrio. ar em um recipiente aberto
e) para separar a amnia dos reagentes resfriam-se os gases,
obtendo amnia lquida a 33 C, retornando o H2 e o N2
que no reagiram, para a cmara de reao. Assinale a alternativa que apresenta os sistemas a que o
princpio de le Chatelier pode ser aplicado.
48) (UFMG-2001) concentrada, normalmente, o HOCl
gerado, no momento do uso, por meio de uma das seguintes A) I e III.
reaes:
B) I , II e III.
C) I e II.
Com relao a esses processos, INCORRETO afirmar
que: D) II e III.
9 | Projeto Medicina www.projetomedicina.com.br
51) (UFRN-1997) O equilbrio qumico entre os gases N2O4 lado, o CO2 em soluo fica em equilbrio com o CO2 no
(incolor) e NO2 (castanho avermelhado) utilizado em solubilizado, como representado a seguir:
experimentos com objetivo didtico, por causa das
mudanas de cor que ocorrem quando se aplicam sobre o CO2(g) CO2(aq) H = -14,8kJ/mol de CO2
sistema variaes de temperatura ou presso.
A equao qumica que representa o equilbrio, com a a) Suponha que a gerao de espuma esteja relacionada
respectiva variao de entalpia (H) : quantidade de gs liberado durante a abertura da garrafa de
N2O4(g) 2NO2(g) ; H = + 57,2 kJ/mol cerveja.
1. Calcule a constante de equilbrio, Kc, considerando-se Se duas cervejas so abertas no mesmo bar, uma a 6 C e
que, a determinada temperatura, as concentraes de outra a 25 C, qual apresentar a maior quantidade de
equilbrio so iguais a 0,12 mol/L para o NO2 e 0,04 mol/L espuma? Justifique sua resposta.
para o N2O4
2. Explique o que ocorre com o equilbrio quando se aplica b) Explique por que o CO2, em soluo aquosa, pode ser
aumento de temperatura sobre o sistema. considerado um cido.
52) (UFPE-2002) Em meio bsico, alguns ctions metlicos 56) (UFRJ-1999) Observe a reao qumica:
precipitam na forma de hidrxidos gelatinosos, que so
usados para adsorver impurezas slidas e posteriormente 2 NO2 (g) N 2O4(g)
decant-las, ajudando a purificar a gua. Um desses ctions reagente produto
metlicos o alumnio, cuja formao inicial de flocos
pode ser descrita pela seguinte equao qumica: O grfico de concentrao versus tempo a seguir apresenta
Al2(SO4)3(s) + 6 OH (aq) 2 Al(OH)3(s) + 3 SO42(aq) alteraes na concentrao das substncias NO2 e N2O4 a
Para que este processo seja eficiente, o equilbrio deve ser presso constante. O diagrama auxiliar de temperatura
deslocado em direo aos produtos, o que pode ser versus tempo permite analisar a dinmica da reao
realizado atravs: apresentada; observe que a reao se d a uma temperatura
de 80 C no intervalo de tempo de t0 a t4 e de 120 C entre
A) da adio de cido clordrico. t6 e t.
B) da adio de sulfato de sdio.
C) do aumento da presso externa.
D) da adio de cloreto de potssio.
E) da adio de hidrxido de sdio.
53) (Mack-2002) N2(g) + 3H2(g) 2NH3(g)
O rendimento da reao de obteno da amnia diminui, se
a:
a) presso do sistema diminuir.
b) concentrao do gs nitrognio aumentar.
c) concentrao do gs hidrognio aumentar.
d) temperatura do sistema diminuir.
e) presso do sistema aumentar.
H = 26,0 kcal
54) (UFRN-1997) Para a reao A + B C + D, em que
H = 2,40 kJ.mol-1, a alternativa que leva diminuio do
produto C :
a) retirada de D do meio reacional.
b) adio de A.
c) adio de B. a) Calcule a constante de equilbrio (Kc) da reao a 80 C.
d) aumento da temperatura.
e) diminuio da temperatura. b) Analisando o comportamento do sistema entre t4 e t5
explique por que a reao qumica representada
exotrmica.
55) (UFRJ-1999) Na fabricao de cerveja, adiciona-se gs
carbnico durante o processo de engarrafamento (parte do
CO2 j produzido durante a fermentao). Isto faz com
que o produto final apresente uma acidez maior. Por outro
10 | Projeto Medicina www.projetomedicina.com.br
57) (PUC - SP-2003) O grfico abaixo correlaciona os representa o equilbrio envolvido neste sistema, o aumento
valores da constante de equilbrio (KC) em funo da da concentrao de ons hidrogenocarbonato produz
temperatura para a reao de sntese da amnia: elevao da acidez. Admita que apenas elevados valores de
pH acarretem a degradao do ovo.
Considere uma cmara de armazenamento de ovos que
possibilita o controle da composio da atmosfera em seu
interior. Com base na equao de equilbrio, indique a
condio atmosfrica na qual a cmara deve ser regulada
para maximizar a conservao dos ovos. Justifique sua
resposta.
60) (Fuvest-2003) Cobalto pode ser obtido a partir de seu
Sobre o comportamento dessa reao, no intervalo de
xido, por reduo com hidrognio ou com monxido de
temperatura considerado no experimento, foram feitas
carbono. So dadas as equaes representativas dos
algumas afirmaes:
equilbrios e suas respectivas constantes a
I. A reao exotrmica no sentido de formao da amnia.
550 C.
II. Com o aumento da temperatura, a velocidade da reao
I. CoO(s) + H2(g) Co(s) + H2O(g) K1 = 67
diminui.
II. CoO(s) + CO(g) Co(s) + CO2(g) K2 = 490
III. Com o aumento da temperatura, o rendimento da reao
a) Mostre como se pode obter a constante (K3) do
diminui, formando-se menos amnia na situao de
equilbrio representado por
equilbrio.
CO(g) + H2O(g) CO2(g) + H2(g) a 550 C, a partir das
SOMENTE est correto o que se afirma em
constantes dos equilbrios I e II.
A) I.
b) Um dos processos industriais de obteno de hidrognio
B) II.
est representado no item a. A 550 C,
C) III.
a reao, no sentido da formao de hidrognio,
D) I e II.
exotrmica. Para este processo, discuta a influncia de cada
E) I e III.
um dos seguintes fatores:
aumento de temperatura.
58) (Vunesp-2003) O hipoclorito ClO pode ser uso de catalisador.
preparado pela reao representada pela seguinte equao: variao da presso.
Cl2(aq) + 2OH(aq) ClO(aq) + Cl(aq) + H2O(l)
61) (Unicamp-2003) ons como Cu2+, Fe3+ e Fe2+, presentes
em certos alimentos, como por exemplo maionese, podem
causar a sua deteriorao atravs da formao de perxidos.
Para evitar este problema, em alguns alimentos
industrializados pode ser adicionada uma substncia que
complexa (reage com) estes ons, impedindo a sua ao.
Esta substncia, genericamente conhecida como EDTA,
Considerando, ainda, as informaes constantes na tabela, adicionada na forma de seu sal de sdio e clcio.
qual substncia, ao ser adicionada ao sistema, aumentar o A reao que ocorre entre os ons indesejveis e o
rendimento da reao? EDTA adicionado pode ser representada pela equao:
a) HCl.
b) AgNO3. Ca EDTA2 + Men+ = Me EDTAn 4 + Ca2+
c) AgCl. Os valores dos logaritmos das constantes de equilbrio para
d) KNO3. as reaes de complexao desses ons com EDTA so:
e) KCl.
59) (UERJ-2003) A clara do ovo de galinha um sistema
complexo, contendo protenas, sais e gases dissolvidos em
soluo aquosa. Para uma boa conservao do ovo, faz-se
necessrio manter seu pH prximo neutralidade.
Entretanto, devido porosidade da casca, ocorrem trocas
gasosas com a atmosfera externa ao ovo, o que pode levar a
alteraes do pH. Na equao qumica a seguir, que
11 | Projeto Medicina www.projetomedicina.com.br
D) reduo do consumo de CO2 e aumento do consumo de
a) Qual dos ons Men+ ser removido com mais eficincia? H2O.
Justifique. E) aumento da energia de ativao da reao.
b) Escreva a equao qumica que representa a reao entre
CaEDTA2 e o on escolhido no item a da questo.
65) (UFSCar-2004) A gua contendo ons como Ca2+, HCO
62) (UEL-2003) Uma parte do CO2 formado durante o 2
3 e CO 3 , em concentraes elevadas, conhecida como
processo da respirao dissolve-se no sangue e um dos
componentes responsveis pela constncia de seu pH. gua dura. A presena desses ons pode no ser prejudicial
Entretanto, a perda ou o acmulo excessivo de CO2 no sade, mas torna a gua imprpria para muitos usos
sangue pode provocar uma pequena variao em seu pH. domsticos e industriais. Para remoo do excesso de Ca2+,
Considere, a uma dada temperatura, a seguinte reao e a pode-se tratar a gua dura em tanques de decantao, de
sua respectiva constante de equilbrio: acordo com os equilbrios representados pelas equaes:
Ca2+(aq) + 2HCO 3 (aq) CaCO3(s) +
Com base nessas informaes, correto afirmar: CO2(g) + H2O(l)
a) A constante de equilbrio varia com a concentrao de CO2(g) + 2H2O(l) HCO
gua. +
3 (aq) + H3O (aq)
b) Ao aumentar o pH do meio, a reao deslocada para a
esquerda.
c) O acmulo excessivo de CO2 diminui o pH. a) O que acontece se, aps o tratamento da gua dura, for
d) No instante em que diminuir o pH do meio, o valor de K adicionada soluo de HNO3 ao tanque de decantao?
aumenta. Justifique sua resposta.
e) O excesso de HCO3 provoca uma diminuio de pH. b) O que acontece se, durante o tratamento da gua dura,
for adicionada soluo de NaOH? Justifique sua resposta.
63) (UEL-2003) Os clculos renais, popularmente 66) (FGV-2004) O gs castanho NO2 um poluente
conhecidos como pedras nos rins, contm com freqncia atmosfrico que em recipiente fechado sofre dimerizao,
compostos de oxalato de clcio (CaC2O4(s)) ou fosfato de formando o gs incolor N2O4. A reao de dimerizao
clcio (Ca3(PO4)2(s)). A formao desses compostos pode representada pela seguinte equao de equilbrio
ser representada pelas seguintes equaes qumicas: 2 NO2(g) N2O4(g) + 58 kJ
castanho incolor
Ca2+(aq) + C2O42-(aq) CaC2O4(s)
3 Ca2+(aq) + 2 PO43-(aq) Ca3(PO4)2(s) Sobre o sistema em equilbrio, correto afirmar que
a) a cor castanha ser intensificada com o aumento da
De acordo com as reaes representadas, espera-se que
ocorra formao desses precipitados: temperatura do sistema.
a) Sempre que a concentrao dos ons de clcio ultrapassar b) o sistema em equilbrio insensvel variao de
a concentrao dos ons de oxalato ou fosfato. presso que atua sobre ele.
b) Todas as vezes que a concentrao dos ons de clcio for c) a retirada de NO2 do equilbrio, atravs de sua reao
menor que a concentrao dos ons de oxalato ou fosfato. com gua lquida introduzida no sistema, aumentar a
produo de N2O4.
c) Quando o produto inico das concentraes dos ons de
clcio e oxalato ou fosfato for menor que o produto de d) a constante de equilbrio Kp, expressa em termos das
solubilidade dos compostos correspondentes. presses parciais dos gases, tem valor numrico idntico
d) Quando o produto inico das concentraes dos ons de da constante de equilbrio Kc, expressa em termos de suas
clcio e oxalato ou fosfato for maior que o produto de concentraes molares.
solubilidade dos compostos correspondentes. e) a adio de um catalisador ao sistema, inicialmente em
equilbrio, aumentar a massa de N2O4 produzida.
e) Quando o produto inico das concentraes dos ons de
clcio e oxalato ou fosfato for igual ao produto de
solubilidade dos compostos correspondentes.
67) (FGV-2005) A gua dura no adequada para usos
domsticos e industriais. Uma das maneiras para remoo
64) (Vunesp-2000) A formao de glicose envolve o do excesso de Ca2+ consiste em tratar a gua dura em
equilbrio: tanques de decantao, envolvendo os equilbrios
6CO2(g) + 6H2O () C6H12O6(s) + 6O2(g) representados pelas equaes:
glicose Ca2+(aq) + 2HCO3 (aq) CaCO3(s) + CO2(g) + H2O(l)
temperatura constante, a remoo de O2(g) provoca: CO2(g) + 2H2O(l) HCO3(aq) + H3O+(aq)
Trs solues so adicionadas, separadamente, no processo
A) aumento da massa de glicose.
B) reduo da velocidade da reao direta e aumento da de tratamento da gua dura:
velocidade da reao inversa. I. cido ntrico;
C) aumento no valor da constante de equilbrio da reao. II. hidrxido de sdio;
III. bicarbonato de sdio.
12 | Projeto Medicina www.projetomedicina.com.br
Pode-se afirmar que favorece a remoo de ons clcio da
2
gua dura o contido em HCO 3(aq) CO 3(aq) + H (aq)
a) I, II e III.
b) II e III, apenas. De acordo com as informaes acima, assinale a(s)
c) I e III, apenas. proposio(es) CORRETA(S).
d) I e II, apenas.
+
e) I, apenas. 01. O aumento da concentrao de H implica na elevao
do pH do meio.
2
02. Os produtos de ionizao do H2CO3 so CO 3 e OH
68) (Vunesp-2005) Sabendo que a reao representada pela
equao .
H2(g) + Br2(g) 2HBr(g) 2
04. O aumento das concentraes de CO 3 e de HCO 3
exotrmica, correto afirmar que o equilbrio
A) se deslocar para a esquerda, no sentido da formao do aumenta a disponibilidade do CO2 na gua do mar.
H2 e do Br2, com o aumento da presso. 08. CO2 dissolvido diminui o pH do ambiente marinho.
B) se deslocar para a direita, no sentido de formao do
2
HBr, com o aumento da presso. 16. CO2 dissolvido na gua do mar pode gerar CO 3 e
C) se deslocar para a direita, no sentido de formao do HCO
HBr, com o aumento da temperatura.
D) se deslocar para a direita, no sentido da formao do 71) (UFSC-2005) No sistema aquoso representado abaixo,
HBr, com a diminuio da temperatura. existe o seguinte equilbrio qumico:
E) no alterado por mudanas apenas na temperatura do
sistema. 4
Sn (aq)
I (aq )
69) (Mack-2005) [CoCl4] 2
aq. + 6H2O
endo
SnI2(s)
[Co(H2O)6] 2+
aq. + 4Cl 1
aq.
I2(s)
azul rosa
Essa equao representa a reao que ocorre no galinho
do tempo, enfeite cuja superfcie impregnada por uma
4
soluo em que se estabelece o equilbrio dado acima. O Sn (aq) + 4I (aq ) SnI2(s) + I2(s)
galinho do tempo indica, pela cor, como o tempo vai
ficar. Ao balo foi acrescentado tolueno, que um lquido incolor
Fazem-se as afirmaes: e imiscvel com a gua, no qual, dentre as espcies do
I Quando a umidade relativa do ar est alta, o galinho equilbrio, somente o iodo solvel, conferindo-lhe cor
fica rosa. vermelha.
II Quando a temperatura aumenta, o galinho fica azul. Como resultado de tal perturbao, aps agitao e repouso,
III Quando o galinho fica azul, h indicativo de tempo estabelece-se um novo estado de equilbrio.
bom, sem previso de chuva.
Das afirmaes, Assinale a(s) proposio(es) CORRETA(S).
a) somente II est correta.
b) somente I e III esto corretas. 01. Em relao situao inicial, o novo estado de
c) somente III est correta. equilbrio apre-senta uma diminuio nas concentraes de
d) I, II e III esto corretas. 4
Sn (aq) e I (aq) , e o tolueno fica vermelho.
e) somente I e II esto corretas.
02. Em relao situao inicial, o novo estado de
equilbrio apresenta um aumento na quantidade de SnI2(s) e
70) (UFSC-2005) A maricultura vem se intensificando em o tolueno fica vermelho.
Santa Catarina. Apesar de ser uma atividade recente, o 04. Em relao situao inicial, o novo estado de
Estado ocupa a liderana nacional na produo de ostras equilbrio apresenta um aumento na quantidade de SnI2(s) e
e mexilhes. Para a manuteno da qualidade da gua e
dos moluscos cultivados, o pH da gua do mar deve se na concentrao de I (aq) , e o tolueno continua incolor.
situar prximo de 8,0 (oito). Assim sendo, os equilbrios 08. Em relao situao inicial, o novo estado de
qumicos abaixo devem ser considerados. equilbrio apresenta um aumento nas concentraes de Sn
4
CO 2(g) + H2O(l) H 2 CO3(aq) (aq) e I (aq) , e o tolueno continua incolor.
H 2 CO3(aq) HCO 3(aq) + H (aq)
13 | Projeto Medicina www.projetomedicina.com.br
4+
16. No sistema acima apresentado o Sn atua como agente
oxidante e o on I como agente redutor.
72) (Mack-2004) C2H4(g) + H2(g) C2H6(g) H =
32,7kcal
Da hidrogenao cataltica do eteno, equacionada acima,
fazem-se as afirmaes:
I) aumentando-se a presso do sistema, aumenta a
quantidade de etano produzido.
II) aumentando-se a concentrao de C2H4, diminui a
quantidade de produto.
III) a presena do catalisador no interfere no equilbrio.
IV) aumentando-se a temperatura do sistema, o equilbrio O grfico representa a porcentagem, em mols, de C na
desloca-se no sentido endotrmico. mistura, sob vrias condies de presso e temperatura.
So corretas, somente: Com base nesses dados, pode-se afirmar que essa reao
a) I, III e IV. a) exotrmica, sendo x + y = z
b) II e IV. b) endotrmica, sendo x + y < z
c) I e III. c) exotrmica, sendo x + y > z
d) I e II. d) endotrmica, sendo x + y = z
e) I, II e IV
e) endotrmica, sendo x + y > z
73) (Mack-2004) CHCl3(g) + Cl2(2(g) CCl4(g) + HCl(g)
No sistema em equilbrio acima equacionado, para
76) (UFMG-2006) A amnia, NH3 (g), obtida,
aumentar a produo de tetracloreto de carbono, deve-se:
industrialmente, pela reao entre os gases hidrognio e
a) aumentar a presso do sistema.
nitrognio, representada nesta equao:
b) diminuir a concentrao de Cl2.
c) aumentar a concentrao de HCl.
d) aumentar a concentrao de CHCl3. N2 (g) + 3 H2 (g) 2 NH3 (g) ; H < 0
e) diminuir a presso do sistema.
O processo industrial feito em alta presso e alta
temperatura, em condies de equilbrio. Obtida a amnia,
a mistura de gases borbulhada em gua lquida, o que
74) (Mack-2005) O equilbrio qumico que no ser afetado permite separar a amnia do nitrognio e do hidrognio que
pelo aumento ou diminuio da presso no reagiram.
Considerando-se essas informaes, CORRETO afirmar
a) Fe2O3(s) + 3CO(g) 2Fe(s) + 3CO2(g)
que
b) N2O4(g)2NO2(g) A) o princpio de Le Chatelier prev que se forma mais
c) 2H2(g) + S2(g) 2H2S(g) amnia num equilbrio em alta temperatura.
d) N2(g) + 3H2(g) 2NH3(g) B) a reao de formao da amnia mais rpida que sua
e) PCl3(g) + Cl2(g) PCl5(g) decomposio pela reao inversa, no equilbrio.
C) o rendimento em amnia maior num equilbrio em alta
presso.
75) (FUVEST-2006) Em determinado processo industrial, D) o borbulhamento da mistura dos trs gases em gua
ocorre uma transformao qumica, que pode ser retm, nesse lquido, em maior quantidade, os reagentes
representada pela equao genrica nitrognio e hidrognio.
xA(g) + yB(g) zC(g)
em que x, y e z so, respectivamente, os coeficientes
estequiomtricos das substncias A, B e C. 77) (VUNESP-2006) O cloro (grupo 17 da classificao
peridica) um gs irritante e sufocante. Misturado gua,
reage produzindo os cidos clordrico e hipocloroso que
age como desinfetante, destruindo ou inativando os
microorganismos.
a) Identifique os reagentes e os produtos desta reao e
fornea suas frmulas qumicas.
b) A gua de lavadeira uma soluo aquosa de hipoclorito
e o cido muritico uma soluo concentrada de cido
clordrico. Ambos podem ser utilizados separadamente na
limpeza de alguns tipos de piso. Explique a inconvenincia,
14 | Projeto Medicina www.projetomedicina.com.br
para a pessoa que faz a limpeza, de utilizar uma mistura c) a quantidade de H2S menor com a acidificao do
destes dois produtos. meio.
d) a solubilidade do PbS menor com a acidificao do
meio.
78) (UFSCar-2007) Em 1912, o qumico alemo Fritz Haber
desenvolveu um processo para sintetizar amnia
diretamente dos gases nitrognio e hidrognio. Este 80) (PUC - RJ-2007) Considere o equilbrio entre os ons
processo muito importante economicamente, porque a 2 2
amnia bastante utilizada, por exemplo, na indstria de cromato (CrO 4 ) e dicromato (Cr2O 7 ) em soluo
fertilizantes. Considere a reao em equilbrio qumico num aquosa, descrito abaixo.
2 2
sistema fechado
Cr2O 7 (aq) + H2O(l) 2H+ (aq) + 2CrO 4 (aq)
N2(g) + 3H2(g) 2NH3(g) Assinale a alternativa INCORRETA.
a) O nmero de oxidao do cromo nos ons cromato e
Mantendo-se a temperatura constante, algumas dicromato o mesmo e igual a 6+.
modificaes podem ser realizadas nesse sistema: b) Ao se diminuir o pH da soluo, o equilbrio se desloca
I. introduo de N2(g); favorecendo a formao de on cromato.
II. aumento da presso do sistema; c) A expresso da constante de equilbrio para esta reao
III. adio de catalisador.
As modificaes que iro provocar o deslocamento do
equilbrio, favorecendo a formao de NH3, so: H xCrO
2 2 2
Cr O
4
a) I e II, apenas. 2
K= 2 7
b) I e III, apenas.
c) III, apenas.
d) II e III, apenas. d) Ao se elevar a temperatura da soluo, o valor da
e) I, II e III. constante de equilbrio se alterar.
e) O cromo um metal de transio.
79) (UFMG-2007) Analise estes dois equilbrios que
envolvem as espcies provenientes do PbS, um mineral 81) (UFSC-2007)
depositado no fundo de certo lago: O esmalte dos dentes constitudo de hidroxiapatita,
PbS (s) Pb2+ (aq) + S2- (aq) Ca5(PO4)3OH, um composto inico muito pouco solvel em
gua. Os principais fatores que determinam a estabilidade
S2- (aq) + 2 H+ (aq) H2S (aq)
desse composto na presena da saliva so o pH e as
Neste grfico, esto representadas as concentraes de Pb2+
concentraes dos ons clcio e fosfato em soluo aquosa.
e S2-, originadas exclusivamente do PbS, em funo do pH
Sabe-se que alimentos contendo acar so transformados
da gua:
em cidos orgnicos pela ao da placa bacteriana. O pH
normal da boca apresenta-se em torno de 6,8 e em poucos
minutos aps a ingesto de alimentos com acar pode
atingir um valor abaixo de 5,5. Uma hora aps o consumo
de acar o pH retorna ao seu valor normal. O processo de
mineralizao/desmineralizao do esmalte do dente pode
ser representado pela equao I:
Ca5(PO4)3OH(s) + H2O(l) 5
Ca2+(aq) + 3 PO43- (aq) + OH-(aq) (I)
Na presena de ons fluoreto, estabelecido outro
Considere que a incidncia de chuva cida sobre o mesmo equilbrio, indicado pela equao II:
lago altera a concentrao das espcies envolvidas nos dois
equilbrios.
Com base nessas informaes, CORRETO afirmar que,
na situao descrita, 5 Ca2+(aq) + 3 PO43- (aq) + F-(aq)
a) a concentrao de ons Pb2+ e a de S2-, em pH igual a 2,
so iguais. Ca5(PO4)3F(s) (II)
b) a contaminao por ons Pb2+ aumenta com a
acidificao do meio.
15 | Projeto Medicina www.projetomedicina.com.br
Nesse processo (equao II) uma nova substncia 83) (FUVEST-2009) Compostos de enxofre (IV) podem
formada, a fluorapatita [Ca5(PO4)3F(s))], a qual menos ser adicionados ao vinho como conservantes. A
suscetvel ao ataque por cidos. depender do pH do meio, iro predominar diferentes
Algumas substncias presentes nos dentifrcios espcies qumicas de S (IV) em soluo aquosa,
desempenham funes importantes, atuando como fator conforme mostra a tabela:
abrasivo, corante, espumante, umectante (polialcois),
edulcorante (confere sabor doce) e agente teraputico. pH composto de S (IV)
Um creme dental tpico apresenta as seguintes informaes < 1,5 dixido de enxofre hidratado,
em sua embalagem: Ingredientes: 1.500 ppm (partes por SO2(aq)
milho) de fluoreto, sorbitol [C6H8(OH)6], carbonato de De 1,5 at 6,5 on hidrogenossulfito hidratado,
clcio, carboximetilcelulose, lauril sulfato de sdio,
sacarina sdica, pirofosfato tetrassdico, silicato de sdio, HSO 3 (aq)
aroma, formaldedo, gua. Contm monofluorfosfato de > 6,5 2
sdio. on sulfito hidratado, SO 3 (aq)
De acordo com o enunciado acima, assinale a(s)
proposio(es) CORRETA(S). a) Em gua, as espcies qumicas SO2(aq) e HSO 3
(aq) esto em equilbrio. Escreva a equao qumica
01. O processo de desmineralizao do esmalte do balanceada que representa esse equilbrio.
dente consiste na dissoluo de pequenas quantidades de b) Explique por que, em solues aquosas com pH
hidroxiapatita.
- baixo, predomina o SO2(aq) e no o HSO 3 (aq).
02. Os ons OH so essenciais no processo de
c) Analisou-se uma amostra de vinho a 25C,
mineralizao do esmalte do dente.
encontrando-se uma concentrao de ons OH- igual
04. A ingesto de frutas cidas e refrigerantes favorece
a 1,0 . 10-10 mol/L.
a formao da hidroxiapatita.
08. A ingesto de leite de magnsia (pH 10) facilita a
desmineralizao.
14 2
16. A presena de ons fluoreto na saliva contribuiDado - Produto inico da gua, a 25C: kW= 1,0 . 10 (mol/L) .
para o processo de desmineralizao dos dentes.
84) (Fuvest-2002) Considere os equilbrios abaixo e o efeito
82) (PUC - RJ-2008) Considere: (i) a variao de entalpia ( trmico da reao da esquerda para a direita, bem como a
H) na combusto de 1 mol de etanol o calor de reao espcie predominante nos equilbrios A e B, temperatura
que ocorre em presso constante (qp), (ii) essa reao, de 175C.
nessas condies, se d com expanso de volume (variao
de energia na forma de trabalho), (iii) a densidade do etanol
0,79 g mL1
C2H5OH(l) + 3O2(g) 2CO2 + 3H2O
H = 326,7 kcal
A esse respeito, est correto afirmar que:
a) o valor de H para a combusto de 5 mol de etanol
igual a - 3267 kJ. O equilbrio A foi estabelecido misturando-se, inicialmente,
b) a reao exotrmica e o trabalho de expanso quantidades estequiomtricas de N2(g) H2(g). Os equilbrios
produzido na combusto do etanol no fundamental para B e C foram estabelecidos a partir de, respectivamente,
que este seja utilizado como combustvel em motores a N2O4 e MgCO3 puros.
pisto. A tabela abaixo traz os valores numricos das constantes
c) o volume dos gases produzidos pela reao completa de desses trs equilbrios, em funo da temperatura, no
1 mol de etanol igual a 44,8 L em condies normais de necessariamente na mesma ordem em que os equilbrios
temperatura e presso (CNTP). foram apresentados. As constantes referem-se a presses
d) a reao inversa ao indicado no problema endotrmica, parciais em atm.
e o volume de 1 mol etanol lquido produzido no processo
igual a 22,4 L.
e) se o etanol lquido for aquecido at seu ponto de ebulio
(78,3 C a 1 atm), a mudana de fase, C2H5OH(l)
C2H5OH(g) ocorre em temperatura constante.
16 | Projeto Medicina www.projetomedicina.com.br
Logo, as constantes K1 , K2 e K3 devem corresponder,
respectivamente, a
Aps a adio de bicarbonato de sdio slido, NaHCO3 (s),
ao tubo de ensaio, observou-se que,
no lquido contido no tubo de ensaio, se formaram bolhas
de um gs, que se transferiu para o bquer;
progressivamente, a soluo contida no bquer se
descoloriu, at se tornar incolor.
85) (UFPE-2003) A constante de equilbrio a 298 K para a Todas as alternativas apresentam concluses compatveis
reao N2O4(g) 2NO2(g), igual a 1,0. Num recipiente com essas observaes, EXCETO:
fechado, a 298 K, foi preparada uma mistura dos gases A) A cor rosa da soluo do bquer indica que ela est
N2O4 e NO2 com presses parciais iniciais de 2,0 e 1,0 bar, bsica.
respectivamente. Com relao a esta mistura reacional a B) A descolorao da soluo do bquer causada pelo
298 K, pode-se afirmar que: vinagre.
0-0) est em equilbrio C) A descolorao da soluo do bquer indica um
1-1) no equilbrio, a presso parcial do gs N2O4 ser maior abaixamento do pH do meio.
que sua presso parcial inicial D) As bolhas formadas no tubo de ensaio so de gs
2-2) no equilbrio, a presso parcial do gs NO2 ser maior carbnico.
que sua presso parcial inicial
3-3) no equilbrio, as presses parciais do N2O4 e NO2 sero
as mesmas que as iniciais 88) (UFMG-2002) A hidroxiapatita, Ca5(PO4)3OH (s), um
4-4) no equilbrio, a velocidade da reao direta ser igual dos principais componentes dos dentes, participa do sistema
velocidade da reao inversa em equilbrio representado pela equao:
Ca5(PO4)3OH (s) 5 Ca2+ (aq) + 3 PO4 3-(aq) + OH (aq)
86) (Unifesp-2002) Em princpio, a fluorita (CaF2) poderia Na formao das cries dentrias, ocorre a
ser usada na fluoretao da gua, pois sua soluo saturada desmineralizao correspondente ao deslocamento do
apresenta uma concentrao de ons fluoreto superior a 1 equilbrio para a direita.
mg/L (1 ppm), que a concentrao recomendada na gua A fluoretao dos dentes ajuda na preveno das cries,
de consumo. A fluorita no usada para a fluoretao, pois porque favorece a formao de outro mineral, a
a sua solubilizao lenta e difcil de ser conseguida. No fluoroapatita, Ca5(PO4)3F (s), que mais duro e menos
entanto, sua solubilidade aumenta quando se adicionam sais solvel que a hidroxiapatita:
de alumnio gua. 5 Ca2+ (aq) + 3 PO43- (aq) + F (aq) Ca5(PO4)3F (s)
a) Mostre que a concentrao de F- numa soluo saturada Com relao a esses processos, INCORRETO afirmar
de CaF2 superior a 1 ppm. que:
Dados: KPS do CaF2 a 25 C = 3,2 x 10-11. A) a desmineralizao da hidroxiapatita dificultada por
Massa molar do F = 19 g/mol. uma dieta rica em ons clcio.
b) Explique, usando apenas equaes qumicas B) a desmineralizao da hidroxiapatita favorecida por
representativas, por que a solubilidade aumenta com a cidos.
adio de sais de alumnio, sabendo-se que o Al3+ hidrolisa C) a fluoretao desloca o primeiro equilbrio para a
e que o HF um cido fraco. esquerda.
D) o pH da saliva influi na estabilidade da hidroxiapatita
dos dentes.
87) (UFMG-2002) Na figura, est representado um tubo de
ensaio, que contm vinagre, ligado, por uma mangueira, a 89) (Faculdades Positivo-1998) O tradicional cheiro de
um bquer, que contm uma soluo diluda de hidrxido peixe causado pela presena da metil amina (H3C
de sdio, qual foram adicionadas gotas do indicador NH2), que se trata de uma substncia gasosa e solvel em
fenolftalena, o que resultou numa soluo de cor rosa: gua, resultante da decomposio de protenas quando da
morte do peixe. A soluo aquosa de metil amina apresenta
o seguinte equilbrio inico.
H3C-NH2 + H2O H3C-NH3+ + OH-
17 | Projeto Medicina www.projetomedicina.com.br
Considerando o equilbrio inico, indique a alternativa a) Atingido o equilbrio em A e em B, possvel distinguir
correta: os recipientes pela intensidade da colorao
a) A soluo apresenta carter cido. violeta?Justifique.
b) A soluo apresenta [H+] > [OH]. b) Para a experincia A, calcule a concentrao de cada gs
c) A soluo apresenta pH = 7,0. no equilbrio. Mostre em um grfico de concentrao, no
d) A soluo apresenta carter bsico. quadriculado, como variam, em funo do tempo, as
e) A soluo apresenta pH < 7,0. concentraes desses gases at que o equilbrio seja
atingido. Identifique as curvas no grfico.
90) (CeDERJ-2001) Refrigerantes so bebidas no alcolicas
que possuem uma considervel quantidade de gs
carbnico. 93) (UFC-2003) O oxignio (O2), gs essencial ao processo
Recentemente, foi lanado no mercado um de respirao humana, liga-se protena hemoglobina nos
refrigerante cujo pH depende, somente, do gs carbnico pulmes para formar a oxihemoglobina, que transportada
que contm. Um consumidor recusou-se a beber o no sangue. O oxignio ento liberado nos msculos a
refrigerante de uma garrafa aberta h algum tempo, partir da oxihemoglobina, conforme o equilbrio qumico
explicando: descrito abaixo, que dependente do pH do sangue.
Dessa garrafa eu no bebo, porque o pH do refrigerante hemoglobina + O2 oxihemoglobina
foi alterado. Um maior valor do pH do sangue, nos pulmes, favorece a
Na verdade, desprezando-se o efeito da diluio reao de formao da oxihemoglobina, e um menor valor
infinita, o que de fato aconteceu foi o seguinte: do pH do sangue nos msculos favorece a decomposio da
oxihemoglobina com liberao de O2.
a) Com a garrafa aberta a presso interna aumentou, o que Considerando o equilbrio qumico descrito, e assumindo os
fez aumentar a solubilidade do gs e, tambm, a acidez, valores de pH = 7,8 nos pulmes e pH = 7,3 nos msculos,
baixando o valor do pH. assinale a alternativa correta.
A) A concentrao de HO menor nos pulmes que nos
b) Com a garrafa aberta a presso interna diminuiu, o que msculos, e o equilbrio desloca-se para a direita.
fez baixar a solubilidade do gs e, tambm, a acidez, B) A concentrao de H+ maior nos pulmes que nos
baixando o valor do pH. msculos, e o equilbrio desloca-se para a esquerda.
C) As concentraes de H+ e HO so iguais nos pulmes e
c) Com a garrafa aberta a presso interna diminuiu, o que nos msculos e no afetam o equilbrio.
fez baixar a solubilidade do gs e, tambm, a acidez, D) A concentrao de H+ menor nos pulmes que nos
aumentando o valor do pH. msculos, e o equilbrio desloca-se para a direita.
E) A concentrao de H+ menor nos msculos que nos
d) Com a garrafa aberta a presso interna se igualou pulmes, e o equilbrio desloca-se para a esquerda.
presso ambiente, no alterando o valor do pH.
e) Com a garrafa aberta a presso interna diminuiu, o que 94) (ITA-2003) Considere os equilbrios qumicos abaixo e
fez aumentar a solubilidade do gs e, tambm, a acidez, seus respectivos valores de pK (pK = logK), vlidos para a
baixando o valor do pH. temperatura de 25C (K representa constante de equilbrio
qumico).
92) (Fuvest-1999) O equilbrio:
H2(g) + I2(g) 2HI (g) Na temperatura de 25C e numa razo de volumes 10,
incolor violeta incolor misturam-se pares de solues aquosas de mesma
concentrao. Assinale a opo que apresenta o par de
tem, a 370C, constante Kc igual a 64. solues aquosas que ao serem misturadas formam uma
Para estudar esse equilbrio, foram feitas 2 experincias soluo tampo com pH prximo de 10.
independentes A e B. A) C6H5OH(aq)/C6H5NH2(aq).
B) C6H5NH2(aq)/C6H5NH3Cl(aq).
1- 0,10 mol de cada gs, H e I, foram colocados em um C) CH3COOH(aq)/NaCH3COO(aq).
recipiente adequado de 1 L, mantido a 370 C at atingir o D) NH3(aq)/NH4Cl(aq).
equilbrio (a intensidade da cor no muda mais). E) NaCH3COO(aq)/NH4Cl(aq).
2- 0,20 mol do gs HI foi colocado em um recipiente de 1
L, idntico ao utilizado em A, mantido a 370 C at atingir
o equilbrio (a intensidade da cor no muda mais).
95) (UFSCar-2002) O xido ntrico, NO, um importante
intermedirio na fabricao do cido ntrico pelo processo
Ostwald. produzido na atmosfera por fenmenos naturais,
18 | Projeto Medicina www.projetomedicina.com.br
como relmpagos, sendo tambm liberado em decorrncia
de atividades humanas, tornando-se um dos responsveis
pela formao da chuva cida. A reao de formao de NO
representada pela equao:
N2(g) + O2(g) 2 NO(g) Ho = + 180 kJ
a) Neste sistema em equilbrio a 25C, num recipiente de 10
L, existem 0,10 mol de N2 e 0,02 mol de O2. Se a constante
de equilbrio Kc a 25C igual a 4,5 . 1031, qual ser a
concentrao em mol/L de NO no equilbrio, nesta
temperatura?
b) O que se verifica com o equilbrio e a constante de
equilbrio, quando a temperatura do sistema
aumentada?Justifique.
96) (UFMG-2003) Os calores envolvidos na solubilizao de A respeito dessa transformao qumica, as seguintes
iodo slido em etanol e em tetracloreto de carbono, CCl4 afirmaes foram feitas:
foram investigados. Os resultados obtidos esto resumidos
nestas equaes: a diminuio da temperatura aumenta o rendimento da
I2 (s)I2 (em etanol) H = + 6,7 kJ/mol reao;
I2 (s)I2 (em CCl4) H = + 24,2 kJ/mol a elevao da temperatura diminui a velocidade da
Considerando-se esses equilbrios, INCORRETO afirmar reao;
que a reao de sntese da amnia exotrmica;
A) o aumento da temperatura desloca os equilbrios no a elevao da temperatura favorece o consumo de N2 e H2.
sentido da formao dos produtos.
B) os valores de H correspondem energia gasta para a Dessas afirmaes, so corretas apenas
fuso do iodo slido.
C) a dissoluo do iodo endotrmica em ambos os I e II.
solventes. I e III.
D) a desorganizao das molculas de iodo aumenta III e IV.
durante a dissoluo. II e III.
II e IV.
97) (FMTM-2003) O Ca2+ o ction mais comum em rios e 100) (PUC - SP-2006) A pessoa alcoolizada no est apta a
lagos. Sua procedncia deve-se dissoluo do mineral dirigir ou operar mquinas industriais, podendo causar
calcita, CaCO3 , pela ao do CO2 , conforme equilbrio graves acidentes. possvel determinar a concentrao de
qumico: etanol no sangue a partir da quantidade dessa substncia
presente no ar expirado. Os aparelhos desenvolvidos com
Analise as seguintes afirmaes, considerando que o essa finalidade so conhecidos como bafmetros. O
sistema est em equilbrio. bafmetro mais simples e descartvel baseado na reao
I. Quando uma base adicionada a tal gua, o equilbrio entre o etanol e o dicromato de potssio (K2Cr2O7) em
deslocado para a esquerda. meio cido, representada pela equao a seguir:
2
II. A adio de cido a tal gua favorece a dissoluo da Cr2O 7 (aq) + 8H+(aq) + 3CH3CH2OH(g) 2Cr3+(aq) +
calcita. 3CH3CHO(g) + 7H2O(l)
III. A adio de uma substncia que complexa os ons Laranja etanol verde
clcio favorece a dissoluo da calcita. etanal
Dentre as afirmaes, est correto o contido em (lcool etlico)
A) I, apenas (acetaldeido)
B) II, apenas
C) III, apenas Sobre o funcionamento desse bafmetro foram feitas
D) I e II, apenas algumas consideraes:
E) I, II e III I. Quanto maior a intensidade da cor verde, maior a
concentrao de lcool no sangue da pessoa testada.
99) (Fatec-2005) O grfico abaixo mostra como varia a II. A oxidao de um mol de etanol a acetaldedo envolve 2
constante de equilbrio (Kc) em funo da temperatura para mol de eltrons.
a reao de sntese da amnia. III. O nion dicromato age com agente oxidante no
processo.
Est correto o que se afirma apenas em
19 | Projeto Medicina www.projetomedicina.com.br
A) I e II Quando a concentrao de HIn muito maior do que a de
B) I e III In, a soluo tem a cor da forma cida do indicador; no
C) II e III caso contrrio, a soluo ter a cor da forma bsica do
D) I indicador.
E) I, II e III a) Escreva a constante de equilbrio para a fenolftalena
num equilbrio de transferncia de prtons com a molcula
de gua.
101) (FUVEST-2006) Considere uma soluo aquosa diluda b) Qual deve ser o ponto final de uma titulao cido-base
de dicromato de potssio, a 25C. Dentre os equilbrios que em relao s concentraes das formas HIn e Indo
esto presentes nessa soluo, destacam-se: indicador.
Constantes de equilbrio (25C)
2
Cr2O 7 + H2O 2HCrO4 . . . . . . . . . . K1 = 2,0 102 103) (Mack-2007)
No equilbrio acima:
on dicromato
I. Aumentando-se a presso do sistema, o equilbrio
HCrO 4 H+ + CrO 24 . . . . . . . . . . K2 = 7,1 107 desloca-se no sentido endotrmico.
on cromato II. Diminuindo-se a temperatura do sistema, o
2
Cr2O 7 + H2O 2H+ + 2CrO 24 . . . . . . . . . . K3 = ? equilbrio desloca-se no sentido da reao indireta.
III. Adicionando-se um catalisador, o equilbrio
H2O H+ + OH . . . . . . . . . . Kw = 1,0 1014 desloca-se no sentido exotrmico.
a) Calcule o valor da constante de equilbrio K3.
b) Essa soluo de dicromato foi neutralizada. Para a
2
soluo neutra, qual o valor numrico da relao [CrO 4
Das afirmaes feitas,
/ 2
]2 [Cr2O 7 ]? Mostre como obteve esse valor. a) I, II e III esto corretas.
c) A transformao de ons dicromato em ons cromato, em b) somente I est correta.
meio aquoso, uma reao de oxirreduo? Justifique. c) somente II est correta.
d) somente I e II esto corretas.
e) somente II e III esto corretas.
102) (VUNESP-2006) Um indicador cido-base um cido
fraco que tem uma cor na sua forma cida HIn (onde In
significa indicador) e outra na sua forma base conjugada In 104) (UFSCar-2008) As equaes apresentadas a seguir
. Na figura, representa-se essas duas formas para o representam equilbrios qumicos estabelecidos
indicador fenolftalena. separadamente no interior de cilindros dotados de mbolos
mveis. Considerando que cada cilindro ter seu volume
reduzido metade do valor inicial, mantida a temperatura
constante, assinale a alternativa que representa o equilbrio
afetado por esta alterao.
a) C(s) + O2 CO2(g)
b) H2(g) + Br2(g) 2HBr(g)
c) CH4(g) + 2O2(g) CO2(g) + 2H2O(g)
d) CaCO3(s) CaO(s) + CO2(g)
e) FeO(s) + CO(g) Fe(s) + CO2(g)
105) (UFPR-2009) O cido acetilsaliclico um
medicamento antiinflamatrio utilizado pela humanidade
desde o final do sculo XIX. A frmula molecular desse
cido C9H8O4 e a constante de ionizao cida (Ka)
3,0.10-4. O equilbrio do cido acetilsaliclico pode ser
esquematizado da seguinte forma:
cido acetilsaliclico nion- + H+
A forma no-ionizada do cido consegue atravessar a
membrana do estmago, enquanto que a forma ionizada no
consegue. No entanto, dentro do estmago a concentrao
de ons H+ elevada, o que facilita a absoro do
medicamento pela membrana do estmago. Sobre esse
assunto, considere as seguintes afirmativas:
20 | Projeto Medicina www.projetomedicina.com.br
1. No estmago ocorre o deslocamento do equilbrio para a A) no ar que expiramos existe vinagre, produzindo ons
esquerda, devido a maior concentrao de H+. CH3COO e H+ na soluo.
2. O cido acetilsaliclico mais fraco que o cido B) no ar que expiramos existe soda custica, produzindo
ciandrico (Ka = 4,9.10-10). ons Na+ e OH na soluo.
3. Devido a alta concentrao de H+, o pH do estmago tem C) no ar que expiramos h um gs que, ao reagir com a
valor maior que 7. gua, produz ons H+.
Est/Esto correta(s) a(s) afirmativa(s): D) o ar que expiramos reage com a gua do repolho
a) 1 apenas. formando cido clordrico e produzindo ons H+ e Cl na
b) 1 e 2 apenas. soluo.
c) 2 apenas. E) o ar que expiramos comporta-se, em soluo aquosa,
d) 2 e 3 apenas. como uma base.
e) 3 apenas.
106) (Vunesp-2001) O processo industrial Haber-Bosch de 109) (PUC - SP-2005) O fosfato est presente em soluo
obteno da amnia se baseia no equilbrio qumico aquosa, principalmente sob a forma das espcies
expresso pela equao: diidrogenofosfato (H2PO4-) e
N2 3H2NH3 monohidrogenofosfato(HPO42-). Em soluo aquosa neutra
Nas temperaturas de 25 C o e de 450 C, as constantes de (pH=7), a concentrao de cada espcie praticamente a
equilbrio KP so 3,5 x 108 e 0,16, respectivamente. mesma. Qual espcie de predominar em meio de pH=5?.
a) Com base em seus conhecimentos sobre equilbrio e nos Justifique sua resposta a partir da anlise da reao de
dados fornecidos, quais seriam, teoricamente, as condies ionizo do H2PO4-
de presso e temperatura que favoreceriam a formao de
NH3? Justifique sua resposta.
b) Na prtica, a reao efetuada nas seguintes condies: H2PO4- + H2O HPO42- + H3O+
presso entre 300 e 400 atmosferas, temperatura de 450 C
e emprego de ferro metlico como catalisador. Justifique O nitrato de potssio (KNO3) uma das substncias
por que estas condies so utilizadas industrialmente para presentes nosfertilizantes, fornecendo ao solo os elementos
a sntese de NH3. essenciais nitrognio e potssio. Essa substncia apresenta
temperatura de fuso 334 C e solubilidade em gua
35g/100 g de gua a 25 C e a sua soluo aquosa conduz
107) (UFSCar-2003) Solues aquosas de dicromato de corrente eltrica. Represente o processo de dissoluo do
potssio so alaranjadas, enquanto que solues aquosas de KNO3 em gua atravs da sua equao de dissociao e
cromato de potssio so amareladas. O equilbrio qumico esquematize um modelo que evidencie adequadamente as
dessas duas solues pode ser representado pela mesma interaes existentes entre as espcies qumicas presentes
equao: nessa soluo.
Cr2O72 (aq) + H2O(l ) 2CrO42 (aq) + 2H+(aq)
110) (PUC - RJ-2005) O processo Haber-Bosch, um dos mais
a) Ao adicionarmos gotas de soluo aquosa de hidrxido utilizados para a obteno de amnia sinttica, conforme
de sdio na soluo de dicromato de potssio, o que reao dada abaixo, utiliza temperatura na faixa de 550 C e
acontecer com a colorao dessa soluo? Justifique. presso de 200-300 atm.
b) Considere o cromato de brio um sal insolvel em gua e
o dicromato de brio solvel. Se adicionarmos gotas de Fe
soluo aquosa contendo ons Ba2+ numa soluo de N2(g) + 3 H2(g) 2 NH3(g) H (25 C) = - 22,04
dicromato de potssio haver a formao de um kcal/mol de N2 reagido
precipitado. O que acontece com o precipitado se for Sabendo disso, pergunta-se:
adicionada soluo aquosa de cido clordrico? Justifique
a) Qual a funo do Fe nessa reao?
b) Qual o valor da entalpia padro da amnia a 25 C.
108) (Vunesp-2004) Ao cozinhar repolho roxo, a gua do Explique sua resposta.
cozimento apresenta-se azulada. Esta soluo pode ser c) O que deve acontecer com o equilbrio dessa reao
utilizada como um indicador cido-base. Adicionando caso a mesma seja realizada em:
vinagre (cido actico), a colorao mudar para o I) Temperaturas maiores que 550 C? Explique sua
vermelho e, adicionando soda custica (hidrxido de sdio), resposta.
a colorao mudar para o verde. Se voc soprar atravs de II) Presses maiores que 200 atmosferas? Explique
um canudinho na gua de cozimento do repolho roxo sua resposta.
durante alguns segundos, sua colorao mudar do azul
para o vermelho. Destas observaes, pode-se concluir que:
21 | Projeto Medicina www.projetomedicina.com.br
111) (ITA-2006) So descritos, a seguir, dois experimentos e o conhecimento qumico (vestibular UNICAMP 2002).
respectivas observaes envolvendo ossos limpos e secos Hoje esto se preparando para celebrar uma data muito
provenientes de uma ave. especial. Faa uma boa prova e tenha uma boa festa depois
I. Um osso foi imerso em uma soluo aquosa 10% (v/v) dela.
em cido frmico. Aps certo tempo, observou-se que o
mesmo havia se tornado flexvel. As pessoas adoravam essas demonstraes qumicas. Dina
II. Um outro osso foi colocado em uma cpsula de e Rango sabiam disso, pois eles prprios tinham sido
porcelana e submetido a aquecimento em uma chama de fisgados por esse tipo de atividade (Vestibular da
bico de Bunsen. Aps um longo perodo de tempo, Unicamp-2001). Chamando a ateno de todos, Dina
observou-se que o mesmo se tornou frgil e quebradio. colocou sobre o balco um copo que aparentemente
a) Explique as observaes descritas nos dois experimentos. continha gua, e nele adicionou algumas gotas de uma
b) Baseando-se nas observaes acima, preveja o que soluo que tingiu aquela gua. Dina disse que aquela
acontecer se um terceiro osso limpo e seco for imerso em soluo colorida mudaria de cor no berro. Um dos
uma soluo aquosa 1mgL1 em fluoreto de sdio e, a convidados, com a boca bem aberta e prxima do copo, deu
seguir, em uma soluo aquosa a 10% (v/v) em cido um longo berro. Como num passe de mgica, o lquido
frmico. Justifique a sua resposta. mudou de cor.
a) O lquido que estava no copo era, na verdade, uma
soluo aquosa de amnia, cujo Kb soluo aquosa
112) (FUVEST-2007) Na produo de hidrognio por via estavam em equilbrio, antes da adio do indicador,
petroqumica, sobram traos de CO e CO2 nesse gs, o que amnia, on amnio e on hidrxido.
impede sua aplicao em hidrogenaes catalticas, uma Escreva a expresso de Kc em termos das concentraes
vez que CO veneno de catalisador. Usando-se o prprio dessas espcies. Nesse equilbrio, o que est em maior
hidrognio, essas impurezas so removidas, sendo concentrao: amnia ou o on amnio? Justifique.
transformadas em CH4 e H2O. Essas reaes ocorrem a b) O que foi gotejado no copo era uma soluo de vermelho
temperaturas elevadas, em que reagentes e produtos so de fenol, um indicador cido-base, que apresenta cor
gasosos, chegando a um equilbrio de constante K I no caso vermelha em pH acima de 8,5 e cor amarela em pH abaixo
do CO e a um equilbrio de constante K II no caso do CO2. O de 6,8. Qual foi a mudana de cor observada? Como se
grfico traz a variao dessas constantes com a temperatura. explica que o berro tenha promovido a mudana de cor?
a) Num experimento de laboratrio, realizado a 460C, as
presses parciais de CO, H2, CH4 e H2O, eram,
respectivamente, 4 10-5atm; 2atm; 0,4atm; e 0,4atm.
Verifique se o equilbrio qumico foi alcanado. Explique.
b) As transformaes de CO e CO2 em CH4 mais H2O so
exotrmicas ou endotrmicas? Justifique sua resposta.
c) Em qual das duas transformaes, na de CO ou na de
CO2, o calor desprendido ou absorvido maior? Explique,
em termos do mdulo da quantidade de calor (|Q|)
envolvida.
113) (Unicamp-2008) Eles esto de volta! Omar Mitta,
vulgo Rango, e sua esposa Dina Mitta, vulgo Estrondosa, a
dupla explosiva que j resolveu muitos mistrios utilizando
22 | Projeto Medicina www.projetomedicina.com.br
Gabarito c) O catalisador no desloca o equilbrio, mas faz com que
esse seja atingido em um tempo menor.
1) a) Em um local de altitude mais elevada, a [O2] no ar
11) a) Com a menor temperatura o equilbrio se deslocar
menor e, segundo o Princpio de L Chatelier, o equilbrio
para a direita, pois a reao endotrmico, logo haver
qumico em questo desloca-se para a esquerda. Em outras
mais oxignio dissolvidob) No p da montanha a presso
palavras, a diminuio da [O2] favorece a reao inversa, o
maior e favorece a solubilizao do O2
que diminui a capacidade respiratria do atleta.
b) Durante o perodo de adaptao altitude mais elevada,
o organismo do atleta sintetiza mais hemoglobina 12) a) a remoo do NO2 faz o equilbrio se deslocar para a
aumentando a sua concentrao. Pelo Princpio de Le direita.
Chatelier, isso favorece a reao direta, o que aumenta a b) O aumento da presso no desloca o equilbrio, pois o
capacidade respiratria do atleta. nmero de mols do produto igual ao nmero de mols do
Para cada molcula de hemoglobina sintetizada, so reagente.
consumidos quatro tomos de ferro, o que diminui as
reservas desse metal no organismo do atleta. 13) a) o aumento da concentrao do N2 faz o equilbrio se
deslocar para a esquerda.b) o aumento da presso desloca o
equilbrio para o lado de menor nmero de mols gasosos,
2) Alternativa: A logo para a esquerda(7).
3) Alternativa: C 14) Alternativa: A
4) Resposta: C 15) Alternativa: A
5) Resposta: A 16) Resposta: E
Resoluo: O Princpio de Le Chatelier estabelece que: se
uma fora externa aplicada a um sistema em equilbrio, o
6) a) Havendo aquecimento, o equilbrio desloca-se para o
sistema se ajusta de tal modo que a fora seja parcialmente
lado direito, pois o aumento da temperatura favorece a
anulada, de modo que o mesmo volte posio de
reao endotrmica, e a soluo passa a adquirir a cor azul,
equilbrio. A palavra fora significa uma mudana na
devido a um aumento da concentrao da espcie [CoCl4] 2
concentrao de uma das espcies, presso, volume, ou
(aq).
temperatura do sistema em equilbrio. Um aumento da
b) Ao adicionarmos mais cido clordrico (HCl), estaremos
concentrao de uma das espcies, faz com que a reao
aumentando a concentrao molar de Cl (efeito do on
tenda a se deslocar no sentido do maior consumo daquela
comum); o equilbrio se deslocar para o lado direito, e a
espcie. Um aumento na temperatura favorece a reao
soluo ir adquirir a cor azul.
endotrmica (H > 0), contrariamente, uma diminuio na
temperatura favorece a reao exotrmica (H < 0). Na
reao descrita na questo, um aumento na temperatura
7) Alternativa: D
favorece a formao do [CoCl4]2 (reao endotrmica), e
uma diminuio favorece a formao do [Co(H2O))]2+
8) a) A reao de sntese da amnia no um processo (reao exotrmica). A adio de cloreto de sdio aquoso
endotrmico, e sim exotrmico, pois observa-se no grfico soluo acarreta o aumento da concentrao dos ons Cl no
que, a uma dada presso, uma diminuio na temperatura meio. Conseqentemente, a reao se deslocar no sentido
acarreta um aumento na porcentagem de amnia na mistura. de consumir os ons Cl adicionados, ou seja, formao do
b) 75 toneladas a mais de NH3 [CoCl4]2+ (cor azul). Portanto, somente a alternativa E est
c) No. A presena de um catalisador no ir alterar a correta.
porcentagem de NH3 no equilbrio.
17) Resposta: E
9) a) Em meio cido, a reao de ionizao do HIn estar
deslocada para a esquerda, fazendo com que o tornassol Resoluo
fique vermelho (Princpio de L Chatelier). I (correta)
b) O ltimo pargrafo no leva em considerao a hidrlise Soluo tampo sofre pequenas variaes de pH pela
salina. Sais como o acetato de sdio e o cloreto de amnio adio de pequenas quantidades de substncias cidas ou
tornam o meio alcalino (tornassol azul) e cido (tornassol bsicas.
vermelho), respectivamente. II (correta)
O aumento de ons bicarbonato no sangue desloca o
equilbrio para a esquerda, consumindo ons H+,
10) a) a concentrao do C(s) no alterada, logo o aumentando o pH.
equilbrio no se desloca.b) Desloca para a esquerda j que III (correta)
a reao direta endotrmica.
23 | Projeto Medicina www.projetomedicina.com.br
O aumento da concentrao de CO2 no sangue desloca o 32-V
equilbrio para a direita, produzindo ons H+, diminuindo o 64-F
pH.
31) Alternativa: E
18) Alternativa: A 32) Considerando a equao qumica
CO2(g) + H2O(l) H2CO3(aq) H+(aq) + HCO 3 (aq),
19) a) NH3(g) + H2O(l) NH4OH(aq) NH 4 (aq)
+ OH (aq) temos:
A presena de ons OH provenientes da reao caracteriza O aumento na intensidade da respirao diminui o teor de
uma soluo bsica com pH > 7. CO2 no sangue, o que provoca um deslocamento no
b) O cido Clordrico, pois os ons H+ iro retirar os ons equilbrio acima para a esquerda, causando diminuio do
OH deslocando o equilbrio para a direita, diminuindo a nvel de acidez do sangue (diminuio da concentrao de
concentrao de NH3(g) e, conseqentemente, o cheiro. H+), com elevao de seu pH.
O aumento no teor de bicarbonato na urina diminui sua
concentrao no sangue, o que faz o equilbrio inicial se
20) a) deslocar para a direita, produzindo ons H+ e deixando o
sangue mais cido, ou seja, diminui seu pH.
b) A 2-feniletilamina mais solvel em meio cido. 33) a) O equilbrio ser deslocado no sentido dos reagentes,
+
Quanto maior a concentrao do on H (aq), mais ou seja, no sentido de diminuir a
ionizao do cido actico.
deslocado o equilbrio estar no sentido de formao b) Sendo a temperatura constante, o valor de Ka permanece
do on 2-etilfenilamnio. constante. Para a reao qumica
CH3COOH(aq) + H2O(l) H3O 3(aq) + CH3COO- (aq), tem-se
21) a) CO(g) + 2H2(g) CH3OH(g) que:
H O CH COO
CH COO
3 3
ka =
3
b) De acordo com o princpio de Le Chatelier, o aumento Portanto, para que Ka permanea constante, o aumento da
da presso vai deslocar o equilbrio para a direita (menor concentrao de ons acetato no
volume gasoso), favorecendo a formao de metanol. A meio implicar aumento da concentrao de cido
actico.
34) Alternativa: D
22) Alternativa: E
35) a) Processo exotrmico
23) Alternativa: A b) O aumento da presso desloca o equilbrio para o lado
direito favorecendo um aumento de rendimento
24) Alternativa: D
36) Resposta C:
25) Alternativa: D Resoluo:
26) Alternativa: E Os equilbrios qumicos esto associados e podem ser
deslocados em seqncia. De modo simplificado podemos
27) Alternativa: E estud-los da seguinte maneira:
28) Alternativa: C
29) Alternativa: A
30) Resposta: 44
01-F
02-F Pelo Princpio de Le Chatelier, um aumento da [CO2]
04-V causar deslocamentos para a esquerda
08-V
16-F
24 | Projeto Medicina www.projetomedicina.com.br
nos equilbrios, de modo que teremos um aumento nas
[Ca(aq)2+ ] e [CO3(aq)2-] nos fluidos das aves, 42) Alternativa: C
possibilitando a formao de cascas de ovos mais espessas.
43) Itens Certos: (1), (2) e (3)
Itens Errados: (4) e (5)
37) Alternativa: C Resoluo:
(4) O uso de catalisador no processo propicia um estado de
38) a) No sistema 1, a presso parcial de CO2 no ar transio com menor energia.
praticamente desprezvel, e, portanto, a quantidade de (5) A unidade da constante de equilbrio da equao
CaCO3(s) dissolvida ser menor. mencionada (mol/L)-2.
b) A solubilidade de um gs em um lquido aumenta
medida que diminui a temperatura do lquido. Ainda, de
acordo com o princpio de Le Chatelier, para o equilbrio 44) a) Kc=9>4
representado por: Portanto, para se atingir o equilbrio, as concentraes dos
CO2(g)CO2(aq) + calor produtos devem diminuir, enquanto que as dos reagentes
a diminuio da temperatura desloca o equilbrio para a devem aumentar. A velocidade da reao ser maior no
direita, favorecendo a dissoluo do sentido de formao de CO (reao inversa).
CO2(g) e, conseqentemente, tambm a dissoluo do b) [CO2]=[H2]=2,67 M
CaCO3(s). [CO]=[H2O]=1,33 M
39) Alternativa: E 45) a) I NH4+ (aq) + H2O(l) NH4OH(aq) + H+ (aq)
II NH4OH(aq) NH3(g) + H2O(l)
40) a) 9,0 x 104 mol b) Percebe-se cheiro mais forte de amnia no tubo 2. A
b) Na gua pura, temos apenas o equilbrio de dissoluo do adio de Na2CO3 torna o meio mais bsico (maior Kb), o
gs oxignio. que provoca maior consumo de H+, deslocando o equilbrio
No sangue, alm do equilbrio de dissoluo do gs I para a direita e favorecendo a formao de NH4OH(aq),
oxignio, temos o consumo de O2(aq) para formar a oxi- que por sua vez se decompe produzindo mais amnia
hemoglobina. O equilbrio de dissoluo ser deslocado (NH3).
para a direita, a fim de aumentar a concentrao de c) O cloreto de amnio um sal de carter cido, pois
O2(aq). A solubilidade do O2 em gua aumenta. proveniente de um cido forte (HCl) e uma base fraca
(NH4OH). Logo a sua hidrlise salina origina uma soluo
cida (pH<7):
41) Situao inicial a 25C e 1atm: 46) a) De maneira geral, a presso parcial do CO2 no
sangue venoso maior que a do sangue arterial, isto , a
concentrao em quantidade de mol de CO2 dissolvido
maior; logo, o sangue venoso deve apresentar um carter
cido mais acentuado, ou seja, um menor pH.
b) 72 min
Nessa soluo, existe o equilbrio dado por:
47) Alternativa: A
NaHCO3(s) Na+(aq) + HCO 3 (aq) (Eq. I)
a) O nion bicarbonto, em soluo aquosa, sofre hidrlise, 48) Alternativa: D
resultanto em meio bsico de acordo com:
HCO 3 (aq) + H2O(l) H2CO3(aq)_ + OH(aq) (Eq. II) 49) Alternativa: D
O aquecimento favorece a decomposio do cido
carbnico, produzindo H2O e CO2: 50) Alternativa: C
< H2CO3(aq) H2O(l) + CO2(g) (Eq. III)
Durante o processo de aquecimento e considerando 51) a) Kc=0,36
desprezvel o volume de gua perdido por evaporao, b) O aumento da temperatura desloca o equilbrio para o
haver desprendimento de CO2(g), o que leva a um lado da reao endotrmica, isto , do NO2 tornando o
deslocamento dos equilbrios I, II e III para a direita. equilbrio mais alaranjado.
b) Aps o resfriamento, ainda resta slido no sistema,
portanto ainda temos uma soluo saturada de NaHCO3; 52) Alternativa: E
porm a quantidade de NaHCO3(s) ser menor que a inicial.
25 | Projeto Medicina www.projetomedicina.com.br
53) Alternativa: A 61) Resposta:
54) Alternativa: D a) A reao com o on Fe3+ apresenta o maior valor de
constante de equilbrio, portanto estar mais deslocada no
55) Resposta: sentido da complexao (para a direita). O Fe3+ ser
a) A cerveja que se encontra a 25 C. Como o processo de removido com mais eficincia.
transformao de CO2 (aq) em CO2 (g) endotrmico,
quanto maior a temperatura, maior ser a quantidade de gs b) CaEDTA2 + Fe3+ = FeEDTA1 + Ca2+
liberado (espuma).
b) CO2 + H2O H2CO3 2H+ + CO32-
62) Alternativa: C
56) Resposta:
63) Alternativa: D
a) Kc = [N2O4] = 0,2 = 0,2 = 2 Kc = 2,2
[NO2]2 0,32 0,09 0,9 64) Alternativa: A
b)A reao exotrmica porque, quando ocorre uma 65) a) A adio de HNO3, que um cido forte, aumentar
elevao da temperatura (entre t4 e t5), observa-se a a concentrao de H3O+, resultando num deslocamento para
diminuio da concentrao de produto (N2O4), mostrando a esquerda dos equilbrios acima e aumentando a
que o equilbrio deslocado no sentido da formao do concentrao de Ca2+. Essa situao anular parcialmente o
reagente (NO2). tratamento da gua dura.
b) A adio de NaOH libera OH, que, reagindo com o
H3O+, deslocar os equilbrios para a direita, reduzindo
57) Alternativa: E ainda mais a concentrao de Ca2+. Essa situao levar a
uma gua com menor teor de Ca2+.
58) Resposta: B
Aumentar o rendimento da reao significa deslocar o 66) Alternativa: A
equilbrio no sentido de formao dos produtos (para a
direita). Ao adicionar nitrato de prata (AgNO3), que 67) Alternativa: B
solvel, ocorre uma reao entre o on Ag+, proveniente do
AgNO3, com o on Cl, formando o cloreto de prata, AgCl , 68) Alternativa: D
que insolvel. Esta reao diminui a concentrao do on
Cl, deslocando o equilbrio para a direita, de acordo com 69) Alternativa: D
o princpio de Le Chatelier. A adio de HCl desloca o
equilbrio no sentido de formao dos reagentes devido 70)
neutralizao dos ons OH. A adio de KCl desloca o
01 02 04 08 16
equilbrio, no sentido de formao dos reagentes. A adio
de AgCl (insolvel) e de KNO3 no desloca o equilbrio. V V F F F
TOTAL = 28
59) Aumento das concentraes de CO2 e de H2O, na 71)
atmosfera. Deslocamento do equilbrio no sentido de
01 02 04 08 16
consumo de carbonato e conseqente aumento da acidez no
interior do ovo. V V F F V
TOTAL = 19
60) Resposta: 72) Alternativa: A
a) K3 = K2/K1 ------ K3 = 7,3
73) Alternativa: D
b)
O catalisador no desloca o equilbrio, pois aumenta a
74) Alternativa: A
velocidade direta e inversa na mesma proporo.
A presso no influi nesse equilbrio, pois o nmero de
mols dos dois lados da equao so iguais. 75) Alternativa: C
O aumenta da temperatura desloca a reao no sentido
endotrmico, diminuindo assim o rendimento. 76) Alternativa: A
77) a) Reagentes: Cl2(g) e H2O(l)
Produtos: HCl(aq) e HClO(aq)
26 | Projeto Medicina www.projetomedicina.com.br
b)
b) Ao se adicionar uma soluo de cido clordrico I. Al3+ + 3H2O Al(OH)3+3H+
concentrado (cido muritico) na gua de lavadeira, que II. H+ + F- HF
contm o hipoclorito, ocorrer um deslocamento da reao III. CaF2 Ca2+ + 2F-
Cl2(g) + H2O(l) HCl(aq) + HClO(aq) A adio de sal de alumnio ao sistema aquoso provoca o
para a esquerda, com conseqente formao de Cl2(g), que deslocamento do equilbrio I para a direita. Com o aumento
um gs irritante e sufocante. da concentrao de ons H+ , o equilbrio II deslocado
para a direita, com consumo de ons F- . A diminuio da
concentrao de ons F. favorece o deslocamento do
78) Alternativa: A equilbrio III para a direita, com dissoluo da fluorita (Le
Chatelier).
79) Alternativa: B
80) Alternativa: B 87) Alternativa: B
81) Resposta: 03 88) Alternativa: C
01-V
02-V 89) Alternativa: D
04-F
08-F 90) Alternativa: C
16-F
91) Alternativa: A
82) Alternativa: E 92) a) No possvel distinguir os recipientes, pois, se em
A a reao se completasse, formar-se-ia 0,20 mol de HI,
que exatamente a quantidade de partida na experincia B.
83) a) SO2(aq) + H2O(l) H (aq) + HSO 3 (aq)
Como equilbrio pode ser atingido de ambos os lados, as
b) Solues de baixo pH apresentam elevada concentrao quantidades finais de cada gs no equilbrio finais de cada
hidrogeninica (H+), o que ir deslocar o equilbrio acima gs no equilbrio sero as mesmas.
para a esquerda, favorecendo a formao de SO2(aq).
c) KW= [H ] . [OH ]
14
1,0 . 10 mol/L
pH = 4
Nesse pH, de acordo com a tabela, a espcie que
prevalece o on hidrogenossulfito hidratado (HSO 3 (aq)).
84) Resposta: A
Resoluo
A anlise da tabela Kp/t(C) permite o estabelecimento das
seguintes associaes decorrentes do Princpio de Le
Chatelier:
1. T KP (processo endotrmico)
2. T KP (processo endotrmico)
3. T KP (processo exotrmico)
Concluses:
K3 processo A (exotrmico)
K2 processo C (endotrmico)
K1 processo B (endotrmico a predominncia
do NO2 sugere que os valores de KP so elevados).
85) Resposta: FFVFV 93) Resposta: D
Resoluo: Como o equilbrio qumico determinado pelo
pH do sangue, um maior valor de pH nos pulmes (pH =
86) a) 7,6 ppm maior que 1 ppm
27 | Projeto Medicina www.projetomedicina.com.br
7,8) implica em menor concentrao de H+. Por outro lado,
conforme dado na questo, um maior valor de pH nos 104) Alternativa: D
pulmes favorece a captao de O2, ou seja, formao de
oxihemoglobina. Conseqentemente, ocorre o 105) Alternativa: A
deslocamento do equilbrio para a direita. Portanto, a
alternativa D a correta. 106) a) A diminuio do Kp com a temperatura significa
que temperaturas elevadas desfavorecem a reao direta
94) Alternativa: D (formao de amnia). Alm disso, no sentido direto ocorre
uma diminuio do nmero de molculas presentes no
95) Resposta: sistema. Ento, pelo Princpio de Le Chatelier, podemos
a) [NO] = 3x1018 mol/L afirmar que as seguintes condies favorecem a sntese de
b) Temos um processo endotrmico (H > 0), portanto o amnia:
aumento da temperatura ir deslocar o equilbrio para a I. Temperaturas ao redor de 25 C;
direita, favorecendo a formao de NO, conseqentemente II. Presses elevadas.
o valor da constante de equilbrio aumentar. b) Na prtica, como a reao entre N2 e H2 ocorre com
grande energia de ativao, a temperatura utilizada
elevada (450 C). O catalisador usado para aumentar a
velocidade da reao de sntese e a amnia formada
96) Alternativa: B constantemente removida do sistema qumico, o que
desfavorece a reao inversa.
97) Alternativa: B
98) 107) a) Ao adicionarmos ao sistema gotas de soluo
01 02 04 08 16 32 aquosa de hidrxido de sdio, a colorao da soluo torna-
se amarela devido ao consumo dos ons H+ e o equilbrio
V F F V F V deslocado para a direita.
TOTAL = 41 H+ (aq) + OH(aq) H2O (l )
b) A equao qumica de precipitao pode ser expressa
99) Alternativa: B pelo equilbrio:
Ba2+ (aq) + CrO42 (aq) BaCrO4 (s)
100) Alternativa: E Com a adio de ons H+ ao sistema, o equilbrio fornecido
(Cr2O72(aq) + H2O (l ) 2 CrO42(aq) + 2H+ (aq))
deslocado para a esquerda, diminuindo a concentrao
101) a) K3 = 1,0 1014
de ons CrO42. A diminuio da concentrao de ons
CrO42 desloca o equilbrio de precipitao do BaCrO4
b) 1,0
para a esquerda diminuindo a quantidade do precipitado.
c) No ocorre mudana de nmero de oxidao nas espcies
participantes da reao, portanto a reao no de
oxirreduo. 108) Alternativa: C
109) O valor do pH = 5 indica que o meio est cido, ou
seja, h excesso de H3O+(aq) em relao ao on OH(aq).
[ H 3O ].[ In ] Esse excesso deslocar o equilbrio para a esquerda, com
102) a) Kc =
[ HIn] aumento da concentrao de H2PO4
b) O ponto final da titulao cido-base ocorre quando se
tem a proporo estequiomtrica entre essas substncias, o H2PO4(aq) + H2O(l) HPO42(aq) + H3O+(aq)
que deve ser notado pela mudana de cor do indicador.
1- possibilidade: Adio de uma base a um cido. A Em resumo:
soluo inicialmente cida (portanto incolor) e o ponto de pH = 7 [H2PO4] = [HPO42 ]
equivalncia ser notado quando a soluo ficar rosa, ou (meio neutro)
seja, prevalecer a forma bsica (In).
2- possibilidade: Adio de um cido a uma base. A
soluo inicialmente bsica (predomina a forma ionizada) pH = 5 [H2PO4] > [HPO42 ]
e o ponto de equivalncia ser notado quando a soluo (meio cido)
ficar incolor, indicando que prevalecer a forma cida
(HIn). Dissoluo do KNO3 em gua:
KNO3(s) gua K+(aq) + NO3(aq)
Esquema de um modelo de interaes existentes entre as
espcies qumicas presentes na soluo:
103) Alternativa: C
28 | Projeto Medicina www.projetomedicina.com.br
110) a) O Fe atua como catalisador da reao.
b) A entalpia padro da amnia a 25 C vale -11,02 kcal
mol-1. Explicao: como o valor da entalpia padro de
substncias simples zero, o H da reao a 25 C duas
vezes o valor da entalpia padro da amnia.
c)
Como | KI| > | KII|, podemos concluir que o equilbrio I
i- Uma vez que a reao de formao de amnia (reao
sofre uma maior influncia da variao da temperatura;
direta) exotrmica, pelo Princpio de Le Chatelier, um
aumento na temperatura desloca o equilbrio logo o calor liberado em I ser maior que em II |Q I| > |QII|.
termodinmico da reao para o sentido da reao
endotrmica, ou seja, para a formao de reagentes (N2 e
H2) (reao inversa). 113) a)
ii- Tambm pelo princpio de Le Chatelier, um aumento da Kb = [NH 4 ] [OH-] / [NH3].
presso desloca o equilbrio termodinmico para o sentido Nesse equilbrio, a amnia est em maior concentrao,
da reao envolvendo uma diminuio no nmero de mols, pois se trata de uma base fraca, j que o valor de Kb
ou seja, desloca o equilbrio para o sentido da reao direta muito pequeno (1,8 x 10-5). (Uma base pouco ionizada.)
(de formao de amnia).
Observao - O item poderia ser resolvido usando-se a
expresso da constante de equilbrio e atribuindo-se valores
111) a) Um osso pode ser considerado, a grosso modo, para a concentrao de OH- das seguintes formas ou
como uma mistura de substncias orgnicas (que conferem variantes delas:
flexibilidade a ele) e substncias inorgnicas (que lhe
conferem rigidez).
Kb = [NH 4 ] [OH-] / [NH3] Kb / [OH-] = [NH 4 ] / [NH3]
A adio de cidos desloca esse equilbrio para a direita,
provocando dissoluo da hidroxiapatita, e por isso o osso = 1,8.10-5 / [OH-]
amolece. J o aquecimento provoca a decomposio da
parte orgnica, restando apenas a hidroxiapatita, o que Assim, [NH 4 ] / [NH3] > 1, quando [OH-]< 1,8.10-5, ou
deixa o osso mais quebradio. seja, pOH > 4,75, ou pH< 9,25.
b) Ao se tratar o osso com uma soluo de fluoreto de
sdio, ocorrer uma substituio da hidroxila da Ou [NH 4 ] / [NH3] < 1, quando [OH-] > 1,8.10-5, ou seja,
hidroxiapatita pelo fluoreto, de acordo com a equao: A pOH < 4,75, ou pH > 9,25.
partir desse instante, tem-se no osso a fluorapatita, que no Ou [NH 4 ] / [NH3] = 1, quando [OH-] = 1,8.10-5, ou seja,
atacada por cidos; logo, o osso permanecer intacto aps pOH = 4,75, ou pH = 9,25.
a adio de cido frmico. Generalizando, para solues de amnia em gua, prevalece
NH 4 em pHs abaixo de 9,25 e prevalece NH3 em pHs
112) a) Equilbrio I acima de 9,25.
QPI = 500 atm-2 Todas essas possibilidades so vlidas como justificativas.
Como QPI = KI, o equilbrio foi alcanado.
b) A soluo de amnia bsica. O pH estava acima de 8,5
b) Com a elevao da temperatura, tanto K I quanto KII tm e ao berrar sobre o copo, o convidado exalou gs
seus valores diminudos. Logo podemos concluir que as carbnico que, ao se dissolver na soluo, diminuiu o pH
reaes inversas so endotrmicas, portanto as para um valor inferior a 6,8. Dessa forma, o indicador
transformaes de CO e CO2 em CH4 e H2O so mudou da cor vermelha (pH > 8,5) para a cor amarela ( pH
exotrmicas. < 6,8 ).
c) Observando-se o grfico:
Para uma variao na temperatura de 430C a 460C temos:
29 | Projeto Medicina www.projetomedicina.com.br
Você também pode gostar
- Deslocamento de EquilíbrioDocumento29 páginasDeslocamento de EquilíbrioFernandes YoshimotoAinda não há avaliações
- 2012 - TEmescam - Química - Borges - Deslocamento de EquilíbrioDocumento7 páginas2012 - TEmescam - Química - Borges - Deslocamento de EquilíbrioKlebson Santos da SilvaAinda não há avaliações
- Química - Prof. Rafael - Equilíbrio Químico e Deslocamento de EquilíbrioDocumento12 páginasQuímica - Prof. Rafael - Equilíbrio Químico e Deslocamento de EquilíbrioRafael VaristeloAinda não há avaliações
- Fisico Quimica Equilibrio Quimico PDFDocumento20 páginasFisico Quimica Equilibrio Quimico PDFEricson Andre MonteiroAinda não há avaliações
- Fisico Quimica Equilibrio Quimico PDFDocumento20 páginasFisico Quimica Equilibrio Quimico PDFLeonardo PyrrhoAinda não há avaliações
- Equilíbrio QuímicoDocumento4 páginasEquilíbrio Químicolucas_cmaAinda não há avaliações
- Revisao 2 Serie Quim ADocumento7 páginasRevisao 2 Serie Quim AHenrique CaldasAinda não há avaliações
- Espcex - Lista 14 Equilíbrio QuímicoDocumento3 páginasEspcex - Lista 14 Equilíbrio Químico27.marcos9521Ainda não há avaliações
- Exercícios Deslocamento de EquilíbrioDocumento5 páginasExercícios Deslocamento de EquilíbrioBruna FerreiraAinda não há avaliações
- 82336-Lista de Exercicios de Equilibrio QuimicoDocumento4 páginas82336-Lista de Exercicios de Equilibrio QuimicoYasmin silvaAinda não há avaliações
- Aula 07 Especifico VestibularDocumento2 páginasAula 07 Especifico VestibularDiogo MoreiraAinda não há avaliações
- UntitledDocumento4 páginasUntitledGustavo BroedelAinda não há avaliações
- Prof. Rafa - Química - Equilíbrio QuímicoDocumento9 páginasProf. Rafa - Química - Equilíbrio QuímicoRafael VaristeloAinda não há avaliações
- Prova 2 ANO Unidade 2 (QUÌMICA)Documento5 páginasProva 2 ANO Unidade 2 (QUÌMICA)Anna CarllaAinda não há avaliações
- 2º ANO - Equilibrio QuimicoDocumento8 páginas2º ANO - Equilibrio Quimicomatheus xexeuAinda não há avaliações
- Resolvidas - Equilibrio Quimico IDocumento15 páginasResolvidas - Equilibrio Quimico IMariaAinda não há avaliações
- 44.deslocamento de EquilíbrioDocumento23 páginas44.deslocamento de EquilíbrioPaulo VictorAinda não há avaliações
- Exercícios Das Provas Da Unitau - DEMAIS CURSOS - 1 .FaseDocumento9 páginasExercícios Das Provas Da Unitau - DEMAIS CURSOS - 1 .FaseAshkittenAinda não há avaliações
- Lista de Exercicio 1 Equilbrio QumicoDocumento3 páginasLista de Exercicio 1 Equilbrio QumicoGuilherme VieiraAinda não há avaliações
- Lista Sobre Equilíbrio Químico Química Geral PresençaDocumento4 páginasLista Sobre Equilíbrio Químico Química Geral PresençaAriélly RolimAinda não há avaliações
- Exercicios de Forças e NoxDocumento8 páginasExercicios de Forças e NoxpedromsjAinda não há avaliações
- 5º Teste 3º P 11º A 18-19 v9Documento5 páginas5º Teste 3º P 11º A 18-19 v9sofiaAinda não há avaliações
- Lista de Exercicios - Equilibrios - Acidez e Basicidade - Quimica GeralDocumento4 páginasLista de Exercicios - Equilibrios - Acidez e Basicidade - Quimica GeralBruno Leandro VieiraAinda não há avaliações
- Físico-Química - Cinética Química (20 Questões)Documento10 páginasFísico-Química - Cinética Química (20 Questões)Ciencias PPT100% (1)
- Provbim2ºano3 Etcmm 22Documento5 páginasProvbim2ºano3 Etcmm 22Daniel SousaAinda não há avaliações
- DF Quimica Ita 5ebbd95959f26Documento7 páginasDF Quimica Ita 5ebbd95959f26Vitor BernardesAinda não há avaliações
- Exercicios Estequio InorganicaDocumento17 páginasExercicios Estequio Inorganicaanon-430322100% (2)
- Equilíbrio Químico - Hidrólise - 99 QuestõesDocumento39 páginasEquilíbrio Químico - Hidrólise - 99 QuestõesFrancivaldo BalbinoAinda não há avaliações
- Questionario 02 - Equilibrio Quimico - RESPOSTASDocumento5 páginasQuestionario 02 - Equilibrio Quimico - RESPOSTASmisaelinacioAinda não há avaliações
- Class AppDocumento5 páginasClass AppThaayna BarroosAinda não há avaliações
- Equilibrio Quimico Questoes ObjetivasDocumento14 páginasEquilibrio Quimico Questoes ObjetivasharoldoalencarAinda não há avaliações
- 1º Lista de Exercícios - Equilibrio 2021-2Documento8 páginas1º Lista de Exercícios - Equilibrio 2021-2bernardo garciaAinda não há avaliações
- Revisão Unesp 2021Documento7 páginasRevisão Unesp 2021ALLANA OLIVEIRAAinda não há avaliações
- Equilíbio Químico e Constantes de EquilíbrioDocumento13 páginasEquilíbio Químico e Constantes de EquilíbrioRenato SouzaAinda não há avaliações
- Teste 3 - CeppeaDocumento4 páginasTeste 3 - CeppeaMartins AiupaAinda não há avaliações
- Lista de Exercícios - Deslocamento de EquilíbrioDocumento21 páginasLista de Exercícios - Deslocamento de EquilíbrioAlielson BotelhoAinda não há avaliações
- Lista de Exercícios II - Equilíbrio QuímicoDocumento6 páginasLista de Exercícios II - Equilíbrio QuímicoErenilson SantosAinda não há avaliações
- Lista de Exercícios - Ácidos e Bases - Equilíbrio QuímicoDocumento4 páginasLista de Exercícios - Ácidos e Bases - Equilíbrio Químiconãoimporta doiAinda não há avaliações
- ListaequilibrioDocumento17 páginasListaequilibriolinynhaline100% (1)
- Lista de Equilíbrio Químico 22Documento5 páginasLista de Equilíbrio Químico 22TORRES PREPARATÓRIO MILITARAinda não há avaliações
- Equilibrios ConstantesDocumento6 páginasEquilibrios ConstantesFred DiasAinda não há avaliações
- Questões - Equilíbrio Químico e IônicoDocumento20 páginasQuestões - Equilíbrio Químico e IônicoMariana BarçanteAinda não há avaliações
- Equi Lib RioDocumento3 páginasEqui Lib RioJhennifer FonsecaAinda não há avaliações
- EXERCÍCIOS - Estequiometria - FULL 2017.1Documento8 páginasEXERCÍCIOS - Estequiometria - FULL 2017.1Ale WentzAinda não há avaliações
- Teste 1Documento8 páginasTeste 1Claudia QueirosAinda não há avaliações
- 4teste - 11º Ano V1-1101 VFFDocumento6 páginas4teste - 11º Ano V1-1101 VFFSofia DiasAinda não há avaliações
- Lista de Exercícios - Equilíbrio QuímicoDocumento7 páginasLista de Exercícios - Equilíbrio QuímicoIzabelleAinda não há avaliações
- 42 20termoqu C3 ADmica 20IVDocumento13 páginas42 20termoqu C3 ADmica 20IVTito EdsonAinda não há avaliações
- Resolução: Resposta: ADocumento6 páginasResolução: Resposta: AIsadora HaupenthalAinda não há avaliações
- Revisão Da Av Trimestral 3º TRIM - 231117 - 155919Documento5 páginasRevisão Da Av Trimestral 3º TRIM - 231117 - 155919pvictorsoares29Ainda não há avaliações
- Equilíbrio Iônico - Ime - Ita: CO HO HCO HCO H + +Documento34 páginasEquilíbrio Iônico - Ime - Ita: CO HO HCO HCO H + +GuiAinda não há avaliações
- Específica Uece Prof. Eduardo CostaDocumento8 páginasEspecífica Uece Prof. Eduardo CostaEduardo CostaAinda não há avaliações
- Texto Editora - Teste 1 (2023) - QuímicaDocumento6 páginasTexto Editora - Teste 1 (2023) - QuímicaLuis VarelaAinda não há avaliações
- Quim EspcexDocumento25 páginasQuim EspcexAna Paula Machado0% (1)
- Ita Quimica 1969Documento8 páginasIta Quimica 1969Diego VidalAinda não há avaliações
- Exercícios de QuímicaDocumento44 páginasExercícios de QuímicaJessé AcácioAinda não há avaliações
- Apostila Química Orgânica: Carbono, Dienos E AromáticosNo EverandApostila Química Orgânica: Carbono, Dienos E AromáticosAinda não há avaliações
- Apostila Química Orgânica: Terpenos E Rotas De SínteseNo EverandApostila Química Orgânica: Terpenos E Rotas De SínteseAinda não há avaliações
- Apresentação: EletrocirurgiaDocumento14 páginasApresentação: EletrocirurgiaAdolfo GomesAinda não há avaliações
- Tarefa C5 CursoDE Quimica 20aulas ProfDocumento16 páginasTarefa C5 CursoDE Quimica 20aulas ProfAdolfo GomesAinda não há avaliações
- Simulado 881 BPA9783Documento69 páginasSimulado 881 BPA9783Adolfo GomesAinda não há avaliações
- Mat 450questoesDocumento53 páginasMat 450questoesAdolfo Gomes100% (1)
- TermoquímicaDocumento8 páginasTermoquímicaFabiano SousaAinda não há avaliações
- Breve Listinha de Exercicios Sobre Coeficiente de SolubilidadeDocumento6 páginasBreve Listinha de Exercicios Sobre Coeficiente de SolubilidadeÉrica LimaAinda não há avaliações
- Atmosfera Radiacao-SolarDocumento14 páginasAtmosfera Radiacao-SolarInês Neves LoioAinda não há avaliações
- Tabela PeriodicaLigacoes QuimicasFinalDocumento33 páginasTabela PeriodicaLigacoes QuimicasFinalMariana CarvalhoAinda não há avaliações
- Alfa GPCDocumento2 páginasAlfa GPCRafaela LopesAinda não há avaliações
- Química Farmacêutica - Práticas 1, 2 e 3Documento9 páginasQuímica Farmacêutica - Práticas 1, 2 e 3JOYCE FAZOLLO FERRAZAinda não há avaliações
- Centro Universitário Franciscano SeminárioDocumento52 páginasCentro Universitário Franciscano SeminárioOmegasGloryAinda não há avaliações
- Produção Do EstirenoDocumento3 páginasProdução Do EstirenoLilianaAinda não há avaliações
- Exercicios Balanço Termico de Caldeira Estequiometria Da CombustãoDocumento4 páginasExercicios Balanço Termico de Caldeira Estequiometria Da CombustãoGabriela SantosAinda não há avaliações
- Aula para Upload Aula7Documento11 páginasAula para Upload Aula7Pércio De JesusAinda não há avaliações
- Materiais de Construção Mecânica 2Documento18 páginasMateriais de Construção Mecânica 2fabiofambhAinda não há avaliações
- P1 - TranscalDocumento6 páginasP1 - TranscalLuís HenriqueAinda não há avaliações
- Reacoes Quimicas1aDocumento20 páginasReacoes Quimicas1aClaudinei MartinsAinda não há avaliações
- Condutividade de EletrólitosDocumento11 páginasCondutividade de EletrólitosadrianoAinda não há avaliações
- Atividade Ligação IônicaDocumento1 páginaAtividade Ligação IônicaProfessora Enaj KarlaAinda não há avaliações
- Aula 8Documento4 páginasAula 8knesonAinda não há avaliações
- Ficha 2 - Humidade AtmosféricaDocumento2 páginasFicha 2 - Humidade AtmosféricaKauannyAinda não há avaliações
- Projeto - Dimensionamento de CompressorDocumento17 páginasProjeto - Dimensionamento de CompressordanielfortalAinda não há avaliações
- Beneficiamentos TêxteisDocumento217 páginasBeneficiamentos TêxteisFernando Monteiro100% (6)
- Data Sheet KlingerDocumento1 páginaData Sheet KlingerantonyAinda não há avaliações
- Resumo de Formulas de Termodinâmica AplicadaDocumento6 páginasResumo de Formulas de Termodinâmica AplicadaFabricio MartinsAinda não há avaliações
- Doq Cgcre 54 - 01 Term. InfravermelhoDocumento22 páginasDoq Cgcre 54 - 01 Term. InfravermelhoLucas RamosAinda não há avaliações
- Relatório Laboratorial - Acido Forte - Base ForteDocumento12 páginasRelatório Laboratorial - Acido Forte - Base ForteSofiaPinheiro100% (2)
- Apostila de Operações Unitárias I - Valdir PDFDocumento65 páginasApostila de Operações Unitárias I - Valdir PDFDyogo Mondego Moraes0% (1)
- TERMOGRAFIADocumento6 páginasTERMOGRAFIABRUNO HENRIQUE FERNANDES DA COSTAAinda não há avaliações
- Borges Quimica Exercicios Calculos Quimicos 060308Documento1 páginaBorges Quimica Exercicios Calculos Quimicos 060308Fernandes YoshimotoAinda não há avaliações
- Energia BermoDocumento17 páginasEnergia BermoAlex LopesAinda não há avaliações
- Relatório 3 e 4Documento9 páginasRelatório 3 e 4Thais AntunesAinda não há avaliações