Escolar Documentos
Profissional Documentos
Cultura Documentos
Apostila
Enviado por
Jonathan Silva DuarteDireitos autorais
Formatos disponíveis
Compartilhar este documento
Compartilhar ou incorporar documento
Você considera este documento útil?
Este conteúdo é inapropriado?
Denunciar este documentoDireitos autorais:
Formatos disponíveis
Apostila
Enviado por
Jonathan Silva DuarteDireitos autorais:
Formatos disponíveis
TRANSFORMAES BIOQUMICAS
Guia de Normas e Experimentos
3 quadrimestre/2013
Coordenao: Prof. Dr. Tiago Rodrigues
Autores: Ncleo Docente da UFABC
2013
AULA CONTEDO
Introduo
Experimento 1
Apresentao e Disposies Gerais do Curso Experimental
Uso e Calibrao de Micropipetadores
Experimento 2 Espectrofotometria: Conceitos e Aplicao
Experimento 3 Aminocidos: Estudo da Estrutura e Propriedade cido-Base
Experimento 4 Desnaturao e Precipitao de Protenas: Atividade
Enzimtica Presente no Suco do Abacaxi sobre Gelatina
(Colgeno)
Experimento 5 Extrao e Caracterizao de Lipdios
Experimento 6 Extrao e Caracterizao Bioqumica do Amido da Batata:
Reao com Iodo e Poder Redutor de Carboidratos
!"#$%&'
APRESENTAO
A disciplina Transformaes Bioqumicas composta por aulas expositivas em sala
de aula e por aulas prticas nos laboratrios didticos. Este guia traz ao estudante o contedo
das aulas prticas, com introduo, objetivos, procedimentos e normas que regem a execuo
destas atividades.
OBJETIVOS E COMPETNCIAS
Os mdulos prticos desta disciplina tm como objetivo apresentar uma seqncia de
experimentos que permitir ao aluno identificar aspectos estruturais, funcionais e de
reatividade de aminocidos, carboidratos, lipdeos e enzimas.
Espera-se que, aps a realizao das aulas prticas, o aluno seja capaz de compreender
os conceitos fundamentais das Transformaes Bioqumicas, fazendo a conexo entre o
macroscpico, acessvel aos nossos sentidos, e os eventos que ocorrem em escala molecular.
AULAS PRTICAS
Existem normas de segurana para o trabalho em laboratrio que devem ser
seguidas e respeitadas. Um conjunto destas normas ser entregue ao aluno no incio das
aulas de laboratrio juntamente com um termo de compromisso (caso no o tenha recebido
em disciplina anterior) no qual o aluno se compromete a ler e seguir as mesmas. Todos os
trabalhos em laboratrio sero realizados por equipes de no mximo 5 alunos. Espera-se que
os resultados obtidos sejam obra de um esforo conjunto e que todos os componentes estejam
presentes na hora marcada para o incio das aulas. Haver uma tolerncia de 10 minutos e
)*%+,+-./01' + 2&,*',&03+, 4+%/&, 5' 6"%,' 78*+%&#+-./9
aps esse tempo os alunos retardatrios no podero realizar as atividades do dia. A aula ser
encerrada no horrio pr-estabelecido, no havendo prorrogao para os alunos que no
tenham concludo os experimentos dentro do prazo previsto por motivos alheios prtica.
IMPORTANTE: No haver reposio de experimentos no caso de falta, ficando o aluno
prejudicado com o aprendizado daquele contedo.
AVALIAO
Para a avaliao das atividades prticas, ser utilizado o contedo do caderno de
laboratrio elaborado individualmente pelo aluno sobre cada experimento. O aluno dever
fazer um pr-relatrio no caderno anteriormente a aula em questo e utiliz-lo para as
anotaes durante a aula, bem como as anotaes referentes discusso dos resultados
obtidos. Esse caderno deve ser apenas manuscrito e no poder conter cpia xerogrfica do
caderno dos colegas ou de qualquer outro material. O aluno no poder participar, em
hiptese alguma, da aula prtica sem o caderno de laboratrio contendo o pr-relatrio.
O aprendizado na disciplina de Transformaes Bioqumicas ser avaliado continuamente ao
longo da disciplina pelo acompanhamento direto do docente e tambm ao final por meio de
provas tericas e prticas. O componente da teoria da nota final ter peso 6 e o prtico, peso 4.
A prova prtica envolver a execuo de experimentos no laboratrio e resposta a questes
propostas durante a execuo.
Alunos com rendimento igual ou superior a 86% obtero conceito A; com rendimento
entre 70 e 85%, conceito B; com rendimento entre 56 e 70%, conceito C; de 50 a 55%,
conceito D e rendimento inferior a 50% com conceito F. O aluno reprovado (conceito F)
poder fazer EXAME com o contedo todo do quadrimestre, cuja nota constituir uma
nova mdia aritmtica com a mdia quadrimestral obtida previamente para chegar em
seu conceito final.
RECOMENDAES PARA AS AULAS EXPERIMENTAIS
1. obrigatrio o uso de avental (jaleco) no laboratrio; o mesmo deve ser comprido, de
mangas compridas e ser usado fechado (com os botes fechados);
2. No ser permitido fazer a aula de laboratrio usando sandlias, bermudas, shorts ou saia;
3. No permitida a execuo da aula de Transformaes Bioqumicas de bon, culos
escuros nos olhos ou na cabea e fones de ouvido;
4. proibido comer ou beber no laboratrio;
5. Proibido o uso de telefone celular durante as aulas de Transformaes Bioqumicas;
5. Cabelos compridos devem estar devidamente presos;
5. No dia da aula experimental todos devem apresentar um fluxograma individual (PR-
RELATRIO) e feito mo no caderno de laboratrio para dar incio aula, sendo que o
mesmo poder ser utilizado durante a execuo do experimento;
5. Evitar ao mximo faltar ou chegar atrasado s aulas prticas para no ser prejudicado;
6. O aluno que faltou em aula prtica ter prejuzo no componente da parte prtica da nota e
nos seus conhecimentos daquele tpico, uma vez que no h possibilidade de reposio da
aula;
Modelo de Fluxograma
O fluxograma pode ser feito de maneira esquemtica ou na forma descritiva.
O objetivo fazer com que todos leiam os contedos do experimento e resumam as
atividades experimentais, ou seja, cheguem sabendo exatamente o que ser feito.
Sem o fluxograma no ser permitido realizar a aula experimental.
Modelo de Fluxograma 2: Descritivo
Modelo de Fluxograma 1: Esquemtico
Experimento 1 Parte 1:
Abstract
The purpose of this didactic experiment is to make students of Biochemical Transformations
have the knowledge of correct use of micropipettes, pipetting modes applied to normal, volatile,
foaming and viscous liquids, precision limits, and pipette calibration tests.
Resumo
Este experimento didtico tem como proposta fazer com que os estudantes de Transformaes
Bioqumicas tenham conhecimento e desenvolvam a habilidade do uso correto de micropipetas, modos
de pipetagem dos lquidos normais, volteis, espumantes e viscosos, limites de preciso e testes da
calibrao de pipetas.
Introduo
A transferncia de volume exato de lquidos fundamental para vasta maioria dos
experimentos nas reas de bioqumica, biologia molecular, qumica, etc. De uma maneira geral, o
conhecimento sobre o pipetamento de lquidos, a compreenso de seus limites de preciso, bem como
o estudo de sua importncia na execuo reprodutvel de experimentos justifica a relevncia e
abordagem deste tema nesta aula do curso de Transformaes Bioqumicas da UFABC.
Fundamentao Terica
Pipetas automticas
Micropipetas so aparelhos designados para a transferncia de pequenos volumes
(entre 0,2 a 5000 l) com mxima preciso. A construo das micropipetas consiste em um
corpo anatmico de polipropileno (autoclavvel) equipado com um boto dispensador e um
ejetor de ponteiras no topo, um indicador de volume na lateral e uma haste para encaixe de
ponteiras descartveis na parte inferior. Existem vrios tipos de micropipetas:
pipetas monocanal ou multicanal
pipetas com volume fixo ou com volume varivel
pipetas com deslocamento de ar ou com deslocamento positivo
Experimento 1 Uso e Calibrao de Micropipetadores
Funcionamento de micropipetas com deslocamento de ar
Este tipo de pipetas o mais utilizado, por ser muito verstil. O boto dispensador
ligado a um pisto dentro da pipeta. Ao pressionar o boto, o pisto se move deslocando o ar
que por sua vez desloca um lquido para dentro ou para fora da ponteira. A trajetria de boto
dispensador tem dois estgios que podem ser percebidos por diferena da resistncia de molas
que retornam o boto dispensador para posio de repouso aps ele ser liberado. Os dois
estgios permitem fazer a pipetagem usando duas tcnicas diferentes: a pipetagem direta
(esgotamento total) ou a pipetagem reversa (esgotamento parcial). A escolha da tcnica
depende das caractersticas do lquido a ser pipetado (viscosidade, volatilidade,
hidrofilicidade) e do processo da pipetagem (pipetagem nica, titulante ou repetida).
A preciso da pipetagem influenciada por vrios fatores:
- encaixe da ponteira na haste: antes de pipetar, a compatibilidade do tipo de ponteira
(fabricante) com o tipo de haste deve ser verificada para evitar passagem de ar no encaixe. A
ponteira deve ser encaixada por movimento circular que assegura boa vedao entre a
ponteira e a haste, alm de maior durabilidade pelo uso correto da haste. Por estas razes, o
encaixe da ponteira por batimentos repetidos de haste na ponteira deve ser evitado.
- ajuste de volume (pipetas com volume varivel): cada indicador de volume tem uma
pequena folga. Assim, para a maior preciso, o volume deve ser ajustado sempre e somente de
um lado (de preferncia, no sentido horrio). Quando o ajuste ultrapassa o volume desejado,
recomenda-se voltar <1/3 da rotao e ajustar o volume de novo. Para ajustar corretamente o
volume, deve ser considerado o erro paraltico; o eixo da viso tem que ser perpendicular
escala do indicador do volume.
Figura 1: A - Pipeta de Deslocamento Positivo; B - Pipeta Deslocamento de Ar (monocanal) e C - Pipeta Deslocamento
de Ar (multicanal).
boto dispensador
boto dispensador
haste
Indicador do volume
- a poro imersa no lquido: por causa da compressibilidade do ar, existe uma medida ideal
da imerso da ponta da ponteira que minimiza tais imprecises (Tabela 1).
- tenso lateral do lquido: os lquidos podem molhar a parede da ponteira, o que pode
resultar em perdas de volume ejetado (parte dele fica nas paredes). A minimizao dessa
impreciso consiste em aspirao e ejeo de lquido sem efetuar a transferncia (no mesmo
recipiente). Assim, as paredes j estaro molhadas e o volume da 2
a
aspirao ser transferido
por completo.
- volatilidade do lquido: para diminuir gotejamento do lquido durante a transferncia e
quando a natureza do lquido permite (no corrosivo, no infectante ou no radioativo), o
lquido pode ser aspirado/ejetado no mesmo recipiente vrias vezes at o ar em cima do
lquido ser trocado completamente por vapor do lquido.
Pipetagem direta (esgotamento total)
a tcnica de pipetagem mais conhecida. Utiliza-se para transferir volumes nicos de
lquidos aquosos ou de lquidos no volteis, no viscosos e no espumantes. O princpio de
transferncia de lquido mostrado na Figura 2:
Figura 2: Esquema de procedimento usado por a tcnica de pipetagem direta. Linhas pontilhadas representam
as posies de boto de esgotamento: Repouso (linha superior), 1
o
estgio (linha no meio) e 2
o
estgio (linha
inferior).
Tabela 1: Imerso ideal da ponta da ponteira em relao do tipo de ponteira - volume pipetado
Pipetagem reversa (esgotamento parcial)
uma tcnica de pipetagem pouco conhecida. Recomenda-se fortemente o uso desta
tcnica em casos de pipetagem de lquidos viscosos, volteis e espumantes. Uso da pipetagem
reversa em casos de pipetagem repetida de um volume do mesmo lquido (por exemplo, em
dosagens de protena amostra e curva padro) pode melhorar a confiabilidade do mtodo at
10 vezes.
A transferncia de lquidos por esta tcnica resulta em um volume que sobra na
ponteira aps da transferncia que pode ser uma desvantagem caso de lquidos caros ou de
volume limitado. Porm, a grande vantagem consiste em ejeo de lquido viscoso ou
espumante, onde praticamente impossvel realizar o esgotamento total (da tcnica direta).
Caso de lquidos volteis, a transferncia do lquido pode ser acompanhada por gotejamento
do lquido fora da ponteira (vapor do lquido voltil expande o ar dentro da pipeta). A tcnica
da pipetagem reversa garante um volume de reserva na ponteira que permite a transferncia
de volume correto at de lquido bastante voltil.
O princpio de transferncia de lquido mostrado na Figura 3:
Teste de calibrao
Cada micropipeta calibrada para o valor indicado (valor terico) corresponder ao
valor efetivamente medido (valor real) na faixa da preciso de micropipeta (erro 2% para
pipetas P10, P20, P100, P200, P1000 e 5% para pipetas P2 e P5000). Porm, com tempo e
uso prolongado, os componentes mecnicos so sujeitos ao desgaste ou disfuno resultante
de uso inadequado.
Figura 3: Esquema de procedimento usado por a tcnica de pipetagem reversa. Linhas pontilhadas representam
as posies de boto de esgotamento: Repouso (linha superior), 1
o
estgio (linha no meio) e 2
o
estgio (linha
inferior)
A medio de volume um passo importante em qualquer laboratrio porque um
pequeno erro de pipetagem pode causar um erro significativo no resultado obtido. Assim,
essencial a verificao da calibrao das micropipetas nas mesmas condies em que so
utilizadas no laboratrio. Esta verificao consiste essencialmente em um conjunto de
medies usadas para restabelecer/atualizar a relao entre o valor indicado e o valor
efetivamente medido.
Normalmente, a verificao deve ser realizada nas seguintes situaes:
- aps uma manuteno e/ou troca de peas;
- aps de um perodo de uso (~ 1 ano);
- quando a pipeta sofre um dano: queda, contaminao da haste, etc;
- de acordo com orientaes do fabricante;
Empregam-se geralmente trs mtodos de calibrao de pipetas automticas:
1. Mtodo gravimtrico: uma srie de medies do peso de lquido pipetado (considerando a
temperatura, umidade, presso atmosfrica e coeficiente de expanso) posteriormente
convertida em volume. Este mtodo realizado por laboratrios de
calibrao especializados.
2. Mtodo titrimtrico: uma srie de medies de quantidades de NaOH com concentrao
conhecida em volumes pipetados (sem interferncia da temperatura, umidade ou presso
atmosfrica). Exige uma padronizao das solues envolvidas.
3. Mtodo fotomtrico: uma srie de medies fotomtricas de diferentes diluies de um
cromforo com concentrao conhecida. Este mtodo pode ser facilmente implantado no
laboratrio.
Para a anlise dos resultados da calibrao, as sries de medies so convertidas para
volume (valor efetivamente medido) e comparados com volumes ajustados no indicador da
micropipeta (valores indicados). Calcula-se uma mdia (para mesmos volumes) ou regresso
linear (para volumes diferentes) desvio padro.
Objetivo Geral
Aprender o modo de pipetagem direta (esgotamento total) no modo positivo,
determinar o limite de preciso de micropipetas e testar a sua calibrao (volume real).
Materiais
gua destilada
1 unidade de micropipeta automtica de volume varivel por grupo (P100, P200 ou
P1000)
Balana de preciso de 1 mg (3 ou 4 casas decimais)
Ponteiras
1 bquer de 50 mL
Papel absorvente
Procedimento
Para as pipetagens utilize a micropipeta de volume varivel disponvel para o seu grup
(P100, P200 ou P1000).
1) Determine a massa do bquer seco e anote. Sem retirar o bquer da balana, execute o
item 2. Evite manusear o bquer durante a pesagem para os resduos das mos
(gorduras, ceras, cosmticos) no interferirem com a massa real.
2) Pipete gua com volume mximo (nominal) da micropipeta no modo positivo para o
bquer e pese o bquer com o lquido. Anote o peso na tabela. Repita este passo
10 vezes.
3) Repita o item 1 e pipete gua com 50% do volume mximo (nominal) da micropipeta
no modo positivo para o bquer e pese o bquer com o lquido. Anote o peso na
tabela. Repita este passo 10 vezes.
4) Repita o item 1 e pipete gua com 40%, 60%, 80% e 100% do volume mximo
(nominal) da micropipeta no modo positivo, ajustando o volume sempre no sentido
horrio, para o bquer e pese o bquer com o lquido. Anote o peso na tabela.
5) Repita o item 4, ajustando o volume aleatoriamente, isto , 2 volumes (a sua escolha)
no sentido horrio e 2 volumes restantes no sentido anti-horrio.
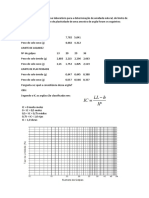
Anlise dos dados
Fazer uma tabela contendo os valores de massa de cada pipetagem.
Fazer grficos dos valores de peso de pipetagem de gua com volumes 100% e 50%
do volume nominal da micropipeta.
Fazer anlise da variao de volume por pipetagem. Expresse o valor mdio do
volume pipetado erro padro. Discuta a preciso da calibrao da pipeta (diferena
do volume mdio determinado experimentalmente com o volume garantido pelo
fabricante).
Discuta a importncia de tipo de ajuste de um lado s do volume no marcador da
pipeta em relao da preciso da pipetagem e compare o volume real com volume
ajustado.
Abstract
The light absorption phenomenon directly by macromolecules or chromophores
formed by secondary reactions is used by spectral characterization and/or quantification of
such substances through spectrophotometry. The purpose of this experiment is to present UV-
vis electronic absorption spectrometry technique applied to Biochemistry, exploring the
Lambert-Beers law. To this class, it will be used Biuret method to protein quantification,
firstly determining the wavelength of maximum absorbance of the cromophore to build a
standard curve for the molar extinction coefficient calculation that will be used after to
determine the concentration of an unknown sample.
Resumo
O fenmeno de absoro de luz diretamente por macromolculas ou cromforos
formados por reaes secundrias usado para caracterizao espectral e/ou quantificao
dessas substncias por espectrofotometria. Este experimento didtico tem como proposta
apresentar a tcnica de espectrometria de absoro eletrnica no UV-vis aplicada
Bioqumica, explorando a Lei de Lambert-Beer. Para esta aula, ser usado o mtodo do
Biureto para quantificao de protenas, primeiramente determinando o comprimento de onda
de mxima absoro do cromforo para se construir uma curva-padro (curva de calibrao).
Esta curva ser usada para a determinao da concentrao de protenas de uma amostra
desconhecida.
Experimento 2 Espectrofotometria: Conceitos e Aplicao
Introduo
O termo medida fotomtrica foi definido originalmente como o ato de medir a
intensidade da luz, independente do comprimento de onda (energia). A maioria dos
instrumentos tem, contudo, mecanismos para isolar uma faixa estreita de comprimentos de
onda do espectro. Os instrumentos que usam filtros para esse propsito so referidos como
fotmetros de filtro ou colormetros e os que utilizam prismas ou grades de difreo so
chamados de espectrofotmetros.
Comprimento de onda refere-se a distncia entre dois picos da propagao da luz que
ocorre na forma de onda, e essa distncia normente dada em nanmetros (nm). A radiao
eletromagntica inclui desde a energia radiante dos comprimentos de onda curtos dos raios
aos comprimentos de onda longos das ondas de rdio. O termo luz usado para descrever a
energia dos comprimentos de onda visveis ao olho humano e queles limtrofes. O olho
humano capaz de detectar comprimentos de onda entre 380 e 750 nm, entretanto
espectrofotmetros so capazes de medir tambm comprimentos de onda mais curtos (ultra-
violeta, UV) ou mais longos (infra-vermelho, IV) (Fig. 1).
Fig. 1. Espectro eletromagntico evidenciando a faixa dos comprimentos de onda visveis. (fonte:
http://www.arq.ufsc.br/labcon/arq5656/Curso_Iluminacao/07_cores/luz_01.htm e
http://www.wordpress.com/2009/03/teoriadacor_01.jpg).
A espectrofotometria um dos mtodos pticos de anlises mais usados nas
investigaes bioqumicas (Fig. 2). O espectrofotmetro um instrumento que permite
comparar a intensidade de luz absorvida ou transmitida por uma soluo que contm uma
quantidade desconhecida de soluto, e uma quantidade conhecida da mesma substncia. Todas
as substncias podem absorver energia radiante, como por exemplo, a gua que absorve
fortemente na regio do IV. A absoro das radiaes ultravioletas, visveis e infravermelhas
dependem da estrutura molecular e caracterstica para cada substncia qumica. Quando a
luz atravessa uma soluo de determinada substncia, parte da energia absorvida
(absorbncia). A cor das substncias se deve a no absoro (transmitncia) de certos
comprimentos de ondas da luz branca que incide sobre elas, deixando transmitir aos nossos
olhos apenas aqueles comprimentos de ondas no absorvidos. Esse fenmeno pode ser usado
para quantificao de substncias por meio da intensidade de absorbncia em um
comprimento de onda especfico, com base em uma curva-padro, utilizando-se da Lei de
Lambert-Beer (PUNGOR, 1995).
Fig. 2. Esquema ptico simplificado de um espectrofotmetro. (fonte:
http://www.ufpa.br/ccen/quimica/espect2.jpg)
Fundamentao Terica
Considere um feixe de luz incidente com intensidade I
o
passando por uma cubeta
contendo uma soluo de uma determinada substncia que absorve luz de certo comprimento
de onda (Fig. 3). A intensidade do feixe de luz transmitido (I) ser sempre menor que I
o
,
sendo que a transmitncia (T) definida como uma relao entre a intensidade da luz
transmitida e a intensidade da luz incidente (Lei de Beer).
T = I/I
o
Fig. 3. Esquema demonstrando a incidncia de um feixe de luz em
uma cubeta e sua transmitncia.
(fonte:http://upload.wikimedia.org/wikipedia/commons/thumb/0/04/B
eer_lambert.png/300px-Beer_lambert.png)
medida que aumentamos a concentrao da substncia em soluo, a transmitncia
varia em relao inversa ao logaritmo da concentrao. Em conseqncia disso, pode-se
definir um novo termo, absorbncia (A), que ser diretamente proporcional concentrao.
Portanto,
A = log I/I
o
= log T
A = log 1/T
Dessa forma, a absorbncia direta e linearmente proporcional concentrao. Esta
varia tambm de forma direta com o caminho ptico (dimetro interno) da cubeta, ou seja, se
dobrarmos o caminho ptico mantendo a concentrao constante, teremos um valor de
absorbncia duas vezes maior. Essa relao frequentemente referida como Lei de Lambert-
Beer:
A = a.b.c
Onde A = abosrbncia, a = constante de proporcionalidade (absortividade ou
coeficiente de extino), b = caminho ptico (em centmetros) e c = concentrao. Como os
valores de A so adimensionais, a unidade de a so as recprocas daquelas para b e c. Quando
b = 1 cm (geralmente ) e c expresso em mol/L, a constante a pode ser chamada de
absortividade ou coeficiente de extino molar (, epsilon) e constante para dado
comprimento de onda, temperatura, pH, solvente, etc.
Assim, a proporcionalidade direta entre absorbncia e concentrao pode ser usada
para a determinao da absortividade de uma determinada substncia em determinada
condio experimental por meio de realizao de uma curva-padro. Para a construo dessa
curva, solues de concentraes conhecidas da substncia devem ser preparadas e as
absorbncias determinadas em determinado comprimento de onda. Posteriormente, essa
absortividade pode ser utilizada para quantificao dessa substncia em uma soluo, cuja
concentrao desconhecida (VOET & VOET, 2006).
Objetivo Geral
Introduzir os conceitos de espectrofotometria ao aluno utilizando como exemplo a
dosagem de protenas em uma amostra pelo mtodo do Biureto.
Objetivos especficos
1. Determinar o espectro de absoro UV-visvel do complexo formado entre os ons Cu
2+
presentes no reagente de Biureto e as protenas.
2. Utilizar o comprimento de onda de absorbncia mxima para a elaborao de uma curva-
padro e determinao da absortividade.
3. Calcular a concentrao protena de uma soluo de albumina.
Materiais
Reagente de Biureto
H
2
O destilada
espectrofotmetros
cubetas
papel absorvente macio para limpeza das cubetas
2 pipetas volumtricas de 2 mL
pera
estante com 2 tubos de ensaio + 9 tubos de ensaio
agitador tipo vrtex
Solues-padro de soro albumina bovina (BSA) com as seguintes concentraes em
% (m/v): 0,125; 0,25; 0,5; 0,75; 1,0; 1,25 e 1,75.
amostra de concentrao desconhecida
Procedimento
As solues a serem utilizadas sero previamente preparadas pelos colaboradores da
disciplina ou preparadas pelos estudantes dependendo da disponibilidade de tempo. Caso
sejam fornecidas aos estudantes solues prontas, os mesmos devero apresentar os clculos
para a preparao de todas as solues envolvidas no experimento, admitindo a preparao de
1 mL de cada soluo-padro e 100 mL da soluo de Biureto.
O reagente de Biureto composto por CuSO
4
0,15 % (m/v), tartarato de sdio e
potssio 0,6 % (m/v) e NaOH 0,75 mol/L. Este reagente no deve ser guardado por mais de
30 dias, devido a possibilidade de precipitao do cobre na forma de xidos ou sais
insolveis. As solues de BSA usadas como padro devem ser preparadas com o maior rigor
possvel a fim de garantir a exatido da concentrao desejada.
REAO: Adicionar 0,5 mL da amostra, branco ou padro em cada tubo e completar o
volume para 1,5 mL com H
2
O destilada. Aps agitao, adicionar 1,5 mL do reagente de
Biureto e tornar a agitar. Aps 5 minutos a absorbncia pode ser determinada (Cain &
Skilleter, 1987).
1. Para a determinao do comprimento de onda, inicialmente, deve fazer a reao com a
amostra de concentrao 0,25 %. NO ESQUECER de fazer um tubo branco com a adio de
gua no lugar da amostra. Fazer a aquisio do espectro de varredura (EM
ESPECTROFOTMETRO) da reao obtida com a amostra de concentrao 0,25 % de 400 a
800 nm, de 10 em 10 nm, zerando sempre com o branco a cada mudana de comprimento de
onda.
2. Para a elaborao da curva padro, numerar os nove tubos de ensaio, sendo um branco, oito
padres e uma amostra desconhecida. Realizar a reao de Biureto e determinar a absorbncia
no comprimento de onda onde a absoro mxima, conforme dados obtidos no item 1
acima. Usar os padres para o clculo da absortividade e, aps isso, usar a absortividade para
calcular a concentrao da amostra desconhecida.
Anlise dos dados
1) Demonstrar os clculos para a obteno do reagente Biureto e das solues-padro de
BSA;
2) Plotar a absorbncia da amostra do item 1 em funo do comprimento de onda,
determinando o comprimento de onda de mxima absorbncia;
3) Plotar as absorbncias das solues padro em funo da concentrao e calcular a
absortividade;
4) Determinar a concentrao da amostra desconhecida;
Exerccio: Descreva o princpio do mtodo de Biureto para a dosagem de protenas,
relacionando suas vantagens e desvantagens em relao a outros mtodos para dosagem de
protenas.
Referncias Bibliogrficas
1. PUNGOR, E. A practical guide to instrumental analysis. Boca Raton: CRC Press, c1995.
384 p.
2. VOET, D; VOET, J.G. Bioqumica, 3 ed., Porto Alegre: Artmed, 2006.
3. ZAIA, D.A.M.; ZAIA, C.T.B.V.; LICHTIG, J. Determinao de protenas totais via
espectrofotometria: vantagens e desvantagens dos mtodos existentes. Qum. Nova 21(6):787-
793, 1998.
Abstract
The purpose of this experiment is to introduce structural aspects of the amino acids,
study their properties and structural differences, in order to learn some characteristics of
protein "building blocks" through the acid-base titrations. From the experimental point of
view, will just be used acid-base titration techniques, however, the aim is to illustrate several
characteristics of these compounds, in order to lead the students beyond to the discussion
presented in the practical class.
Resumo
Este experimento didtico tem como proposta fazer com que os estudantes de
Transformaes Bioqumicas tenham contato com os aspectos estruturais dos aminocidos,
estudem suas propriedades e diferenas estruturais e aprendam, por meio de titulao, as
propriedades cido-base das unidades monomricas que constituem as protenas. Do ponto de
vista experimental, sero utilizadas tcnicas simples de titulao cido-base, porm, permitir
que o estudante correlacione diversas caractersticas estruturais destes compostos com seu
comportamento qumico fixando conceitos tericos.
Experimento 3 Aminocidos: Estudo da Estrutura e Propriedade cido-Base.
Introduo
Em qumica, um aminocido qualquer molcula que contm simultaneamente
grupos funcionais amina e cido carboxlico. Em bioqumica, este termo usado como termo
curto e geral para referir os -aminocidos, ou seja, cidos carboxlicos em que as funes
amino esto ligadas s posies (ou posio 2 em relao carboxila).
Na natureza existem cerca de 200-300 aminocidos, entretanto, somente 21 podem ser
metabolizados pelo organismo humano, sendo 20 aqueles que geralmente constituem as
protenas. Dentre estes, 8 so chamados aminocidos essenciais, isto , no podem ser
sintetizados pelo organismo humano, e precisam ser obtidos atravs de alimentos de origem
animal ou vegetal. Os outros 12 aminocidos que geralmente constituem as protenas so
produzidos por grande parte dos organismos superiores e so chamados no essenciais. H
um aminocido, a taurina, que est presente nos organismos superiores, mas no na
constituio das protenas.
Aminocidos essenciais (no sintetizados pelo organismo humano): isoleucina,
leucina, lisina, metionina, fenilalanina, treonina, triptofano e valina.
Aminocidos no-essenciais (sintetizados pelo organismo humano): arginina,
alanina, asparagina, cistena, glicina, glutamina, histidina, prolina, cido asprtico,
cido glutmico, serina e tirosina.
Contudo, esta classificao no pode ser tomada como algo geral para todos os
organismos superiores e em todas as etapas de seus ciclos de vida. Em crianas, por exemplo,
os aminocidos cistena, tirosina, histidina e arginina so considerados semi-essenciais uma
vez que as etapas metablicas para sintetizar estes aminocidos no esto completamente
desenvolvidas. Portanto, esta classificao de essencial e no-essencial no reflete a
importncia destes -aminocidos, uma vez que, todos os 20 -aminocidos so necessrios
na constituio de protenas e peptdeos, conseqentemente, de toda a matria viva.
O aminocido mais simples a glicina (Figura 1), e possui apenas um tomo de
hidrognio em sua cadeia lateral. A alanina vem a seguir, com um grupamento metila.
Cadeias laterais hidrocarbnicas maiores so encontradas na valina, leucina e isoleucina. A
prolina tambm tem uma cadeia lateral aliftica, mas difere dos outros membros do conjunto
dos vinte por sua cadeia lateral ser ligada tanto ao nitrognio quanto ao tomo de carbono .
Esta resultante estrutura cclica influencia fortemente a arquitetura das protenas. Trs
aminocidos com cadeias laterais aromticas fazem parte do conjunto dos vinte. A
fenilalanina contm um substituinte fenila ligado a um grupamento metileno. O anel
aromtico da tirosina contm uma hidroxila, o que torna a tirosina menos hidrofbica do que a
fenilalanina. O triptofano tem um anel indlico ligado a um grupamento metileno. Dois
aminocidos, serina e treonina , contm hidroxilas alifticas, o que as tornam muito mais
hidroflicas e reativas. Vamos agora aos aminocidos com cadeias laterais muito polares,
sendo altamente hidroflicos. A lisina e a arginina tm cargas positivas em pH neutro. A
histidina pode no ter carga ou t-la positiva, dependendo de seu ambiente local. As cadeias
laterais da arginina e da lisina so as mais longas no conjunto dos vinte.
O
OH
NH
2
L-isoleucina
O
OH
NH
2
L-leucina
O
OH
H
2
N
NH
2
L-lisina
O
OH
S
NH
2
L-metionina
OH
O
NH
2
L-fenilalanina
O OH
NH
2
OH
L-treonina
O
OH
HN
NH
2
L-triptof ano
O
OH
NH
2
L-valina
O
OH
NH
2
L-alanina
O
OH
H
2
N
O NH
2
L-aspargina
O
OH
O
HO
NH
2
cido L-asprtico
O
OH HS
NH
2
L-cistena
O
OH
O
HO
NH
2
cido L-glutmico
O
OH H
2
N
O
NH
2
L-glutamina
O
OH
NH
2
glicina
H
N
O
OH
L-prolina
O
OH HO
NH
2
L-serina
O
OH
HO
NH
2
L-tirosina
O
OH
NH
2
N
H
NH
H
2
N
L-arginina
O
OH
N
HN
NH
2
L-histidina
Figura 1. Estrutura dos 20 L-aminocidos encontrados em protenas.
Existem dois aminocidos com cadeias laterais cidas, o cido asprtico e o cido
glutmico. Esses aminocidos so geralmente chamados de aspartato e glutamato para
salientar que suas cadeias laterais tm, quase sempre, cargas negativas no pH fisiolgico. A
glutamina e a asparagina so derivados no carregados de glutamato e aspartato que contm
uma amida terminal em vez de um carboxilato. Sete dos vinte aminocidos tm cadeias
laterais facilmente ionizveis. Um tomo de enxofre est presente nas cadeias laterais de dois
aminocidos. A cistena contm uma sulfidrila (-SH) e a metionina possui um tomo de
enxofre em uma ligao tioter (-S-CH
3
). Ambas as cadeias laterais que contm enxofre so
hidrofbicas. Deve-se destacar que a maioria destes aminocidos presentes em protenas
possui pelo menos um centro quiral definido com estereoqumica (S) com exceo da cistena
que (R) (notaes de Cahn-Ingold-Prelog) e da glicina que no possui centro quiral (Figura
1); ainda, todos os aminocidos comuns em protenas so freqentemente denominados L-
aminocidos, baseados na nomenclatura do gliceraldedo (configuraes de Fisher). Estas
caractersticas conferem a estes compostos uma grande diversidade qumica e estrutural,
permitindo que estes possam constituir uma gama enorme de diferentes protenas com
diferentes arranjos espaciais e as mais diversas funes (Figura 2).
Alguns autores relatam que para formar uma protena necessria uma cadeia com mais
de 70 aminocidos. J os peptdeos (fragmentos de protenas) podem ser formados por dois
ou mais aminocidos.
Figura 2. Esquema representativo dos diferentes nveis de estrutura protica da hemoglobina
(LEHNINGER, NELSON & COX, 2006).
Todos os aminocidos so derivados de intermedirios da gliclise, do ciclo do cido
ctrico (Krebs) ou da via das pentoses. O nitrognio entra nessas vias atravs do glutamato.
H uma grande variao no nvel de complexidade destas vias, sendo que alguns aminocidos
esto a apenas alguns passos enzimticos dos seus precursores e em outros as vias so
complexas, como no caso dos aminocidos aromticos.
De uma maneira geral, o conhecimento sobre as estruturas de aminocidos, a
compreenso de suas peculiaridades estruturais e reacionais, bem como o estudo de sua
importncia na qumica da vida (constituio de protenas) justifica a relevncia e abordagem
deste tema nesta primeira aula do curso de Transformaes Bioqumicas da UFABC.
FUNDAMENTAO TERICA
Propriedades cido-base dos aminocidos
No organismo, os aminocidos existem na forma de zwitterion, ou seja, compostos com
cargas positivas e negativas totalizando uma carga nula (Figura 3).
R
O
O
NH
3
Figura 3. Estrutura de um aminocido na forma de zwitterion.
Quimicamente, os aminocidos podem ser considerados como compostos anfotricos
uma vez que podem atuar como cidos na presena de bases (Equao 1) ou como bases na
presena de cidos (Equao 2), seguindo a definio de Brnsted.
(aq)
R
OH
O
NH
2
OH
(aq) +
(aq)
R
O
O
NH
2
+
H
2
O
(l)
cido
Base
cido
Base
Equao 1. Aminocido atuando como cido.
(aq)
R
OH
O
NH
2
H
3
O
(aq) +
(aq)
R
OH
O
NH
3
+
H
2
O
(l)
cido
Base
cido
Base
Equao 2. Aminocido atuando como base.
Um estudo destas propriedades cido-base pode ser realizado utilizando-se titulaes
partindo-se de aminocidos contidos em solues cidas (completamente protonados na
funo amina). Nestes casos, quando se adiciona base (OH
) na soluo, o pH aumenta
gradativamente, sendo possvel monitorar o seu valor em funo das quantidades adicionadas
pelo o uso de pHmetros ou papel de indicador universal (0-14 unidades). Se forem lanados
em grfico o volume ou numero de mols de base (OH
) em funo do pH da mistura
resultante, possvel obter algumas das propriedades intrnsecas dos aminocidos como o pK
a
(logaritmo negativo da constante de ionizao) e pI (ponto isoeltrico logaritmo negativo do
pH em que os aminocidos esto completamente na forma de zwitterion) (Figura 4).
Figura 4. Curva de Titulao da Alanina.
De uma maneira geral, quando consideramos um cido do tipo HA ionizado em
soluo aquosa (Equao 3), podemos escrever a seguinte equao para descrever o pH do
meio (Equao 4 Equao de Henderson-Hasselbach):
HA
(aq)
+
H
2
O
(l)
H
3
O
(aq)
A
(aq) +
Equao 3. cido de Brnsted em equilbrio aquoso.
pH = pK
a
+ log
[A ]
[HA]
Equao 4. Equao de Henderson-Hasselbach.
Uma anlise simples da equao de HendersonHasselbach pode fornecer o pK
a
de um
determinado cido de Brnsted. Se o termo logartmico da Equao 4 da for igual a 0 (zero),
ou seja, quando as [HA] e [A
] so idnticas no equilbrio, teremos que o pH do meio igual
ao pK
a
(pH = pK
a
).
!"#$%&'() +& ,-,./.,
01$"2&%34#35 +3 67
8
Tomando como exemplo o aminocido alanina (Figura 4), pode-se verificar
experimentalmente que durante sua titulao com base surge um primeiro ponto de inflexo
na curva (ponto (I), pK
a1
) onde as variaes de pH do meio so muito pequenas em funo
das adies de base. Assim, pode-se dizer que as concentraes relativas das espcies em
equilbrio [A
]/[HA] (no caso, considere as duas espcies de aminocidos da Equao 5) no
variam significativamente nas imediaes deste ponto porque o sistema est tamponado. O
ponto de inflexo (II) obtido numa faixa muito pequena da variao da quantidade de base
adicionada, caracterizando o ponto de viragem na titulao da funo cido carboxlico
(funo mais acdica) e neste caso o pI (ponto isoeltrico). No ponto (III), de maneira similar
ao que ocorre para o ponto (I), obtm-se o pK
a2
da funo amina protonada. As Equaes 5 e
6 descrevem os equilbrios das espcies qumicas durante as titulaes.
(aq)
H
3
C
OH
O
NH
3
H
2
O
(l) +
(aq)
H
3
C
O
O
NH
3
+
H
3
O
(aq)
K
a1
Equao 5. Equilbrio envolvido na primeira ionizao.
(aq)
H
3
C
O
O
NH
3
H
2
O
(l)
+
(aq)
H
3
C
O
O
NH
2
+
H
3
O
(aq)
K
a2
Equao 6. Equilbrio envolvido na segunda ionizao.
Objetivo
Determinar os valores de pK
a
de aminocidos por titulaes cido-base. Construir os
grficos e comparar os perfis das curvas, correlacionando os valores de pK
a
. Estudar as
estruturas dos aminocidos por meio de exerccios com as estruturas moleculares em 3
dimenses.
Materiais
Solues 0,05 mol/L de glicina, arginina e cido glutmico.
Soluo 4 mol/L de HCl
Soluo 0,125 mol/L de NaOH
pHmetro
1 pipetas volumtricas de 20 mL
1 pipetas de Pasteur
1 Bureta
1 bquer de 100 mL
Procedimento
As solues a serem utilizadas sero previamente preparadas pelos colaboradores da
disciplina ou preparadas pelos estudantes dependendo da disponibilidade de tempo. Caso
sejam fornecidas aos estudantes solues prontas, os mesmos devero apresentar os clculos
para a preparao de todas as solues envolvidas no experimento, admitindo a preparao de
100 mL de cada e partindo dos reagentes comerciais.
Para as titulaes, podero ser utilizados vrios aminocidos, sendo recomendado
didaticamente o uso de glicina, arginina e cido glutmico.
1) Pipete 20 mL de uma soluo 0,05 mol/L da soluo de aminocido e adicione em um
bquer de 100 mL. Insira o eletrodo do pHmetro (devidamente calibrado) no bquer e
faa a medida do pH e anote o valor. Em seguida, acidifique a soluo do aminocido
com HCl 4 mol/L at o pH do meio atingir 1,0. Seja cuidadoso com a adio de cido
para no baixar demasiadamente o pH. Utilize conta-gotas para esta etapa.
2) Em seguida, complete uma bureta de 50 mL com soluo de NaOH 0,125 mol/L e
inicie a titulao adicionando pores de 0,5 mL da base, medindo o pH aps cada
adio. Lembre-se de agitar com cuidado a mistura titulada e ento aferir o pH. (Muito
cuidado ao agitar a soluo para no quebrar o eletrodo do pHmetro!).
3) Efetue adies sucessivas at que o pH do meio atinja valores entre 12,0 a 12,5. Aps
isso, lave o eletrodo com gua destilada e coloque-o imerso na soluo tampo de
armazenamento do eletrodo.
4) Faa o procedimento para um aminocido sugerido. Cada grupo dever titular um
aminocido e os resultados devero ser trocados entre os grupos de modo que cada
grupo possua as trs titulaes para elaborar o relatrio.
Anlise dos dados
1) Uma tabela contendo os valores de pH juntamente com os respectivos volumes de
NaOH adicionados para cada aminocido titulado.
2) Lance em grfico os valores de pH (eixo y) em funo dos volumes da soluo
titulante de NaOH (eixo x). Faa isso para cada aminocido (trs grficos separados) e
depois faa um grfico contendo as trs curvas superpostas.
3) Indique nos grficos lanados individualmente os valores dos pK
a
(pK
a1
, pK
a2
e pK
aR
se houver) e indique o ponto isoeltrico (pI). Obtenha os valores de pK
a
determinados
experimentalmente (localizando os pontos de inflexo na curvas) e compare-os com os
valores de referncia da literatura. (Sugesto: no exerccio localizado no final deste
experimento esto listados todos estes valores de referncia da literatura!)
4) Escreva as equaes de equilbrio (todas as etapas) das espcies qumicas envolvidas
nas titulaes.
5) Faa uma anlise do perfil das curvas obtidas correlacionando com os valores de pK
a
obtidos e as funes orgnicas presentes. Voc acha que se fossem realizadas adies
sucessivas de 0,25 mL de soluo de NaOH seria possvel calcular o valor de pK
a
com
maior preciso? E se fosse utilizada uma soluo 0,1 mol/L de NaOH?
6) No caso especfico do cido glutmico, os primeiros valores de pK
a
so relativamente
difceis de serem obtidos experimentalmente. Explique estes fatos dizendo se as
medidas citadas acima podem melhorar a qualidade da curva e facilitar a obteno
destes valores de pK
a
.
7) Aps construir todas as curvas aponte qual a espcie predominante nas solues
iniciais de aminocidos utilizadas (medida inicial do pH antes da adio do HCl).
Explique suas respostas.
EXERCCIO
Atribua o nome de cada aminocido (como exemplificado para a L-alanina)
comparando as estruturas qumicas (Figura 1) com as projees moleculares 3D abaixo. Nas
estruturas, considere os tomos de carbono em cinza, oxignio em vermelho, nitrognio em
azul, enxofre em amarelo e hidrognio em branco. No se esquea de considerar as mltiplas
ligaes que esto implcitas nestes modelos (por exemplo, uma nica ligao entre um dos
carbonos e um dos oxignios da L-alanina, significando que h uma dupla ligao pois o
oxignio bivalente veja a posio circulada).
-8&%&4"4&
! 4,3 ! 3,9
Referncias Bibliogrficas
1. LEHNINGER, A.L; NELSON, D.L; COX, M.M. Princpios de bioqumica. 4 ed. So
Paulo: Sarvier, 2006. 1202 p.
2. BERG, M.J.; TYMOCZKO, J.L., STRYER, L. Biochemistry 5th. Edition. W. H. Freeman
and Company. New York, 2002.
3. BETTELHEIM, F.A.; LANDESBERG, J.M. Laboratory Experiments for General, Organic
& Biochemistry, Harcourt College Pub, New York, 2000.
4. VOET, D.; VOET, J.G. Bioqumica, 3 ed., Porto Alegre: Artmed, 2006.
Abstract
The first aim of this experiment is to demonstrate the enzyme activity present in
pineapple, these activities promote the degradation of collagen, additionally, the experiment
shows that the proteolytic activity can be destroyed boiling the pineapple juice, probably due
the protein denaturation process caused by the heating. The second aim of this experiment is
to demonstrate the protein precipitation by the addition of alcohol (coagulation) or ammonium
sulfate (salting out) in the collagen solution, showing the modification of protein solubility.
Resumo
O primeiro objetivo desse experimento demonstrar a atividade enzimtica presente
no abacaxi, essas atividades promovem a degradao do colgeno, adicionalmente o
experimento mostra que a atividade proteoltica pode ser destruda pela fervura do suco de
abacaxi, provavelmente devido ao processo de desnaturao protica causado pelo
aquecimento. O segundo objetivo do experimento mostrar a precipitao protica pela
adio de lcool (coagulao) ou sulfato de amnio (salting out) na soluo de colgeno,
mostrando a alterao da solubilidade protica.
Experimento 4 - Desnaturao e Precipitao de Protenas: Atividade Enzimtica
Presente no Suco do Abacaxi sobre Gelatina (Colgeno).
Introduo
Enzimas proteolticas ou proteases catalisam o rompimento das ligaes peptdicas em
protenas. So enzimas da classe 3, as hidrolases, e subclasse 3.4, as peptdeo-hidrolases ou
peptidases. Estas enzimas constituem uma grande famlia (EC 3.4), dividida em
endopeptidases ou proteinases (EC 3.4. 21-99) e exopetidases (EC 3.4.11-19), de acordo com
a posio da ligao peptdica a ser clivada na cadeia peptdica. Estas endopeptidases podem
ser ainda subdivididas de acordo com o grupo reativo no stio ativo envolvido com a catlise
em serina- (EC 3.4.21), cistena- (EC 3.4.22), asprtico-proteinases ou endopeptidases (EC
3.4.23) e metalloproteinases ou metalloendopeptidases (EC 3.4.24). As enzimas cujo
mecanismo de ao no est completamente elucidado so classificadas no subgrupo EC.
3.4.99.
Exopeptidases
As exopeptidases atuam somente nos finais das cadeias polipeptdicas na regio N ou
C terminal. Aquelas que atuam na regio amino terminal livre liberam um nico resduo de
aminocido (aminopeptidases), um dipeptdeo (dipeptidil-peptidases) ou um tripeptdeo
(tripeptidil-peptidases). As exopeptidases que atuam na regio carboxi terminal livre liberam
um nico aminocido (carboxipeptidases) ou um dipeptdeo (peptidil-dipeptidases).
Endopeptidases
Endopeptidases atuam preferencialmente nas regies internas da cadeia polipeptdica,
entre as regies N e C terminal.
Tipos catalticos
Segundo Barret, 1994 as proteases so classificadas em carboxipeptidases e as
endopeptidases e so divididas em subclasses, tendo como base o seu mecanismo cataltico.
As carboxipeptidases foram subdivididas em serino-, metalo- e cisteno- carboxipeptidases e
as endopeptidases em serino-, cisteino-, asprtico- e metaloendopeptidases. Serino peptidases
possuem um resduo de serina em seu centro ativo, enquanto as asprtico-peptidases tm duas
unidades de cido asprtico no seu centro cataltico. Cisteno-proteases apresentam um
aminocido cistena e as metalo-proteases usam um on metal no seu mecanismo cataltico.
Proteases: funo e aplicao
Proteases representam uma classe de enzimas com importantes papis em processos
fisiolgicos. Alm disto, elas possuem aplicao comercial, estando entre os trs maiores
grupos de enzimas industriais, sendo responsveis por 60% da venda internacional de
enzimas. Estas enzimas esto envolvidas em processos biolgicos essenciais, como a
coagulao sangunea, morte celular e diferenciao de tecidos. Vrias etapas proteolticas
importantes ocorrem no mecanismo invasivo de tumores, assim como no ciclo de infeco de
um grande nmero de vrus e microrganismos patognicos. Estes fatos tornam as proteases
um alvo quimioterpico valioso para o desenvolvimento de novos compostos farmacuticos.
As enzimas proteolticas tambm participam no catabolismo de protenas, tanto nas vias
degradativas como nas biossintticas, e na liberao de hormnios peptdeos
farmaceuticamente ativos a partir de protenas precursoras. Certas modificaes especficas e
seletivas de protenas durante a ativao de enzimas ocorrem via protelise, que tambm
colabora no transporte de protenas secretrias na membrana. As proteases tm tambm uma
variedade de aplicaes principalmente na indstria de detergentes e de alimentos. Tendo em
vista os recentes acordos mundiais para uso de tecnologias no poluentes, as proteases
comearam a ser usadas em larga escala no tratamento do couro, em substituio aos
compostos txicos e poluentes at ento usados. Na indstria farmacutica, as proteases so
usadas em pomadas cicatrizantes e tm um uso potencial para outros medicamentos. Proteases
hidrolisam as protenas em peptdeos e aminocidos, facilitando a sua absoro pelas clulas;
devido a seu papel despolimerizante, as enzimas extracelulares tm um papel importante na
nutrio.
Objetivo
Demonstrar a atividade proteoltica presente no suco de abacaxi, o efeito da
desnaturao protica por temperatura e o efeito da alterao de solubilidade protica, e
conseqente precipitao, provocados pela adio de lcool ou sal de amnio em soluo de
gelatina (colgeno).
Materiais
8 tubos de ensaio de 20 mL
1 tubo de ensaio de 30 mL
Estante para tubos de ensaio
Bquer de vidro de 100 mL (para aquecer gua)
Bquer de 25 ou 50 mL (para gua destilada)
Funil de vidro pequeno e papel de filtro, tesoura para cortar o papel de filtro
Recipiente com gelo
Almofariz e pistilo
Pipetadores automticos de 1,0 mL e ponteiras, ou pipetas de vidro de 5,0 mL
Faca ou estilete
Luvas de ltex
Basto de vidro (para dissolver a gelatina)
Placa aquecida ou banho-maria 100C
Banho-maria 60C
Banho-maria 30C
Balana
Reagentes
Soluo de sulfato de amnio 3 mol/L
Etanol absoluto ou comercial 99,3 INPM
Abacaxi maduro (1 fatia mdia)
Gelatina incolor e sem sabor
gua destilada
Procedimento
Parte 1: Atividade enzimtica do suco de abacaxi e desnaturao protica por
aquecimento.
Extrao do suco de abacaxi
Uma fatia de abacaxi deve ser cortada em pequenos pedaos. A extrao do suco ser
feita macerando-se os pedaos utilizando almofariz e pistilo. O suco deve em seguida ser
filtrado utilizando funil de vidro e papel de filtro em um tubo de ensaio de 20 mL. O tubo
dever ser armazenado no gelo.
Preparo da gelatina
Pesar 2 g de gelatina incolor e sem sabor de qualquer marca comercialmente
disponvel e dissolver em 20 mL de gua destilada, em tudo de ensaio de 30 mL, aps
solubilizao a soluo de gelatina deve ser aquecida a 60C e mantida nessa temperatura at
o uso.
Ensaio
Primeiramente, deve-se preparar as amostras de abacaxi. Para isso, utilizando tubos de
ensaio de 20 mL, deve-se pipetar 2,0 mL de gua no tubo 1 e 2,0 mL do extrato de abacaxi
nos tubos 2, 3 e 4. O tubo 2 deve ser mantido temperatura ambiente, o tubo 3 aquecido
60C e o tubo 4 fervido por 5 minutos. Aps este tempo de tratamento de cada uma das
amostras, resfriar no gelo imediatamente por 1 minuto. Aps o resfriamento das amostras
fervidas adicionar em todos os tubos a soluo de gelatina. Homogneizar. Incubar as amostras
por 10 minutos a 37
o
C e em seguida resfriar todas as amostras no gelo por 7 minutos,
observar e anotar o resultado.
Tabela 1. Resumo do procedimento experimental.
Tubo 1 Tubo 2 Tubo 3 Tubo 4
gua 2,0 mL - - -
Amostra Abacaxi - 2,0 mL - -
Amostra Abacaxi 60C - - 2,0 mL -
Amostra Abacaxi Fervida - - - 2,0 mL
Gelatina 2,0 mL 2,0 mL 2,0 mL 2,0 mL
Parte 2: Precipitao de protenas.
Pipetar nos tubos de ensaio de 20 mL os reagentes conforme a tabela 2, realizar o
experimento em temperatura ambiente (~ 25C). Observar e anotar o resultado para posterior
discusso.
Tabela 2. Resumo do procedimento experimental.
Tubo 1 Tubo 2 Tubo 3
gua 2,0 mL - -
Sulfato de amnio - 2,0 mL -
Etanol Absoluto - - 2,0 mL
Gelatina 2,0 mL 2,0 mL 2,0 mL
Anlise dos dados:
1. Prepara uma tabela indicando os resultados observados de cada experimento.
2. Tirar uma fotografia dos resultados para anexar ao relatrio como figura.
3. Discutir o efeito do suco de abacaxi sobre o colgeno (gelatina).
4. Discutir o efeito da temperatura sobre as enzimas (proteases) presentes no suco do abacaxi.
5. Discutir o efeito do etanol e do sulfato de amnio sobre as protenas em soluo. Qual o
princpio de cada efeito.
Para discusso:
1. Pesquisar: qual(is) protease(s) est(o) presente(s) no suco de abacaxi.
2. Como poderia ser realizada a purificao dessa(s) protena(s)?
3. A atividade das proteases pode ser otimizada? Como?
4. Discuta o efeito da temperatura sobre a desnaturao de protenas no processo de
cozimento dos alimentos, qual a importncia disso?
5. Por que se pode utilizar abacaxi para amaciar carnes? Qual a relao entre o suco do
abacaxi e os amaciantes de carnes comerciais.
Referncias Bibliogrficas
URL: http://www.protease.ufrj.br/ProteaseApres.htm
Rawling, N.D., Barret, A. 1994. Families of serine peptidases. Meth. Enzymol. 244:18-61.
Rawling, N.D., Barret, A. 1994. Families of cysteine peptidases. Meth. Enzymol. 244:461-
486.
Rawling, N.D., Barret, A. 1994. Families of aspartic peptidases, and those of unknown
mechanism. Meth. Enzymol. 248:105-120.
Rawling, N.D., Barret, A. 1994. Families of metallopeptidases. Meth. Enzymol. 248:183-228.
Francisco Jr, W.E. et Francisco W. Protenas: hidrlise, precipitao e um tema para o ensino
de qumica. Qumica Nova na Escola, 24, 2006.
Abstract
The aim of this experiment is to introduce the students of the Federal University of
ABC to the procedures related to the extraction and characterization of lipids employing
soybean as a source of triacylglycerol, one type of biologic lipids. Furthermore the students
will learn the saponification concept through the alcaline hydrolysis of soybean
triacylglycerol and the physical and chemical properties of the soap obtained will be
exploited.
Resumo
O presente experimento visa introduo dos alunos de Bacharelado em Cincias e
Tecnologia, da Universidade Federal do ABC, s tcnicas de extrao e caracterizao de
lipdios utilizando soja como fonte de triacilgliceris, um dos tipos de lipdios biolgicos.
Adicionalmente, ser abordado o conceito de saponificao, demonstrado atravs da hidrlise
alcalina dos triacilgliceris obtidos da soja, e sero exploradas as propriedades fsico-
qumicas dos sabes.
Introduo
Os lipdios so representados por um grupo de biomolculas baixa massa molecular
que apresentam estruturas qumicas bastante variadas e so praticamente insolveis em
gua. A diversidade de estruturas apresentadas pelos lipdios faz com que esses compostos
tenham a capacidade de exercer diversas funes biolgicas atuando desde componentes de
membranas celulares, isolantes trmicos, sinalizadores celulares, pigmentos e reservas de
energia (leos e gorduras). Adicionalmente, os prprios lipdios ou seus derivados, podem
tambm exercer funes de vitaminas e hormnios. As principais classes de compostos
pertencentes ao grupo dos lipdios so os triacilgliceris, glicerofosfolipdeos, esfingolipdios,
glicolipdios e esterides (Figura 1).
Experimento 5 - Extrao e Caracterizao de Lipdios
(A)
(B)
Figura 1. As principais classes de lipdios biolgicos. Em (A) todos os lipdios mostrados
apresentam glicerol ou esfingosina, estrutura central, ligados a cidos graxos. (B) Estrutura
de trs hormnios esterides.
Tipicamente, os lipdios apresentam em suas estruturas longas cadeias carbnicas,
como os cidos graxos e isoprenos, ou mltiplos anis interligados, como no caso dos
esterides. Vrias classes de lipdios apresentam cidos graxos como componentes
estruturais. cidos graxos so cidos monocarboxlicos, molculas anfipticas que
apresentam uma regio polar, representada pelo grupo carboxila (ionizado em pH neutro), e
uma regio apolar, representada por uma cadeia carbnica com comprimento variando entre
4 a 36 tomos de carbono (Figura 2). Estruturalmente, a cadeia carbnica dos cidos graxos
caracterizada pela presena de nmero par de carbonos formando uma estrutura no
ramificada que pode ser saturada ou conter uma, duas ou mais insaturaes.
Grupo
carboxila
Cadeia
carbnica
Insaturao
(A) (B)
Figura 2. Estrutura de cidos graxos. Os cidos graxos so compostos anfipticos formados por uma
longa cadeia carbnica apolar e um grupo carboxila polar. As cadeias carbnicas dos cidos graxos
no possuem ramificaes e podem ser saturadas, como no caso do cido esterico, (A) ou
insaturadas, como no caso do cido oleico (B).
Lipdios como triacilgliceris, fosfolipdios, glicolipdios e esfingolipdios apresentam
cidos graxos esterificados em suas estruturas. Uma das funes mais importantes dos cidos
graxos nas clulas a participao na construo das membranas celulares, finas camadas
lipdicas que circundam todas as clulas e suas organelas internas. As membranas celulares
so compostas em grande parte por fosfolipdios, pequenas molculas constitudas
principalmente por cidos graxos e glicerol. Outra importante funo desempenhada pelos
cidos graxos est associada manuteno de uma reserva energtica celular. De fato, os
cidos graxos podem ser estocados no citoplasma celular na forma de gotculas lipdicas
constitudas por molculas de triacilgliceris. Os triacilgliceris, tambm conhecidos como
triglicerdeos, triglicrides ou gorduras neutras, representam os lipdios mais abundantes na
natureza sendo formados pela esterificao de trs cidos graxos a uma molcula de glicerol.
este estabelecimento de ligaes ster entre os precursores polares dos triacilgliceris
(hidroxilas do glicerol e carboxilas dos cidos graxos) que confere ao composto carter
essencialmente apolar, permitindo com que seja armazenado nas clulas de forma
praticamente anidra (Figura 3).
Glicerol
Triacilglicerol
Figura 3. Triacilglicerois so compostos apolares resultantes da formao de ligaes ster entre as
hidroxilas livres de uma molcula de glicerol e os grupos carboxila dos cidos graxos.
As gorduras animais e leos vegetais so misturas de triacilgliceris, que diferem na
sua composio em cidos graxos e, conseqentemente, no seu ponto de fuso. Os
triacilgliceris das gorduras animais so ricos em cidos graxos saturados, o que atribui a
esses lipdeos uma consistncia slida temperatura ambiente. J os triacilgliceris origem
vegetal so ricos em cidos graxos poliinsaturados sendo, portanto, lquidos temperatura
ambiente. Os leos vegetais so utilizados para a fabricao de margarinas atravs de um
processo de hidrogenao que reduz parte de suas duplas ligaes e os torna slidos
temperatura ambiente.
cidos graxos saturados Cadeia carbnica no apresentam ligaes duplas entre
os tomos de carbono e, assim, contem o nmero mximo possvel de hidrognios.
cidos graxos insaturados Cadeia carbnica possui uma ou mais ligaes duplas
entre tomos de carbono contendo o nmero mximo possvel de hidrognios.
Os lipdios anfipticos, tais como os cidos graxos, quando so adicionados a um meio
aquoso, tendem a agregar-se, organizando-se espontaneamente em estruturas
plurimoleculares. Essas estruturas permitem maximizar as interaes hidrofbicas entre as
cadeias carbnicas, isolando-as da gua, e deixar os grupos polares em contato com o
solvente, com o qual podem interagir. Tais arranjos moleculares constituem o estado de
menor energia livre para esses lipdios em gua e resultam da presena de duas regies com
solubilidades diferentes na mesma molcula.
O tipo de estrutura formada determinado pela geometria da molcula do lipdio
anfiptico (Figura 4). Lipdios com uma nica cadeia carbnica, como sabes de detergentes,
devido a forma cnica e afilada de suas molculas, formam, preferencialmente, micelas.
Nesta estrutura esfrica, as cadeias carbnicas organizam-se no interior, isolando-se da gua,
e os grupos polares posicionam-se na superfcie externa, interagindo com o solvente. A
formao de micelas uma etapa importante na digesto dos lipdios da dieta. A maioria dos
fosfolipdios e glicolipdios associam-se em uma camada dupla de molculas, chamada
bicamada lipdica. Esta estrutura permite uma agregao mais estvel das molculas desses
lipdios, que tm forma cilndrica pela presena de duas cadeias apolares.
As molculas de lipdios alinham-se lado a lado, compondo duas monocamadas e as
cadeias carbnicas das monocamadas agrupam-se frente a frente de modo a criar um domnio
hidrofbico no meio da bicamada; os grupos hidroflicos dispem-se na superfcie das duas
faces da bicamada, interagindo com a gua. Bicamadas lipdicas tendem a se converter em
estruturas fechadas, chamadas lipossomos, que so mais estveis porque no apresentam
caudas hidrofbicas expostas ao solvente, como acontece na periferia das bicamadas planas.
Lipossomos so, portanto, vesculas sintticas esfricas formadas por uma bicamada lipdica
contnua, que delimita uma cavidade interna preenchida por solvente.
(A) Micela (B) Bicamada Lipdica (C) Lipossomo
Cavidade Aquosa
Figura 4. Estruturas formadas por lipdios anfipticos em meio aquoso. (A) Micelas so formadas por
molculas de lipdios com uma nica cadeia carbnica, cadeias estas que se localizam no interior
dessas estruturas. (B) Bicamada lipdica uma estrutura bidimensional na qual as cadeias carbnicas
formam um domnio central hidrofbico, isolando-se da gua, exceto nas extremidades da bicamada;
a estrutura comumente formada por lipdios anfipticos com duas cadeias de hidrocarbonetos. (C)
Liposssomo uma vescula oca, resultante do fechamento de uma bicamada lipdica, dotada de uma
cavidade central preenchida por solvente.
1. Fundamentao Terica
Os lipdios representam um grupo de compostos com estrutura bastante variada.
Vrias classes de lipdios apresentam cidos graxos como componentes estruturais entre eles,
os fosfolipdeos, glicolipdeos e os triacilgliceris. Os lipdios podem ser caracterizados por
suas propriedades fsico-qumicas. Em geral, so praticamente insolveis em gua enquanto
apresentam alta solubilidade em solventes orgnicos como clorofrmio, ter, benzeno, mistura
de Folch (clorofrmio:metanol), entre outros.
Os triacilgliceris, que constituem o principal grupo de lipdios, podem ser
hidrolisados liberando cidos graxos e glicerol. Se esta hidrlise feita mediante aquecimento
em meio alcalino (hidrlise alcalina), formam-se sais de cidos graxos (sabes) e o processo
chamado saponificao (Figura 5). Este o princpio da fabricao dos sabes a partir de
gordura animal fervida em presena de NaOH ou KOH.
Triestearina Glicerol Estearato de Sdio
Figura 5. Hidrlise alcalina de triacilgliceris. Triacilgliceris, mediante aquecimento em presena
de bases fortes, como hidrxido de sdio (NaOH) ou hidrxido de potssio (KOH), sofrem hidrlise
produzindo sais de cidos graxos (sabes). No esquema acima mostrada a hidrlise do triestearina
na presena de NaOH dando origem a glicerol e sal sdico (estereato de sdio).
Assim como os cidos graxos, os sabes so molculas anfipticas apresentando em
sua estrutura uma longa cadeia carbnica (cauda apolar, lipoflica) e um grupo carboxilato
(cabea polar, hidroflica). Dessa maneira, os sabes, quando em soluo aquosa, associam-se
por interaes hidrofbicas entre as caudas apolares formando um uma pelcula lipdica na
superfcie do liquido ou dando origem a estruturas como as micelas (Figura 6).
Sabo
Grupo carboxilato
Cadeia carbnica
Micela
Pelcula lipdica
Figura 6. Formao de micelas a partir das interaes entre sabes dispersos em soluo aquosa.
Propriedades dos sabes:
Sob condies especficas, os cidos graxos dos sabes podem ser precipitados. A
adio de cidos fracos, como cido actico, leva a formao de cidos graxos insolveis por
causa do baixo grau de dissociao (Figura 7).
OLEATO DE POTSSIO CIDO ACTICO CIDO OLICO
(precipita)
ACETATO DE
POTSSIO
Figura 7. Precipitao de cidos graxos a partir da hidrlise cida de sabes. Em presena de cido
actico (cido fraco), cido olico (cido graxo) precipitado a partir da hidrlise cida do oleato de
potssio (sabo).
Os sabes precipitam quando so usados em guas ricas em sais de clcio ou magnsio
(guas duras). Os ons clcio e magnsio da gua reagem com cidos graxos formando sais
insolveis. Os sabes tambm podem precipitar pela adio de excesso de eletrlitos, os quais
reprimem a dissociao dos sabes, fazendo com que as micelas percam a carga e precipitem.
OLEATO DE POTSSIO CLORETO DE
CLCIO
OLEATO DE CLCIO
(precipita)
CLORETO DE
POTSSIO
Figura 8. Reao de precipitao de sabo atravs de salificao. A exposio de sabes, como o
oleato de potssio, ambientes ricos em sais de clcio ou magnsio induz a formao de sabes
insolveis.
Os sabes possuem propriedades emulsificantes. Emulso a mistura entre dois
lquidos imiscveis em que um deles (fase dispersa) encontra-se na forma de pequenos
glbulos dispersos em meio ao outro (fase contnua). Minsculas partculas de leo ou
solventes orgnicos so sustentadas em suspenso numa soluo aquosa. Porm, quando as
duas fases so misturadas ou agitadas vigorosamente, essas partculas formam uma emulso
onde os leos ou os solventes orgnicos tendem a dispersar-se pela soluo. Com o tempo, as
emulses tendem a retornar para o estado estvel podendo se observar duas ou mais fases
distintas (Figura 9A). Os sabes so agentes emulsificantes, pois quando adicionados s
emulses, tendem a torn-las mais estveis e homogneas (Figura 9B).
AGITAO
MISTURA EMULSO
(A)
TEMPO
MISTURA
AGITAO
MISTURA EMULSO
(B)
SABO
MICELA
Figura 9. Propriedade emulsificante dos sabes. Uma mistura de dois lquidos imiscveis
pode formar uma emulso atravs de agitao (fornecimento de energia). Contudo, as
emulses so instveis e tendem a tornar-se misturas com o passar do tempo (A). Os sabes
agem como surfactantes estabilizando a emulso formada atravs da formao de micelas
com leos ou solventes orgnicos. As cadeias hidrocarbnicas no-polares dos sabes
dissolvem-se no leo ou solvente orgnico enquanto os grupos inicos polares na fase
aquosa. As gotculas carregadas negativamente repelem-se mutuamente (B).
Curiosidade: Um subproduto da manufatura de sabes a glicerina (glicerol), da qual se pode
obter a nitroglicerina, um poderoso explosivo. Durante a I e II Guerras Mundiais, as donas de
casa guardavam o excesso de leo e gorduras de cozinha e o devolviam para a recuperao da
glicerina.
2. Objetivos da aula
A aula apresenta como objetivo a extrao de leo de soja, a saponificao do leo
extrado e a caracterizao das propriedades fsico-qumicas dos sabes. Para isso devero ser
realizados os seguintes procedimentos:
I- Extrao do leo de soja
Obteno de leo (triacilgliceris) a partir de sementes de soja.
Determinao da solubilidade do leo de soja em diferentes solventes;
II- Saponificao do leo extrado
Obteno de sais de potssio de cido graxo (sabes) a partir da hidrlise alcalina dos
triacilgliceris obtidos das sementes de soja.
III- Caracterizao das propriedades fsico-qumicas dos sabes
Precipitao de cidos graxos atravs de hidrlise cida;
Purificao de sabo atravs de salificao;
Propriedade emulsificante dos sabes;
Ressaponificao a partir de cidos graxos.
Materiais
1. Reagentes
leo de soja
Soja moda e seca
gua destilada
Etanol
ter etlico
Acetona
Hidrxido de potssio
Hidrxido de sdio
Fenolftalena
cido clordrico
Cloreto de Sdio
2. Materiais e vidrarias
Liquidificador
Balana analtica
Banho de aquecimento fervente (
50C e 100C)
Estante para tubos de ensaio
Pina de madeira
Pipeta graduada de 10 mL
Pipetador automtico e ponteiras de
1000 L
Conta gotas ou pipeta de Pasteur
Esptula para pesagem
Proveta de 25 mL
Tubos de ensaio
Bquer de 100 mL
Bquer de 10 mL
Erlenmeyer de 125 mL
Papel de filtro
3. Procedimento experimental
3.1. Extrao de leo vegetal da soja.
1. Em um bquer de 100 mL (bquer A), pesar 10 g de soja moda e seca.
2. Adicionar 25 mL de acetona e agitar por 5 minutos.
3. Pesar um segundo bquer (bquer B) e anotar sua massa.
4. Utilizando o bquer B e papel de filtro, filtrar a soluo obtida no bquer A.
5. Lavar o resduo obtido com 10 mL de acetona uma vez.
6. Evaporar o filtrado em chapa de aquecimento (200C), com agitao peridica, at a
eliminao da acetona. Ao final, ser obtido um resduo amarelo e viscoso.
7. Determinar o peso do produto obtido na etapa anterior e calcular o rendimento da extrao.
3.2. Solubilidade do leo de soja.
1. Numere 4 tubos de ensaio e coloque 1 mL dos seguintes solventes: gua, etanol, ter etlico
e acetona.
2. Adicione 1,0 mL de leo de soja a cada tubo e agite-os. Classifique os solventes segundo a
solubilidade apresentada pelo leo de soja.
TUBO SOLVENTE
SOLUBILIDADE
(+, ++, +++ ou ++++)
1 gua
2
etanol
3
ter etlico
4 acetona
3.3. Reao de saponificao.
1. Preparar uma soluo de potassa alcolica 20% Em um erlenmeyer de 125 mL, misture
10 mL de soluo aquosa de hidrxido de potssio (KOH) 40% a 10 mL de etanol.
2. Adicionar 5,0 mL de leo vegetal a soluo de potassa alcolica e aquecer o sistema em
banho-maria FERVENTE durante 20 minutos.
3. Em um tubo de ensaio, adicionar 2 gotas da soluo obtida a 2,0 mL de gua destilada.
Agitar. Observe se h ou no formao de espuma e explique.
5. Esquematize a reao de hidrlise alcalina de um triacilglicerol na presena de hidrxido de
sdio e, alternativamente, na presena de hidrxido de potssio.
6. Esquematize uma molcula de sabo.
3.4. Separao de cidos graxos.
1. Transferir 4,0 mL do erlenmeyer contendo o sabo para um tubo de ensaio.
2. Adicionar 1 gota de fenolftalena (indicador de pH).
3. Manter o tubo de ensaio EM AGITAO e colocar, gota a gota, cido clordrico (HCl)
concentrado at que a soluo mude de colorao (rosa para incolor) indicando a viragem
do indicador.
4. Observe a diviso da mistura em duas fases. Que compostos representam cada uma das
duas fases? Esquematize a reao ocorrida.
5. Reserve a soluo para teste posterior (item 3.5)
3.5. Ressaponificao.
1. Transferir 4 gotas da soluo obtida no item 3.4 para um tubo de ensaio contendo 5 mL de
gua destilada quente.
2. Adicionar, gota a gota, soluo de hidrxido de sdio (NaOH) 1 mol.L
-1
ate que seja
solubilizada a parte oleosa.
3. Agitar o tubo e verificar se h formao de espuma.
4. Explicar a reao qumica ocorrida, seu mecanismo de ao e indicar o produto formado.
3.6. Propriedades emulsificantes dos sabes.
1. Agitar 5 gotas de leo de soja num tubo de ensaio contendo 5 mL de gua. Observe a
formao temporria de uma emulso gua-leo.
2. Repetir o mesmo teste, adicionando 5 gotas de sabo (obtido no item anterior) antes de
agitar. O que acontece com a emulso gua-leo?
3. Comparar a aparncia das duas emulses obtidas no 1 e 2 passos.
Anlise dos dados
1) Tabela apresentada no item 3.1 com os respectivos valores de solubilidade do leo de sojas
nos diferentes solventes utilizados.
2) Resultado do rendimento da reao de extrao de leo da soja. Esquematizar frmula
utilizada para o clculo.
3) Esquema da reao de saponificao do leo de soja em presena de KOH.
4) Esquematizar uma molcula de sabo e discutir suas propriedades fsico-qumicas:
- Mostrar a reao de formao de cidos graxos a partir de sabes em meio cidos.
- Mostrar a reao de precipitao de sabes em solues rica em sal.
- Esquematizar uma molcula de sabo e discutir suas propriedades fsico-qumicas.
- Esquematizar e caracterizar uma reao de ressaponificao.
Exerccios
1. Como podem ser explicadas as diferenas de solubilidade do leo de soja nos diferentes
solventes usados no experimento?
2. Qual a importncia da determinao da solubilidade do leo de soja em diferentes solventes
para a parte de extrao de leo vegetal a partir da soja?
3. Por que se utiliza etanol na reao de saponificao?
4. Se o sabo feito de leos e gorduras, como capaz de limpar superfcies engorduradas?
Como o sabo remove a sujeira?
Referncias Bibliogrficas
1. MARZZOCO, A.; TORRES, B. B. Bioqumica Bsica, 3 ed., Rio de Janeiro: Guanabara
Koogan, 2007.
2. ALBERTS, B.; JOHNSON, A.; LEWIS, J.; RAFF, M.; ROBERTS, K.; WALTER, P.
Molecular Biology of the Cell, 5 ed., Garland Science, New York, 2008.
3. LEHNINGER, ALBERT L.; NELSON, DAVID L.; COX, MICHAEL M. Princpios de
bioqumica, 4 ed., So Paulo: Sarvier, 2006.
4. NEPOMUCENO, M. F.; RUGGIERO, A. C. Manual de Bioqumica: Roteiros de Anlises
Bioqumicas Qualitativas e Quantitativas, 1 ed., Ribeiro Preto: Tecmedd, 2004.
5. PETKOWICZ, I.; DE OLIVEIRA, C. L. Bioqumica: Aulas Prticas, 7 Ed., Editora UFPR,
Paran, 2007.
Abstract
In this experiment the extraction and purification of the polysaccharide starch from
potatoes will be performed. After the microscopic characterization of the starch granules
morphology, biochemical reactions using iodide will be performed at several experimental
conditions. Besides, a qualitative analysis of reducing power of starch will be done in
comparison with glucose. The observed results will be discussed in terms of chemical
structure of the polymer. This practical application of the theoretical concepts learned inside
the classes about the spatial structure of starch is helpful for the improvement of biochemistry
understanding of UFABC students.
Resumo
Nesta aula prtica os alunos realizaro a extrao e purificao do amido da batata.
Aps a caracterizao microscpica dos grnulos de amido, observando a morfologia
especfica, sero feitas reaes bioqumicas de caracterizao utilizando iodo em diversas
condies experimentais. Alm disso, uma anlise qualitativa do poder redutor do amido ser
feita em comparao com a glicose e a sacarose. Os resultados obtidos sero discutidos em
funo da estrutura qumica espacial adquirida em meio aquoso por este polissacardeo. Este
experimento permite a aplicao dos conceitos tericos adquiridos durante as aulas sobre a
conformao espacial do amido extremamente importante para o aprendizado de bioqumica
estrutural pelos estudantes da UFABC.
Experimento 6 - Extrao e Caracterizao Bioqumica do Amido da
Batata: Reao com Iodo e Poder Redutor de Carboidratos
Introduo
O amido um polissacardeo que tem como funo reserva energtica na forma de
carboidratos em plantas, que so consumidas por organismos heterotrficos como principal
fonte de glicose para gerao de ATP (LEHNINGER, NELSON, & COX, 2006). O amido
constitui de 50% a 65% do peso das sementes de cereais secos, e at 80% da substncia seca
dos tubrculos. Nos pases europeus e nos Estados Unidos, mais de 50% da produo de
amido destinada produo de hidrolisados, tais como glicose, maltose, dextrinas e
maltodextrinas. Esses hidrolisados, por suas propriedades especficas e seus diferentes usos
no setor alimentcio, constituem uma excelente valorizao da fcula (SUMERLY et al.,
2002).
Embora a distribuio do amido seja ampla no reino vegetal, poucas plantas o
produzem em grandes quantidades. Milho e outros cereais, como o arroz, o sorgo e o trigo,
contribuem significativamente para o suprimento mundial de amido. Nos Estados Unidos
mais de 95% do amido comercializado proveniente do milho. Em muitos pases, como por
exemplo, no Brasil, o amido tambm extrado da batata, dos rizomas da araruta e das razes
da mandioca.
Comercialmente, o amido usado na alimentao, fabricao de xaropes, preparo de
colas e gomas, com excipiente farmacutico, na fabricao de etanol, entre outros.
O amido ocorre em grnulos (ou gros) que tm estrias tpicas. Estas, aliadas ao
tamanho e forma dos grnulos, so especficas de cada espcie de planta e esta caracterstica
morfolgica pode servir de meio de identificao microscpica da origem botnica do amido
(Fig. 1).
Fig. 1 Microscopia eletrnica de varredura (MEV) esquerda e microscopia ptica
direita de um grnulo de amido. (fonte:
http://www.cheng.cam.ac.uk/research/groups/polymer/RMP/nitin/Granule.jpg).
Estruturalmente, o amido classificado como um homopolissacardeo, sendo que a
hidrlise de suas ligaes glicosdicas fornece unidades de glicose livres. Tal hidrlise pode
ser qumica ou enzimtica e a glicose formada que pode ter diversos destinos, variando desde
uma aplicao biolgica, sendo fundamental fonte de energia para as clulas vivas sendo
convertida em ATP por reaes catablicas oxidativas, at aplicaes biotecnolgicas,
servindo como fonte de carboidratos para reaes fermentativas para produo de etanol em
indstrias qumicas, de alimentos, de bebidas ou de combustveis.
Fundamentao Terica
O amido um polissacardeo sintetizado pelos vegetais e tem a funo de reserva
energtica, semelhante ao glicognio nas clulas animais. Estruturalmente, o amido formado
pela mistura de dois polmeros, a amilose e a amilopectina, que so homopolissacardeos
constitudos por resduos de -D-glicopiranose ligados entre si por ligaes glicosdicas. A
amilopectina constitui aproximadamente 80% do peso seco dos polissacardeos existentes no
gro de amido e menos hidrossolvel que a amilose. formada por resduos de -D-glicose
unidos entre si por ligaes glicosdicas (14) com ramificaes (16), enquanto que a
amilose no possui tais ramificaes, formando um polmero linear (Fig. 2).
Fig. 2 Estruturas qumicas da amilose e amilopectina, evidenciando as ligaes
glicosdicas.
AMILOSE
ligao
14
O
CH
2
OH
H
H H
OH
H
H
OH
O
CH
2
OH
H
H H
OH
H
H
OH
O O
n
AMILOSE
ligao
14
O
CH
2
OH
H
H H
OH
H
H
OH
O
CH
2
OH
H
H H
OH
H
H
OH
O O
n
O
CH
2
OH
H
H H
OH
H
H
OH
O
CH
2
OH
H
H H
OH
H
H
OH
O
CH
2
OH
H
H H
OH
H
H
OH
O O
n
AMILOPECTINA
ligao
14
O
CH
2
H
H H
OH
H
H
OH
O
CH
2
OH
H
H H
OH
H
H
OH
O O
n
O
CH
2
OH
H
H H
OH
H
H
OH
O
ligao
16
AMILOPECTINA
ligao
14
O
CH
2
H
H H
OH
H
H
OH
O
CH
2
OH
H
H H
OH
H
H
OH
O O
n
O
CH
2
OH
H
H H
OH
H
H
OH
O
CH
2
OH
H
H H
OH
H
H
OH
O
ligao
16
Os tipos de ligaes presentes na amilose e amilopectina foram esses polmeros a
adquirem uma conformao espacial helicoidal (Fig. 3). Estas estruturas compactas produzem
os grnulos densos de estocagem do amido, j mostrados na Fig. 1.
O amido tem estrutura qumica muito parecida com o glicognio, porm possui menos
ramificaes. Sua sntese em plantas tambm bastante semelhante sntese do glicognio
em animais, com a substituio da forma ativada da glicose de UDP-glicose por ADP-glicose,
com catlise pela enzima amido sintase. No processo de digesto, a hidrlise do amido
catalisada enzimaticamente pelas -amilases salivar e pancretica, que clivam as ligaes
glicosdicas 14 da amilose originando uma mistura de maltose, amilopectina e glicose, e
tambm as ligaes 14 da amilopectina, originando uma mistura de polissacardeos
denominados dextrinas.
Os monossacardeos so definidos como poli-hidroxialdedos ou poli-hidroxicetonas
ou compostos que os liberem por hidrlise. Apresentam a frmula geral [C(H
2
O)]
n
e
apresentam uma propriedade qumica muito importante em meio aquoso devido reatividade
ca carbonila: ciclizao em meio aquoso. Este processo de ciclizao leva a formao de um
carbono anomrico, sendo que a hidroxila formada ligada a esse carbono apresenta
propriedades redutoras.
Diversos reagentes so utilizados para a anlise de poder redutor em acares. Alguns
desses mtodos utilizam agentes oxidantes suaves, tais como ons frrico (Fe
3+
) e cprico
(Cu
2+
) em meio alcalino, fazendo deteco qualitativa. Mtodos quantitativos utilizam
tcnicas espectrofotomtricas, titulomtricas ou gravimtricas (SILVA et al., 2003).
Dissacardeos ligados pelas suas hidroxilas redutores como o caso da sacarose no
apresentam poder redutor, porm quando hidrolisados passam a exibir esta caracterstica.
Fig. 3 Representao da estrutura helicoidal de uma
cadeia de amilose, polmero que compe a estrutura do
amido (fonte: LEHNINGER, NELSON & COX, 2006).
Tais propriedades so muito importantes e, por muitas vezes, utilizadas para
identificao de acares, verificao de adulterao e falsificao de alimentos, entre outros.
Objetivo
Permitir a compreenso de processos de extrao do amido da batata e, aps etapa de
purificao e secagem, realizar sua caracterizao bioqumica. Para isso, so propostos os
seguintes objetivos especficos:
- extrair e purificar o amido da batata;
- realizar observao morfolgica por microscopia ptica;
- fazer a reao de identificao com iodo, variando condies de temperatura, utilizando
tubos abertos e tampados;
- fazer a reao qualitativa de identificao de acares redutores no amido utilizando o
reagente de Benedict, em comparao com solues de glicose e sacarose.
MATERIAIS E MTODOS
1. Reagentes
- batatas in natura;
- gua destilada;
- lugol;
- reagente de Benedict;
- soluo de glicose 1,0 % (m/v);
- soluo de sacarose 1,0 % (m/v);
- suspenso de amido 1,0 % (m/v);
2. Materiais e Vidrarias
- liquidificador;
- bquer 200 mL;
- gaze;
- estufa de secagem;
- papel de filtro;
- bomba de vcuo;
- funil de Bchner;
- balana analtica;
- papel de pesagem (ou vidro de relgio) e esptulas;
- proveta 50 mL;
- estante para tubos de ensaio;
- 5 tubos de ensaio, um deles com tampa;
- bico de Bunsen;
- banho de aquecimento fervente (~ 100C);
- pipetador automtico e ponteiras de 500 e 1000 L;
- conta-gotas ou pipeta de Pasteur;
- pina de madeira
3. Procedimento Experimental
3.1. Extrao do amido da batata (j realizado previamente pelo tcnico de laboratrio).
Homogeneizar 50g de batata descascada em liquidificador com 200 mL de gua destilada.
Filtrar em gaze dobrada, recolhendo a suspenso de amido em um bquer. Deixar o amido
depositar no fundo do bquer (~ 5 min). Desprezar cuidadosamente o sobrenadante. Adicionar
cerca de 100 mL de gua. Agitar, deixar decantar (~5 min), remover o sobrenadante. Repetir
esse procedimento de lavagem por 5 vezes. Juntar ao amido 200 mL de gua destilada, filtrar
em Bchner e deixar secar em estufa.
3.2. Preparo da suspenso de amido. Pesar 0,5 g do amido seco e ressuspender em 50 mL
de gua destilada (suspenso de amido 1,0 % (m/v)).
3.3. Exame microscpico dos grnulos de amido. Adicionar 2 mL desta soluo em 2 tubos
de ensaio numerados 1 e 2. Ferver um deles at que a soluo fique opalescente, agitando
sempre. Pingar uma gota das solues dos tubos 1 e 2 um uma lmina, cobrir com uma
lamnula e observar em microscpio ptico. Pingar uma gota de lugol e observar novamente
em microscpio ptico.
3.4. Reao de caracterizao com iodo. Tomar 4 tubos de ensaio, sendo um deles com
tampa, e adicionar em dois deles (sendo um com tampa) 1 mL de amido 1 % (m/v) e nos
demais 1 mL de gua destilada e 1 mL de glicose 1 % (m/v). Em seguida, adicionar 1 gota da
soluo de lugol em cada um dos tubos de ensaio e observar o resultado. Aquecer
cuidadosamente o tubo tampado contendo amido (direto na chama) e observar o resultado.
Deixar o tubo resfriar e observar o resultado. Repetir o procedimento para o tubo sem tampa
contendo amido e anotar o resultado. ***CUIDADOS ESPECIAIS: 1. O tubo com tampa
deve estar com a mesma pouco (frouxa) e no muito apertada. 2. O aquecimento direto na
chama deve ser feito com auxlio da pina, com quantos ciclos forem necessrios (CADA
CICLO: no mximo 2 segundos na chama agitao fora da chama).
3.5. Pesquisa de poder redutor. Tomar 4 tubos de ensaio e seguir procedimento abaixo:
Tubos Amostras (mL) H
2
O (mL) Benedict (mL)
B - 1,5 1,0
1* 1,0 0,5 1,0
2* 1,0 0,5 1,0
3* 1,0 0,5 1,0
*onde, 1, 2 e 3 so as amostras numeradas fornecidas para o experimento.
Em seguida, ferver os tubos em banho-maria por 5 minutos e observar as possveis
alteraes. Sabendo que entre as amostras 1, 2 e 3 tratam-se de glicose, amido e sacarose,
identifique as amostras em funo da colorao observada e discuta os resultados.
BIBLIOGRAFIA
1
LEHNINGER, A. L.; NELSON, D. L.; COX, M. M. Princpios de Bioqumica, 4. ed. New
York: Worth Publishers, 2006, p.685-686.
2
SUMERLY, R.; ALVAREZ, H.; CEREDA, M.P.; VILPOUX, O.F. Tecnologia, usos e
potencialidades de tuberosas amilceas latino-americanas. Em: Culturas de tuberosas
amilceas latino-americanas. v. 3, p. 377-448, 2002.
3
SILVA, R.N.; MONTEIRO, V.N.; ALCANFOR, J.D.X.; ASSIS, E.M.; ASQUIERI, E.R.
Comparao de Mtodos para a Determinao de Acares Redutores e Totais em Mel. Cin.
Tecnol. Aliment., v. 23, n. 3, p. 337-341, 2003.
Você também pode gostar
- Treinamento Falhas Scroll Danfoss PDFDocumento49 páginasTreinamento Falhas Scroll Danfoss PDFrodrigo dias martins100% (1)
- FMEA SistemaDocumento6 páginasFMEA Sistemamarcelokyamamoto100% (1)
- TCC - Patologias ConstrutivasDocumento24 páginasTCC - Patologias ConstrutivasLeandro Santana FerreiraAinda não há avaliações
- CQFQ 0xx - Não Conformidades - Rev.01Documento3 páginasCQFQ 0xx - Não Conformidades - Rev.01Lyca Ribeiro da FonsecaAinda não há avaliações
- Aula 3 CienciasDocumento4 páginasAula 3 CienciasValquiria PalhanoAinda não há avaliações
- O Funcionamento Do Sistema GNV TradicionalDocumento6 páginasO Funcionamento Do Sistema GNV TradicionalFernando AndradeAinda não há avaliações
- Características Das PedrasDocumento4 páginasCaracterísticas Das PedrasGiuliano FavaretoAinda não há avaliações
- Exper 7 DifusãoDocumento3 páginasExper 7 DifusãoMarina Vieira de OliveiraAinda não há avaliações
- Agentes AntiestáticosDocumento23 páginasAgentes AntiestáticosAndré Luís Aganeti0% (1)
- Resumo Das Fórmulas de Rendimentos e Eficiência Utilizadas Na Indústria Açucareira Do BrasilDocumento16 páginasResumo Das Fórmulas de Rendimentos e Eficiência Utilizadas Na Indústria Açucareira Do BrasilFernanda Lima Silva100% (1)
- MicrocultivoDocumento14 páginasMicrocultivoFernando GomesAinda não há avaliações
- Rima Cargas Pesadas ComperjDocumento63 páginasRima Cargas Pesadas ComperjCentro de Documentação Técnica e Científica de Maricá - CDTCMAinda não há avaliações
- Ficha Formativa 4 - 9ano (Classificação Materiais)Documento4 páginasFicha Formativa 4 - 9ano (Classificação Materiais)Adelaide SantosAinda não há avaliações
- Acetileno PDFDocumento9 páginasAcetileno PDFFerreira SouzaAinda não há avaliações
- Aula 1Documento3 páginasAula 1gambetzAinda não há avaliações
- Lista de Exercícios 1Documento2 páginasLista de Exercícios 1Olympio NetoAinda não há avaliações
- Capítulo 1 Conceitos Introdutórios e DefiniçõesDocumento24 páginasCapítulo 1 Conceitos Introdutórios e DefiniçõesBruno DantasAinda não há avaliações
- Avaliações 1º, 3º, 4º e 5º AnosDocumento107 páginasAvaliações 1º, 3º, 4º e 5º Anosjaqueline AbreuAinda não há avaliações
- Massa MolarDocumento10 páginasMassa MolarsegecsAinda não há avaliações
- Tabela de Materiais (Durezas)Documento1 páginaTabela de Materiais (Durezas)Projetos Geiger100% (1)
- Lista de Exercício 1 PDFDocumento2 páginasLista de Exercício 1 PDFArtur CasteloAinda não há avaliações
- Materiais de Construção Mecânica 3Documento20 páginasMateriais de Construção Mecânica 3fabiofambhAinda não há avaliações
- Estudo Do Comportamento Mecânico de Solos Lateríticos Da Formação BarreirasDocumento291 páginasEstudo Do Comportamento Mecânico de Solos Lateríticos Da Formação BarreirasAdson FrançaAinda não há avaliações
- Lista de Exercícios Quimica OrgânicaDocumento6 páginasLista de Exercícios Quimica OrgânicaSem fins fan AlêAinda não há avaliações
- Os Dados Obtidos No Laboratório para A Determinação de Umidade NaturalDocumento4 páginasOs Dados Obtidos No Laboratório para A Determinação de Umidade NaturalWendel MeloAinda não há avaliações
- Aplicação Da Ressonância Magnética Nuclear 1H Na Identificação de Produtos NaturaisDocumento47 páginasAplicação Da Ressonância Magnética Nuclear 1H Na Identificação de Produtos NaturaisNelson Filho100% (1)
- Apostila 02-Físico-Química Cursos Militares-Episteme Cursos Online Professor AlexandreDocumento169 páginasApostila 02-Físico-Química Cursos Militares-Episteme Cursos Online Professor AlexandreIssei HyoudouAinda não há avaliações
- Trocadores de Calor Nas Usinas de Açúcar, Etanol e Energia (Amostra)Documento22 páginasTrocadores de Calor Nas Usinas de Açúcar, Etanol e Energia (Amostra)Thiago LinsAinda não há avaliações
- Cap 1 - Nomenclatura ResumoDocumento42 páginasCap 1 - Nomenclatura Resumosofis2013Ainda não há avaliações
- Exercícios RESOLVIDOS Nomenclatura Orgânica 3Documento3 páginasExercícios RESOLVIDOS Nomenclatura Orgânica 3Suzani Menegon0% (1)