Escolar Documentos
Profissional Documentos
Cultura Documentos
Aula 02 - Cálculos Das Reações Químicas
Enviado por
Plano ENEMTítulo original
Direitos autorais
Formatos disponíveis
Compartilhar este documento
Compartilhar ou incorporar documento
Você considera este documento útil?
Este conteúdo é inapropriado?
Denunciar este documentoDireitos autorais:
Formatos disponíveis
Aula 02 - Cálculos Das Reações Químicas
Enviado por
Plano ENEMDireitos autorais:
Formatos disponíveis
Livro Digital
Aula 02 –
Cálculos das
Reações
Químicas
Fuvest Medicina 2021
Professor Prazeres
Professor Prazeres
Aula 02: Fuvest Medicina 2021
Sumário
Introdução ......................................................................................................................... 4
1. Notação Das Reações Químicas...................................................................................... 4
2. Leis Ponderais ................................................................................................................ 5
Lei de Lavoisier .................................................................................................................................. 5
Lei de Proust .................................................................................................................................... 12
3. Balanceamento das Equações Químicas ....................................................................... 13
4. Teoria Atômico Molecular............................................................................................ 14
Massas atômicas ............................................................................................................................. 17
Mol .................................................................................................................................................. 22
Massa Molar ................................................................................................................................... 24
5. Lei Volumétrica e Volume Molar .................................................................................. 30
Lei de Gay-Lussac ............................................................................................................................ 31
Volume Molar .................................................................................................................................. 31
6. Fórmulas Químicas ...................................................................................................... 32
Fórmula Molecular ou Fórmula Iônica ............................................................................................ 32
Fórmula Mínima ou Empírica .......................................................................................................... 32
Fórmula Percentual ou Centesimal ................................................................................................. 32
7. Cálculo Estequiométrico .............................................................................................. 35
8. Aspectos Reais do Cálculo Estequiométrico ................................................................. 40
Pureza .............................................................................................................................................. 40
Rendimento ..................................................................................................................................... 41
Excesso e Limitante ......................................................................................................................... 42
Reações Sucessivas .......................................................................................................................... 44
9. Questões Fundamentais .............................................................................................. 45
10. Já Caiu na Fuvest ........................................................................................................ 47
Aula 02 – Cálculos das reações químicas 2
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
11. Já Caiu Nos Principais Vestibulares............................................................................. 59
Leis Ponderais .................................................................................................................................. 59
Teoria Atômico Molecular e Volume Molar .................................................................................... 63
Fórmulas Químicas .......................................................................................................................... 64
Cálculo Estequiométrico .................................................................................................................. 66
Aspectos Reais do Cálculo Estequiométrico .................................................................................... 68
12. Gabarito Sem Comentários ........................................................................................ 72
13. Resoluções Das Questões Fundamentais .................................................................... 72
14. Questões Resolvidas E Comentadas ........................................................................... 78
15. Considerações Finais das Aulas ................................................................................ 124
16. Referências .............................................................................................................. 124
Aula 02 – Cálculos das reações químicas 3
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
Introdução
Se prepare para um dos capítulos mais importantes da Química. Cálculo estequiométrico,
normalmente, se encontra no top 5 de qualquer vestibular. Alguns alunos e algumas alunas
apresentam trauma nesse capítulo, em contrapartida, outros alunos e outras alunas já entenderam
a lógica das questões e precisam apenas exercitar. Portanto, vou apresentar duas propostas para
vocês.
Se você tem facilidade... pule para as questões!
Cálculo
estequiométrico
Se você tem dificuldade
leia a parte teórica!
ou insegurança...
A parte teórica foi escrita passo a passo de forma a não deixar nenhuma dúvida existir. Dessa
vez, você, que possui dificuldade nesse tema, vai entender e acertar as questões do vestibular.
Então separe um lanchinho e sua água/café/suco.
Are you ready? Let’s do it!
1. Notação Das Reações Químicas
Toda transformação química da matéria é representada por uma equação química que indica
a(s) substância(s) consumida(s) e a(s) substância(s) formada(s) separadas por uma seta. As
substâncias consumidas são denominadas reagentes, enquanto as substâncias formadas são
chamadas de produtos.
𝑅𝑒𝑎𝑔𝑒𝑛𝑡𝑒𝑠 → 𝑃𝑟𝑜𝑑𝑢𝑡𝑜𝑠
Até o século XVIII, acreditava-se que a água poderia ser um átomo ou uma substância simples.
Porém, Lavoisier, em 1783, descobriu que a água sofria uma reação de decomposição quando
entrava em contato com ferro incandescente e, assim, produzia gás hidrogênio e gás oxigênio.
Atualmente, utiliza-se corrente elétrica para essa decomposição da água. Normalmente, as reações
químicas são representadas em quatro maneiras: somente as fórmulas; fórmulas e estados físicos;
fórmulas, estados físicos e coeficientes; fórmulas, estados físicos, coeficientes e condições da reação
(temperatura, catalisador, etc.). A reação de decomposição da água, através da corrente elétrica,
pode ser representada pelas seguintes equações:
Aula 02 – Cálculos das reações químicas 4
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
H2O → H2 + O2
• Somente as fórmulas
H2O (l) → H2 (g) + O2 (g)
• Fórmulas e estados físicos
2 H2O (l) → H2 (g) + 2 O2 (g)
• Fórmulas, estados físicos e coeficientes.
↯
2 H2O (l) → H2 (g) + 2 O2 (g)
• Fórmulas, estados físicos, coeficientes e condições da reação.
2. Leis Ponderais
No século XIX, Dalton, Lavoisier e Proust fizeram importantes descobertas no ramo da
Química. O modelo atômico de Dalton, acreditado na época, classificava o elemento químico de
acordo com sua massa e tamanho. Com isso, Lavoisier foi um dos primeiros cientistas a descobrir a
relação de conservação das massas e, assim, elaborar sua lei.
As leis ponderais foram as primeiras leis que estabelecem proporção em massa das
substâncias em reações e fórmulas químicas.
Lei de Lavoisier
Ao realizar reações químicas em sistemas fechados, Lavoisier observou que a massa inicial do
sistema é sempre igual à massa final. Ele denominou essa observação de Lei da Conservação das
Massas ou Lei de Lavoisier. Um sistema fechado é aquele em que não ocorre saída nem entrada de
partículas, ou seja, a quantidade de partículas é constante. Embora Lavoisier tenha descoberto essa
conservação das massas em sistemas fechados, essa lei se aplica a todos os sistemas sejam fechados,
abertos ou isolados.
Aula 02 – Cálculos das reações químicas 5
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
Sistema aberto
• pode ocorrer troca de partículas e de energia com o meio
envolvente.
Sistema fechado
• não ocorre troca de partículas, mas pode ocorrer troca de
energia com o meio envolvente.
Sistema isolado
• não ocorre troca de partículas e nem de energia com o meio
envolvente.
Figura 1 - Sistema aberto [fonte: Unsplash].
Figura 2 - Sistemas fechado [Fonte: Unsplash].
Figura 3 - Sistemas isolado. [Fonte: Shutterstock].
O que queima na vela?
Muitas pessoas pensam que o combustível da vela é o pavio (barbante
ou algodão), mas não é. O pavio também é queimado, mas ele é importante
como meio de transporte do combustível. A cera da vela ou parafina é
formada por uma mistura de hidrocarbonetos de cadeias carbônicas abertas,
saturadas e apresentam 20 ou mais carbonos por molécula.
O pavio foi previamente preparado saturando-o com cera líquida. Ao
se acender o pavio, ocorre a fusão da cera que, ao entrar em contato com o
Figura 4 - vela acesa
pavio, sobe por capilaridade até atingir a chama. Quando a cera entra em contato com [Fonte: unsplash].
a chama, ocorre a sua vaporização que, imediatamente, o vapor da cera sofre
combustão com liberação de energia térmica e luminosa. A reação de combustão de uma vela é
classificada como combustão incompleta sendo comprovada pela liberação da fumaça preta,
denominada fuligem, a qual é composta, principalmente, por átomos de carbono.
Aula 02 – Cálculos das reações químicas 6
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
A chama de uma vela é identificada em 4 principais regiões:
Região 1 Região 2
Zona azul (≈800 °C): zona Zona escura (≈1000 °C): reação
responsável pela manutenção de pirólise da parafina que não
da sua fusão da vela. foi queimada na região 1.
Região 3
Zona luminosa (≈1200 °C):
região responsável pela Região 4
iluminação da vela. Zona pobre Zona externa não-luminosa
em oxigênio, logo ocorre a (≈1400 °C): zona responsável
reação de combustão pela combustão completa. Figura 5 - A chama de uma
incompleta liberando a fumaça vela [fonte: Wikipedia]
preta, fuligem (carbono).
Uma vela nunca mais será a mesma em sua vida, né?!
Vamos observar dois sistemas com reação:
Sistema: Combustão da vela Combustão da vela em um recipiente fechado
Reação: Vela + oxigênio → gás carbônico e água Vela + oxigênio → gás carbônico e água
Observação: Não se observa conservação da massa Se observa conservação da massa porque o
porque o sistema é aberto. sistema é fechado.
Nos dois sistemas acima ocorre conservação das massas, porém somente em um é
observável.
Figura 6 - prego enferrujado [Fonte: Unsplash].
A ferrugem de um prego é resultado da reação do ferro com o oxigênio do ar formando o
óxido de ferro, representado pela equação:
Aula 02 – Cálculos das reações químicas 7
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
Sabe-se que, experimentalmente, a reação de 56 gramas de ferro com 16 gramas de oxigênios
são formados 72 gramas de óxido de ferro. Assim, temos:
Para os principais vestibulares, é importante saber a relação, em massa, de dois tipos de
reação de combustão. Algumas reações de combustão apresentam o produto com massa maior que
os reagentes, enquanto, em outras, é menor. Em reações de combustão dos metais ocorre aumento
de massa, enquanto a de matérias orgânicas ocorre diminuição da massa.
Combustão de metais.
• aumento da massa.
• metal + oxigênio → óxido
Combustao de matéria orgânica.
• diminuição da massa.
• matéria orgânica + oxigênio → gás carbônico + água
A combustão de um material que contém carbono e hidrogênio (papel, madeira, etc.)
apresenta diminuição de massa no produto formado porque esses liberam gás carbônico e água,
respectivamente.
Aula 02 – Cálculos das reações químicas 8
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
Figura 7 - A fumaça contém partículas que ao serem liberadas diminuem a massa retida na parte sólida [fonte: Unsplash].
(UEPG PR/2017 - adaptado)
Nas reações de decomposição apresentadas abaixo, identifique aquelas que se
apresentam de acordo com a lei de Lavoisier e assinale o que for correto.
01. 9 g de água → 1 g de hidrogênio + 8 g de oxigênio.
02. 27 g de água → 3 g de hidrogênio + 24 g de oxigênio.
04. 11 g de gás carbônico → 4 g de carbono + 8 g de oxigênio.
08. 60 g de monóxido de nitrogênio → 28 g de nitrogênio + 32 g de oxigênio.
16. 34 g de amônia → 4 g de hidrogênio + 28 g de nitrogênio.
Comentários:
01. Certo. A massa de consumo da água (9 gramas) é igual às massas de formação de
hidrogênio e de oxigênio (1 gramas + 8 gramas = 9 gramas).
02. Certo. A massa de consumo da água (27 gramas) é igual às massas de formação de
hidrogênio e de oxigênio (3 gramas + 24 gramas = 27 gramas).
04. Errado. A massa de consumo do gás carbônico (11 gramas) não é igual às massas de
formação de carbono e de oxigênio (4 gramas + 8 gramas = 12 gramas).
08. Certo. A massa de consumo de monóxido de nitrogênio (60 gramas) é igual às massas de
formação de nitrogênio e de oxigênio (28 gramas + 32 gramas = 60 gramas).
16. Errado. A massa de consumo de amônia (34 gramas) não é igual às massas de formação de
hidrogênio e de nitrogênio (4 gramas + 28 gramas = 32 gramas).
Gabarito: 11
Aula 02 – Cálculos das reações químicas 9
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
(UECE/2013)
Em um laboratório de química, realizou-se a combustão de 10 g de palha de aço em um
recipiente aberto e, após sua queima, a massa resultante obtida foi de 10,9 g. Assinale a única
opção que explica corretamente por que esse valor obtido não invalida a lei da conservação
das massas.
a) Como após a queima, a massa resultante deveria ser de 10 g, deve ter ocorrido um erro
durante a pesagem.
b) Na combustão, o ferro reage com o oxigênio do ar, formando óxido, com 0,9 g a mais; esse
acréscimo deve-se apenas à massa do oxigênio do ar que foi fixado na formação do óxido.
c) Não invalida a lei, porque a massa resultante de 10,9 g é normal, por estar dentro da
margem de erro em uma pesagem, que é de 10%.
d) Como a combustão foi realizada em um recipiente aberto, impurezas contidas na
atmosfera misturaram-se à massa resultante.
Comentários:
A queima da palha de aço corresponde à combinação de 10 gramas de palha de aço mais
0,9 gramas de oxigênio formando um produto com 10,9 gramas.
a) Errado. Só manteria as 10 gramas caso não ocorresse nenhuma reação química. Porém, o
ferro aumenta a sua massa ao se combinar com o oxigênio.
b) Certo. A conservação das massas se aplica a todas as reações. A reação correspondente à
palha de aço foi: 10 g de palha de aço + massa oxigênio = 10,9 g. Logo, a massa de oxigênio é igual
a 0,9 g.
c) Errado. Não existe massa de erro. A massa de 0,9 g é devido à combinação dos átomos de
oxigênio.
d) Errado. O acréscimo de massa é devido à combinação dos átomos de oxigênio.
Gabarito: B
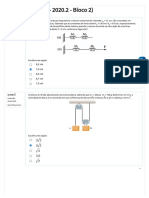
(UFPB/2013)
As reações químicas estão presentes em vários fenômenos do cotidiano, como a queima
de combustíveis, oxidação de metais, etc. Com o intuito de esclarecer esses fenômenos, um
professor de Química propôs aos seus alunos a realização de um experimento, em que utilizou
balança de dois pratos, uma folha de papel (1) e um pedaço de esponja de ferro (2), ambos
com massas idênticas, como ilustrado a seguir. Após a montagem do experimento, a folha de
papel e a esponja de ferro foram queimadas.
Aula 02 – Cálculos das reações químicas 10
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
Com base no exposto, a figura que representa corretamente a situação final observada é:
a)
b)
c)
d)
e)
Comentários:
O papel – matéria orgânica – quando queimado libera gás carbônico e água, restando como
material sólido somente as cinzas.
Papel (s) + oxigênio (g) → gás carbônico (g) + água (g) + cinzas (s)
Os produtos gasosos, gás carbônico e água, são liberados para o meio, portanto a massa
que permanece no prato da balança será menor que a massa inicial, fazendo com que o prato
que continha o papel fique mais leve e suba.
O pedaço da esponja de ferro, quando queimado, se combina com o oxigênio e forma um
material sólido.
Esponja de aço (s) + oxigênio (g) → produto (s)
Como a combinação do ferro e do oxigênio formam um material sólido, a massa que fica
apoiada no prato da balança será maior que a massa inicial. Portanto, se a massa do produto é
maior, o prato da balança ficará para baixo.
IMPORTANTE: nos dois casos de queima ocorre conservação das massas. O que a questão
está analisando é a massa que fica apoiada sobre o prato da balança, ou seja, a questão está
analisando, somente, a massa dos sólidos finais.
Aula 02 – Cálculos das reações químicas 11
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
Gabarito: D
Lei de Proust
O químico francês Joseph Louis Proust, ao utilizar balanças nas reações químicas, percebeu
uma lei na proporção das massas das substâncias. A lei de Proust ou Lei das Proporções Definidas
ou Constantes diz que dois ou mais elementos químicos, ao se combinarem, mantém uma
proporção, em números inteiros, e constante. Consequentemente, em uma reação química, a
proporção entre as substâncias participantes se mantém constante.
Partindo do exemplo visto na lei de Lavoisier, temos:
A proporção de ferro, oxigênio e óxido é de 32, 16 e 72 gramas. Logo, podemos calcular a
quantidade de todos as substâncias envolvidas na reação, a partir da massa de uma delas. Por
exemplo, para reagir 16 gramas de ferro, metade da quantidade da substância usada no exemplo,
precisaremos da metade da quantidade de todas as outras.
Perceba que as duas leis ponderais acontecem juntas. A soma dos reagentes 16 + 8 é igual a
massa do produto 26 gramas.
Aula 02 – Cálculos das reações químicas 12
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
(Uni-FaceF SP/2017)
Foram realizados dois experimentos cujos dados constam na tabela.
Os valores de x, y e z, em gramas, que completam, correta e respectivamente, a tabela são
a) 4,0; 12,0 e 12,5.
b) 16,0; 6,0 e 5,5.
c) 4,0; 0,75 e 1,25.
d) 16,0; 0,75 e 0,25.
e) 4,0; 1,5 e 2,0.
Comentários:
Gabarito: C
3. Balanceamento das Equações Químicas
Em uma reação química, os átomos sofrem rearranjo, ou seja, quebram ligações para formar
novas ligações e, assim, nenhum átomo se perde ou se cria. O balanceamento das equações químicas
corresponde ao ajuste dos índices estequiométricos para adequar a conservação dos átomos. Um
dos métodos de balanceamento é denominado método das tentativas:
Aula 02 – Cálculos das reações químicas 13
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
1º Passo: escolha um elemento químico. Dê preferência ao elemento
que apareça em uma única substância no reagente e no produto.
2º Passo: inverta os índices de atomicidade do elemento
escolhido.
3º Passo: determine a quantidade dos demais átomos, a partir das
substâncias fixadas no 2º passo.
Exemplo: Balanceie a equação a seguir.
C6H12O6 + O2 → CO2 + H2O
Portanto, a equação balanceada é: 1 C6H12O6 + 6 O2 → 6 CO2 + 6 H2O.
4. Teoria Atômico Molecular
Como verificar a massa de um átomo se não é possível pesá-lo separadamente? Esse é um
dos desafios do mundo da Química. Pelo menos 5 cientistas já receberam prêmios Nobel por
trabalhos associados determinação de massa de átomos e substâncias:
Aula 02 – Cálculos das reações químicas 14
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
J. J. Thomson: "investigações teóricas e experimentais sobre a condução de eletricidade de
gases".
• 1906
F. W. Aston: "descoberta, por meio de um espectógrafo de massa, de isótopos em um grande
número de elementos não radioativos".
• 1922
W. Paul: "desenvolvimento da técnica de armadilha de íons".
• 1989
J. B. Fenn e K. Tanaka: "desenvolvimento de métodos suaves de ionização e dessorção em
análise espectrométricas da massa de macromoléculas biológicas".
• 2002
Não existe balança sensível o suficiente que tenha mais de 20 casas decimais e seja capaz de
pesar um átomo ou molécula. Portanto, como verificamos essas massas?
Como medimos a massa dos átomos?
Atualmente, a espectrometria de massas é a técnica mais utilizada para determinar a massa
de átomos e substâncias. Essa técnica analítica física baseia-se, principalmente, na intensidade do
desvio de partículas carregadas. Basicamente, o espectrômetro de massa é composto de 5 partes:
1: a unidade de entrada da amostra.
2: a fonte de íons. Onde as partículas são transformadas em íons em fase gasosa e,
posteriormente, acelerados por um campo magnético.
3: o analisador de massa: separa os íons baseando-se na relação massa/carga.
4: a contagem de íons: o detector conta os íons que são registrados pelo sistema de dados.
Este gera um gráfico chamado espectrômetro de massa.
Aula 02 – Cálculos das reações químicas 15
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
Adotando como o exemplo uma amostra 100% pura de cromo, ao passar essa amostra pelo
equipamento, o cromo é divido em quatro isótopos de massas distintas, sendo a massa mais leve e
a mais pesada, as menos abundantes. O átomo de cromo mais pesado movimenta-se pela trajetória
da curva mais aberta, enquanto o cromo mais leve movimenta-se pela mais fechada. Esse fenômeno
é explicado pelos fundamentos da inércia, ou seja, o corpo de maior massa, em movimento, terá
maior resistência a modificar a sua trajetória. O sistema de dados gera o seguinte gráfico para o
elemento cromo:
Portanto, o elemento cromo apresenta quatro isótopos: 50, 52, 53 e 54. Porém, o isótopo
mais abundante é o cromo-52 com 84% de abundância. Com essa técnica foi possível comparar as
massas das partículas, porém esses valores de massa – 50, 52, 53 e 54 – são arbitrários de acordo
com uma referência inicial qualquer. Lembre-se que medir é comparar, por exemplo, antigamente,
a massa de 1 grama foi adotada como a massa de um volume de água igual a um cubo com aresta
da centésima parte do metro. Concluindo, a partir do desvio das partículas é possível determinar a
massa comparativa entre elas. A nova questão é: qual “massa-referência” adotar?
Aula 02 – Cálculos das reações químicas 16
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
Massas atômicas
Unidade de Massa Atômica (u)
Historicamente, muitos critérios foram adotados para determinar a massa-referência para os
átomos, tais como o hidrogênio, o oxigênio e o carbono. Entende-se massa-referência por unidade
de massa atômica. Desde 1962, define-se:
1
A unidade de massa atômica (u): é a massa de do átomo de carbono-12.
12
1 u equivale a 1,66 ∙ 10-24 gramas.
Portanto, a massa de todos os átomos é comparada à massa de uma fatia do átomo de
carbono-12. Exemplos:
12 14 16 1 24
C C O H Mg
12 u 14 u 16 u 1u 24 u
1 12 1 12 1 12 1 12 1 12
12 · C 14 · C 16 · C 1· C 24 · C
12 12 12 12 12
1
Ou seja, a massa do magnésio-24 é 24 vezes maior que a massa de 12C e duas vezes maior
12
que a massa do carbono-12.
Massa Atômica de Um Elemento Químico
Lembre-se que um elemento químico é definido pelo conjunto de átomos que apresentam o
mesmo número de prótons (número atômico). Por exemplo, conforme visto na seção anterior, o
elemento cromo é formado por quatro isótopos: cromo-50, cromo-52, cromo-53 e cromo-54.
Porém, qual a massa que será adotada para representar todos os cromos? O mais abundante? Uma
média? Que média? Média aritmética? Não! A média ponderada!
A massa de um elemento químico é calculada pela média ponderada das massas atômicas
de seus isótopos.
Aula 02 – Cálculos das reações químicas 17
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
A média ponderada leva em consideração a massa atômica e a abundância de cada isótopo.
Extraindo os dados do gráfico abaixo, temos:
Portanto, o cálculo da massa atômica do elemento cromo é dado por:
𝑚𝑎𝑠𝑠𝑎𝐶𝑟𝑜𝑚𝑜−50 ∙ %𝑐𝑟𝑜𝑚𝑜−50 + 𝑚𝑎𝑠𝑠𝑎𝐶𝑟𝑜𝑚𝑜−52 ∙ %𝑐𝑟𝑜𝑚𝑜−52 + 𝑚𝑎𝑠𝑠𝑎𝐶𝑟𝑜𝑚𝑜−53 ∙ %𝑐𝑟𝑜𝑚𝑜−53 + 𝑚𝑎𝑠𝑠𝑎𝐶𝑟𝑜𝑚𝑜−54 ∙ %𝑐𝑟𝑜𝑚𝑜−54
𝑀𝐶𝑟 =
100 %
50 𝑢 ∙ 4% + 52𝑢 ∙ 84% + 53𝑢 ∙ 10% + 54𝑢 ∙ 2%
𝑀𝐶𝑟 =
100 %
𝑴𝑪𝒓 = 𝟓𝟐, 𝟎𝟔 𝒖
Dessa forma, a massa atômica do elemento cromo que representa a contribuição de todos os
isótopos de cromo é 52,06 u. Ao observar a tabela periódica, verificamos os valores das massas
atômicas dos elementos químicos que foram determinados tal qual o cálculo para o cromo.
Massa Molecular
Sabendo que molécula é uma porção da matéria na qual os átomos estão ligados
covalentemente (um tipo de ligação química que os átomos compartilham elétrons). As ligações
covalentes serão abordadas na aula de ligações químicas. Assim, a massa de uma molécula é definida
pelo somatório das massas dos átomos que a compõem.
Sabendo que as massas atômicas, em u, dos elementos H, C, N, O e S são iguais a 1, 12, 14,
16 e 32, respectivamente, temos:
H2O CH4 NH3 H2SO4 CO(NH2)2
Água Metano Amônia Ácido sulfúrico Ureia
1 átomo de carbono,
2 átomos de
1 átomo de 1 átomo de 1 átomo de
2 átomos de hidrogênio, 1
carbono e 4 nitrogênio e 3 oxigênio, 2 átomos
hidrogênio e 1 átomo de enxofre e
átomos de átomos de de nitrogênio e 4
átomo de oxigênio. 4 átomos de
hidrogênio. hidrogênio. átomos de
oxigênio.
hidrogênio.
2∙1 u + 16 u = 18 u 12 u + 4∙1 u = 16 u 14 u + 3∙1 u = 17 u 2∙1 u + 32 u + 4 ∙ 16 12 u + 16 u + 2 ∙ 14
u = 98 u u + 4 ∙ 1u = 60 u
Massa Fórmula
Aula 02 – Cálculos das reações químicas 18
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
Os compostos iônicos apresentam ligações iônicas entre suas partículas, portanto não são
classificados como moléculas. Assim, os compostos iônicos não apresentam massa molecular, esses
apresentam massa-fórmula.
O sódio e o oxigênio combinam-se para formar o composto de fórmula iônica Na2O. Sabendo
que a massa do sódio é 23 u e a massa do oxigênio é 16 u, temos:
𝑀𝑁𝑎2𝑂 = 2∙23 u + 16 u = 62 u
(UFAM/2015)
Grande parte dos elementos químicos ocorre na natureza como mistura de isótopos. Sabendo
que um elemento hipotético X possui massa atômica igual a 69,8 u e dois isótopos com as
características descritas no quadro a seguir:
Isotopo Massa (u )
69
X 69
71
X 71
As abundâncias relativas dos isótopos 69X e 71X, são respectivamente:
a) 35% e 75%
b) 45% e 65%
c) 50% e 50%
d) 60% e 40%
e) 70% e 30%
Comentários:
A massa de um elemento químico é determinada pela média ponderada das massas
atômicas de seus isótopos. Sabendo que o somatório das porcentagens de 69X e 71X é igual a
100% e que a massa do elemento é igual 69,8 u, temos:
69
𝑋 −−−− 𝑥%
71
𝑋 −−−− 100 − 𝑥 %
69 𝑢∙x%+71𝑢∙(100−x)%
69,8 =
100 %
𝑥 = 60 % , portanto o outro isótopo apresenta 40 %.
Gabarito: D
Aula 02 – Cálculos das reações químicas 19
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
(ESCS DF/2014 - adaptado)
Há muitos séculos, a humanidade aprendeu a utilizar as propriedades biológicas de substâncias
presentes nas plantas. Por exemplo, no século V a.C., o médico grego Hipócrates relatou que a
casca do salgueiro branco (Salix alba) aliviava dores e diminuía a febre. O responsável por essas
atividades terapêuticas é o ácido salicílico, [...]. A seguir, são apresentadas as estruturas
moleculares da salicilina, do ácido salicílico e do ácido acetilsalicílico.
OH
OH O OH
O
OH
O
OH
OH
OH
salicilina ácido salicílico
O OH
O CH3
ácido acetilsalicílico
A partir da estrutura molecular apresentada, infere-se que a salicilina tem massa molecular
igual a
a) 286 u.
b) 292 u.
c) 258 u.
d) 273 u.
Comentários:
Contando a quantidade de átomos de carbono, hidrogênio e oxigênio do composto, temos:
Aula 02 – Cálculos das reações químicas 20
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
C13H18O7 : 13·12 u + 18·1 u + 7·16 u = 286 u
Gabarito: A
(UERJ/2015)
Em 1815, o médico inglês William Prout formulou a hipótese de que as massas atômicas de
todos os elementos químicos corresponderiam a um múltiplo inteiro da massa atômica do
hidrogênio. Já está comprovado, porém, que o cloro possui apenas dois isótopos e que sua
massa atômica é fracionária.
Os isótopos do cloro, de massas atômicas 35 e 37, estão presentes na natureza,
respectivamente, nas porcentagens de:
a) 55% e 45%
b) 65% e 35%
c) 75% e 25%
d) 85% e 15%
Comentários:
A massa de um elemento químico é determinada pela média ponderada das massas
atômicas de seus isótopos. A prova da UERJ fornece a tabela periódica ao final da prova,
portanto a massa atômica do elemento químico cloro é igual a 35,5, assim temos:
35 𝑢∙x %+37 u∙(100−x)%
𝑀𝐶𝑙 =
100 %
35x+37(100−x)
35,5 𝑢 =
100
𝑥 = 75 %, portanto o outro isótopo apresenta 25 %.
Gabarito: C
Aula 02 – Cálculos das reações químicas 21
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
Mol
Se tivéssemos uma máquina capaz de contar 1 milhão de
moléculas por segundo, quanto tempo ela demoraria para contar as
moléculas de água em um cubo de gelo (4cm de aresta)? 1 dia? 1
década? 1 século? 1 milênio? NÃO! 68 BILHÕES DE ANOS!
Isso mesmo, o Universo possui 17,8 bilhões de anos e o tempo
necessário para contar moléculas de um cubo de gelo seria, quase, 4
vezes maior. Portanto, temos um problema: como determinar o
número de átomos e moléculas se não há tempo para contar e nem é Figura 8 - cubo de gelo [fonte: Unsplash].
possível enxergá-los?
O advogado e físico italiano Lorenzo Romano Amedeo Carlo Avogadro (1776 – 1856)
determinou que quando um elemento apresenta a massa, em gramas, numericamente igual à sua
massa atômica, ele apresentará uma quantidade fixa n de partículas. Avogadro não determinou o
valor dessa constante da forma que sabemos atualmente, porém foi nomeada de Constante de
Avogadro ou Número de Avogadro por Jean Perrin, em 1909. Em 1971, a constante de Avogadro
foi, oficialmente, publicada no Sistema Internacional de Unidades (SI) como unidade padrão para a
determinação da quantidade de matéria, conhecida por mol. Existem várias formas de determinar
o valor da constante de Avogadro: pela eletricidade, radioatividade, etc. A dedução do valor da
constante de Avogadro não se aplica aos assuntos de interesse dos vestibulares, portanto iremos
adotar alguns valores possíveis:
Constante
de
Avogradro
6,022140857∙10
1 mol 23
6∙1023 6,02∙1023
Para você entender de uma vez por todas: mol é um número! Existem palavras que significam
números, por exemplo, dezena, centena, dúzia, milhar, etc. De mesmo modo mol é 6∙1023,
Aula 02 – Cálculos das reações químicas 22
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
aproximadamente. Pronto, apenas um novo nome em seu vocabulário! Que sonho seria ter 1 mol
de reais, ou seja, 600000000000000000000000 reais.
Uma maneira matemática para representar a constante de Avogadro como uma quantidade
que representa 1 mol é:
Constante de Avogadro = 6,02·1023 mol-1
Contagem
Dúzia Mol
1 dúzia de cadernos → 12 cadernos 1 mol de cadernos → 6∙1023 cadernos
1 dúzia de canetas → 12 canetas 1 mol de canetas → 6∙1023 canetas
1 dúzia de átomos → 12 átomos 1 mol de átomos → 6∙1023 átomos
A partir do valor da constante de Avogadro, podemos estabelecer:
6·1023 moléculas de água
1 molécula de H2O
1 molécula de água 1 mol de H2O
2 átomos de 2·6·1023 = 12·1023 átomos
hidrogênio de hidrogênio
1 átomo de 1·6·1023 = 6·1023 átomos
oxigênio de oxigênio
5·6·1023 = 30·1023
5 moléculas de H2O
5 moléculas de água
moléculas de água
5 mol de H2O
2·5 = 10 átomos de 5·2·6·1023 = 60·1023
hidrogênio átomos de hidrogênio
1·5 = 5 átomos de 5·1·6·1023 = 30·1023
oxigênio átomos de oxigênio
Segundo o Bureau Internacional de Pesos e Medidas (BIPM), que é umas das três
organizações que estabelece o Sistema Internacional de Unidades (SI): mol é a
Aula 02 – Cálculos das reações químicas 23
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
quantidade de substância de um sistema que contém tantas entidades elementares
quanto são os átomos contidos em 0,012 quilograma de carbono-12.
Massa Molar
A massa molar corresponde à massa, em gramas, de 1 mol de uma entidade química.
Lembrando que a massa molar é numericamente igual à massa atômica ou massa molecular ou
massa fórmula.
Massa atômica → Massa molar
C: 12 u → 12 g/mol
O: 16 u → 16 g/mol
Ca: 40 u → 40 g/mol
Massa molecular → Massa molar
H2O: 18 u → 18 g/mol
CO2: 44 u → 44 g/mol
C6H12O6: 180 u → 180 g/mol
Massa fórmula → Massa molar
NaCl: 58,5 u → 58,5 g/mol
K2O: 94 u → 94 g/mol
CaCO3: 100 u → 100 g/mol
Numericamente igual não significa igual. Por exemplo, sua idade pode ser numericamente
igual ao número do apartamento ou casa em que vive. A massa atômica do carbono é 12 u, logo a
sua massa molar é 12 g/mol, ou seja, um átomo de carbono apresenta a massa de 12 u, porém a
massa de 1 mol de carbonos, 6·1023 átomos, possui 12 gramas. Jamais escreva que um átomo de
carbono apresenta 12 gramas.
A massa molar é a principal ferramenta dos cálculos químicos. A
partir dos dados das massas da tabela periódica, pode-se determinar a
quantidade de partículas de qualquer massa e vice-versa. Sabendo que a
grafite é formada, somente, por átomos de carbono, quantos átomos de
carbono existem em 6 gramas de grafite?
1 mol é igual a 6·1023 e, consultando a tabela periódica, sabe- Figura 9 - O grafite é formado por
átomos de carbono [fonte: flickr].
se que a massa molar do carbono é igual 12 g/mol, temos:
12 g/mol de carbono pode ser rescrito por 12 g/ 6·1023 átomos de carbono.
Aula 02 – Cálculos das reações químicas 24
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
12 𝑔 −−−− 6 · 1023 á𝑡𝑜𝑚𝑜𝑠 𝑑𝑒 𝑐𝑎𝑟𝑏𝑜𝑛𝑜
6𝑔 −−−− 𝑥 á𝑡𝑜𝑚𝑜𝑠 𝑑𝑒 𝑐𝑎𝑟𝑏𝑜𝑛𝑜
x = 3·1023 átomos de carbono
Outra forma de calcular o número de mols é utilizando a equação matemática a seguir:
𝑚𝑎𝑠𝑠𝑎 (𝑔)
𝑛 (𝑚𝑜𝑙) = 𝑔
𝑚𝑎𝑠𝑠𝑎 𝑚𝑜𝑙𝑎𝑟 ( )
𝑚𝑜𝑙
Acredito que a construção do raciocínio lógico é uma ferramenta imprescindível para a
aprovação nos vestibulares, portanto durante essa aula usarei somente proporções diretas. Não irei
usar fórmulas nas resoluções das questões. Acredito que a utilização das proporções diretas constrói
clarezas de conceitos químicos, além de aprimoração em matemática. Enfim, só confia e se joga!
24 quilates de diamante é o mesmo que ouro 24 quilates?
O termo quilates é utilizado para designar valor de pedras preciosas. Porém os termos quilate
utilizados para diamante e para ouro são diferentes.
Diamante Ouro
• 1 quilate (ct) equivale a 0,2 1
• 1 quilate (k) significa ou
gramas. 4,17% de pureza.
24
• 1 diamante de 24 quilates • Um anel de ouro de 24
quer dizer 4,8 gramas de quilates quer dizer um anel de
diamante. 1
ouro 24 · 24 = 1 = 100 % de
ouro.
Figura 10 - Diamante e ouro [fonte: pixabay].
Aula 02 – Cálculos das reações químicas 25
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
A palavra quilate pode, gramaticalmente, significar:
Significa Exemplo: Tenho
Como
unidade de 10 quilates de
substantivo
medida diamante.
Quilate
Exemplo: tenho
como adjetivo Significa pureza 10 gramas de
ouro 18 quilates.
Portanto, é permitido dizer “tenho um anel de 20 quilates de ouro 24 quilates”, ou seja, tenho
um anel de 4 gramas de ouro que apresenta 75% de pureza.
Conheça o anel mais caro do mundo: o anel Shawish. A empresa
suíça Shawish criou o primeiro anel esculpido em um único diamante. O
anel de 150 quilates foi construído durante 1 ano através de laser, de
cortes tradicionais e de polimentos. Esse anel está avaliado em 127
milhões de dólares.
Pare, pense e calcule: sabendo que o diamante é formado Figura 11 - Shawish: o anel mais caro do
mundo [fonte: simplyme-nodoubt].
somente por átomos de carbono, quantos átomos de carbono esse
anel possui?
1 𝑞𝑢𝑖𝑙𝑎𝑡𝑒 (𝑐𝑡) − − − − 0,2 𝑔𝑟𝑎𝑚𝑎𝑠
150 𝑞𝑢𝑖𝑙𝑎𝑡𝑒𝑠 − − − − 𝑥 𝑔𝑟𝑎𝑚𝑎𝑠
x = 30 gramas. Sabendo que a massa molar, em g/mol, do carbono é igual a 12.
12 𝑔 −−−− 1 𝑚𝑜𝑙 = 6 · 1023 á𝑡𝑜𝑚𝑜𝑠 𝑑𝑒 𝑐𝑎𝑟𝑏𝑜𝑛𝑜
30 𝑔 −−−− 𝑦 á𝑡𝑜𝑚𝑜𝑠
y = 15·1023 átomos de carbono
(UFRGS RS/2016)
Aula 02 – Cálculos das reações químicas 26
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
O sal rosa do Himalaia é um sal rochoso muito apreciado em gastronomia, sendo obtido
diretamente de uma reserva natural aos pés da cordilheira. Apresenta baixo teor de sódio e é
muito rico em sais minerais, alguns dos quais lhe conferem a cor característica.
Considere uma amostra de 100 g de sal rosa que contenha em sua composição, além de sódio
e outros minerais, os seguintes elementos nas quantidades especificadas:
Magnésio = 36 mg
Potássio = 39 mg
Cálcio = 48 mg
Os elementos, colocados na ordem crescente de número de mols presentes na amostra, são
a) K, Ca, Mg.
b) K, Mg, Ca.
c) Mg, K, Ca.
d) Ca, Mg, K.
e) Ca, K, Mg.
Comentário:
A fim de calcular o número de mols a partir da massa, precisa-se dos dados das massas
molares dos elementos magnésio, potássio, e cálcio que são, respectivamente, 24, 39 e 40
g/mol.
Portanto, a ordem crescente, em mol, dos elementos é: potássio, cálcio e magnésio.
Gabarito: A
(UNIUBE MG/2017)
A sulfacrisoidina (uma sulfa) foi o primeiro agente antimicrobiano utilizado clinicamente,
em 1935, marcando o início da moderna era da quimioterapia antimicrobiana. As sulfas são
uma classe de agentes bacteriostáticos derivados da sulfanilamida, que têm estrutura similar
Aula 02 – Cálculos das reações químicas 27
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
à do ácido p-amino benzoico. O grupo das sulfonamidas compreende seis drogas principais:
sulfanilamida, sulfisoxazol, sulfacetamida, ácido p-amino benzoico, sulfadiazina e
sulfametoxazol, sendo as duas últimas de maior importância clínica. A seguir, estão
representadas as estruturas químicas da sulfadiazina e do sulfametoxazol.
A sulfadiazina é um agente bacteriostático derivado da sulfanilamida, eficiente no
tratamento das infecções gonocócicas, estafilocócicas, estreptocócicas e meningocócicas. Para
adultos, a dose diária prescrita no combate à infecção é de 4 · 750 mg do medicamento, de 6
em 6 h. Analisando a estrutura química do fármaco, o número aproximado de mols do
medicamento ingerido diariamente por um adulto no combate à infecção, considerando a dose
diária recomendada, é de:
a) 0,042 mol
b) 0,083 mol
c) 0,012 mol
d) 0,066 mol
e) 0,050 mol
Comentário:
Dose diária = 4·50 mg = 3000 mg = 3g de sulfadiazina.
A fórmula molecular da sulfadiazina é C10H10O2N4S, portanto a sua massa molar é calculada
por 10·10 g/mol + 10·1 g/mol + 2·16 g/mol + 4·14 g/mol + 32 g/mol = 250 g/mol.
Assim, tem-se:
250 𝑔 −−−− 1 𝑚𝑜𝑙 𝑑𝑒 𝑠𝑢𝑙𝑓𝑎𝑑𝑖𝑎𝑧𝑖𝑛𝑎
3𝑔 −−−− 𝑥 𝑚𝑜𝑙 𝑑𝑒 𝑠𝑢𝑙𝑓𝑎𝑑𝑖𝑎𝑧𝑖𝑛𝑎
x = 0,012 mol
Gabarito: C
(UNESP SP/2017)
O gluconato de cálcio (massa molar = 430 g/mol) é um medicamento destinado principalmente
ao tratamento da deficiência de cálcio. Na forma de solução injetável 10%, ou seja, 100 mg/mL,
este medicamento é destinado ao tratamento da hipocalcemia aguda.
(www.medicinanet.com.br. Adaptado.)
Aula 02 – Cálculos das reações químicas 28
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
(www.hospitalardistribuidora.com.br)
OH OH
O
HO
OH OH O
Ca2+
OH OH
O
HO
OH OH O
gluconato de cálcio
Considere que a constante de Avogadro seja 6,0 1023 mol–1 e que uma pessoa receba uma
dose de 10 mL de uma solução injetável de gluconato de cálcio a 10%. O número total de íons
Ca2+ que entrará no organismo dessa pessoa após ela receber essa dose será
a) 7,1 · 1022.
b) 1,0 · 1023.
c) 5,5 · 1025.
d) 1,4 · 1021.
e) 4,3 · 1024.
Comentário:
Uma pessoa recebe um medicamento na porção de 100 mg/mL, ou seja, 100 mg a cada 1
mL do medicamento. Administrou-se à pessoa 10 mL, logo:
100 𝑚𝑔
· 10 𝑚𝐿 = 1000 𝑚𝑔 = 1 𝑔 de medicamento
𝑚𝐿
O medicamento apresenta em sua fórmula 1 íon de cálcio, portanto 1 mol de moléculas
apresenta 1 mol de íons de cálcio. Sabendo que a massa de 1 mol do medicamento apresenta
430 gramas e que 1 mol de cálcio é o mesmo que 6·1023 íons de cálcio, temos:
Aula 02 – Cálculos das reações químicas 29
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
430 𝑔 𝑑𝑒 𝑚𝑒𝑑𝑖𝑐𝑎𝑚𝑒𝑛𝑡𝑜 −−−− 6 · 1023 íons de cálcio
1 𝑔 𝑑𝑒 𝑚𝑒𝑑𝑖𝑐𝑎𝑚𝑒𝑛𝑡𝑜 −−−− x íons de cálcio
x = 1,39·1021 íons de cálcio
Gabarito: D
(UFAM/2015)
Dados recentes publicados pelo Ministério de Minas e Energia no Balanço Energético Nacional
(BEN 2014 - Ano base 2013, http://www.epe.gov.br) revelam que em 2013, cada brasileiro,
consumindo e produzindo energia, emitiu em média 2,3 t de CO 2. Considerando que a
população brasileira em 2013 era de aproximadamente 200 milhões de habitantes, quantas
moléculas de CO2 foram produzidas, aproximadamente, pela população brasileira?
a) 3 · 1028 moléculas
b) 3 · 1036 moléculas
c) 6 · 1023 moléculas
d) 6 · 1030 moléculas
e) 6 · 1036 moléculas
Comentário:
Primeiramente, calcula-se a massa de CO2 liberada por 200 milhões de pessoas:
Sabendo que 1 mol é igual a 6· 1023 e que a massa molar do CO2 é igual a 44 g/mol, calcula-
se o número de moléculas de CO2 presentes em 460·1012 g:
44 𝑔 𝑑𝑒 𝐶𝑂2 −−−− 6 · 1023 𝑚𝑜𝑙é𝑐𝑢𝑙𝑎𝑠 𝑑𝑒 𝐶𝑂2
460 · 1012 𝑔 𝑑𝑒 𝐶𝑂2 −−−− x 𝑚𝑜𝑙é𝑐𝑢𝑙𝑎𝑠 𝑑𝑒 𝐶𝑂2
x = 6,2·1036 moléculas de CO2
Gabarito: D
5. Lei Volumétrica e Volume Molar
Em 1808, Louis Joseph Gay-Lussac (1778-1850) elaborou a lei volumétrica observando a
proporção, em volume, das substâncias em sistemas de reações químicas gasosas.
Aula 02 – Cálculos das reações químicas 30
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
Lei de Gay-Lussac
Lei de Gay-Lussac ou lei volumétrica: em uma reação química, nas mesmas condições de
temperatura e pressão, os volumes das substâncias no estado gasoso apresentam-se em
proporção em números inteiros e pequenos.
A reação gasosa: 2 H2 (g) + O2 (g) → 2H2O (g), apresenta a proporção, em volume de números
inteiros e pequenos, de 2:1:2.
2 H2 (g) + O2 (g) → 2 H2O (g)
Exemplo 1: 2L 1L 2L
Exemplo 2: 4 mL 2 mL 4 mL
Exemplo 3: 10 L 5L 10 L
Volume Molar
Para materiais gasosos, o volume ocupado por um gás corresponde ao volume do recipiente,
contudo, nas mesmas condições de temperatura e pressão, o volume é proporcional à quantidade
de partículas. Essa afirmação apresenta um detalhamento matemático que será explorado na aula
de gases, por enquanto, a atenção desta aula se mantém nos estudos de mol e suas conversões.
Portanto:
Volume molar: é o volume ocupado por 1 mol de partículas no estado gasoso, a uma dada
pressão e temperatura.
Simplificadamente, o volume molar não depende da natureza do gás (atômica ou molecular),
somente das condições de temperatura e pressão.
Volume
molar na As Condições Normais de
CNTP é Temperatura e Pressão
igual a 22,4 (CNTP) são 0 °C e 1 atm.
L/mol.
Volume
As Condições Ambientes de molar na
Temperatura e Pressão
(CNTP) são 25 °C e 1 atm. CATP é igual
a 25 L/mol.
Aula 02 – Cálculos das reações químicas 31
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
6. Fórmulas Químicas
As fórmulas químicas são classificadas em três tipos: fórmula molecular, fórmula percentual
e fórmula mínima.
Fórmula Molecular ou Fórmula Iônica
A fórmula molecular indica a quantidade real de átomos dos elementos químicos que formam
a molécula, enquanto a fórmula iônica indica a quantidade real de íons na fórmula iônica.
C2H6O • 2 átomos de carbono.
• 6 átomos de hidrogênio.
(fórmula molecular)
• 1 átomo de oxigênio.
• 2 átomos de nitrogênio.
(NH4)2SO4 • 8 átomos de hidrogênio.
(fórmula iônica) • 1 átomo de enxofre.
• 4 átomos de oxigênio.
Fórmula Mínima ou Empírica
A fórmula mínima ou empírica indica a menor proporção, em números inteiros, entre os
elementos químicos da substância.
Fórmula molecular Fórmula mínima
C2H4 CH2
C6H12O6 CH2O
NO2 NO2
Fórmula Percentual ou Centesimal
A fórmula percentual ou centesimal indica a porcentagem, em massa, dos elementos
químicos da substância.
Exemplo: o etanol apresenta fórmula molecular C2H6O. Para calcular a fórmula percentual
desse composto deve-se determinar a contribuição em massa de cada elemento químico e fazer a
proporção percentual pela massa da substância.
Carbono Hidrogênio Oxigênio
Aula 02 – Cálculos das reações químicas 32
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
Massa dos carbonos: Massa dos hidrogênios: Massa do oxigênio:
2·12u = 24 u 6·1u = 6 u 1·16u = 16 u
A massa molecular (24 u + 6 u + 16 u = 46 u) é 100% da massa da fórmula.
Porcentagem, em massa, de Porcentagem, em massa, de Porcentagem, em massa, de
carbono: hidrogênio: oxigênio:
46 𝑢 − − − − 100% 46 𝑢 − − − − 100% 46 𝑢 − − − − 100%
24 𝑢 − − − − 𝑥% 6𝑢 −−−− 𝑥% 16 𝑢 − − − − 𝑥%
x = 52% x = 13% x = 35%
Portanto, a fórmula percentual do etanol é C52%H13%O35%.
(IME RJ/2017 - adaptado)
Um isótopo de cromo, de massa atômica 54, constitui 53% da massa de um óxido formado
exclusivamente pelo isótopo e por oxigênio. A partir dessa informação, pode-se estimar
que a fórmula mínima do óxido é:
a) CrO3.
b) CrO6.
c) Cr2O6.
d) Cr2O3.
e) Cr4O.
Comentário:
Sabendo que as massas molares dos elementos cromo e oxigênio são, respectivamente, 53
g/mol e 16 g/mol, calcula-se:
Aula 02 – Cálculos das reações químicas 33
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
Gabarito: A
(Mackenzie SP/2016)
O ácido acetilsalicílico é um medicamento muito comum e muito utilizado em todo o
mundo possuindo massa molar de 180 g mol–1. Sabendo que a sua composição centesimal
é igual a 60% de carbono, 35,55% de oxigênio e 4,45% de hidrogênio, é correto afirmar
que a sua fórmula molecular é
Dados: massas molares (g mol–1): H = 1, C = 12 e O = 16.
a) C9H8O4
b) C6H5O4
c) C6H4O3
d) C5H4O2
e) C4H2O
Comentário:
Aula 02 – Cálculos das reações químicas 34
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
Gabarito: A
7. Cálculo Estequiométrico
Desde os estudos de Lavoisier e Proust, a humanidade já conseguia prever as quantidades
consumidas e formadas pelas substâncias em uma reação química. A estequiometria consiste na
análise dessa proporção, que pode ser em massa, em mol, em número de partículas (íons, moléculas,
elétrons e outros), em volume, etc.
Para que você consiga fazer todos os cálculos estequiométricos, vou montar um passo a passo
para a sua resolução.
Proporção em Adequação da
Balanceamento Regra de 3
mol proporção
1º Passo
Balanceie as equações químicas. Não é obrigatório que os coeficientes estequiométricos
sejam representados como menores números inteiros.
Aula 02 – Cálculos das reações químicas 35
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
2º Passo
A partir dos números estabelecidos na equação balanceada, leia a proporção, em mol, entre
as substâncias.
3º Passo
Adeque a proporção, em mol, de acordo com as unidades do dado e da incógnita fornecidos
pela questão.
4º Passo
Monte a regra de 3. A 1ª linha da regra de 3 corresponde às transformações elaboradas nos
dois primeiros passos, enquanto a 2ª linha corresponde ao valor do dado e da incógnita.
Exemplo de Estequiometria
A partir do consumo de 10 gramas de hidrogênio, calcule a massa, em gramas, de oxigênio
consumida na reação a seguir:
H2 (g) + O2 (g) → H2O (g)
Resolvendo:
Aula 02 – Cálculos das reações químicas 36
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
Proporção: Mol - Mol
Determine a quantidade de matéria, em mol, de monóxido de carbono produzida pela reação
de 6 mols de oxigênio com quantidade suficiente de carbono na reação: C + O2 → CO.
Resolvendo:
1º Passo – balanceamento: 2 C + 1 O2 → 2 CO
2º Passo – proporção: 1 mol O2 : 2 mol CO
3º Passo – adequação: 1 mol O2 : 2 mol CO
4º Passo – regra de 3: 1 𝑚𝑜𝑙 𝑂2 − − − − 2 𝑚𝑜𝑙 𝐶𝑂
6 𝑚𝑜𝑙 𝑂2 − − − − 𝑥 𝑚𝑜𝑙 𝐶𝑂
x = 12 mols de CO
Proporção: Mol - Massa
Determine a massa, em gramas, de enxofre necessária para a produção de 10 mols de dióxido
de enxofre, tendo quantidade suficiente de oxigênio, na reação: S 8 + O2 → SO2.
Resolvendo:
1º Passo – balanceamento: 1 S8 + 8 O2 → 8 SO2
2º Passo – proporção: 1 mol S8 : 8 mol SO2
3º Passo – adequação: 1 · 256 g S8 : 8 mol SO2
4º Passo – regra de 3: 1 · 256 𝑔 𝑆8 − − − − 8 𝑚𝑜𝑙 𝑆𝑂2
𝑥 𝑔 𝑆8 − − − − 10 𝑚𝑜𝑙 𝑆𝑂2
Aula 02 – Cálculos das reações químicas 37
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
x = 320 gramas de SO2
Proporção: Massa - volume
Nas CNTP, determine o volume, em litros, de nitrogênio necessário para o consumo de 24
gramas de hidrogênio durante a formação da amônia: N2 (g) + H2 (g) → NH3 (g).
Resolvendo: (CNTP: 22,4 L/mol)
1º Passo – balanceamento: 1 N2 + 3 H2 → 2 NH3
2º Passo – proporção: 1 mol N2 : 3 mol H2
3º Passo – adequação: 1·22,4 L N2 : 3·2 g H2
4º Passo – regra de 3: 22,4 𝐿 𝑁2 − − − − 6 𝑔 𝐻2
𝑥 𝐿 𝑁2 − − − − 24 𝑔 𝐻2
x = 89,6 L de N2
Proporção: Massa - Partículas
Determine o número de átomos de ferro consumido em uma reação química, com
quantidade suficiente de ácido clorídrico, que produziu 32,5 gramas de cloreto férrico pela reação:
Fe + HC → FeC3 + H2
Resolvendo:
1º Passo – balanceamento: 1 Fe + 3 HC → 1 FeC3 + 3/2 H2
2º Passo – proporção: 1 mol Fe : 1 mol FeC3
3º Passo – adequação: 1 · 6·1023 átomos Fe : 1·162,5 g FeC3
4º Passo – regra de 3: 6 · 1023 á𝑡𝑜𝑚𝑜𝑠 𝑑𝑒 𝐹𝑒 − − − − 162,5 𝑔 𝐹𝑒𝐶𝑙3
𝑥 á𝑡𝑜𝑚𝑜𝑠 𝑑𝑒 𝐹𝑒 − − − − 32,5 𝑔 𝐹𝑒𝐶𝑙3
23
x = 1,2·10 átomos de Fe
Você já percebeu que às vezes se usa mol e as vezes se usa mols? Sabe a diferença? Essa
confusão ocorre porque mol é o símbolo da unidade e a unidade por extenso. Essa confusão não
ocorre com outras unidades, por exemplo pode-se escrever 2 gramas (por extenso) ou 2 g (símbolo
da unidade). Analogamente, 2 mols (por extenso) ou 2 mol (símbolo da unidade).
(Uni-FaceF SP/2017)
Aula 02 – Cálculos das reações químicas 38
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
Durante o processo de fermentação das uvas, seus açúcares são transformados em etanol.
Esse processo pode ser representado pela equação:
C6H12O6 → 2 C2H5OH + 2 CO2
Considerando que a reação tenha rendimento total, a massa de açúcar necessária para
sintetizar 414 g de etanol é próxima de
a) 1 656 g.
b) 810 g.
c) 552 g.
d) 108 g.
e) 40 g.
Comentário:
180 𝑔 𝑑𝑒 𝐶6 𝐻12 𝑂6 −−−− 2 · 46 𝑔 𝑑𝑒 𝐶2 𝐻5 𝑂𝐻
𝑥 𝑔 𝑑𝑒 𝐶6 𝐻12 𝑂6 −−−− 414 𝑔 𝑑𝑒 𝐶2 𝐻5 𝑂𝐻
x = 810 g de C6H12O6
Gabarito: B
(Fac. Direito de São Bernardo do Campo SP/2018)
Observe a reação, não balanceada, que representa uma das maneiras de produção do gás
cloro.
MnO2(s) + HCl(aq) → MnCl2(aq) + H2O(l) + Cl2(g)
Para produção de 3 mols de Cl2 quantos gramas de HCl são necessários?
a) 219 g
b) 438 g
c) 109,5 g
d) 213 g
Comentário:
Balanceando a reação química: 1 MnO2(s) + 4 HCl(aq) → 1 MnCl2(aq) + 2 H2O(l) + 1 Cl2(g)
1 𝑚𝑜𝑙 𝑑𝑒 𝐶𝑙2 −−−− 4 · 36,5 𝑔 𝑑𝑒 𝐻𝐶𝑙
3 𝑚𝑜𝑙 𝑑𝑒 𝐶𝑙2 −−−− 𝑥 𝑔 𝑑𝑒 𝐻𝐶𝑙
x = 438 g de HC
Aula 02 – Cálculos das reações químicas 39
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
Gabarito: B
8. Aspectos Reais do Cálculo Estequiométrico
Conforme visto nas aulas anteriores, a maior parte dos materiais é encontrada impura,
portanto, em uma reação química, são encontradas outras substâncias além dos reagentes
necessários. Então, para o cálculo estequiométrico preciso e exato, é necessário averiguar quatro
aspectos reais: a pureza dos materiais, o rendimento da reação, a possibilidade de reagentes em
excesso e a probabilidade de reações sucessivas.
Pureza
Denominaremos pureza como a porção que participa da reação, que pode ou não ser o
componente mais abundante do material. Para o cálculo da pureza, antes ou depois do cálculo
estequiométrico, monte uma regra de 3 à parte:
𝑚𝑎𝑡𝑒𝑟𝑖𝑎𝑙 𝑖𝑚𝑝𝑢𝑟𝑜 −−−− 100%
𝑚𝑎𝑡𝑒𝑟𝑖𝑎𝑙 𝑝𝑢𝑟𝑜 𝑜𝑢 𝑠𝑢𝑏𝑠𝑡â𝑛𝑐𝑖𝑎 −−−− 𝑥% (𝑝𝑢𝑟𝑒𝑧𝑎)
Exemplo: Considere uma amostra de 500 g de bauxita, minério formado por 75% de óxido de
alumínio, que sofreu reação com carbono e produziu alumínio metálico e dióxido de carbono.
Calcule, em gramas, a quantidade de alumínio produzida a partir do consumo de toda quantidade
de óxido de alumínio, considerando que existem quantidades suficientes de carbono para ocorrer a
reação.
Resolução:
𝑚𝑎𝑡𝑒𝑟𝑖𝑎𝑙 𝑖𝑚𝑝𝑢𝑟𝑜 −−−− 100% 100 𝑔 𝑏𝑎𝑢𝑥𝑖𝑡𝑎 − − − − 100%
𝑚𝑎𝑡𝑒𝑟𝑖𝑎𝑙 𝑝𝑢𝑟𝑜 𝑜𝑢 𝑠𝑢𝑏𝑠𝑡â𝑛𝑐𝑖𝑎 −−−− 𝑥% (𝑝𝑢𝑟𝑒𝑧𝑎) 𝑥 𝑔 𝐴𝑙2 𝑂3 − − − − 75%
x = 375 g de Al2O3
A partir do cálculo da quantidade da substância que participa da reação, pode-se realizar o
cálculo estequiométrico:
1 Al2O3 + 3 C → 2 Al + 3 CO2
Proporção: 1 mol Al2O3 – 2 mols Al
1 · 102 g 𝐴𝑙2 𝑂3 −−−− 2 · 27 𝑔 𝑑𝑒 𝐴𝑙
375 g 𝐴𝑙2 𝑂3 −−−− 𝑥 g 𝑑𝑒 𝐴𝑙
x = 198,53 g de A
Aula 02 – Cálculos das reações químicas 40
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
Não realize o cálculo estequiométrico com a quantidade da amostra total, ou seja, impura.
Então, fique atento nas questões sobre pureza e impureza e já separe as quantidades do que é
mistura e do que é substância.
Rendimento
Nem toda quantidade colocada em um sistema de reação é, realmente, consumida. Esse fato
pode ser explicado por diversos motivos: falta de tempo para o término da reação, impureza dos
reagentes, outras reações indevidas, interrupção da energia de ativação, etc. O objetivo dessa aula
não é buscar explicações para explicar o rendimento do processo, mas sim calculá-lo.
A fim de realizar o cálculo do rendimento, é necessário montar uma regra de 3 à parte. Irei
utilizar dois termos: porção teórica e porção experimental. A porção teórica refere-se à quantidade
disponível no sistema para participar da reação, ou seja, uma quantidade hipotética que pode reagir
ou ser formada no processo. A porção experimental corresponde à parte que, realmente, participa
da reação, ou seja, é a quantidade consumida ou formada no processo. Para calcular a porção
experimental ou o rendimento, a questão precisa fornecer dados da realidade do processo.
porção
rendimento
experimental
Normalmente, ou a questão fornece a quantidade experimental e solicita o rendimento, ou a
operação contrária.
𝑝𝑜𝑟çã𝑜 𝑡𝑒ó𝑟𝑖𝑐𝑎 −−−− 100%
𝑝𝑜𝑟çã𝑜 𝑒𝑥𝑝𝑒𝑟𝑖𝑚𝑒𝑛𝑡𝑎𝑙 −−−− 𝑥% (𝑟𝑒𝑛𝑑𝑖𝑚𝑒𝑛𝑡𝑜)
Exemplo:
O carbonato de cálcio sofre decomposição térmica e produz óxido de cálcio e dióxido de
carbono. Em um laboratório, 10 gramas de uma amostra de carbonato de cálcio produziram 4
gramas de óxido de cálcio. Determine o rendimento percentual desse processo.
Resolução:
1 CaCO3 → 1 CaO + 1 CO2
𝑝𝑜𝑟çã𝑜 𝑡𝑒ó𝑟𝑖𝑐𝑎 −−−− 100%
𝑝𝑜𝑟çã𝑜 𝑒𝑥𝑝𝑒𝑟𝑖𝑚𝑒𝑛𝑡𝑎𝑙 − − − − 𝑥% (𝑟𝑒𝑛𝑑𝑖𝑚𝑒𝑛𝑡𝑜)
10 𝑔 𝑑𝑒 𝐶𝑎𝐶𝑂3 −−−− 100%
? 𝑝𝑜𝑟çã𝑜 𝑒𝑥𝑝𝑒𝑟𝑖𝑚𝑒𝑛𝑡𝑎𝑙 𝑑𝑒 𝑐𝑜𝑛𝑠𝑢𝑚𝑜 𝑑𝑒 𝐶𝑎𝐶𝑂3 −−−− 𝑥% (𝑟𝑒𝑛𝑑𝑖𝑚𝑒𝑛𝑡𝑜)
Aula 02 – Cálculos das reações químicas 41
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
Para calcular o rendimento do procedimento laboratorial, é necessário determinar a
quantidade de carbonato de cálcio que, efetivamente, participou da reação. A questão não informou
quantos dos 10 gramas foram consumidos, mas sim que existe esse consumo no procedimento. A
quantidade que regiu de carbonato de cálcio é proporcional à quantidade formada de óxido de
cálcio, 4 gramas. Portanto:
Proporção: 1 mol CaCO3 – 1 mol de CaO
1 · 100 g 𝐶𝑎𝐶𝑂3 − − − − 1 · 56 𝑔 𝑑𝑒 𝐶𝑎𝑂
y g 𝐶𝑎𝐶𝑂3 −−−− 4 g 𝑑𝑒 𝐶𝑎𝑂
y = 7,14 g de CaCO3
(essa é a quantidade que, efetivamente, foi consumida na reação).
Finalizando:
10 𝑔 𝑑𝑒 𝐶𝑎𝐶𝑂3 −−−− 100%
? 𝑝𝑜𝑟çã𝑜 𝑒𝑥𝑝𝑒𝑟𝑖𝑚𝑒𝑛𝑡𝑎𝑙 𝑑𝑒 𝑐𝑜𝑛𝑠𝑢𝑚𝑜 𝑑𝑒 𝐶𝑎𝐶𝑂3 −−−− 𝑥% (𝑟𝑒𝑛𝑑𝑖𝑚𝑒𝑛𝑡𝑜)
10 𝑔 𝑑𝑒 𝐶𝑎𝐶𝑂3 −−−− 100%
7,14 𝑔 𝐶𝑎𝐶𝑂3 − − − − 𝑥% (𝑟𝑒𝑛𝑑𝑖𝑚𝑒𝑛𝑡𝑜 )
x = 71,4 %
A reação apresenta 71,4% de rendimento.
Excesso e Limitante
Segundo Proust, a proporção, em massa, das substâncias envolvidas em uma reação é
constante. Atualmente, entende-se que essa proporção é determinada não somente em massa, mas
em qualquer relação de quantidade. Porém, o que acontece quando os reagentes, de uma reação
química, não se encontram na proporção exata para reagirem?
Considerando uma reação com 100% de rendimento, quando os reagentes não estão em
proporção estequiométrica para reagirem, um deles será o reagente limitante, ou seja, se esgotará
enquanto o outro permanecerá no sistema. O reagente que permanece no sistema é denominado
reagente em excesso.
O segredo está na leitura da questão. Preste atenção nas palavras “colocados”, “reagiu”,
“consumiu”, etc. no comando da questão. Exemplos: “foram colocados 5 gramas de cloreto de
sódio” é diferente de “foram consumidos 5 gramas de cloreto de sódio”. O termo “colocado” é
empregado no sentido de que existe no sistema, podendo ou não, ser consumido totalmente,
enquanto os termos “consumido” e “reagiu” indicam a participação na reação.
Para identificar o reagente em excesso e o reagente limitante, basta fazer o teste de consumo
total de um dos reagentes que foram colocados no sistema: calcule a quantidade necessária do outro
Aula 02 – Cálculos das reações químicas 42
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
reagente e avalie a possibilidade da reação completa do reagente testado. Feito a identificação do
reagente limitante, utilize-o para calcular o consumo/formação das espécies envolvidas na
transformação.
1º Passo: escolha um dos reagentes para testar como reagente limitante.
2º Passo: monte a regra de 3 entre os reagentes e calcule a quantidade
necessária do outro reagente para o consumo de todo o reagente testado
3º Passo: avalie a possibilidade do consumo a partir das quantidades que
foram colocadas no sistema.
Vide o exemplo a seguir:
Em uma reação química, foram colocados 20 gramas de gás hidrogênio e 50 gramas de gás
nitrogênio, identifique o reagente limitante e o em excesso.
1 N2 + 3 H2 → 2NH3
1º Passo: Foram colocados 20 g de H2 e 50 g de N2. Escolherei, aleatoriamente, o hidrogênio
para testar se esse é o reagente limitante.
2º Passo: Proporção de reação entre nitrogênio e hidrogênio: 1 mol e 3 mol.
3º Passo: Para consumir, totalmente, os 20 gramas de hidrogênio são necessários 93,3
gramas de N2, porém no sistema só há 50 gramas de N2; logo o hidrogênio é o reagente em excesso
porque não será totalmente consumido. Identificamos, assim, o reagente em excesso como o
hidrogênio e o reagente limitante como nitrogênio.
Se em vez dos 20 g de hidrogênio testado, tivessem sido testados os 50 g de N 2, teríamos
chegado a mesma conclusão:
Aula 02 – Cálculos das reações químicas 43
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
Para consumir, totalmente, os 50 gramas de nitrogênio são necessários 10,71 gramas de H 2,
essa possibilidade é permitida porque no sistema existem 20 gramas de hidrogênio. Assim, conclui-
se que o nitrogênio é o reagente limitante e o hidrogênio é o excesso.
Reações Sucessivas
As reações sucessivas são reações sequenciais em que para determinar o consumo e a
formação das substâncias é possível somar as equações e calcular a partir de uma reação global.
Essas reações sucessivas são possíveis, pois existe substância que se comporta como reagente em
uma etapa e como produto em outra. Essa substância é denominada intermediária.
1º passo: balanceie 2º passo: iguale a
3º passo: some as
cada reação quantidade dos
equações.
separadamente. intermediários.
Exemplo:
Determine a equação global das reações sucessivas abaixo.
S8 + O2 → SO2
SO2 + O2 → SO3
SO3 + H2O → H2SO4
1º Passo: balanceamento.
S8 + 8 O2 → 8 SO2
2 SO2 + O2 → 2 SO3
SO3 + H2O → H2SO4
2º Passo: iguale a quantidade dos intermediários.
S8 + 8 O2 → 8 SO2
2 SO2 + O2 → 2 SO3 S8 + 8 O2 → 8 SO2
(multiplico todos os índices por 4)
8 SO2 + 4 O2 → 8 SO3
SO3 + H2O → H2SO4
(multiplico todos os índices por 8) 8 SO3 + 8 H2O → 8 H2SO4
3º Passo: Ao somar as equações, cancele os intermediários.
Aula 02 – Cálculos das reações químicas 44
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
E assim se obtém a equação global.
9. Questões Fundamentais
I. Questão fundamental 01
A partir da reação abaixo, complete o quadro a seguir.
Carbono + Oxigênio → Gás carbônico OBSERVAÇÃO
12 g 32 g X
6g Y Z
W 6,4 g T
4g Q R Restou 1 g de carbono ao final da reação
II. Questão fundamental 02
Balanceie as equações químicas seguintes.
a) C2H6O + O2 → CO2 + H2O
b) Na2CO3 + HC → NaC + H2O + CO2
c) C6H12O6 → C2H6O + CO2
d) C4H10 + O2 → CO2 + H2O
e) FeC3 + Na2CO3 → Fe2(CO3)3 + NaC
f) NH4C + Ba(OH)2 → BaC2 + NH3 + H2O
g) Ca(OH)2 + H3PO4 → Ca3(PO4)2 + H2O
h) Fe2(CO3)3 + H2SO4 → Fe2(SO4)3 + H2O + CO2
i) Na2O + (NH4)2SO4 → Na2SO4 + H2O + NH3
j) NaN3 → Na + N2
k) Fe2O3 + C → Fe + CO
l) FeS2 + O2 → Fe2O3 + SO2
m) NH3 + O2 → NO + H2O
n) KMnO4 + H2SO4 → Mn2O7 + K2SO4 + H2O
Aula 02 – Cálculos das reações químicas 45
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
o) CS2 + O2 → CO2 + SO2
p) H3PO4 + CaO → Ca3(PO4)2 + H2O
III. Questão fundamental 03- cálculos sem excesso, 100% de rendimento e 100% de pureza.
a) A partir da equação abaixo, calcule a massa, em gramas, de CO 2 obtida pelo consumo de 4,6
gramas de etanol.
C2H6O + O2 → CO2 + H2O
b) A partir da equação abaixo, calcule a quantidade de matéria, em mol, de NaCl obtida pelo
consumo de 5 mols de carbonato de sódio.
Na2CO3 + HCl → NaCl + H2O + CO2
c) A partir da equação abaixo, calcule o número de moléculas de C 6H12O6 necessários para obter
2,2 gramas de dióxido de carbono.
C6H12O6 → C2H6O + CO2
d) A partir da equação abaixo, calcule a massa, em gramas, de gás oxigênio necessária para
consumir 2 mols de butano.
C4H10 + O2 → CO2 + H2O
e) A partir da equação abaixo, calcule a quantidade de matéria, em mol, de carbonato férrico
obtida ao se obter 175,5 gramas de cloreto de sódio.
FeCl3 + Na2CO3 → Fe2(CO3)3 + NaCl
Reagentes em excesso.
f) A partir da equação abaixo, calcule a quantidade de matéria, em mol, de cloreto de bário
produzido a partir da reação de 10 mols de cloreto de amônio e 7 mols de hidróxido de bário.
NH4Cl + Ba(OH)2 → BaCl2 + NH3 + H2O
g) A partir da equação abaixo, calcule a massa, em gramas, de fosfato de cálcio produzida a
partir da reação de 74 g de hidróxido de cálcio e 98 gramas de ácido fosfórico.
Ca(OH)2 + H3PO4 → Ca3(PO4)2 + H2O
h) A partir da equação abaixo, calcule o número de moléculas de dióxido de carbono produzido
a partir da reação de 10 mols de carbonato férrico e 98 gramas de ácido sulfúrico.
Fe2(CO3)3 + H2SO4 → Fe2(SO4)3 + H2O + CO2
i) A partir da equação abaixo, calcule a massa, em gramas, de amônia produzida a partir da
reação de 124 gramas de óxido de sódio e 3 mols de sulfato de amônio.
Na2O + (NH4)2SO4 → Na2SO4 + H2O + NH3
Pureza.
Aula 02 – Cálculos das reações químicas 46
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
j) A partir da equação abaixo, calcule a massa, em gramas, de gás nitrogênio produzida a partir
da reação completa de 78 gramas de uma amostra com 80% de pureza de NaN 3.
NaN3 → Na + N2
k) A partir da equação abaixo, calcule a massa, em gramas, de carvão (com 60% de pureza de
carbono) necessária para obter 5,6 gramas de ferro metálico.
Fe2O3 + C → Fe + CO
l) A partir da equação abaixo, calcule a massa, em gramas, de ar (com 70% de oxigênio)
necessária para obter 5 mols de dióxido de enxofre.
FeS2 + O2 → Fe2O3 + SO2
m) A partir da equação abaixo, calcule a massa, em gramas, de monóxido de nitrogênio
produzida a partir da reação completa de 4,76 gramas de uma amostra, que possui 60% de
pureza de amônia.
NH3 + O2 → NO + H2O
Rendimento.
n) A partir da equação abaixo, calcule o número de moléculas de água produzido a partir da
reação, com 70% de rendimento, de 0,98 gramas de ácido sulfúrico.
KMnO4 + H2SO4 → Mn2O7 + K2SO4 + H2O
o) A partir da equação abaixo, calcule a quantidade de matéria, em mol, de dióxido de enxofre
produzida a partir da reação, com 80% de rendimento, de 9,6 gramas de gás oxigênio.
CS2 + O2 → CO2 + SO2
p) A partir da equação abaixo, calcule o rendimento, em porcentagem, sabendo que o consumo
de 9,8 gramas de ácido fosfórico produziu 0,04 mol de fosfato de cálcio.
H3PO4 + CaO → Ca3(PO4)2 + H2O
10. Já Caiu na Fuvest
1. (FUVEST SP/2019)
O cinamaldeído é um dos principais compostos que dão o sabor e o aroma da canela.
Quando exposto ao ar, oxida conforme a equação balanceada:
Aula 02 – Cálculos das reações químicas 47
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
Uma amostra de 19,80 g desse composto puro foi exposta ao ar por 74 dias e depois
pesada novamente, sendo que a massa final aumentou em 1,20 g A porcentagem desse
composto que foi oxidada no período foi de
Note e adote:
- Massas molares (g/mol): Cinamaldeído = 132; O2 = 32.
- Considere que não houve perda de cinamaldeído ou do produto de oxidação por
evaporação.
a) 10%
b) 25%
c) 50%
d) 75%
e) 90%
2. (FUVEST SP/2016)
Uma dieta de emagrecimento atribui a cada alimento um certo número de pontos, que
equivale ao valor calórico do alimento ao ser ingerido. Assim, por exemplo, as combinações abaixo
somam, cada uma, 85 pontos:
• 4 colheres de arroz + 2 colheres de azeite + 1 fatia de queijo branco.
• 1 colher de arroz + 1 bife + 2 fatias de queijo branco.
• 4 colheres de arroz + 1 colher de azeite + 2 fatias de queijo branco.
• 4 colheres de arroz + 1 bife.
Com base nas informações fornecidas, e na composição nutricional dos alimentos,
considere as seguintes afirmações:
I. A pontuação de um bife de 100 g é 45.
II. O macronutriente presente em maior quantidade no arroz são os carboidratos.
III. Para uma mesma massa de lipídeo de origem vegetal e de carboidrato, a razão
é 1,5.
É correto o que se afirma em
Aula 02 – Cálculos das reações químicas 48
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
a) I, apenas.
b) II, apenas.
c) I e II, apenas.
d) II e III, apenas.
e) I, II e III.
3. (FUVEST SP/2002)
O aspartame, um adoçante artificial, pode ser utilizado para substituir o açúcar de cana.
Bastam 42 miligramas de aspartame para produzir a mesma sensação de doçura que 6,8 gramas
de açúcar de cana. Sendo assim, quantas vezes, aproximadamente, o número de moléculas de
açúcar de cana deve ser maior do que o número de moléculas de aspartame para que se tenha
o mesmo efeito sobre o paladar?
Dados:
massas molares aproximadas (g/mol)
açúcar de cana : 340
adoçante artificial : 300
a) 30
b) 50
c) 100
d) 140
e) 200
4. (FUVEST SP/1995)
Linus Pauling, prêmio Nobel de Química e da Paz, faleceu recentemente aos 93 anos. Era
um ferrenho defensor das propriedades terapêuticas da vitamina C. Ingeria diariamente cerca
de 2,1 x 10-2 mol dessa vitamina.
Dose diária recomendada de vitamina C (C6H8O6) .......... 62 mg
Quantas vezes, aproximadamente, a dose ingerida por Pauling é maior que a
recomendada?
a) 10
b) 60
c) 1,0 · 102
d) 1,0 · 103
e) 6,0 · 104
5. (FUVEST SP/2004)
Aula 02 – Cálculos das reações químicas 49
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
Com a finalidade de determinar a fórmula de certo carbonato de um metal Me, seis
amostras, cada uma de 0,0100 mol desse carbonato, foram tratadas, separadamente, com
volumes diferentes de ácido clorídrico de concentração 0,500 mol/L. Mediu-se o volume de gás
carbônico produzido em cada experiência, à mesma pressão e temperatura.
O volume molar do gás carbônico, nas condições da experiência, é igual a 24,8 L/mol.
Então, a fórmula do carbonato deve ser:
a) Me2CO3
b) MeCO3
c) Me2(CO3)3
d) Me(CO3)2
e) Me2(CO3)5
6. (FUVEST SP/2017)
Em uma aula experimental, dois grupos de alunos (G1 e G2) utilizaram dois
procedimentos diferentes para estudar a velocidade da reação de carbonato de cálcio com
excesso de ácido clorídrico. As condições de temperatura e pressão eram as mesmas nos dois
procedimentos e, em cada um deles, os estudantes empregaram a mesma massa inicial de
carbonato de cálcio e o mesmo volume de solução de ácido clorídrico de mesma concentração.
O grupo G1 acompanhou a transformação ao longo do tempo, realizada em um sistema
aberto, determinando a variação de massa desse sistema (Figura 1 e Tabela).
O grupo G2 acompanhou essa reação ao longo do tempo, porém determinando o volume
de dióxido de carbono recolhido (Figura 2).
Comparando os dois experimentos, os volumes aproximados de CO2, em litros, recolhidos
pelo grupo G2 após 60, 180 e 240 segundos devem ter sido, respectivamente,
a) 0,14; 0,20 e 0,25
Aula 02 – Cálculos das reações químicas 50
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
b) 0,14; 0,34 e 0,60
c) 0,34; 0,48 e 0,60
d) 0,34; 0,48 e 0,88
e) 0,62; 0,88 e 1,10
Note e adote:
massa molar do CO2: 44 g/mol;
volume molar do CO2: 24 L/mol;
desconsidere a solubilidade do CO2 em água.
7. (FUVEST SP/2017)
Nas mesmas condições de pressão e temperatura, 50 L de gás propano (C 3H8) e 250 L de
ar foram colocados em um reator, ao qual foi fornecida energia apenas suficiente para iniciar a
reação de combustão. Após algum tempo, não mais se observou a liberação de calor, o que
indicou que a reação havia-se encerrado.
Com base nessas observações experimentais, três afirmações foram feitas:
I. Se tivesse ocorrido apenas combustão incompleta, restaria propano no reator.
II. Para que todo o propano reagisse, considerando a combustão completa, seriam
necessários, no mínimo, 750 L de ar.
III. É provável que, nessa combustão, tenha se formado fuligem.
Está correto apenas o que se afirma em
a) I.
b) III.
c) I e II.
d) I e III.
e) II e III.
Note e adote:
Composição aproximada do ar em volume: 80% de N2 e 20%de O2.
8. (FUVEST SP/2016)
Um dirigível experimental usa hélio como fluido ascensional e octano (C8H18) como
combustível em seu motor, para propulsão. Suponha que, no motor, ocorra a combustão
completa do octano:
25
C8H18(g) + O2(g) → 8 CO2(g) + 9 H2O(g)
2
Aula 02 – Cálculos das reações químicas 51
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
Para compensar a perda de massa do dirigível à medida que o combustível é queimado,
parte da água contida nos gases de exaustão do motor é condensada e armazenada como lastro.
O restante do vapor de água e o gás carbônico são liberados para a atmosfera.
Qual é a porcentagem aproximada da massa de vapor de água formado que deve ser
retida para que a massa de combustível queimado seja compensada?
a) 11%
b) 16%
c) 39%
d) 50%
e) 70%
Note e adote:
Massa molar (g/mol):
H2O ...... 18
O2 ............. 32
CO2 ....... 44
C8H18 ...... 114
9. (FUVEST SP/2015)
Amônia e gás carbônico podem reagir formando ureia e água. O gráfico ao lado mostra as
massas de ureia e de água que são produzidas em função da massa de amônia, considerando as
reações completas.
A partir dos dados do gráfico e dispondo-se de 270 g de amônia, a massa aproximada, em
gramas, de gás carbônico minimamente necessária para reação completa com essa quantidade
de amônia é
a) 120
b) 270
c) 350
d) 630
e) 700
Aula 02 – Cálculos das reações químicas 52
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
10. (FUVEST SP/2015)
Uma estudante de Química realizou o seguinte experimento: pesou um tubo de ensaio
vazio, colocou nele um pouco de NaHCO3 (s) e pesou novamente. Em seguida, adicionou ao tubo
de ensaio excesso de solução aquosa de HCl, o que provocou a reação química representada por
NaHCO3 (s) + HCl (aq) → NaCl (aq) + CO2 (g) + H2O (l)
Após a reação ter-se completado, a estudante aqueceu o sistema cuidadosamente, até que
restasse apenas um sólido seco no tubo de ensaio. Deixou o sistema resfriar até a temperatura
ambiente e o pesou novamente. A estudante anotou os resultados desse experimento em seu
caderno, juntamente com dados obtidos consultando um manual de Química:
A estudante desejava determinar a massa de
I. HCl que não reagiu;
II. NaCl que se formou;
III. CO2 que se formou.
Considerando as anotações feitas pela estudante, é possível determinar a massa de
a) I, apenas.
b) II, apenas.
c) I e III, apenas.
d) II e III, apenas.
e) I, II e III.
11. (FUVEST SP/2013)
Uma moeda antiga de cobre estava recoberta com uma camada de óxido de cobre (II).
Para restaurar seu brilho original, a moeda foi aquecida ao mesmo tempo em que se passou
sobre ela gás hidrogênio. Nesse processo, formou-se vapor de água e ocorreu a redução
completa do cátion metálico.
Aula 02 – Cálculos das reações químicas 53
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
As massas da moeda, antes e depois do processo descrito, eram, respectivamente, 0,795
g e 0,779 g.
Assim sendo, a porcentagem em massa do óxido de cobre (II) presente na moeda, antes
do processo de restauração, era
Dados:
Massas molares (g/mol)
H = 1,00
O = 16,0
Cu = 63,5
a) 2%
b) 4%
c) 8%
d) 10%
e) 16%
12. (FUVEST SP/2012)
Volumes iguais de uma solução de I2 (em solvente orgânico apropriado) foram colocados
em cinco diferentes frascos. Em seguida, a cada um dos frascos foi adicionada uma massa
diferente de estanho (Sn), variando entre 0,2 e 1,0 g. Em cada frasco, formou-se uma certa
quantidade de SnI4, que foi, então, purificado e pesado. No gráfico abaixo, são apresentados os
resultados desse experimento.
Com base nesses resultados experimentais, é possível afirmar que o valor da relação
é, aproximadamente,
a) 1:8
b) 1:4
c) 1:2
d) 2:1
Aula 02 – Cálculos das reações químicas 54
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
e) 4:1
13. (FUVEST SP/2010)
Sob condições adequadas, selênio (Se) e estanho (Sn) podem reagir, como representado
pela equação
2 Se + Sn → SnSe2
Em um experimento, deseja-se que haja reação completa, isto é, que os dois reagentes
sejam totalmente consumidos. Sabendo-se que a massa molar do selênio (Se) é 2/3 da massa
molar do estanho (Sn), a razão entre a massa de selênio e a massa de estanho (mSe : mSn), na
reação, deve ser de
a) 2:1
b) 3:2
c) 4:3
d) 2:3
e) 1:2
14. (FUVEST SP/2006)
Com a chegada dos carros com motor Flex, que funcionam tanto com álcool quanto com
gasolina, é importante comparar o preço do litro de cada um desses combustíveis. Supondo-se
que a gasolina seja octano puro e o álcool, etanol anidro, as transformações que produzem
energia podem ser representadas por:
25
C8H18(l) + O2 (g) → 8 CO2(g) + 9 H2O (g) + 5100kJ
2
C2H5OH(l) + 3 O2 (g) → 2 CO2 (g) + 3 H2O (g) + 1200kJ
Considere que, para o mesmo percurso, idêntica quantidade de energia seja gerada no
motor Flex, quer se use gasolina, quer se use álcool. Nesse contexto, será indiferente, em termos
econômicos, usar álcool ou gasolina se o quociente entre o preço do litro de álcool e do litro de
gasolina for igual a:
a) 1/2
b) 2/3
c) 3/4
d) 4/5
e) 5/6
Aula 02 – Cálculos das reações químicas 55
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
15. (FUVEST SP/2006)
Embalagens de fertilizantes do tipo NPK trazem três números, compostos de dois
algarismos, que se referem, respectivamente, ao conteúdo de nitrogênio, fósforo e potássio,
presentes no fertilizante. O segundo desses números dá o conteúdo de fósforo, porém expresso
como porcentagem, em massa, de pentóxido de fósforo. Para preparar 1 kg de um desses
fertilizantes, foram utilizados 558 g de mono-hidrogenofosfato de amônio e 442 g de areia
isenta de fosfatos. Na embalagem desse fertilizante, o segundo número, relativo ao fósforo, deve
ser, aproximadamente,
a) 10
b) 20
c) 30
d) 40
e) 50
16. (FUVEST SP/2006)
O tanque externo do ônibus espacial Discovery carrega, separados, 1,20·106 L de
hidrogênio líquido a –253 °C e 0,55 · 106 L de oxigênio líquido a –183 °C. Nessas temperaturas,
a densidade do hidrogênio é 34 mol/L (equivalente a 0,068 g/mL) e a do oxigênio é 37 mol/L
(equivalente a 1,18 g/mL).
Dados:
H = 1,0; O =16
Considerando o uso que será feito desses dois líquidos, suas quantidades (em mols), no
tanque, são tais que há
a) 100% de excesso de hidrogênio.
b) 50% de excesso de hidrogênio.
c) proporção estequiométrica entre os dois.
d) 25% de excesso de oxigênio.
e) 75% de excesso de oxigênio.
17. (FUVEST SP/2016)
Sabe-se que os metais ferro (Fe0), magnésio (Mg0) e estanho (Sn0) reagem com soluções
de ácidos minerais, liberando gás hidrogênio e formando íons divalentes em solução.
Aula 02 – Cálculos das reações químicas 56
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
Foram feitos três experimentos em que três amostras metálicas de mesma massa
reagiram, separada e completamente, com uma solução aquosa de ácido clorídrico (HC (aq))
de concentração 0,1 mol/L.
Os resultados obtidos foram:
Massa da Volume da solução de
Composição da
Experimento amostra HC (aq) (0,1 mol /L) gasto na reação
amostra metálica
metálica (g) completa
1 5,6 Fe0 puro V1
Fe0 contendo Mg0
2 5,6 V2
como impureza
Fe0 contendo Sn0
3 5,6 V3
como impureza
Colocando-se os valores de V1, V2 e V3 em ordem decrescente, obtém-se
Note e adote:
Massa molar (g/ mol) : Mg ....... 24
Fe ....... 56
Sn ..... 119
a) V2>V3>V1
b) V3>V1>V2
c) V1>V3>V2
d) V2>V1>V3
e) V1>V2>V3
18. (FUVEST SP/2009)
Em três balanças aferidas, A, B e C, foram colocados três béqueres de mesma massa, um
em cada balança. Nos três béqueres, foram colocados volumes iguais da mesma solução aquosa
de ácido sulfúrico. Foram separadas três amostras, de massas idênticas, dos metais magnésio,
ouro e zinco, tal que, havendo reação com o ácido, o metal fosse o reagente limitante. Em cada
um dos béqueres, foi colocada uma dessas amostras, ficando cada béquer com um metal
diferente. Depois de algum tempo, não se observando mais nenhuma transformação nos
béqueres, foram feitas as leituras de massa nas balanças, obtendo-se os seguintes resultados
finais:
balança A: 327,92 g
balança B: 327,61 g
balança C: 327,10 g
As massas lidas nas balanças permitem concluir que os metais magnésio, ouro e zinco
foram colocados, respectivamente, nos béqueres das balanças.
Dados: massa molar em g·mol-1
Mg .......... 24,3
Au ......... 197,0
Zn .......... 65,4
Aula 02 – Cálculos das reações químicas 57
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
a) A, B e C
b) A, C e B
c) B, A e C
d) B, C e A
e) C, A e B
19. (FUVEST SP/2007)
Alguns problemas de saúde, como bócio endêmico e retardo mental, são causados pela
ingestão de quantidades insuficientes de iodo. Uma maneira simples de suprir o organismo
desse elemento químico é consumir o sal de cozinha que contenha de 20 a 60 mg de iodo por
quilograma do produto. No entanto, em algumas regiões do País, o problema persiste, pois o sal
utilizado ou não foi produzido para consumo humano, ou não apresenta a quantidade mínima
de iodo recomendada. A fonte de iodo utilizada na indústria do sal é o iodato de potássio, KIO 3,
cujo custo é de R$ 20,00/kg.
Considerando que o iodo representa aproximadamente 60 % da massa de KIO 3 e que 1
kg do sal de cozinha é comercializado ao preço médio de R$ 1,00, a presença da quantidade
máxima de iodo permitida por lei (60 miligramas de iodo por quilograma de sal) representa, no
preço, a porcentagem de
a) 0,10 %
b) 0,20 %
c) 1,20 %
d) 2,0 %
e) 12 %
20. (FUVEST SP/2000)
Recentemente, na Bélgica, descobriu-se que frangos estavam contaminados com uma
dioxina contendo 44%, em massa, do elemento cloro. Esses frangos apresentavam, por kg,
2,0·10-13 mol desse composto, altamente tóxico.
Supondo que um adulto possa ingerir, por dia, sem perigo, no máximo 3,23·10-11 g desse
composto, a massa máxima diária, em kg de frango contaminado, que tal pessoa poderia
consumir seria igual a:
Dados:
1 mol da dioxina contém 4 mols de átomos de cloro.
massa molar do cloro (Cℓ) = 35,5 g/mol
a) 0,2
b) 0,5
c) 1
d) 2
Aula 02 – Cálculos das reações químicas 58
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
e) 3
21. (FUVEST SP/1998)
A dose diária recomendada do elemento cálcio para um adulto é de 800 mg. Suponha
certo suplemento nutricional à base de casca de ostras que seja 100% CaCO3. Se um adulto
tomar diariamente dois tabletes desse suplemento de 500mg cada, qual porcentagem de cálcio
da quantidade recomendada essa pessoa está ingerindo?
massas molares (g/mol)
Ca ........................... 40
O ............................. 16
C ............................. 12
a) 25%
b) 40%
c) 50%
d) 80%
e) 125%
11. Já Caiu Nos Principais Vestibulares
Leis Ponderais
22. (UEA AM/2017)
Até a época dos trabalhos de Lavoisier, considerado o grande responsável pelo
nascimento da Química Moderna, acreditava-se que a água era uma substância simples.
Essa ideia foi invalidada quando ele demonstrou que a água líquida poderia ser
a) vaporizada, misturando-se com o ar em diferentes proporções.
b) obtida, como um único produto, pela reação entre hidrogênio e oxigênio.
c) misturada com o álcool em diferentes proporções.
d) transformada em gelo por abaixamento de temperatura.
e) obtida, como único produto, da liquefação do vapor de água.
23. (UEPB/2011)
Aula 02 – Cálculos das reações químicas 59
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
Um professor realizou um experimento em um laboratório no qual ele realizou a queima
de papel amassado e de esponja de aço, respectivamente, em balanças artesanais, conforme
figura 1.
Figura 1: balanças contendo papel amassado e esponja de aço, respectivamente, antes da
queima desses materiais.
Nos pratos da esquerda de cada balança são adicionados pesos de modo que os pratos
ficam em equilíbrio (mesmo peso) antes da queima. Considere que as balanças estão expostas
às condições ambiente e que nenhum produto sólido escapa dos pratos após a queima. Assuma
ainda que o papel seja um polímero cuja unidade polimérica é um monômero de fórmula
mínima (C6H10O5)n e que a esponja de aço utilizada é constituída unicamente de átomos de
Ferro.
Assinale a alternativa que apresenta o comportamento qualitativo mais provável da
balança após a queima de cada material:
a)
b)
c)
d)
Aula 02 – Cálculos das reações químicas 60
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
e) Nenhuma das alternativas, pois a esponja de aço não queima.
24. (PUC SP/2011)
Um determinado metal queima ao ar para formar o respectivo óxido, um sólido de alta
temperatura de fusão. A relação entre a massa do metal oxidado e a massa de óxido formado
está representada no gráfico a seguir.
Durante um experimento, realizado em recipiente fechado, foi colocado para reagir 1,00
g do referido metal, obtendo-se 1,40 g do seu óxido. Considerando-se que todo o oxigênio
presente no frasco foi consumido, pode-se determinar que a massa de oxigênio presente no
sistema inicial é x. Em outro recipiente fechado, foram colocados 1,50 g do referido metal em
contato com 1,20 g de oxigênio. Considerando que a reação ocorreu até o consumo total de pelo
menos um dos reagentes, pode-se afirmar que a massa de óxido gerado é y.
Sabendo que o metal em questão forma apenas um cátion estável e considerando que em
todas as reações o rendimento foi de 100 %, os valores de x e y são, respectivamente,
a) 0,40 g e 2,70 g.
b) 0,40 g e 2,50 g.
c) 0,56 g e 2,50 g.
d) 0,56 g e 3,00 g.
e) 0,67 g e 2,70 g.
25. (PUC Camp SP/2011)
Aula 02 – Cálculos das reações químicas 61
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
Em três experimentos sobre a combustão do carvão, C (s), foram obtidos os seguintes
resultados:
Os experimentos que seguem a lei de Lavoisier são:
a) I e II, somente.
b) I, II e III, somente.
c) II, III e IV, somente.
d) III e IV, somente.
e) I, II, III e IV.
26. (UFF RJ/2009)
Desde a Antiguidade, diversos povos obtiveram metais, vidro, tecidos, bebidas alcoólicas,
sabões, perfumes, ligas metálicas, descobriram elementos e sintetizaram substâncias que
passaram a ser usadas como medicamentos. No século XVIII, a Química, a exemplo da Física,
torna-se uma ciência exata. Lavoisier iniciou na Química o método científico, estudando os
porquês e as causas dos fenômenos. Assim, descobriu que as transformações químicas e físicas
ocorrem com a conservação da matéria. Outras leis químicas também foram propostas e, dentre
elas, as ponderais, ainda válidas.
Com base nas leis ponderais, pode-se afirmar que, segundo:
I. a Lei da Conservação da Massa (Lavoisier), 1,0 g de Ferro ao ser oxidado pelo
Oxigênio, produz 1,0 g de Óxido Férrico;
II. a Lei da Conservação da Massa, ao se usar 16,0 g de Oxigênio molecular para reagir
completamente com 40,0 g de Cálcio, são produzidas 56 g de Óxido de Cálcio;
III. a Lei das Proporções Definidas, se 1,0 g de Ferro reage com 0,29 g de Oxigênio para
formar o composto Óxido Ferroso, 2,0 g de Ferro reagirão com 0,87 g de Oxigênio, produzindo
o mesmo composto;
IV. a Lei das Proporções Múltiplas, dois mols de Ferro reagem com dois mols de
Oxigênio para formar Óxido Ferroso; logo, dois mols de Ferro reagirão com três mols de
Oxigênio para formar Óxido Férrico.
Assinale a opção correta.
a) As afirmativas I e II estão corretas.
b) A afirmativa II está correta.
c) As afirmativas II e III estão corretas.
d) As afirmativas II e IV estão corretas.
Aula 02 – Cálculos das reações químicas 62
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
e) A afirmativa III está correta.
Teoria Atômico Molecular e Volume Molar
27. (IME RJ/2016)
Em 33,65 g de um sal de magnésio está presente 1 mol deste elemento. Sendo trivalente
o ânion deste sal, é correto afirmar que a massa de 1 mol do ânion é
(Massa molar: Mg = 24,31 g/mol)
a) 6,23 g
b) 14,01 g
c) 24,31 g
d) 42,03 g
e) 48,62 g
28. (PUC Camp SP/2016)
O bronze campanil, ou bronze de que os sinos são feitos, é uma liga composta de 78% de
cobre e 22% de estanho, em massa.
Assim, a proporção em mol entre esses metais, nessa liga, é, respectivamente, de 1,0 para
Dados:
Massas molares (g/mol)
Cu = 63,5
Sn = 118,7
a) 0,15.
b) 0,26.
c) 0,48.
d) 0,57.
e) 0,79.
29. (UNESP SP/2016)
Considere amostras de 1 g de cada uma das seguintes substâncias: eteno (C 2H4),
monóxido de carbono (CO) e nitrogênio (N2). Essas três amostras
a) apresentam a mesma quantidade, em mol, de moléculas.
b) apresentam a mesma quantidade, em mol, de átomos.
c) apresentam ligações covalentes polares.
Aula 02 – Cálculos das reações químicas 63
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
d) são de substâncias isômeras.
e) são de substâncias simples.
30. (UNICAMP SP/2013)
Entre os vários íons presentes em 200 mililitros de água de coco há aproximadamente
320 mg de potássio, 40 mg de cálcio e 40 mg de sódio. Assim, ao beber água de coco, uma pessoa
ingere quantidades diferentes desses íons, que, em termos de massa, obedecem à sequência:
potássio>sódio=cálcio. No entanto, se as quantidades ingeridas fossem expressas em mol, a
sequência seria:
a) potássio>cálcio=sódio.
b) cálcio=sódio>potássio.
c) potássio>sódio>cálcio.
d) cálcio>potássio>sódio.
Dados de massas molares em g/mol: cálcio = 40, potássio = 39 e sódio = 23.
Fórmulas Químicas
31. (UNICAMP SP/2016)
Podemos obter energia no organismo pela oxidação de diferentes fontes. Entre essas
fontes destacam-se a gordura e o açúcar. A gordura pode ser representada por uma fórmula
mínima (CH2)n enquanto um açúcar pode ser representado por (CH2O)n. Considerando essas
duas fontes de energia, podemos afirmar corretamente que, na oxidação total de 1 grama de
ambas as fontes em nosso organismo, os produtos formados são
a) os mesmos, mas as quantidades de energia são diferentes.
b) diferentes, mas as quantidades de energia são iguais.
c) os mesmos, assim como as quantidades de energia.
d) diferentes, assim como as quantidades de energia.
32. (FGV SP/2016)
Um certo polímero é produzido a partir de um monômero, que é um hidrocarboneto que
contém somente uma instauração. A análise elementar por combustão completa de 0,5 mol de
moléculas desse hidrocarboneto resultou em 1,5 mol de moléculas de CO 2.
A massa molar, em g·mol–1, desse monômero é
a) 28.
b) 42.
c) 44.
Aula 02 – Cálculos das reações químicas 64
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
d) 56.
e) 58.
33. (Unioeste PR/2015)
Uma molécula cuja massa molar é 74 g/mol possui a seguinte composição centesimal:
C 64,9%, H 13,5% e O 21,6%.
Das fórmulas moleculares mostradas abaixo, aquela que se enquadra nesta análise é:
a) C4H10O.
b) C3H6O2.
c) C5H2O.
d) C4H8O2.
e) C2H2O3.
34. (PUC Camp SP/2014)
Nos processos de fermentação, pode-se usar o fermento biológico, formado por lêvedos,
ou o fermento químico, cujo componente principal é o bicarbonato de sódio, NaHCO 3. Nessa
substância, a porcentagem, em massa, do elemento hidrogênio é igual a
Dados:
Massas molares (g/mol)
H = 1,0 C = 12,0
O = 16,0 Na = 23,0
a) 1,2%.
b) 3,4%.
c) 7,4%.
d) 10%.
e) 12%.
35. (FMJ SP/2012)
Dioxinas são substâncias altamente tóxicas formadas como subprodutos em diversos
processos industriais. Quando um mol de uma determinada dioxina, constituída apenas por
carbono, oxigênio e hidrogênio, é queimado com excesso de oxigênio, formam-se 2 mol de água
e 4 mol de CO2. Nessa dioxina, a massa de oxigênio corresponde a oito vezes a massa de
hidrogênio na molécula. Sua fórmula mínima é
a) CHO.
b) CHO2.
Aula 02 – Cálculos das reações químicas 65
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
c) CHO4.
d) C2HO.
e) C2H2O.
Cálculo Estequiométrico
36. (UNESP SP/2018)
Bicarbonato de sódio sólido aquecido se decompõe, produzindo carbonato de sódio
sólido, além de água e dióxido de carbono gasosos. O gráfico mostra os resultados de um
experimento em que foram determinadas as massas de carbonato de sódio obtidas pela
decomposição de diferentes massas de bicarbonato de sódio.
Os dados do gráfico permitem concluir que as massas de carbonato de sódio e
bicarbonato de sódio nessa reação estão relacionadas pela equação 𝑚𝑁𝑎2𝐶𝑂3 = 𝑘 · 𝑚𝑁𝑎𝐻𝐶𝑂3 , e
que o valor aproximado de k é
a) 0,3.
b) 1,0.
c) 0,2.
d) 0,7.
e) 1,2.
37. (UNESP SP/2016)
A luz branca é composta por ondas eletromagnéticas de todas as frequências do espectro
visível. O espectro de radiação emitido por um elemento, quando submetido a um arco elétrico
Aula 02 – Cálculos das reações químicas 66
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
ou a altas temperaturas, é descontínuo e apresenta uma de suas linhas com maior intensidade,
o que fornece “uma impressão digital” desse elemento. Quando essas linhas estão situadas na
região da radiação visível, é possível identificar diferentes elementos químicos por meio dos
chamados testes de chama. A tabela apresenta as cores características emitidas por alguns
elementos no teste de chama:
Uma estudante preparou 10,0 mL de uma solução 1,00 mol· L–1 de cloreto de um dos
metais apresentados na tabela do texto a fim de realizar um teste de chama em laboratório. No
teste de chama houve liberação de luz vermelha intensa. A partir das informações contidas no
texto e utilizando a classificação periódica dos elementos, assinale a alternativa que apresenta
a massa do sal utilizado pela estudante, em gramas, e a sua fórmula.
a) 1,11 e CaCl2.
b) 7,56 e CaCl.
c) 11,1 e CaCl2.
d) 0,756 e CaCl.
e) 0,111 e CaCl2.
38. (UERJ/2015)
A proporção de moléculas de água presentes na forma hidratada de um sal pode ser
representada da seguinte forma, na qual X corresponde ao número de mols de água por mol
desse sal:
CuSO4· x H2O
Uma amostra de 4,99 g desse sal hidratado foi aquecida até que toda a água nela contida
evaporou, obtendo-se uma massa de 3,19 g de sulfato de cobre II.
O número de mols de água por mol de sulfato de cobre II na composição do sal hidratado
equivale a:
a) 2
b) 5
c) 10
d) 20
39. (UERJ/2018)
A hemoglobina é uma proteína de elevada massa molar, responsável pelo transporte de
oxigênio na corrente sanguínea. Esse transporte pode ser representado pela equação química
abaixo, em que HB corresponde à hemoglobina.
Aula 02 – Cálculos das reações químicas 67
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
HB + 4 O2 → HB(O2)4
Em um experimento, constatou-se que 1 g de hemoglobina é capaz de transportar
2,24·10–4 L de oxigênio molecular com comportamento ideal, nas CNTP.
A massa molar, em g/mol, da hemoglobina utilizada no experimento é igual a:
a) 1·105
b) 2·105
c) 3·105
d) 4·105
40. (FAMERP SP/2018)
Um isqueiro descartável contém gás isobutano (C4H10). Mesmo após o uso total desse
isqueiro, resta um resíduo do gás em seu interior. Considerando que o volume desse resíduo
seja igual a 1 mL e que o volume molar de gás nas condições de pressão e temperatura no
interior do isqueiro seja 25 L/mol, a massa de isobutano restante no isqueiro é,
aproximadamente,
a) 3 mg.
b) 4 mg.
c) 1 mg.
d) 2 mg.
e) 5 mg.
Aspectos Reais do Cálculo Estequiométrico
41. (Fac. Israelita de C. da Saúde Albert Einstein SP/2018)
A pirita (FeS2) é encontrada na natureza agregada a pequenas quantidades de níquel,
cobalto, ouro e cobre. Os cristais de pirita são semelhantes ao ouro e, por isso, são chamados de
ouro dos tolos. Esse minério é utilizado industrialmente para a produção de ácido sulfúrico. Essa
produção ocorre em várias etapas, sendo que a primeira é a formação do dióxido de enxofre,
segundo a equação a seguir.
4 FeS2(s) + 11 O2(g) → 2 Fe2O3 (s) + 8 SO2 (g)
Na segunda etapa, o dióxido de enxofre reage com oxigênio para formar trióxido de
enxofre e, por fim, o trióxido de enxofre reage com água, dando origem ao ácido sulfúrico.
Sabendo que o minério de pirita apresenta 92% de pureza, calcule a massa aproximada
de dióxido de enxofre produzida a partir de 200 g de pirita.
a) 213,7 g.
b) 196,5 g.
c) 512,8 g.
d) 17,1 g.
Aula 02 – Cálculos das reações químicas 68
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
42. (Fac. Israelita de C. da Saúde Albert Einstein SP/2017)
Um resíduo industrial é constituído por uma mistura de carbonato de cálcio (CaCO 3) e
sulfato de cálcio (CaSO4). O carbonato de cálcio sofre decomposição térmica se aquecido entre
825 e 900 °C, já o sulfato de cálcio é termicamente estável. A termólise do CaCO 3 resulta em
óxido de cálcio e gás carbônico.
CaCO3 (s) → CaO(s) + CO2(g)
Uma amostra de 10,00 g desse resíduo foi aquecida a 900 °C até não se observar mais
alteração em sua massa. Após o resfriamento da amostra, o sólido resultante apresentava 6,70
g.
O teor de carbonato de cálcio na amostra é de, aproximadamente,
a) 33%.
b) 50%.
c) 67%.
d) 75%.
43. (PUC Camp SP/2017)
Muitos resíduos industriais podem ser utilizados novamente no processo produtivo. Por
exemplo, resíduos de mármore possuem um potencial de uso nos processos de fabricação de
aços, devido à sua composição química, como mostra os resultados da análise desse material
(Disponível em: http://www.scielo.br)
Nesses processos, o CaCO3 calcinado produz o CaO, usado para a dessulfuração do ferro
gusa.
A massa, em kg, de CaO produzida quando se utiliza 1,0 kg de resíduos de mármore é de,
aproximadamente,
Dados:
Massas molares
C = 12
O = 16
Ca = 40
a) 0,2.
b) 0,4.
c) 0,1.
d) 0,3.
e) 0,5.
Aula 02 – Cálculos das reações químicas 69
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
44. (ESCS DF/2015)
Em 2013, o comércio internacional de minério de ferro foi de 1,23 bilhão de toneladas,
dado que ilustra claramente o fenômeno da globalização. Nesse cenário, o Brasil ocupa posição
de destaque porque possui a segunda maior reserva do planeta, em termos de ferro contido no
minério. Os dois principais minérios encontrados no Brasil são a hematita (Fe2O3) e a magnetita
(Fe3O4). O ferro também é comumente encontrado na siderita (FeCO3).
Se, em determinado ano, o Brasil exportou 300 milhões de toneladas de minério de ferro,
sendo 60% de hematita e 40% de magnetita, então a massa de ferro, em milhões de toneladas,
contida no minério de ferro exportado foi
a) superior a 215.
b) inferior a 205.
c) superior 205 e inferior a 210.
d) superior a 210 e inferior a 215.
45. (Mackenzie SP/2018)
A partir de um minério denominado galena, rico em sulfeto de chumbo II (PbS), pode-se
obter o metal chumbo em escala industrial, por meio das reações representadas pelas equações
de oxirredução a seguir, cujos coeficientes estequiométricos encontram-se já ajustados:
3
PbS(s) + O2 (g) → PbO(s) + SO2 (g)
2
PbO(s) + CO(g) → Pb(s) + CO2 (g)
Considerando-se uma amostra de 717 kg desse minério que possua 90 % de sulfeto de
chumbo II, sendo submetida a um processo que apresente 80 % de rendimento global, a massa
a ser obtida de chumbo será de, aproximadamente,
Dados: massas molares (g·mol–1) S = 32 e Pb = 207
a) 621 kg.
b) 559 kg.
c) 447 kg.
d) 425 kg.
e) 382 kg.
46. (Mackenzie SP/2015)
Vazamento de gás provocou chuva ácida em Cubatão, diz Cetesb
A Companhia Ambiental do Estado de São Paulo (Cetesb) identificou emissão de dióxido
de enxofre (SO2) na atmosfera em Cubatão, após vazamento de uma fábrica de fertilizantes no
Polo Industrial. Segundo o órgão, com isso e com a umidade existente, devido às fortes chuvas,
Aula 02 – Cálculos das reações químicas 70
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
além de outros compostos na atmosfera, é possível uma formação de vapor d’agua e gotículas
de ácido sulfúrico ou sulfuroso, conhecida popularmente como chuva ácida.
Em nota, a Cetesb informa que tal situação só aconteceu no período em que houve
corrente dos gases na atmosfera.
http://www.atribuna.com.br/cidades/cubat%C3%A3o/
vazamento-de-g%C3%A1sprovocou-chuva-%C3%A1cida-em-cubat%
C3%A3o-diz-cetesb-1.426246
Supondo-se que o volume de dióxido de enxofre, descarregado na atmosfera, tenha sido
de 1120 L, nas CNTP, a massa de ácido sulfuroso que foi produzida, por meio da reação
representada pela equação SO2 + H2O → H2SO3, considerando o rendimento do processo igual a
60%, é
Dado: massa molar (g·mol–1) H = 1, O = 16 e S = 32.
a) 1230 g.
b) 2460 g.
c) 4100 g.
d) 5000 g.
e) 8200 g.
47. (UNICAMP SP/2018)
A calda bordalesa é uma das formulações mais antigas e mais eficazes que se conhece. Ela
foi descoberta na França no final do século XIX, quase por acaso, por um agricultor que aplicava
água de cal nos cachos de uva para evitar que fossem roubados; a cal promovia uma mudança
na aparência e no sabor das uvas. O agricultor logo percebeu que as plantas assim tratadas
estavam livres de antracnose. Estudando-se o caso, descobriu-se que o efeito estava associado
ao fato de a água de cal ter sido preparada em tachos de cobre. Atualmente, para preparar a
calda bordalesa, coloca-se o sulfato de cobre em um pano de algodão que é mergulhado em um
vasilhame plástico com água morna. Paralelamente, coloca-se cal em um balde e adiciona-se
água aos poucos. Após quatro horas, adiciona-se aos poucos, e mexendo sempre, a solução de
sulfato de cobre à água de cal.
(Adaptado de Gervásio Paulus, André Muller e Luiz Barcellos, Agroecologia aplicada:
práticas e métodos para uma agricultura de base ecológica.
Porto Alegre: EMATER-RS, 2000, p. 86.)
Na preparação da calda bordalesa são usados 100 g de sulfato de cobre (II) pentaidratado
e 100 g de hidróxido de cálcio (cal extinta). Para uma reação estequiométrica entre os íons cobre
e hidroxila, há um excesso de aproximadamente
a) 1,9 mol de hidroxila.
b) 2,3 mol de hidroxila.
c) 2,5 mol de cobre.
d) 3,4 mol de cobre.
Dados de massas molares em g.mol–1: sulfato de cobre (II) pentaidratado = 250; hidróxido
de cálcio = 74.
Aula 02 – Cálculos das reações químicas 71
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
12. Gabarito Sem Comentários
1. C 17. D 33. A
2. E 18. E 34. A
3. D 19. B 35. E
4. B 20. B 36. D
5. C 21. C 37. A
6. C 22. B 38. B
7. D 23. D 39. D
8. E 24. C 40. D
9. C 25. E 41. B
10. D 26. D 42. D
11. D 27. B 43. D
12. D 28. A 44. D
13. C 29. A 45. C
14. B 30. C 46. B
15. C 31. A 47. A
16. C 32. B
13. Resoluções Das Questões Fundamentais
I. Questão fundamental 01
A partir da reação abaixo, complete o quadro a seguir.
Carbono + Oxigênio → Gás carbônico OBSERVAÇÃO
12 g 32 g 44 g
6g 16 g 22 g
2,4 g 6,4 g 8,8 g
4g 8g 11 g Restou 1 g de carbono ao final da reação
X = 12 + 32 = 44 g
Como 12 ÷ 2 = 6, Y = 32 ÷ 2 = 16 g.
Z = 44 ÷ 2 = 22 g.
Como 32 ÷ 5 = 6,4 g, W = 12 ÷ 5 = 2,4 g.
Aula 02 – Cálculos das reações químicas 72
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
T = 2,4 + 6,4 = 8,8 g
1 g de carbono é excesso, reagiram 3 g. Como a massa consumida de carbono é 6 ÷ 2 = 3 g, Q =
16 ÷ 2 = 8 g.
R = 3 g + 8 g = 11 g.
II. Questão fundamental 02
Balanceie as equações químicas seguintes.
a) C2H6O + 3 O2 → 2 CO2 + 3 H2O
b) Na2CO3 + 2 HC → 2 NaC + H2O + CO2
c) C6H12O6 → 2 C2H6O + 2 CO2
d) C4H10 + 13/2 O2 → 4 CO2 + 5 H2O
e) 2 FeC3 + 3 Na2CO3 → Fe2(CO3)3 + 6 NaC
f) 2 NH4C + Ba(OH)2 → BaC2 + 2 NH3 + 2 H2O
g) 3 Ca(OH)2 + 2 H3PO4 → Ca3(PO4)2 + 6 H2O
h) Fe2(CO3)3 + 3 H2SO4 → Fe2(SO4)3 + 3 H2O + 3 CO2
i) Na2O + (NH4)2SO4 → Na2SO4 + H2O + 2 NH3
j) 2 NaN3 → 2 Na + 3 N2
k) Fe2O3 + 3 C → 2 Fe + 3 CO
l) 4 FeS2 + 11 O2 → 2 Fe2O3 + 8 SO2
m) 4 NH3 + 5 O2 → 4 NO + 6 H2O
n) 2 KMnO4 + H2SO4 → Mn2O7 + K2SO4 + H2O
o) CS2 + 3 O2 → CO2 + 2 SO2
p) 2 H3PO4 + 3 CaO → Ca3(PO4)2 + 3 H2O
IV. Questão fundamental 03- cálculos sem excesso, 100% de rendimento e 100% de pureza.
a) A partir da equação abaixo, calcule a massa, em gramas, de CO 2 obtida pelo consumo de 4,6
gramas de etanol.
C2H6O + 3 O2 → 2 CO2 + 3 H2O
46 𝑔 𝑑𝑒 𝐶2 𝐻6 𝑂 − − − − 2 · 44 𝑔 𝑑𝑒 𝐶𝑂2
4,6 𝑔 𝑑𝑒 𝐶2 𝐻6 𝑂 − − − − 𝑥 𝑔 𝑑𝑒 𝐶𝑂2
x = 8,8 g de C2H6O
Aula 02 – Cálculos das reações químicas 73
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
b) A partir da equação abaixo, calcule a quantidade de matéria, em mol, de NaCl obtida pelo
consumo de 5 mol de carbonato de sódio.
Na2CO3 + 2 HCl → 2 NaCl + H2O + CO2
1 𝑚𝑜𝑙 𝑑𝑒 𝑁𝑎2 𝐶𝑂3 − − − − 2 𝑚𝑜𝑙 𝑑𝑒 𝑁𝑎𝐶𝑙
5 𝑚𝑜𝑙 𝑑𝑒 𝑁𝑎2 𝐶𝑂3 − − − − 𝑥 𝑚𝑜𝑙 𝑑𝑒 𝑁𝑎𝐶𝑙
x =10 mol de NaCl
c) A partir da equação abaixo, calcule o número de moléculas de C 6H12O6 necessários para obter
2,2 gramas de dióxido de carbono.
C6H12O6 → 2 C2H6O + 2CO2
1 · 6 · 1023 𝑚𝑜𝑙é𝑐𝑢𝑙𝑎𝑠 𝑑𝑒 𝐶6 𝐻12 𝑂6 − − − − 2 · 44𝑔 𝐶𝑂2
𝑥 𝑚𝑜𝑙é𝑐𝑢𝑙𝑎𝑠 𝑑𝑒 𝐶6 𝐻12 𝑂6 − − − − 2,2 𝑔 𝐶𝑂2
23
x = 0,15 · 10 𝑚𝑜𝑙é𝑐𝑢𝑙𝑎𝑠 𝑑𝑒 𝐶6 𝐻12 𝑂6
d) A partir da equação abaixo, calcule a massa, em gramas, de gás oxigênio necessária para
consumir 2 mols de butano.
13
C4H10 + O2 → 4 CO2 + 5 H2O
2
13
1 𝑚𝑜𝑙 𝑑𝑒 𝐶4 𝐻10 −−−− · 32𝑔 𝑑𝑒 𝑂2
2
2 𝑚𝑜𝑙 𝑑𝑒 𝐶4 𝐻10 − − − − 𝑥 𝑔 𝑑𝑒 𝑂2
x = 416 𝑔 𝑑𝑒 𝑂2
e) A partir da equação abaixo, calcule a quantidade de matéria, em mol, de carbonato férrico
obtida ao se obter 175,5 gramas de cloreto de sódio.
2 FeCl3 + 3 Na2CO3 → Fe2(CO3)3 + 6 NaCl
1 𝑚𝑜𝑙 𝑑𝑒 𝐹𝑒2 (𝐶𝑂3 )3 − − − − 6 · 58,5 𝑔 𝑑𝑒 𝑁𝑎𝐶𝑙
𝑥 𝑚𝑜𝑙 𝑑𝑒 𝐹𝑒2 (𝐶𝑂3 )3 − − − − 175,5 𝑔 𝑑𝑒 𝑁𝑎𝐶𝑙
x = 0,5 𝑔 𝑑𝑒 𝑁𝑎𝐶𝑙
Reagentes em excesso
f) A partir da equação abaixo, calcule a quantidade de matéria, em mol, de cloreto de bário
produzido a partir da reação de 10 mols de cloreto de amônio e 7 mols de hidróxido de bário.
2 NH4Cl + Ba(OH)2 → BaCl2 + 2 NH3 + 2 H2O
Identificação do reagente limitante e do reagente em excesso:
2 𝑚𝑜𝑙 𝑑𝑒 𝑁𝐻4 𝐶𝑙 − − − − 1 𝑚𝑜𝑙 𝑑𝑒 𝐵𝑎(𝑂𝐻 )2
10 𝑚𝑜𝑙 𝑑𝑒 𝑁𝐻4 𝐶𝑙 − − − − 𝑥 𝑚𝑜𝑙 𝑑𝑒 𝐵𝑎(𝑂𝐻 )2
x = 5 𝑚𝑜𝑙 𝐵𝑎(𝑂𝐻 )2
Logo, o NH4Cl é o reagente limitante.
Aula 02 – Cálculos das reações químicas 74
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
2 𝑚𝑜𝑙 𝑑𝑒 𝑁𝐻4 𝐶𝑙 − − − − 1 𝑚𝑜𝑙 𝑑𝑒 𝐵𝑎𝐶𝑙2
10 𝑚𝑜𝑙 𝑑𝑒 𝑁𝐻4 𝐶𝑙 − − − − 𝑦 𝑚𝑜𝑙 𝑑𝑒 𝐵𝑎𝐶𝑙2
𝑦 = 5 mol de BaCl2
g) A partir da equação abaixo, calcule a massa, em gramas, de fosfato de cálcio produzida a
partir da reação de 74 g de hidróxido de cálcio e 98 gramas de ácido fosfórico.
3 Ca(OH)2 + 2 H3PO4 → Ca3(PO4)2 + 6 H2O
Identificação do reagente limitante e do reagente em excesso:
3 · 74 𝑔 𝑑𝑒 𝐶𝑎(𝑂𝐻 )2 − − − − 2 · 98 𝑔 𝑑𝑒 𝐻3 𝑃𝑂4
74 𝑔 𝑑𝑒 𝐶𝑎 (𝑂𝐻 )2 −−−− 𝑥 𝑔 𝑑𝑒 𝐻3 𝑃𝑂4
x = 65,3 𝑔 𝑑𝑒 𝐻3 𝑃𝑂4
Logo, o Ca(OH)2 é o reagente limitante.
3 · 74 𝑔 𝑑𝑒 𝐶𝑎(𝑂𝐻 )2 − − − − 310 𝑔 𝑑𝑒 𝐶𝑎3 (𝑃𝑂4 )2
74 𝑔 𝑑𝑒 𝐶𝑎(𝑂𝐻 )2 −−−− 𝑥 𝑔 𝑑𝑒 𝐶𝑎3 (𝑃𝑂4 )2
x = 103,3 𝑔 𝑑𝑒 𝐶𝑎3 (𝑃𝑂4 )2
h) A partir da equação abaixo, calcule o número de moléculas de dióxido de carbono produzido
a partir da reação de 10 mols de carbonato férrico e 98 gramas de ácido sulfúrico.
Fe2(CO3)3 + 3 H2SO4 → Fe2(SO4)3 + 3 H2O + 3 CO2
Identificação do reagente limitante e do reagente em excesso:
1 𝑚𝑜𝑙 𝑑𝑒 𝐹𝑒2 (𝐶𝑂3 )3 − − − − 3 · 98 𝑔 𝑑𝑒 𝐻2 𝑆𝑂4
10 𝑚𝑜𝑙 𝑑𝑒 𝐹𝑒2 (𝐶𝑂3 )3 − − − − 𝑥 𝑔 𝑑𝑒 𝐻2 𝑆𝑂4
x = 2940 𝑔 𝑑𝑒 𝐻2 𝑆𝑂4
Logo, o H2SO4 é o reagente limitante.
3 · 98 𝑔 𝑑𝑒 𝐻2 𝑆𝑂4 − − − − 3 · 6 · 1023 𝑚𝑜𝑙é𝑐𝑢𝑙𝑎𝑠 𝑑𝑒 𝐶𝑂2
98 𝑔 𝑑𝑒 𝐻2 𝑆𝑂4 −−−− 𝑥 𝑚𝑜𝑙é𝑐𝑢𝑙𝑎𝑠 𝑑𝑒 𝐶𝑂2
23
x = 6 · 10 𝑚𝑜𝑙é𝑐𝑢𝑙𝑎𝑠 𝑑𝑒 𝐶𝑂2
i) A partir da equação abaixo, calcule a massa, em gramas, de amônia produzida a partir da
reação de 124 gramas de óxido de sódio e 3 mols de sulfato de amônio.
Na2O + (NH4)2SO4 → Na2SO4 + H2O + 2 NH3
Identificação do reagente limitante e do reagente em excesso:
62 𝑔 𝑑𝑒 𝑁𝑎2 𝑂 − − − − 1 𝑚𝑜𝑙 𝑑𝑒 (𝑁𝐻4 )2 𝑆𝑂4
124 𝑔 𝑑𝑒 𝑁𝑎2 𝑂 − − − − 𝑥 𝑚𝑜𝑙 𝑑𝑒 (𝑁𝐻4 )2 𝑆𝑂4
x = 2 𝑚𝑜𝑙 𝑑𝑒 (𝑁𝐻4 )2 𝑆𝑂4
Logo, o Na2O é o reagente limitante.
Aula 02 – Cálculos das reações químicas 75
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
62 𝑔 𝑑𝑒 𝑁𝑎2 𝑂 − − − − 2 · 17 𝑔 𝑑𝑒 𝑁𝐻3
124 𝑔 𝑑𝑒 𝑁𝑎2 𝑂 − − − − 𝑥 𝑔 𝑑𝑒 𝑁𝐻3
x = 68 𝑔 𝑑𝑒 𝑁𝐻3
Pureza.
j) A partir da equação abaixo, calcule a massa, em gramas, de gás nitrogênio produzida a partir
da reação completa de 78 gramas de uma amostra com 80% de pureza de NaN3.
2 NaN3 → 2 Na + 3 N2
Determinando a parte pura, ou seja, a massa da substância.
80
𝑝𝑎𝑟𝑡𝑒 𝑝𝑢𝑟𝑎 = · 78 𝑔 = 62,4 g de NaN3
100
2 · 65 𝑔 𝑑𝑒 𝑁𝑎𝑁3 − − − − 3 · 28 𝑔 𝑑𝑒 𝑁2
62,4 𝑔 𝑑𝑒 𝑁𝑎𝑁3 − − − − 𝑥 𝑔 𝑑𝑒 𝑁2
x = 40,32 𝑔 𝑑𝑒 𝑁𝐻3
k) A partir da equação abaixo, calcule a massa, em gramas, de carvão (com 60% de pureza de
carbono) necessária para obter 5,6 gramas de ferro metálico.
Fe2O3 + 3 C → 2 Fe + 3 CO
Determine a massa da substância C pura:
3 · 12 𝑔 𝑑𝑒 𝐶 − − − − 2 · 56 𝑔 𝑑𝑒 𝐹𝑒
𝑥 𝑔 𝑑𝑒 𝐶 −−−− 5,6 𝑔 𝑑𝑒 𝐹𝑒
x = 1,8 𝑔 𝑑𝑒 𝐶
A massa determinada corresponde a parte pura, porém a questão solicitou a massa da
mistura.
60 % − − − − 1,8 𝑔 𝑑𝑒 𝐶
100 % − − − − 𝑦 𝑔 𝑑𝑒 𝑐𝑎𝑟𝑣ã𝑜
y = 3 g de carvão
l) A partir da equação abaixo, calcule a massa, em gramas, de ar (com 70% de oxigênio)
necessária para obter 5 mols de dióxido de enxofre.
11
2 FeS2 + O2 → Fe2O3 + 4 SO2
2
Determine a massa da substância O2 pura:
11
· 32 𝑔 𝑑𝑒 𝑂2 − − − − 4 𝑚𝑜𝑙 𝑑𝑒 𝑆𝑂2
2
𝑥 𝑔 𝑑𝑒 𝑂2 − − − − 5 𝑚𝑜𝑙 𝑑𝑒 𝑆𝑂2
x = 220 𝑔 𝑑𝑒 𝑂2
A massa determinada corresponde a parte pura, porém a questão solicitou a massa da
mistura.
70 % − − − − 220 𝑔 𝑑𝑒 𝑂2
100 % − − − − 𝑦 𝑔 𝑑𝑒 𝑎𝑟
y = 314,28 g de ar
Aula 02 – Cálculos das reações químicas 76
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
m) A partir da equação abaixo, calcule a massa, em gramas, de monóxido de nitrogênio
produzida a partir da reação completa de 4,76 gramas de uma amostra, que possui 60% de
pureza de amônia.
5
2 NH3 + O2 → 2 NO + 3 H2O
2
Determinando a parte pura, ou seja, a massa da substância.
60
𝑝𝑎𝑟𝑡𝑒 𝑝𝑢𝑟𝑎 = · 4,76 𝑔 = 2,856 g de NH3
100
2 · 17 𝑔 𝑑𝑒 𝑁𝐻3 − − − − 2 · 30 𝑔 𝑑𝑒 𝑁𝑂
2,856 𝑔 𝑑𝑒 𝑁𝐻3 − − − − 𝑥 𝑔 𝑑𝑒 𝑁𝑂
x = 5,04 𝑔 𝑑𝑒 𝑁𝑂
Rendimento.
n) A partir da equação abaixo, calcule o número de moléculas de água produzido a partir da
reação, com 70% de rendimento, de 0,98 gramas de ácido sulfúrico.
2 KMnO4 + H2SO4 → Mn2O7 + K2SO4 + H2O
Somente 70% dos 0,98 g de ácido sulfúrico foram consumidos na reação, portanto calcula-se
a quantidade que, efetivamente, será consumida na reação:
70
𝑝𝑎𝑟𝑡𝑒 𝑞𝑢𝑒 𝑝𝑎𝑟𝑡𝑖𝑐𝑖𝑝𝑎 𝑑𝑎 𝑟𝑒𝑎çã𝑜 = · 0,98 𝑔 = 0,686 g de H2SO4
100
1 · 98 𝑔 𝑑𝑒 𝐻2 𝑆𝑂4 − − − − 6 · 1023 𝑚𝑜𝑙é𝑐𝑢𝑙𝑎𝑠 𝑑𝑒 á𝑔𝑢𝑎
0,686 𝑔 𝑑𝑒 𝐻2 𝑆𝑂4 − − − − 𝑥 𝑚𝑜𝑙é𝑐𝑢𝑙𝑎𝑠 𝑑𝑒 á𝑔𝑢𝑎
x = 4,2 · 1021 𝑚𝑜𝑙é𝑐𝑢𝑙𝑎𝑠 𝑑𝑒 𝐻2 𝑂
o) A partir da equação abaixo, calcule a quantidade de matéria, em mol, de dióxido de enxofre
produzida a partir da reação, com 80% de rendimento, de 9,6 gramas de gás oxigênio.
CS2 + 3 O2 → CO2 + 2 SO2
Somente 80% dos 9,6 g de gás oxigênio foram consumidos na reação, portanto calcula-se a
quantidade que, efetivamente, será consumida na reação:
80
𝑝𝑎𝑟𝑡𝑒 𝑞𝑢𝑒 𝑝𝑎𝑟𝑡𝑖𝑐𝑖𝑝𝑎 𝑑𝑎 𝑟𝑒𝑎çã𝑜 = · 9,6 𝑔 = 7,68 g de O2
100
3 · 32 𝑔 𝑑𝑒 𝑂2 − − − − 2 𝑚𝑜𝑙 𝑑𝑒 𝑆𝑂2
7,68 𝑔 𝑑𝑒 𝑂2 − − − − 𝑥 𝑚𝑜𝑙 𝑑𝑒 𝑆𝑂2
x = 0,16 𝑚𝑜𝑙 𝑑𝑒 𝑆𝑂2
p) A partir da equação abaixo, calcule o rendimento, em porcentagem, sabendo que o consumo
de 9,8 gramas de ácido fosfórico produziu 0,04 mol de fosfato de cálcio.
2 H3PO4 + 3 CaO → Ca3(PO4)2 + 3 H2O
Calcule a massa, em gramas, de fosfato de cálcio para o consumo de todos os reagentes, ou
seja, rendimento de 100%.
2 · 98 𝑔 𝑑𝑒 𝐻3 𝑃𝑂4 − − − − 1 𝑚𝑜𝑙 𝑑𝑒 𝐶𝑎3 (𝑃𝑂4 )2
9,8 𝑔 𝑑𝑒 𝐻3 𝑃𝑂4 − − − − 𝑥 𝑚𝑜𝑙 𝑑𝑒 𝐶𝑎3 (𝑃𝑂4 )2
Aula 02 – Cálculos das reações químicas 77
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
x = 0,05 mol de Ca3(PO4)2
Calcula-se o rendimento da reação:
100 % 𝑑𝑒 𝑟𝑒𝑛𝑑𝑖𝑚𝑒𝑛𝑡𝑜 − − − − 0,05 𝑚𝑜𝑙 𝑑𝑒 𝐶𝑎3 (𝑃𝑂4 )2
𝑦 % 𝑑𝑒 𝑟𝑒𝑛𝑑𝑖𝑚𝑒𝑛𝑡𝑜 − − − − 0,04 𝑚𝑜𝑙 𝑑𝑒 𝐶𝑎3 (𝑃𝑂4 )2
y = 80 % de rendimento
14. Questões Resolvidas E Comentadas
1. (FUVEST SP/2019)
O cinamaldeído é um dos principais compostos que dão o sabor e o aroma da canela.
Quando exposto ao ar, oxida conforme a equação balanceada:
Uma amostra de 19,80 g desse composto puro foi exposta ao ar por 74 dias e depois
pesada novamente, sendo que a massa final aumentou em 1,20 g. A porcentagem desse
composto que foi oxidada no período foi de
Note e adote:
- Massas molares (g/mol): Cinamaldeído = 132; O2 = 32.
- Considere que não houve perda de cinamaldeído ou do produto de oxidação por
evaporação.
a) 10%
b) 25%
c) 50%
d) 75%
e) 90%
Comentários
A massa que aumentou é exatamente a incorporação dos átomos de oxigênio porque se trata
de uma reação de acréscimo de átomos. Portanto, pode-se dizer que a massa de O2 consumida na
reação foi de 1,20 g.
Proporção:
1 mol de cinamaldeído → ½ mol de O2, adaptando para a relação massa-massa, tem-se:
1
1 · 132 𝑔 𝑑𝑒 𝑐𝑖𝑛𝑎𝑚𝑎𝑙𝑑𝑒í𝑑𝑜 − − − − · 32 𝑔 𝑑𝑒 𝑂2
2
𝑥 𝑔 𝑑𝑒 𝑐𝑖𝑛𝑎𝑚𝑎𝑙𝑑𝑒í𝑑𝑜 − − − − 1,20 𝑔 𝑑𝑒 𝑂2
x = 9,9 g de cinamaldeído
Porcentagem, em massa, do cinamaldeído consumido:
Aula 02 – Cálculos das reações químicas 78
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
9,9 𝑔
%= 𝑥 100% = 50%
19,80 𝑔 =
Gabarito: C
2. (FUVEST SP/2016)
Uma dieta de emagrecimento atribui a cada alimento um certo número de pontos, que
equivale ao valor calórico do alimento ao ser ingerido. Assim, por exemplo, as combinações abaixo
somam, cada uma, 85 pontos:
• 4 colheres de arroz + 2 colheres de azeite + 1 fatia de queijo branco.
• 1 colher de arroz + 1 bife + 2 fatias de queijo branco.
• 4 colheres de arroz + 1 colher de azeite + 2 fatias de queijo branco.
• 4 colheres de arroz + 1 bife.
Com base nas informações fornecidas, e na composição nutricional dos alimentos,
considere as seguintes afirmações:
I. A pontuação de um bife de 100 g é 45.
II. O macronutriente presente em maior quantidade no arroz são os carboidratos.
III. Para uma mesma massa de lipídeo de origem vegetal e de carboidrato, a razão
é 1,5.
É correto o que se afirma em
a) I, apenas.
b) II, apenas.
c) I e II, apenas.
d) II e III, apenas.
e) I, II e III.
Comentários
Aula 02 – Cálculos das reações químicas 79
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
I. Adotaremos os seguintes critérios:
x y z w
1 colher de arroz 1 colher de azeite 1 fatia de queijo branco 1 bife
Portanto, substituindo nas equações, temos:
4x + 2y + 1z = 85 (A)
x + w + 2z = 85 (B)
4x + y + 2z = 85 (C)
4x + w = 85 (D)
Igualando as equações A e B, temos:
4x + 2y + 1z = 4x + y + 2z
y=z
- Substituindo todas as incógnitas de z por y nas equações, temos:
4x + 3y = 85 (E)
x + w + 2y = 85 (F)
4x + 3y = 85 (G)
4x + w = 85 (H).
Observe que as equações E e G são idênticas.
Igualando as equações E e H, temos:
4x + 3y = 4x + w
w = 3y
- Substituindo todas as incógnitas de w por 3y nas equações, temos:
4x + 3y = 85 (I)
x + 5y = 85 (J)
4x + 3y = 85 (K)
Observe que as equações I e K são idênticas.
Igualando as equações I e J, temos:
4x + 3y = x + 5y
2
x= y
3
2
- Substituindo x por y em J, temos:
3
2
y + 3 y = 85
3
17
y = 85
3
y = 15
Assim, substituindo em todas as definições em relação a y, temos:
y = z = 15
w = 3y = 3·15= 45
Aula 02 – Cálculos das reações químicas 80
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
2 2
x = y = · 15 = 10
3 3
x y z w
1 colher de arroz 1 colher de azeite 1 fatia de queijo branco 1 bife
10 pontos 15 pontos 15 pontos 45 pontos
II. Certo. O carboidrato é o macronutriente mais abundante no arroz. O carboidrato corresponde a
25% da fonte de energia do arroz.
III. Certo.
1 colher de azeite – 15 pontos – 5 g
1 colher de arroz – 10 pontos – 20 g
Montando a proporção em relação as massas de lipídeo e carboidrato.
Sabendo que:
Azeite: 5 g - 100% de lipídeo
Arroz: 20 g – 25% de carboidrato.
1 colher de azeite – 15 pontos – 5 g de lipídeo.
1 colher de arroz – 10 pontos – 20·25% = 5 g de carboidrato
15 𝑝𝑜𝑛𝑡𝑜𝑠
A razão entre os pontos é igual a = 1,5.
10 𝑝𝑜𝑛𝑡𝑜𝑠
Gabarito: E
3. (FUVEST SP/2002)
O aspartame, um adoçante artificial, pode ser utilizado para substituir o açúcar de cana.
Bastam 42 miligramas de aspartame para produzir a mesma sensação de doçura que 6,8 gramas
de açúcar de cana. Sendo assim, quantas vezes, aproximadamente, o número de moléculas de
açúcar de cana deve ser maior do que o número de moléculas de aspartame para que se tenha
o mesmo efeito sobre o paladar?
Dados:
massas molares aproximadas (g/mol)
açúcar de cana : 340
adoçante artificial : 300
a) 30
b) 50
c) 100
d) 140
e) 200
Aula 02 – Cálculos das reações químicas 81
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
Comentários
Sabendo que as massas molares, g/mol, do açúcar e do adoçante são 340 e 300,
respectivamente e que 1 mol é igual a 6·1023, calcula-se o número de moléculas dos dois materiais:
340 𝑔 𝑑𝑒 𝑎çú𝑐𝑎𝑟 −−−− 6 · 1023 𝑚𝑜𝑙é𝑐𝑢𝑙𝑎𝑠
Açúcar 6,8 𝑔 𝑑𝑒 𝑎çú𝑐𝑎𝑟 −−−− 𝑥 𝑚𝑜𝑙é𝑐𝑢𝑙𝑎𝑠
x = 0,12·1023 moléculas de açúcar
340 𝑔 𝑑𝑒 𝑎𝑑𝑜ç𝑎𝑛𝑡𝑒 −−−− 6 · 1023 𝑚𝑜𝑙é𝑐𝑢𝑙𝑎𝑠
Adoçante 42 · 10−3 𝑔 𝑑𝑒 𝑎𝑑𝑜ç𝑎𝑛𝑡𝑒 −−−− 𝑥 𝑚𝑜𝑙é𝑐𝑢𝑙𝑎𝑠
x = 0,74·1020 moléculas de adoçante
Determina-se a razão do número de moléculas de açúcar pelo o de adoçante:
0,12·1023
= 162
0,74·1020
Gabarito: D
4. (FUVEST SP/1995)
Linus Pauling, prêmio Nobel de Química e da Paz, faleceu recentemente aos 93 anos. Era
um ferrenho defensor das propriedades terapêuticas da vitamina C. Ingeria diariamente cerca
de 2,1 x 10-2 mol dessa vitamina.
Dose diária recomendada de vitamina C (C6H8O6) .......... 62 mg
Quantas vezes, aproximadamente, a dose ingerida por Pauling é maior que a
recomendada?
a) 10
b) 60
c) 1,0 · 102
d) 1,0 · 103
e) 6,0 · 104
Comentários
Sabendo que a massa molar, em g/mol, da vitamina C é igual a 6·12 + 8·1 + 6·16 = 176, calcula-
se:
176 𝑔 𝑑𝑒 𝑉𝑖𝑡 𝐶 −−−− 1 mol
𝑥 𝑔 𝑑𝑒 𝑉𝑖𝑡 𝐶 − − − − 2,1 · 10−2 𝑚𝑜𝑙
x = 3,696 g de Vit C
Portanto:
3,696 g
= 59,61
0,062 g
Gabarito: B
Aula 02 – Cálculos das reações químicas 82
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
5. (FUVEST SP/2004)
Com a finalidade de determinar a fórmula de certo carbonato de um metal Me, seis
amostras, cada uma de 0,0100 mol desse carbonato, foram tratadas, separadamente, com
volumes diferentes de ácido clorídrico de concentração 0,500 mol/L. Mediu-se o volume de gás
carbônico produzido em cada experiência, à mesma pressão e temperatura.
O volume molar do gás carbônico, nas condições da experiência, é igual a 24,8 L/mol.
Então, a fórmula do carbonato deve ser:
a) Me2CO3
b) MeCO3
c) Me2(CO3)3
d) Me(CO3)2
e) Me2(CO3)5
Comentários
Cada amostra apresentava 0,01 mol do carbonato, a fim de facilitar os cálculos podemos
multiplicar todos os dados por 100 para que possamos calcular as quantidades proporcionais para 1
mol de carbonato. A fórmula geral do carbonato é: Mex(CO3)y.
Reação: Mex(CO3)y + HC → Mez(C)w + H2O + CO2
A partir da liberação de CO2 sabemos a quantidade que apresenta de CO32- na estrutura,
portanto começaremos calculando o número de mols de CO2 liberados pelo consumo total de 1 mol
da amostra.
Analisando os dados da tabela, percebemos que a partir de 120 mL de HCl a quantidade de
gás liberado se mantém constante. A explicação se deve ao fato do que a partir de 120 mL do ácido
clorídrico, toda a massa da amostra foi consumida. Logo 0,01 mol do carbonato reage
completamente com 120 mL de ácido clorídrico e produz 744 mL de CO 2.
Montando a proporção para o consumo de 1 mol de carbonato, temos: 1 mol do carbonato
reage completamente com 12 L de ácido clorídrico e produz 74,4 L de CO 2. Determinaremos o
número de mols de ácido clorídrico e de CO2 envolvidos na equação química:
𝑚𝑜𝑙
nmol de HCl = 12 L · 0,5 = 6 mol
HC 𝐿
O volume molar dos gases nas condições da questão é igual a 24,8
L/mol, portanto:
CO2 74,4 𝐿
nmol de CO2 = 𝑚𝑜𝑙 = 3 mol
24,8
𝐿
Assim, a proporção de reação é:
1 mol Mex(CO3)y : 3 mol CO2
Aula 02 – Cálculos das reações químicas 83
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
A única opção que apresenta a quantidade de 3 carbonatos é a letra C. Infelizmente, a questão
não fornece dados suficientes para calcular a quantidade de íons do metal Me, portanto a resposta
da questão será escolhida pelo número de carbonatos.
Gabarito: C
6. (FUVEST SP/2017)
Em uma aula experimental, dois grupos de alunos (G1 e G2) utilizaram dois
procedimentos diferentes para estudar a velocidade da reação de carbonato de cálcio com
excesso de ácido clorídrico. As condições de temperatura e pressão eram as mesmas nos dois
procedimentos e, em cada um deles, os estudantes empregaram a mesma massa inicial de
carbonato de cálcio e o mesmo volume de solução de ácido clorídrico de mesma concentração.
O grupo G1 acompanhou a transformação ao longo do tempo, realizada em um sistema
aberto, determinando a variação de massa desse sistema (Figura 1 e Tabela).
O grupo G2 acompanhou essa reação ao longo do tempo, porém determinando o volume
de dióxido de carbono recolhido (Figura 2).
Aula 02 – Cálculos das reações químicas 84
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
Comparando os dois experimentos, os volumes aproximados de CO2, em litros, recolhidos
pelo grupo G2 após 60, 180 e 240 segundos devem ter sido, respectivamente,
a) 0,14; 0,20 e 0,25
b) 0,14; 0,34 e 0,60
c) 0,34; 0,48 e 0,60
d) 0,34; 0,48 e 0,88
e) 0,62; 0,88 e 1,10
Note e adote:
massa molar do CO2: 44 g/mol;
volume molar do CO2: 24 L/mol;
desconsidere a solubilidade do CO2 em água.
Comentários
O grupo 1 analisa a reação em relação à massa de um sistema gasoso que libera gás, logo a
massa observada do sistema diminui ao longo da reação devido à liberação do CO 2.
O grupo 2 analisa a reação em um sistema fechado recolhendo o volume de gás carbônico
produzido, logo o volume do gás aumenta no decorrer da reação.
Sabendo que 1 mol de CO2 apresenta 24 litros e 44 gramas, converte-se as massas 0,62, 0,88
e 1,1 gramas em volume:
44 𝑔 𝑑𝑒 𝐶𝑂2 −−−− 24 L
0 a 60 s 0,62 𝑔 𝑑𝑒 𝐶𝑂2 −−−− 𝑥𝐿
x = 0,34 L
44 𝑔 𝑑𝑒 𝐶𝑂2 − − − − 24 L
0 a 180 s 0,88 𝑔 𝑑𝑒 𝐶𝑂2 − − − − 𝑦𝐿
y = 0,48 L
Aula 02 – Cálculos das reações químicas 85
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
44 𝑔 𝑑𝑒 𝐶𝑂2 −−−− 24 L
0 a 240 s 1,10 𝑔 𝑑𝑒 𝐶𝑂2 −−−− 𝑧𝐿
z = 0,6 L
Gabarito: C
7. (FUVEST SP/2017)
Nas mesmas condições de pressão e temperatura, 50 L de gás propano (C 3H8) e 250 L de
ar foram colocados em um reator, ao qual foi fornecida energia apenas suficiente para iniciar a
reação de combustão. Após algum tempo, não mais se observou a liberação de calor, o que
indicou que a reação havia-se encerrado.
Com base nessas observações experimentais, três afirmações foram feitas:
I. Se tivesse ocorrido apenas combustão incompleta, restaria propano no reator.
II. Para que todo o propano reagisse, considerando a combustão completa, seriam
necessários, no mínimo, 750 L de ar.
III. É provável que, nessa combustão, tenha se formado fuligem.
Está correto apenas o que se afirma em
a) I.
b) III.
c) I e II.
d) I e III.
e) II e III.
Note e adote:
Composição aproximada do ar em volume: 80% de N2 e 20%de O2.
Comentários
Existem 3 opções de reação de combustão do propano.
Aula 02 – Cálculos das reações químicas 86
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
Combustão
incompleta completa
C3H8 + 3,5 O2 → 3 CO + 4 C3H8 + 2 O2 → 3 C + 4 H2O C3H8 + 5 O2 → 3 CO2 + 4 H2O
H2O
20
No sistema apresenta 50 L de propano e 50 L de oxigênio (250 L · = 50 L).
100
Ao observar as equações percebe-se que a proporção entre propano e O2 não é 1:1, sendo
necessário mais oxigênio para consumo de todo propano. Portanto, conclui-se que o oxigênio é o
reagente limitante e o propano é o reagente em excesso.
I. Certo. Restaria propano em qualquer situação de combustão.
II. Errado. A proporção em combustão completa é de 1 mol de propano : 5 mols de oxigênio, sabendo
que os dois componentes são gasosos e nas mesmas condições de temperatura e pressão, pode-se
equivaler à 1 L de propano : 5 L de oxigênio. Portanto, a quantidade necessária para consumir 50 L
de propano será 250 L de oxigênio (cinco vezes mais que a quantidade de propano). O oxigênio
corresponde a 20% do volume do ar, logo 100% equivale a 1250 L.
III. Certo. Não existe quantidade suficiente de oxigênio para consumir todo o propano, logo as
combustões incompletas apresentam menor proporção em volume de oxigênio. Assim, há a
probabilidade de ter acontecido as reações de combustão incompleta e liberado fuligem.
Gabarito: D
8. (FUVEST SP/2016)
Um dirigível experimental usa hélio como fluido ascensional e octano (C8H18) como
combustível em seu motor, para propulsão. Suponha que, no motor, ocorra a combustão
completa do octano:
25
C8H18(g) + O2(g) → 8 CO2(g) + 9 H2O(g)
2
Para compensar a perda de massa do dirigível à medida que o combustível é queimado,
parte da água contida nos gases de exaustão do motor é condensada e armazenada como lastro.
O restante do vapor de água e o gás carbônico são liberados para a atmosfera.
Qual é a porcentagem aproximada da massa de vapor de água formado que deve ser
retida para que a massa de combustível queimado seja compensada?
a) 11%
Aula 02 – Cálculos das reações químicas 87
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
b) 16%
c) 39%
d) 50%
e) 70%
Note e adote:
Massa molar (g/mol):
H2O ...... 18
O2 ............. 32
CO2 ....... 44
C8H18 ...... 114
Comentários
A massa de água retida tem que ser igual à massa de octano queimado, ou seja, 114 gramas
de água retida.
162 𝑔 𝑑𝑒 á𝑔𝑢𝑎 − − − − 100 %
114 𝑔 𝑑𝑒 á𝑔𝑢𝑎 − − − − 𝑥%
x = 70,3 %
Gabarito: E
9. (FUVEST SP/2015)
Amônia e gás carbônico podem reagir formando ureia e água. O gráfico ao lado mostra as
massas de ureia e de água que são produzidas em função da massa de amônia, considerando as
reações completas.
A partir dos dados do gráfico e dispondo-se de 270 g de amônia, a massa aproximada, em
gramas, de gás carbônico minimamente necessária para reação completa com essa quantidade
de amônia é
a) 120
Aula 02 – Cálculos das reações químicas 88
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
b) 270
c) 350
d) 630
e) 700
Comentários
Reação:
Segundo o gráfico, monta-se duas proporções:
Amônia → ureia 90 𝑔 𝑎𝑚ô𝑛𝑖𝑎 −−−− 160 𝑔 𝑑𝑒 𝑢𝑟𝑒𝑖𝑎
270 𝑔 𝑎𝑚ô𝑛𝑖𝑎 −−−− 𝑥 𝑔 𝑑𝑒 𝑢𝑟𝑒𝑖𝑎
x = 480 g de ureia
Amônia → água 110 𝑔 𝑎𝑚ô𝑛𝑖𝑎 − − − − 60 𝑔 𝑑𝑒 á𝑔𝑢𝑎
270 𝑔 𝑎𝑚ô𝑛𝑖𝑎 − − − − 𝑦 𝑔 𝑑𝑒 á𝑔𝑢𝑎
y = 147,27 g de água
Considerando a lei da conservação das massas, tem-se:
270 g + massa(gás carbônico) = 480 g + 147,27
massa(gás carbônico) = 357,27 g
Gabarito: C
10. (FUVEST SP/2015)
Uma estudante de Química realizou o seguinte experimento: pesou um tubo de ensaio
vazio, colocou nele um pouco de NaHCO3 (s) e pesou novamente. Em seguida, adicionou ao tubo
de ensaio excesso de solução aquosa de HCl, o que provocou a reação química representada por
NaHCO3 (s) + HCl (aq) → NaCl (aq) + CO2 (g) + H2O (l)
Após a reação ter-se completado, a estudante aqueceu o sistema cuidadosamente, até que
restasse apenas um sólido seco no tubo de ensaio. Deixou o sistema resfriar até a temperatura
ambiente e o pesou novamente. A estudante anotou os resultados desse experimento em seu
caderno, juntamente com dados obtidos consultando um manual de Química:
Aula 02 – Cálculos das reações químicas 89
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
A estudante desejava determinar a massa de
I. HCl que não reagiu;
II. NaCl que se formou;
III. CO2 que se formou.
Considerando as anotações feitas pela estudante, é possível determinar a massa de
a) I, apenas.
b) II, apenas.
c) I e III, apenas.
d) II e III, apenas.
e) I, II e III.
Comentários
Aplicando a lei da conservação das massas para os processos, julga-se os itens acima:
I. Errado. HCl que não reagiu não é possível determinar, pois encontra-se misturado à água tanto no
início quanto ao final do procedimento e não é proporcional à quantidade da substância formada.
II. Certo. O NaCl formado é determinado pela massa final do procedimento menos a massa do tubo
de ensaio vazio.
III. Certo. A massa de CO2 formada pode ser calculada a partir da massa de qualquer substância
consumida ou formada na reação, nesse caso a massa desse gás é determinada pela massa de NaCl
produzida.
Gabarito: D
11. (FUVEST SP/2013)
Uma moeda antiga de cobre estava recoberta com uma camada de óxido de cobre (II).
Para restaurar seu brilho original, a moeda foi aquecida ao mesmo tempo em que se passou
Aula 02 – Cálculos das reações químicas 90
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
sobre ela gás hidrogênio. Nesse processo, formou-se vapor de água e ocorreu a redução
completa do cátion metálico.
As massas da moeda, antes e depois do processo descrito, eram, respectivamente, 0,795
g e 0,779 g.
Assim sendo, a porcentagem em massa do óxido de cobre (II) presente na moeda, antes
do processo de restauração, era
Dados:
Massas molares (g/mol)
H = 1,00
O = 16,0
Cu = 63,5
a) 2%
b) 4%
c) 8%
d) 10%
e) 16%
Comentários
Porém a questão pergunta sobre a massa do óxido de cobre II (CuO). Na fórmula do óxido,
para cada átomo de oxigênio liga-se a um átomo de cobre. Sabendo que as massas molares, em
g/mol, dos elementos cobre e oxigênio são 63,5 e 16, respectivamente, sabe-se que a proporção,
em massa, de oxigênio e óxido de cobre II é 16g : 79,5g (79,5 g = 16 g + 63,5 g). Portanto, calcula-se:
16 𝑔 𝑑𝑒 𝑂 − − − − 79,5 𝑔 𝑑𝑒 𝐶𝑢𝑂
0,016 𝑔 𝑑𝑒 𝑂 − − − − 𝑦 𝑔 𝑑𝑒 𝐶𝑢𝑂
y = 0,0795 g de CuO
Determina-se a pureza:
0,0795 𝑔 𝐶𝑢𝑂
% = · 100% = 10%
0,795 𝑔 𝑚𝑜𝑒𝑑𝑎
Gabarito: D
Aula 02 – Cálculos das reações químicas 91
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
12. (FUVEST SP/2012)
Volumes iguais de uma solução de I2 (em solvente orgânico apropriado) foram colocados
em cinco diferentes frascos. Em seguida, a cada um dos frascos foi adicionada uma massa
diferente de estanho (Sn), variando entre 0,2 e 1,0 g. Em cada frasco, formou-se uma certa
quantidade de SnI4, que foi, então, purificado e pesado. No gráfico abaixo, são apresentados os
resultados desse experimento.
Com base nesses resultados experimentais, é possível afirmar que o valor da relação
é, aproximadamente,
a) 1:8
b) 1:4
c) 1:2
d) 2:1
e) 4:1
Comentários
A equação da reação balanceada é: Sn + 2 I2 → SnI4.
Analisando os valores exatos do gráfico e colocando em uma tabela, temos:
Aula 02 – Cálculos das reações químicas 92
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
Porém, a massas determinadas corresponde à proporção em massa para o dobro do número
de mols de I2. Dividindo os valores por 2, temos: 0,4g , 0,8g e 1,2g, que correspondem ao dobro da
quantidade de Sn.
Gabarito: D
13. (FUVEST SP/2010)
Sob condições adequadas, selênio (Se) e estanho (Sn) podem reagir, como representado
pela equação
2 Se + Sn → SnSe2
Em um experimento, deseja-se que haja reação completa, isto é, que os dois reagentes
sejam totalmente consumidos. Sabendo-se que a massa molar do selênio (Se) é 2/3 da massa
molar do estanho (Sn), a razão entre a massa de selênio e a massa de estanho (m Se : mSn), na
reação, deve ser de
a) 2:1
b) 3:2
c) 4:3
d) 2:3
e) 1:2
Comentários
A proporção na reação entre selênio e estanho é:
2 mol Se : 1 mol Sn
Aula 02 – Cálculos das reações químicas 93
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
Transformando para massa, temos:
2mol x massa molar do Se : 1 mol x massa molar do Sn.
Sabendo que a massa do Se é 2/3 da massa do Sn, tem-se:
2 mol x 2/3 massa molar do Sn : 1 mol x massa molar do Sn
4/3 massa do Sn : 1 massa do Sn
Gabarito: C
14. (FUVEST SP/2006)
Com a chegada dos carros com motor Flex, que funcionam tanto com álcool quanto com
gasolina, é importante comparar o preço do litro de cada um desses combustíveis. Supondo-se
que a gasolina seja octano puro e o álcool, etanol anidro, as transformações que produzem
energia podem ser representadas por:
25
C8H18(l) + O2 (g) → 8 CO2(g) + 9 H2O (g) + 5100kJ
2
C2H5OH(l) + 3 O2 (g) → 2 CO2 (g) + 3 H2O (g) + 1200kJ
Considere que, para o mesmo percurso, idêntica quantidade de energia seja gerada no
motor Flex, quer se use gasolina, quer se use álcool. Nesse contexto, será indiferente, em termos
econômicos, usar álcool ou gasolina se o quociente entre o preço do litro de álcool e do litro de
gasolina for igual a:
a) 1/2
b) 2/3
c) 3/4
d) 4/5
e) 5/6
Comentários
A partir do texto da questão, infere-se que, para o mesmo percurso, foi desprendida a mesma
quantidade de energia pelo octano e pelo etanol.
Portanto, partindo de 5100 kJ de energia para ambos os combustíveis, massas diferentes para
eles:
Octano 5100 kJ → 1 mol C8H18 → 114 g de octano
1200 𝑘𝐽 − − − − 46 𝑔 𝑑𝑒 𝑒𝑡𝑎𝑛𝑜𝑙
Etanol 5100 𝑘𝐽 − − − − 𝑥 𝑔 𝑑𝑒 𝑒𝑡𝑎𝑛𝑜𝑙
x = 195,5 g de etanol
Aula 02 – Cálculos das reações químicas 94
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
Portanto, para ocorrer a equivalência no preço de octano e etanol, temos:
Preçooctano · Volumeoctano = Preçoetanol · Volumeetanol
Preçooctano · 162,85mL = Preçoetanol · 244,375mL
Preçoetanol 162,85 mL 2
= =
Preçooctano 244,375 mL 3
Gabarito: B
15. (FUVEST SP/2006)
Embalagens de fertilizantes do tipo NPK trazem três números, compostos de dois
algarismos, que se referem, respectivamente, ao conteúdo de nitrogênio, fósforo e potássio,
presentes no fertilizante. O segundo desses números dá o conteúdo de fósforo, porém expresso
como porcentagem, em massa, de pentóxido de fósforo. Para preparar 1 kg de um desses
fertilizantes, foram utilizados 558 g de mono-hidrogenofosfato de amônio e 442 g de areia
isenta de fosfatos. Na embalagem desse fertilizante, o segundo número, relativo ao fósforo, deve
ser, aproximadamente,
a) 10
b) 20
c) 30
d) 40
e) 50
Comentários
Para resolver essa questão é imprescindível saber as fórmulas das substâncias:
Pentóxido de fósforo: P2O5
Mono-hidrogenofosfato de amônio: (NH4)2HPO4
Aula 02 – Cálculos das reações químicas 95
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
Balanceando a quantidade de fósforos, temos: 2 (NH4)2HPO4 → P2O5
2 · 132 𝑔 𝑑𝑒 Mono − hidrogenofosfato de amônio − − − − 1 · 142 𝑔 𝑑𝑒 𝑝𝑒𝑛𝑡ó𝑥𝑖𝑑𝑜 𝑑𝑒 𝑓ó𝑠𝑓𝑜𝑟𝑜
538 𝑔 𝑑𝑒 Mono − hidrogenofosfato de amônio −−−− 𝑥 𝑔 𝑑𝑒 𝑝𝑒𝑛𝑡ó𝑥𝑖𝑑𝑜 𝑑𝑒 𝑓ó𝑠𝑓𝑜𝑟𝑜
x = 300 g de P2O5
Portanto, a pureza é determinada por:
300 𝑔 𝑑𝑒 𝑃2 𝑂5
%=
1000 𝑔 𝑡𝑜𝑡𝑎𝑙
300 𝑔 𝑑𝑒 𝑃2 𝑂5
%= · 100 % = 30 %
1000 𝑔 𝑡𝑜𝑡𝑎𝑙
Gabarito: C
16. (FUVEST SP/2006)
O tanque externo do ônibus espacial Discovery carrega, separados, 1,20·106 L de
hidrogênio líquido a –253 °C e 0,55 · 106 L de oxigênio líquido a –183 °C. Nessas temperaturas,
a densidade do hidrogênio é 34 mol/L (equivalente a 0,068 g/mL) e a do oxigênio é 37 mol/L
(equivalente a 1,18 g/mL).
Dados:
H = 1,0; O =16
Considerando o uso que será feito desses dois líquidos, suas quantidades (em mols), no
tanque, são tais que há
a) 100% de excesso de hidrogênio.
b) 50% de excesso de hidrogênio.
c) proporção estequiométrica entre os dois.
d) 25% de excesso de oxigênio.
e) 75% de excesso de oxigênio.
Comentários
Em um ônibus espacial o gás hidrogênio é o combustível e o oxigênio é o comburente para a
reação a seguir:
2 H2 (g) + O2 (g) → 2 H2O (g)
Determinando o número de mols de cada reagente, temos:
Hidrogênio Oxigênio
1,20·106 L 0,55 · 106 L
densidade do hidrogênio é 34 mol/L. densidade do oxigênio é 37 mol/L.
1,20·106 L · 34 mol/L = 40,8·106 mol H2 0,55·106 L · 37 mol/L = 20,35·106 mol O2
Aula 02 – Cálculos das reações químicas 96
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
A proporção da reação é 2 mol de H2 para 1 mol de O2, portanto os materiais estão,
aproximadamente, em proporção estequiométrica.
Gabarito: C
17. (FUVEST SP/2016)
Sabe-se que os metais ferro (Fe0), magnésio (Mg0) e estanho (Sn0) reagem com soluções
de ácidos minerais, liberando gás hidrogênio e formando íons divalentes em solução.
Foram feitos três experimentos em que três amostras metálicas de mesma massa
reagiram, separada e completamente, com uma solução aquosa de ácido clorídrico (HC (aq))
de concentração 0,1 mol/L.
Os resultados obtidos foram:
Massa da Volume da solução de
Composição da
Experimento amostra HC (aq) (0,1 mol /L) gasto na reação
amostra metálica
metálica (g) completa
1 5,6 Fe0 puro V1
Fe0 contendo Mg0
2 5,6 V2
como impureza
Fe0 contendo
3 5,6 V3
Sn0como impureza
Colocando-se os valores de V1, V2 e V3 em ordem decrescente, obtém-se
Note e adote:
Massa molar (g/ mol) : Mg ....... 24
Fe ....... 56
Sn ..... 119
a) V2>V3>V1
b) V3>V1>V2
c) V1>V3>V2
d) V2>V1>V3
e) V1>V2>V3
Comentários
Todas as amostras apresentam a mesma massa, portanto a amostra que apresentará maior
consumo de ácido será aquela que tiver o maior número de partículas nos 5,6 gramas testados. Para
uma mesma massa de substâncias diferentes, quanto maior a massa molar, menor a quantidade de
partículas. A amostra contendo magnésio (menor massa molar) será a que apresentará mais
partículas e consumirá mais ácido clorídrico, portanto a amostra contendo estanho propiciará o
menor consumo de ácido clorídrico.
Gabarito: D
Aula 02 – Cálculos das reações químicas 97
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
18. (FUVEST SP/2009)
Em três balanças aferidas, A, B e C, foram colocados três béqueres de mesma massa, um
em cada balança. Nos três béqueres, foram colocados volumes iguais da mesma solução aquosa
de ácido sulfúrico. Foram separadas três amostras, de massas idênticas, dos metais magnésio,
ouro e zinco, tal que, havendo reação com o ácido, o metal fosse o reagente limitante. Em cada
um dos béqueres, foi colocada uma dessas amostras, ficando cada béquer com um metal
diferente. Depois de algum tempo, não se observando mais nenhuma transformação nos
béqueres, foram feitas as leituras de massa nas balanças, obtendo-se os seguintes resultados
finais:
balança A: 327,92 g
balança B: 327,61 g
balança C: 327,10 g
As massas lidas nas balanças permitem concluir que os metais magnésio, ouro e zinco
foram colocados, respectivamente, nos béqueres das balanças.
Dados: massa molar em g·mol-1
Mg .......... 24,3
Au ......... 197,0
Zn .......... 65,4
a) A, B e C
b) A, C e B
c) B, A e C
d) B, C e A
e) C, A e B
Comentários
A reação de um metal com ácido procede de forma geral como:
Metal (s) + ácido (l) → sal(s) + hidrogênio (g)
Quanto maior o número de partículas de metal reagindo, maior a quantidade de gás
hidrogênio liberado e, consequentemente, menor a massa restante no frasco aberto. O metal que
apresenta a maior massa molar, possui menor quantidade de partículas, para uma mesma massa.
A balança C teve maior desprendimento de gás hidrogênio, portanto maior variação na massa
contido no béquer. A utilização de um metal que apresente maior quantidade de partículas justifica
essa alteração na massa, portanto, esse metal é o magnésio. Ao passo que, na balança A foi utilizado
ouro.
Balança A → ouro
Balança B → zinco
Balança C → magnésio
Gabarito: E
Aula 02 – Cálculos das reações químicas 98
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
19. (FUVEST SP/2007)
Alguns problemas de saúde, como bócio endêmico e retardo mental, são causados pela
ingestão de quantidades insuficientes de iodo. Uma maneira simples de suprir o organismo
desse elemento químico é consumir o sal de cozinha que contenha de 20 a 60 mg de iodo por
quilograma do produto. No entanto, em algumas regiões do País, o problema persiste, pois o sal
utilizado ou não foi produzido para consumo humano, ou não apresenta a quantidade mínima
de iodo recomendada. A fonte de iodo utilizada na indústria do sal é o iodato de potássio, KIO 3,
cujo custo é de R$ 20,00/kg.
Considerando que o iodo representa aproximadamente 60% da massa de KIO3 e que 1 kg
do sal de cozinha é comercializado ao preço médio de R$ 1,00, a presença da quantidade máxima
de iodo permitida por lei (60 miligramas de iodo por quilograma de sal) representa, no preço, a
porcentagem de
a) 0,10%
b) 0,20%
c) 1,20%
d) 2,0%
e) 12%
Comentários
60 mg de iodo/kg de sal → custo de 60 mg de iodo/ 1 real de sal de cozinha.
Cálculo do custo de 60 mg de iodo.
60 𝑚𝑔 𝑑𝑒 𝑖𝑜𝑑𝑜 − − − − 60 %
𝑥 𝑚𝑔 𝑑𝑒 𝐾𝐼𝑂3 − − − − 100 %
x = 100 mg de KIO3
106 𝑚𝑔 𝑑𝑒 𝐾𝐼𝑂3 − − − − 20 𝑟𝑒𝑎𝑖𝑠
100 𝑚𝑔 𝑑𝑒 𝐾𝐼𝑂3 − − − − 𝑦 𝑟𝑒𝑎𝑖𝑠
y = 0,002 reais.
O custo percentual é igual a:
0,002 𝑟𝑒𝑎𝑖𝑠
%= · 100 % = 0,2 %
1 𝑟𝑒𝑎𝑙
Gabarito: B
20. (FUVEST SP/2000)
Recentemente, na Bélgica, descobriu-se que frangos estavam contaminados com uma
dioxina contendo 44%, em massa, do elemento cloro. Esses frangos apresentavam, por kg,
2,0·10-13 mol desse composto, altamente tóxico.
Supondo que um adulto possa ingerir, por dia, sem perigo, no máximo 3,23·10-11 g desse
composto, a massa máxima diária, em kg de frango contaminado, que tal pessoa poderia
consumir seria igual a:
Aula 02 – Cálculos das reações químicas 99
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
Dados:
1 mol da dioxina contém 4 mols de átomos de cloro.
massa molar do cloro (Cℓ) = 35,5 g/mol
a) 0,2
b) 0,5
c) 1
d) 2
e) 3
Comentários
O frango apresenta contaminação de 2·10-13 mol de dioxina/kg de frango. Para poder
comparar a quantidade de dioxina presente no frango com a quantidade permitida para um adulto,
é necessário converter a unidade mol para grama de dioxina.
Cálculo da massa molar da dioxina, sabendo que para 1 mol de dioxina apresenta 4 mols de
átomos de cloro (massa molar 35,5 g/mol).
44 % − − − − 4 · 35,5 𝑔 𝑑𝑒 𝐶𝑙
100 % − − − − 𝑥𝑔
x = 322,72 g em 1 mol de dioxina
Cálculo da massa de dioxina presente em 1 kg de frango:
322,72 𝑔
· 2·10-13 mol = 645,45·10-13 g de dioxina/kg de frango
1 𝑚𝑜𝑙 𝑑𝑒 𝑑𝑖𝑜𝑥𝑖𝑛𝑎
Cálculo da quantidade de frango que um indivíduo pode comer, sabendo que o limite humano
é de 3,23·10-11 g de dioxina:
645,45 · 10−13 g de dioxina − − − − 1 𝑘𝑔 𝑑𝑒 𝑓𝑟𝑎𝑛𝑔𝑜
3,23 · 10−11 g de dioxina −−−− 𝑦 𝑘𝑔 𝑑𝑒 𝑓𝑟𝑎𝑛𝑔𝑜
y = 0,5 kg
Gabarito: B
21. (FUVEST SP/1998)
A dose diária recomendada do elemento cálcio para um adulto é de 800 mg. Suponha
certo suplemento nutricional a base de casca de ostras que seja 100% CaCO 3. Se um adulto
tomar diariamente dois tabletes desse suplemento de 500mg cada, qual porcentagem de cálcio
da quantidade recomendada essa pessoa está ingerindo?
massas molares (g/mol)
Ca ........................... 40
O ............................. 16
C ............................. 12
a) 25%
b) 40%
c) 50%
Aula 02 – Cálculos das reações químicas 100
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
d) 80%
e) 125%
Comentários
A massa ingerida de suplemento é 2·500 mg = 1000 mg = 1g de CaCO 3.
Calcula-se a massa de cálcio presente em 1 g de CaCO3, sabendo que as massas molares de
CaCO3 e de Ca são iguais a 100 e 40 g/mol.
100 𝑔 𝐶𝑎𝐶𝑂3 − − − − 40 𝑔 𝐶𝑎
1 𝑔 𝐶𝑎𝐶𝑂3 − − − − 𝑥 𝑔 𝐶𝑎
x = 0,4 g = 400 mg de Ca
400 𝑚𝑔 𝑑𝑒 𝐶𝑎
%= · 100 % = 50%
800 𝑚𝑔 𝑡𝑜𝑡𝑎𝑙
Gabarito: C
22. (UEA AM/2017)
Até a época dos trabalhos de Lavoisier, considerado o grande responsável pelo
nascimento da Química Moderna, acreditava-se que a água era uma substância simples.
Essa ideia foi invalidada quando ele demonstrou que a água líquida poderia ser
a) vaporizada, misturando-se com o ar em diferentes proporções.
b) obtida, como um único produto, pela reação entre hidrogênio e oxigênio.
c) misturada com o álcool em diferentes proporções.
d) transformada em gelo por abaixamento de temperatura.
e) obtida, como único produto, da liquefação do vapor de água.
Comentários
a) Errado. A vaporização é uma transformação física que não fornece informações sobre a
composição da matéria.
b) Certo. A reação das duas substâncias – hidrogênio e oxigênio – produz uma substância
composta formada pela combinação desses elementos.
c) Errado. A dissolução é um fenômeno físico e não fornece informações sobre a composição.
d) Errado. A fusão é uma transformação física que não fornece informações sobre a
composição da matéria.
e) Errado. A liquefação é uma transformação física que não fornece informações sobre a
composição da matéria.
Gabarito: B
Aula 02 – Cálculos das reações químicas 101
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
23. (UEPB/2011)
Um professor realizou um experimento em um laboratório no qual ele realizou a queima
de papel amassado e de esponja de aço, respectivamente, em balanças artesanais, conforme
figura 1.
Figura 1: balanças contendo papel amassado e esponja de aço, respectivamente, antes da
queima desses materiais.
Nos pratos da esquerda de cada balança são adicionados pesos de modo que os pratos
ficam em equilíbrio (mesmo peso) antes da queima. Considere que as balanças estão expostas
às condições ambiente e que nenhum produto sólido escapa dos pratos após a queima. Assuma
ainda que o papel seja um polímero cuja unidade polimérica é um monômero de fórmula
mínima (C6H10O5)n e que a esponja de aço utilizada é constituída unicamente de átomos de
Ferro.
Assinale a alternativa que apresenta o comportamento qualitativo mais provável da
balança após a queima de cada material:
a)
b)
c)
Aula 02 – Cálculos das reações químicas 102
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
d)
e) Nenhuma das alternativas, pois a esponja de aço não queima.
Comentários
A queima de papel libera gás carbônico e água, logo, o prato contendo papel se torna mais
leve e sobe.
Papel + oxigênio → gás carbônico/monóxido de carbono + água
A queima da esponja de aço incorpora átomos de oxigênio, logo, o prato contendo a esponja
de aço se torna mais pesado e desce.
ferro + oxigênio → óxido de ferro
Gabarito: D
24. (PUC SP/2011)
Um determinado metal queima ao ar para formar o respectivo óxido, um sólido de alta
temperatura de fusão. A relação entre a massa do metal oxidado e a massa de óxido formado
está representada no gráfico a seguir.
Aula 02 – Cálculos das reações químicas 103
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
Durante um experimento, realizado em recipiente fechado, foi colocado para reagir 1,00
g do referido metal, obtendo-se 1,40 g do seu óxido. Considerando-se que todo o oxigênio
presente no frasco foi consumido, pode-se determinar que a massa de oxigênio presente no
sistema inicial é x. Em outro recipiente fechado, foram colocados 1,50 g do referido metal em
contato com 1,20 g de oxigênio. Considerando que a reação ocorreu até o consumo total de pelo
menos um dos reagentes, pode-se afirmar que a massa de óxido gerado é y.
Sabendo que o metal em questão forma apenas um cátion estável e considerando que em
todas as reações o rendimento foi de 100 %, os valores de x e y são, respectivamente,
a) 0,40 g e 2,70 g.
b) 0,40 g e 2,50 g.
c) 0,56 g e 2,50 g.
d) 0,56 g e 3,00 g.
e) 0,67 g e 2,70 g.
Comentários
Preste atenção ao enunciado da questão: “foi colocado para reagir 1,00 g do referido metal,
obtendo-se 1,40 g do seu óxido”, ou seja, a questão não afirmou que todo o metal foi consumido,
mas informou a quantidade do produto formado. Posteriormente, afirma que todo o oxigênio foi
consumido, mas nada foi dito do consumo total do metal. No segundo experimento a questão volta
a fornecer dados das substâncias colocadas.
Portanto, a proporção da reação terá que ser extraída do gráfico fornecido. Qualquer ponto
do gráfico, que seja preciso, pode ser utilizado, porque trata-se de uma proporção direta.
Aula 02 – Cálculos das reações químicas 104
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
Proporção das substâncias participantes: 120 g do metal → 200 g do óxido.
A partir da proporção de consumo e produção destacada acima, completa-se a primeira
reação a partir da quantidade do produto formado.
O valor de x é 0,56 g.
A questão forneceu a quantidade de dois reagentes, logo é necessário testar se ocorre caso
de excesso e limitante. Para isso, escolha o valor fornecido de um dos reagentes e faça a proporção
estequiométrica entre eles.
Aula 02 – Cálculos das reações químicas 105
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
120 𝑔 𝑑𝑒 𝑚𝑒𝑡𝑎𝑙 − − − − 80 𝑔 𝑑𝑒 𝑜𝑥𝑖𝑔ê𝑛𝑖𝑜
1,50 𝑔 𝑑𝑒 𝑚𝑒𝑡𝑎𝑙 − − − − 𝑦 𝑔 𝑑𝑒 𝑜𝑥𝑖𝑔ê𝑛𝑖𝑜
y = 1 g de oxigênio
Explicação do teste: para consumir todos os 1,5 g do metal é necessário 1 g de oxigênio. A
questão informou que possui 1,2 g de oxigênio, ou seja, o oxigênio apresenta 0,2 g de excesso.
A massa do produto formado será resultado do consumo de 1,5 g do metal mais 1 g do
oxigênio, o que é igual a 2,5 g.
Gabarito: C
25. (PUC Camp SP/2011)
Em três experimentos sobre a combustão do carvão, C (s), foram obtidos os seguintes
resultados:
Os experimentos que seguem a lei de Lavoisier são:
a) I e II, somente.
b) I, II e III, somente.
c) II, III e IV, somente.
d) III e IV, somente.
e) I, II, III e IV.
Comentários
Para satisfazer a lei da conservação das massas, o somatório das massas dos reagentes
consumidos deve ser igual ao somatório das massas dos produtos formados.
Experimento I: 12 g de carbono reagem com 32 g de oxigênio e produz 44 g de dióxido de
carbono.
Experimento II: 18 g + 48 g = 66 g.
Experimento III: 24 g + 64 g (massa consumida) = 88 g
Experimento IV: 36 g (massa de carbono) + 96 g = 132 g
Portanto, todas as reações satisfazem a lei da conservação das massas.
Gabarito: E
26. (UFF RJ/2009)
Aula 02 – Cálculos das reações químicas 106
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
Desde a Antiguidade, diversos povos obtiveram metais, vidro, tecidos, bebidas alcoólicas,
sabões, perfumes, ligas metálicas, descobriram elementos e sintetizaram substâncias que
passaram a ser usadas como medicamentos. No século XVIII, a Química, a exemplo da Física,
torna-se uma ciência exata. Lavoisier iniciou na Química o método científico, estudando os
porquês e as causas dos fenômenos. Assim, descobriu que as transformações químicas e físicas
ocorrem com a conservação da matéria. Outras leis químicas também foram propostas e, dentre
elas, as ponderais, ainda válidas.
Com base nas leis ponderais, pode-se afirmar que, segundo:
I. a Lei da Conservação da Massa (Lavoisier), 1,0 g de Ferro ao ser oxidado pelo
Oxigênio, produz 1,0 g de Óxido Férrico;
II. a Lei da Conservação da Massa, ao se usar 16,0 g de Oxigênio molecular para reagir
completamente com 40,0 g de Cálcio, são produzidas 56 g de Óxido de Cálcio;
III. a Lei das Proporções Definidas, se 1,0 g de Ferro reage com 0,29 g de Oxigênio para
formar o composto Óxido Ferroso, 2,0 g de Ferro reagirão com 0,87 g de Oxigênio, produzindo
o mesmo composto;
IV. a Lei das Proporções Múltiplas, dois mols de Ferro reagem com dois mols de
Oxigênio para formar Óxido Ferroso; logo, dois mols de Ferro reagirão com três mols de
Oxigênio para formar Óxido Férrico.
Assinale a opção correta.
a) As afirmativas I e II estão corretas.
b) A afirmativa II está correta.
c) As afirmativas II e III estão corretas.
d) As afirmativas II e IV estão corretas.
e) A afirmativa III está correta.
Comentários
I. Errado. Ao se combinar com o oxigênio, a massa do óxido férrico será maior que a do
ferro inicial.
II. Certo. A soma dos reagentes consumidos (16 g + 40 g) é igual à massa do produto 56
g.
III. Errado. Ao dobrar a quantidade de ferro de consumo é necessário dobrar a quantidade
de oxigênio também, porque a proporção entre as substâncias de uma reação é sempre constante.
IV. Certo. A lei das proporções múltiplas detalha que dois elementos podem realizar
reações distintas, sendo que cada reação possui sua própria proporção definida.
Gabarito: D
27. (IME RJ/2016)
Aula 02 – Cálculos das reações químicas 107
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
Em 33,65 g de um sal de magnésio está presente 1 mol deste elemento. Sendo trivalente
o ânion deste sal, é correto afirmar que a massa de 1 mol do ânion é
(Massa molar: Mg = 24,31 g/mol)
a) 6,23 g
b) 14,01 g
c) 24,31 g
d) 42,03 g
e) 48,62 g
Comentários
Ao formar um composto iônico, um sal no caso da questão, o magnésio apresenta-se como
cátion bivalente. A combinação de um ânion trivalente genérico (X3-) e o cátion bivalente de
magnésio (Mg2+) produz o sal de fórmula Mg3X2.
A proporção das fórmulas é: 1 mol de Mg3X2 → 3 mol de Mg2+ → 2 mol X3-
A questão forneceu que 1 mol de magnésio é proporcional a 33,65 g do sal (composto iônico),
logo 3 mols de magnésio equivalem a 100,95 g, que é a massa molar desse sal.
Portanto, sabendo que a massa molar do magnésio é igual a 24,31, calcula-se a massa do
ânion:
100,95 g = 3·24,31 g + 2·X3-
X3- = 14,01 g/mol
Gabarito: B
28. (PUC Camp SP/2016)
O bronze campanil, ou bronze de que os sinos são feitos, é uma liga composta de 78% de
cobre e 22% de estanho, em massa.
Assim, a proporção em mol entre esses metais, nessa liga, é, respectivamente, de 1,0 para
Dados:
Massas molares (g/mol)
Cu = 63,5
Sn = 118,7
a) 0,15.
b) 0,26.
c) 0,48.
d) 0,57.
e) 0,79.
Aula 02 – Cálculos das reações químicas 108
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
Comentários
Para qualquer massa inicial da mistura, constrói-se a relação, em menores números inteiros,
em mols entre os elementos químicos. Adota-se 100 g da mistura.
Cobre (63,5 g/mol) Estanho (118,7 g/mol)
78% 22%
A partir de 100 g da mistura → 78 g de Cobre A partir de 100 g da mistura → 22 g de Estanho
Determinando o número de mols: Determinando o número de mols:
1 𝑚𝑜𝑙 𝑑𝑒 𝐶𝑢 − − − − 63,5 𝑔 1 𝑚𝑜𝑙 𝑑𝑒 𝑆𝑛 − − − − 118,7 𝑔
𝑥 𝑚𝑜𝑙 𝑑𝑒 𝐶𝑢 − − − − 78 𝑔 𝑦 𝑚𝑜𝑙 𝑑𝑒 𝑆𝑛 − − − − 22 𝑔
x = 1,228 mol de Cu y = 0,185 mol de Sn
A menor proporção em números inteiros de mols dos elementos é:
1,228 𝑚𝑜𝑙 𝐶𝑢 0,185 𝑚𝑜𝑙 𝑆𝑛
: = 1 : 0,15
1,228 𝑚𝑜𝑙 1,228 𝑚𝑜𝑙
Gabarito: A
29. (UNESP SP/2016)
Considere amostras de 1 g de cada uma das seguintes substâncias: eteno (C 2H4),
monóxido de carbono (CO) e nitrogênio (N2). Essas três amostras
a) apresentam a mesma quantidade, em mol, de moléculas.
b) apresentam a mesma quantidade, em mol, de átomos.
c) apresentam ligações covalentes polares.
d) são de substâncias isômeras.
e) são de substâncias simples.
Comentários
a) Certa. As três substâncias apresentam o mesmo valor de massa molar que é 28
g/mol e, consequentemente, para uma mesma massa, apresentarão a mesma quantidade, em
mol, de partículas.
b) Errada. Apresentarão número de átomos diferentes porque, mesmo apresentando
a mesma massa por molécula, possuem diferentes quantidades de átomos por molécula.
c) Errada. A molécula N2 é formada por uma ligação covalente entre átomos iguais
que não apresentam diferença de eletronegatividade e, consequentemente, formam uma ligação
covalente apolar.
d) Errada. Isômeros são substâncias que apresentam a mesma fórmula molecular,
mas diferentes propriedades.
e) Errada. Eteno e monóxido de carbono são substâncias compostas.
Aula 02 – Cálculos das reações químicas 109
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
Gabarito: A
30. (UNICAMP SP/2013)
Entre os vários íons presentes em 200 mililitros de água de coco há aproximadamente
320 mg de potássio, 40 mg de cálcio e 40 mg de sódio. Assim, ao beber água de coco, uma pessoa
ingere quantidades diferentes desses íons, que, em termos de massa, obedecem à sequência:
potássio>sódio=cálcio. No entanto, se as quantidades ingeridas fossem expressas em mol, a
sequência seria:
a) potássio>cálcio=sódio.
b) cálcio=sódio>potássio.
c) potássio>sódio>cálcio.
d) cálcio>potássio>sódio.
Dados de massas molares em g/mol: cálcio = 40, potássio = 39 e sódio = 23.
Comentários
Potássio (39 g/mol) Cálcio (40 g/mol) Sódio (23 g/mol)
39 𝑔 − − − − 1 𝑚𝑜𝑙 40 𝑔 − − − − 1 𝑚𝑜𝑙 23 𝑔 − − − − 1 𝑚𝑜𝑙
0,320 𝑔 − − − − 𝑥 𝑚𝑜𝑙 0,040 𝑔 − − − − 𝑦 𝑚𝑜𝑙 0,040 𝑔 − − − − 𝑧 𝑚𝑜𝑙
x = 0,008 mol y = 0,001 mol z = 0,0017 mol
Potássio > sódio > cálcio
Gabarito: C
31. (UNICAMP SP/2016)
Podemos obter energia no organismo pela oxidação de diferentes fontes. Entre essas
fontes destacam-se a gordura e o açúcar. A gordura pode ser representada por uma fórmula
mínima (CH2)n enquanto um açúcar pode ser representado por (CH2O)n. Considerando essas
duas fontes de energia, podemos afirmar corretamente que, na oxidação total de 1 grama de
ambas as fontes em nosso organismo, os produtos formados são
a) os mesmos, mas as quantidades de energia são diferentes.
b) diferentes, mas as quantidades de energia são iguais.
c) os mesmos, assim como as quantidades de energia.
d) diferentes, assim como as quantidades de energia.
Comentários
A combustão de um material orgânico gera gás carbônico e água, porém as ligações
rompidas dos reagentes são diferentes. O açúcar apresenta ligações com o oxigênio, enquanto a
gordura não apresenta (em grande quantidade).
Aula 02 – Cálculos das reações químicas 110
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
Gabarito: A
32. (FGV SP/2016)
Um certo polímero é produzido a partir de um monômero, que é um hidrocarboneto que
contém somente uma instauração. A análise elementar por combustão completa de 0,5 mol de
moléculas desse hidrocarboneto resultou em 1,5 mol de moléculas de CO 2.
A massa molar, em g·mol–1, desse monômero é
a) 28.
b) 42.
c) 44.
d) 56.
e) 58.
Comentários
O polímero formado a partir de um monômero monoinsaturado apresenta fórmula geral
CnH2n+2 (hidrocarboneto saturado). A polimerização por adição de um monômero monoinsaturado
produz um polímero saturado.
Como 0,5 mol do polímero produz 1,5 mol de CO2, a combustão de 1 mol do polímero produz
3 mols de CO2. Reescrevendo a equação e balanceando com essa nova proporção, tem-se:
1 CnH2n+2 + O2 → 3 CO2 + H2O
Portanto, n = 3. Como a fórmula geral do monômero monoinsturado é igual C nH2n, sendo n=3,
tem-se: C3H6 e massa molar 42 g/mol.
Gabarito: B
33. (Unioeste PR/2015)
Uma molécula cuja massa molar é 74 g/mol possui a seguinte composição centesimal:
C 64,9%, H 13,5% e O 21,6%.
Das fórmulas moleculares mostradas abaixo, aquela que se enquadra nesta análise é:
a) C4H10O.
b) C3H6O2.
c) C5H2O.
d) C4H8O2.
e) C2H2O3.
Aula 02 – Cálculos das reações químicas 111
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
Comentários
Gabarito: A
34. (PUC Camp SP/2014)
Nos processos de fermentação, pode-se usar o fermento biológico, formado por lêvedos,
ou o fermento químico, cujo componente principal é o bicarbonato de sódio, NaHCO 3. Nessa
substância, a porcentagem, em massa, do elemento hidrogênio é igual a
Dados:
Massas molares (g/mol)
H = 1,0 C = 12,0
O = 16,0 Na = 23,0
a) 1,2%.
b) 3,4%.
c) 7,4%.
d) 10%.
e) 12%.
Comentários
Sabendo que a massa molar do NaHCO3 é igual a 72 g/mol, calcula-se:
1 𝑔 𝑑𝑒 ℎ𝑖𝑑𝑟𝑜𝑔ê𝑛𝑖𝑜
%= · 100 % = 1,38 %
72 𝑔 𝑡𝑜𝑡𝑎𝑙
Gabarito: A
35. (FMJ SP/2012)
Aula 02 – Cálculos das reações químicas 112
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
Dioxinas são substâncias altamente tóxicas formadas como subprodutos em diversos
processos industriais. Quando um mol de uma determinada dioxina, constituída apenas por
carbono, oxigênio e hidrogênio, é queimado com excesso de oxigênio, formam-se 2 mol de água
e 4 mol de CO2. Nessa dioxina, a massa de oxigênio corresponde a oito vezes a massa de
hidrogênio na molécula. Sua fórmula mínima é
a) CHO.
b) CHO2.
c) CHO4.
d) C2HO.
e) C2H2O.
Comentários
A reação de combustão da dioxina é:
? CxHyOz + ? O2 → ? CO2 + ? H2O
1 CxHyOz + ? O2 → 4 CO2 + 2 H2O
Logo, completando a equação, tem-se:
1 C4H4Oz + ? O2 → 4 CO2 + 2 H2O
Na molécula, a massa de oxigênio é oito vezes maior que a massa do hidrogênio:
massahidrogênio x 8 = massaoxigênio
4 x 8 = massaoxigênio
32 = massaoxigênio
Sabendo que a massa do oxigênio é igual a 16, tem-se dois oxigênios na fórmula.
Portanto, C4H4O2 e fórmula mínima C2H2O.
Gabarito: E
36. (UNESP SP/2018)
Bicarbonato de sódio sólido aquecido se decompõe, produzindo carbonato de sódio
sólido, além de água e dióxido de carbono gasosos. O gráfico mostra os resultados de um
experimento em que foram determinadas as massas de carbonato de sódio obtidas pela
decomposição de diferentes massas de bicarbonato de sódio.
Aula 02 – Cálculos das reações químicas 113
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
Os dados do gráfico permitem concluir que as massas de carbonato de sódio e
bicarbonato de sódio nessa reação estão relacionadas pela equação 𝑚𝑁𝑎2𝐶𝑂3 = 𝑘 · 𝑚𝑁𝑎𝐻𝐶𝑂3 , e
que o valor aproximado de k é
a) 0,3.
b) 1,0.
c) 0,2.
d) 0,7.
e) 1,2.
Comentários
𝑚𝑁𝑎2𝐶𝑂3 = 𝑘 · 𝑚𝑁𝑎𝐻𝐶𝑂3
40 = k·60
k = 0,666 = 0,7
Gabarito: D
37. (UNESP SP/2016)
A luz branca é composta por ondas eletromagnéticas de todas as frequências do espectro
visível. O espectro de radiação emitido por um elemento, quando submetido a um arco elétrico
ou a altas temperaturas, é descontínuo e apresenta uma de suas linhas com maior intensidade,
o que fornece “uma impressão digital” desse elemento. Quando essas linhas estão situadas na
região da radiação visível, é possível identificar diferentes elementos químicos por meio dos
chamados testes de chama. A tabela apresenta as cores características emitidas por alguns
elementos no teste de chama:
Aula 02 – Cálculos das reações químicas 114
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
Uma estudante preparou 10,0 mL de uma solução 1,00 mol·L–1 de cloreto de um dos
metais apresentados na tabela do texto a fim de realizar um teste de chama em laboratório. No
teste de chama houve liberação de luz vermelha intensa. A partir das informações contidas no
texto e utilizando a classificação periódica dos elementos, assinale a alternativa que apresenta
a massa do sal utilizado pela estudante, em gramas, e a sua fórmula.
a) 1,11 e CaCl2.
b) 7,56 e CaCl.
c) 11,1 e CaCl2.
d) 0,756 e CaCl.
e) 0,111 e CaCl2.
Comentários
O sal utilizado foi o cloreto de cálcio de fórmula CaCl2. O cálcio forma cátions de valência fixa,
perdendo dois elétrons, por ser um alcalinoterroso.
1 𝑚𝑜𝑙
· 0,01𝐿 = 0,01 𝑚𝑜𝑙 de CaCl2
1𝐿
111 𝑔
𝑚𝑎𝑠𝑠𝑎 = · 0,01𝑚𝑜𝑙 = 1,11 𝑔
1 𝑚𝑜𝑙
Gabarito: A
38. (UERJ/2015)
A proporção de moléculas de água presentes na forma hidratada de um sal pode ser
representada da seguinte forma, na qual X corresponde ao número de mols de água por mol
desse sal:
CuSO4· x H2O
Uma amostra de 4,99 g desse sal hidratado foi aquecida até que toda a água nela contida
evaporou, obtendo-se uma massa de 3,19 g de sulfato de cobre II.
O número de mols de água por mol de sulfato de cobre II na composição do sal hidratado
equivale a:
a) 2
b) 5
c) 10
d) 20
Aula 02 – Cálculos das reações químicas 115
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
Comentários
Portanto, a proporção 0,02 mol CuSO4 : 0,1 mol H2O → 1 mol CuSO4 : 5 mol H2O
Gabarito: B
39. (UERJ/2018)
A hemoglobina é uma proteína de elevada massa molar, responsável pelo transporte de
oxigênio na corrente sanguínea. Esse transporte pode ser representado pela equação química
abaixo, em que HB corresponde à hemoglobina.
HB + 4 O2 → HB(O2)4
Em um experimento, constatou-se que 1 g de hemoglobina é capaz de transportar
2,24·10–4 L de oxigênio molecular com comportamento ideal, nas CNTP.
A massa molar, em g/mol, da hemoglobina utilizada no experimento é igual a:
a) 1·105
b) 2·105
c) 3·105
d) 4·105
Comentários
A proporção, em mols, na equação de HB e O2 é de 1:4. Portanto, basta calcular a quantidade
em massa de HB consumida por 4 mols de oxigênio molecular.
A partir do volume molar 22,4 L/mol (fornecido no início da prova da UERJ), calcula-se o
volume, em litros, de 4 mols de O2.
22,4 𝐿 − − − − 1 𝑚𝑜𝑙
𝑥𝐿 − − − − 4 𝑚𝑜𝑙
Aula 02 – Cálculos das reações químicas 116
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
x = 89,6 L De O2 (equivale ao volume de 4 mol).
Compara-se o volume de 4 mol com a proporção encontrada na reação entre as substâncias:
1 𝑔 𝑑𝑒 𝐻𝐵 − − − − 2,24 · 10−4 𝐿 𝑑𝑒 𝑂2
𝑦 𝑔 𝑑𝑒 𝐻𝐵 −−−− 89,6 𝐿 𝑑𝑒 𝑂2
y = 4·105 g/mol
Gabarito: D
40. (FAMERP SP/2018)
Um isqueiro descartável contém gás isobutano (C4H10). Mesmo após o uso total desse
isqueiro, resta um resíduo do gás em seu interior. Considerando que o volume desse resíduo
seja igual a 1 mL e que o volume molar de gás nas condições de pressão e temperatura no
interior do isqueiro seja 25 L/mol, a massa de isobutano restante no isqueiro é,
aproximadamente,
a) 3 mg.
b) 4 mg.
c) 1 mg.
d) 2 mg.
e) 5 mg.
Comentários
A partir do volume molar – 25 L/mol – e da massa molar – 58 g/mol, calcula-se a massa, em
mg, de 1 mL de butano. (1 mol = 25 L (condições de temperatura e pressão da questão) = 58 g).
25 𝐿 − − − − 58 𝑔 𝑑𝑒 𝑏𝑢𝑡𝑎𝑛𝑜
1 𝑚𝐿 = 0,001 𝐿 − − − − 𝑥𝑔
x = 2,32 mg
Gabarito: D
41. (Fac. Israelita de C. da Saúde Albert Einstein SP/2018)
A pirita (FeS2) é encontrada na natureza agregada a pequenas quantidades de níquel,
cobalto, ouro e cobre. Os cristais de pirita são semelhantes ao ouro e, por isso, são chamados de
ouro dos tolos. Esse minério é utilizado industrialmente para a produção de ácido sulfúrico. Essa
produção ocorre em várias etapas, sendo que a primeira é a formação do dióxido de enxofre,
segundo a equação a seguir.
4 FeS2(s) + 11 O2(g) → 2 Fe2O3 (s) + 8 SO2 (g)
Na segunda etapa, o dióxido de enxofre reage com oxigênio para formar trióxido de
enxofre e, por fim, o trióxido de enxofre reage com água, dando origem ao ácido sulfúrico.
Sabendo que o minério de pirita apresenta 92% de pureza, calcule a massa aproximada
de dióxido de enxofre produzida a partir de 200 g de pirita.
Aula 02 – Cálculos das reações químicas 117
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
a) 213,7 g.
b) 196,5 g.
c) 512,8 g.
d) 17,1 g.
Comentários
Primeiramente, determina-se a quantidade da substância FeS2 (pura):
92
𝑚𝑎𝑠𝑠𝑎 = · 200 𝑔 = 184 𝑔 𝑑𝑒 𝐹𝑒𝑆2
100
Calcula-se a massa, em gramas, do dióxido de enxofre formado a partir do consumo total de
184 g de FeS2.
Proporção: 4 mol FeS2 → 8 mol SO2, sabendo que as massas molares do FeS2 e SO2 são iguais
a 120 g/mol e 64 g/mol.
4 · 120 𝑔 𝑑𝑒 𝐹𝑒𝑆2 − − − − 8 · 64 𝑔 𝑑𝑒 𝑆𝑂2
184 𝑔 𝑑𝑒 𝐹𝑒𝑆2 −−−− 𝑥 𝑔 𝑑𝑒 𝑆𝑂2
x = 196 g
Gabarito: B
42. (Fac. Israelita de C. da Saúde Albert Einstein SP/2017)
Um resíduo industrial é constituído por uma mistura de carbonato de cálcio (CaCO 3) e
sulfato de cálcio (CaSO4). O carbonato de cálcio sofre decomposição térmica se aquecido entre
825 e 900 °C, já o sulfato de cálcio é termicamente estável. A termólise do CaCO 3 resulta em
óxido de cálcio e gás carbônico.
CaCO3 (s) → CaO(s) + CO2(g)
Uma amostra de 10,00 g desse resíduo foi aquecida a 900 °C até não se observar mais
alteração em sua massa. Após o resfriamento da amostra, o sólido resultante apresentava 6,70
g.
O teor de carbonato de cálcio na amostra é de, aproximadamente,
a) 33%.
b) 50%.
c) 67%.
d) 75%.
Comentários
Dadas as massas molares: 100 g/mol CaCO3 e 44g/mol CO2.
Análise da massa sólida durante a transformação:
Aula 02 – Cálculos das reações químicas 118
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
massa inicial sólida: massa final sólida:
CaSO4 + CaCO3 = 10 g CaSO4 + CaO = 6,70 g
A partir da quantidade de CO2, determina-se a quantidade de CaCO3 que sofreu consumo:
Proporção, em mol, na reação: 1 mol CaCO3 → 1 mol CaO.
100 𝑔 𝑑𝑒 𝐶𝑎𝐶𝑂3 − − − − 44 𝑔 𝑑𝑒 𝐶𝑂2
𝑥 𝑔 𝑑𝑒 𝐶𝑎𝐶𝑂3 − − − − 3,30 𝑔 𝑑𝑒 𝐶𝑂2
x = 7,5 g de CaCO3
7,5 𝑔
%= · 100% = 75%
100 𝑔
Gabarito: D
43. (PUC Camp SP/2017)
Muitos resíduos industriais podem ser utilizados novamente no processo produtivo. Por
exemplo, resíduos de mármore possuem um potencial de uso nos processos de fabricação de
aços, devido à sua composição química, como mostra os resultados da análise desse material
(Disponível em: http://www.scielo.br)
Nesses processos, o CaCO3 calcinado produz o CaO, usado para a dessulfuração do ferro
gusa.
A massa, em kg, de CaO produzida quando se utiliza 1,0 kg de resíduos de mármore é de,
aproximadamente,
Dados:
Massas molares
Aula 02 – Cálculos das reações químicas 119
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
C = 12
O = 16
Ca = 40
a) 0,2.
b) 0,4.
c) 0,1.
d) 0,3.
e) 0,5.
Comentários
Dados: massas molares= CaCO3 100 g/mol e CaO = 56 g/mol.
Sabendo que o CaO é formado pela decomposição térmica do CaCO 3, calcula-se a massa do
óxido formado pelo consumo de 1 kg de mármore que apresenta 59,7% de pureza em carbonato de
cálcio.
1 kg de mármore = 1000 g · 0,597 = 597 g de CaCO3
A proporção em mol de CaCO3 e CO2 é extraído da equação:
CaCO3 → CaO + CO2
Proporção, em mol, na reação: 1 mol CaCO3 → 1 mol CaO
100 𝑔 𝑑𝑒 𝐶𝑎𝐶𝑂3 − − − − 56 𝑔 𝑑𝑒 𝐶𝑎𝑂
597 𝑔 𝑑𝑒 𝐶𝑎𝐶𝑂3 − − − − 𝑥 𝑔 𝑑𝑒 𝐶𝑎𝑂
x = 334,32 g = 0,3 kg de CaO
Gabarito: D
44. (ESCS DF/2015)
Em 2013, o comércio internacional de minério de ferro foi de 1,23 bilhão de toneladas,
dado que ilustra claramente o fenômeno da globalização. Nesse cenário, o Brasil ocupa posição
de destaque porque possui a segunda maior reserva do planeta, em termos de ferro contido no
minério. Os dois principais minérios encontrados no Brasil são a hematita (Fe2O3) e a magnetita
(Fe3O4). O ferro também é comumente encontrado na siderita (FeCO3).
Se, em determinado ano, o Brasil exportou 300 milhões de toneladas de minério de ferro,
sendo 60% de hematita e 40% de magnetita, então a massa de ferro, em milhões de toneladas,
contida no minério de ferro exportado foi
a) superior a 215.
b) inferior a 205.
c) superior 205 e inferior a 210.
d) superior a 210 e inferior a 215.
Aula 02 – Cálculos das reações químicas 120
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
Comentários
Dados: massas molares: 160 g/mol de Fe2O3, 232 g/mol de Fe3O4 e 56 g/mol de Fe.
A soma das massas do ferro é igual a 126 milhões + 86,88 milhões = 212,88 milhões de t
Gabarito: D
45. (Mackenzie SP/2018)
A partir de um minério denominado galena, rico em sulfeto de chumbo II (PbS), pode-se
obter o metal chumbo em escala industrial, por meio das reações representadas pelas equações
de oxirredução a seguir, cujos coeficientes estequiométricos encontram-se já ajustados:
3
PbS(s) + O2 (g) → PbO(s) + SO2 (g)
2
PbO(s) + CO(g) → Pb(s) + CO2 (g)
Considerando-se uma amostra de 717 kg desse minério que possua 90 % de sulfeto de
chumbo II, sendo submetida a um processo que apresente 80 % de rendimento global, a massa
a ser obtida de chumbo será de, aproximadamente,
Dados: massas molares (g·mol–1) S = 32 e Pb = 207
a) 621 kg.
b) 559 kg.
c) 447 kg.
d) 425 kg.
e) 382 kg.
Comentários
Somando as duas equações, tem-se a equação global:
3
PbS + O2 + CO → Pb + CO2 + SO2
2
Determinando a massa de sulfeto de chumbo II: 717 kg · 0,9 = 645,3 kg de PbS.
Aula 02 – Cálculos das reações químicas 121
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
Sabendo que somente 80 % do PbS será consumido: 645,3 kg · 0,8 = 516,24 kg de PbS reagirão.
Sabendo que as massas molares de Pb e PbS são iguais a 207 g/mol e 239 g/mol, calcula-se:
239 𝑔 𝑑𝑒 𝑃𝑏𝑆 − − − − 207 𝑔 𝑑𝑒 𝑃𝑏
516,24 𝑘𝑔 𝑑𝑒 𝑃𝑏𝑆 − − − − 𝑥 𝑘𝑔 𝑑𝑒 𝑃𝑏
x = 447,12 kg de Pb
Gabarito: C
46. (Mackenzie SP/2015)
Vazamento de gás provocou chuva ácida em Cubatão, diz Cetesb
A Companhia Ambiental do Estado de São Paulo (Cetesb) identificou emissão de dióxido
de enxofre (SO2) na atmosfera em Cubatão, após vazamento de uma fábrica de fertilizantes no
Polo Industrial. Segundo o órgão, com isso e com a umidade existente, devido às fortes chuvas,
além de outros compostos na atmosfera, é possível uma formação de vapor d’agua e gotículas
de ácido sulfúrico ou sulfuroso, conhecida popularmente como chuva ácida.
Em nota, a Cetesb informa que tal situação só aconteceu no período em que houve
corrente dos gases na atmosfera.
http://www.atribuna.com.br/cidades/cubat%C3%A3o/
vazamento-de-g%C3%A1sprovocou-chuva-%C3%A1cida-em-cubat%
C3%A3o-diz-cetesb-1.426246
Supondo-se que o volume de dióxido de enxofre, descarregado na atmosfera, tenha sido
de 1120 L, nas CNTP, a massa de ácido sulfuroso que foi produzida, por meio da reação
representada pela equação SO2 + H2O → H2SO3, considerando o rendimento do processo igual a
60%, é
Dado: massa molar (g.mol–1) H = 1, O = 16 e S = 32.
a) 1230 g.
b) 2460 g.
c) 4100 g.
d) 5000 g.
e) 8200 g.
Comentários
Volume molar nas CNTP: 22,4 L/mol.
Massa molar do H2SO3:
Sabendo que somente 60% da quantidade de dióxido de enxofre sofrerá consumo, então:
0,6·1120 L = 672 L de SO2
22,4 𝐿 𝑑𝑒 𝑆𝑂3 − − − − 82 𝑔 𝑑𝑒 𝐻2 𝑆𝑂3
672 𝐿 𝑑𝑒 𝑆𝑂3 − − − − 𝑥 𝑔 𝑑𝑒 𝐻2 𝑆𝑂3
x = 2460 g de H2SO3
Aula 02 – Cálculos das reações químicas 122
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
Gabarito: B
47. (UNICAMP SP/2018)
A calda bordalesa é uma das formulações mais antigas e mais eficazes que se conhece. Ela
foi descoberta na França no final do século XIX, quase por acaso, por um agricultor que aplicava
água de cal nos cachos de uva para evitar que fossem roubados; a cal promovia uma mudança
na aparência e no sabor das uvas. O agricultor logo percebeu que as plantas assim tratadas
estavam livres de antracnose. Estudando-se o caso, descobriu-se que o efeito estava associado
ao fato de a água de cal ter sido preparada em tachos de cobre. Atualmente, para preparar a
calda bordalesa, coloca-se o sulfato de cobre em um pano de algodão que é mergulhado em um
vasilhame plástico com água morna. Paralelamente, coloca-se cal em um balde e adiciona-se
água aos poucos. Após quatro horas, adiciona-se aos poucos, e mexendo sempre, a solução de
sulfato de cobre à água de cal.
(Adaptado de Gervásio Paulus, André Muller e Luiz Barcellos, Agroecologia aplicada:
práticas e métodos para uma agricultura de base ecológica.
Porto Alegre: EMATER-RS, 2000, p. 86.)
Na preparação da calda bordalesa são usados 100 g de sulfato de cobre(II) pentaidratado
e 100 g de hidróxido de cálcio (cal extinta). Para uma reação estequiométrica entre os íons cobre
e hidroxila, há um excesso de aproximadamente
a) 1,9 mol de hidroxila.
b) 2,3 mol de hidroxila.
c) 2,5 mol de cobre.
d) 3,4 mol de cobre.
Dados de massas molares em g.mol–1: sulfato de cobre (II) pentaidratado = 250;
hidróxido de cálcio = 74.
Comentários
CuSO4·5H2O + Ca(OH)2 → Cu(OH)2 + CaSO4 + 5 H2O
Determina-se o reagente em excesso, escolhendo um dos reagentes para testar:
250 𝑔 𝑑𝑒 𝑠𝑢𝑙𝑓𝑎𝑡𝑜 𝑝𝑒𝑛𝑡𝑎𝑖𝑑𝑟𝑎𝑡𝑎𝑑𝑜 − − − − 74 𝑔 𝑑𝑒 ℎ𝑖𝑑𝑟ó𝑥𝑖𝑑𝑜 𝑑𝑒 𝑐á𝑙𝑐𝑖𝑜
100 𝑔 𝑑𝑒 𝑠𝑢𝑙𝑓𝑎𝑡𝑜 𝑝𝑒𝑛𝑡𝑎𝑖𝑑𝑟𝑎𝑡𝑎𝑑𝑜 − − − − 𝑥 𝑔 𝑑𝑒 ℎ𝑖𝑑𝑟ó𝑥𝑖𝑑𝑜 𝑑𝑒 𝑐á𝑙𝑐𝑖𝑜
x = 29,6 g de sulfato de cálcio.
Assim, 29,6 g de ℎ𝑖𝑑𝑟ó𝑥𝑖𝑑𝑜 𝑑𝑒 𝑐á𝑙𝑐𝑖𝑜 serão consumidos na reação e restarão 70,4 g em
excesso.
74 𝑔 𝑑𝑒 𝐶𝑎 (𝑂𝐻 )2 − − − − 2 𝑚𝑜𝑙 𝑑𝑒 𝑂𝐻 −1
70,4 𝑔 𝑑𝑒 𝐶𝑎 (𝑂𝐻 )2 − − − − 𝑦 𝑚𝑜𝑙 𝑑𝑒 𝑂𝐻 −1
y = 1,9 mol de OH-
Gabarito: A
Aula 02 – Cálculos das reações químicas 123
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
15. Considerações Finais das Aulas
ACABAMOS MAIS UMA AULA!!! AEWW!!!!
Definitivamente, um dos capítulos mais importantes da Química Geral. Todos os vestibulares
apresentam questões desse tema. Essa aula é pré-requisito para toda a Físico-Química. Não deixe
de praticar.
Agora é respirar fundo e vamos para a próxima aula!
Are you ready?
16. Referências
Figura 1 – Unsplash. Disponível em https://unsplash.com/photos/KY6NHtBWJB8. Acesso em 18 de
fevereiro de 2019.
Figura 2 – Unsplash. Disponível em https://unsplash.com/photos/iKHXbvNHXPQ . Acesso em 18 de
fevereiro de 2019.
Figura 3 – Shutterstock. Disponível em
https://www.shutterstock.com/pt/download/confirm/567195634?size=medium_jpg . Acesso em
18 de fevereiro de 2019.
Figura 4 – Unsplash. Disponível em https://unsplash.com/photos/wYckK8YvwSM . Acesso em 19
de fevereiro de 2019.
Figura 5 – Wikipedia. Disponível em https://pt.wikipedia.org/wiki/Ficheiro:Kaarsvlam-kl.jpg .
Acesso em 18 de fevereiro de 2019.
Figura 6 – Unsplash. Disponível em https://unsplash.com/photos/NpIZhur97aA . Acesso em 18 de
fevereiro de 2019.
Figura 7 – Unsplash. Disponível em https://unsplash.com/photos/_gI_sP5K3Hc. Acesso em 09 de
março de 2019.
Figura 8 – Unsplash. Disponível em https://unsplash.com/photos/WvFn76kmdok . Acesso em 19
de fevereiro de 2019.
Figura 9 – Flickr. Disponível em
https://www.flickr.com/photos/damongman/6078862114/in/photolist-agaKVu-numHmD-p7n4uY-
7Fjzvg-efb85C-rhVqML-rhVoEu-ogC9WK-5kGcQB-rhVq6A-gyied3-2bhXgyM-U6uRQ3-4C1FWs-
4m7eMU-fdzhV-9co2Se-A8Ups-5k63xH-7ZPs8Y-r1rXSm-ebPc26-6ZNXgc-e97mbh-au3A1k-e97m3y-
djqCGH-e91Gj8-nZ9ryM-9t2e9h-ebURmJ-67Ts4Z-CELv4x-SqHwGJ-24UCvyN-eU36xp-e93exB-
ebUViC-S1kKA-iZM7oB-grEeDv-9t2e9b-73XfUA-21h3TZo-7tfxr6-dcM3mS-7R4n4K-e98LYW-e91Gtk-
6dVopB . Acesso em 19 de fevereiro de 2019.
Figura 10 – Pixabay. Disponível em https://pixabay.com/pt/diamante-brilhante-gema-j%C3%B3ia-
nobre-1186139/ e disponível em https://pixabay.com/pt/anel-ouro-terra-m%C3%A9dia-anel-de-
ouro-1692713/ . Acesso em 19 de fevereiro de 2019.
Aula 02 – Cálculos das reações químicas 124
www.estrategiavestibulares.com.br
125
Professor Prazeres
Aula 02: Fuvest Medicina 2021
Figura 11 – simplyme-nodoubt. Disponível em http://simplyme-
nodoubt.blogspot.com/2012/04/worlds-first-all-diamond-ring-by.html . Acesso em 19 de fevereiro
de 2019.
Bibliografia
Disponível em: http://www.ufjf.br/quimicaead/files/2013/05/8-Espectrometria-de-massa.pdf
Acesso em 19 de fevereiro de 2019.
Folha de versão
12/12/2019 – versão 1
23/03/2020 – versão 2
- Atualização da resolução da Questão da UFAM da página 30.
Aula 02 – Cálculos das reações químicas 125
www.estrategiavestibulares.com.br
125
Você também pode gostar
- Lista 04.2Documento3 páginasLista 04.2CheilaSilvaAinda não há avaliações
- LMC 1a 2a 3a UnidadeDocumento53 páginasLMC 1a 2a 3a UnidadeGabriella Colaço Correia100% (1)
- Apostila Quimica Quantica V3Documento125 páginasApostila Quimica Quantica V3Rapha De Moraes0% (1)
- Transmissão de Calor em AglomeradosDocumento31 páginasTransmissão de Calor em AglomeradosmarceloAinda não há avaliações
- Ensaio Motor Assíncrono TrifásicoDocumento8 páginasEnsaio Motor Assíncrono TrifásicomiguelAinda não há avaliações
- Relatório Aula 2Documento5 páginasRelatório Aula 2Hana PradoAinda não há avaliações
- Estudo Das Reações Químicas PDFDocumento5 páginasEstudo Das Reações Químicas PDFJacinto CezarAinda não há avaliações
- Medição elétrica com multímetroDocumento6 páginasMedição elétrica com multímetroSétima Eng. AmbientalAinda não há avaliações
- AL2.3-Comunicações Por Radiação ElectromagnéticaDocumento3 páginasAL2.3-Comunicações Por Radiação Electromagnéticafqa11esqf6682Ainda não há avaliações
- Lei de Ohm comprovada em experimento de laboratórioDocumento5 páginasLei de Ohm comprovada em experimento de laboratórioEliomar ResplandisAinda não há avaliações
- Relatório de Laboratório de Química - Densidade de Sólidos e LiquídosDocumento11 páginasRelatório de Laboratório de Química - Densidade de Sólidos e LiquídosVitória Cintra PintorAinda não há avaliações
- Relatório 2 - Queda LivreDocumento20 páginasRelatório 2 - Queda LivreJeferson CaioAinda não há avaliações
- Cinética Química: Fatores que Influenciam a Velocidade de uma ReaçãoDocumento3 páginasCinética Química: Fatores que Influenciam a Velocidade de uma ReaçãoMaria MarquesAinda não há avaliações
- Variação de temperatura em reações químicasDocumento12 páginasVariação de temperatura em reações químicasLucas CAinda não há avaliações
- Energia Elétrica e CircuitosDocumento157 páginasEnergia Elétrica e CircuitosMarta SousaAinda não há avaliações
- Relatório PMTDocumento33 páginasRelatório PMTSerginho VieiraAinda não há avaliações
- Apostila Lab de Física Geral II IFSC USP 2018Documento121 páginasApostila Lab de Física Geral II IFSC USP 2018Rodrigo Rosatelli AndradeAinda não há avaliações
- Avaliação de Física e Química sobre Reações QuímicasDocumento3 páginasAvaliação de Física e Química sobre Reações QuímicasIara Penha RibeiroAinda não há avaliações
- Livro de Eletricidade e Magnetismo Livro 1 PDFDocumento242 páginasLivro de Eletricidade e Magnetismo Livro 1 PDFRenan OrleansAinda não há avaliações
- FQ Avaliação Sumativa Módulo Q4Documento6 páginasFQ Avaliação Sumativa Módulo Q4GetlowAinda não há avaliações
- Lei de Ohm experimentalDocumento7 páginasLei de Ohm experimentalNicholas OliveiraAinda não há avaliações
- Processos de fabricação de âncoras por fundição e forjamentoDocumento9 páginasProcessos de fabricação de âncoras por fundição e forjamentoEvandro Machado100% (1)
- Resistência dos materiais - Ensaios de traçãoDocumento15 páginasResistência dos materiais - Ensaios de traçãoVictor Lopes MirandaAinda não há avaliações
- Relatório de Física III - Experimento 3Documento10 páginasRelatório de Física III - Experimento 3adriolibahAinda não há avaliações
- Unidade II - Átomos, Moléculas e ÍonsDocumento4 páginasUnidade II - Átomos, Moléculas e ÍonsMatheus EduardoAinda não há avaliações
- Analise Do VinagreDocumento18 páginasAnalise Do VinagreMauroArantes100% (1)
- Magnético: Estudo do campo magnético de ímãsDocumento22 páginasMagnético: Estudo do campo magnético de ímãsEduardo OliveiraAinda não há avaliações
- Revisao f1Documento4 páginasRevisao f1Elisangela AmorimAinda não há avaliações
- Ficha de Exercicios 1Documento4 páginasFicha de Exercicios 1Manuela SofiaAinda não há avaliações
- Fenômenos de transporte PUC MinasDocumento10 páginasFenômenos de transporte PUC MinasCristian B.Ainda não há avaliações
- 2018 Qui126 Aula 5 Modelo Atômico de BohrDocumento9 páginas2018 Qui126 Aula 5 Modelo Atômico de BohrPedro Henrique AlmeidaAinda não há avaliações
- 275 PDFDocumento36 páginas275 PDFDias ManuelAinda não há avaliações
- Relatorio Lei de Kirchhoff Das CorrentesDocumento2 páginasRelatorio Lei de Kirchhoff Das CorrentesGabocAinda não há avaliações
- Aula 2 Estrutura Atômica e Ligação InteratômicaDocumento10 páginasAula 2 Estrutura Atômica e Ligação InteratômicaMatheus MoraesAinda não há avaliações
- Ciência dos Materiais Estrutura AtômicaDocumento42 páginasCiência dos Materiais Estrutura AtômicaFernando MarquesAinda não há avaliações
- Lista de exercícios de mecânica dos sólidos sobre reações de apoioDocumento11 páginasLista de exercícios de mecânica dos sólidos sobre reações de apoioXimbikaModasXimbikinhaModasAinda não há avaliações
- Momento de inércia e centróide de figuras planasDocumento27 páginasMomento de inércia e centróide de figuras planasRodrigues100% (1)
- Apostila Oficial Engenharia Quimica GeralDocumento93 páginasApostila Oficial Engenharia Quimica GeralClaudenor PiedadeAinda não há avaliações
- Relatório Da Prática Do Laboratório - Resistores e OhmímetroDocumento15 páginasRelatório Da Prática Do Laboratório - Resistores e OhmímetroRocky0% (1)
- Força eletromotriz e eficiência de fontesDocumento11 páginasForça eletromotriz e eficiência de fontesKEZIA NEGRAO DA COSTA PINHEIROAinda não há avaliações
- Dinâmica de rotação de corpos rígidosDocumento5 páginasDinâmica de rotação de corpos rígidosArthur Silva100% (1)
- Gases Ideais PDFDocumento26 páginasGases Ideais PDFGuilhermeMachado_54Ainda não há avaliações
- Análise da cinética química de reaçõesDocumento2 páginasAnálise da cinética química de reaçõesAlter EgoAinda não há avaliações
- Volume e número de moléculas em gotas de águaDocumento3 páginasVolume e número de moléculas em gotas de águaSónia FariaAinda não há avaliações
- Al 1.1.queda Livre 2013Documento1 páginaAl 1.1.queda Livre 2013Sofia SilvaAinda não há avaliações
- Equilibrio Quimico - Parte 1Documento28 páginasEquilibrio Quimico - Parte 1Maria Luísa M. LiraAinda não há avaliações
- Relatório FQDocumento5 páginasRelatório FQMaria AlmeidaAinda não há avaliações
- Relatório Resistência e ResistividadeDocumento16 páginasRelatório Resistência e ResistividadeVictor SaidAinda não há avaliações
- Reações Químicas: Tipos e ExemplosDocumento11 páginasReações Químicas: Tipos e ExemplosRafael ErdmannAinda não há avaliações
- Efeito PH Cromato-DicromatoDocumento19 páginasEfeito PH Cromato-DicromatoZëky NhächëngöAinda não há avaliações
- Relatório 1 - DensidadeDocumento11 páginasRelatório 1 - DensidadeTayane GaruzziAinda não há avaliações
- Lei de Ohm - Resistência ElétricaDocumento11 páginasLei de Ohm - Resistência Elétricajulio100% (1)
- Física Nuclear - Teste 2Documento7 páginasFísica Nuclear - Teste 2Denny FranciscoAinda não há avaliações
- Simulado AV1 - Física Teórica e Experimental III - 2019.2Documento3 páginasSimulado AV1 - Física Teórica e Experimental III - 2019.2Christiane BarbosaAinda não há avaliações
- Electricidade Geral 1o Semestre 2019Documento123 páginasElectricidade Geral 1o Semestre 2019Abreu Miguel Liliano LilianoAinda não há avaliações
- Física I - Questões de mola, queda livre, força centrífuga e atritoDocumento3 páginasFísica I - Questões de mola, queda livre, força centrífuga e atritoCheilaSilvaAinda não há avaliações
- Teste Texto Editora - 2018Documento4 páginasTeste Texto Editora - 2018Luis VarelaAinda não há avaliações
- Teste - Global Quimica 11Documento10 páginasTeste - Global Quimica 11Juliana NóbregaAinda não há avaliações
- Relatório Equilíbrio QuímicoDocumento8 páginasRelatório Equilíbrio QuímicoIan BarretoAinda não há avaliações
- Lavoisier e Proust: Leis da conservação de massa e proporções constantesDocumento10 páginasLavoisier e Proust: Leis da conservação de massa e proporções constantesjonatas duarteAinda não há avaliações
- Balanço material indústriaDocumento37 páginasBalanço material indústriaAmorimdbAinda não há avaliações
- 300 Anos de Lomonosov PDFDocumento24 páginas300 Anos de Lomonosov PDFIndi Assis RodriguesAinda não há avaliações
- Calculos QuimicosDocumento13 páginasCalculos QuimicosLaudyson J B AraújoAinda não há avaliações
- Wa0199.Documento3 páginasWa0199.Ana Júlia OliveiraAinda não há avaliações
- Transformações Químicas e Leis PonderaisDocumento4 páginasTransformações Químicas e Leis PonderaisMoema LimaAinda não há avaliações
- Lei de Lavoisier e conservação da massa em reações químicasDocumento2 páginasLei de Lavoisier e conservação da massa em reações químicasWendell HenriqueAinda não há avaliações
- Ficha Acerto Equacoes QuimicasDocumento3 páginasFicha Acerto Equacoes QuimicasClaudia Resende100% (2)
- Exp8 - PPT - 06 Lei Da Conservação Da MassaDocumento19 páginasExp8 - PPT - 06 Lei Da Conservação Da MassaMariana RosadoAinda não há avaliações
- Reações Química-1 - Ano.Documento6 páginasReações Química-1 - Ano.Nykholle B. Almeida100% (1)
- Aula 11 - 9º CN - Aspectos Quantitativos Das Transformações QuímicasDocumento4 páginasAula 11 - 9º CN - Aspectos Quantitativos Das Transformações Químicasquero maisAinda não há avaliações
- Leis PonderaisDocumento14 páginasLeis PonderaisJorge Henrique DiasAinda não há avaliações
- Exp8 03 Teste Aval 1 Crit ClassDocumento3 páginasExp8 03 Teste Aval 1 Crit ClassSEAinda não há avaliações
- QUÍMICA GERALDocumento3 páginasQUÍMICA GERALMatheus De Araujo SilvaAinda não há avaliações
- Pregação - Deus Tudo Faz Por Nós - Is 64-4Documento2 páginasPregação - Deus Tudo Faz Por Nós - Is 64-4Daniel Deusdete100% (3)
- Miolo EQG Vol1Documento272 páginasMiolo EQG Vol1DaniloGomesAinda não há avaliações
- Prova SesiDocumento12 páginasProva SesiJaildo SilvaAinda não há avaliações
- Balanço de massa e energiaDocumento40 páginasBalanço de massa e energiaAnedito ArmandoAinda não há avaliações
- Aula - Lei Da Conservação de Massas PDFDocumento2 páginasAula - Lei Da Conservação de Massas PDFGeovane Silva CostaAinda não há avaliações
- EstequiometriaDocumento17 páginasEstequiometriaMaria BiaAinda não há avaliações
- Avaliação Diagnótica 2º Ano OficialDocumento3 páginasAvaliação Diagnótica 2º Ano OficialAmanda BarcelosAinda não há avaliações
- Análise Processos Físico-QuímicosDocumento44 páginasAnálise Processos Físico-QuímicosCinthia MoraesAinda não há avaliações
- GabaritoDocumento2 páginasGabaritoRoberto NeivaAinda não há avaliações
- Lavoisier!2Documento23 páginasLavoisier!2Paola Oliveira0% (1)
- Filo SofiaDocumento30 páginasFilo SofiaregianeAinda não há avaliações
- As leis das combinações químicasDocumento5 páginasAs leis das combinações químicassamuel souzaAinda não há avaliações
- Antoine Lavoisier - Pai Da QuímicaDocumento11 páginasAntoine Lavoisier - Pai Da QuímicalojaserafimoficialAinda não há avaliações
- 1° Atividade Quimica - LEIS PONDERAISDocumento2 páginas1° Atividade Quimica - LEIS PONDERAISGabriela SantosAinda não há avaliações
- Leis das combinações químicasDocumento30 páginasLeis das combinações químicasjparatyAinda não há avaliações