Escolar Documentos
Profissional Documentos
Cultura Documentos
Atividade de Cinética I - 2 Ano
Enviado por
Elany Pereira0 notas0% acharam este documento útil (0 voto)
4 visualizações2 páginasTítulo original
Atividade de Cinética i - 2 Ano
Direitos autorais
© © All Rights Reserved
Formatos disponíveis
PDF, TXT ou leia online no Scribd
Compartilhar este documento
Compartilhar ou incorporar documento
Você considera este documento útil?
Este conteúdo é inapropriado?
Denunciar este documentoDireitos autorais:
© All Rights Reserved
Formatos disponíveis
Baixe no formato PDF, TXT ou leia online no Scribd
0 notas0% acharam este documento útil (0 voto)
4 visualizações2 páginasAtividade de Cinética I - 2 Ano
Enviado por
Elany PereiraDireitos autorais:
© All Rights Reserved
Formatos disponíveis
Baixe no formato PDF, TXT ou leia online no Scribd
Você está na página 1de 2
ATIVIDADE 01 CINÉTICA QUÍMICA - 2º
06- (PUC-RS) Relacione os fenômenos descritos na coluna I com
ANOS os fatores que influenciam sua velocidade mencionados na coluna
01- Sobre os fatores que influenciam a velocidade de uma reação II.
química é INCORRETO afirmar que: Coluna I
a) Quanto maior a concentração dos reagentes, maior a velocidade 1 - Queimadas alastrando-se rapidamente quando está ventando;
da reação. 2 - Conservação dos alimentos no refrigerador;
b) Quanto maior a superfície de contato, maior a velocidade da 3 - Efervescência da água oxigenada na higiene de ferimentos;
reação. 4 - Lascas de madeiras queimando mais rapidamente que uma tora
c) Quanto maior a pressão, maior a velocidade da reação. de madeira.
d) Quanto maior a temperatura, maior a velocidade da reação. Coluna II
e) A presença de um catalisador mantém constante a velocidade da A - superfície de contato
reação. B - catalisador
C - concentração
02- Segundo a _____________ devem ocorrer colisões efetivas D – temperatura
entre os reagentes para a formação dos produtos. Além disso, A alternativa que contém a associação correta entre as duas
existe uma ___________ suficiente para romper as ligações colunas é
químicas dos reagentes e formar um ___________, que é um a) 1 - C; 2 - D; 3 - B; 4 – A.
estado intermediário antes da formação dos produtos. b) 1 - D; 2 - C; 3 - B; 4 – A.
As palavras que preenchem corretamente as lacunas são, c) 1 - A; 2 - B; 3 - C; 4 – D.
respectivamente: d) 1 - B; 2 - C; 3 - D; 4 – A.
a) variação de entalpia, energia cinética e catalisador. e) 1 - C; 2 - D; 3 - A; 4 – B.
b) teoria das colisões, energia de ativação e complexo ativado.
c) velocidade da reação, entalpia e inibidor. 07- (UnB-DF) Considere os estudos cinéticos de uma reação
d) pressão parcial, entropia e substrato. química e julgue os itens abaixo como V verdadeiro e F falso:
( ) Toda reação é produzida por colisões, mas nem toda colisão
03- Sobre os catalisadores são feitas as quatro afirmações gera uma reação.
seguintes: ( ) Uma colisão altamente energética pode produzir uma reação.
I. Um catalisador atua aumentado a velocidade de uma reação, mas ( ) Toda colisão com orientação adequada produz uma reação.
não altera seu rendimento. ( ) A energia mínima para uma colisão efetiva é denominada
II. Em uma reação química o catalisador não é consumido no energia da reação.
caminho da reação. ( ) A diferença energética entre produtos e reagentes é denominada
III. Os catalisadores criam uma rota alternativa de transformação energia de ativação da reação.
de reagentes em produtos. Para isso, uma maior energia de
ativação é necessária. 08- Indique a afirmação incorreta:
IV. O catalisador só é capaz de aumentar a velocidade da reação a) Quanto menor for à temperatura, maior será a velocidade de
no sentido direto. uma reação.
As opções que apresentam informações corretas sobre os b) O aumento da temperatura aumenta a velocidade tanto da
catalisadores são: reação endotérmica quanto da reação exotérmica.
a) I e II b) II e III c) I e IV d) Todas c) A velocidade de um reagente no estado sólido é menor que no
estado líquido.
04- A rapidez com que ocorre uma reação química depende de: d) A diferença energética entre os produtos e os reagentes é
I. Número de colisões efetivas entre os reagentes. chamada de entalpia de reação.
II. Energia suficiente para promover o rearranjo dos átomos. e) A velocidade de uma reação depende da natureza do reagente.
III. Orientação favorável das moléculas.
IV. Formação de um complexo ativado. 09- Assinale a alternativa que apresenta agentes que tendem a
a) I e II b) II e IV c) I, II e III d) I, II, III e IV. aumentar a velocidade de uma reação:
a) calor, obscuridade, catalisador.
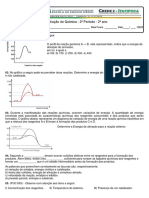
05- Observe a representação gráfica do desenvolvimento de uma b) calor, maior superfície de contato entre reagentes, ausência de
reação química hipotética, que relaciona a energia e o caminho catalisador.
reacional. c) calor, maior superfície de contato entre reagentes, catalisador.
d) frio, obscuridade, ausência de catalisador.
e) catalisador e congelamento dos reagentes.
10- (UFMG) Dois recipientes contêm a mesma quantidade de
H2SO4. No sistema I, coloca-se uma mola de ferro comprimida, no
sistema II, outra mola, idêntica à primeira, mas não comprimida.
Ambas são corroídas pelo ácido. Sobre esses sistemas, a afirmativa
CORRETA é:
a) O sistema I, no estado final, terá mais ligações químicas do que
o sistema II.
b) As espécies químicas do sistema I ficam mais aglomeradas do
que as do sistema II.
Assinale a alternativa que substitui corretamente (1), (2), (3) e (4), c) A temperatura final do sistema I é mais alta do que a do sistema
respectivamente. II.
a) substratos, calor liberado, estado máximo de energia e final da d) O rendimento da reação do sistema I é mais alto do que o do
reação. sistema II.
b) reagentes, energia de ativação, complexo ativado e produtos. e) A concentração final da solução do sistema I é maior do que a
c) reagentes, energia cinética, catalisador e substratos. do sistema II.
d) reagentes, calor absorvido, energia térmica e produtos.
11- Um químico realizou em laboratório alguns experimentos com
o intuito de observar a velocidade em que uma solução aquosa do
ácido HBr reagia com o magnésio metálico. Para isso, foram
contadas, durante 20 segundos, as bolhas referentes à produção de
gás hidrogênio logo após os reagentes serem misturados. Na
execução dos experimentos, foi utilizado o mesmo material
metálico (magnésio), o mesmo volume de uma solução de HBr e a
mesma massa do metal magnésio. Os critérios que sofreram
alteração ao longo do experimento foram a forma de apresentação
do magnésio (barra ou pedaços pequenos) e a temperatura. A
tabela abaixo indica todas as condições utilizadas em cada
experimento:
a) 25 b) 85 c) 110 d) 6 e) 40
16- Observe o gráfico e assinale a alternativa correta.
Assinale a alternativa que apresenta os experimentos na ordem
crescente do número de bolhas observado.
a) B, A, C b) C, B, A c) A, B, C d) B, C, A e) nda.
12- A sabedoria popular indica que, para cozinhar batatas, é
indicado cortá-las em pedaços. Em condições reacionais idênticas
e utilizando massas iguais de batata, mas algumas inteiras e outras
cortadas verifica-se que a cortada cozinha em maior velocidade. O
fator determinante para essa maior velocidade da reação é o
aumento da:
a) pressão b) temperatura c) concentração
d) superfície de contato e) natureza dos reagentes
13- (ACAFE-SC) O conhecimento da velocidade das reações
químicas é de extrema importância para a produção industrial de
uma série de produtos. Analise as afirmações a seguir.
I. A velocidade de uma reação química geralmente cresce com o
aumento da temperatura. a) 42 kcal é a energia liberada na reação: z → x + y
II. A velocidade de uma reação química sempre independe da b) 30 kcal é a energia do complexo ativado.
concentração dos reagentes. c) 12 kcal é a energia absorvida na reação: x + y → z
III. A velocidade de uma reação química depende da orientação d) 32 kcal é a energia de ativação para a reação: x + y → z
apropriada das moléculas na hora do choque.
IV. Para os sólidos, quanto maior a superfície de contato, menor 17- Analisando o gráfico representativo do caminho da reação A +
será a velocidade da reação química. B → C, pode-se dizer que o valor da energia de ativação, em
Assinale a alternativa que indica somente as afirmações corretas. kcal/mol, e o tipo de reação são, respectivamente:
a) II – III b) I – IV c) II – IV d) I – II e) I – II
14-. (UFRGS) Observe o gráfico a seguir.
O perfil da reação genérica A → B, nele representado, indica que a a) 8 e exotérmica.
energia de ativação do processo, em kJ, é igual a b) 10 e endotérmica.
a) 100. b) 150. c) 250. d) 300. e) 400. c) 20 e exotérmica.
d) 28 e endotérmica.
15- No diagrama abaixo, o valor da energia de ativação e) 30 e endotérmica.
correspondente em (Kcal):
Você também pode gostar
- Apostila Química Orgânica: Carbono, Dienos E AromáticosNo EverandApostila Química Orgânica: Carbono, Dienos E AromáticosAinda não há avaliações
- Atv - Cinética QuímicaDocumento3 páginasAtv - Cinética Químicamourabraga09Ainda não há avaliações
- Química 2cDocumento2 páginasQuímica 2cmanuelaescola295Ainda não há avaliações
- Exercicio Teórico de Cinética QuímicaDocumento4 páginasExercicio Teórico de Cinética Químicacapudinho004Ainda não há avaliações
- Lista Cionetica TecnicoDocumento2 páginasLista Cionetica TecnicoLivia FerreiraAinda não há avaliações
- Qui MicaDocumento8 páginasQui Micamaria.hsvh0Ainda não há avaliações
- CINÉTICADocumento7 páginasCINÉTICAVaneilton ReynaudAinda não há avaliações
- Lista de Termoquímica e Cinética - 2º AnoDocumento24 páginasLista de Termoquímica e Cinética - 2º AnoFernanda BarretoAinda não há avaliações
- AVALIAÇÃO - Cinetica - 2º AnoDocumento3 páginasAVALIAÇÃO - Cinetica - 2º AnoLaiane AmericoAinda não há avaliações
- Lista de Exercícios Sobre A Velocidade Das Reações QuímicasDocumento1 páginaLista de Exercícios Sobre A Velocidade Das Reações QuímicasJoalson eng ArliAinda não há avaliações
- Av 4º B 2º Ano QuímicaDocumento4 páginasAv 4º B 2º Ano QuímicaJulioAinda não há avaliações
- Fatores Que Alteram A Velocidade Das Reações QuímicasDocumento3 páginasFatores Que Alteram A Velocidade Das Reações QuímicasGiovani AraújoAinda não há avaliações
- 4 Avaliação (Turma 2T4) - MBDocumento2 páginas4 Avaliação (Turma 2T4) - MBPaula FerreiraAinda não há avaliações
- Cinetica QuimicaDocumento2 páginasCinetica QuimicaCMJ O caderno mágico do JamesAinda não há avaliações
- Ficha 12Documento9 páginasFicha 12Gustavo FernandoAinda não há avaliações
- Lista Cinética (Monitoria)Documento4 páginasLista Cinética (Monitoria)Raineldes CruzAinda não há avaliações
- 2017 - 1a - 2 - Físico-Química PDFDocumento3 páginas2017 - 1a - 2 - Físico-Química PDFEdgar GóesAinda não há avaliações
- Ficha de Exercicios de Preparacao-1Documento27 páginasFicha de Exercicios de Preparacao-1Damião JeremiasAinda não há avaliações
- Lista Da Aula 3 - Cinética QuímicaDocumento5 páginasLista Da Aula 3 - Cinética QuímicaE P Som RJAinda não há avaliações
- Estudo Dirigido Provão 4º BimestreDocumento5 páginasEstudo Dirigido Provão 4º BimestreJerusaFreitasAinda não há avaliações
- Prof. Rafa - Química - Cinética Química - Prova P2 - 1 BimDocumento3 páginasProf. Rafa - Química - Cinética Química - Prova P2 - 1 BimRafael VaristeloAinda não há avaliações
- Lista de Exercícios Cinética QuimicaDocumento7 páginasLista de Exercícios Cinética Quimicatrilha AAinda não há avaliações
- Atividade Formativa - Equilibrio e Movimento - 2º EM - Semana 07 - Prof Valdir - 114122Documento3 páginasAtividade Formativa - Equilibrio e Movimento - 2º EM - Semana 07 - Prof Valdir - 114122Julia SeixasAinda não há avaliações
- 2021 PV Qui4 L3 ResDocumento9 páginas2021 PV Qui4 L3 Reslidiacarolineferreira.silva2Ainda não há avaliações
- Atividade de Revisão 2 Série Quimica 4º BimestreDocumento6 páginasAtividade de Revisão 2 Série Quimica 4º BimestreElvandira NapoleãoAinda não há avaliações
- Avaliação de QuímicaDocumento4 páginasAvaliação de QuímicaKleto JknAinda não há avaliações
- Exercicios Cinetica Com RespostasDocumento4 páginasExercicios Cinetica Com Respostasgabrielcosta124loudAinda não há avaliações
- Exerc - Fatores Que Interferem Na VelocidadeDocumento2 páginasExerc - Fatores Que Interferem Na VelocidadeGa GagoAinda não há avaliações
- Qui MicaDocumento6 páginasQui MicaIanne PinhoAinda não há avaliações
- Lista 08 - Fatores Que Alteram A VelocidadeDocumento10 páginasLista 08 - Fatores Que Alteram A VelocidadevagnererenataAinda não há avaliações
- 2º Ano - Avaliação - Quimica - 08-07-2021 - JulhoDocumento3 páginas2º Ano - Avaliação - Quimica - 08-07-2021 - JulhoSelma Eliane Quatroque TavaresAinda não há avaliações
- Lista de Exercícios I (2º Bimestre) - 3º AnoDocumento3 páginasLista de Exercícios I (2º Bimestre) - 3º AnoMikeas LimaAinda não há avaliações
- Lista de Exercícios Sobre Cinética QuímicaDocumento3 páginasLista de Exercícios Sobre Cinética Químicalayse vitóriaAinda não há avaliações
- Cinetica Quimica 21 Questoes Com GabaritoDocumento6 páginasCinetica Quimica 21 Questoes Com GabaritoCíntia GhettiAinda não há avaliações
- Prova de Fisico Química 2 AnoDocumento7 páginasProva de Fisico Química 2 AnoProf. Marcelo França PinheiroAinda não há avaliações
- Atividade 05 PDFDocumento4 páginasAtividade 05 PDFCassio RezendeAinda não há avaliações
- Lista de Exercícios de Fixação Cinética QuímicaDocumento5 páginasLista de Exercícios de Fixação Cinética Químicabruno.amarques05Ainda não há avaliações
- Avaliação Quimica 2ºano OutubroDocumento2 páginasAvaliação Quimica 2ºano OutubroLaércio souzaAinda não há avaliações
- Exercícios CinéticaDocumento2 páginasExercícios CinéticaYory PereiraAinda não há avaliações
- CINÉTICA2Documento7 páginasCINÉTICA2WeberBraganteAinda não há avaliações
- 2 Ano Atividade Fatores Aurélio Buarque de HolandaDocumento2 páginas2 Ano Atividade Fatores Aurélio Buarque de HolandaCelicris DiasAinda não há avaliações
- Aula 09.1 - Lista de Exercícios Fatores Que Influenciam Na Velocidade Da ReaçãoDocumento4 páginasAula 09.1 - Lista de Exercícios Fatores Que Influenciam Na Velocidade Da ReaçãoRosah Gabryellyh100% (1)
- Cinetica 04Documento2 páginasCinetica 04Sandro BaldezAinda não há avaliações
- Estudo Dirigido de Química - Ceja - Fascículo 5 (Unidades 11, 12 e 13) .Documento4 páginasEstudo Dirigido de Química - Ceja - Fascículo 5 (Unidades 11, 12 e 13) .falecomarilsonAinda não há avaliações
- Cinetqui 001Documento31 páginasCinetqui 001Anonymous QMpWb7Vc3XAinda não há avaliações
- 20 - 21 - Cinetica QuimicaDocumento9 páginas20 - 21 - Cinetica QuimicaPauloMesquitaAinda não há avaliações
- Cinética Química 2 OkDocumento3 páginasCinética Química 2 OkIbrahim AlhannaAinda não há avaliações
- Atividade Extra - Episódio 11 - Cinética QuímicaDocumento9 páginasAtividade Extra - Episódio 11 - Cinética QuímicaGabriel BoaventuraAinda não há avaliações
- 48 20cin C3 A9tica 20qu C3 ADmicaDocumento14 páginas48 20cin C3 A9tica 20qu C3 ADmicaFrancis Francisco Johane SemanaAinda não há avaliações
- FQ Cap3Documento6 páginasFQ Cap3filipelima.graveAinda não há avaliações
- Cinética Química - Lista 02Documento3 páginasCinética Química - Lista 02Thays Schwambach GaiotiAinda não há avaliações
- Lista de Cinética IIDocumento4 páginasLista de Cinética IIRtyu IuytAinda não há avaliações
- Exercicios de Cinetica QuimicaDocumento21 páginasExercicios de Cinetica QuimicaThiago SáAinda não há avaliações
- Cinetica ExerciciosDocumento2 páginasCinetica ExercicioscarlostucupiAinda não há avaliações
- Aula de Cinética QuímicaDocumento22 páginasAula de Cinética QuímicaLucasAinda não há avaliações
- Lista de Cinética Sem RespostaDocumento13 páginasLista de Cinética Sem RespostaLuiz Filipe Oliveira Mansão LuizAinda não há avaliações
- Qui, Ica EliDocumento2 páginasQui, Ica EliPedro MartellAinda não há avaliações
- Cinetica Quimica UniDocumento6 páginasCinetica Quimica UnicarlostucupiAinda não há avaliações
- Estudo Dirigido A - M2Documento8 páginasEstudo Dirigido A - M2lpraxedesAinda não há avaliações
- Cinetica - Fatores Que Alteram A Velocidade - 20220215124854 - U2FsdDocumento7 páginasCinetica - Fatores Que Alteram A Velocidade - 20220215124854 - U2FsdJoao MaiaAinda não há avaliações
- GenéticaDocumento19 páginasGenéticaElany PereiraAinda não há avaliações
- Revisão Da Avaliação Parcial 4º PeríodoDocumento3 páginasRevisão Da Avaliação Parcial 4º PeríodoElany PereiraAinda não há avaliações
- Saber 18 - Português IIDocumento34 páginasSaber 18 - Português IIElany PereiraAinda não há avaliações
- Exercício - Docx 2º Anos IIDocumento3 páginasExercício - Docx 2º Anos IIElany PereiraAinda não há avaliações
- Redes de Computadores - Slide 5 - Modelo Osi 1Documento11 páginasRedes de Computadores - Slide 5 - Modelo Osi 1Elany PereiraAinda não há avaliações
- Segurança Da Redes de Computadores Slide - 04 - RevDocumento11 páginasSegurança Da Redes de Computadores Slide - 04 - RevElany PereiraAinda não há avaliações
- Saber 06Documento32 páginasSaber 06Elany PereiraAinda não há avaliações
- Relações Ecologicas: Lucilene CarvalhoDocumento21 páginasRelações Ecologicas: Lucilene CarvalhoElany PereiraAinda não há avaliações
- Virus e VirosesDocumento50 páginasVirus e VirosesIndira CarvalhoAinda não há avaliações
- Exercício - Docx 2º Anos IIDocumento3 páginasExercício - Docx 2º Anos IIElany PereiraAinda não há avaliações
- Massas Moleculares: Cálculos QuímicosDocumento17 páginasMassas Moleculares: Cálculos QuímicosElany PereiraAinda não há avaliações
- Tipos de Biomas No Brasil: Bioma Amazônia Bioma Cerrado Bioma Caatinga Bioma Mata Atlântica Bioma Pantanal Bioma PampaDocumento2 páginasTipos de Biomas No Brasil: Bioma Amazônia Bioma Cerrado Bioma Caatinga Bioma Mata Atlântica Bioma Pantanal Bioma PampaElany PereiraAinda não há avaliações
- 2º Anos - Revisão de Filosofia - 1º Bimestre de 2023Documento1 página2º Anos - Revisão de Filosofia - 1º Bimestre de 2023Elany PereiraAinda não há avaliações
- Catálogo de Bombas de Engrenagem - FBIDocumento16 páginasCatálogo de Bombas de Engrenagem - FBInrogernAinda não há avaliações
- AglomeranteDocumento272 páginasAglomeranteelisa120Ainda não há avaliações
- Tecnolita - Espec Primer PP EP5Documento1 páginaTecnolita - Espec Primer PP EP5Douglas TondelloAinda não há avaliações
- Tecnologia de Aplicação de Defensivos - UNESPDocumento28 páginasTecnologia de Aplicação de Defensivos - UNESPsartooriAinda não há avaliações
- Bomba CentrifugaDocumento18 páginasBomba CentrifugaMichael CamargoAinda não há avaliações
- Relatório 10 - Determinação de Água de Critalização Por Gravimetria de VolatilizaçãoDocumento5 páginasRelatório 10 - Determinação de Água de Critalização Por Gravimetria de VolatilizaçãoandresaAinda não há avaliações
- Discussão e Resultados de Experimentos TBQ LaboratorioDocumento20 páginasDiscussão e Resultados de Experimentos TBQ LaboratorioWilliam PachecoAinda não há avaliações
- Codigos de Falhas Rede Can Fiat PDFDocumento13 páginasCodigos de Falhas Rede Can Fiat PDFtadeu87% (30)
- NBR 09479 1994 Cura de CP de ConcretoDocumento2 páginasNBR 09479 1994 Cura de CP de ConcretoDavi FonsecaAinda não há avaliações
- Velocidade de Hidratação Da CalDocumento4 páginasVelocidade de Hidratação Da CalVictor ReginoAinda não há avaliações
- Proteg TCC - TriclorocarbanDocumento2 páginasProteg TCC - TriclorocarbanallanHF100% (1)
- FISPQ WEBER Manta Lquida Branca QuartzolitDocumento6 páginasFISPQ WEBER Manta Lquida Branca QuartzolitEwerton EspindolaAinda não há avaliações
- FISPQ SGQ VT20 Limpa Estofados PDFDocumento6 páginasFISPQ SGQ VT20 Limpa Estofados PDFjsbarcellosAinda não há avaliações
- 112.025 - Sumazinc s659 Primer Rico em ZincoDocumento2 páginas112.025 - Sumazinc s659 Primer Rico em ZincoLaertes JuniorAinda não há avaliações
- Ficha de Emergência - FET - Standak® TopDocumento1 páginaFicha de Emergência - FET - Standak® TopPCdoB de PinheirosAinda não há avaliações
- Manual de Proprietário Max 150Documento78 páginasManual de Proprietário Max 150Eduardo Gimenez80% (5)
- Minerais e Rochas - ResumoDocumento7 páginasMinerais e Rochas - ResumoVal TeixeiraAinda não há avaliações
- RELATÓRIODocumento41 páginasRELATÓRIOeliaszamarkiAinda não há avaliações
- Plano de Prevenção e Proteção Contra IncêndioDocumento8 páginasPlano de Prevenção e Proteção Contra IncêndioDavi Alves BatalhaAinda não há avaliações
- Guia Prático Do Pêndulo - D. Jurriaanse - Doc - IlustradoDocumento56 páginasGuia Prático Do Pêndulo - D. Jurriaanse - Doc - IlustradoTerezinha Flores Canabarro100% (1)
- Descrição Dos Principais Materiais de LaboratórioDocumento4 páginasDescrição Dos Principais Materiais de LaboratórioAna Carolina Monteiro100% (1)
- Estufa de Esterilização e Secagem Solid SteelDocumento6 páginasEstufa de Esterilização e Secagem Solid SteelLeandro GonçalvesAinda não há avaliações
- Pirometalurgia, Hidrometalurgia, EletrometalurgiaDocumento31 páginasPirometalurgia, Hidrometalurgia, EletrometalurgiaMoysés Araújo0% (1)
- Verticalização de Molar Com Mini ImplanteDocumento4 páginasVerticalização de Molar Com Mini ImplanterfbsAinda não há avaliações
- Cultura Da CebolaDocumento7 páginasCultura Da CebolaMarcos OkunoAinda não há avaliações
- Tairo, Hidroresfriamento e Embalagens Na ConservaçãoDocumento10 páginasTairo, Hidroresfriamento e Embalagens Na ConservaçãoThayse RochaAinda não há avaliações
- Feijão EmaterDocumento7 páginasFeijão EmaterEzio JuniorAinda não há avaliações
- Hikari HK-936bDocumento7 páginasHikari HK-936bPaulo Henrique S100% (1)
- Fispq Borden CleanDocumento6 páginasFispq Borden CleanMarcos AntonioAinda não há avaliações
- Treinamento cerebral: Compreendendo inteligência emocional, atenção e muito maisNo EverandTreinamento cerebral: Compreendendo inteligência emocional, atenção e muito maisNota: 4.5 de 5 estrelas4.5/5 (169)
- Biomecânica Básica dos Exercícios: Membros InferioresNo EverandBiomecânica Básica dos Exercícios: Membros InferioresNota: 3.5 de 5 estrelas3.5/5 (8)
- Inteligência artificial: O guia completo para iniciantes sobre o futuro da IANo EverandInteligência artificial: O guia completo para iniciantes sobre o futuro da IANota: 5 de 5 estrelas5/5 (6)
- 365 Ideias De Posts Para Ter Um Instagram De Sucesso!No Everand365 Ideias De Posts Para Ter Um Instagram De Sucesso!Ainda não há avaliações
- Cérebro Singular: Como estimular crianças no espectro autista ou com atrasos no desenvolvimentoNo EverandCérebro Singular: Como estimular crianças no espectro autista ou com atrasos no desenvolvimentoNota: 5 de 5 estrelas5/5 (1)
- Inteligência artificial: Como aprendizado de máquina, robótica e automação moldaram nossa sociedadeNo EverandInteligência artificial: Como aprendizado de máquina, robótica e automação moldaram nossa sociedadeNota: 5 de 5 estrelas5/5 (3)