Escolar Documentos
Profissional Documentos
Cultura Documentos
4 Avaliação (Turma 2T4) - MB
Enviado por
Paula Ferreira0 notas0% acharam este documento útil (0 voto)
5 visualizações2 páginasDireitos autorais
© © All Rights Reserved
Formatos disponíveis
PDF, TXT ou leia online no Scribd
Compartilhar este documento
Compartilhar ou incorporar documento
Você considera este documento útil?
Este conteúdo é inapropriado?
Denunciar este documentoDireitos autorais:
© All Rights Reserved
Formatos disponíveis
Baixe no formato PDF, TXT ou leia online no Scribd
0 notas0% acharam este documento útil (0 voto)
5 visualizações2 páginas4 Avaliação (Turma 2T4) - MB
Enviado por
Paula FerreiraDireitos autorais:
© All Rights Reserved
Formatos disponíveis
Baixe no formato PDF, TXT ou leia online no Scribd
Você está na página 1de 2
EEEM ESCOLA ESTADUAL MAGALHÃES BARATA
Diretor: Jerônimo Baía
Professor (es): Waldemir Souza, Anthoniel Hendel, Luiz Henrique.
Aluno (a) :________________________.Turma: ___Data ___/___/___
4a Avaliação Bimestral de Química
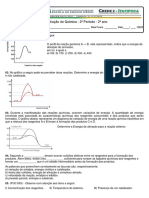
1. (Uerj) A sabedoria popular indica que, para 3. Analisando o gráfico representativo do
acender uma lareira, devemos utilizar caminho da reação A + B → C, pode-se dizer
inicialmente lascas de lenha e só depois
colocarmos as toras. Em condições reacionais
idênticas e utilizando massas iguais de
madeiras em lascas e em toras, verifica-se que
a madeira em lascas queima com mais
velocidade. O fator determinante, para essa
maior velocidade da reação, é o aumento da:
a) pressão
b) temperatura
c) superfície de contato que o valor da energia de ativação, em
d) catalisador Kcal/mol, é o tipo de reação são
respectivamente:
2. (Fuvest)
𝑁𝑎𝐻𝑆𝑂4 + 𝐶𝐻3𝐶𝑂𝑂𝑁𝑎 → 𝐶𝐻3𝐶𝑂𝑂𝐻 + 𝑁𝑎2𝑆𝑂4 a) 8 e exotérmica
A reação representada pela equação acima é b) 20 e endotérmica
realizada segundo dois procedimentos: 1. c) 20 e exotérmica
Triturando reagentes sólidos; 2. Misturando d) 28 e endotérmica
soluções aquosas concentradas dos reagentes. e) 30 e endotérmica
Utilizando a mesma quantidade de Na2SO4 , 4. Considere as seguintes afirmações
considere a mesma quantidade de CH3COONa envolvendo reações químicas, e assinale a
nesses procedimentos, à mesma temperatura, a única INCORRETA.
formação do ácido acético: a) O complexo ativado possui mais energia
a) é mais rápida em 2 porque em solução a que os reagentes ou os produtos;
frequência de colisões entre os reagentes é b) A adição de um catalisador aumenta a
maior; energia de ativação;
b) é mais rápida em 1 porque no estado sólido c) O aumento da energia de colisão favorece a
a concentração dos reagentes é maior; reação;
c) ocorre em 1 e 2 com igual velocidade d) A concentração, a temperatura e o
porque os reagentes são os mesmos; catalisador são fatores que afetam a velocidade
d) é mais rápida em 1 porque o ácido acético é de uma reação;
liberado na forma de vapor; e) Maior será a velocidade da reação, quanto
e) é mais rápida em 2 porque o ácido acético maior for a energia de ativação.
se dissolve na água.
Obs: Questões rasuradas serão anuladas!
5. Assinale a alternativa que apresenta agentes C- Concentração
que tendem a aumentar a velocidade de uma D- Temperatura
reação:
a) calor, obscuridade, catalisador. A alternativa que contém a associação correta
b) calor, maior superfície de contato entre entre as duas colunas é:
reagentes, ausência de catalisador.
c) calor, maior superfície de contato entre os a) 1-C; 2-D; 3-B; 4-A.
reagentes, catalisador. b) 1-D; 2-C; 3-B; 4-A.
d) frio, obscuridade, ausência de catalisador. c) 1-A; 2-B; 3-C; 4-D;
e) catalisador e congelamento dos reagentes. d) 1-B; 2-C; 3-D; 4-A;
e) 1-C; 2-D; 3-A; 4-B.
6. (UDESC) A cinética química é a área da
química que trata das velocidades das reações.
Analise os processos em relação à cinética
química:
I. Quando o carvão está iniciando a sua
queima, as pessoas ventilam o sistema
para que a queima se propague mais
rapidamente.
II. Um comprimido efervescente se
dissolve mais rapidamente quando
triturado.
Assinale a alternativa que contém os fatores
que influenciam as velocidades das reações
nos processos descritos em I e II,
respectivamente.
a) Concentração, superfície de contato;
b) Catalisador, concentração;
c) Temperatura, concentração;
d) Superfície de contato, catalisador;
e) Temperatura, catalisador.
7.(PUC-RS) Relacione os fenômenos descritos
na coluna I com os fatores que influenciam sua
velocidade mencionados na coluna II.
Coluna I
1- Queimadas alastrando-se rapidamente
quando está ventando;
2- Conservação dos alimentos no refrigerador;
3- Efervescência da água oxigenada na higiene
de ferimentos;
4- Lascas de madeira queimando mais
rapidamente que uma tora de madeira.
Coluna II
A- Superfície de contato
B- Catalisador
Obs: Questões rasuradas serão anuladas!
Você também pode gostar
- Apostila Química Orgânica: Carbono, Dienos E AromáticosNo EverandApostila Química Orgânica: Carbono, Dienos E AromáticosAinda não há avaliações
- Análise das tensões em estruturas de concreto devido a variações de temperatura entre os anos de 2009 e 2018No EverandAnálise das tensões em estruturas de concreto devido a variações de temperatura entre os anos de 2009 e 2018Ainda não há avaliações
- Cinetica QuimicaDocumento2 páginasCinetica QuimicaCMJ O caderno mágico do JamesAinda não há avaliações
- Ficha de Exercicios de Preparacao-1Documento27 páginasFicha de Exercicios de Preparacao-1Damião JeremiasAinda não há avaliações
- Cinetica 04Documento2 páginasCinetica 04Sandro BaldezAinda não há avaliações
- Qui MicaDocumento8 páginasQui Micamaria.hsvh0Ainda não há avaliações
- Lista de Termoquímica e Cinética - 2º AnoDocumento24 páginasLista de Termoquímica e Cinética - 2º AnoFernanda BarretoAinda não há avaliações
- Lista de Exercícios Sobre A Velocidade Das Reações QuímicasDocumento1 páginaLista de Exercícios Sobre A Velocidade Das Reações QuímicasJoalson eng ArliAinda não há avaliações
- AVALIAÇÃO - Cinetica - 2º AnoDocumento3 páginasAVALIAÇÃO - Cinetica - 2º AnoLaiane AmericoAinda não há avaliações
- CINÉTICADocumento7 páginasCINÉTICAVaneilton ReynaudAinda não há avaliações
- 2º Ano - Avaliação - Quimica - 08-07-2021 - JulhoDocumento3 páginas2º Ano - Avaliação - Quimica - 08-07-2021 - JulhoSelma Eliane Quatroque TavaresAinda não há avaliações
- Atividade 05 PDFDocumento4 páginasAtividade 05 PDFCassio RezendeAinda não há avaliações
- Estudo Dirigido Provão 4º BimestreDocumento5 páginasEstudo Dirigido Provão 4º BimestreJerusaFreitasAinda não há avaliações
- Qui MicaDocumento6 páginasQui MicaIanne PinhoAinda não há avaliações
- Atividade de Cinética I - 2 AnoDocumento2 páginasAtividade de Cinética I - 2 AnoElany PereiraAinda não há avaliações
- Cinética Química - Lista de ExercíciosDocumento2 páginasCinética Química - Lista de ExercíciosMateus DinizAinda não há avaliações
- 19.4.prova - Aula 19 - Cinética QuímicaDocumento4 páginas19.4.prova - Aula 19 - Cinética QuímicaAndreia AnnaAinda não há avaliações
- Prof. Rafa - Química - Cinética Química - Prova P2 - 1 BimDocumento3 páginasProf. Rafa - Química - Cinética Química - Prova P2 - 1 BimRafael VaristeloAinda não há avaliações
- Prova de Fisico Química 2 AnoDocumento7 páginasProva de Fisico Química 2 AnoProf. Marcelo França PinheiroAinda não há avaliações
- Fatores Que Alteram A Velocidade Das Reações QuímicasDocumento3 páginasFatores Que Alteram A Velocidade Das Reações QuímicasGiovani AraújoAinda não há avaliações
- Lista Cionetica TecnicoDocumento2 páginasLista Cionetica TecnicoLivia FerreiraAinda não há avaliações
- 2017 - 1a - 2 - Físico-Química PDFDocumento3 páginas2017 - 1a - 2 - Físico-Química PDFEdgar GóesAinda não há avaliações
- Ficha de QuimicaDocumento4 páginasFicha de QuimicavivaldoAinda não há avaliações
- Cinetica ExerciciosDocumento2 páginasCinetica ExercicioscarlostucupiAinda não há avaliações
- Química 2cDocumento2 páginasQuímica 2cmanuelaescola295Ainda não há avaliações
- Qui, Ica EliDocumento2 páginasQui, Ica EliPedro MartellAinda não há avaliações
- Lista de Exercícios I (2º Bimestre) - 3º AnoDocumento3 páginasLista de Exercícios I (2º Bimestre) - 3º AnoMikeas LimaAinda não há avaliações
- Atividade de Química 3 ANOS Fatores Que Influenciam As Reaçoes 0405 A 08052020Documento3 páginasAtividade de Química 3 ANOS Fatores Que Influenciam As Reaçoes 0405 A 08052020marques.gui2015Ainda não há avaliações
- Exercicio Teórico de Cinética QuímicaDocumento4 páginasExercicio Teórico de Cinética Químicacapudinho004Ainda não há avaliações
- Lista de Exercícios - Cinética QuímicaDocumento3 páginasLista de Exercícios - Cinética QuímicaAllison Evangelista da SilvaAinda não há avaliações
- Aula 09.1 - Lista de Exercícios Fatores Que Influenciam Na Velocidade Da ReaçãoDocumento4 páginasAula 09.1 - Lista de Exercícios Fatores Que Influenciam Na Velocidade Da ReaçãoRosah Gabryellyh100% (1)
- Lista Da Aula 3 - Cinética QuímicaDocumento5 páginasLista Da Aula 3 - Cinética QuímicaE P Som RJAinda não há avaliações
- Atividade Cinética QuímicaDocumento3 páginasAtividade Cinética Químicasophia costaAinda não há avaliações
- Lista Cinética (Monitoria)Documento4 páginasLista Cinética (Monitoria)Raineldes CruzAinda não há avaliações
- Extensivoenem-química-Cinética Química Fatores Que Alteram A Velocidade de Uma Reação-30!06!2020Documento11 páginasExtensivoenem-química-Cinética Química Fatores Que Alteram A Velocidade de Uma Reação-30!06!2020Felipe AlmeidaAinda não há avaliações
- Lista de Exercícios de Fixação Cinética QuímicaDocumento5 páginasLista de Exercícios de Fixação Cinética Químicabruno.amarques05Ainda não há avaliações
- 3º Ano - 3º Trim - Sem 31 - Exercícios de Fixação de Química para o TC2Documento5 páginas3º Ano - 3º Trim - Sem 31 - Exercícios de Fixação de Química para o TC2Henrique AraujoAinda não há avaliações
- Cinética QuímicaDocumento43 páginasCinética Químicammarqueslemn0% (2)
- Alunos Exercícios CinéticaDocumento3 páginasAlunos Exercícios CinéticaRiaAinda não há avaliações
- Atv - Cinética QuímicaDocumento3 páginasAtv - Cinética Químicamourabraga09Ainda não há avaliações
- Lista 08 - Fatores Que Alteram A VelocidadeDocumento10 páginasLista 08 - Fatores Que Alteram A VelocidadevagnererenataAinda não há avaliações
- 20 - 21 - Cinetica QuimicaDocumento10 páginas20 - 21 - Cinetica QuimicaGustavo MoraisAinda não há avaliações
- 48 20cin C3 A9tica 20qu C3 ADmicaDocumento14 páginas48 20cin C3 A9tica 20qu C3 ADmicaFrancis Francisco Johane SemanaAinda não há avaliações
- Cinetica - Fatores Que Alteram A Velocidade - 20220215124854 - U2FsdDocumento7 páginasCinetica - Fatores Que Alteram A Velocidade - 20220215124854 - U2FsdJoao MaiaAinda não há avaliações
- AP DE QUIMICA 12aa Classe 2023 PDFDocumento2 páginasAP DE QUIMICA 12aa Classe 2023 PDFDinis JustinoAinda não há avaliações
- Cinetqui 001Documento31 páginasCinetqui 001Anonymous QMpWb7Vc3XAinda não há avaliações
- Cinetica 1Documento8 páginasCinetica 1Nanda OdebrechtAinda não há avaliações
- Alfa - Módulo 40Documento28 páginasAlfa - Módulo 40Luiza FreitasAinda não há avaliações
- Cinética QuímicaDocumento12 páginasCinética QuímicaJeyciane RosaAinda não há avaliações
- Lista de Exercicio de Fixacao de Quimica A Av02 - 3o Bim. - 2o AnoDocumento6 páginasLista de Exercicio de Fixacao de Quimica A Av02 - 3o Bim. - 2o AnoNatalia AmaralAinda não há avaliações
- CinéticaDocumento3 páginasCinéticaDavid LunaAinda não há avaliações
- Atividade Extra - Episódio 11 - Cinética QuímicaDocumento9 páginasAtividade Extra - Episódio 11 - Cinética QuímicaGabriel BoaventuraAinda não há avaliações
- Exercícios Cinética Química LivretoDocumento8 páginasExercícios Cinética Química LivretoJoão Ribeiro Franco NetoAinda não há avaliações
- Questões CinéticaDocumento1 páginaQuestões Cinéticarubens.costaAinda não há avaliações
- Atividade de Revisão 2 Série Quimica 4º BimestreDocumento6 páginasAtividade de Revisão 2 Série Quimica 4º BimestreElvandira NapoleãoAinda não há avaliações
- Revisao Cinetica BasicaDocumento5 páginasRevisao Cinetica BasicaXavier EliúdeAinda não há avaliações
- Av 4º B 2º Ano QuímicaDocumento4 páginasAv 4º B 2º Ano QuímicaJulioAinda não há avaliações
- Estudo Dirigido de Química - Ceja - Fascículo 5 (Unidades 11, 12 e 13) .Documento4 páginasEstudo Dirigido de Química - Ceja - Fascículo 5 (Unidades 11, 12 e 13) .falecomarilsonAinda não há avaliações
- Quimica 4Documento4 páginasQuimica 4João PedroAinda não há avaliações
- Plano de Aula Eletroquímica - Eletrolise.-1Documento3 páginasPlano de Aula Eletroquímica - Eletrolise.-1Paula FerreiraAinda não há avaliações
- Indepedencia e Dependencia Linear-ExDocumento2 páginasIndepedencia e Dependencia Linear-ExPaula FerreiraAinda não há avaliações
- Modelo e Orientação de Relatório FinalDocumento4 páginasModelo e Orientação de Relatório FinalPaula FerreiraAinda não há avaliações
- Cap. Psidium GuineenseDocumento12 páginasCap. Psidium GuineensePaula FerreiraAinda não há avaliações
- IntroduoDocumento33 páginasIntroduoPaula FerreiraAinda não há avaliações
- 1 Avaliação de Química - Prova Vermelha-1Documento1 página1 Avaliação de Química - Prova Vermelha-1Paula FerreiraAinda não há avaliações
- Galoa Proceedings Epqa 2019 108222Documento6 páginasGaloa Proceedings Epqa 2019 108222Paula FerreiraAinda não há avaliações
- 2018 Qui126 Aula 10 EletroquímicaDocumento11 páginas2018 Qui126 Aula 10 EletroquímicaNiltoncientistaAinda não há avaliações
- Crescimento Dos Microorganismos Do ChuléDocumento1 páginaCrescimento Dos Microorganismos Do ChuléPaula FerreiraAinda não há avaliações
- ATIVIDADE DISSERTATIVA - Antropologia IDocumento3 páginasATIVIDADE DISSERTATIVA - Antropologia ICeloPlay Santos100% (1)
- Analise de Leite em PóDocumento6 páginasAnalise de Leite em PóMarli CorreaAinda não há avaliações
- Apostila CCNA 200 301 v1 PDFDocumento428 páginasApostila CCNA 200 301 v1 PDFMisael SilveiraAinda não há avaliações
- Esquema Eletrico Peugeot 306Documento35 páginasEsquema Eletrico Peugeot 306Alcindo Taro80% (15)
- Revisao 1 - Curso Positivo - FinalDocumento200 páginasRevisao 1 - Curso Positivo - FinalMarina Franzoi PereiraAinda não há avaliações
- 2021 - Cartilha Vamos Falar Sobre AnsiedadeDocumento19 páginas2021 - Cartilha Vamos Falar Sobre AnsiedadeJade FalcãoAinda não há avaliações
- A Diferença Básica Entre o Diodo Zener e o Diodo Retificador É Que o Diodo Zener Opera Na Região de Ruptura Ao Passo Que o Diodo Retificador Será Danificado Se Atingir Esta RegiãoDocumento11 páginasA Diferença Básica Entre o Diodo Zener e o Diodo Retificador É Que o Diodo Zener Opera Na Região de Ruptura Ao Passo Que o Diodo Retificador Será Danificado Se Atingir Esta RegiãoEvanildo PalmaAinda não há avaliações
- FATURA Claro 2023 306541723Documento3 páginasFATURA Claro 2023 306541723patriciamdlaraAinda não há avaliações
- Relatório Final Do Estagio I PDFDocumento11 páginasRelatório Final Do Estagio I PDFGessicaAinda não há avaliações
- Funcao Do Rubisco No Ciclo de CalvinDocumento10 páginasFuncao Do Rubisco No Ciclo de CalvinDário Cristovão CristovãoAinda não há avaliações
- Relatório 02 - Sistema de AlimentaçãoDocumento10 páginasRelatório 02 - Sistema de AlimentaçãoBruno LimaAinda não há avaliações
- Kelvin Mitinick X ShimomuraDocumento6 páginasKelvin Mitinick X ShimomuraAlexandre Torquato RufinoAinda não há avaliações
- Síntese de Pla - TabelaDocumento3 páginasSíntese de Pla - TabelaDriNay13Ainda não há avaliações
- Dara - Rosemary - PB+H-1750-1Documento4 páginasDara - Rosemary - PB+H-1750-1Shemina Romano Diniz FonsecaAinda não há avaliações
- Cintura PelvicaDocumento3 páginasCintura PelvicaTaynara BissAinda não há avaliações
- Projeto Elétrico PiscinaDocumento13 páginasProjeto Elétrico Piscinapolarf6Ainda não há avaliações
- Procedimento de Instalação em Rede Softwares ProDocumento8 páginasProcedimento de Instalação em Rede Softwares ProcmtonioloAinda não há avaliações
- Check-List NP en ISO 9001-2015Documento54 páginasCheck-List NP en ISO 9001-2015Anonymous 3sOtS4Uvqm86% (7)
- Memorial DescritivoDocumento4 páginasMemorial DescritivoWill LimaAinda não há avaliações
- Script Banho e TosaDocumento3 páginasScript Banho e TosarafaelsilvacursoshotmailcomAinda não há avaliações
- Cana de Açúcar - FermentaçãoDocumento2 páginasCana de Açúcar - FermentaçãoRobson RodriguesAinda não há avaliações
- AULA 26 - Números Complexos - Frente 1 - Versao 1Documento19 páginasAULA 26 - Números Complexos - Frente 1 - Versao 1Joao MoneziAinda não há avaliações
- Ceará Científico Digital 2021Documento2 páginasCeará Científico Digital 2021Allan DiasAinda não há avaliações
- Decreto de Regeneração CelularDocumento2 páginasDecreto de Regeneração CelularMob Luiz Flavio100% (1)
- Gestão Pública No Brasil - Temas Preservados e Temas Emergentes Na Formação Da AgendaDocumento25 páginasGestão Pública No Brasil - Temas Preservados e Temas Emergentes Na Formação Da AgendaLuis FelippeAinda não há avaliações
- IAGODocumento1 páginaIAGOJoão Paulo MocellinAinda não há avaliações
- Do 20032020 1532Documento3 páginasDo 20032020 1532Benedicta SodréAinda não há avaliações
- Questões para o SimuladoDocumento13 páginasQuestões para o SimuladoCarlos BraynerAinda não há avaliações
- Estudo de CasoDocumento1 páginaEstudo de CasoJéssicaTavaresAinda não há avaliações
- Aululária - Plauto PDFDocumento28 páginasAululária - Plauto PDFGabriela VarelaAinda não há avaliações