Escolar Documentos
Profissional Documentos
Cultura Documentos
Atividade 1 FQ2A
Enviado por
Alfredo Sahade Vespa0 notas0% acharam este documento útil (0 voto)
184 visualizações3 páginasO documento apresenta questões sobre solubilidade de sais em função da temperatura. As questões abordam conceitos como solubilidade, saturação, supersaturação e precipitação de sais quando soluções saturadas são resfriadas ou aquecidas. Gráficos de curvas de solubilidade em função da temperatura são apresentados para análise.
Descrição original:
Direitos autorais
© © All Rights Reserved
Formatos disponíveis
PDF, TXT ou leia online no Scribd
Compartilhar este documento
Compartilhar ou incorporar documento
Você considera este documento útil?
Este conteúdo é inapropriado?
Denunciar este documentoO documento apresenta questões sobre solubilidade de sais em função da temperatura. As questões abordam conceitos como solubilidade, saturação, supersaturação e precipitação de sais quando soluções saturadas são resfriadas ou aquecidas. Gráficos de curvas de solubilidade em função da temperatura são apresentados para análise.
Direitos autorais:
© All Rights Reserved
Formatos disponíveis
Baixe no formato PDF, TXT ou leia online no Scribd
0 notas0% acharam este documento útil (0 voto)
184 visualizações3 páginasAtividade 1 FQ2A
Enviado por
Alfredo Sahade VespaO documento apresenta questões sobre solubilidade de sais em função da temperatura. As questões abordam conceitos como solubilidade, saturação, supersaturação e precipitação de sais quando soluções saturadas são resfriadas ou aquecidas. Gráficos de curvas de solubilidade em função da temperatura são apresentados para análise.
Direitos autorais:
© All Rights Reserved
Formatos disponíveis
Baixe no formato PDF, TXT ou leia online no Scribd
Você está na página 1de 3
1ª Lista de Exercícios Físico-Química 2ºA
Nome: nº
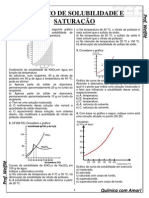
4 – O gráfico abaixo representa a curva de
solubilidade de NaNO3, em função da
1 – Se dissolvermos totalmente uma certa temperatura, e seis pontos, que correspondem
quantidade de sal em solvente e por qualquer aos sistemas preparados.
perturbação uma parte do sal se depositar, qual a
solução que teremos no final?
a) saturada com corpo de fundo.
b) supersaturada com corpo de fundo.
c) insaturada.
d) supersaturada sem corpo de fundo.
e) saturada sem corpo de fundo.
2 – Observe a figura abaixo, que representa a
solubilidade, em g por 100 g de H2O, de 3 sais
inorgânicos em determinada faixa de
temperatura. Identifique a afirmativa correta.
A partir da análise desse gráfico, identifique os
dois sistemas em que há precipitado.
5 – O gráfico apresenta a curva de solubilidade
de um sal AX2.
a) A solubilidade dos 3 sais aumenta com a
temperatura.
b) O aumento de temperatura favorece a
solubilização do Li2SO4.
c) A solubilidade do KI é maior que as
solubilidades dos demais sais, na faixa de
temperatura dada.
d) A solubilidade do NaCl varia com a
temperatura.
e) A solubilidade de 2 sais diminui com a
temperatura. Quando uma solução aquosa saturada de AX2 a
70 °C contendo 50 g de água é resfriada para 10
3 –A dissolução de uma quantidade fixa de um °C, quais são, em gramas, a massa de sal
composto inorgânico depende de fatores tais cristalizada e a massa que permanece em
como temperatura e tipo de solvente. solução?
Analisando a tabela de solubilidade do sulfato
de potássio (K2SO4) em 100 g de água (H2O) a) 25 e 20 b) 30 e 15 c) 35 e 10
ao lado, indique a massa de K2SO4 que d) 35 e 15 e) 40 e 10
precipitará quando a solução for devidamente
resfriada de 80 °C até atingir a temperatura de 6 – A tabela a seguir mostra a solubilidade de
20 °C. vários sais, à temperatura ambiente, em g/100
mL.
Se 25 mL de uma solução saturada de um desses
sais foram completamente evaporados, e o
resíduo sólido pesou 13 g, identifique o sal.
a) 28g b) 18g c) 10g d) 8 g
9 – Analise o gráfico abaixo. Julgue os itens
seguintes, identificando os corretos.
7 – Considere as experiências descritas a seguir,
efetuadas na mesma temperatura.
I. Um litro de água é adicionado lentamente, sob
agitação, a 500 g de sal de cozinha. Apenas
parte do sal é dissolvido.
II. 500 g de sal de cozinha são adicionados aos
poucos, sob agitação, a um litro de água. Sobre
as experiências acima e levando em conta os
conhecimentos sobre o processo da
solubilidade, é correto afirmar:
a) A substância mais solúvel em água a 10 °C é
a) Em I e II a massa de sal dissolvida é a
KNO3.
mesma.
b) A substância que apresenta menor variação
b) Apenas em I forma-se uma solução saturada
da solubilidadeVentre 30 °C e 80 °C é o cloreto
sobre a fase sólida.
de sódio.
c) A massa de sal dissolvida nas experiências
c) A solubilidade de qualquer sólido aumenta
não depende da temperatura.
com a elevação da temperatura da solução.
d) Em II a mistura resultante é homogênea.
d) A mistura de 20 g de NH4Cl com 100 g de
e) Em I e II resulta um estado de equilíbrio entre
água a 50 °C resultará em uma solução
uma fase sólida e uma fase líquida.
insaturada.
f) A massa inicial de sal pode ser recuperada,
e) Uma solução preparada com 80 g de KNO3
nas duas experiências, por meio de um processo
em 100 g de água, a 40 °C, apresentará sólido
de destilação.
no fundo do recipiente
8 – Um estudante pretende separar os
10 – A solubilidade da soda cáustica (NaOH)
componentes de uma amostra contendo três sais
em água, em função da temperatura, é dada na
de chumbo II: Pb(NO3)2, PbSO4 e PbI2. Após
tabela abaixo.
analisar a tabela de solubilidade abaixo,
Considerando soluções de NaOH em 100 g de
água, escolha a alternativa correta.
a) a 20 °C, uma solução com 120 g de NaOH é
ele propôs o seguinte procedimento:
concentrada.
b) a 20 °C, uma solução com 80 g de NaOH é
“Adicionar água destilada em ebulição à
diluída.
mistura, agitando o sistema vigorosamente.
c) a 30 °C, uma solução com 11,9 g de NaOH é
Filtrar a suspensão resultante, ainda quente.
concentrada.
Secar o sólido obtido no papel de filtro; este
d) a 30 °C, uma solução com 119 g de NaOH é
será o sal A. Recolher o filtrado em um béquer,
supersaturada.
deixando-o esfriar em banho de água e gelo.
e) a 40 °C, uma solução com 129 g de NaOH é
Proceder a uma nova filtração e secar o sólido
saturada.
obtido no papel de filtro; este será o sal B.
Aquecer o segundo filtrado até a evaporação
11 – Uma solução saturada de NH4Cl foi
completa da água; o sólido resultante será o sal
preparada a 80 °C utilizando-se 200 g de água.
C.” Identifique os sais A, B, e C,
Posteriormente, essa solução sofre um
respectivamente.
resfriamento sob agitação até atingir 40 °C.
Determine a massa de sal depositada nesse I. O filtrado é uma solução saturada de KCl em
processo. A solubilidade do NH4Cl varia com a água.
temperatura, conforme mostrado no gráfico. II. O coeficiente de solubilidade do KCl é 38
g/100 mL de água (dágua % 1,0 g/mL) à
temperatura do experimento.
III. Após a quarta adição obteve-se uma mistura
heterogênea, e nenhuma partícula de KCl da
quinta adição passa para a solução.
Escolha as corretas e justifique as incorretas.
12 - (Osec-SP) A solubilidade do K2Cr2O7, a
20 °C, é 12 g/100 g de água e, a 60 °C, é 43
g/100 g de água. Sabendo que uma solução foi
preparada dissolvendo-se 20 g do sal em 100 g
de água a 60 °C e que depois ela foi resfriada a
20 °C, podemos concluir que:
a) todo sal continuou na solução.
b) todo sal passou a formar um corpo de chão.
c) 8 g do sal foram depositados no fundo do
recipiente.
d) 12 g do sal foram depositados no fundo do
recipiente.
e) 31 g do sal passou a formar um corpo de
chão.
13 – Um laboratorista preparou uma mistura, a
80 °C, constituída por 70 g de cloreto de
potássio (KCl) e 150 g de água. Em seguida, a
mistura foi resfriada até 20 °C, mantendo-se a
temperatura nesse valor. Considerando-se os
dados de solubilidade do KCl em 100 g de água,
apresentados na tabela abaixo:
a) determine se a mistura (KCl + água), nas
temperaturas de 80 °C e 20 °C, é homogênea ou
heterogênea. Em cada caso, justifique sua
resposta por meio de cálculos;
14 – Foi realizado o seguinte procedimento no
laboratório: a um béquer contendo 50,0 mL de
água destilada adicionou-se KCl sólido em
porções de 5,0 g cada. Obteve-se das três
primeiras adições, após agitação e repouso, uma
solução límpida. Na quarta adição observou-se a
permanência de um resíduo não dissolvido e na
quinta adição não houve mais a solubilização do
KCl. Essa solução foi então filtrada, e o
precipitado seco. A massa deste foi determinada
como sendo 6,0 g. Considere as afirmações
seguintes sobre esse procedimento.
Você também pode gostar
- Atividade 2 FQ2ADocumento4 páginasAtividade 2 FQ2AAlfredo Sahade VespaAinda não há avaliações
- DispersõeDocumento5 páginasDispersõeHelton ClistenesAinda não há avaliações
- Quimica 2 Ano 2 ParteDocumento19 páginasQuimica 2 Ano 2 ParteJoão PauloAinda não há avaliações
- Lista de Exercícios - SolubilidadeDocumento3 páginasLista de Exercícios - Solubilidadealexchacal100% (2)
- Atividade 5 de Abril - Pré ProvaDocumento5 páginasAtividade 5 de Abril - Pré ProvaAlfredo Sahade VespaAinda não há avaliações
- Aula de Resolução de Questões Soluções QuimicasDocumento5 páginasAula de Resolução de Questões Soluções Quimicasi46555497Ainda não há avaliações
- Lista de Exercicios 12 - Revisao para A 2 Avaliacao - Hidrolise Salina e Solubilidade - 3 Bimestre 2013 - 3 SeriesDocumento2 páginasLista de Exercicios 12 - Revisao para A 2 Avaliacao - Hidrolise Salina e Solubilidade - 3 Bimestre 2013 - 3 SeriesJosimar Lima FerreiraAinda não há avaliações
- Lista de Exercc3adcio Soluc3a7c3b5esDocumento5 páginasLista de Exercc3adcio Soluc3a7c3b5esAna Ester CavalcanteAinda não há avaliações
- Coeficiente de SolubilidadeDocumento5 páginasCoeficiente de SolubilidadeRubia MariathAinda não há avaliações
- Estudo Das Solucoes Coeficiente de SolubilidadeDocumento13 páginasEstudo Das Solucoes Coeficiente de SolubilidadeGildo Silva100% (1)
- 31-Soluções e SolubilidadeDocumento4 páginas31-Soluções e Solubilidadenv77vnm100% (2)
- Coeficiente de Solub.Documento8 páginasCoeficiente de Solub.Rafael MottaAinda não há avaliações
- Capítulo 1 - SoluçõesDocumento18 páginasCapítulo 1 - SoluçõesGerson LimaAinda não há avaliações
- 16 SolubilidadeDocumento7 páginas16 SolubilidadeFRANKE MERO TESTEAinda não há avaliações
- Graficos Solubilidade 2 Ano 2Documento1 páginaGraficos Solubilidade 2 Ano 2lopesqui1766Ainda não há avaliações
- Química - 2° Ano - PReus.Documento4 páginasQuímica - 2° Ano - PReus.Kauã CostaAinda não há avaliações
- Coeficiente de Solubilidadeaula 12 04 12blogDocumento7 páginasCoeficiente de Solubilidadeaula 12 04 12blogThania ArrudaAinda não há avaliações
- 16 SolubilidadeDocumento6 páginas16 SolubilidadeEverton FisicoAinda não há avaliações
- SOLUCOESDocumento15 páginasSOLUCOESRaquel Reis Duarte PinheiroAinda não há avaliações
- Lista de SolubilidadeDocumento2 páginasLista de SolubilidadeRtyu IuytAinda não há avaliações
- Exercicios de SolubilidadeDocumento6 páginasExercicios de Solubilidadesua mae de 4Ainda não há avaliações
- 36 20solubilidade 20 - 20conceitos 20e 20curvas PDFDocumento12 páginas36 20solubilidade 20 - 20conceitos 20e 20curvas PDFCarolynne MourãoAinda não há avaliações
- Solucoes PDFDocumento15 páginasSolucoes PDFThiago Magno Tavares Machado100% (1)
- CoeficienteDocumento12 páginasCoeficienteOtoazevedo OtoazevedoAinda não há avaliações
- Química: 3 Lista de ResoluçãoDocumento5 páginasQuímica: 3 Lista de ResoluçãoJader Pereira de AraujoAinda não há avaliações
- CE Quimica 2 Ano 1 BimDocumento12 páginasCE Quimica 2 Ano 1 Bimguilhermestadlerdefreitas1Ainda não há avaliações
- Cbae4ae1 Db5c 4fc9 8184 5115d78789b8 Fisico QuimicaDocumento79 páginasCbae4ae1 Db5c 4fc9 8184 5115d78789b8 Fisico QuimicaNina Bob Brown100% (1)
- Química Lista de ExercíciosDocumento4 páginasQuímica Lista de Exercícioshtq87rbdjgAinda não há avaliações
- Exercicios Coeficiente de SolubilidadeDocumento4 páginasExercicios Coeficiente de SolubilidadeAndré Luís Della VolpeAinda não há avaliações
- Exercício 1Documento2 páginasExercício 1Romulo AlvesAinda não há avaliações
- Coeficiente de Solubilidade e Tipos de SaturaçãoDocumento5 páginasCoeficiente de Solubilidade e Tipos de SaturaçãoWelff Junior100% (2)
- Lista SoluçoesDocumento2 páginasLista SoluçoesVitor GabrielAinda não há avaliações
- Exercicios de Coeficiente de SolubilidadeDocumento4 páginasExercicios de Coeficiente de SolubilidadeCleber SerafinAinda não há avaliações
- 20080325103157Documento6 páginas20080325103157Renan Barcelos MendesAinda não há avaliações
- Lista de Exercicio de Quimica Introducao As SolucoesDocumento3 páginasLista de Exercicio de Quimica Introducao As SolucoesEtiany Oliveira SantosAinda não há avaliações
- OlucoesDocumento22 páginasOlucoesRebecaAinda não há avaliações
- Lista de Exercícios de Química 3 AnoDocumento3 páginasLista de Exercícios de Química 3 AnoAlex CardozoAinda não há avaliações
- Lista+de+exercícios+para+1 +prova+Quimica+AnalíticaDocumento5 páginasLista+de+exercícios+para+1 +prova+Quimica+Analíticabenedito.nasaAinda não há avaliações
- Lista 1 QG 1-19Documento6 páginasLista 1 QG 1-19schottbpAinda não há avaliações
- Gama - Módulo 19Documento23 páginasGama - Módulo 19Koelho CoelhoAinda não há avaliações
- Gabarito Lista 1 - SoluçõesDocumento5 páginasGabarito Lista 1 - Soluçõesbrigida.lucinAinda não há avaliações
- Exercicios de Coeficiente de SolubilidadeDocumento4 páginasExercicios de Coeficiente de SolubilidadeJardson Ramos SilvaAinda não há avaliações
- Exercicios de Coeficiente de SolubilidadeDocumento4 páginasExercicios de Coeficiente de SolubilidadeEng Renato De Marchi Vieira Dos SantosAinda não há avaliações
- Alex 04 - Soluções - Coeficiente de SolubilidadeDocumento2 páginasAlex 04 - Soluções - Coeficiente de Solubilidaderomezioh7716Ainda não há avaliações
- Breve Listinha de Exercicios Sobre Coeficiente de Solubilidade PDFDocumento6 páginasBreve Listinha de Exercicios Sobre Coeficiente de Solubilidade PDFFarmacia Artur NogueiraAinda não há avaliações
- 12 - Soluções Curvas de SolubilidadeDocumento4 páginas12 - Soluções Curvas de SolubilidadeRodrigo MetteAinda não há avaliações
- Alista 16 - Solucoes I A Solubilidade Das SubstanciasDocumento7 páginasAlista 16 - Solucoes I A Solubilidade Das SubstanciasHeitorAinda não há avaliações
- SOLUÇÕESDocumento8 páginasSOLUÇÕESVitóriaAinda não há avaliações
- Breve Listinha de Exercicios Sobre Coeficiente de SolubilidadeDocumento6 páginasBreve Listinha de Exercicios Sobre Coeficiente de SolubilidadeÉrica LimaAinda não há avaliações
- Soluções 321 QuestõesDocumento83 páginasSoluções 321 QuestõesThiago Alonso Rodrigues da Hora67% (3)
- Exercícios Coeficiente de SolubilidadeDocumento7 páginasExercícios Coeficiente de SolubilidadeGraciete QuentalAinda não há avaliações
- SolubilidadeDocumento4 páginasSolubilidadeCleber SerafinAinda não há avaliações
- Resumo 02 FQDocumento3 páginasResumo 02 FQAlexandre MagnoAinda não há avaliações
- Atividade Sobre Coeficiente de SolubilidadeDocumento13 páginasAtividade Sobre Coeficiente de SolubilidadePedro HélioxAinda não há avaliações
- Ensino Médio Turno Matutino Exercícios de Química "Coeficiente de Solubilidade"Documento1 páginaEnsino Médio Turno Matutino Exercícios de Química "Coeficiente de Solubilidade"Igor SamuelAinda não há avaliações
- 2012 - TMedicina - Quimica - Borges - Exercícios de Solubilidade - SiteDocumento12 páginas2012 - TMedicina - Quimica - Borges - Exercícios de Solubilidade - SiteDhieniffer FerreiraAinda não há avaliações
- Apostila Química Orgânica: Carbono, Dienos E AromáticosNo EverandApostila Química Orgânica: Carbono, Dienos E AromáticosAinda não há avaliações
- 1 Lista de Exercícios Operações - Conversão de UnidadesDocumento3 páginas1 Lista de Exercícios Operações - Conversão de UnidadesAlfredo Sahade VespaAinda não há avaliações
- 1 Lista de Exercícios 1B - 3FQ - Massa MolecularDocumento2 páginas1 Lista de Exercícios 1B - 3FQ - Massa MolecularAlfredo Sahade VespaAinda não há avaliações
- PicnometroDocumento4 páginasPicnometroAlfredo Sahade VespaAinda não há avaliações
- Atividade 09-07 MM - TítuloDocumento1 páginaAtividade 09-07 MM - TítuloAlfredo Sahade VespaAinda não há avaliações
- Atividade 23-07 Concentração MolarDocumento1 páginaAtividade 23-07 Concentração MolarAlfredo Sahade VespaAinda não há avaliações
- Corrosão - Taxa de CorrosãoDocumento3 páginasCorrosão - Taxa de CorrosãoAlfredo Sahade VespaAinda não há avaliações
- Cálculo Estequiométrico IIDocumento5 páginasCálculo Estequiométrico IIAlfredo Sahade VespaAinda não há avaliações
- Cálculo Estequiométrico IDocumento4 páginasCálculo Estequiométrico IAlfredo Sahade VespaAinda não há avaliações
- Experimento Corrosão Aula 1Documento1 páginaExperimento Corrosão Aula 1Alfredo Sahade VespaAinda não há avaliações
- Corrosão - Abordagem em Cinética QuímicaDocumento4 páginasCorrosão - Abordagem em Cinética QuímicaAlfredo Sahade VespaAinda não há avaliações
- Corrosão - Colorimetria Sulfato de CobreDocumento4 páginasCorrosão - Colorimetria Sulfato de CobreAlfredo Sahade VespaAinda não há avaliações
- 1 Lista EletróliseDocumento3 páginas1 Lista EletróliseAlfredo Sahade Vespa100% (1)
- 1 Lista - NoxDocumento1 página1 Lista - NoxAlfredo Sahade Vespa50% (2)
- 2 Lista - Balanceamento RedoxDocumento1 página2 Lista - Balanceamento RedoxAlfredo Sahade VespaAinda não há avaliações
- Saneantes Anvisa PDFDocumento6 páginasSaneantes Anvisa PDFAlfredo Sahade VespaAinda não há avaliações
- Cinetica PermanganatoDocumento2 páginasCinetica PermanganatoAlfredo Sahade VespaAinda não há avaliações
- Em Deus Faremos ProezasDocumento3 páginasEm Deus Faremos ProezasLivraria OlimpicaAinda não há avaliações
- Psicologia Da EducaçãoDocumento2 páginasPsicologia Da Educaçãovanessa.scarlattoAinda não há avaliações
- Apostila InformaticaDocumento128 páginasApostila Informaticawilson netto100% (1)
- Tarot de Mago: A AscensãoDocumento66 páginasTarot de Mago: A Ascensãosoldadodareal100% (1)
- Cerveja PDFDocumento28 páginasCerveja PDFLucas Beirao Do ValleAinda não há avaliações
- Tutorial Como Desbloquear e Rotear o Modem SpeedTouch 510v6 - Downloads, Drivers, Jailbreak de iOS, Notícias, SEO, TutoriaisDocumento54 páginasTutorial Como Desbloquear e Rotear o Modem SpeedTouch 510v6 - Downloads, Drivers, Jailbreak de iOS, Notícias, SEO, TutoriaisZionAinda não há avaliações
- Slide BioéticaDocumento13 páginasSlide Bioéticaiza machadoAinda não há avaliações
- Ligações QuímicasDocumento66 páginasLigações QuímicasBenites PatrickAinda não há avaliações
- Termodinamica Q Geral-Parte1aDocumento48 páginasTermodinamica Q Geral-Parte1avito xxxAinda não há avaliações
- Retificador Controlado de Onda Completa em PonteDocumento4 páginasRetificador Controlado de Onda Completa em Pontepedro_joao_lemuel100% (1)
- 2 Va Quimica 2a 2022Documento1 página2 Va Quimica 2a 2022Marcos Vinicius Sousa de Oliveira CarvalhoAinda não há avaliações
- Nelson LehmannDocumento6 páginasNelson LehmannHorácio SilvaAinda não há avaliações
- 07 - Escravizada - Daniella WrightDocumento25 páginas07 - Escravizada - Daniella Wrightprofessora AdrianaAinda não há avaliações
- Netuno Nas Casas de Uma Revolução SolarDocumento4 páginasNetuno Nas Casas de Uma Revolução Solarroberthnmd67% (3)
- Espécies de Peixes Marinhos Desembarcados Pela Colônia de Pescadores Z-34 Do Malhado em 2004 (Ilhéus, Ba)Documento3 páginasEspécies de Peixes Marinhos Desembarcados Pela Colônia de Pescadores Z-34 Do Malhado em 2004 (Ilhéus, Ba)Fênix SampaioAinda não há avaliações
- Recuperação JudicialDocumento21 páginasRecuperação JudicialJulia AndradeAinda não há avaliações
- Atividade - FaculesteDocumento2 páginasAtividade - FaculesteLayla MartinsAinda não há avaliações
- Fundamentos Históricos Do Serviço Social em YazbeckDocumento23 páginasFundamentos Históricos Do Serviço Social em YazbeckBarbosa DavidAinda não há avaliações
- A Psicologia Do Desenvolvimento PDFDocumento3 páginasA Psicologia Do Desenvolvimento PDFpetter_355279Ainda não há avaliações
- Cronograma Semana 22 Extensivo OnlineDocumento1 páginaCronograma Semana 22 Extensivo OnlineThomas HaasAinda não há avaliações
- Os Autores Contemporâneos e Suas Concepções de Mundo (Salvo Automaticamente)Documento10 páginasOs Autores Contemporâneos e Suas Concepções de Mundo (Salvo Automaticamente)Clesio Oliveira LiraAinda não há avaliações
- IPANDocumento2 páginasIPANClark Araujo ReisAinda não há avaliações
- Catalogo Pecas UsinadasDocumento6 páginasCatalogo Pecas UsinadasBento FranciscoAinda não há avaliações
- Empreendedorismo - Um Estudo Sobre A ImportânciaDocumento9 páginasEmpreendedorismo - Um Estudo Sobre A ImportânciagodinhofmAinda não há avaliações
- Ética e Testes Genéticos - O Caso de Nahaniel WuDocumento2 páginasÉtica e Testes Genéticos - O Caso de Nahaniel WuJ Ricardo VeigaAinda não há avaliações
- Alfajor Receita - Pesquisa GoogleDocumento1 páginaAlfajor Receita - Pesquisa GoogleIsabela RodriguesAinda não há avaliações
- FAULSTICH, Enilde L. de J. Como Ler, Entender e Redigir Um TextoDocumento118 páginasFAULSTICH, Enilde L. de J. Como Ler, Entender e Redigir Um TextoOPS100% (2)
- Silêncio e Palavra - AmatuzziDocumento16 páginasSilêncio e Palavra - AmatuzziLeandro Santos100% (1)
- Dissertacao Final4 - Soraia - 180118 PDFDocumento97 páginasDissertacao Final4 - Soraia - 180118 PDFSoraia MendesAinda não há avaliações
- DANDARA SujeitoPeriferico DigitalDocumento289 páginasDANDARA SujeitoPeriferico DigitalWesley Fraga100% (1)