Escolar Documentos
Profissional Documentos
Cultura Documentos
Ficha de Trabalho Global - Equilíbrio
Enviado por
Diogo NunesDescrição original:
Título original
Direitos autorais
Formatos disponíveis
Compartilhar este documento
Compartilhar ou incorporar documento
Você considera este documento útil?
Este conteúdo é inapropriado?
Denunciar este documentoDireitos autorais:
Formatos disponíveis
Ficha de Trabalho Global - Equilíbrio
Enviado por
Diogo NunesDireitos autorais:
Formatos disponíveis
Ficha de trabalho Equilíbrio químico – 11º Ano
1. O óxido nítrico, NO, pode ser formado a altas temperaturas, a partir da reação entre o nitrogénio, N2, e o oxigénio, 02,
de acordo com a seguinte equação química: N2 (g) + O2 (g) ) ⇄ 2 NO (g)
Esta reação aconteceu num reator fechado que suporta, no máximo, temperaturas de 2500 K. Na tabela seguinte estão
registados os valores da constante de equilíbrio, Kc, desta reação, medidos para diferentes valores de temperatura.
T/K Kc
2000 1,98 X 10-2
2250 3,64 x 10-2
2500 5,90 x 10-2
1.1 A partir dos valores da tabela acima, faça uma estimativa do valor da temperatura da reação de formação do NO,
quando o valor da constante de equilíbrio é de 5,02x 10-2. Utilize a máquina de calcular gráfica, assumindo uma variação
linear entre as grandezas consideradas.
Apresente a equação da reta obtida e o valor estimado da temperatura.
1.2 Considere que, à temperatura de 2000 K, se misturaram no reator iguais quantidades de N2 e 02. Atingido o equilíbrio,
a quantidade de NO era de 0,6 moI. Calcule as quantidades iniciais de N2 e 02, apresentando todas as etapas de resolução.
1.3 No limite de temperatura suportado pelo reator, o sistema sofreu uma perturbação. O valor do quociente da reação
calculado com os valores das novas concentrações das espécies envolvidas correspondia a 5,90 x 10-2.
Indique, justificando, que tipo de perturbação foi aplicada ao sistema.
2. Num balão fechado e indeformável, de 5,0 dm3, a uma dada temperatura, introduziram-se 0,46 g de N204(g), que se dissociou
em NO2 (g), de acordo com a seguinte equação química: N2O4 (g) ⇄ 2 NO2 (g)
Quando se atingiu o equilíbrio, verificou-se que se tinham dissociado 42% do N204 colocado inicialmente no balão.
2.1 Determine a quantidade de matéria de N204 existente no estado de equilíbrio.
2.2 Calcule a concentração de dióxido de nitrogénio no estado de equilíbrio.
3. Considere a reação seguinte: 4 HCl (g) + 02 (g) ⇄ 2 H2O(g) + 2 Cl2 (g)
Num recipiente fechado de capacidade igual a 4,0 dm3 foram encerrados 0,16 mol de HCl (g) e 0,080 mol de 02 (g) que
reagiram até atingirem o equilíbrio, a uma dada temperatura.
No equilíbrio a concentração de HCl é de 1,5 x 10-2 moldm-3, a essa temperatura.
Calcule:
3.1 A percentagem de HCl (g) que se dissociou.
3.2 A constante de equilíbrio a esta temperatura.
4. O amoníaco, NH3, é uma substância inorgânica importante, sendo um dos compostos de azoto mais bem conhecidos.
Obtém-se industrialmente através do processo de Haber-Bosch, fazendo reagir, em condições apropriadas, hidrogénio e azoto
gasosos. A síntese do amoníaco pode ser representada por:
N2(g) + H2(g) ⇄ 2 NH3(g)
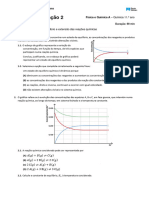
O gráfico apresentado na figura traduz o modo como varia a constante de
equilíbrio, K c, daquela reação, em função da temperatura, T.
Para a reação em causa, compare a energia envolvida na rutura e na formação das
ligações químicas, fundamentando a sua resposta a partir da informação fornecida
pelo gráfico.
5. Um sistema químico muito estudado é o que corresponde à reação entre o hidrogénio gasoso e o vapor de íodo para formar
iodeto de hidrogénio, HI. Esta reação reversível é traduzida pela seguinte equação química:
Tal como qualquer outro sistema químico em equilíbrio, também este sistema é capaz de evoluir num sentido ou noutro, devido
a algumas alterações que nele se produzam.
5.1 À temperatura de 430°C, fez-se reagir 0,500 mol de H2 e 0,500 mol
de I2(g), num recipiente fechado, de capacidade igual a 1,00 L.
A reação química progrediu, tendo-se estabelecido, num dado instante,
uma situação de equilíbrio. Este equilíbrio foi, no instante t5 ,
perturbado.
Simulando esta situação experimental, obteve-se o gráfico apresentado
na figura, que representa a evolução das concentrações dos reagentes e
do produto da reação, ao longo do tempo, à mesma temperatura.
Tendo em conta a informação fornecida pelo gráfico, selecione a
alternativa que completa corretamente a frase seguinte.
Os instantes que correspondem ao estabelecimento do equilíbrio
inicial, à igualdade das concentrações de reagentes e de produto, e à perturbação imposta ao sistema são, respetivamente, ...
(A) ... t1 , t3 e t5 (B) ... t3, t1 e t6 (C) ... t3, t1 e t5 (D) ... t2, t4 e t6
5.2 A que perturbação ficou sujeito o sistema? Em que sentido evolui o sistema após ter sido perturbado?
5.3 Escreva a expressão que traduz a constante de equilíbrio, Kc , da reação em causa.
Utilizando a informação contida no gráfico, calcule o valor dessa constante, à temperatura referida.
Apresente todas as etapas de resolução.
1.
5.4 Indique a opção que traduz a leitura correta do gráfico.
(A) A adição de diiodo em t5 , torna a solução incolor.
(B) A adição de di-hidrogénio em t6 acentua a cor violeta do sistema.
(C) A adição de di-hidrogénio em t6 conduz o sistema a um estado de equilíbrio.
(D) A adição de di-hidrogénio em t5, provoca um aumento da concentração de HI no novo estado de equilíbrio.
6. Considere a reação de equilíbrio que envolve o sulfureto de hidrogénio, traduzida pela seguinte equação química:
2 H2S (g) + 302 (g) ⇄ 2 H2O(g) + 2 SO2 (g) H= - 1036 KJ
6.1 Das alterações seguintes, indique aquelas que favorecem) a quantidade de S02 produzida.
(A) Diminuição da temperatura do sistema.
(B) Aumento da pressão do sistema.
(C) Adição de dióxido de enxofre ao sistema.
(D) Remoção de dioxigénio do sistema.
6.2 Selecione a opção que completa corretamente a seguinte frase.
Um aumento da temperatura do sistema reacional, mantendo o volume constante, ...
(A) ... não altera o valor da constante de equilíbrio químico.
(B) ... não altera o rendimento da reação.
(C) … provoca a diminuição da concentração de todas as espécies químicas presentes no sistema reacional.
(D) ... provoca uma variação do valor da constante de equilíbrio químico.
Você também pode gostar
- Ficha 2 - Equilíbrio QuímicoDocumento5 páginasFicha 2 - Equilíbrio QuímicoBeatriz AmorimAinda não há avaliações
- Equilíbrio QuímicoDocumento17 páginasEquilíbrio QuímicojulioAinda não há avaliações
- Exercícios de Aplicação - Equilíbrio Químico 3Documento4 páginasExercícios de Aplicação - Equilíbrio Químico 3sevinchrajabova027Ainda não há avaliações
- FICHA 2 - Equilibrio QuimicoDocumento4 páginasFICHA 2 - Equilibrio QuimicoINES DE LEMOS SARGENTO E ALMEIDAAinda não há avaliações
- 11FQA Ficha Trab Ini Q1.2 - N.º 2Documento4 páginas11FQA Ficha Trab Ini Q1.2 - N.º 2Andrei GalanAinda não há avaliações
- 11FQA Ficha Trab Ini Q1.2 - N.º 2Documento4 páginas11FQA Ficha Trab Ini Q1.2 - N.º 2carlosAinda não há avaliações
- Equilíbrio QuímicoDocumento7 páginasEquilíbrio QuímicoVânia Maria SantosAinda não há avaliações
- FT - FQA11 - Equilíbrio QuímicoDocumento5 páginasFT - FQA11 - Equilíbrio QuímicoRui RodriguesAinda não há avaliações
- FichaprinchatDocumento4 páginasFichaprinchatAndrei GalanAinda não há avaliações
- Ficha 2 - QuímicaDocumento6 páginasFicha 2 - QuímicaBeatriz VenâncioAinda não há avaliações
- Ficha6 QuímicaDocumento4 páginasFicha6 QuímicaRodrigo lopesAinda não há avaliações
- 11FQA Ficha Formativa Q1.2Documento3 páginas11FQA Ficha Formativa Q1.2Andrei GalanAinda não há avaliações
- ExercíciosDocumento6 páginasExercíciosCaroline Paglia NadalAinda não há avaliações
- (4.2.1) 11Q - CAP - (Fichas 1.2)Documento25 páginas(4.2.1) 11Q - CAP - (Fichas 1.2)Catarina FerreiraAinda não há avaliações
- Q2-Ficha Trabalho Nº2Documento3 páginasQ2-Ficha Trabalho Nº2Ana SilvaAinda não há avaliações
- 11FQA Ficha Trab Ini Q1.2 - N.º 2 - SoluçãoDocumento8 páginas11FQA Ficha Trab Ini Q1.2 - N.º 2 - SoluçãoLara JesusAinda não há avaliações
- Go Tarefa Semanal Curso 5e8b7a80d74e8Documento22 páginasGo Tarefa Semanal Curso 5e8b7a80d74e8rafinhagebrinAinda não há avaliações
- Lista de Equilíbrio Químico PDFDocumento3 páginasLista de Equilíbrio Químico PDFMarcelo SatorresAinda não há avaliações
- Ficha EquilibrioDocumento12 páginasFicha EquilibrioPaulo SantosAinda não há avaliações
- Ficha 2 - Extensão Das ReaçõesDocumento3 páginasFicha 2 - Extensão Das ReaçõesRafael TeixeiraAinda não há avaliações
- Atividades Globais SD2Documento4 páginasAtividades Globais SD2milenerato2240Ainda não há avaliações
- Equilibrio QuimicoDocumento4 páginasEquilibrio QuimicoEfraim Nobre SoaresAinda não há avaliações
- Ficha de Trabalho 7 - Aspetos Quantitativos Das RQ e Equilíbrio Químico e Extensão Das RQDocumento4 páginasFicha de Trabalho 7 - Aspetos Quantitativos Das RQ e Equilíbrio Químico e Extensão Das RQFranciscaAinda não há avaliações
- FIcha - Equlibrio Quimico-2Documento3 páginasFIcha - Equlibrio Quimico-2Alda Maria Dinis Ginja100% (1)
- Ficha NR 3 PerguntasDocumento5 páginasFicha NR 3 PerguntasernildoernestomalajissaAinda não há avaliações
- Teste 1 (2019) - QuímicaDocumento6 páginasTeste 1 (2019) - QuímicaLuis VarelaAinda não há avaliações
- Ficha - 14 - Estado de Equilíbrio e Extensão Das Reações Químicas - AlunoDocumento3 páginasFicha - 14 - Estado de Equilíbrio e Extensão Das Reações Químicas - AlunoJoão MoreiraAinda não há avaliações
- Teste 1 (2018-2019)Documento9 páginasTeste 1 (2018-2019)Luísa Carmo100% (1)
- Ficha Formativa - Equilíbrio QuímicoDocumento3 páginasFicha Formativa - Equilíbrio Químiconelson_honorioAinda não há avaliações
- Teste 4 v1Documento5 páginasTeste 4 v1André MatosAinda não há avaliações
- 11FQA Ficha Trab Ini Q1.2 - N.º 1Documento4 páginas11FQA Ficha Trab Ini Q1.2 - N.º 1Quim Caçador TransdufiAinda não há avaliações
- 5 Ficha de Trabalho - Cálculos Estequiométricos e Equilíbrio Químico - 12-13 PDFDocumento3 páginas5 Ficha de Trabalho - Cálculos Estequiométricos e Equilíbrio Químico - 12-13 PDFMaria Do Carmo BrazAinda não há avaliações
- Questões Objetivas CinéticaDocumento10 páginasQuestões Objetivas CinéticaMônica Cecato100% (1)
- Pcasd - Uploads - Rogerio - Arquivos - Lista 12 - Equilbrio Qumico - Constante de Equlibrio KCDocumento9 páginasPcasd - Uploads - Rogerio - Arquivos - Lista 12 - Equilbrio Qumico - Constante de Equlibrio KCRaisson HolandaAinda não há avaliações
- Equilibrio Quimico e Deslocamento de EquilibrioDocumento6 páginasEquilibrio Quimico e Deslocamento de Equilibrioshiro mimiAinda não há avaliações
- Ae q11 Fich Form 1Documento5 páginasAe q11 Fich Form 1carla50% (2)
- Caderno - 11Q - Equilíbrio Químico - Trofa - 20-21Documento17 páginasCaderno - 11Q - Equilíbrio Químico - Trofa - 20-21jotaAinda não há avaliações
- Ficha 1 - Equilíbrio QuímicoDocumento5 páginasFicha 1 - Equilíbrio QuímicoBeatriz AmorimAinda não há avaliações
- Teste - 2 - PORTO EDITORA 2023 - Enunciado - sd2 - Estado - Equilibrio - Extensao - Reacoes - QuimicasDocumento6 páginasTeste - 2 - PORTO EDITORA 2023 - Enunciado - sd2 - Estado - Equilibrio - Extensao - Reacoes - QuimicasLuis VarelaAinda não há avaliações
- Trabalho de Química 3º ANODocumento9 páginasTrabalho de Química 3º ANOdubequimaoAinda não há avaliações
- Lista Equilibrio Quimico 2012Documento12 páginasLista Equilibrio Quimico 2012Luelc SouzaAinda não há avaliações
- LEQuímica EquilíbrioDocumento5 páginasLEQuímica EquilíbrioLussandra MarquezAinda não há avaliações
- Alfa - Módulo 42Documento22 páginasAlfa - Módulo 42Deborah LGAinda não há avaliações
- FT - Princípio de Le ChâtelierDocumento2 páginasFT - Princípio de Le ChâtelierAndré MatosAinda não há avaliações
- 1 Ae q11 Teste5 v1Documento14 páginas1 Ae q11 Teste5 v1Luísa CarmoAinda não há avaliações
- Exercícios Equilíbrio QuímicoDocumento3 páginasExercícios Equilíbrio QuímicoDayane TelesAinda não há avaliações
- Ficha Formativa - UFCD 6708Documento5 páginasFicha Formativa - UFCD 6708cristinajlopesAinda não há avaliações
- Entalpia de NeutralizaçãoDocumento13 páginasEntalpia de NeutralizaçãoHélio BellagambaAinda não há avaliações
- Ae q11 Fich Form 1Documento5 páginasAe q11 Fich Form 1Ana Raquel PintoAinda não há avaliações
- Calor de ReaçãoDocumento4 páginasCalor de ReaçãoMatheus DiasAinda não há avaliações
- IEx Equilíbrio EMDocumento6 páginasIEx Equilíbrio EMChristian CostaAinda não há avaliações
- Equilibrio QuimicoDocumento2 páginasEquilibrio QuimicomuriloneaimeAinda não há avaliações
- 3.1 GABARITO Exercícios Equilíbrio QuímicoDocumento4 páginas3.1 GABARITO Exercícios Equilíbrio QuímicoDayane TelesAinda não há avaliações
- Ae q11 Fich Form 1Documento5 páginasAe q11 Fich Form 1Mariana Coelho100% (4)
- FT6 - Aspetos Quantitativos Das Reações QuímicasDocumento4 páginasFT6 - Aspetos Quantitativos Das Reações QuímicasCarlos Eduardo FukudaAinda não há avaliações
- Análise das tensões em estruturas de concreto devido a variações de temperatura entre os anos de 2009 e 2018No EverandAnálise das tensões em estruturas de concreto devido a variações de temperatura entre os anos de 2009 e 2018Ainda não há avaliações
- B Omer AngDocumento1 páginaB Omer AngDiogo NunesAinda não há avaliações
- Gião Apresentaçao Oral - DiogoNunesDocumento2 páginasGião Apresentaçao Oral - DiogoNunesDiogo NunesAinda não há avaliações
- De StijlDocumento6 páginasDe StijlDiogo NunesAinda não há avaliações
- Ficha Trabalho - HumeDocumento2 páginasFicha Trabalho - HumeDiogo NunesAinda não há avaliações
- Projeto Do Trabalho CidadaniaDocumento5 páginasProjeto Do Trabalho CidadaniaDiogo NunesAinda não há avaliações
- Rubrica EletromagnetismoDocumento5 páginasRubrica EletromagnetismoDiogo NunesAinda não há avaliações
- Apresentação Oral - TemasDocumento1 páginaApresentação Oral - TemasDiogo NunesAinda não há avaliações
- Roteiro CompletoDocumento46 páginasRoteiro CompletoDiogo NunesAinda não há avaliações
- Diogo Nunes - 12º ADocumento1 páginaDiogo Nunes - 12º ADiogo NunesAinda não há avaliações
- NBR 10007Documento14 páginasNBR 10007Heroi VicenteAinda não há avaliações
- NBR 5410 - Instalações Elétricas de Baixa TensãoDocumento2 páginasNBR 5410 - Instalações Elétricas de Baixa TensãoGustavo Dos Santos LimaAinda não há avaliações
- Apostila Instrumentação - Ifpa-CmiDocumento94 páginasApostila Instrumentação - Ifpa-CmiMikéias KbralAinda não há avaliações
- Quimica - Propiedades FisicasDocumento7 páginasQuimica - Propiedades FisicasLThalía Gachúz HdezAinda não há avaliações
- TermoquimicaDocumento51 páginasTermoquimicaluizAinda não há avaliações
- Especif Técn Do Cbmac Etcb (Cópia)Documento106 páginasEspecif Técn Do Cbmac Etcb (Cópia)renatosantosacAinda não há avaliações
- A04 Caracterização de Partículas Câmaras Gravitacionais CiclonesDocumento58 páginasA04 Caracterização de Partículas Câmaras Gravitacionais CiclonesVictor Patrick Batista100% (1)
- Dicionario Da ConstrucaoDocumento114 páginasDicionario Da ConstrucaoIgor SaraivaAinda não há avaliações
- Relatório de FQ Exp. DIFUSÃO DE GASESDocumento10 páginasRelatório de FQ Exp. DIFUSÃO DE GASESLeonardo AndradeAinda não há avaliações
- 24 PF TraçagemDocumento12 páginas24 PF TraçagemJobson GomesAinda não há avaliações
- Relatório PectinasesDocumento5 páginasRelatório PectinasesPatríciaPradoAinda não há avaliações
- Apresentação de Casing para Marinização e Ar CondicionadosDocumento3 páginasApresentação de Casing para Marinização e Ar CondicionadosTenda Dos MarujosAinda não há avaliações
- MM h60 20sw Port PDFDocumento17 páginasMM h60 20sw Port PDFRicardo Martins SilvaAinda não há avaliações
- 2020 Ligacao Quimica 11aDocumento13 páginas2020 Ligacao Quimica 11aIsac ManuelAinda não há avaliações
- Instalacao Eletrica RaioxDocumento20 páginasInstalacao Eletrica RaioxDebora Pereira Salgado100% (2)
- Relatorio 1 Ipl Balança AnalíticaDocumento5 páginasRelatorio 1 Ipl Balança AnalíticaJulia XimenesAinda não há avaliações
- Lista de Exercícios N1 Lista 2 - Fundamentos de Mecânica Dos SolosDocumento4 páginasLista de Exercícios N1 Lista 2 - Fundamentos de Mecânica Dos SolosRicardo Diniz MagroAinda não há avaliações
- Relatorio 1 InorgDocumento7 páginasRelatorio 1 InorgReyvisson ViniciusAinda não há avaliações
- Catalogo SOLOTEST Solos PDFDocumento27 páginasCatalogo SOLOTEST Solos PDFJose RibeiroAinda não há avaliações
- Tubos Com Aço PatinávelDocumento8 páginasTubos Com Aço PatinávelBludo LuccianoAinda não há avaliações
- Exercicios Instrumentação1Documento2 páginasExercicios Instrumentação1sharedmanfull6410Ainda não há avaliações
- QAE-Apostila de Química ExperimentalDocumento71 páginasQAE-Apostila de Química Experimentallindojamir02Ainda não há avaliações
- Código ANSIDocumento5 páginasCódigo ANSIJamie SmithAinda não há avaliações
- Asma Ocupacional PDFDocumento65 páginasAsma Ocupacional PDFClayton Baruch HashemAinda não há avaliações
- Química - Pré-Vestibular Impacto - Introdução Às Reações IDocumento2 páginasQuímica - Pré-Vestibular Impacto - Introdução Às Reações IQuímica Qui100% (2)
- Segunda Lista de Exercicios1Documento3 páginasSegunda Lista de Exercicios1CamilaAinda não há avaliações
- 5eaafa806e818FT.13009.01 ISOVIT-REV-FINO MEDIODocumento3 páginas5eaafa806e818FT.13009.01 ISOVIT-REV-FINO MEDIOCarlos AlvesAinda não há avaliações
- Notas de Aula de Eletrostática e Eletrodinâmica Com Todos Os Exercícios ResolvidosDocumento94 páginasNotas de Aula de Eletrostática e Eletrodinâmica Com Todos Os Exercícios ResolvidosedgarAinda não há avaliações
- Hidrocarbonetos Ramificado. Lista de ExercíciosDocumento10 páginasHidrocarbonetos Ramificado. Lista de ExercíciosDenis Claudio Silva BarrosAinda não há avaliações
- TamisaçãoDocumento12 páginasTamisaçãoDaniela BatistaAinda não há avaliações