Escolar Documentos
Profissional Documentos
Cultura Documentos
APOSTILA TABELA PERIÓDICA 2023 Promaf 9 Ano
Enviado por
João Lucas0 notas0% acharam este documento útil (0 voto)
15 visualizações2 páginasTítulo original
APOSTILA TABELA PERIÓDICA 2023 promaf 9 ano
Direitos autorais
© © All Rights Reserved
Formatos disponíveis
PDF, TXT ou leia online no Scribd
Compartilhar este documento
Compartilhar ou incorporar documento
Você considera este documento útil?
Este conteúdo é inapropriado?
Denunciar este documentoDireitos autorais:
© All Rights Reserved
Formatos disponíveis
Baixe no formato PDF, TXT ou leia online no Scribd
0 notas0% acharam este documento útil (0 voto)
15 visualizações2 páginasAPOSTILA TABELA PERIÓDICA 2023 Promaf 9 Ano
Enviado por
João LucasDireitos autorais:
© All Rights Reserved
Formatos disponíveis
Baixe no formato PDF, TXT ou leia online no Scribd
Você está na página 1de 2
“A melhor Experiência é o amor de DeUS”.
ESCOLA ESTADUAL DE E.F.M. PROMAF
PROFESSOR: MIGUEL NIVALDO
ALUNO(A):
__ nº
DATA: ___/___/______ TABELA PERIÓDICA 9°ANO
TURMA:
CLASSIFICAÇÃO PERIÓDICA DOS ELEMENTOS ✓ Família ou Grupo “B”
Encontra-se na parte central da tabela, sendo
enumerados de 1B até 8B. Os elementos destes grupos
É a organização dos elementos químicos em
são chamados elementos de transição. Para estes
linhas e colunas.
elementos a distribuição eletrônica termina no subnível
É importante para o estudo de Química e foi
“d” ou “f”.
idealizada por Mendeleev em 1869.
As duas fileiras localizadas à parta da tabela constituem
Cada elemento pertence a um período e a u m
a
os elementos actinídios e lantinídios, denominados de
família.
elementos de transição interna.
A tabela periódica está organizada em ordem
crescente de número atômico (Z)
b) PERÍODO
Cada fila horizontal da Tabela periódica, reunindo
1 –DIVISÃO DA TABELA PERIÓDICA
elementos da seqüência de seus números atômicos.
A atual tabela periódica dos elementos é dividida
em famílias ou grupos e períodos.
2–OUTRA DIVISÃO DA TABELA PERIÓDICA
A tabela periódica também está dividida em 4
a) FAMÍLIA OU GRUPO
grandes grupos: metais, ametais ou não metais, gases
São as 18 colunas verticais da tabela periódica. Os
nobres e hidrogênio. Veja o esquema abaixo: G
elementos de uma mesma família são quimicamente A
semelhantes. S
H E
AMETAIS S
N
A IUPAC recomenda atualmente a numeração dos O
grupos em algarismos arábicos de 1 a 18, da esquerda B
para a direita, sem distinção de A e B. R
✓ Família ou Grupo “A” METAIS E
S
São enumerados de 1A até 8A (ou zero). Seus
elementos são conhecidos como representativos.
Obs: Para os elementos representativos (Grupo A) a
distribuição eletrônica termina no subnível “s” ou “p”.
METAIS
Atenção!!! O número de elétrons da última camada
equivale ao número da família. METAIS
a) METAIS: são elementos geralmente sólidos,
Nº de
brilhosos, bons condutores de calor e eletricidade,
elétrons da ELEMENTOS
dúcteis (fáceis de transformar em fios) e maleáveis
última “MAIS
NOME DAS FAMÍLIAS (fáceis de transformar em lâminas). Em geral
camada COMUNS”
apresentam 1, 2 e 3 elétrons na camada de valência,
perdem elétrons (eletropositivos) da camada de
1A ou 1: Metais Alcalinos 1 e- Li, Na, K valência transformando-se em cátions.
2A ou 2:Metais Alcalino- 2e- Mg, Ca
Terrosos b) AMETAIS OU NÃO-METAIS: são elementos que
formam materiais não sólidos, não brilhosos, ruins
3A ou 13: Família do 3e- B, Al
condutores de calor e eletricidade, não dúcteis e não
boro
maleáveis. Possuem 4, 5, 6 e 7 elétrons na camada de
4A ou 14: Família do 4e- N, , As
valência, ganham elétrons (eletronegativos)
Nitrogênio transformando-se em ânions.
5ª ou 15: Família do 5e- C,Si, Pb
carbono c) GASES NOBRES: são gases raros, esses elementos
não formam compostos espontaneamente, pois são
6A ou 16: Calcogênios 6e- 0, S muito estáveis na forma isolada. Possuem 8 elétrons na
7A ou 17: Halogênios 7e- F, Cl, Br, I camada de valência, com exceção do He (hélio) que
8A, 0 ou 18: Gases 8e- He, Ne possui apenas 2 e-.
Nobres
d) HIDROGÊNIO: é um elemento atípico ,não se
enquadra em nenhum grupo da tabela periódica. É o
mais simples dos átomos, possui apenas um nível de
energia, com 1 único elétron.
Você também pode gostar
- Tabela Periódica 2022Documento45 páginasTabela Periódica 2022qeduardo.ferreiraAinda não há avaliações
- Tabela PeriodicaDocumento17 páginasTabela PeriodicaMayanderson RodriguesAinda não há avaliações
- Aula 3 - Tabela PeriódicaDocumento4 páginasAula 3 - Tabela PeriódicaMorgana VasconcellosAinda não há avaliações
- Slides Tabela Periodica 2Documento17 páginasSlides Tabela Periodica 2Aliane FormigaAinda não há avaliações
- CSL 9 AnoDocumento34 páginasCSL 9 AnoKleyton LopesAinda não há avaliações
- AULA TABELA PERIÓDICA imprimirDocumento2 páginasAULA TABELA PERIÓDICA imprimirCarlos Henrique Marques MonteiroAinda não há avaliações
- Aula 4 Tabela Periódica e ExercíciosDocumento30 páginasAula 4 Tabela Periódica e ExercíciosTamires CalgaroAinda não há avaliações
- Tabela PeriódicaDocumento25 páginasTabela PeriódicaLaiz OliveiraAinda não há avaliações
- Classificação Periódica Dos Elementos Químicos 1º AnoDocumento4 páginasClassificação Periódica Dos Elementos Químicos 1º AnoAlbertina VieiraAinda não há avaliações
- Medicina Quimica Classificacao Periodica 20 02 2017Documento11 páginasMedicina Quimica Classificacao Periodica 20 02 2017Luis Filipi RodriguesAinda não há avaliações
- Organização Periódica Dos ElementosDocumento21 páginasOrganização Periódica Dos ElementosAlex CotrimAinda não há avaliações
- Apostila Tabela Periódica 3Documento6 páginasApostila Tabela Periódica 3be9593690Ainda não há avaliações
- Propriedades Periódicas da Tabela PeriódicaDocumento36 páginasPropriedades Periódicas da Tabela PeriódicaPereira CarlosAinda não há avaliações
- Estrutura Atômica e Propriedades PeriódicasDocumento36 páginasEstrutura Atômica e Propriedades PeriódicasCarlos RomãoAinda não há avaliações
- Fichas de apoioDocumento22 páginasFichas de apoioagrapacanatejugaAinda não há avaliações
- Tabela Periódica - MaterialDocumento5 páginasTabela Periódica - MaterialGabriela Rodrigues GonçalvesAinda não há avaliações
- Tabela periódica Atual - 1º ano do Ensino MédioDocumento46 páginasTabela periódica Atual - 1º ano do Ensino Médionei nunesAinda não há avaliações
- 28-06 Ciências Fernando e Gisele 9 AnosDocumento5 páginas28-06 Ciências Fernando e Gisele 9 AnosGisele VasconcellosAinda não há avaliações
- Resumo QuímicaDocumento4 páginasResumo QuímicalumenbrunoAinda não há avaliações
- Tabela PeriódicaDocumento1 páginaTabela PeriódicaSAYZINxl100% (1)
- Tabela periódica dos elementos químicosDocumento18 páginasTabela periódica dos elementos químicosAmália AnjosAinda não há avaliações
- Tabela Periódica 2024Documento30 páginasTabela Periódica 2024Dara SavioAinda não há avaliações
- Organização da Tabela PeriódicaDocumento6 páginasOrganização da Tabela PeriódicaJakendry 12Ainda não há avaliações
- Química - Aula 04 - Tabela Periódica PDFDocumento12 páginasQuímica - Aula 04 - Tabela Periódica PDFDJNUNESAinda não há avaliações
- Tabela periódica dos elementos: propriedades e organizaçãoDocumento27 páginasTabela periódica dos elementos: propriedades e organizaçãoraphael12stringsAinda não há avaliações
- Tabela PeriodicaDocumento3 páginasTabela PeriodicaMarcelo FaustinoAinda não há avaliações
- A Tabela Periódica: Organização e Propriedades PeriódicasDocumento20 páginasA Tabela Periódica: Organização e Propriedades PeriódicasCleyton SantosAinda não há avaliações
- Tabela PeriódicaDocumento9 páginasTabela Periódicadavidsousa1627Ainda não há avaliações
- Tabela Periódica - AulaDocumento23 páginasTabela Periódica - AulaReno EduardoAinda não há avaliações
- Tabela-Periodica-Caracteristicas-Gerais-IIDocumento2 páginasTabela-Periodica-Caracteristicas-Gerais-IIMarcelo GfteamAinda não há avaliações
- Estudo Dirigido 1 AnoDocumento4 páginasEstudo Dirigido 1 AnokattiaeugeniaAinda não há avaliações
- APOSTILA QUÍMICA 1 - Tabela Periodica IFMSDocumento6 páginasAPOSTILA QUÍMICA 1 - Tabela Periodica IFMSGeilson SilvaAinda não há avaliações
- 5.2_Aula_Tabela _Periodica RESUMODocumento3 páginas5.2_Aula_Tabela _Periodica RESUMOMarcio NascimentoAinda não há avaliações
- Apostila A9 e A10 - Tabela PeriódicaDocumento24 páginasApostila A9 e A10 - Tabela PeriódicaJouffre NetoAinda não há avaliações
- A Tabela PeriódicaDocumento44 páginasA Tabela PeriódicaPaulaAinda não há avaliações
- QuímicaDocumento12 páginasQuímicaRicely FeitosaAinda não há avaliações
- Resumo de Química Geral BásicaDocumento6 páginasResumo de Química Geral BásicaRonaldoPiresAinda não há avaliações
- Tabela Periodica 1 Ano SER BDocumento3 páginasTabela Periodica 1 Ano SER BDébora OlímpioAinda não há avaliações
- Tabela Periódica ComentadaDocumento8 páginasTabela Periódica ComentadaEverton AlvesAinda não há avaliações
- 9_301_-_9o_ano_aula_07_2024Documento17 páginas9_301_-_9o_ano_aula_07_2024Isabelly Alves Santos AlberghiniAinda não há avaliações
- Localização de elementos na tabela periódicaDocumento9 páginasLocalização de elementos na tabela periódicaDiógenes Jacinto DJAinda não há avaliações
- Cap 2 - Periodicidade Química MILENA 230619 142437Documento35 páginasCap 2 - Periodicidade Química MILENA 230619 142437Israel LopesAinda não há avaliações
- Tabela PeriódicaDocumento6 páginasTabela PeriódicaJrangelAinda não há avaliações
- Tabela Periódica - 9ANODocumento19 páginasTabela Periódica - 9ANOMárcia VidigalAinda não há avaliações
- Trabalho de Química 02Documento10 páginasTrabalho de Química 02Diógenes Jacinto DJAinda não há avaliações
- Aul at Abel A Periodic ADocumento33 páginasAul at Abel A Periodic ALuiz R SimaoAinda não há avaliações
- 7 - Lista de Exercícios - 2021-TABELADocumento10 páginas7 - Lista de Exercícios - 2021-TABELAJosé LourençoAinda não há avaliações
- Quimica 2 - Texto - Avaliação 4 - Ceja LeilaDocumento6 páginasQuimica 2 - Texto - Avaliação 4 - Ceja LeilaLEILA PARENTEAinda não há avaliações
- Química 1 ano VA 1Documento42 páginasQuímica 1 ano VA 1lazaro.v.crispimAinda não há avaliações
- Classificacao Periodica Dos ElementosDocumento32 páginasClassificacao Periodica Dos ElementosJuliane Froncheti de MouraAinda não há avaliações
- TABELA PERIÓDICA - 101 AnosDocumento5 páginasTABELA PERIÓDICA - 101 AnosAndria TuraAinda não há avaliações
- Tabela Periodica AtualizadaDocumento16 páginasTabela Periodica AtualizadaFernanda LiraAinda não há avaliações
- Quimica 4Documento1 páginaQuimica 4Marlon BrunoAinda não há avaliações
- 11015017012017quimica Inorganica IDocumento22 páginas11015017012017quimica Inorganica Igabriel.brivAinda não há avaliações
- Tabela PeriódicaDocumento41 páginasTabela PeriódicaSarahGiselleMedeirosLimaAinda não há avaliações
- Tabela Periã DicaDocumento13 páginasTabela Periã DicaSeren IketaniAinda não há avaliações
- Propriedades periódicas e histórico da tabela periódicaDocumento12 páginasPropriedades periódicas e histórico da tabela periódicaErik Spam100% (1)
- SONDA ROTATIVA CHECK LIST Atualizada 08 06 2020Documento1 páginaSONDA ROTATIVA CHECK LIST Atualizada 08 06 2020Marcos Antonio FelisardoAinda não há avaliações
- O significado cultural do lenço de cabeça afro-americanoDocumento22 páginasO significado cultural do lenço de cabeça afro-americanoLuciana GorgonhaAinda não há avaliações
- Resumo+7ºDocumento4 páginasResumo+7ºCatia RosaAinda não há avaliações
- Aula 09.replicação Do DNADocumento42 páginasAula 09.replicação Do DNArmdsAinda não há avaliações
- Curso Técnico em Eletrotécnica: EletricidadeDocumento161 páginasCurso Técnico em Eletrotécnica: EletricidadeferanbaAinda não há avaliações
- Radiestesia - Reiki - e - Radiestesia - ApostilaDocumento368 páginasRadiestesia - Reiki - e - Radiestesia - ApostilaANDRÔMEDA.Ainda não há avaliações
- Autoridade Do CrenteDocumento21 páginasAutoridade Do CrenteedivarbarrosoAinda não há avaliações
- 6ºano Slides Aula 03Documento12 páginas6ºano Slides Aula 03MICHIELI OLIVEIRA RIBEIROAinda não há avaliações
- Plano de Atividade de Estágio Não ObrigatórioDocumento3 páginasPlano de Atividade de Estágio Não ObrigatórioJose CiceroAinda não há avaliações
- Equipamentos para corte e recolha de forragensDocumento26 páginasEquipamentos para corte e recolha de forragensAndré QuirinoAinda não há avaliações
- VampiroDocumento79 páginasVampiroLuiz Henrique Matias MarcondesAinda não há avaliações
- Unicesumar - Atividade 04 - GODocumento4 páginasUnicesumar - Atividade 04 - GOGabrielAinda não há avaliações
- Grande Hino A AtonDocumento20 páginasGrande Hino A AtonFrank C. SilvaAinda não há avaliações
- Simplesmente Sobrenatural - Rose Nascimento - LETRAS - MusDocumento4 páginasSimplesmente Sobrenatural - Rose Nascimento - LETRAS - MusmesaxmelAinda não há avaliações
- Regime de Lubrificação PDFDocumento2 páginasRegime de Lubrificação PDFMarcelo PereiraAinda não há avaliações
- Regras lotação servidores educação AMDocumento6 páginasRegras lotação servidores educação AMDanielaCarvalhoAinda não há avaliações
- EJA e sua importância socialDocumento82 páginasEJA e sua importância socialJose Roberto Junior Costa100% (1)
- Diagnóstico tridimensional da faceDocumento180 páginasDiagnóstico tridimensional da facePaula Andrea MonroyAinda não há avaliações
- 1946 - 1964 A Experiência Democrática No BrasilDocumento8 páginas1946 - 1964 A Experiência Democrática No BrasilJosé Renato TeixeiraAinda não há avaliações
- Aula 7 - Farmacodinâmica 1 (Odontologia 2023 - 1)Documento14 páginasAula 7 - Farmacodinâmica 1 (Odontologia 2023 - 1)Júnia Rosa De SouzaAinda não há avaliações
- Manual Procedimentos - Rodopar - FinanceiroDocumento37 páginasManual Procedimentos - Rodopar - Financeirofinanceiro escolha75% (4)
- Heterósidos cardíacos: estrutura, classificação e atividadeDocumento30 páginasHeterósidos cardíacos: estrutura, classificação e atividadeIsabela Honorato100% (1)
- (Aluno) Av. Form Mat 2anoDocumento11 páginas(Aluno) Av. Form Mat 2anoFernanda Lima de Pinho Reis ReisAinda não há avaliações
- Aula de Desfibrilador-Cardioversor EC TranspDocumento15 páginasAula de Desfibrilador-Cardioversor EC Transpjosuemax3Ainda não há avaliações
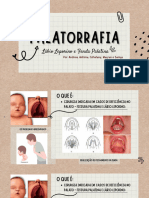
- PALATORRAFIADocumento10 páginasPALATORRAFIAAndréia NunesAinda não há avaliações
- Doc3 - ISO 9001 - Comunicação Interna PDFDocumento3 páginasDoc3 - ISO 9001 - Comunicação Interna PDFzeliaornelasAinda não há avaliações
- Cobrança de dívidaDocumento1 páginaCobrança de dívidaDiego LimeiraAinda não há avaliações
- Questões sobre bullying na escolaDocumento5 páginasQuestões sobre bullying na escolaNarieth Sobral de JesusAinda não há avaliações
- Avaliação intercalar EB 2,3 VisoDocumento1 páginaAvaliação intercalar EB 2,3 VisoprofalexramosAinda não há avaliações
- Filosofia e LiteraturaDocumento270 páginasFilosofia e Literaturapizzolatto100% (1)