Escolar Documentos
Profissional Documentos
Cultura Documentos
FF1 Massa e Tamanho Dos Átomos
Enviado por
Ines CostaDireitos autorais
Formatos disponíveis
Compartilhar este documento
Compartilhar ou incorporar documento
Você considera este documento útil?
Este conteúdo é inapropriado?
Denunciar este documentoDireitos autorais:
Formatos disponíveis
FF1 Massa e Tamanho Dos Átomos
Enviado por
Ines CostaDireitos autorais:
Formatos disponíveis
Escola secundária de Serpa 10º Física e Química A
Ficha 1 – Massa e tamanho dos átomos
Domínio 1: Elementos químicos e sua organização
NOME ___________________________________________________ Turma______ Número______
Consulte a Tabela Periódica, tabelas de constantes e formulários sempre que necessário e salvo
indicação em contrário.
7 μm 224 pm
1400000 km 12700 km 40 a 170 cm 120 μm 35 μm
Glóbulo Átomo
Sol Terra Ser humano Óvulo Célula da pele
vermelho de berílio
Terra
1. Observe as representações de várias estruturas,
Terra Sernas quais estão Óvulo
humano indicadas as
respetivas dimensões. Célula da pele Célula da pele
a) Indique o nome da estrutura
Terra de menor tamanho.
Terra Ser humano
b) A altura de uma criança de 40 cm pode representar-se por:
Sol Óvulo Óvulo
(A) 4000 m. Terra
Sol Terra
(B) 400 m. Ser humano Ser humano
(C) 4,0 m. Terra
Sol Terra Terra
(D) 0,40 m.
c) Um micrómetro (1 μm) é a milésima parte do milímetro o que significa que o
Terra Terra
Sol
tamanho de um glóbulo vermelho é:
(A) 0,7 mm. (B) 0,07 mm. (C) 0,007 mm. (D) 0,0007 mm.
d) Sobre o Sol e a Terra podemos afirmar que um diâmetro: Sol Sol
(A) solar, 1 400 000 km, está mais próximo de dez milhões de quilómetros
do que de um milhão de quilómetros.
(B) solar, 1 400 000 km, está mais próximo de um milhão de quilómetros do
que de dez milhões de quilómetros.
(C) terrestre, 12 700 km, está mais próximo de dez mil quilómetros do que de
doze mil quilómetros.
(D) terrestre, 12 700 km, está mais próximo de doze mil quilómetros do que
de treze mil quilómetros.
e) O tamanho do óvulo humano está mais próximo de qual dos seguintes valores?
(A) 100 μm.
(B) 101 μm.
(C) 102 μm.
(D) 103 μm.
f) Indique a ordem de grandeza expressa em metros, do diâmetro da Terra, da célula
da pele e do átomo de berílio.
2. Indique o número de protões, neutrões e eletrões:
34 2− 27 3+
a) em 22
10Ne, 16S e 13Al .
63
b) em Cu e na prata-107.
c) no isótopo mais abundante do titânio, da figura.
Isótopos
e abundância
relativa
d) indique a posição relativa dos protões, neutrões e eletrões num átomo ou num ião.
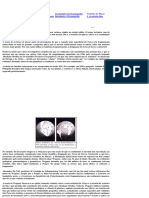
3. Observe a imagem obtida por STM (Scanning
Tunneling Microscope), uma técnica de micros-
copia aplicada à escala atómica, para um cristal
do cloreto de sódio.
a) Determine, em unidade SI, o valor
aproximado do raio iónico do ião cloreto.
b) O raio iónico do ião cloreto, obtido através de
mapas de densidade eletrónica de elevada
resolução, é 1,64 Å. Compare com o
resultado obtido em a) com referência às
respetivas ordens de grandeza.
4. A figura permite fazer uma ideia da pequenez das
unidades estruturais, átomos e moléculas.
Em 18 g de água existem 602 200 000 000 000 000 000 000 moléculas de água e,
como se compreende, não é prático escrever o número de moléculas desta
forma.
a) Indique qual é o número de moléculas de
água que existe em 36 g de água.
b) A massa de uma molécula de estearina é:
6,022 6,022 × 1023
(A) 890 × 1023 g (B) 890
g
890 × 10−23 890
(C) 6,022
g (D) 6,022 × 10−23 g
c) Um átomo de mercúrio é mais:
(A) leve que uma molécula de água e mais pesado que uma molécula de
sacarose.
(B) leve que uma molécula de água e que uma molécula de sacarose.
(C) pesado que uma molécula de água e mais leve que uma molécula de sacarose.
(D) pesado que uma molécula de água e que uma molécula de sacarose.
d) Determine o número de átomos que existe em 36 g de água.
e) Indique a massa atómica relativa do mercúrio e relacione-a com a duodécima
parte da massa do átomo de carbono-12.
5. Na tabela encontram-se informações sobre o silício.
Isótopo Massa isotópica Abundância relativa/Fração
30
Si 29,973770 0,03092
29
Si 28,976495 0,04685
28
Si 27,976927 0,92223
a) Determine a massa atómica relativa média do silício.
Apresente o resultado com cinco algarismos significativos.
b) O valor da massa atómica relativa média para o silício é apresentado na
Tabela Periódica no formato 28,084; 28,086. Tal significa que é válida a
expressão:
(A) Ar(Si) 28,084.
(B) Ar(Si) 28,086.
(C) 28,084 Ar(Si) 28,086.
(D) 28,084 Ar(Si) 28,086.
c) Relacione o resultado obtido em a) com a informação dada em b).
d) Interprete a proximidade do valor da massa atómica relativa do silício com o
valor da massa isotópica do Si-28.
6. Determine a quantidade (número de moles) de átomos que existem em 23,04 g
etanol, C2H6O.
7. Identifique, pelo nome, a substância de fórmula química (Uu)2SO4 sabendo que a
massa molar é 142,01 g/mol, e que Uu não representa o verdadeiro símbolo
químico do elemento.
8. De 28,87 g de uma amostra de ar, 6,72 g são de oxigénio, O2. Considere que o ar
da amostra é constituído apenas por oxigénio e nitrogénio, N2.
a) Determine a fração molar de cada componente na amostra de ar.
b) Determine a fração mássica de cada componente na amostra de ar.
Ano letivo 2020/21
Você também pode gostar
- O Paradoxo de FermiDocumento26 páginasO Paradoxo de FermiajchagasAinda não há avaliações
- Avaliacao Diagnostica Quimica 2 Ano PDFDocumento6 páginasAvaliacao Diagnostica Quimica 2 Ano PDFRoney A. Gomes GomesAinda não há avaliações
- Fichas Formativas # Teste 1Documento20 páginasFichas Formativas # Teste 1Marília Pacheco100% (1)
- Geografia Física de MoçambiqueDocumento15 páginasGeografia Física de MoçambiqueAnilda100% (1)
- F 10-11 Ano (Com SOLUÇÕES, Todas As Unidades), Banco de Questoes Com Itens de Exames PDFDocumento205 páginasF 10-11 Ano (Com SOLUÇÕES, Todas As Unidades), Banco de Questoes Com Itens de Exames PDFSandra DominguesAinda não há avaliações
- Massa Atômica Massa Molecular e Massa Molar 1 Prof Rui MedeirosDocumento3 páginasMassa Atômica Massa Molecular e Massa Molar 1 Prof Rui MedeiroslivisAinda não há avaliações
- Ae rq10 Ficha 1Documento6 páginasAe rq10 Ficha 1Leonor ChoçasAinda não há avaliações
- Testes Globais Editora + SoluçõesDocumento23 páginasTestes Globais Editora + SoluçõesAngela Carvalho50% (2)
- Eq10 Dossie Prof Teste Avaliacao Global 1 EnunciadoDocumento6 páginasEq10 Dossie Prof Teste Avaliacao Global 1 EnunciadoMagda RafaelAinda não há avaliações
- Avaliação de QuímicaDocumento2 páginasAvaliação de QuímicaAngela Cristina Schneider100% (1)
- Ficha Formativa - Mais Questões - e ResoluçãoDocumento15 páginasFicha Formativa - Mais Questões - e ResoluçãoÍris VianaAinda não há avaliações
- qr10 02 Teste Aval 1 sd1 EnunciadoDocumento5 páginasqr10 02 Teste Aval 1 sd1 EnunciadoBeatriz RodriguesAinda não há avaliações
- Ficha 1Documento11 páginasFicha 1João PauloAinda não há avaliações
- 10Q - CadProf - Ficha 1 Massa e Tamanho AtomosDocumento3 páginas10Q - CadProf - Ficha 1 Massa e Tamanho AtomosAna AlbuquerqueAinda não há avaliações
- Aula 03 - Biofísica - Noções de TermodinâmicaDocumento12 páginasAula 03 - Biofísica - Noções de TermodinâmicaCleuton Braga LandreAinda não há avaliações
- qr10 02 Teste Aval 7 d1 EnunciadoDocumento7 páginasqr10 02 Teste Aval 7 d1 EnunciadoMariaAinda não há avaliações
- 10ºq - Teste1 10q TextoDocumento4 páginas10ºq - Teste1 10q Textomaria-28095100% (1)
- qr10 - 02 - Teste - Aval - 1 - sd1 - Enunciado + SoluçãoDocumento9 páginasqr10 - 02 - Teste - Aval - 1 - sd1 - Enunciado + SoluçãoLuísa Carmo100% (2)
- Massa e Termanho Dos Átomos - Ficha Formativa 10 AnoDocumento3 páginasMassa e Termanho Dos Átomos - Ficha Formativa 10 AnobibiAinda não há avaliações
- Fichas Formativa Subdomínio 1.1Documento3 páginasFichas Formativa Subdomínio 1.1Miguel Angélico GonçalvesAinda não há avaliações
- Ficha 1 - Massa e Tamanho Dos ÁtomosDocumento4 páginasFicha 1 - Massa e Tamanho Dos ÁtomosMarília PachecoAinda não há avaliações
- 1 FQ 10 Ano Massa e Tamanho Dos AtomosDocumento3 páginas1 FQ 10 Ano Massa e Tamanho Dos AtomosjferAinda não há avaliações
- Ficha Formativa 1.1 - 10FQADocumento2 páginasFicha Formativa 1.1 - 10FQAAlexandre PereiraAinda não há avaliações
- Ficha Formativa - 1-Massa e Tamanho Dos Átomos - MúltiplaDocumento3 páginasFicha Formativa - 1-Massa e Tamanho Dos Átomos - MúltiplaTiagoAinda não há avaliações
- Ficha Formativa 1.1 - 10FQADocumento2 páginasFicha Formativa 1.1 - 10FQABiaAinda não há avaliações
- Ficha Formativa 1.1 - 10FQADocumento2 páginasFicha Formativa 1.1 - 10FQAAndrei GalanAinda não há avaliações
- Fichas de Trabalho 1-3Documento7 páginasFichas de Trabalho 1-3rita machadoAinda não há avaliações
- Compilado - Fichas de Treino Nº1Documento11 páginasCompilado - Fichas de Treino Nº1Miguel AntonioAinda não há avaliações
- 02 Teste 1 Massa Tamanho AtomosDocumento5 páginas02 Teste 1 Massa Tamanho Atomosgorete71Ainda não há avaliações
- Fichas de Avaliação 1-12Documento41 páginasFichas de Avaliação 1-12elisabetesilvaAinda não há avaliações
- 10q-Teste 1Documento8 páginas10q-Teste 1madalenasantiago2008Ainda não há avaliações
- 1ºteste 10ºano Outubro 2019Documento9 páginas1ºteste 10ºano Outubro 2019Guilherme MartinsAinda não há avaliações
- 2º Teste de Avaliação Fisico QuimicaDocumento4 páginas2º Teste de Avaliação Fisico Quimicajonas47Ainda não há avaliações
- Teste Aval 1 sd1 EnunciadoDocumento5 páginasTeste Aval 1 sd1 EnunciadoBeatriz EstalagemAinda não há avaliações
- Ficha Formativa 9Documento5 páginasFicha Formativa 9Emma Oliveira MendesAinda não há avaliações
- Questões Propostas - 9º Ano LP 2023Documento7 páginasQuestões Propostas - 9º Ano LP 2023Victor RogérioAinda não há avaliações
- Ficha TrabalhoDocumento5 páginasFicha TrabalhoJoão PereiraAinda não há avaliações
- Lista de Exercícios - AlunosDocumento4 páginasLista de Exercícios - AlunosEnzo MiassiAinda não há avaliações
- Ficha de Trabalho-ArealDocumento7 páginasFicha de Trabalho-ArealticAinda não há avaliações
- Q10-1.1-Massa Tamanho Atomos - 1Documento12 páginasQ10-1.1-Massa Tamanho Atomos - 1Marta CancelaAinda não há avaliações
- Ficha 1 - Massa e Tamanho Dos ÁtomosDocumento4 páginasFicha 1 - Massa e Tamanho Dos ÁtomosBruna FrancoAinda não há avaliações
- APSA - 3 - Massa e Tamanho Dos ÁtomosDocumento7 páginasAPSA - 3 - Massa e Tamanho Dos ÁtomossofiaAinda não há avaliações
- Questões e Problemas-SD1.1 - 2022-2023Documento5 páginasQuestões e Problemas-SD1.1 - 2022-2023Matilde AlvesAinda não há avaliações
- Cap1 (Estrutura Atômica & Tabela Periódica) - ExercícioDocumento5 páginasCap1 (Estrutura Atômica & Tabela Periódica) - ExercícioLucas CarvalhoAinda não há avaliações
- Prova de Avaliação Nº1-V1Documento6 páginasProva de Avaliação Nº1-V1dr.joao alcobiaAinda não há avaliações
- 02 - Teste 10 - Elementos - Quimicos - Sua - Organizacao - v1 Nov 2018Documento10 páginas02 - Teste 10 - Elementos - Quimicos - Sua - Organizacao - v1 Nov 2018David MrspAinda não há avaliações
- Lista de Exercicios Notacao CientificaDocumento2 páginasLista de Exercicios Notacao CientificaPedro Henrique MilagreAinda não há avaliações
- 02 Teste 1 Massa Tamanho AtomosDocumento6 páginas02 Teste 1 Massa Tamanho AtomosPaula FernandesAinda não há avaliações
- Ficha - 1 - Química - 10º Ano - 2021 - 22Documento6 páginasFicha - 1 - Química - 10º Ano - 2021 - 22Catarina OliveiraAinda não há avaliações
- Ficha de TrabalhoDocumento3 páginasFicha de TrabalhoCristina SoaresAinda não há avaliações
- Teste 02 - 10ºCDocumento4 páginasTeste 02 - 10ºCInes BarbosaAinda não há avaliações
- 02 - Teste 10 - Elementos - Quimicos - Sua - Organizacao - v1 Nov 2018Documento12 páginas02 - Teste 10 - Elementos - Quimicos - Sua - Organizacao - v1 Nov 2018Rodrigo Correia100% (1)
- Ficha Formativa Q3 - 10º AnoDocumento5 páginasFicha Formativa Q3 - 10º AnoMaria David LopesAinda não há avaliações
- Lista de Quimica 1Documento2 páginasLista de Quimica 1Vinicius GobiAinda não há avaliações
- Avaliação 9 Ano RecuperaçãoDocumento2 páginasAvaliação 9 Ano Recuperaçãofernando martinsAinda não há avaliações
- Preparação para o Teste NovembroDocumento6 páginasPreparação para o Teste NovembroSara SilvaAinda não há avaliações
- Ficha 1 de QuimicaDocumento4 páginasFicha 1 de QuimicaStephanie MariaAinda não há avaliações
- Lista1qui102 100716121952 Phpapp01Documento5 páginasLista1qui102 100716121952 Phpapp01iolandafrotaAinda não há avaliações
- Ficha Nº1Documento9 páginasFicha Nº1Rafael MarquesAinda não há avaliações
- Teste 1Documento9 páginasTeste 1Luis CidAinda não há avaliações
- Grandezas QuímicasDocumento5 páginasGrandezas Químicaswagner_etepAinda não há avaliações
- Teste de Físico-Química 10º AnoDocumento6 páginasTeste de Físico-Química 10º AnoMafalda MendesAinda não há avaliações
- Fis 12006Documento4 páginasFis 12006gui_carinhaAinda não há avaliações
- Recuperação - 9 Ano - 1 Trimestre - CiênciasDocumento2 páginasRecuperação - 9 Ano - 1 Trimestre - CiênciasCAMILA CAMACHO LUZIANOAinda não há avaliações
- Questões Militares - Qconcursos - Com - Página 2Documento2 páginasQuestões Militares - Qconcursos - Com - Página 2Francisco KarlanAinda não há avaliações
- ABPEM010Documento4 páginasABPEM010UgoRibeiroAinda não há avaliações
- Lista de Atividades QuímicaDocumento4 páginasLista de Atividades QuímicaguitovanAinda não há avaliações
- Eletricidade (Salvo Automaticamente)Documento4 páginasEletricidade (Salvo Automaticamente)Anderson NunesAinda não há avaliações
- Historia FototerapiaDocumento80 páginasHistoria FototerapiaRenata Formiga100% (1)
- DILATAÇÃODocumento3 páginasDILATAÇÃOsuldamerica_suldamerica50% (2)
- QUESTAO Empuxo 9o AnoDocumento18 páginasQUESTAO Empuxo 9o Anoivan talonAinda não há avaliações
- Tectonica de PlacasDocumento7 páginasTectonica de PlacasGervasio Do Rosário RoqueAinda não há avaliações
- Lista 1 QuímicaDocumento2 páginasLista 1 QuímicaMaria LaeneAinda não há avaliações
- Fichamento 01 A História Da Vida Na TerraDocumento2 páginasFichamento 01 A História Da Vida Na TerraMarcelo SilvaAinda não há avaliações
- Relatório de Diagnóstico Da Situação Actual: Ilha de Moçambique - Bairro de MacicateDocumento31 páginasRelatório de Diagnóstico Da Situação Actual: Ilha de Moçambique - Bairro de MacicateSamuly João SamulyAinda não há avaliações
- A Lei 12.651 - 2012 e Seus Impactos Sobre As Áreas Destinadas À Preservação No Município de Paraty (RJ - Brasil)Documento10 páginasA Lei 12.651 - 2012 e Seus Impactos Sobre As Áreas Destinadas À Preservação No Município de Paraty (RJ - Brasil)CPDOC PARATYAinda não há avaliações
- ENC - Processo de Transporte de Resíduos - Angela Cristina Souza Gomes - OutlookDocumento5 páginasENC - Processo de Transporte de Resíduos - Angela Cristina Souza Gomes - OutlookAngela Cristina GomesAinda não há avaliações
- Lista Física 1 UemDocumento2 páginasLista Física 1 UemLuanna HolsbachAinda não há avaliações
- A Radiaã Ã o HawkingDocumento4 páginasA Radiaã Ã o HawkingJúlia ÍvineAinda não há avaliações
- Respostas 4Documento17 páginasRespostas 4ellensilveira_7173Ainda não há avaliações
- Planejamento Anual - 1 2 e 3° Ano - Ensino Medio Ciencias Da Natureza e Suas Tecnologias PDFDocumento14 páginasPlanejamento Anual - 1 2 e 3° Ano - Ensino Medio Ciencias Da Natureza e Suas Tecnologias PDFJosiel PotyAinda não há avaliações
- Trocas Nutricionais Entre o Organismo e o Meio - PlantasDocumento13 páginasTrocas Nutricionais Entre o Organismo e o Meio - PlantasPaula AbrantesAinda não há avaliações
- Efeito Penetração e BlindagemDocumento5 páginasEfeito Penetração e BlindagemMárcio Silva100% (1)
- Revisão Conceitos BásicosDocumento15 páginasRevisão Conceitos BásicosDanielli Cristina da SilvaAinda não há avaliações
- Bg10 Subsistemaseminteracao Suportedocumental Tarefa2Documento4 páginasBg10 Subsistemaseminteracao Suportedocumental Tarefa2Lia SantosAinda não há avaliações
- Lista de QuímicaDocumento4 páginasLista de QuímicaVitoria De Oliveira Do Nascimento GoncalvesAinda não há avaliações
- Aula 6 Empuxo de TerraDocumento35 páginasAula 6 Empuxo de TerraDaniel AssefAinda não há avaliações
- Sistema Mecânico Redutível A Uma PartículaDocumento1 páginaSistema Mecânico Redutível A Uma PartículaInês PimentaAinda não há avaliações
- Bioenergética e Metabolismo - Parte 2Documento41 páginasBioenergética e Metabolismo - Parte 2Bruna Niccoli RamirezAinda não há avaliações