Escolar Documentos
Profissional Documentos
Cultura Documentos
Aula 2 Serie 09 - 03
Enviado por
LuaraDescrição original:
Título original
Direitos autorais
Formatos disponíveis
Compartilhar este documento
Compartilhar ou incorporar documento
Você considera este documento útil?
Este conteúdo é inapropriado?
Denunciar este documentoDireitos autorais:
Formatos disponíveis
Aula 2 Serie 09 - 03
Enviado por
LuaraDireitos autorais:
Formatos disponíveis
Aula 2 serie 09/03/2024
ROTEIRO DA ATIVIDADE CURRICULAR COMPLEMENTAR
Data: 09/03
Série: 2° SÉRIE
Componente: Química
Conteúdo: soluções
1.Tema da Aula: coeficiente de solubilidade e classificação de soluções
3.Síntese do Conteúdo:
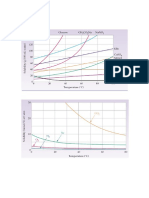
- O coeficiente de solubilidade (CS) é uma medida da capacidade máxima de um soluto se
dissolver em um solvente a uma temperatura específica. Ele indica a quantidade máxima de
soluto que pode ser dissolvida em 100g de solvente, geralmente expressa em g/100g.
Fatores que influenciam o CS:
Temperatura: A solubilidade da maioria dos solutos aumenta com a temperatura.
Natureza do soluto e do solvente: Solutos polares se dissolvem melhor em solventes polares,
enquanto solutos apolares se dissolvem melhor em solventes apolares.
Presença de outros solutos: A presença de outros solutos pode influenciar a solubilidade de um
soluto em um solvente.
Classificação de soluções:
As soluções podem ser classificadas quanto à quantidade de soluto dissolvido em relação ao seu
CS:
Saturada: Contém a quantidade máxima de soluto dissolvido a uma temperatura específica.
Insaturada: Contém menos soluto do que a quantidade máxima que pode ser dissolvida a
uma temperatura específica.
Sobressaturada: Contém mais soluto do que a quantidade máxima que pode ser dissolvida a
uma temperatura específica.
Exercício
1- ao dissolver 50g de NaCl em 100g de H20, teremos que tipo de soluções ?
2- Considerando 100g de H20 a 20 *C classifique
A) 50 g de NaCl
B) 33g de açúcar
C) 5,0 g de KCl
D) 0,15g de Ca(OH)
Cs dos solutos em 100 g de água a 20 *C
NaCl 36g
Açúcar 203
KCl 34
Ca(OH) 0,185
. á 20° o cs do KNO3 é de 32g em 100g de água, que tipo de solução obteremos se
dissolvemos 45g do soluto?
. A 40°C A solubilidade do NaCl é de 39g em 100g de água. Se resfriarmos lentamente essa
solução ate 20 C obteremos que tipo de solução?
Você também pode gostar
- Aula #01 - SoluçõesDocumento14 páginasAula #01 - SoluçõesAnna Luiza LopesAinda não há avaliações
- Resumo Sobre SoluçõesDocumento19 páginasResumo Sobre SoluçõesFabíola FelixAinda não há avaliações
- Gama - Módulo 19Documento23 páginasGama - Módulo 19Koelho CoelhoAinda não há avaliações
- Estudo Das Solucoes Coeficiente de SolubilidadeDocumento13 páginasEstudo Das Solucoes Coeficiente de SolubilidadeGildo Silva100% (1)
- Quimica - 002 SolucoesDocumento5 páginasQuimica - 002 Solucoescon_seguir100% (1)
- QuimicaDocumento4 páginasQuimicaAntonio EduardoAinda não há avaliações
- SOLUÇÕESDocumento8 páginasSOLUÇÕESAlineAinda não há avaliações
- Solues 120808142105 Phpapp01Documento9 páginasSolues 120808142105 Phpapp01tissiaraujoAinda não há avaliações
- Semana 6 A 10 Soluções Solubilidade Concentrações e MisturasDocumento70 páginasSemana 6 A 10 Soluções Solubilidade Concentrações e Misturasnogueirax7Ainda não há avaliações
- 01 - SoluçõesDocumento5 páginas01 - SoluçõesJaque SoaresAinda não há avaliações
- Coeficiente de Solubilidadeaula 12 04 12blogDocumento7 páginasCoeficiente de Solubilidadeaula 12 04 12blogThania ArrudaAinda não há avaliações
- Apostila de Exercícios Com Gabarito de Soluções - Concentração Comum A Mistura de Soluções de Solutos DiferentesDocumento16 páginasApostila de Exercícios Com Gabarito de Soluções - Concentração Comum A Mistura de Soluções de Solutos DiferentesProf. Maych Melo QuímicaAinda não há avaliações
- Soluções - 2 AnoDocumento5 páginasSoluções - 2 AnoGiovanni RodriguesAinda não há avaliações
- Aula de SoluçõesDocumento35 páginasAula de Soluçõesbianca vieiraAinda não há avaliações
- Aula 17 - SoluesDocumento53 páginasAula 17 - Soluesgabrielmolozzi377Ainda não há avaliações
- Composição Qualitativa de SoluçõesDocumento18 páginasComposição Qualitativa de SoluçõesCátia GomesAinda não há avaliações
- Soluções e SolubilidadeDocumento7 páginasSoluções e SolubilidaderpovilsAinda não há avaliações
- SOLUÇÕESDocumento8 páginasSOLUÇÕESVitóriaAinda não há avaliações
- LE - Dispersão e SolubilidadeDocumento3 páginasLE - Dispersão e SolubilidadeMatheus PetryAinda não há avaliações
- Exercícios Resolvidos - SolubilidadeDocumento14 páginasExercícios Resolvidos - SolubilidadeMouraci Santana RibeiroAinda não há avaliações
- Aula04 QA SoluçõesDocumento27 páginasAula04 QA SoluçõesIzabelli de Castro BaptistaAinda não há avaliações
- Equilibrio Solubilidade 2011 UFRPEDocumento10 páginasEquilibrio Solubilidade 2011 UFRPEJosé Beckham SantosAinda não há avaliações
- Atividades Quimica ColigaçoesDocumento4 páginasAtividades Quimica Coligaçoes1011004012Ainda não há avaliações
- DISPERSOES Prof. CleberDocumento62 páginasDISPERSOES Prof. CleberceliogardeonAinda não há avaliações
- Química 11 e 12 SoluçõesDocumento7 páginasQuímica 11 e 12 SoluçõesJonathan AraujoAinda não há avaliações
- Solucoes Alunos 2022Documento27 páginasSolucoes Alunos 2022Renan Eler CenciAinda não há avaliações
- Erick Leal Dos Santos Souza - NOTAS de AULA 1 Soluções 5 UnidadeDocumento6 páginasErick Leal Dos Santos Souza - NOTAS de AULA 1 Soluções 5 UnidadeNyxAinda não há avaliações
- Resumo 02 FQDocumento3 páginasResumo 02 FQAlexandre MagnoAinda não há avaliações
- Aula 1 - SoluçõesDocumento38 páginasAula 1 - SoluçõesPEMapperAinda não há avaliações
- Soluções - Parte 1 - Classificação de SoluçõesDocumento2 páginasSoluções - Parte 1 - Classificação de SoluçõesLyeniferAinda não há avaliações
- Lista de Exercício Ponto Extra 2CDocumento3 páginasLista de Exercício Ponto Extra 2CSALSICHA FFAinda não há avaliações
- INTRODUÇÃO AquosaDocumento8 páginasINTRODUÇÃO AquosaMauro ErnestoAinda não há avaliações
- 16 SolubilidadeDocumento7 páginas16 SolubilidadeFRANKE MERO TESTEAinda não há avaliações
- SolucoesDocumento63 páginasSolucoesBianca conceiçãoAinda não há avaliações
- 378870-Módulo 01 - Soluções 1 PDFDocumento8 páginas378870-Módulo 01 - Soluções 1 PDFÍtalo SantosAinda não há avaliações
- Fisicoquimica II ApostilaDocumento36 páginasFisicoquimica II ApostilaMario SantanaAinda não há avaliações
- Soluções - Módulo 1Documento24 páginasSoluções - Módulo 1neyzanata5043Ainda não há avaliações
- 16.0.apresentaçao Solucoes - PpsDocumento97 páginas16.0.apresentaçao Solucoes - PpsDaiane PinheiroAinda não há avaliações
- Lista 1 QG 1-19Documento6 páginasLista 1 QG 1-19schottbpAinda não há avaliações
- Lista de Exercicios 12 - Revisao para A 2 Avaliacao - Hidrolise Salina e Solubilidade - 3 Bimestre 2013 - 3 SeriesDocumento2 páginasLista de Exercicios 12 - Revisao para A 2 Avaliacao - Hidrolise Salina e Solubilidade - 3 Bimestre 2013 - 3 SeriesJosimar Lima FerreiraAinda não há avaliações
- Soluções QuímicasDocumento8 páginasSoluções QuímicasGuilherme FranciscoAinda não há avaliações
- Matriz - SolubilidadeDocumento3 páginasMatriz - SolubilidadeEtiene Pereira de AndradeAinda não há avaliações
- Soluções Teoria e ExercíciosDocumento15 páginasSoluções Teoria e ExercíciosANA RITA MACHADOAinda não há avaliações
- Exercicios de SolubilidadeDocumento6 páginasExercicios de Solubilidadesua mae de 4Ainda não há avaliações
- Aula 2 Teoria Das SoluçõesDocumento32 páginasAula 2 Teoria Das SoluçõesCarlos EmidioAinda não há avaliações
- Lista de Exercicios de SolucoesDocumento2 páginasLista de Exercicios de SolucoesGraciano ComboioAinda não há avaliações
- Aula03-BasesAnalíticas AlunosDocumento27 páginasAula03-BasesAnalíticas AlunosbernardoAinda não há avaliações
- Exercicios de Coeficiente de SolubilidadeDocumento4 páginasExercicios de Coeficiente de SolubilidadeEng Renato De Marchi Vieira Dos SantosAinda não há avaliações
- SOLUÇÕESDocumento21 páginasSOLUÇÕESliineesoouzaaAinda não há avaliações
- SOLUÇÕESDocumento20 páginasSOLUÇÕESmarcellebrunamartelliAinda não há avaliações
- Trabalho de Quimica 301Documento5 páginasTrabalho de Quimica 301GRAZIELLI SILVAAinda não há avaliações
- Aula de Resolução de Questões Soluções QuimicasDocumento5 páginasAula de Resolução de Questões Soluções Quimicasi46555497Ainda não há avaliações
- Quimica 2 Ano 2 ParteDocumento19 páginasQuimica 2 Ano 2 ParteJoão PauloAinda não há avaliações
- Soluções-Definições (Net)Documento32 páginasSoluções-Definições (Net)Ricardo AlvesAinda não há avaliações
- Introdução SoluçõesDocumento13 páginasIntrodução SoluçõesNiko Bellic50% (2)
- BiomedicinaDocumento56 páginasBiomedicinaDaniela LealAinda não há avaliações
- Soluà à Es Aula 2 - 231018 - 132153Documento33 páginasSoluà à Es Aula 2 - 231018 - 132153theuzlara344tyAinda não há avaliações
- Apostila Química Orgânica: Carbono, Dienos E AromáticosNo EverandApostila Química Orgânica: Carbono, Dienos E AromáticosAinda não há avaliações