0% acharam este documento útil (0 voto)
599 visualizações4 páginasEstados Físicos Da Água Conceitos
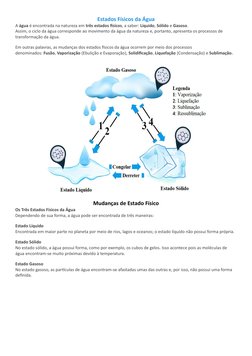
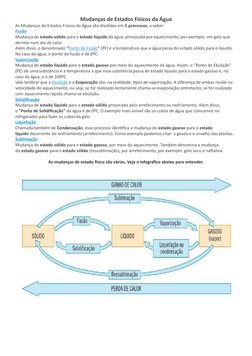
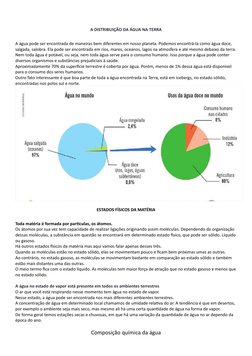
O documento discute os três estados físicos da água (líquido, sólido e gasoso) e as mudanças entre esses estados através de processos como fusão, vaporização, solidificação e liquefação. Também aborda a distribuição da água na Terra entre rios, oceanos, atmosfera e subsolo, além da composição química da água.
Enviado por
Cesar Cruz Cabral SousaDireitos autorais
© © All Rights Reserved
Levamos muito a sério os direitos de conteúdo. Se você suspeita que este conteúdo é seu, reivindique-o aqui.
Formatos disponíveis
Baixe no formato DOC, PDF, TXT ou leia on-line no Scribd
0% acharam este documento útil (0 voto)
599 visualizações4 páginasEstados Físicos Da Água Conceitos
O documento discute os três estados físicos da água (líquido, sólido e gasoso) e as mudanças entre esses estados através de processos como fusão, vaporização, solidificação e liquefação. Também aborda a distribuição da água na Terra entre rios, oceanos, atmosfera e subsolo, além da composição química da água.
Enviado por
Cesar Cruz Cabral SousaDireitos autorais
© © All Rights Reserved
Levamos muito a sério os direitos de conteúdo. Se você suspeita que este conteúdo é seu, reivindique-o aqui.
Formatos disponíveis
Baixe no formato DOC, PDF, TXT ou leia on-line no Scribd