Escolar Documentos
Profissional Documentos
Cultura Documentos
QUI116 - 3a Lista de Exercícios - Parte A
Enviado por
Herbert Marques0 notas0% acharam este documento útil (0 voto)
13 visualizações2 páginasTítulo original
QUI116 - 3a lista de exercícios - Parte A
Direitos autorais
© © All Rights Reserved
Formatos disponíveis
PDF, TXT ou leia online no Scribd
Compartilhar este documento
Compartilhar ou incorporar documento
Você considera este documento útil?
Este conteúdo é inapropriado?
Denunciar este documentoDireitos autorais:
© All Rights Reserved
Formatos disponíveis
Baixe no formato PDF, TXT ou leia online no Scribd
0 notas0% acharam este documento útil (0 voto)
13 visualizações2 páginasQUI116 - 3a Lista de Exercícios - Parte A
Enviado por
Herbert MarquesDireitos autorais:
© All Rights Reserved
Formatos disponíveis
Baixe no formato PDF, TXT ou leia online no Scribd
Você está na página 1de 2
Universidade Federal de Ouro Preto
ICEB – Instituto de Ciências Exatas e Biológicas
Disciplina: QUI116(T21,22) – Físico-Química II – Prof. Dr. Mateus Xavier Silva
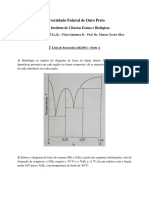
3a Lista de Exercícios (2021/01) – Parte A
1) Exprima as forças iônicas de soluções de (a) MgCl2, (b) Al2(SO4)3 e (c) Fe2(SO4)3, em função
das respectivas molalidades, b.
2) Calcule a força iônica de uma solução que é 0,040 molal em K3[Fe(CN)6](aq), 0,030 molal em
KCl(aq) e 0,050 molal em NaBr(aq).
3) Qual a molalidade que uma solução de Al2(SO4)3 deve ter para apresentar a mesma força
iônica que uma solução de Ca(NO3)2(aq) 0,500 molal?
4) Estime o coeficiente médio de atividade iônica e a atividade de uma solução que é 0,020 molal
em NaCl(aq) e 0,035 molal em Ca(NO3)2(aq).
5) Imagine uma pilha na qual a seguinte reação ocorra:
Cd(s) + Ni(OH)3(s) Cd(OH)2(s) + Ni(OH)2(s)
Forneça as meias-reações dos eletrodos e identifique qual é o ânodo e qual é o cátodo.
6) Escreva a reação da pilha, as respectivas meias-reações (indicando o eletrodo no qual
ocorrem) e calcule a FEM padrão para cada uma das células eletroquímicas abaixo:
a) Pt |Cl2(g) | HCl(aq) || K2CrO4(aq) | Ag2CrO4(s) | Ag
b) Pt | Fe3+(aq), Fe2+(aq) || Sn4+(aq), Sn2+(aq) | Pt
c) Cu | Cu2+(aq) || Mn2+(aq), H+(aq) | MnO2(s) | Pt
7) A FEM da pilha Pt | H2(g) | HI(aq) | AgI(s) | Ag é 1,00 V, a 25 °C. Qual o pH da solução
eletrolítica?
Você também pode gostar
- Corrosão e Proteção dos MateriaisNo EverandCorrosão e Proteção dos MateriaisNota: 5 de 5 estrelas5/5 (1)
- Ácidos e Bases de Brönsted e Lowry: Uma visão aplicada ao meio ambienteNo EverandÁcidos e Bases de Brönsted e Lowry: Uma visão aplicada ao meio ambienteAinda não há avaliações
- Lista de Exercícios - Força Iônica e Coeficiente de AtividadeDocumento3 páginasLista de Exercícios - Força Iônica e Coeficiente de AtividadeFernanda SilvaAinda não há avaliações
- 13b-Lista Exercicios - Geral 2 - EletroquimicaDocumento14 páginas13b-Lista Exercicios - Geral 2 - EletroquimicaDouglasAinda não há avaliações
- Exercícios de eletroquímicaDocumento17 páginasExercícios de eletroquímicaDiógenes GramachoAinda não há avaliações
- Quimica Estequiometria Geometria Molecular Carga Formal Energia Reticular Balanceamento RedoxDocumento3 páginasQuimica Estequiometria Geometria Molecular Carga Formal Energia Reticular Balanceamento RedoxJonas SaldanhaAinda não há avaliações
- LISTA de EXERCICIOS Equilibrios de Complexacao e RedoxDocumento3 páginasLISTA de EXERCICIOS Equilibrios de Complexacao e RedoxVictor CarvalhoAinda não há avaliações
- Rutherford bombardeia ouro com partículas alfaDocumento14 páginasRutherford bombardeia ouro com partículas alfaRodrigo SilveiraAinda não há avaliações
- Química Analítica Clássica Lista ExercíciosDocumento2 páginasQuímica Analítica Clássica Lista ExercíciosAntonio FelipeAinda não há avaliações
- exercícios_QFL1150Documento9 páginasexercícios_QFL1150Renata MullerAinda não há avaliações
- Lista Exercícios Química AtômicaDocumento4 páginasLista Exercícios Química AtômicaRenato MartinsAinda não há avaliações
- LISTA_7_ (1)Documento1 páginaLISTA_7_ (1)evelinoliveiraAinda não há avaliações
- Lista Exercicios Qui203 2020Documento16 páginasLista Exercicios Qui203 2020Brenda BacelarAinda não há avaliações
- Ex1 17.06.2021Documento2 páginasEx1 17.06.2021ngdqyvcyopckcyjtsnAinda não há avaliações
- Lista QuimicaDocumento5 páginasLista QuimicaYanAinda não há avaliações
- Exerc Equil-Analitica222Documento4 páginasExerc Equil-Analitica222JefferoiAinda não há avaliações
- Lista de exercícios química geral conceitos cálculosDocumento1 páginaLista de exercícios química geral conceitos cálculosDébora MastroleoAinda não há avaliações
- 1 Alista CQ049Documento4 páginas1 Alista CQ049Ingrid AlvesAinda não há avaliações
- Lista8 QAC KMB Equilbrio e Volumetria RedoxDocumento2 páginasLista8 QAC KMB Equilbrio e Volumetria RedoxMARIA PEREIRAAinda não há avaliações
- Lista 05Documento4 páginasLista 05Nicole PacíficoAinda não há avaliações
- Lista de Exercício - 2021Documento4 páginasLista de Exercício - 2021JAILTON NONATO 02Ainda não há avaliações
- Lista de Exercícios 1 - Química GeralDocumento7 páginasLista de Exercícios 1 - Química GeralMarry YoungAinda não há avaliações
- Métodos eletroanalíticos e termogravimetriaDocumento3 páginasMétodos eletroanalíticos e termogravimetriaEric Johnn MascarenhasAinda não há avaliações
- Química Analítica ClássicaDocumento3 páginasQuímica Analítica ClássicaRamon Marques0% (1)
- Eletroquímica e pilhas galvânicasDocumento3 páginasEletroquímica e pilhas galvânicasTiago BezerraAinda não há avaliações
- Soluções e Equilíbrio QuímicoDocumento5 páginasSoluções e Equilíbrio QuímicoGuilherme FernandesAinda não há avaliações
- Questões de Nersnt e FaradayDocumento11 páginasQuestões de Nersnt e FaradayedeceAinda não há avaliações
- Lista de Exercício EletroquímicaDocumento3 páginasLista de Exercício EletroquímicaLael EduardoAinda não há avaliações
- Lista de Exercícios 2 - FQBIII - 2023.2Documento2 páginasLista de Exercícios 2 - FQBIII - 2023.2Giulia EspositoAinda não há avaliações
- Cálculos de equilíbrio químico e titulação de cátions metálicosDocumento1 páginaCálculos de equilíbrio químico e titulação de cátions metálicosWeslei Roberto Correia CabralAinda não há avaliações
- 5 Ficha de Oxidação Redução - 230117 - 204311Documento7 páginas5 Ficha de Oxidação Redução - 230117 - 204311Maria Antónia PereiraAinda não há avaliações
- UERJ lista exercícios eletroquímicaDocumento3 páginasUERJ lista exercícios eletroquímicaRay Sant'AnnaAinda não há avaliações
- Lista de exercícios de eletroquímicaDocumento5 páginasLista de exercícios de eletroquímicaJhiovane AlexsanderAinda não há avaliações
- Lista de exercícios de íons complexos com reações e estruturasDocumento2 páginasLista de exercícios de íons complexos com reações e estruturasMarcius ViniciusAinda não há avaliações
- Exercícios de Cálculos Químicos e TermodinâmicaDocumento6 páginasExercícios de Cálculos Químicos e TermodinâmicaFernanda Abbate dos SantosAinda não há avaliações
- Prova de Conhecimento em Química para Ingresso na Pós-Graduação do DQ/UFMGDocumento16 páginasProva de Conhecimento em Química para Ingresso na Pós-Graduação do DQ/UFMGAnanda DiasAinda não há avaliações
- Lista de Exercícios de Química Geral sobre Reações Químicas e Células EletroquímicasDocumento2 páginasLista de Exercícios de Química Geral sobre Reações Químicas e Células EletroquímicasMarco AurelioAinda não há avaliações
- Exercícios de Condutometria e PotenciometriaDocumento2 páginasExercícios de Condutometria e Potenciometriavictor lucchettiAinda não há avaliações
- Lista de Exercício 5Documento1 páginaLista de Exercício 5crislaniaAinda não há avaliações
- Química das Transformações – 2012: Turma-A Lista de Exercícios – 01Documento2 páginasQuímica das Transformações – 2012: Turma-A Lista de Exercícios – 01Kalvin LeiteAinda não há avaliações
- Lista EletroDocumento4 páginasLista EletroMariana MagalhãesAinda não há avaliações
- 2a Lista de ExercíciosDocumento6 páginas2a Lista de Exercíciosramon7789Ainda não há avaliações
- UFCE - Lista 3 de exercícios de QuímicaDocumento2 páginasUFCE - Lista 3 de exercícios de Químicapedro alcantara100% (1)
- Lista de Exercícios - Força Iônica e Coeficiente de AtividadeDocumento3 páginasLista de Exercícios - Força Iônica e Coeficiente de AtividadeFernanda Silva100% (1)
- Lista Exercícios QuímicaDocumento2 páginasLista Exercícios QuímicaGuto TakaAinda não há avaliações
- Lista03 QB76K 2s 2017 PDFDocumento2 páginasLista03 QB76K 2s 2017 PDFsakurachanfanAinda não há avaliações
- 4º Lista de Exercícios-EletroquímicaDocumento2 páginas4º Lista de Exercícios-EletroquímicaNewson Leal FernandesAinda não há avaliações
- ListaseqDocumento6 páginasListaseqDayse_sbAinda não há avaliações
- Química - Produtos de solubilidadeDocumento2 páginasQuímica - Produtos de solubilidadeDuarteAinda não há avaliações
- Cálculos de concentrações e equilíbrios de complexos em soluções químicasDocumento2 páginasCálculos de concentrações e equilíbrios de complexos em soluções químicasCynthia VanessaAinda não há avaliações
- Exercícios - Lista 04Documento22 páginasExercícios - Lista 04raquel vianaAinda não há avaliações
- 2º Lista de Exercícios - Quimica InorganicaDocumento3 páginas2º Lista de Exercícios - Quimica InorganicaliviacerbinoAinda não há avaliações
- Lista de exercícios de química com equilíbrio químico, ácido-base e eletroquímicaDocumento3 páginasLista de exercícios de química com equilíbrio químico, ácido-base e eletroquímicaAlmeida Malembe100% (1)
- 7 Lista - Equilíbrio - SolubilidadeDocumento2 páginas7 Lista - Equilíbrio - SolubilidadeNatã LuizAinda não há avaliações
- Lista Ligacao IonicaDocumento3 páginasLista Ligacao IonicaJefferson CândidoAinda não há avaliações
- Ficha de Trabalho 1 de Fundamentos de Química (2012:2013) PDFDocumento3 páginasFicha de Trabalho 1 de Fundamentos de Química (2012:2013) PDFFCiênciasAinda não há avaliações
- TopD Reacoes em Solucao Aquosa e Estequiometria RESPOSTASDocumento7 páginasTopD Reacoes em Solucao Aquosa e Estequiometria RESPOSTASMaria AliceAinda não há avaliações
- Apostila Química Orgânica: Carbono, Dienos E AromáticosNo EverandApostila Química Orgânica: Carbono, Dienos E AromáticosAinda não há avaliações
- Princípio de Arquimedes na UFOP: experimentos e análisesDocumento3 páginasPrincípio de Arquimedes na UFOP: experimentos e análisesHerbert MarquesAinda não há avaliações
- Diagrama de fases e exercícios de físico-químicaDocumento2 páginasDiagrama de fases e exercícios de físico-químicaHerbert MarquesAinda não há avaliações
- 3a Lista de Exercícios de Físico-Química II da UFOP com cálculos de equilíbrio químico e velocidade de reaçõesDocumento2 páginas3a Lista de Exercícios de Físico-Química II da UFOP com cálculos de equilíbrio químico e velocidade de reaçõesHerbert MarquesAinda não há avaliações
- Introdução às Equações Diferenciais Ordinárias - Lista de Exercícios 9Documento1 páginaIntrodução às Equações Diferenciais Ordinárias - Lista de Exercícios 9Herbert MarquesAinda não há avaliações
- Diagrama eutético Naftaleno-DifenilaminaDocumento7 páginasDiagrama eutético Naftaleno-DifenilaminaHerbert MarquesAinda não há avaliações