Escolar Documentos
Profissional Documentos
Cultura Documentos
Paper 161
Enviado por
Elson OliveiraDescrição original:
Título original
Direitos autorais
Formatos disponíveis
Compartilhar este documento
Compartilhar ou incorporar documento
Você considera este documento útil?
Este conteúdo é inapropriado?
Denunciar este documentoDireitos autorais:
Formatos disponíveis
Paper 161
Enviado por
Elson OliveiraDireitos autorais:
Formatos disponíveis
13° Congresso Internacional de Tintas
13ª Exposição Internacional de Fornecedores para Tintas
PROCESSO DE OBTENÇÃO E CARACTERIZAÇÃO DE PIGMENTOS A PARTIR DE
RESÍDUOS FERROSOS
Célia do Rocio de Jesus Valente, Adriana H. Coleto de Assis, Carlos F. Panichi, Elson Oliveira e Gladson
Oliveira
Centro Estadual de Educação Profissional de Curitiba (CEEP) - Curso Técnico em Química
A reciclagem de material é uma importante atividade comercial observada desde o Império Romano, sendo o
ferro o material mais reciclado no mundo pelo setor industrial. Estima-se que 17,82% dos resíduos metálicos
de ferro não sofrem nenhum tipo de transformação ou recuperação. O Brasil que em 2010 consumiu,
aproximadamente, 25 milhões de toneladas, gerou um desperdício significativo. Nesse contexto, vê-se nestes
resíduos um potencial econômico a ser explorado e que pode ser convertido em benefício da sociedade. Os
resíduos em um processo produtivo cumpre um papel fundamental na melhoria da qualidade de vida de
comunidades carentes, na limpeza das cidades, bem como na preservação do meio ambiente. A medida se
efetiva com a redução de lixo metálico enviado para aterros e terrenos baldios. Inúmeros empregos podem ser
gerados em uma extensa cadeia de pequenos e médios empreendedores que se dedicam a atividade de
separação e processo produtivo. Desse modo, esse estudo tem por finalidade a obtenção e caracterização
dos pigmentos de coloração primária (azul, amarelo e vermelho) a partir do óxido de ferro proveniente do
tratamento de resíduos selecionados. Os pigmentos foram obtidos, caracterizados e testados quanto a sua
dispersabilidade, capacidade de conferir cor em um sistema (tintas) e solubilidade. Os pigmentos são
largamente empregados como matéria-prima nas indústrias de tintas automotivas, imobiliárias, têxteis,
cosméticos, papéis, polímeros, borracha, dentre outros.
Palavras-chave: Pigmentos. Óxidos de ferro. Tintas.
1.0 INTRODUÇÃO
É crescente a preocupação da sociedade quanto as ações que o homem desenvolve com o
meio ambiente. Muitas vezes, como resultado dessa ação, surge certo desequilíbrio ambiental
em função dos resíduos gerados pelas indústrias ou das ações domésticas desenvolvidas pelo
ser humano. Há muito tempo o homem já observa a ação depreciadora do meio em que vive
devido as atividades industriais (FERREIRA & ANJOS, 2001). Porém, com a velocidade com
que vem crescendo as atividades industriais, a quantidade de resíduos gerados são cada vez
maiores em detrimentos das atividades humanas, tanto de materiais orgânicos como
inorgânicos, como é o caso de: restos de comida, bagaço de cana, computadores, garrafas,
papelão, papel, baterias, saquinhos plásticos, lâmpadas queimadas, aparas de couro, sucata
de metal, produtos químicos dentre outros (MESQUITA, 2007). A ação de depositar os
resíduos gerados em local inapropriado pode se reverter e atingir o próprio homem, afinal é um
hospedeiro natural deste sistema, e, segundo Ferreira & Anjos (2001, apud COLOMBI et al,
1995), agentes físicos, químicos e biológicos são capazes de causar danos à saúde do
homem. A definição de materiais recicláveis para Giansanti (2003) é de que todos os materiais
capazes de serem processados, ou seja, transformados por ação física ou química, e obterem
uma nova utilidade são considerados recicláveis, como exemplo o vidro, metais, plásticos e o
lixo orgânico. Nesse sentido, nota-se uma preocupação positiva do homem que busca
ABRAFATI 2013 | ASSOCIAÇÃO BRASILEIRA DOS FABRICANTES DE TINTAS
13° Congresso Internacional de Tintas
13ª Exposição Internacional de Fornecedores para Tintas
minimizar essa ação, que pode ocasionar a contaminação do solo, rios e mananciais.
Atualmente, a atividade de reciclar tem sido incorporada às atividades comuns da indústria, do
comércio, domésticas e de segmentos educacionais, como é o caso deste trabalho. Assim, a
atividade de reciclar vem tornando-se uma ótima oportunidade de contribuir na preservação do
meio ambiente, contribuindo para a saúde da população e ainda colaborando como fonte de
renda para aqueles que pretendem atuar neste segmento. Este trabalho inicialmente surge com
a intenção de aprofundar os estudos de alunos que escolheram o tema tintas aliado à
sustentabilidade para defesa de seu curso técnico em química. O objetivo deste estudo é o de
obter pigmentos a partir do tratamento de resíduos de origem ferrosa, empregando um
processo químico, sendo os resíduos provenientes do descarte de restos industriais e
domésticos, que muitas vezes destinam-se a um descarte não recomendado, como é o caso de
aterros sanitários e terrenos baldios. Os pigmentos são largamente comercializados como
matéria-prima de inúmeros segmentos, como é o caso das indústrias de tintas automotivas e
imobiliárias, têxteis, comésticos, papéis, polímeros, borracha, dentre outro. A definição de
pigmentos são um sólido finamente particulado (pós), coloridos e insolúveis no meio a que se
destinam. Estes tem a finalidade de fornecer a coloração, tenacidade e textura, bem como
encorpar e secar a tinta (HANDBOOK,1998; BRANCO, 2009). Com o tratamento do resíduo
industrial ou doméstico de origem ferrosa, busca-se colaborar em ações que visem a
manutenção e sustentabilidade do meio ambiente evitando impactos ambientais não
desejados.
2.0 METODOLOGIA
O tratamento dos resíduos, de origem ferrosa, foram utilizando acessórios e reagentes
comuns a qualquer laboratório de química. Já, os equipamentos empregados foram a capela
de exaustão, para o manuseio de ácidos voláteis, um sistema de filtração a vácuo, a estufa
para a secagem do óxido de ferro e um forno mufla para calcinação do óxido de ferro. Os
materiais utilizados na produção dos óxidos de ferro foram pregos e outros pequenos pedaços
de materiais ferrosos e tratados no laboratório do Centro Estadual de Educação Profissional de
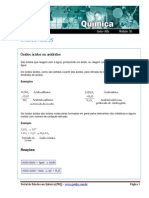
Curitiba (CEEP – Curitiba), como descrito nas etapas mostradas na Figura 1. Os óxidos podem
ser obtidos por vários processos, sendo escolhido para este estudo um de fácil execução
(ASTRALL) e que produza um material de boa qualidade. Todo o processo de produção dos
óxidos de ferro é descrito em seis etapas, conforme apresentado o fluxograma da Figura 1.
ABRAFATI 2013 | ASSOCIAÇÃO BRASILEIRA DOS FABRICANTES DE TINTAS
13° Congresso Internacional de Tintas
13ª Exposição Internacional de Fornecedores para Tintas
LIMPEZA DO
METAIS
TRATAMENTO
MOAGEM
ÁCIDO
SECAGEM TRATAMENTO
(ÓXIDO) ALCALINO
OXIDAÇÃO
DO
Fe(OH)3
Figura 1: Etapas do processo de obtenção de pigmentos de origem ferrosa em laboratório.
1ª Etapa: O material coletado é limpo de possíveis sujeiras como terra, pedaços de madeira,
tecidos e plásticos.
2ª Etapa: O material limpo é depositado num tanque contendo uma solução com ácido
sulfúrico que vai reagir com o metal, de acordo com a equação química:
H2SO4 + Fe0 Fe2SO4 + H2(g) (1)
Nesta etapa, a reação é de simples troca e produz o sal sulfato de ferro (II) e gás hidrogênio, a
solução resultante é escura devido às impurezas contidas nos metais que foram dissolvidos. As
Figuras 2 (a) e (b) mostram a referida solução antes e depois da filtração. Essa solução deve
ser filtrada para a retirada das impurezas, resultando numa solução de cor verde.
(a) (b) (c)
Figuras 2 (a), (b) e (c): Solução aquosa de ácido sulfúrico com resíduos de ferro dissolvidos. A solução
com sulfato de ferro (II) após a filtração. E os cristais de sulfato ferroso formados.
À medida que a solução ácida que contém o sulfato de ferro vai evaporando, ocorre a formação
de cristais de sulfato de ferro (II) de coloração verde claro, podendo ser observado na Figura 2
(b) e (c).
ABRAFATI 2013 | ASSOCIAÇÃO BRASILEIRA DOS FABRICANTES DE TINTAS
13° Congresso Internacional de Tintas
13ª Exposição Internacional de Fornecedores para Tintas
3ªEtapa: Após a filtração, a solução contando o sulfato de ferro (II) é imersa em um tanque
contendo uma solução alcalina, e é convertido no hidróxido de ferro (III), conforme
demonstrado na reação química (2):
Fe2SO4 + NaOH Fe(OH)3 + H2O (2)
Nessa mesma etapa, se reação for controlada, mantendo-se baixo a concentração do nível de
oxigênio é possível ocorrer à formação do hidróxido de ferro II.
4ª Etapa: Através da reação entre o hidróxido de ferro III (Fe(OH)3) e o oxigênio do ar se
origina o óxido de ferro de cor amarela. A equação (3) que evidencia a reação é mostra a
formação do óxido de ferro hidratado:
2 Fe(OH)3 Fe2O3.H2O (3)
Para a equação de obtenção do Fe2O3.H2O algumas fontes literárias indicam a
formação do pigmento de cor amarela, porém, o óxido de ferro produzido gerou um pigmento
de coloração castanho-avermelhada, conforme sugerido por Merçon (2004). As Figuras 3 (a) e
(b) mostram a solução contendo o óxido, e o óxido seco em estufa, em temperatura de 60ºC.
(a) (b)
Figuras 3 (a) e (b): Solução contendo o óxido de ferro hidratado – Óxido de ferro filtrado, seco em estufa
a 60ºC e moído.
5ª Etapa: Esta etapa é destinada a secagem do material em estufa numa temperatura de 50 a
60ºC. O material nesta fase se encontra compacto e deverá ser moído. A secagem do óxido de
ferro hidratado dá origem ao óxido de ferro de cor castanho-vermelhado, mostrado na Figura 3
(b), e quarta equação química indicada, a seguir:
Fe2O3.H2O ∆ Fe2O3 (4)
6ª Etapa: Após o óxido seco é levado para ser moído até obter partículas finíssimas, conforme
mostra a Figura 3 (b).
Concluída a experimentação, no que se refere a obtenção do óxido de ferro Fe2O3,
novas experiências foram realizadas no sentido de obter a coloração primária (amarelo, azul e
vermelho) do óxido ferroso. Para essa nova fase foi realizada três ações indispensáveis:
ABRAFATI 2013 | ASSOCIAÇÃO BRASILEIRA DOS FABRICANTES DE TINTAS
13° Congresso Internacional de Tintas
13ª Exposição Internacional de Fornecedores para Tintas
1º) O óxido de férrico foi calcinado por diferentes temperatura, 100, 200, 300 e 500, 700, 900 e
1100 ºC, das quais obteve-se o óxido de ferro de coloração cinza, marrom, preto e vermelho.
2º) A obtenção do óxido de ferro de coloração amarela e azul só foram possíveis através de
reação química. O pigmento amarelo foi obtido ainda em solução alcalina, na presença de
oxigênio, de acordo com a quinta equação e o pigmento de cor azul pela reação mostrada na
sexta equação química:
FeSO4(aq) + NaOH(aq) + O2(g) Fe2O3.H2O (5)
Fe SO4(aq) + K3[Fe(CN)6 ](aq) KFe[Fe(CN)6 ](aq) + K2SO4(aq) (6)
3º) Outra prática foi colocar os cristais de sulfato ferroso para secar em estufa a 60ºC por
aproximadamente 60 e 90 minutos. Em seguida triturá-los em um grau com pistilo. Os cristais
secos e moídos adquirem uma coloração verde esbranquiçada, conforme é visualizado na
Figura 5.
Figura 5: Sulfato de Ferro II – seco e moído.
3.0 Resultados e Discussão
Os experimentos realizados, conforme descrito no capítulo 2.0 apresentaram como
resultados óxidos de ferro nas cores amarelo, azul, cinza, lilás, marrom, preto e vermelho. O
processo de obtenção dos óxidos de ferro no modo descrito nas seis etapas como através dos
cristais moídos do sulfato de ferro II foi relativamente simples. Contudo, através dos cristais do
sulfato de ferro II o resultado esperado era certo, enquanto que no processo das seis etapas o
controle das reações exigia muita atenção e o resultado esperado nem sempre era obtido na
primeira vez.
Foram realizadas as análises quanto à solubilidade dos óxidos de ferro obtidos, todas
as amostras se mostraram insolúveis em água, conforme característica comum pigmentos.
Também foi analisada a capacidade dos óxidos de produzir cor em tinta acrílica
(dispersabilidade). O resultado mostrou boa dispersabilidade para todos os óxidos produzidos.
Outros testes foram realizados, como o de estabilidade da cor devido a ação da luz. Porém,
devido a intempérie esta análise não foi considerada.
ABRAFATI 2013 | ASSOCIAÇÃO BRASILEIRA DOS FABRICANTES DE TINTAS
13° Congresso Internacional de Tintas
13ª Exposição Internacional de Fornecedores para Tintas
(a) (b)
Figuras 6 (a) e (b): Pigmentos obtidos a partir de resíduos de ferro nas cores: amarelo, cinza,
lilás, marrom, vermelho e azul.
(a) (b) (c)
Figuras 5 (a), (b) e (c): Teste de dispersabilidade dos pigmentos de cores marrom, vermelho 2,
vermelho 1 e vermelho 3 em tinta acrílica.
4.0 Conclusão
As perspectivas de aplicação dos processos mencionados para obtenção de pigmentos
inorgânicos através do sulfato ferroso e de sulfato férrico a partir de resíduos industriais são
bastante promissoras tendo em vista a simplicidade dos equipamentos empregados.
Obviamente que para a produção de qualquer um dos compostos químicos derivados do ferro
pelos processos e matérias-primas aqui descritos, deve ser de responsabilidade de técnicos
capacitados. Recomenda-se ainda desenvolver estudos em escala de laboratório ou escala
piloto para que se possa inferir os parâmetros técnicos e econômicos mais próximos da
realidade para uma análise da viabilidade econômica de um empreendimento em escala
industrial.
5.0 REFERÊNCIAS
Astrall Industria Química Ltda. Acesso em 14.10.2012. Site: < http://www.astrallquimica.com.
br/ oxidodeferrosintetico.php.>.
Branco, P. M. Os pigmentos Minerais - CPRM Serviço Geológico do Brasil:
http//:www.cprm.gov.br/publique/cgi/cgilua.exe/sys/start.htm?infoid=1263&sid=129., 2009.
Acesso em 12/10/2012.
FERREIRA, J. A. & ANJOS, L. A. dos - Aspectos de saúde coletiva e ocupacional associados à
gestão dos resíduos sólidos municipais. Cad. Saúde Pública, 17(3), p. 689-696, R.J., 2001.
ABRAFATI 2013 | ASSOCIAÇÃO BRASILEIRA DOS FABRICANTES DE TINTAS
13° Congresso Internacional de Tintas
13ª Exposição Internacional de Fornecedores para Tintas
GIANSANTI, R. A cidade e o urbano no mundo atual. 1ª ed. Global Ed. e Distr., S.P., 2003.
MESQUITA J., J. M. de - Gestão integrada de resíduos sólidos. R.J., IBAM, 2007.
MERÇON, F. GUIMARÃES, P. I. C., MAINIER, F. B. CORROSÃO: Um Exemplo Usual de
Fenômeno Químico. Química N. na Escola n.19, p. 11, 2004.
Pigment Handbook, Ed. by P. A. Lewis, J. Wiley and Sons, N.Y., Vol. 1, p. 7, 1998.
ABRAFATI 2013 | ASSOCIAÇÃO BRASILEIRA DOS FABRICANTES DE TINTAS
Você também pode gostar
- Terra - A Herança Dos DeusesDocumento480 páginasTerra - A Herança Dos Deusesbelagouveia100% (2)
- Corrosão e Proteção dos MateriaisNo EverandCorrosão e Proteção dos MateriaisNota: 5 de 5 estrelas5/5 (1)
- Apostila Obq JRDocumento15 páginasApostila Obq JRWillian SampaioAinda não há avaliações
- Industria Do FosforoDocumento17 páginasIndustria Do FosfororafaelAinda não há avaliações
- Paper 155Documento4 páginasPaper 155Elson OliveiraAinda não há avaliações
- Cbpol-16216 1367024849Documento4 páginasCbpol-16216 1367024849Elson OliveiraAinda não há avaliações
- Admin, EC25Documento5 páginasAdmin, EC25Bruno Carlos Alves PinheiroAinda não há avaliações
- Obqjr2010 faseIIDocumento4 páginasObqjr2010 faseIIMatheusAinda não há avaliações
- Artigo Lama Vermelha 13de Agosto-Versão FinalDocumento13 páginasArtigo Lama Vermelha 13de Agosto-Versão FinalKATIA ALRELHIAAinda não há avaliações
- Inchamento de Argilas Organofílicas em Solventes Orgânicos: ResumoDocumento9 páginasInchamento de Argilas Organofílicas em Solventes Orgânicos: ResumoPaulo ZurcAinda não há avaliações
- Enxofre - Exercícios ÁcidosDocumento18 páginasEnxofre - Exercícios ÁcidosmarcelodalboAinda não há avaliações
- Química - Aprova TotalDocumento8 páginasQuímica - Aprova TotalGabriela MeirelesAinda não há avaliações
- 1529-Texto Do Artigo-5529-1-10-20191021Documento11 páginas1529-Texto Do Artigo-5529-1-10-20191021Lucas SoaresAinda não há avaliações
- Artigo TCC Incorporação Do LodoDocumento11 páginasArtigo TCC Incorporação Do LodoAnaCatarineMendesAinda não há avaliações
- Alfa AluminaDocumento11 páginasAlfa AluminaGuilherme EstevesAinda não há avaliações
- TD 22 Enem Uece 2 FaseDocumento8 páginasTD 22 Enem Uece 2 FaseseriacontamtoAinda não há avaliações
- Utilização Do Resíduo Proveniente Do Desdobramento de Rochas Ornamentais Na ConfecçãoDocumento5 páginasUtilização Do Resíduo Proveniente Do Desdobramento de Rochas Ornamentais Na Confecçãointelligenic torricelliAinda não há avaliações
- TEMA 6 - V12n2a02Documento7 páginasTEMA 6 - V12n2a02Nadia wiliamoAinda não há avaliações
- Aula 5Documento2 páginasAula 5Giovanna Galvão ScheideggerAinda não há avaliações
- Quimica 28 - 09Documento4 páginasQuimica 28 - 09Ana BeatrizAinda não há avaliações
- Cores de Compostos-Eurico Dias Rumo Ao ITADocumento7 páginasCores de Compostos-Eurico Dias Rumo Ao ITARodrigo HenriqueAinda não há avaliações
- 583 Teoria e Pratica Cores de Compostos ItaDocumento11 páginas583 Teoria e Pratica Cores de Compostos ItaMylena OliveiraAinda não há avaliações
- CT2005 131 00 CETEM BauxitaDocumento28 páginasCT2005 131 00 CETEM Bauxitanelson.damascenoAinda não há avaliações
- Questões Sobre Número de Oxidação 1Documento9 páginasQuestões Sobre Número de Oxidação 1Claudio Ribeiro PereiraAinda não há avaliações
- Atividade Do Experimento 8 (Oxirredução)Documento3 páginasAtividade Do Experimento 8 (Oxirredução)Erick SantosAinda não há avaliações
- Exercícios NOX-1Documento4 páginasExercícios NOX-1claudison123Ainda não há avaliações
- Número de OxidaçãoDocumento8 páginasNúmero de OxidaçãoRafael DantasAinda não há avaliações
- Yes Bras - Química Descritiva - Nelson SantosDocumento8 páginasYes Bras - Química Descritiva - Nelson SantosRaphael FurrierAinda não há avaliações
- Questões Enem EstequiometriaDocumento4 páginasQuestões Enem Estequiometriabininha89Ainda não há avaliações
- 2o Teste q12Documento4 páginas2o Teste q12Sofia DinizAinda não há avaliações
- Beneficiamento de CaulinDocumento14 páginasBeneficiamento de CaulinkensleyoliveiraAinda não há avaliações
- Foscação de VidroDocumento11 páginasFoscação de VidroThomas SilvaAinda não há avaliações
- Apostila Com Questoes EnemDocumento84 páginasApostila Com Questoes EnemLaura GontijoAinda não há avaliações
- Alfa - Módulo 30Documento11 páginasAlfa - Módulo 30Leonardo SoaresAinda não há avaliações
- Ed 5 Vol 5 Nº2 1quinz 1sem Nov 2019Documento10 páginasEd 5 Vol 5 Nº2 1quinz 1sem Nov 2019ANDRE LUIS BRITO BAPTISTAAinda não há avaliações
- Tosato - JR - JC - Paper - 5B1Documento10 páginasTosato - JR - JC - Paper - 5B1squajonAinda não há avaliações
- Simulado Emem 2010Documento2 páginasSimulado Emem 2010Romulo CastroAinda não há avaliações
- Simuladita 01Documento5 páginasSimuladita 01RAMON LORENZOAinda não há avaliações
- ENEM 202014 202a 20aplica C3 A7 C3 A3oDocumento13 páginasENEM 202014 202a 20aplica C3 A7 C3 A3oMarcio M. de CastroAinda não há avaliações
- Revisao Funçoes InorgaDocumento8 páginasRevisao Funçoes InorgaDiego BecalliAinda não há avaliações
- 07Documento7 páginas07Patrick SouzaAinda não há avaliações
- Reciclagem Do Crômio de Resíduos QuímicosDocumento4 páginasReciclagem Do Crômio de Resíduos QuímicosLeilaAinda não há avaliações
- Artigo Sobre Queima de Tijolos CeramicosDocumento5 páginasArtigo Sobre Queima de Tijolos CeramicosRafael Fernandes MaltyAinda não há avaliações
- Teoria e Pratica Quimica Cores de Compostos ItaDocumento11 páginasTeoria e Pratica Quimica Cores de Compostos ItaMonyque LimaAinda não há avaliações
- Relatório Ic AlexandreDocumento16 páginasRelatório Ic AlexandreAlexandre BertolacciniAinda não há avaliações
- Alfa - Módulo 29Documento7 páginasAlfa - Módulo 29Gildásio JúniorAinda não há avaliações
- Síntese Do Óxido de FerroDocumento6 páginasSíntese Do Óxido de FerroGustavo Rossoni RuyAinda não há avaliações
- Aod ProcessDocumento5 páginasAod ProcessMaria Aparecida Almeida AlvesAinda não há avaliações
- Corrigir o PH Do Solo Com CalcárioDocumento7 páginasCorrigir o PH Do Solo Com CalcárioWitalo ReisAinda não há avaliações
- Ferro - Ocorrência, Obtenção Industrial, Propriedades e Utilização - Pesquisa Escolar - UOL Educação PDFDocumento4 páginasFerro - Ocorrência, Obtenção Industrial, Propriedades e Utilização - Pesquisa Escolar - UOL Educação PDFLucas PontesAinda não há avaliações
- Revisão Uepa/ufpaDocumento2 páginasRevisão Uepa/ufpaEWERTON AFONSO100% (1)
- Lista Do ENEM 2020Documento6 páginasLista Do ENEM 2020Suelem SalesAinda não há avaliações
- Noções de Processo BayerDocumento4 páginasNoções de Processo BayerFabio PontesAinda não há avaliações
- OXIDAÇÃO EM METAIS p3Documento3 páginasOXIDAÇÃO EM METAIS p3Paula SilvaAinda não há avaliações
- Técnicas Para o Aproveitamento de Níquel, Cromo e Outros Metais em Resíduos IndustriaisNo EverandTécnicas Para o Aproveitamento de Níquel, Cromo e Outros Metais em Resíduos IndustriaisAinda não há avaliações
- Processos Tecnológicos e Modelagens Matemáticas de Oxidação de Percolados de Aterros SanitáriosNo EverandProcessos Tecnológicos e Modelagens Matemáticas de Oxidação de Percolados de Aterros SanitáriosAinda não há avaliações
- Utilização do lodo gerado na ETA de Alvorada-RS na fabricação de blocos cerâmicosNo EverandUtilização do lodo gerado na ETA de Alvorada-RS na fabricação de blocos cerâmicosAinda não há avaliações
- Efeito da Adição de Coque Verde de Petróleo na Microestrutura e Características Metalúrgicas do CoqueNo EverandEfeito da Adição de Coque Verde de Petróleo na Microestrutura e Características Metalúrgicas do CoqueAinda não há avaliações
- A sociedade do conhecimento e suas tecnologias: estudos em Ciências Exatas e Engenharias: Volume 1No EverandA sociedade do conhecimento e suas tecnologias: estudos em Ciências Exatas e Engenharias: Volume 1Ainda não há avaliações
- Capacidade do fungo Pleurotus ostreatus (cogumelo shimeji) na biorremediação de solos contaminados com chumbo (Pb)No EverandCapacidade do fungo Pleurotus ostreatus (cogumelo shimeji) na biorremediação de solos contaminados com chumbo (Pb)Ainda não há avaliações
- Avaliação da erva-mate como biossorventeNo EverandAvaliação da erva-mate como biossorventeAinda não há avaliações
- CV Elson Oliveira 2022 07Documento7 páginasCV Elson Oliveira 2022 07Elson OliveiraAinda não há avaliações
- Paper 161Documento7 páginasPaper 161Elson OliveiraAinda não há avaliações
- Descubra ZiguratsDocumento10 páginasDescubra ZiguratsElson OliveiraAinda não há avaliações
- (VC.07.ES) - Regulamento Votorantim Cimentos - Desafio em VídeoDocumento11 páginas(VC.07.ES) - Regulamento Votorantim Cimentos - Desafio em VídeoElson OliveiraAinda não há avaliações
- NTC 810030, Fev2016 - Chaves SU e SU Base CDocumento21 páginasNTC 810030, Fev2016 - Chaves SU e SU Base CElson OliveiraAinda não há avaliações
- Copel: Seccionadora de Faca Unipolar NTC 811221/24 Distribuição - 15 e 36,2 KVDocumento4 páginasCopel: Seccionadora de Faca Unipolar NTC 811221/24 Distribuição - 15 e 36,2 KVElson OliveiraAinda não há avaliações
- ASTM F-1185 - Especificação Padrão para Composição de Hidroxilapatita para Implantes Cirúrgicos (1) PortDocumento3 páginasASTM F-1185 - Especificação Padrão para Composição de Hidroxilapatita para Implantes Cirúrgicos (1) PortElson OliveiraAinda não há avaliações
- Elson Oliveira Sbqsul2022Documento1 páginaElson Oliveira Sbqsul2022Elson OliveiraAinda não há avaliações
- MANUAL tsd30Documento32 páginasMANUAL tsd30MARCOSAinda não há avaliações
- Fispq Da 70Documento6 páginasFispq Da 70Paulo OliveiraAinda não há avaliações
- Fispq - Limpador Geral PowerDocumento6 páginasFispq - Limpador Geral PowerFlavio Furtuoso RoqueAinda não há avaliações
- Semana 8 1 CorreçãoDocumento42 páginasSemana 8 1 Correçãojuze márioAinda não há avaliações
- Vigas Inclinadas - ExemploDocumento2 páginasVigas Inclinadas - Exemplojorge25_aguila2832Ainda não há avaliações
- Programa de FANDocumento4 páginasPrograma de FANBeneditoAinda não há avaliações
- Relatório Lançamento de ProjéteisDocumento4 páginasRelatório Lançamento de ProjéteisLuiz Fernando F. De AndradeAinda não há avaliações
- Campo Pescada: Plano de DesenvolvimentoDocumento216 páginasCampo Pescada: Plano de DesenvolvimentoalannymeloAinda não há avaliações
- 11ano F 1 2 2 1 Interacao GraviticaDocumento12 páginas11ano F 1 2 2 1 Interacao GraviticaISLAMICO69Ainda não há avaliações
- Soldagem A Arco SubmersoDocumento6 páginasSoldagem A Arco SubmersoWesley QuirinoAinda não há avaliações
- Aula - Pratica.09 EsterificacaoDocumento3 páginasAula - Pratica.09 Esterificacaodelbianc9579Ainda não há avaliações
- Aula de Formula Percentual e MinimaDocumento24 páginasAula de Formula Percentual e MinimaMarta França100% (1)
- Relatório 4 - Lab de Fluidosmecânicos - Placa de OrifícioDocumento6 páginasRelatório 4 - Lab de Fluidosmecânicos - Placa de OrifícioGabriel MarzolaAinda não há avaliações
- Átomos, Elementos e Tabela PeriódicaDocumento46 páginasÁtomos, Elementos e Tabela PeriódicaRaquel De Deus FreiAinda não há avaliações
- Carimo Lazima. Ap11Documento12 páginasCarimo Lazima. Ap11Tomás MahalambeAinda não há avaliações
- Geodinamica Externa (Orginal)Documento25 páginasGeodinamica Externa (Orginal)jean33% (3)
- Fispqs - Solvente - Baden PDFDocumento8 páginasFispqs - Solvente - Baden PDFLais de OliveiraAinda não há avaliações
- Aula 49 - Energia Mecânica - Sistemas ConservativosDocumento2 páginasAula 49 - Energia Mecânica - Sistemas ConservativosvictorphisisAinda não há avaliações
- Lista de Exercícios 2 AnoDocumento6 páginasLista de Exercícios 2 AnoLuis RibeiroAinda não há avaliações
- Permissividade Dielétrica Dos MateriaisDocumento20 páginasPermissividade Dielétrica Dos MateriaisBrunoAinda não há avaliações
- Técnica Frap - EmbrapaDocumento4 páginasTécnica Frap - EmbrapaVanessa VieraAinda não há avaliações
- Volumetria de ComplexaçãoDocumento16 páginasVolumetria de ComplexaçãoliviasavignonAinda não há avaliações
- Tópicos Especiais II - Aula 1 - Processos de Obtenção de Metais Ferrosos e Não Ferrosos PDFDocumento30 páginasTópicos Especiais II - Aula 1 - Processos de Obtenção de Metais Ferrosos e Não Ferrosos PDFBrStal MetalurgicaAinda não há avaliações
- Prova - Eags 2021 - Cod - 64 - 07 10 2020 10 49 47Documento16 páginasProva - Eags 2021 - Cod - 64 - 07 10 2020 10 49 47Luã VictorAinda não há avaliações
- Nº04 - Análise - Laís Vieira 1Documento16 páginasNº04 - Análise - Laís Vieira 1Laís SantosAinda não há avaliações
- FotoiniciadorescurauvDocumento13 páginasFotoiniciadorescurauvjuvenalllAinda não há avaliações
- Fundamentos de Quimica Experimental PDFDocumento233 páginasFundamentos de Quimica Experimental PDFCleiton ReisAinda não há avaliações
- Macetes e Propriedades Da Tabela PerDocumento1 páginaMacetes e Propriedades Da Tabela PerMarília RosatoAinda não há avaliações
- FQ PosterDocumento1 páginaFQ PosterMatilde MaiaAinda não há avaliações