Escolar Documentos
Profissional Documentos
Cultura Documentos
Modelo atômico de Dalton e Rutherford
Enviado por
Jean Brilhante0 notas0% acharam este documento útil (0 voto)
14 visualizações2 páginasO documento discute os modelos atômicos de Dalton, Thomson e Rutherford. O modelo de Dalton propôs que os átomos são esferas sólidas com partículas de carga negativa na superfície. O modelo de Thomson sugeriu que os átomos contêm partículas negativas espalhadas em um mar de matéria positiva. O modelo de Rutherford foi baseado no experimento de bombardeio de partículas alfa em folhas de ouro e propôs que os átomos contêm um núcleo positivo com partículas neg
Descrição original:
Título original
LISTA REVISÃO
Direitos autorais
© © All Rights Reserved
Formatos disponíveis
PDF, TXT ou leia online no Scribd
Compartilhar este documento
Compartilhar ou incorporar documento
Você considera este documento útil?
Este conteúdo é inapropriado?
Denunciar este documentoO documento discute os modelos atômicos de Dalton, Thomson e Rutherford. O modelo de Dalton propôs que os átomos são esferas sólidas com partículas de carga negativa na superfície. O modelo de Thomson sugeriu que os átomos contêm partículas negativas espalhadas em um mar de matéria positiva. O modelo de Rutherford foi baseado no experimento de bombardeio de partículas alfa em folhas de ouro e propôs que os átomos contêm um núcleo positivo com partículas neg
Direitos autorais:
© All Rights Reserved
Formatos disponíveis
Baixe no formato PDF, TXT ou leia online no Scribd
0 notas0% acharam este documento útil (0 voto)
14 visualizações2 páginasModelo atômico de Dalton e Rutherford
Enviado por
Jean BrilhanteO documento discute os modelos atômicos de Dalton, Thomson e Rutherford. O modelo de Dalton propôs que os átomos são esferas sólidas com partículas de carga negativa na superfície. O modelo de Thomson sugeriu que os átomos contêm partículas negativas espalhadas em um mar de matéria positiva. O modelo de Rutherford foi baseado no experimento de bombardeio de partículas alfa em folhas de ouro e propôs que os átomos contêm um núcleo positivo com partículas neg
Direitos autorais:
© All Rights Reserved
Formatos disponíveis
Baixe no formato PDF, TXT ou leia online no Scribd
Você está na página 1de 2
REVISÃO 2 ANO ATOMÍSTICA conhecido como “pudim de passas”.
POLIVALENTE MODELO Para esse modelo, pode-se afirmar que:
PRIMEIRO BIMESTRE a) O núcleo atômico ocupa um volume
1. De acordo com a teoria atômica de mínimo no centro do átomo.
Dalton (1766-1844) assinale a b) As cargas negativas estão
alternativa correta distribuídas homogeneamente por todo
a) O átomo possui partículas de carga o átomo.
negativa que estão em órbita de um c) Os elétrons estão distribuídos em
núcleo de carga positiva. órbitas fixas ao redor do núcleo.
b) No núcleo atômico existem partículas d) Os átomos são esferas duras, do tipo
de carga nula, denominada nêutrons. de uma bola de bilhar.
c) Átomos de elementos diferentes e) Os elétrons estão espalhados
possuíam diferentes massas e aleatoriamente no espaço ao redor do
propriedades. núcleo.
d) O átomo era uma esfera sólida que 4) Considere as seguintes afirmativas
possuía partículas de carga negativa em sobre o modelo atômico de Rutherford:
sua superfície, semelhante a um “pudim 1. O modelo atômico de Rutherford é
de passas”. também conhecido como modelo
e) Dois elétrons de mesmo spin não planetário do átomo.
podem ser encontrados dentro de um 2. No modelo atômico, considera-se que
mesmo orbital. elétrons de cargas negativas circundam
2) Em 1803, John Dalton propôs um em órbitas ao redor de um núcleo de
modelo de teoria atômica. Considere carga positiva.
que sobre a base conceitual desse 3. Segundo Rutherford, a eletrosfera,
modelo sejam feitas as seguintes local onde se encontram os elétrons,
afirmações: possui um diâmetro menor que o núcleo
I. O átomo apresentará a configuração atômico.
de uma esfera rígida. 5. Na proposição do seu modelo
II. Os átomos caracterizam os elementos atômico, Rutherford se baseou num
químicos e somente os átomos de um experimento em que uma lamínula de
mesmo elemento são idênticos em todos ouro foi bombardeada por partículas
os aspectos. alfa.
III. As transformações químicas Assinale a alternativa correta:
consistem de combinação, separação a) Somente a afirmativa 1 é verdadeira.
e/ou rearranjo de átomos. b) Somente as afirmativas 3 e 4 são
IV. Compostos químicos são formados verdadeiras.
de átomos de dois ou mais elementos c) Somente as afirmativas 1, 2 e 3 são
unidos em uma razão fixa. verdadeiras.
Qual das opções abaixo se refere a todas d) Somente as afirmativas 1, 2 e 4 são
as afirmações CORRETAS? verdadeiras.
e) As afirmativas 1, 2, 3 e 4 são
a) I e IV. b) II e III. c) II e verdadeiras.
IV. d) II, III e IV. e) I, II, III e 5) O átomo é a menor partícula que
IV. identifica um elemento químico. Este
3) No ano de 1897, o cientista britânico possui duas partes, a saber: uma delas é
J.J. Thomson descobriu, através de o núcleo constituído por prótons e
experiências com os raios catódicos, a nêutrons e a outra é a região externa – a
primeira evidência experimental da eletrosfera – por onde circulam os
estrutura interna dos átomos. O modelo elétrons. Alguns experimentos
atômico proposto por Thomson ficou permitiram a descoberta das
características das partículas a) I, II, III e IV
constituintes do átomo. Em relação a b) III, IV, II e I
essas características, assinale a c) IV, II, I e III
alternativa correta. d) II, III, IV e I
a) Prótons e elétrons possuem massas e) III, II, I e IV
iguais e cargas elétricas de sinais 8) Uma distribuição eletrônica possível
opostos. para um elemento X, que pertence à
b) Entre as partículas atômicas, os mesma família do elemento bromo, cujo
elétrons têm maior massa e ocupam número atômico é igual a 35, é:
maior volume no átomo. a) 1s2, 2s2, 2p5
c) Entre as partículas atômicas, os b) 1s2, 2s2, 2p6, 3s2, 3p1
prótons e nêutrons têm maior massa e c) 1s2, 2s2, 2p2
ocupam maior volume no átomo. d) 1s2, 2s2, 2p6, 3s1
d) Entre as partículas atômicas, os e) 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d
prótons e nêutrons têm mais massa, mas 9) O número de elétrons da camada de
ocupam um volume muito pequeno em valência do átomo de cálcio (Z = 20),
relação ao volume total do átomo. no estado fundamental, é
e) todas as partículas atômicas tem a a) 1
mesma carga elétrica b) 2
6) O sódio é um metal que está presente c) 6
no primeiro grupo da tabela periódica. d) 8
O átomo desse elemento pode ser e) 10
representado por 11Na23. O número de 10) A água mineral é
prótons, elétrons e nêutrons desse
elemento é, respectivamente: a) Uma substância pura
a) 23, 23 e 11 b) Uma substância simples
b) 11, 23 e 12 c) Uma substância composta
c) 12, 12 e 11 d) Uma mistura
d) 11, 11 e 12 E) um colóide
e) 13, 11e 11
7) Analise as afirmativas a seguir.
I. Os prótons, partículas carregadas
positivamente, estão numa pequena
região central do átomo, o núcleo, e ao
seu redor movem-se os elétrons.
II. Os estudos sobre a natureza elétrica
da matéria desencadearam a descoberta
de partículas carregadas negativamente,
os elétrons.
III. Os elétrons movem-se em camadas
circulares ao redor do núcleo, que
apresentam valores de energia
específicos.
IV. Os átomos são partículas
minúsculas, esféricas e indivisíveis.
Átomos de elementos químicos distintos
diferem-se pela massa e tamanho.
A seqüência correta que corresponde à
evolução dos modelos atômicos é:
Você também pode gostar
- Lista de Exercicios - Modelo Atomico v3Documento5 páginasLista de Exercicios - Modelo Atomico v3Bruno FernandesAinda não há avaliações
- Modelos atômicos de Dalton, Thomson e RutherfordDocumento5 páginasModelos atômicos de Dalton, Thomson e RutherfordGuilherme Borba100% (1)
- (20160822190740) Evolução Dos Modelos Atômicos e Estrutura Atômica Química Geral Pós AulaDocumento7 páginas(20160822190740) Evolução Dos Modelos Atômicos e Estrutura Atômica Química Geral Pós AulaBárbara MirandaAinda não há avaliações
- Modelos Atômicos: da Esfera à Estrutura NuclearDocumento6 páginasModelos Atômicos: da Esfera à Estrutura NuclearOFA ExtremeAinda não há avaliações
- Exerc Modelos AtomicosDocumento2 páginasExerc Modelos Atomicoslopesqui1766Ainda não há avaliações
- Lista 04 - Modelos AtômicosDocumento3 páginasLista 04 - Modelos AtômicosMarcelo SilvaAinda não há avaliações
- Avaliação de Ciências - 9º Ano - 1º BDocumento5 páginasAvaliação de Ciências - 9º Ano - 1º BLucieudo NascimentoAinda não há avaliações
- Quim01 Livro Propostos PDFDocumento136 páginasQuim01 Livro Propostos PDFElias FreitasAinda não há avaliações
- Modelo atômico Rutherford BohrDocumento5 páginasModelo atômico Rutherford BohrGleidiane FerreiraAinda não há avaliações
- Química 2º AnoDocumento3 páginasQuímica 2º AnoCarlos NeyAinda não há avaliações
- Tabela Periódica ExercDocumento2 páginasTabela Periódica ExercFABIANA TERESINHA PEREIRAAinda não há avaliações
- Modelo atômico de Rutherford e experimento com partículas alfaDocumento2 páginasModelo atômico de Rutherford e experimento com partículas alfacarineboni100% (1)
- Atomistica EXERCICIOSDocumento18 páginasAtomistica EXERCICIOSMario LuizAinda não há avaliações
- Lista de Exerci Cios 8 Modelos Ato Micos 1Documento6 páginasLista de Exerci Cios 8 Modelos Ato Micos 1Juan RiquelmeAinda não há avaliações
- Dia 1 - Física Moderna Projeto EspecialistaDocumento4 páginasDia 1 - Física Moderna Projeto Especialistavictoria riosAinda não há avaliações
- Exercicios Modelos AtomicosDocumento2 páginasExercicios Modelos AtomicoskarolinesnantesAinda não há avaliações
- ANP 9 - 9º Ano - Avaliação de Recuperação Modelos AtomicosDocumento3 páginasANP 9 - 9º Ano - Avaliação de Recuperação Modelos AtomicosIslander SalibaAinda não há avaliações
- Atividade Modelos AtomicosDocumento4 páginasAtividade Modelos AtomicosMinnaAinda não há avaliações
- Exercício Sobre Modelos AtômicosDocumento3 páginasExercício Sobre Modelos AtômicosNutraervas Produtos NaturaisAinda não há avaliações
- Modelos atômicos históricosDocumento6 páginasModelos atômicos históricosfrancyniAinda não há avaliações
- Modelos atômicos de Thomson, Rutherford e BohrDocumento2 páginasModelos atômicos de Thomson, Rutherford e BohrEduarda GomesAinda não há avaliações
- Atomistic ADocumento4 páginasAtomistic AHeloísa ReisAinda não há avaliações
- ExercíciosDocumento3 páginasExercíciosleohsokulskiAinda não há avaliações
- Revisão de QuímicaDocumento4 páginasRevisão de QuímicaJean CarlosAinda não há avaliações
- Evolução Dos Modelos AtomicosDocumento6 páginasEvolução Dos Modelos AtomicosPaulCumbassAinda não há avaliações
- Estrutura Fundamental QuestDocumento4 páginasEstrutura Fundamental QuestMaria FernandaAinda não há avaliações
- Estrutura AtmicaDocumento9 páginasEstrutura AtmicaShoda25Ainda não há avaliações
- Exercicios de Modelos Atomicos Sem GabaritoDocumento6 páginasExercicios de Modelos Atomicos Sem Gabaritojhonatancb48Ainda não há avaliações
- Modelos atômicos: evolução histórica das ideiasDocumento27 páginasModelos atômicos: evolução histórica das ideiasJéssica RamalhoAinda não há avaliações
- Modelos atômicos: evolução históricaDocumento7 páginasModelos atômicos: evolução históricaHenrique Gabriel Barbosa Guida RodriguesAinda não há avaliações
- Química - Pré-Vestibular Impacto - Exercícios Extras - Atomística 05Documento2 páginasQuímica - Pré-Vestibular Impacto - Exercícios Extras - Atomística 05Caty SerejoAinda não há avaliações
- Exercicios Modelos AtomicosDocumento3 páginasExercicios Modelos AtomicoskarolinesnantesAinda não há avaliações
- Modelos Atômicos - Lista de Exercícios de Química 1° SérieDocumento2 páginasModelos Atômicos - Lista de Exercícios de Química 1° SérieSilver HunterAinda não há avaliações
- Atomistica - Exercicios GabaritadosDocumento34 páginasAtomistica - Exercicios Gabaritadosnergal569% (13)
- Aula01QuimicaConceitosbasicosElementoQuimicoProf Manuel23 02 2017comgabarito pdf23022017062528Documento4 páginasAula01QuimicaConceitosbasicosElementoQuimicoProf Manuel23 02 2017comgabarito pdf23022017062528ricardo almeidaAinda não há avaliações
- Modelos atômicos históricosDocumento2 páginasModelos atômicos históricosEversonAinda não há avaliações
- Exercicio de Modelo AtômicoDocumento4 páginasExercicio de Modelo AtômicoAna PaulaAinda não há avaliações
- Lista-De-Exercicios-Estrutura Atômica Modelos e SemelhançasDocumento3 páginasLista-De-Exercicios-Estrutura Atômica Modelos e SemelhançasCiele RibeiroAinda não há avaliações
- 9ºano 2bim Exer de Revisão SiteDocumento7 páginas9ºano 2bim Exer de Revisão SiteAna Alves de SouzaAinda não há avaliações
- Quim01 Livro PropostosDocumento136 páginasQuim01 Livro PropostosValdeir AntonioAinda não há avaliações
- Lista de exercícios de atomísticaDocumento5 páginasLista de exercícios de atomísticaNatalia RibeiroAinda não há avaliações
- ATOMÍSTICA E DISTRIBUIÇÃODocumento17 páginasATOMÍSTICA E DISTRIBUIÇÃORebeca SáAinda não há avaliações
- Modelo atômico de Rutherford comparado ao Sistema SolarDocumento3 páginasModelo atômico de Rutherford comparado ao Sistema SolarCarlos Junior BarrosAinda não há avaliações
- Estudo Dirigido Estrutura AtomicaDocumento2 páginasEstudo Dirigido Estrutura AtomicaCamila D'AvilaAinda não há avaliações
- Modelos atômicos: Thomson, Dalton e RutherfordDocumento4 páginasModelos atômicos: Thomson, Dalton e RutherfordRenilde CastroAinda não há avaliações
- Química Atividade1Documento1 páginaQuímica Atividade1Thiago VictorAinda não há avaliações
- O Modelo Atômico de RutherfordDocumento4 páginasO Modelo Atômico de Rutherfordisabella100% (1)
- Exercício de Modelos AtômicosDocumento4 páginasExercício de Modelos AtômicosDenis Damiana De Castro OliveiraAinda não há avaliações
- Modelos atômicos de Dalton, Bohr e RutherfordDocumento19 páginasModelos atômicos de Dalton, Bohr e RutherfordLuciano JuniorAinda não há avaliações
- C Quim Aula 1Documento14 páginasC Quim Aula 1emillyalvestopAinda não há avaliações
- Modelos atômicos: evolução histórica e conceitos-chaveDocumento5 páginasModelos atômicos: evolução histórica e conceitos-chaveIgor AparecidoAinda não há avaliações
- Exercícios de Atomística - Profº Agamenon RobertoDocumento37 páginasExercícios de Atomística - Profº Agamenon Robertocb_penatrujillo57% (7)
- Modelo-Av. Q 01Documento3 páginasModelo-Av. Q 01Matheus Andrade TorresAinda não há avaliações
- Evolução pele humanaDocumento2 páginasEvolução pele humanaJean BrilhanteAinda não há avaliações
- Prova 3 ADocumento6 páginasProva 3 AJean BrilhanteAinda não há avaliações
- 2 Chamada PROVA BIMESTRAL QUÍMICA POLIVALENTE 2 ANOSDocumento1 página2 Chamada PROVA BIMESTRAL QUÍMICA POLIVALENTE 2 ANOSJean BrilhanteAinda não há avaliações
- Fermentação 2 AnosDocumento9 páginasFermentação 2 AnosJean BrilhanteAinda não há avaliações
- Identificação de plantas medicinais na horta da escolaDocumento2 páginasIdentificação de plantas medicinais na horta da escolaJean BrilhanteAinda não há avaliações
- Atividade biologia - experimentos fermentaçãoDocumento2 páginasAtividade biologia - experimentos fermentaçãoJean BrilhanteAinda não há avaliações
- Questões Biologia 2 Ano Prof Jean Brilhante Metabolismo EnergéticoDocumento1 páginaQuestões Biologia 2 Ano Prof Jean Brilhante Metabolismo EnergéticoJean BrilhanteAinda não há avaliações
- Modelo atômico de Dalton e RutherfordDocumento2 páginasModelo atômico de Dalton e RutherfordJean BrilhanteAinda não há avaliações
- REVISÃO QUÍMICA RADIAÇÃODocumento4 páginasREVISÃO QUÍMICA RADIAÇÃOJean BrilhanteAinda não há avaliações
- AlgasDocumento2 páginasAlgasJean BrilhanteAinda não há avaliações
- REVISÃO DE BIOLOGIA COM QUESTÕES DE METABOLISMO E FOTOSSÍNTESEDocumento1 páginaREVISÃO DE BIOLOGIA COM QUESTÕES DE METABOLISMO E FOTOSSÍNTESEJean BrilhanteAinda não há avaliações
- Filo Dos CordadosDocumento21 páginasFilo Dos CordadosJean BrilhanteAinda não há avaliações
- Reino Protista: Algas e CaracterísticasDocumento58 páginasReino Protista: Algas e CaracterísticasJean BrilhanteAinda não há avaliações
- V 5angiospermas Florfrutoesemente 110814212252 Phpapp01Documento38 páginasV 5angiospermas Florfrutoesemente 110814212252 Phpapp01Gui BotAinda não há avaliações
- Evolução dos Grupos VegetaisDocumento51 páginasEvolução dos Grupos VegetaisJean BrilhanteAinda não há avaliações
- Reino vegetal: Briófitas, Pteridófitas, Gimnospermas e AngiospermasDocumento51 páginasReino vegetal: Briófitas, Pteridófitas, Gimnospermas e AngiospermasJean BrilhanteAinda não há avaliações
- Evolução das plantasDocumento17 páginasEvolução das plantasJean BrilhanteAinda não há avaliações
- V 5angiospermas Florfrutoesemente 110814212252 Phpapp01Documento38 páginasV 5angiospermas Florfrutoesemente 110814212252 Phpapp01Gui BotAinda não há avaliações
- Distúrbios do potássio: hipo e hipercalemiaDocumento5 páginasDistúrbios do potássio: hipo e hipercalemiaLUCAS GUILHERME LINOAinda não há avaliações
- Bioquímica Fundamentos CelularesDocumento9 páginasBioquímica Fundamentos CelularesPriscila CunhaAinda não há avaliações
- Exercícios Sobre Nomenclatura de Hidrocarbonetos - Toda Matéria - SoladoDocumento10 páginasExercícios Sobre Nomenclatura de Hidrocarbonetos - Toda Matéria - Soladodarlan danramAinda não há avaliações
- Pratica Preparo de SolucoesDocumento4 páginasPratica Preparo de SolucoesMatheus RodriguesAinda não há avaliações
- Aula 03 - Catálise e Catalisadores - Cálculo de Reatores II 2020 - 2Documento30 páginasAula 03 - Catálise e Catalisadores - Cálculo de Reatores II 2020 - 2Hebert SutilAinda não há avaliações
- UNIDADE 3 - Materiais e Tecnologia TêxtilDocumento11 páginasUNIDADE 3 - Materiais e Tecnologia TêxtilShiro Quick MassageAinda não há avaliações
- Aplicação do solo grampeado em obra de grande porteDocumento37 páginasAplicação do solo grampeado em obra de grande porteZeDoChaaAinda não há avaliações
- Atividade 1 - Seg - Segurança Do Trabalho Industrial - 51-2023Documento2 páginasAtividade 1 - Seg - Segurança Do Trabalho Industrial - 51-2023Cavalini Assessoria AcadêmicaAinda não há avaliações
- Efeito da adição de nitrogênio na microestrutura e propriedades mecânicas do ADI austemperadoDocumento1 páginaEfeito da adição de nitrogênio na microestrutura e propriedades mecânicas do ADI austemperadoLeonardo PereiraAinda não há avaliações
- AULA 3 - Peeling, Hidratação e AcnesDocumento74 páginasAULA 3 - Peeling, Hidratação e AcnesThayane Diniz100% (1)
- Artigo - Corrosão 2 Unid PDFDocumento6 páginasArtigo - Corrosão 2 Unid PDFNicoly CoelhoAinda não há avaliações
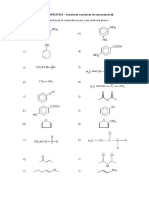
- Exercicios de Estru Ressonancia 2 PDFDocumento5 páginasExercicios de Estru Ressonancia 2 PDFGui LhermeAinda não há avaliações
- Manual do Usuário Kit GNV LandirenzoDocumento44 páginasManual do Usuário Kit GNV LandirenzoJunior MacielAinda não há avaliações
- Revisão - ENEM-SEMANA DDocumento25 páginasRevisão - ENEM-SEMANA DJedaAinda não há avaliações
- Segurança contra incêndios em edificaçõesDocumento30 páginasSegurança contra incêndios em edificaçõesmat_2412Ainda não há avaliações
- Atividades de Revisão de Ciências 2º BimestreDocumento2 páginasAtividades de Revisão de Ciências 2º BimestreAline Castro SilvaAinda não há avaliações
- Termoquímica: Trocas de Energia CalorDocumento17 páginasTermoquímica: Trocas de Energia Caloreng civil Paulo Vitor MedeirosAinda não há avaliações
- Cromatografia SupercríticaDocumento11 páginasCromatografia Supercríticajean.pinheiroAinda não há avaliações
- Manual de Operação - 908EDocumento168 páginasManual de Operação - 908EMicaella SerafimAinda não há avaliações
- Revestimento epóxi para tanques de óleo emDocumento4 páginasRevestimento epóxi para tanques de óleo emDatabook GaleaoAinda não há avaliações
- Aula Destilacao MulticomponentesDocumento18 páginasAula Destilacao MulticomponentesThais OliveiraAinda não há avaliações
- Enunciados Exemplos - AdsorçãoDocumento30 páginasEnunciados Exemplos - AdsorçãoFelipe Castro100% (1)
- Aula 2 e 3 Compressores Distribuição e Condicionamento ACDocumento56 páginasAula 2 e 3 Compressores Distribuição e Condicionamento ACAndré LuisAinda não há avaliações
- Moléculas, Fórmulas Químicas e ReaçõesDocumento11 páginasMoléculas, Fórmulas Químicas e ReaçõesanitadiogoAinda não há avaliações
- Aula Geometria Molecular e PolaridadeDocumento31 páginasAula Geometria Molecular e PolaridadeGabriela ParroAinda não há avaliações
- UFSC - Tratamento de água e efluentes na BLUMENAUDocumento35 páginasUFSC - Tratamento de água e efluentes na BLUMENAUAna Julia CorreiaAinda não há avaliações
- Os Sintagmas Nominais. Cap.13.resumo - Gramática.1º AnoDocumento12 páginasOs Sintagmas Nominais. Cap.13.resumo - Gramática.1º AnoJulia DeluquiAinda não há avaliações
- 3.4.2 - Fainas 2 - Cbinc - ExercícioDocumento8 páginas3.4.2 - Fainas 2 - Cbinc - ExercícioHelson AfonsoAinda não há avaliações
- Estudo Dos Elementos Ferro (Fe), Cobalto (Co) e Cobre (Cu)Documento33 páginasEstudo Dos Elementos Ferro (Fe), Cobalto (Co) e Cobre (Cu)MARIA SERPAAinda não há avaliações
- Memorial Descritivo Hidrossanitário R06Documento6 páginasMemorial Descritivo Hidrossanitário R06Secretaria de Planejamento Governador Celso RamosAinda não há avaliações