Escolar Documentos
Profissional Documentos
Cultura Documentos
Química - Cinetica Quimica Ok
Enviado por
RAFAELA CARMINATTI0 notas0% acharam este documento útil (0 voto)
9 visualizações1 páginaTítulo original
QUÍMICA - CINETICA QUIMICA OK
Direitos autorais
© © All Rights Reserved
Formatos disponíveis
PDF, TXT ou leia online no Scribd
Compartilhar este documento
Compartilhar ou incorporar documento
Você considera este documento útil?
Este conteúdo é inapropriado?
Denunciar este documentoDireitos autorais:
© All Rights Reserved
Formatos disponíveis
Baixe no formato PDF, TXT ou leia online no Scribd
0 notas0% acharam este documento útil (0 voto)
9 visualizações1 páginaQuímica - Cinetica Quimica Ok
Enviado por
RAFAELA CARMINATTIDireitos autorais:
© All Rights Reserved
Formatos disponíveis
Baixe no formato PDF, TXT ou leia online no Scribd
Você está na página 1de 1
QUÍMICA
1) Fatores que alteram
a velocidade da reação CINÉTICA QUÍMICA
a) Concentração ([ ])
↑[ ] = ↑choques efetivos = ↑V
b) Pressão (P) 3) Lei de ação das massas c) Quando o problema fornecer
↑P = ↓d = ↑choques efetivos = ↑V experimentos, os valores de
c) Temperatura (T) aA + bB → cC + dD α e β devem ser cálculados.
↑T = ↑Ec entre moléculas = ↑V N2 + 3H2 → 2NH3
d) Catalisador (CAT)
Adição CAT = ↓Eat = ↑V V = K ⋅ [A]α ⋅ [B]β
[N2] [H2] V
e) Superfície de Contato (SC)
Quanto mais fragmentado, ↑V I 0,01 0,4 1
a) Para uma reação elementar x2 x2
α=a e β=b
II 0,02 0,4 2
b) Quando uma reação ocorrer x2 x4
em mais de uma etapa, a
III 0,02 0,8 8
2) Cálculo da Velocidade Média expressão da velocidade é
dada pela etapa lenta.
2A + B → A2B (lenta) V = K ⋅ [N2 ]α ⋅ [H2 ]β
∆n
Vm = A2B + C → 4D (rápida)
∆t
(I) e (II) (I) e (II)
V = K ⋅ [A]2 ⋅ [B]1
V = [N2 ]α V = [H2 ]β
aA + bB → cC + dD
2 = 2α 4 = 2β
OBS.: Ordem de uma reação (OR) α=1 β=2
VA VB VC VD
Vm = = = = OR = α + β
a b c d OR = 2 + 1 = 3ª ordem
V = K ⋅ [N2 ]1 ⋅ [H2 ]2
Você também pode gostar
- Matemática, Vol. 2, BERNOULLI (Completa) - Edição 2020Documento84 páginasMatemática, Vol. 2, BERNOULLI (Completa) - Edição 2020José MárioAinda não há avaliações
- ABNT NBR 5626-2020 - Sistemas Prediais de Água Fria e Água QuenteDocumento64 páginasABNT NBR 5626-2020 - Sistemas Prediais de Água Fria e Água QuenteFilipe DionisioAinda não há avaliações
- Exercício 4Documento15 páginasExercício 4Diogo Simão100% (1)
- Escola de Engenharia de Lorena - EEL: P1 - Cálculo de Reatores - EBQ7 - GABARITODocumento3 páginasEscola de Engenharia de Lorena - EEL: P1 - Cálculo de Reatores - EBQ7 - GABARITOArmando Mateus MoianaAinda não há avaliações
- Solution BoldriniDocumento102 páginasSolution BoldriniGuilherme Viana100% (1)
- Exames Qualificacao ProfmatDocumento203 páginasExames Qualificacao Profmatacleydson2010100% (1)
- Aula 8 - FiltraçãoDocumento51 páginasAula 8 - FiltraçãoNayara Souza100% (1)
- Quimica Mapa MentalDocumento11 páginasQuimica Mapa MentalMaria Eduarda Dalla Lana de OliveiraAinda não há avaliações
- Teste2 AL2022 23v11netDocumento4 páginasTeste2 AL2022 23v11netLucas CayollaAinda não há avaliações
- Aula 6 - 1 Resolvido FatorialDocumento18 páginasAula 6 - 1 Resolvido FatorialMatheusSáAinda não há avaliações
- ENQ 2017-2 GabaritoDocumento11 páginasENQ 2017-2 Gabaritodaniel dunckAinda não há avaliações
- Exercícios - Lista 1Documento3 páginasExercícios - Lista 1Suwide MarquesAinda não há avaliações
- Gabarito - PENSI - IME - ITA - 24 - Ciclo 2 - IME ObjetivoDocumento34 páginasGabarito - PENSI - IME - ITA - 24 - Ciclo 2 - IME Objetivopaulo.24172608Ainda não há avaliações
- Produtos Notaveis e FatoracaoDocumento6 páginasProdutos Notaveis e FatoracaoMilenaAinda não há avaliações
- Teste II Guia de CorreçãoDocumento4 páginasTeste II Guia de CorreçãoSami NzéAinda não há avaliações
- FatoraçãoDocumento7 páginasFatoraçãoMARCIOAinda não há avaliações
- 9 Ano - Mat 1 - Resolução Dos Exercícios 3 e 4 Da Lista 1Documento3 páginas9 Ano - Mat 1 - Resolução Dos Exercícios 3 e 4 Da Lista 1Thiago ArtiolliAinda não há avaliações
- Aula 13-Adjunta e Regra de CramerDocumento10 páginasAula 13-Adjunta e Regra de CramerMantorras NeloAinda não há avaliações
- RaizesDocumento11 páginasRaizesVIVIAinda não há avaliações
- Respostas Lista 1 GAALDocumento2 páginasRespostas Lista 1 GAALmatheus augustoAinda não há avaliações
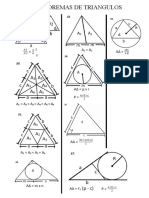
- Teoremas de TriangulosDocumento5 páginasTeoremas de TriangulosKelly Cáceres AceroAinda não há avaliações
- Teste2 AL1617VAsolDocumento4 páginasTeste2 AL1617VAsolAntónio Pedro AbreuAinda não há avaliações
- Livro - Função Do Segundo Grau - 230921 - 124303Documento9 páginasLivro - Função Do Segundo Grau - 230921 - 124303Danilo BarretoAinda não há avaliações
- Alunos SumidosDocumento6 páginasAlunos SumidosEdneyAinda não há avaliações
- Produtos Notáveis - Parte 02Documento10 páginasProdutos Notáveis - Parte 02FranciscoAntonioMartinsdePaivaAinda não há avaliações
- Cinética Química - 2Documento23 páginasCinética Química - 2Gileade ChurchAinda não há avaliações
- 2019 PADRÃO 4 Fundamentos QuímicaDocumento9 páginas2019 PADRÃO 4 Fundamentos QuímicaAriel MorónAinda não há avaliações
- 25-Cinética (Lei e Velocidade)Documento2 páginas25-Cinética (Lei e Velocidade)nv77vnmAinda não há avaliações
- ENQ 2023.1 Prova GabaritoDocumento9 páginasENQ 2023.1 Prova GabaritoJackson PinhoAinda não há avaliações
- Gabarito ENQ 2019.1 Extra PDF ProbabilidadeDocumento1 páginaGabarito ENQ 2019.1 Extra PDF ProbabilidadeThaís MatosAinda não há avaliações
- Exercicios Resolvidos Prova PDFDocumento11 páginasExercicios Resolvidos Prova PDFAnderson SilvaAinda não há avaliações
- ExRecurso (MIEEC)Documento5 páginasExRecurso (MIEEC)joyAinda não há avaliações
- Problemas Fisica Geral IIDocumento64 páginasProblemas Fisica Geral IIHenrique SantosAinda não há avaliações
- Lista04 EQP006Documento2 páginasLista04 EQP006Bruna SelauAinda não há avaliações
- Clubes - Fórmula de Herão - Dedução 1Documento2 páginasClubes - Fórmula de Herão - Dedução 1Ewerton SchroederAinda não há avaliações
- Lista 2Documento8 páginasLista 2Cristiano J FerreiraAinda não há avaliações
- 007-Matemática-1-Função Do 2 Grau-EQUAÇÕES INCOMPLETAS E COMPLETAS E SOMA E PRODUTO DAS RAÍZESDocumento6 páginas007-Matemática-1-Função Do 2 Grau-EQUAÇÕES INCOMPLETAS E COMPLETAS E SOMA E PRODUTO DAS RAÍZESDavid J.CAinda não há avaliações
- FT1 Limites Continuidade TI ENDocumento2 páginasFT1 Limites Continuidade TI ENMafalda SubicaAinda não há avaliações
- TEX Cap 2 RespondidoDocumento5 páginasTEX Cap 2 RespondidoVictor Rodrigues de OliveiraAinda não há avaliações
- Otimo Formulário+EEARDocumento29 páginasOtimo Formulário+EEARdanielbatistapl0% (1)
- Respostas - Lista 7 Q1 2019Documento13 páginasRespostas - Lista 7 Q1 2019Epitacio Junior MaurizAinda não há avaliações
- Prova1 ALGA 2022Documento1 páginaProva1 ALGA 2022779xw7sv9kAinda não há avaliações
- CN EPCAR - Produtos Notáveis PDFDocumento1 páginaCN EPCAR - Produtos Notáveis PDFJoão PedroAinda não há avaliações
- Uniftec Grau BDocumento2 páginasUniftec Grau BSidneiAinda não há avaliações
- ExameDocumento2 páginasExameMaria CarvalhoAinda não há avaliações
- APFQ II - Correção Equilíbrio V.2Documento21 páginasAPFQ II - Correção Equilíbrio V.2Robson RaduanAinda não há avaliações
- Porto Editora - Novo Espaço - 11.º Ano - Teste 3 de 2019-20Documento7 páginasPorto Editora - Novo Espaço - 11.º Ano - Teste 3 de 2019-20Beatriz OliveiraAinda não há avaliações
- Ficha2 2023 IDocumento10 páginasFicha2 2023 IJonas ChachuaioAinda não há avaliações
- ALista18 - Calculo de VolumesDocumento2 páginasALista18 - Calculo de Volumesana luisaAinda não há avaliações
- QQD159 Produtos NotaveisDocumento1 páginaQQD159 Produtos NotaveisFelipe RodriguesAinda não há avaliações
- Trabalho Individual I 3o Trimestre 2023Documento2 páginasTrabalho Individual I 3o Trimestre 2023Angelo Americo MarcelinoAinda não há avaliações
- Roteiro Anos Finais Matemática 9º Ano 16-08Documento4 páginasRoteiro Anos Finais Matemática 9º Ano 16-08Maria Cristina Wink SehnemAinda não há avaliações
- Actividade Formativa 2Documento3 páginasActividade Formativa 2valesternoAinda não há avaliações
- 2a Lista de Exercícios de Álgebra Linear II - 2014-02 - Turmas 01-08Documento5 páginas2a Lista de Exercícios de Álgebra Linear II - 2014-02 - Turmas 01-08Victor BarbozaAinda não há avaliações
- Cap 1 Ex PDFDocumento4 páginasCap 1 Ex PDFPaulo OliveiraAinda não há avaliações
- Apostila - Módulo 04Documento5 páginasApostila - Módulo 04BielzinclAinda não há avaliações
- 1 - Resumo de Geometria Analílica - Cônicas - Elipse, Hipérbole e Parábola - ConcluídoDocumento26 páginas1 - Resumo de Geometria Analílica - Cônicas - Elipse, Hipérbole e Parábola - ConcluídoLeonardo Gonçalves da SilvaAinda não há avaliações
- Algebra Nivel2 1Documento8 páginasAlgebra Nivel2 1Ronald MartinsAinda não há avaliações
- FatoracoesDocumento7 páginasFatoracoesFernanda Marchiori GraveAinda não há avaliações
- Provao 99Documento39 páginasProvao 99Leonardo H. MacedoAinda não há avaliações
- AV 03 - Revisão Da TentativaDocumento5 páginasAV 03 - Revisão Da Tentativathiago gabrielAinda não há avaliações
- 2019 PADRÃO 4 Fundamentos QuímicaDocumento8 páginas2019 PADRÃO 4 Fundamentos QuímicaAriel MorónAinda não há avaliações
- RaisDocumento17 páginasRaismanoel batista de c. filhoAinda não há avaliações
- Bomba Engrenagem RexrothDocumento24 páginasBomba Engrenagem RexrothDiego Baptista FranciscoAinda não há avaliações
- Avaliação On-Line 3 (AOL 3) - Questionário PDFDocumento10 páginasAvaliação On-Line 3 (AOL 3) - Questionário PDFCarlos RodrigoAinda não há avaliações
- Aula 03 - Componentes Do Sistema Hidráulico-1Documento91 páginasAula 03 - Componentes Do Sistema Hidráulico-1uber babacaAinda não há avaliações
- Cap2 Propriedades Dos FluidosDocumento57 páginasCap2 Propriedades Dos FluidosAdilson Joaquim Massingue80% (5)
- TermometriaDocumento26 páginasTermometrialeandro.gutierresAinda não há avaliações
- Catalogo Transair LegrisDocumento32 páginasCatalogo Transair LegrisGabriel Jamariqueli BueresAinda não há avaliações
- Identificac3a7c3a3o e Simbologia de InstrumentosDocumento4 páginasIdentificac3a7c3a3o e Simbologia de InstrumentosAmérico JaiAinda não há avaliações
- Ar de Combustao - CaldeiraDocumento19 páginasAr de Combustao - CaldeiraLUIZ CARLOS MARTINELLI JUNIORAinda não há avaliações
- 1estruturação e TAG Dos Ativos - REV02Documento538 páginas1estruturação e TAG Dos Ativos - REV02Márcio GodoiAinda não há avaliações
- Serie 400 HD PDFDocumento2 páginasSerie 400 HD PDFGiselma ZéoAinda não há avaliações
- Rotor Semiaberto: Bomba Centrífuga MonoestágioDocumento1 páginaRotor Semiaberto: Bomba Centrífuga MonoestágioFelippe Matias RochaAinda não há avaliações
- Lista 4 Balanço de Massa Unidades Multiplas-1Documento29 páginasLista 4 Balanço de Massa Unidades Multiplas-1Gelso LimaAinda não há avaliações
- Cap 6 - Trocadores de CalorDocumento94 páginasCap 6 - Trocadores de CalorGabrielLimaAinda não há avaliações
- Relatório P2 - Viscosidade de Um FluidoDocumento41 páginasRelatório P2 - Viscosidade de Um Fluidotoligado27100% (1)
- Velocidade Média de Uma ReaçãoDocumento34 páginasVelocidade Média de Uma ReaçãoDébora Alvim0% (1)